更新于:2024-06-20
LVRNA002
人用狂犬病mRNA疫苗(艾美疫苗)
更新于:2024-06-20
概要
基本信息
原研机构 |
在研机构 |
非在研机构- |
最高研发阶段临床申请 |
首次获批日期- |
最高研发阶段(中国)临床申请 |
特殊审评- |
关联
100 项与 人用狂犬病mRNA疫苗(艾美疫苗) 相关的临床结果
登录后查看更多信息
100 项与 人用狂犬病mRNA疫苗(艾美疫苗) 相关的转化医学
登录后查看更多信息
100 项与 人用狂犬病mRNA疫苗(艾美疫苗) 相关的专利(医药)
登录后查看更多信息
3
项与 人用狂犬病mRNA疫苗(艾美疫苗) 相关的新闻(医药)2024-05-20
关键词狂犬病;艾美疫苗;成大生物;研究进展近日,河南新野一三岁儿童被狗咬伤注射4剂狂犬疫苗后仍因狂犬病发展死亡的事件在网上传的沸沸扬扬,这也引发了民众对狂犬疫苗质量的质疑。1PART ONE关于狂犬病狂犬病是狂犬病病毒感染引起的以中枢神经系统症状为主的一种动物源性传染病,临床表现为特有的恐水、怕风、咽肌痉挛、进行性瘫痪等,一旦出现症状,病死率接近100%。据WHO统计,全球超150个国家和地区存在狂犬病流行,全球每年约有5.9万人因狂犬病死亡。狂犬病毒(RABV)属于弹状病毒科狂犬病毒属,是单股负链RNA病毒,基因组编码5种蛋白,即糖蛋白、核蛋白、基质蛋白、磷蛋白和RNA聚合酶。RABV主要有核蛋白和糖蛋白两种抗原,其中核蛋白刺激机体后不能产生保护性抗体,但能参与特异抗原识别和免疫记忆。糖蛋白能够刺激机体产生细胞免疫应答和有保护作用的中和抗体,是疫苗发挥作用的主要成分。而且,糖蛋白能与乙酰胆碱等病毒受体结合,这也决定了RABV的嗜神经性。狂犬病主要通过携带狂犬病毒(RABV)的动物咬伤或抓伤宿主传播。RABV具有嗜神经性,病毒在伤口处复制并进入肌神经节最终到达中枢神经系统,潜伏期从数天到几年不等。2PART TWO人用狂犬病疫苗发展历程接种狂犬病疫苗是目前预防狂犬病最主要的手段。而人用狂犬病疫苗最早要追溯到1882年,法国科学家路易巴斯德首次成功发明了第一种可预防人类狂犬病的疫苗,这种疫苗来源于感染狂犬病病毒的兔中枢神经组织,所使用的RABV使用干燥的方法灭活。之后人用狂犬病疫苗经历了早期的动物神经组织疫苗、禽胚疫苗、细胞培养的粗制疫苗,发展到目前技术日趋完善的原代地鼠肾细胞、鸡胚细胞、人二倍体细胞和Vero细胞培养的纯化疫苗。其中早期的神经组织疫苗免疫效果不佳,且疫苗接种后局部和全身反应严重,由于疫苗中含有动物脑组织的髓磷脂成分,接种后可能引起神经性麻痹反应,1984年WHO建议停止生产和使用神经组织疫苗。禽胚疫苗采用鸡胚或者鸭胚作为生产媒介,较神经组织疫苗更安全,但使用含胚胎的禽蛋存在许多限制,如供应不足、产量不一致、耗时长、制造成本高以及对禽蛋成分过敏的潜在可能性等。目前,现代纯化鸭胚疫苗(DEV)的生产,包括将RABV的Pitman-Moore (PM)毒株接种于鸭胚中,在温和的条件下(无任何机械力)从受感染胚胎的脑中提取RABV,以避免释放可造成纯化障碍和诱发不良反应的可溶性禽抗原。当前纯化鸭胚疫苗还在亚洲、非洲和南美洲一些国家使用。细胞培养疫苗是WHO推荐使用的主要人用狂犬病疫苗,分为原代细胞培养疫苗和传代细胞培养疫苗。与神经组织疫苗相比,基于细胞培养的狂犬病疫苗具有良好的安全性和有效性,而且给药剂次大大减少,副作用最小化,细胞培养正成为生产许多病毒疫苗的首选系统。目前,生产人用狂犬病疫苗的细胞包括原代细胞、二倍体细胞和连续细胞系。其中原代细胞直接来源于动物组织,如鸡胚成纤维细胞、原代地鼠肾细胞,其保留了来源组织的特征,培养传代次数有限。二倍体细胞(如人胚肺成纤维细胞)包含全部的遗传物质,保留了来源的细胞类型的许多特征,但体外寿命有限。与原代细胞相比,人二倍体细胞可以在专用的封闭系统中进行多次扩增传代。人二倍体细胞是WHO推荐生产病毒疫苗最安全的细胞培养基质之一,二倍体疫苗(HDCVs)已被证明具有优越的免疫原性和安全性。连续细胞系(来源于动物组织,如Vero细胞系)是生产各种生物药物的重要细胞底物,具有无限的寿命和无限的连续传代扩增特性,也可以在发酵罐的微载体上进行大规模培养,这有助于生产系统的标准化、安全性和大规模生产,从而获得稳定的产量。纯化的Vero细胞狂犬病疫苗(PVRV)是现代狂犬病疫苗的主力军,其免疫原性和安全性以及生产安全性和经济性已经得到广泛认可。随着科学技术以及疫苗质量的提升,狂犬病疫苗的免疫接种程序也在不断优化。巴斯德时代及以后很长一段时间,因疫苗效价的不确定性,免疫程序十分复杂,需连续14-21天接种。上世纪50年代改为6剂次(即第0、3、7、14、30、90天各接种一剂次),之后经过验证,WHO推荐使用五针程序(即第0、3、7、14、28天各接种一剂次)。20世纪,前南斯拉夫Zagreb公共卫生研究院的Vodopija团队受WHO的委托,开发了一种更经济、更简化的免疫程序,即“2-1-1”免疫程序(即第0天在左右上臂三角肌各接种1剂,第7天和第21天各接种1剂,共接种4剂),也称Zagreb免疫程序。1992年,WHO建议全球使用“2-1-1”免疫程序,目前法国、南非、中国等20余个国家使用该程序。相较5针免疫程序,4症免疫程序具有明显的经济学优势,可极大减少疾病负担,节约社会资源。3PART THREE我国人用狂犬病疫苗现状目前,我国批准的狂犬疫苗包括人二倍体细胞疫苗、鸡胚细胞纯化疫苗、Vero细胞纯化疫苗和地鼠肾细胞纯化疫苗,其中人二倍体细胞疫苗和Vero细胞纯化疫苗目前应用比较多。据不完全统计,我国以Vero细胞为基质生产狂犬病疫苗的企业最多,包括成大生物、荣安生物、大连雅立峰、依生生物、诺诚生物、华兰生物、康润生物、卓谊生物等。康华生物和康泰生物是国内两家拥有人二倍体狂犬病疫苗生产批件的企业,其中康华生物是国内人二倍体狂犬疫苗领军者,其冻干人二倍体狂犬疫苗2012年正式获批,2014年投产,是国内第一家获批签发人二倍体狂犬病疫苗的企业。中科生物、吉林亚泰、河南远大、兰州生物、大连汉信等企业拥有地鼠肾原代细胞纯化疫苗生产批件。狂犬病疫苗属于非免疫规划疫苗,民众自愿自费接种,但各地区疫苗的采购价不同。据公开资料,康华生物旗下的冻干人用狂犬病疫苗(人二倍体细胞)价格最高,1支(ml)的价格为300元。人用狂犬病疫苗(Vero细胞)单支价格在100元左右。我国疫苗实行批签发制度,2015年至2020年我国狂犬病疫苗每年的批签发量维持在5-8千万支,其中2020年狂犬病疫苗的批签发量在所有疫苗中排名第一,批签发总量达7860.37万支。据中检院披露的数据,2023年我国人用狂犬病疫苗批签发703批次,同比下降22%(2022为903批次)。从细胞基质种类看,2023年Vero细胞型批签发597批次,人二倍体细胞型批签发79批次,地鼠肾细胞型批签发27批次。而鸡胚细胞型从2020年起没再见有批签发记录。从批签发企业来看,涉及11家企业,其中辽宁成大批签发256批次、长春卓谊批签发130批次、成都康华批签发78批次、宁波荣安(艾美疫苗)批签发72批次、山东亦度批签发55批次、长春所批签发29批次、河南远大批签发27批次、大连雅立峰批签发24批次、辽宁依生生物批签发23批次、华兰生物批签发8批次、北京民海批签发1批次。狂犬病疫苗是2023年国内产值TOP10非免疫规划疫苗之一,2023年其产值高达66.6亿元,但较同期减少22.11%。从企业格局来看,成大生物是狂犬病疫苗赛道的龙头企业,2020年至2023年其人用狂犬病疫苗收入分别为19.56亿元、20.87亿元、17.65亿元和16.43亿元,虽然其人用狂犬病疫苗收入逐年下滑,但其市场份额仍保持第一。卓谊生物产品结果比较单一,99%营收来自其冻干人用狂犬病疫苗(Vero细胞),据悉2020年至2022年其冻干人用狂犬病疫苗(Vero细胞)收入分别为3.06亿元、4.11亿元、5.25亿元,2023上半年收入约为2.68亿元。康华生物是2023年人二倍体狂犬病疫苗赛道唯一一家企业获得批签发的企业,2023年其人二倍体狂犬病疫苗创收14.25亿元,有与成大生物比肩之势。不过康泰生物人二倍体狂犬病疫苗已于2023年12月再国内获批,而且康泰生物人二倍体狂犬病疫苗在免疫接种程序上有明显优势,仅需接种4针,而康华生物的需要接种5针。这种局面下康华生物要保持增势似乎有点困难。艾美疫苗是全球及中国第二大人用狂犬病疫苗供货商,人用狂犬病疫苗是其收入的主要来源,据悉其人用狂犬病疫苗2021年和2022年的收入分别为9.37亿元和7.77亿元。由上可以看出,在国内Vero细胞狂犬病疫苗占绝对主导地位。而人二倍体细胞被称为预防狂犬病的黄金标准疫苗,没有不良反应,过敏体质、老人小孩也都可以接种,未来有望持续放量。4PART FOUR国内狂犬病疫苗在研情况随着宠物经济的发展,狂犬病疫苗市场规模也随之扩张。与国外不同,国内药企更倾向于人用狂犬病疫苗的开发。灼识咨询估计,我国人用狂犬病疫苗的市场规模将由2021年56亿元增加至2030年的148亿元,复合年增长率达11.4%。从目前市场格局来看,我国人用狂犬病疫苗市场企业竞争已十分激烈,尤其是Vero细胞狂犬病疫苗领域。而且,华兰生物和江苏康润生物的冻干人用狂犬病疫苗(Vero细胞)已于2023年在国内获批。不过,目前还有不少企业在进军狂犬病疫苗市场。据不完全统计,目前国内处于临床研究阶段的人用狂犬病疫苗近20种,布局企业除了上市提及的,还包括智飞生物、成都所、武汉所、金迪克生物、荣盛生物、瑞贝斯等。其中成大生物开发的人用二倍体狂犬病疫苗已完成III期临床试验,并取得临床试验总结报告,正在与CDE开展新药注册前的预沟通工作(Pre-NDA)。艾美疫苗还开发了mRNA人用狂犬病疫苗、无血清Vero细胞狂犬病疫苗、人二倍体细胞狂犬病疫苗。其中与Vero细胞狂犬病疫苗相比,无血清Vero细胞狂犬病疫苗能避免与在生产中使用血清有关的生物安全风险,有望提高安全性及免疫原性并减少不良副作用。卓谊生物在狂犬病疫苗领域还开发了冻干人用CpG佐剂狂犬病疫苗(Vero细胞)。此外,卓谊生物还正在开展“2-1-1”和“1-1-1-1”两种四针法狂犬病疫苗免疫程序的安全性及免疫原性研究,且两种免疫程序均已经完成临床试验并提交上市申请。整体来看,在研狂犬病疫苗以Vero细胞型和人二倍体细胞型为主,但不少企业也开始探索新型狂犬病疫苗,其中艾美疫苗、康华生物、云顶新耀等企业正在积极开发人用mRNA狂犬病疫苗。与传统人用狂犬病疫苗相比,mRNA狂犬病疫苗具有更好的免疫原性,只需要更少的剂量即可达到更好的免疫效果(两剂或三剂),以及安全性高等优势。其中艾美疫苗的人用狂犬病mRNA疫苗于2023年6月在国内申请临床。此外,重组疫苗、植物来源疫苗、DNA疫苗、多肽疫苗、亚单位疫苗等新型疫苗,以及安全性高、只需1针免疫的长效疫苗也是狂犬病疫苗的研发方向。总结整体来看,我国狂犬病疫苗市场竞争激烈,批签发企业超10家,批签发的狂犬病疫苗以Vero细胞型为主,但人二倍体狂犬病疫苗的潜力已经显现。市场格局上看,成大生物依然领先,但狂犬病疫苗营收已连续两年下滑。康华生物凭借人二倍体狂犬病疫苗在狂犬病疫苗领域崭露头角,但竞争者已经出现,康泰生物人二倍体狂犬病疫苗已于去年获批,且免疫程序更佳,仅需打4针。不过随着疫苗技术的迭代,mRNA狂犬病疫苗也已在路上,我国狂犬病疫苗研发领域也出现了不少新的企业,如智飞生物、成都所、武汉所等。期待在药企的不懈努力下,早日迎来更安全、预防效果更好、免疫程序更优化的狂犬病疫苗。
疫苗信使RNA
2023-08-31
·药创客
点击上方图片报名参会 艾美疫苗宣布,旗下23价肺炎球菌多糖疫苗启动III期随机、盲法、同类疫苗对照设计临床试验。该临床试验计划入组1920例2岁及以上健康受试者。 艾美疫苗旗下23价肺炎球菌多糖疫苗适用于2岁以上人群(特别是60岁以上老年人群)侵袭性肺炎球菌疾病的预防。该疫苗中含有23种肺炎球菌血清型多糖抗原,可以预防肺炎球菌感染引起的肺炎、脑膜炎、中耳炎及菌血症等,覆盖了最常报道的引起肺炎球菌疾病的近90%的血清型。该款疫苗已于2021年12月开展I期临床试验,截至目前已获得的安全性和免疫原性分析结果显示其安全性良好,且具有较好的免疫原性。而艾美的13价肺炎球菌多糖结合疫苗(PCV13)是全球使用最为广泛的肺炎球菌多糖结合疫苗、也是唯一一款用于全年龄组人群注射的肺炎疫苗,有着全球“疫苗销售之王”的称号。2020年辉瑞PCV13全球销售额高达58.5亿美元,预计国内PCV13市场规模有望达到108亿元。作为公司的重磅大品种之一,艾美疫苗的PCV13疫苗三期临床即将结束、制造技术已经验证,预计于2024年年底获批。受益于公司全产业链、大平台的优势,产品一经获批上市后即可实现大规模产能放量,快速抢占市场份额:据悉,目前艾美疫苗全资子公司艾美卫信已完成肺炎球菌疫苗生产线的重建和升级,设计年产能达4700万剂。 由于流行性脑脊髓膜炎(流脑)具有起病急、进展快、传染性强、病死率与致残率高等特点,且流脑菌群一直在发生变化,相比过往疫苗,四价流脑结合疫苗(MCV4)具有预防A群、C群、Y群和W135群四种血清型的多价优势。而在国内市场,脑膜炎球菌疫苗长期被纳入国家免疫规划,而MCV4市场长期由进口厂商主导,潜在国产替代化机会明显。 目前艾美疫苗的四价流脑结合疫苗(MCV4)已启动I期单中心、开放性临床试验,受试者已经开始入组,本试验计划入组120例。市场需求缺口叠加MCV4单支价格高、利润空间大的特点,上市后预计将为公司贡献充沛的现金流。 手足口病是由肠道病毒引起的自限性疾病,属于儿童常见传染病,2009-2019年我国手足口病报告发病总体呈波动上升趋势。目前市面上获批的单价手足口病疫苗存在仅能针对EV71这一种病毒株的劣势,因此更为创新的的EV71-CA16二价手足口病疫苗已成为技术发展的必然趋势。 目前,艾美疫苗全球首研的EV71-CA16二价手足口病疫苗已进入临床阶段。这也是我国首个获得临床批件的二价手足口病疫苗,上市后有望填补国内市场空白。 预计2023年下半年和2024-2025年间,艾美疫苗将有至少四款产品发布上市,商业化产品数量提升至两位数;同时,市场所关注的二价手足口病疫苗、冻干人用狂犬疫苗(人二倍体细胞)、四价结合流脑疫苗、破伤风疫苗等产品均预计在5年内上市。产品进入密集收获期,无疑将为公司业绩增添强劲的成长动能。作为国内起步较早、深耕疫苗赛道多年的公司,艾美疫苗有着病毒疫苗平台、细菌疫苗平台、mRNA疫苗平台、基因工程疫苗平台、联合疫苗平台这五大技术平台强力支撑研发,目前已经完成针对14种疾病领域23款在研疫苗的布局,且目前已有9个品种取得共计14个临床批件。作为国内首款针对奥密克戎株BA.5的二价广谱mRNA疫苗,已有的试验数据表明其不仅具有良好的防感染效果,期中分析最高保护率达到80.68%,远高于新冠疫苗保护效力的国际标准;还具有广谱作用,对XBB变异株反而表现出更高的保护效力。随着国内“二阳”、甚至“三阳”“四阳”的病例人数逐渐增多,预计该款mRNA新冠疫苗上市后亦将贡献显著业绩增量。根据艾美疫苗发布的2023年中期业绩公告,在研二价Delta-Omicron BA.5 mRNA新冠疫苗海外III期临床正处于收尾阶段。未来公司将使用该款疫苗在国内的I、II期临床数据,结合在巴基斯坦的III期临床数据,申请该款疫苗在国内注册上市。此外,公司研发的人用狂犬病mRNA疫苗是国内首款申报临床获得受理的非新冠mRNA疫苗,目前临床试验申请已获受理。从收入结构来看,乙肝疫苗与人用狂犬病疫苗是公司主要的收入来源,在市场一直占据领先地位,保障了公司现金流。深入探究公司业务就会发现,即使不考虑未来新产品上市,在现有的狂犬疫苗与乙肝疫苗上公司亦早有布局。展望后续研发路线,公司在狂犬疫苗上亦有着完善的迭代升级规划,包括已获临床批件的无血清Vero细胞狂犬病疫苗、人二倍体细胞狂犬病疫苗以及mRNA狂犬病疫苗。其中,公司所研发的人用狂犬病mRNA疫苗是国内首款申报临床的狂犬病mRNA疫苗,目前临床试验申请已获受理。在乙肝疫苗方面,艾美是中国第一家也是唯一一家实现使用汉逊酵母进行抗原表达的乙型肝炎疫苗稳定生产和批签发量的疫苗公司。在所有可用的三种制造技术(汉逊酵母、酿酒酵母及CHO细胞)中,汉逊酵母被公认为是乙型肝炎疫苗的最佳制造技术路线,具有更好的遗传稳定性、更高的纯度及更强的抗原表达能力。识别微信二维码,添加小编,符合条件者即可申请加入微信群!请注明:姓名+单位!声明:本文旨在传递更多信息,版权归原作者所有。原创文章转载均需经过授权并注明来源,如涉及内容、版权或其他问题请时联系小编删除!文章仅代表作者个人观点,并不代表公众号立场。本公众号拥有对此声明的最终解释权!投稿邮箱:yck19876@163.com
临床3期疫苗临床1期
2023-07-22
7月19日,据国家药品监督管理局药品审评中心显示,卓谊生物递交了冻干人用狂犬病疫苗(Vero细胞)的上市申请并获受理,受理号为CXSS2300054。图1:卓谊生物递交了冻干人用狂犬病疫苗(Vero细胞)的上市申请(来源:CDE)01/ 卓谊生物深耕狂犬病疫苗领域卓谊生物是一家从事疫苗产品研发、生产及销售的高新技术企业。目前,公司正处于申请深交所主板上市阶段。6月16日,卓谊生物的上市申请获受理;7月7日,中国证券业协会官网披露了“2023年第三批首发申请企业现场检查抽查名单”,其中卓谊生物赫然在列。据卓谊生物的6月更新的招股书显示,公司目前核心产品为冻干人用狂犬病疫苗(Vero细胞),且该产品已实现商业化,是公司的主要收入和毛利来源。该产品系用源自我国的狂犬病病毒固定毒株 CTN-1V 株接种 Vero 细胞,经生物反应器灌流培养后收获病毒液,再经浓缩、灭活、纯化后,加入赋形剂和稳定剂后冻干制成,是公司自主研发的产品。目前,该产品已进入全国大部分省、自治区及直辖市的疫苗采购目录,公司是国内狂犬病疫苗的主要供应商之一。40份国内人用疫苗申请上市技术审评报告领取方式:关注【药时空】公众号,进入公众号后台,回复关键字“疫苗技术审评资料”,以上资料免费送!PS:药时空还统计汇总了《297份国内治疗用生物制品申请上市技术审评报告》,如有兴趣可点击查看详情及领取方式,请持续关注本公众号~另外,招股书中还提到,公司正在开展“2-1-1”和“1-1-1-1”两种四针法狂犬病疫苗免疫程序的安全性及免疫原性研究,其中“2-1-1”四针法免疫程序已提交新药上市申请,“1-1-1-1”简易四针法免疫程序已完成III期临床试验、拟提交新药上市申请。而查询CDE网站可知,公司在今年4月24日已提交了一项冻干人用狂犬病疫苗(Vero细胞)的上市申请,受理号为CXSS2300020。所以,合理推测一下,公司本次提交的新药上市申请很可能是“1-1-1-1”简易四针法免疫程序。除了公司冻干人用狂犬病疫苗(Vero细胞)外,公司在狂犬病疫苗方面还有其他布局:公司正在开发的冻干人用 CpG 佐剂狂犬病疫苗(Vero 细胞)处于临床申请阶段,冻干人用 CpG 佐剂狂犬病疫苗(Vero 细胞)计划采用“1-1-1”三针法免疫程序,有望进一步减少接种者就医次数、提高依从性并缩短抗体阳转时间;公司兽用狂犬病疫苗已提交新兽药注册申请,待获批上市后将和人用狂犬病疫苗协同针对狂犬病毒传播链条的不同环节,相关产品上市后,公司将在狂犬病疫苗领域拥有丰富的产品梯度。02/ 我国狂犬病疫苗批签发情况1885年,首个人用狂犬疫苗诞生。随后,狂犬病疫苗开启了升级迭代之路。就我国而言,国内的狂犬病疫苗发展经历了四代,根据细胞基质种类进行区分包括狂犬病疫苗(地鼠肾细胞)、狂犬病疫苗(鸡胚细胞)、狂犬病疫苗(Vero细胞)、狂犬病疫苗(人二倍体细胞)。前三者均是动物细胞狂犬疫苗,后者属于人源细胞狂疫苗。图2:四类狂犬病疫苗对比(来源:财通证券)人用狂犬病疫苗的接种需求主要来自暴露后免疫,亦包括少量暴露前免疫。由于狂犬病病毒暴露后病死率接近100%,我国每年狂犬病疫苗使用量基本相对稳定。2015年-2020年,我国狂犬病疫苗每年的批签发量维持在5-8千万支。值得注意的是,2020年,狂犬病疫苗位列我国疫苗批签发量排名第一,共批签发879批次,批签发总量达到7860.37万支。不过,2021年4月开始,中检院不再公布生物制品批签发具体数量,仅公布批签发批次数。图3:2020年中国疫苗销售量Top 10(来源:深度价值投研笔记)据中检院披露的情况显示,2023年上半年,我国狂犬病疫苗批签发357批次,同比增加3.5%(2022H1为344批次)。其中,冻干型批签发310批次,液体型批签发47批次。从细胞基质种类看,Vero细胞型批签发294批次,人二倍体细胞型批签发36批次,地鼠肾细胞型批签发27批次。至于狂犬病疫苗(鸡胚细胞),其从2020年至今没有批签发记录。(文末附详细的狂犬病疫苗批签发信息表)从批签发企业看,涉及10家企业,包括辽宁成大批签发88批次、卓谊生物批签发79批次、荣安生物(艾美疫苗全资控股企业)批签发60批次、康华生物批签发36批次、远大生物批签发27批次、雅立峰生物批签发20批次、亦度生物批签发19批次、长春所批签发18批次、依生生物批签发7批次、华兰生物批签发3批次。图4:2019年-2022年分厂家狂犬疫苗签发批次(来源:中检院,国联证券研究所)可以看出,Vero细胞狂苗占绝对主导地位。Vero细胞可稳定传代,根据WHO建议用于生产的最大工作细胞代次可达到150代,因此适用于大规模生产且生产成本较低、批间质量稳定。而人二倍体细胞则被称为预防狂犬病的黄金标准疫苗,没有不良反应,过敏体质、老人小孩也都可以接种,因此也具有一定优势,未来有望持续放量。而人用狂犬病疫苗(人二倍体细胞)目前在国内仅有康华生物一家在生产。人用狂犬病疫苗(Vero细胞)和人用狂犬病疫苗(人二倍体细胞)是目前企业主要的研发方向。除了上述企业外,狂犬病疫苗的在研企业还有民海生物/康泰生物、智飞生物、成都所、武汉所、金迪克生物等。此外,国内企业也在积极探索其他新型疫苗,如6月10日,艾美疫苗旗下丽凡达生物就递交了一款人用狂犬病mRNA疫苗的临床试验申请并获受理。这也是国内首款申报临床的狂犬病mRNA疫苗。总之,如今狂犬病疫苗市场已经形成了以Vero细胞培养的狂犬病疫苗为主流,人二倍体细胞狂犬病疫苗有望替代传统狂犬疫苗的趋势。附:2023年H1我国狂犬病疫苗批签发情况(来源:中检院,药时空整理)参考资料:[1]《2023-2029年狂犬病疫苗行业深度调研及投资前景预测报告》.普华有策.2023-06-19[2]《“人用+兽用”双管齐下,背后的狂犬疫苗市场》.贝壳社.2023-05-16[3]《狂犬疫苗产业链梳理》.深度价值投研笔记.2023-02-15[4]《2023年6月疫苗批签发》.中银证券.2023-07-06[5]《一年700 多万只狂犬疫苗撑起的 IPO:卓宜生物欲主板上市》.华尔街见闻.2023-07-11[6]卓宜生物招股说明书(2023年6月更新版)[7]中国食品药品检定研究院.生物制品批签发产品公示情况汇总相关阅读:[1]同比下滑85%!2023年上半年我国流感疫苗批签发情况总览[2]PPV23批次量增长165%!2023年上半年我国肺炎疫苗批签发情况总览识别微信二维码,添加药时空小编,符合条件者即可加入药时空微信群!请注明:姓名+研究方向!
疫苗临床3期上市批准申请上市医药出海
100 项与 人用狂犬病mRNA疫苗(艾美疫苗) 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 狂犬病 | 临床申请 | 中国 | 2023-06-10 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
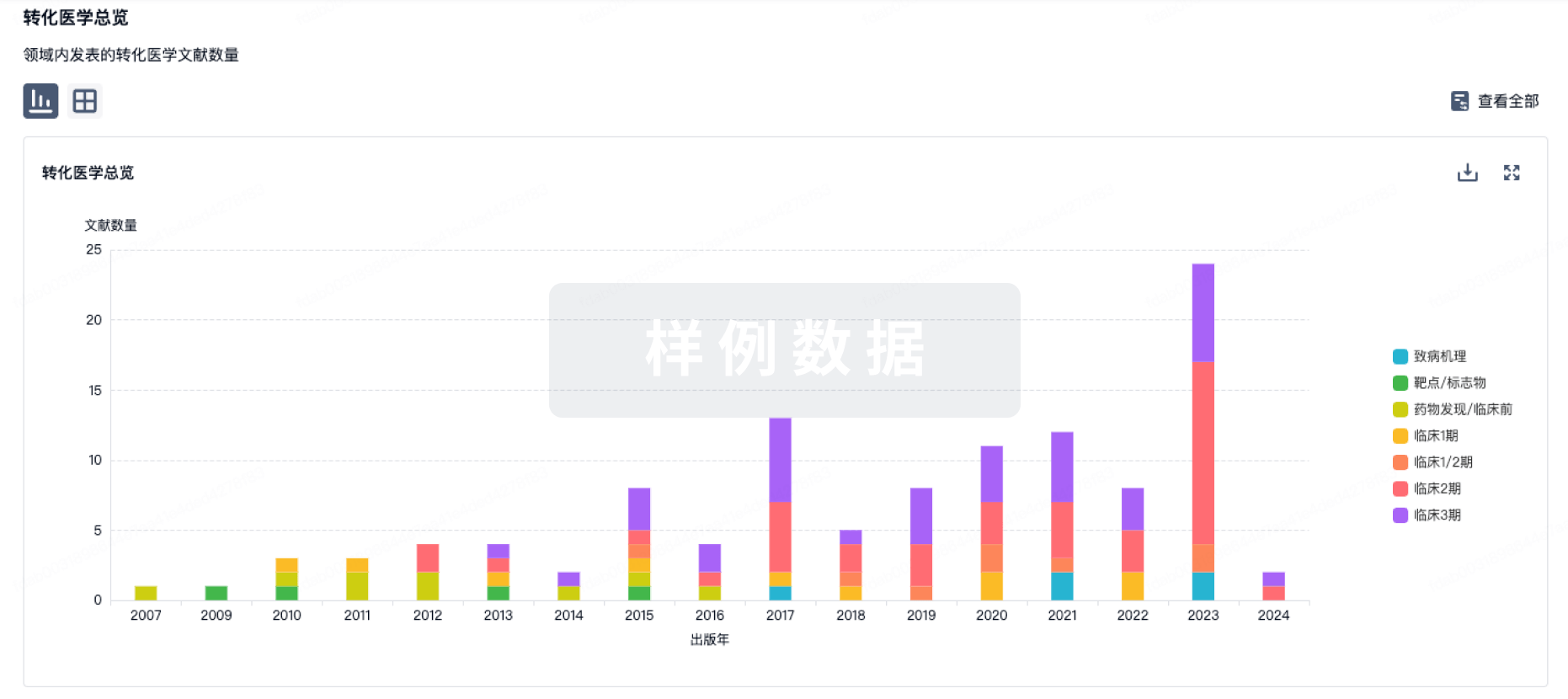
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
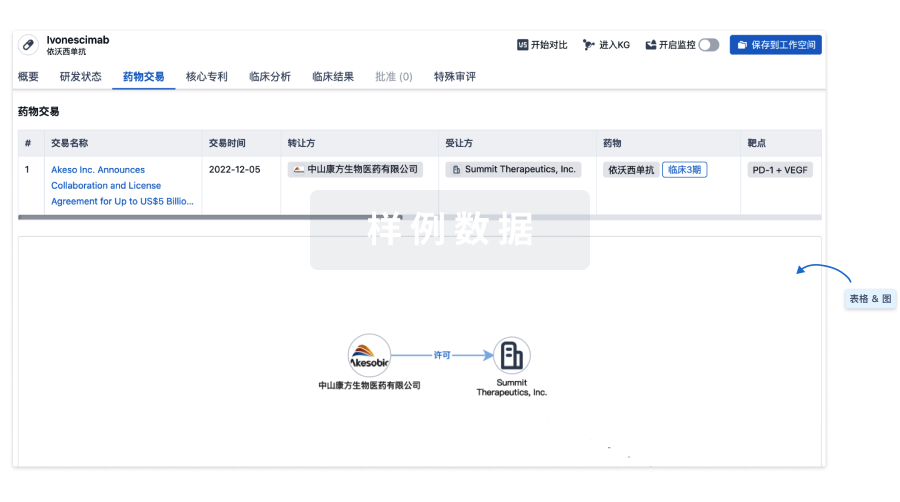
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
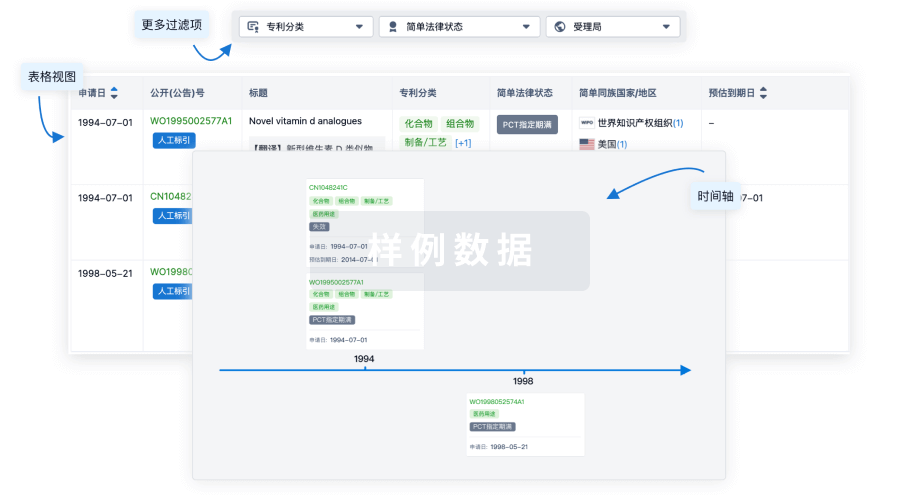
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
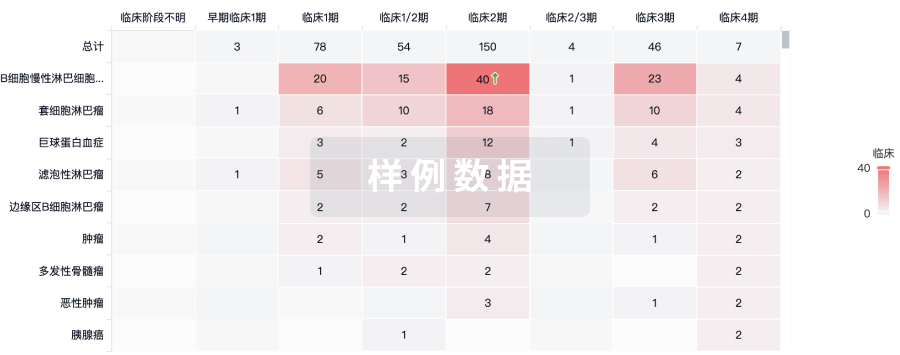
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
批准
利用最新的监管批准信息加速您的研究。
登录
或
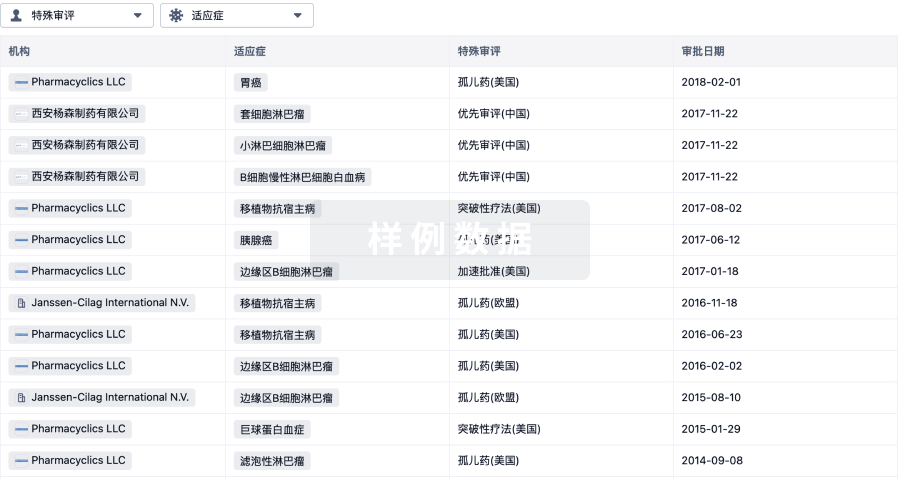
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用

