更新于:2024-06-22
aT19(Immunotech Biopharm Ltd.)
更新于:2024-06-22
概要
基本信息
药物类型 通用型CAR-T |
别名- |
靶点 |
作用机制 CD19抑制剂(B淋巴细胞抗原CD19抑制剂)、基因转移、T淋巴细胞替代物 |
非在研适应症- |
原研机构 |
非在研机构- |
最高研发阶段临床2期 |
首次获批日期- |
最高研发阶段(中国)临床2期 |
特殊审评- |
关联
2
项与 aT19(Immunotech Biopharm Ltd.) 相关的临床试验Phase II Clinical Study of CAR-T-19 (Anti-CD19 Single-chain Antibody Chimeric Antigen Receptor T Cell) Injection in the Treatment of CD19-positive Relapsed/Refractory B-cell Acute Lymphoblastic Leukemia(B-ALL) Under 25 Years of Age (Inclusive)
This is a phase II clinical study to evaluate the safety and efficacy of CAR-T-19 injection in the treatment of CD19-positive relapsed/refractory B-cell acute lymphoblastic leukemia.
开始日期2023-12-31 |
申办/合作机构 |
A single-center, single-arm, open-label, dose escalation study to evaluate the safety & preliminary anti-tumor activity of CD19 single-chain antibody chimeric antigen receptor T cells (CAR-T-19) for the treatment of patients with relapsed / refractory B-cell leukemia / lymphoma
开始日期2017-09-01 |
申办/合作机构- |
100 项与 aT19(Immunotech Biopharm Ltd.) 相关的临床结果
登录后查看更多信息
100 项与 aT19(Immunotech Biopharm Ltd.) 相关的转化医学
登录后查看更多信息
100 项与 aT19(Immunotech Biopharm Ltd.) 相关的专利(医药)
登录后查看更多信息
7
项与 aT19(Immunotech Biopharm Ltd.) 相关的新闻(医药)2024-04-02
·药融圈
▲5月30-31日第八届广州生物医药创新者峰会 扫码立即报名 注:本文不构成任何投资意见和建议,以官方/公司公告为准;本文仅作医疗健康相关药物介绍,非治疗方案推荐(若涉及),不代表平台立场。任何文章转载需得到授权。细胞和基因疗法(Cell and Gene Therapy, CGT)是继小分子、大分子靶向疗法之后的新一代精准疗法。据不完全统计,2024年1-3月已有32款CGT疗法获批IND,CAR-T疗法的药物成为获批上市的CGT药物中的主流。获批的药物中包括22款细胞产品、10款基因治疗产品。小编整理如下:康德赛医疗3月21日,中国国家药品监督管理局药品评审中心(NMPA)公示,莱美药业参股公司四川康德赛医疗科技有限公司(以下简称“康德赛”)自主研发用于治疗中晚期肝硬化的巨噬细胞注射液CUD005获得临床试验申请(IND)批准。CUD005注射液是一款基于患者自身免疫细胞,使其分化为成熟、稳定的个体化抗纤维化巨噬细胞。相较于传统小分子药物而言,CUD005注射液能够通过分泌多种基质金属蛋白酶(MMPs)来有效降解胞外基质,减少肝脏瘢痕淤积;同时释放抗炎因子(IL-1RN等),进而抑制炎症反应的发生,改善肝脏炎症微环境,减缓病情发展。此外,CUD005注射液也展现出强劲的凋亡细胞吞噬能力,对肝脏正常结构的恢复起到推进作用。目前,暂未见到其他针对失代偿期肝硬化的候选巨噬细胞疗法获批临床的报道。齐鲁细胞3月11日,银丰生物集团齐鲁细胞公司马贺然博士团队历时4年研发的人脐带间充质干细胞注射液(代号YFQLXB-UC01)收到国家药品监督管理局核准签发的《药物临床试验批准通知书》,适应症为失代偿期肝硬化。这是银丰生物集团在肝硬化领域继两项国家卫健委备案的IIT 研究后的又一里程碑,同时也是山东省内此适应症的第一款IND产品。YFQLXB-UC01注射液是银丰生物集团齐鲁细胞公司自主研发的冻存细胞制剂,间充质干细胞源自健康新生儿的脐带组织华通氏胶,在经过体外的分离扩增后与临床级冻存保护液混合制成了干细胞制剂。区别于传统的新鲜制剂,该剂型是一种“现货型”的产品,且复苏后无须洗涤即可用于静脉输注。圣因生物2月26日,圣因生物宣布其自主研发的用于治疗补体相关疾病的siRNA药物SGB-9768已于近日获得新西兰药品和医疗器械安全管理局(Medsafe)、健康及残疾伦理委员会(HDEC)批准,在新西兰开展Ⅰ期临床试验,这是圣因生物第2款进入临床试验阶段的siRNA药物。SGB-9768是一种靶向补体C3 的 siRNA-GalNAc 结合物,采用了圣因生物独特创新的新一代LEAD™ GalNAc技术递送到肝脏细胞,通过RNAi抑制肝脏C3的合成。GalNAc递送siRNA药物的安全性、有效性、稳定性已得到大量数据验证。本次临床研究是一项随机、双盲、安慰剂对照、单次给药剂量递增的I期研究,主要目的是评估SGB-9768在健康志愿者中的安全性、耐受性、药代动力学及药效动力学特征。研发管线金唯科生物2月22日,金唯科生物自主研发的针对新生血管性年龄相关性黄斑变性(nAMD)基因治疗产品“JWK001注射液”的新药临床试验(IND)申请顺利获得国家药品监督管理局(NMPA)批准。图片来源:CDE官网JWK001注射液是首个采用“两质粒包装系统”的AAV基因治疗新药。金唯科自主研发的两质粒悬浮HEK293细胞包装技术,大幅提升AAV包装效率、降低生产成本。金唯科的CMC工艺稳定且成本低,在临床阶段以及商业化阶段将具有非常明显的优势,极大提升患者可及性。永泰生物2月18日,永泰生物-B(06978.HK)aT19注射液成功获得国家药品监督管理局药品审评中心(CDE)药物临床试验批准。aT19注射液是一种治疗用生物制品,属于生物制品I类,主要功能成分为CD19抗原呈递T细胞。临床试验方案为aT19序贯CAR-T-19注射液治疗25岁(含)以下CD19阳性复发/难治B细胞急性淋巴细胞白血病的Ⅰ期临床研究,拟定适应症为25岁(含)以下复发/难治B细胞急性淋巴细胞白血病,靶向CD19 CAR-T细胞治疗后临床获益的患者,以增强治疗效应、减少复发。本试验将于2024年内开展。易慕峰2月7日,易慕峰宣布其自主研发的靶向EpCAM的自体CAR-T细胞注射液产品(IMC001)的临床试验申请获得中国国家药品监督管理局药品审评中心(CDE)的默示许可(受理号:CXSL2300792),用于治疗EpCAM表达阳性的晚期消化系统肿瘤,包括但不限于晚期胃癌(GC)/食管胃结合部腺癌(GEJ)。IMC001成为全球首个获批IND的靶向EpCAM的CAR-T产品;IMC001已在IIT研究中展示出良好的安全性和有效性。2月23日,易慕峰又宣布其自主研发的靶向EpCAM的自体CAR-T细胞注射液产品(IMC001)的临床试验申请在中国CDE批准之后,近日又获得了美国FDA的临床研究许可,用于治疗EpCAM表达阳性的晚期消化系统肿瘤,包括但不限于晚期胃癌(GC)/食管胃结合部腺癌(GEJ)。原启生物2024年1月29日,原启生物宣布美国食品药品监督管理局(FDA)正式批准其用于治疗复发/难治性多发性骨髓瘤(R/R MM)患者的OriCAR-017的新药临床申请(IND)。OriCAR-017是原启生物利用自主创新技术平台开发出的一款靶向GPRC5D的嵌合抗原受体T细胞疗法(CAR-T)。该产品的设计和开发整合了原启生物自主创新的Ori®Ab抗体平台、Ori®CAR结构平台和公司在CMC方面的专识,在早期的探索性临床研究中展现了良好且持久的抗肿瘤功效,同时也展现了优异的安全性。随着本次IND获批,原启生物即将启动OriCAR-017在美国的临床开发工作。研发管线中吉智药2024年1月26日,中吉智药申报的基因治疗β-地中海贫血药物GMCN-508B的临床试验(IND)申请,获国家药品监督管理局药品审评中心(CDE)默示许可,标志公司正式进入注册临床试验阶段。此次IND获批,是中吉智药作为专注慢病毒载体和造血干细胞治疗领域的新兴公司,跨越了重要里程碑,标志着中吉智药已经由“科学家”,成功转身为“制药人”。总结在2023年度受理的975项生物制品新药申请中,共有167项CGT产品获得IND受理。其中干细胞产品受理48项、免疫细胞产品受理73项、基因治疗产品受理45项。2024年也将是CGT疗法的爆发之年,仅在第一季度就有很多CGT领域的里程碑事件,比如FDA批准一款慢病毒载体基因药物Lenmeldy上市,定价425万美元,目前为全球最贵药物;辉瑞的基因疗法Beqvez也获批上市;华东医药与科济药业BCMA CAR-T合作产品赛恺泽®在中国获批上市;全球首个TIL疗法Amtagvi获批上市,定价51.5万美元,为实体瘤治疗开启新纪元。CGT未来发展空间巨大,相信CGT在未来可以为更多难治性疾病提供新选择。参考资料:各公司官网版权声明:本文转自细胞基因治疗前沿,如不希望被转载的媒体或个人可与我们联系,我们将立即删除 活动推荐 5月 • 第八届大湾区生物医药创新者峰会 关键词: 小分子,XDC,多肽及GLP-1热点话题,80+行业专家(点击下方图片查看详情)▼【关于药融圈】药融圈PRHub旨在帮助生物医药科技型企业进行品牌推广及商务拓展服务,针对客户的真实需求制定系统化解决方案,通过“翻译-降维-场景化”将客户的品牌信息以直白易懂的方式被公众知悉,同时在流量渠道覆盖100万+垂直用户基础上实现合作目的,帮助合作伙伴完成从品牌开始到商务为终的闭环营销服务。我们已经完成了数十场线下1000人规模的生物医药研发类会议,涵盖小分子新药,大分子新药,改良型新药,BD跨境交易等多个领域,服务了百余家上市/独角兽/生物技术/制药企业。
临床申请细胞疗法siRNA基因疗法核酸药物
2024-03-03
·医药观澜
▎药明康德内容团队编辑根据中国国家药监局药品审评中心(CDE)官网,在刚刚结束的2月,有近50款1类新药首次在中国获得临床试验默示许可,包括细胞和基因疗法(CGT)、抗体药物、抗体偶联药物(ADC)、小分子靶向疗法等不同的药物类型。本文将重点介绍数款于2月获批临床的CGT疗法(排名不分先后),仅供读者参阅。欲知更多2月份在中国获批临床的1类新药信息,请扫描下方二维码,即可获得“2024年2月首次在中国获得临床试验默示许可的1类新药”PDF文件)中因制药:ZVS203e注射液作用机制:体内AAV基因编辑治疗产品适应症:视网膜色素变性ZVS203e是中因科技在研的一款眼科基因编辑1类创新药,利用第三代人工核酸内切酶CRISPR/Cas9,对突变的RHO基因进行定点编辑,针对致病基因从根源对疾病进行治疗,达到一次给药终身治愈的效果。该产品获批临床,拟用于治疗携带RHO-R135W(RHO c.403C>T)突变的视网膜色素变性(RP)患者。RP是一组以视网膜感光细胞和视网膜色素上皮细胞进行性、选择性丧失为特点的进展性单基因致盲眼病,其中RHO基因突变在常染色体显性遗传RP中最常见。ZVS203e已于2022年7月获得美国FDA孤儿药资格,并于2023年9月在北京大学第三医院开展的研究者发起的临床研究(IIT)中完成全球首个RHO基因突变RP患者的注射给药,在首例患者中表现出良好的安全性和有效性。易慕峰生物:IMC001注射液作用机制:EpCAM靶向自体CAR-T适应症:消化系统肿瘤IMC001是易慕峰自主研发的一款靶向EpCAM的自体CAR-T细胞产品。EpCAM在消化道肿瘤等多种上皮来源肿瘤组织上呈现高表达,在结直肠癌和胃癌上表达率均在90%以上[3],且可以作为循环肿瘤细胞(CTC)的治疗靶点。IMC001旨在通过靶向EpCAM,解决转移和复发难题,为晚期消化系统肿瘤提供一种新的治疗选择。2月7日,易慕峰宣布该产品在中国获批临床,拟用于治疗EpCAM表达阳性的晚期消化系统肿瘤,包括但不限于晚期胃癌(GC)/食管胃结合部腺癌(GEJ)。2月23日,易慕峰宣布该产品又获得FDA的临床研究许可,用于治疗上述适应症。在针对晚期胃癌的IIT中,研究人员已确定了IMC001安全有效的推荐剂量,该剂量组5名患者中有2名患者被确认为部分缓解(PR),客观缓解率(ORR)达40%。永泰生物:aT19注射液作用机制:CD19抗原呈递T细胞 适应症:急性淋巴细胞白血病aT19是永泰生物在研的一款经过基因改造而强制表达CD19的自体T细胞。研究显示,CD19靶向CAR-T细胞治疗B细胞急性淋巴细胞白血病(B-ALL)后复发可能与CAR-T细胞体内存续时间不足有关。该产品在CAR-T-19注射液给药后回输,具有再度激活CAR-T细胞,再次启动CAR-T细胞的增殖,增加免疫记忆细胞的潜力。该产品本次获批临床针对的适应症为:拟用于25岁(含)以下复发/难治B-ALL,在靶向CD19 CAR-T细胞治疗后临床获益的患者,以增强治疗效应、减少复发。根据前期IIT结果,受试者在接受aT19序贯CAR-T细胞治疗后,微小残留病灶(MRD)阴性持续缓解均已达3年以上,研究过程中未报告不良反应。初步验证了aT19注射液序贯CAR-T细胞治疗的可行性与有效性。唯源立康:WG1025作用机制:携带人COL7A1基因的复制缺陷型HSV-1载体适应症:营养不良型大疱性表皮松解症WG1025是唯源立康自主研发的一款可重复使用的、外用基因治疗生物新药。该产品活性成分是携带人COL7A1基因【编码VII型胶原(COL7)蛋白】的复制缺陷型I型单纯疱疹病毒(HSV-I)载体。WG1025获批临床拟开发用于营养不良型大疱性表皮松解症(DEB)。DEB是一种临床症状严重的遗传性皮肤病,由COL7A1基因发生突变所致COL7蛋白表达缺乏,从而使得患者皮肤非常脆弱。DEB患者创面涂抹WG1025凝胶剂后可将COL7A1基因递送到患者皮肤细胞并产生内源性COL7蛋白,进而组合成锚定纤维将表皮锚定至真皮,提供正常的皮肤结构粘连作用,促进创口愈合。早前WG1025开展的一项IIT研究显示,受试者用药后观察到70%以上创面超过3个月的持续愈合,皮肤活检显示受试者经过WG1025治疗后表皮与真皮间有连续分布的COL7蛋白,验证了WG1025的安全性和有效性。金唯科:JWK001注射液作用机制:AAV基因治疗产品适应症:新生血管性年龄相关性黄斑变性JWK001是金唯科自主研发的一款AAV基因治疗1类新药。该产品获批临床拟开发用于新生血管性年龄相关性黄斑变性(nAMD)。血管内皮生长因子(VEGF)已被证实在nAMD新生血管形成中具有重要作用。JWK001采用“两质粒包装系统”,通过将携带全新自主设计的抗VEGF蛋白表达框的AAV载体,在视网膜细胞中持续高效表达抗VEGF蛋白。可实现一次治疗,终身有效的目的。金唯科新闻稿显示,从已经开展的IIT跟踪结果来看,JWK001注射液的安全性和耐受性良好,临床起效剂量低,患者只需要一次给药,无需辅助治疗,可以避免传统nAMD治疗中存在的风险,如反复玻璃体腔注射对眼组织的伤害、患者依从性差等,给患者带来了极大的便利性。除了上述药物,2月还有包括ADC、抗体药物、小分子靶向疗法等在内的其它类型药物首次在中国获批临床,限于篇幅,本文不再一一介绍。希望这些新药后续临床研究顺利进行,早日造福患者!扫描下方二维码,您将可以获取“2024年2月首次在中国获得临床试验默示许可的1类新药”PDF文件。参考资料:[1]中国国家药监局药品审评中心(CDE)官网. Retrieved Feb 29,2024,
from https://www.cde.org.cn/main/xxgk/listpage/4b5255eb0a84820cef4ca3e8b6bbe20c[2] 各公司官网及新闻稿[3] P Went ,et al.(2006) Frequent
high-level expression of the immunotherapeutic target Ep-CAM in colon, stomach,
prostate and lung cancers. Br J Cancer. doi: 10.1038/sj.bjc.6602924.PMID:
16404366本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「医药观澜」微信公众号留言联系我们。其他合作需求,请联系wuxi_media@wuxiapptec.com。免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
细胞疗法孤儿药免疫疗法抗体药物偶联物基因疗法
2024-02-26
·医药观澜
根据中国国家药监局药品审评中心(CDE)官网数据,本周有十余款1类新药首次在中国获批临床,这些新药来自罗氏(Roche)、默沙东(MSD)、赛诺菲(Sanofi)、海创药业、金唯科生物、格博生物等公司,涉及细胞与基因疗法(CGT)、抗体偶联药物(ADC)、蛋白降解疗法等多种药物类型。本文将介绍部分1类新药信息,仅供读者参阅(排名不分先后)。
作用机制:使用HSV-1载体的基因治疗药物
适应症:营养不良型大疱性表皮松解症
WG1025是唯源立康自主研发的一款使用I型单纯疱疹病毒(HSV-1)载体作为基因治疗递送工具的1类生物新药,活性成分是携带编码VII型胶原蛋白(COL7)的COL7A1基因的复制缺陷型HSV-1载体。该产品获批临床,拟开发用于营养不良型大疱性表皮松解症(DEB)。DEB是一种临床症状严重的遗传性皮肤病,由COL7A1基因发生突变所致COL7蛋白表达缺乏,从而使得患者皮肤非常脆弱。
作用机制:AAV基因治疗药物
适应症:新生血管性年龄相关性黄斑变性
JWK001是金唯科生物自主研发的一款采用“两质粒包装系统”的腺相关病毒(AAV)基因治疗新药。其通过将携带全新自主设计的抗VEGF蛋白表达框的AAV载体,可在视网膜细胞中持续高效表达抗血管内皮生长因子(VEGF)蛋白。VEGF已被证实在新生血管性年龄相关性黄斑变性(nAMD)新生血管形成中具有重要作用。该产品获批临床,拟开发用于治疗nAMD。
作用机制:表达CD19的自体T细胞
适应症:急性淋巴细胞白血病
aT19是永泰生物旗下永泰瑞科正在开发的一款经过基因改造而强制表达CD19的自体T细胞。靶向CD19的CAR-T细胞治疗B细胞急性淋巴细胞白血病(B-ALL)后复发患者中约有50%为CD19阳性复发。aT19注射液在CAR-T-19注射液给药后回输,具有再度激活CAR-T细胞,再次启动CAR-T细胞的增殖,增加免疫记忆细胞的潜力。该产品获批临床,拟开发用于25岁(含)以下复发/难治B-ALL,在靶向CD19的CAR-T细胞治疗后临床获益的患者,以增强治疗效应、减少复发。
作用机制:IL-13/TSLP双特异性纳米抗体
适应症:哮喘
SAR443765是赛诺菲正在开发的一款靶向胸腺基质淋巴细胞生成素(TSLP)和白细胞介素-13(IL-13)通路的双特异性纳米抗体。赛诺菲在2023年美国胸科学会(ATS)年会上展示的临床数据显示:在一项关键的哮喘测量中,与单独使用TSLP 或IL13相比,SAR443765展现出更好的疗效,显示有协同作用。该产品在中国获批临床,拟开发用于治疗成人中重度哮喘。
上海生物制品研究所:注射用SIBP-A17
作用机制:ADC
适应症:晚期恶性实体瘤
SIBP-A17是上海生物制品研究所自主研发的创新型抗体偶联药物(ADC),具有连接子可裂解、载荷活性强、抗肿瘤“旁观者效应”等药物优势。临床前研究数据显示:SIBP-A17对乳腺癌、胃癌、肺癌、胰腺癌等具有较好的治疗潜力;在动物体内稳定性良好,游离小分子水平显著低于同类产品,具有较好的安全性及耐受性。该产品获批临床拟开发用于难治的或复发的对标准治疗无效的晚期恶性实体瘤。
作用机制:靶向PTK7的ADC
适应症:实体瘤
PRO1107是普方生物正在开发的一款以蛋白酪氨酸激酶7(PTK7)为靶点的ADC,以MMAE作为有效载荷,采用普方生物自主研发的新型亲水性载荷连接子LD343,DAR值为8。PTK7是一种存在于细胞表面的受体蛋白,在肿瘤发生发展中的重要作用,且在肿瘤中的特异表达。PRO1107获批临床拟开发用于实体瘤患者。
作用机制:靶向TL1A的人源化单抗
适应症:溃疡性结肠炎
MK-7240是Prometheus Biosciences开发的一款针对肿瘤坏死因子(TNF)-样配体1A(TL1A)的人源化单克隆抗体。2023年6月,默沙东以总额达108亿美元的款项完成对Prometheus的收购,从而获得这款免疫领域的产品。TL1A是一个与肠炎和纤维化有关的靶标,在免疫调节及炎症性疾病中发挥重要作用。MK-7240在中国获批临床,拟开发用于中度至重度活动性溃疡性结肠炎。
作用机制:CK1α分子胶蛋白降解剂
适应症:髓系恶性肿瘤
GLB-001为格博生物自主研发的一款高选择性的酪蛋白激酶1α(CK1α)口服分子胶蛋白降解剂。CK1α是一种由CSNK1A1基因编码的丝氨酸/苏氨酸蛋白激酶,已被证实对许多不同类型的恶性血液肿瘤和实体瘤的生长和存活至关重要。GLB-001可通过与CRL4CRBN E3泛素连接酶复合物中的底物蛋白受体CRBN相结合,靶向降解CK1α,并触发p53的稳定与蓄积及其下游信号传导通路的激活,导致肿瘤细胞周期停滞和凋亡,发挥抑制肿瘤生长的作用。GLB-001获批临床拟开发用于髓系恶性肿瘤。
作用机制:钾离子竞争性酸阻滞剂
适应症:反流性食管炎
JP-1366(zastaprzan)是由韩国Onconic Therapeutics公司研发的一款创新钾离子竞争性酸阻滞剂(P-CAB),已在韩国提交上市申请。丽珠医药于2023年3月与Onconic达成合作,获得授权可在中国大陆、香港、澳门及台湾地区开发、制造和商业化该产品。JP-1366在中国获批临床拟开发用于治疗反流性食管炎。
作用机制:p300/CBP小分子抑制剂
适应症:血液系统恶性肿瘤
HP537是海创药业自主研发的p300/CBP抑制剂小分子抗肿瘤药物。p300/CBP参与细胞周期进展和细胞生长、分化和发展,在肿瘤中高度表达和激活,是肿瘤细胞生长的关键调控因子。HP537获批临床,拟开发用于血液系统恶性肿瘤,包括但不限于多发性骨髓瘤(MM)、非霍奇金淋巴瘤(NHL)、急性髓系白血病(AML)、骨髓增生异常综合征(MDS)患者。
作用机制:ATR抑制剂
适应症:实体瘤
Camonsertib是Repare公司开发的一款选择性口服ATR抑制剂。ATR全称为共济失调毛细血管扩张突变Rad3相关蛋白,是DNA损伤修复的关键酶之一。研究显示,在ATM缺失的肿瘤细胞中,ATR抑制剂可以产生合成致死效应,在导致ATM缺失肿瘤细胞死亡的同时,并不影响正常细胞。
此外,ATR抑制剂还能与PARP抑制剂联合以增强治疗敏感性。Camonsertib在中国获批临床,拟开发用于实体瘤。除了上述药物,还有一些其它药物也于本周在中国获批临床,限于篇幅,本文不再一一介绍。希望这些药物后续研究顺利进行,早日惠及广大病患。
参考资料:
[1]中国国家药监局药品审评中心(CDE)官网.Retrieved Feb 24,2024, from https://www.cde.org.cn/main/xxgk/listpage/4b5255eb0a84820cef4ca3e8b6bbe20c
[2]各公司官网及公开资料
内容来源于网络,如有侵权,请联系删除。

细胞疗法基因疗法申请上市临床申请免疫疗法
100 项与 aT19(Immunotech Biopharm Ltd.) 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| CD19阳性B细胞急性淋巴细胞白血病 | 临床2期 | 中国 | 2023-12-31 | |
| 复发性 B 细胞急性淋巴细胞白血病 | 临床2期 | 中国 | 2023-12-31 | |
| 难治性 B 细胞急性淋巴细胞白血病 | 临床2期 | 中国 | 2023-12-31 | |
| 急性淋巴细胞白血病 | 临床前 | 中国 | - |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
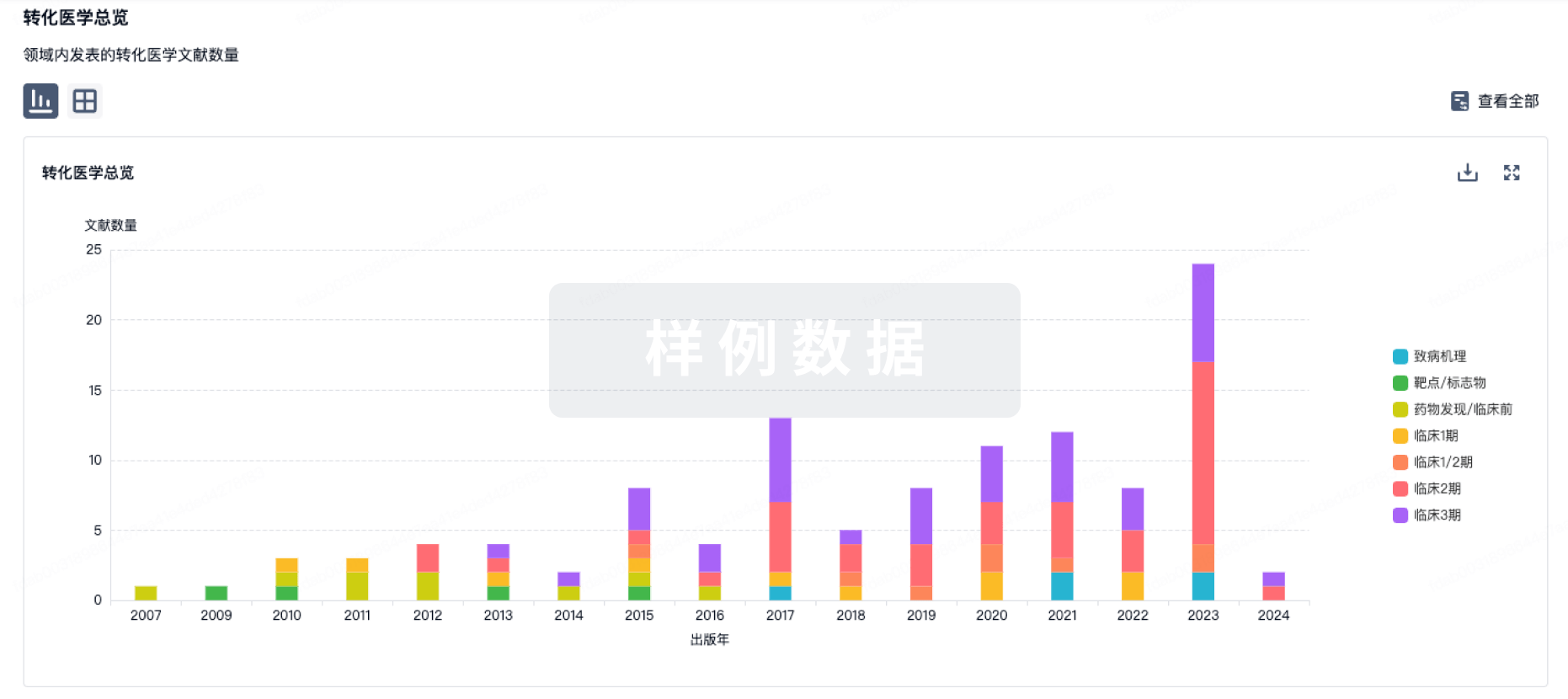
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
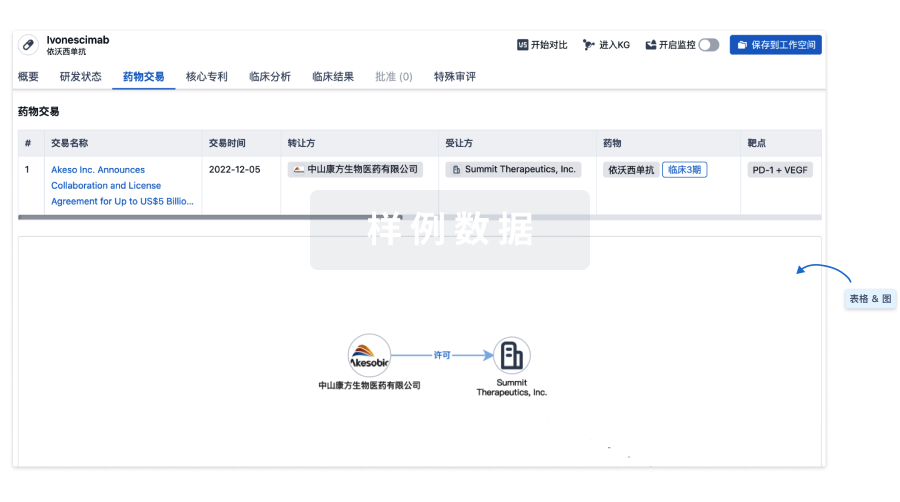
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
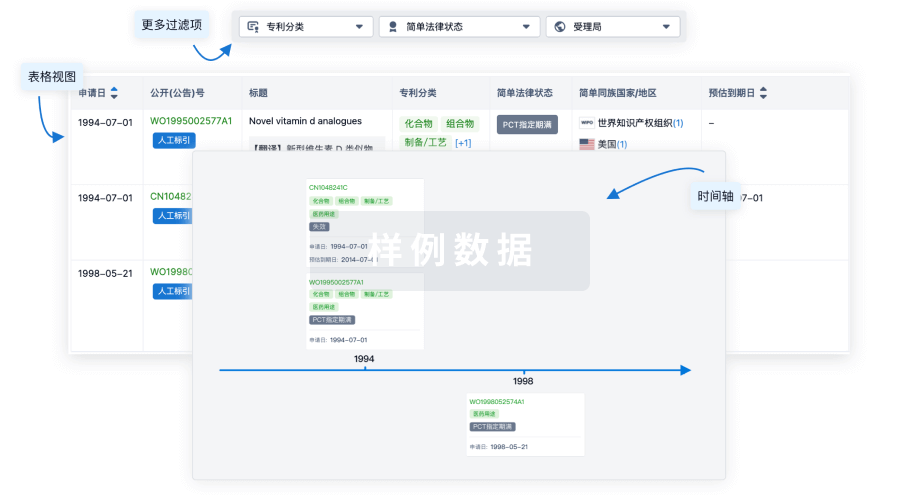
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
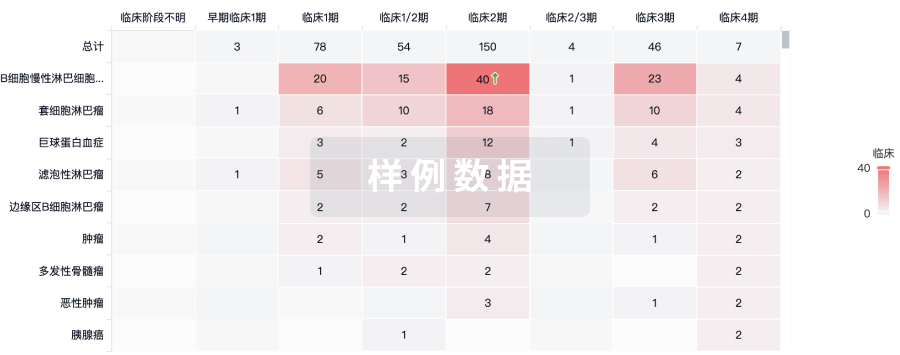
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
批准
利用最新的监管批准信息加速您的研究。
登录
或
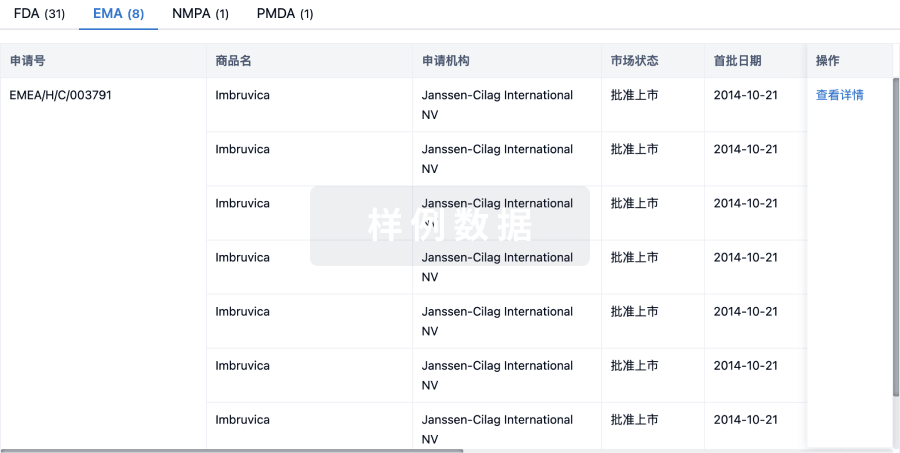
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
