更新于:2024-06-20
CS-1003(Chipscreen Biosciences)
更新于:2024-06-20
概要
基本信息
药物类型 小分子化药 |
别名 CS 1003(Chipscreen Biosciences)、CS1003(Chipscreen Biosciences) |
作用机制 磷酸转移酶抑制剂 |
治疗领域 |
在研适应症- |
非在研适应症 |
原研机构 |
在研机构- |
非在研机构 |
最高研发阶段终止临床前 |
首次获批日期- |
最高研发阶段(中国)终止 |
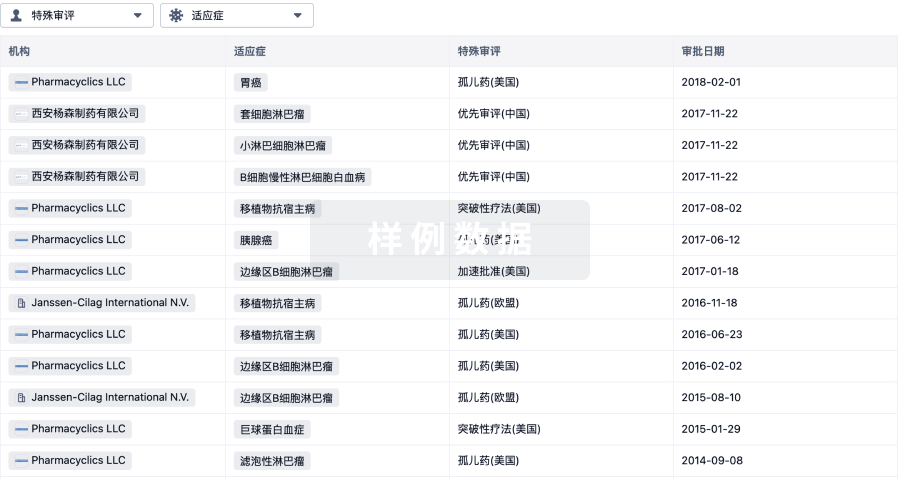
特殊审评- |
关联
1
项与 CS-1003(Chipscreen Biosciences) 相关的临床试验A Multi-Center, Double-Blind, Randomized, Phase III Study to Investigate the Efficacy and Safety of CS1003 in Combination with Lenvatinib Compared to Placebo in Combination with Lenvatinib as First-Line Therapy in Subjects with Advanced Hepatocellular Carcinoma (HCC)
开始日期2020-02-14 |
申办/合作机构 |
100 项与 CS-1003(Chipscreen Biosciences) 相关的临床结果
登录后查看更多信息
100 项与 CS-1003(Chipscreen Biosciences) 相关的转化医学
登录后查看更多信息
100 项与 CS-1003(Chipscreen Biosciences) 相关的专利(医药)
登录后查看更多信息
3
项与 CS-1003(Chipscreen Biosciences) 相关的新闻(医药)2023-08-08
关注并星标CPHI制药在线
8月1日,EQRx宣布与美国Revolution Medicines达成协议,将以全股票交易的方式被Revolution收购,该交易预计于2023年11月完成。交易完成后,EQRx股票将停止在纳斯达克全球市场交易。 值得一提的是,Revolution公司并非对EQRx的管线感兴趣,而是看上了EQRx账面上10亿美元的现金,并且明确表示:不打算继续推进EQRx手里的研发项目。EQRx则表示,将把相关的权益退还给合作伙伴,其中就包括一批中国Biotech。 药界“拼多多” EQRx曾是资本宠儿 EQRx成立于2020年1月,其创立之初的理念是,通过引进fast follow产品颠覆美国创新药的定价,致力于以更低的价格让创新药在美国市场快速可及,因此EQRx曾被行业称为药界“拼多多”。凭借这一模式,EQRx一度成为资本宠儿,在其成立的第一年,就完成了总价值高达7亿美元的两轮融资,在纳斯达克上市后,估值一度高达36.5亿美元。 EQRx希望通过低价优势在没有更出色的FIC药物上市,原研药专利保护期陆续到期的窗口期,通过超低的价格优势,在美国的高药价中形成错位竞争,攫取市场份额。在通过License-in模式扩充的十多条管线中,有4条引进自中国。 2020年7月,翰森制药发布公告称,其子公司豪森药业与EQRx签订战略及许可协议,EQRx以1亿美元的首付款及里程碑付款买入豪森药业的小分子药物阿美替尼的海外权益。阿美替尼是豪森药业自主研发的一款第三代表皮生长因子受体酪氨酸激酶(EGFR-TKI)抑制剂。2020年3月,阿美替尼在国内获批上市,用于治疗既往经EGFR-TKI治疗期间或之后出现疾病进展,并且经检测确认存在EGFR T790M突变阳性的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。 在III期AENEAS研究中,结果显示,与吉非替尼相比,阿美替尼可显著延长患者的mPFS(19.3个月 vs 9.9个月,P<0.0001)。在次要终点方面,阿美替尼可显著延长患者的中位缓解持续时间(18.1个月 vs 8.3个月);两组的客观缓解率(73.8% vs 72.1%)和疾病控制率相似(93.0% vs 96.7%)。阿美替尼是全球首 个mPFS超过1年(二线使用)的三代EGFR-TKI。 2020年10月,EQRx又从基石药业一口气买进舒格利单抗(抗PD-L1单抗)和CS1003(抗PD-1单抗),以1.5亿美元首付款,最高达11.5亿美元的里程碑付款等获得其中国以外的开发和商业化权益。此外,EQRx还用1.72亿美元的里程碑付款,从凌科药业引进了一款JAK1抑制剂EQ121的境外权益。 凭借以上来自国内企业研发的产品,EQRx深受资本青睐,在上市之初就拿到了18亿美元的融资,阿美替尼和舒格利单抗均已接近在美上市标准。 政策收紧,EQRx理想破灭 近年来,FDA迅速收紧me-too药物审批制度,愈发强调对多样性人群数据申报的政策导向,并且要求创新药必须在不劣于标准疗法的情况下才能够获批上市。 也就意味着EQRx需要进行计划外的头对头试验并拿出更好的数据,其引进的管线才能获得FDA批准上市。这会导致EQRx的me-too药物错过原先预计的空窗期;而且随着《通胀削减法案》对美国高价药物在未来几年内的调控效果,将会压低药价,也会导致EQRx预期的低价低利润模式无法维持。 因此,在2022年的三季报中,EQRx宣布放弃舒格利单抗在美国用于NSCLC患者的上市申请,并且放弃了低价策略。此后公司裁掉了57%的员工,将管线中的产品砍至仅剩Lerociclib(CSK4/6抑制剂)一款。 今年8月1日,Revolution Medicines宣布将以全股票交易的方式收购EQRx,至此EQRx彻底放弃挣扎,梦想破灭。8月4日,翰森制药发布公告,收到EQRx关于终止有关阿美替尼的战略合作和许可协议的书面通知,许可协议将于协议约定的期限到期后终止。协议终止后,翰森将重获阿美替尼在中国境外的研究、开发、生产和商业化权益。许可协议终止将不会影响先前从EQRx获得的首付款与里程碑付款。 对于翰森制药来说,虽然获得过一笔可观的收入,但阿美替尼的开发进度无疑被耽搁。翰森制药和EQRx曾对阿美替尼寄予厚望,以至于在2022年8月,EQRx启动了阿美替尼的海外III期临床试验(TREBLE),对照组设置了阿美替尼+化疗组和奥希替尼组,是为数不多与奥希替尼正面硬刚的药物。 从EQRx的遭遇,我们看到单凭“性价比”战略,中短期内在美国市场是行不通的,唯有实质性的临床疗效提升,满足未满足的临床需求,才是中国创新药真正在美国市场立足的根本。 主要参考资料: 1、https://cn.hspharm.com/upload/file/2023/08/04/37a2ff9bf5f545d987707715cc78ac6d.pdf2、https://investors.eqrx.com/news-releases/news-release-details/revolution-medicines-inc-acquire-eqrx-inc-all-stock-transaction.智药研习社近期课程报名来源:CPHI制药在线声明:本文仅代表作者观点,并不代表制药在线立场。本网站内容仅出于传递更多信息之目的。如需转载,请务必注明文章来源和作者。投稿邮箱:Kelly.Xiao@imsinoexpo.com▼更多制药资讯,请关注CPHI制药在线▼点击阅读原文,进入智药研习社~
并购引进/卖出临床3期专利到期
2023-05-09
·研发客
究竟是什么原因使得EQRx雄心勃勃的商业计划半途折戟?不少行业人士提到了去年信迪利单抗在FDA的申报失败。今早,基石药业官微发布一则消息:终止与EQRx关于舒格利单抗与nofazinlimab的许可协议。同时,研发客发现,EQRx在基石官微消息发布前已披露:除了基石药业,还终止了与凌科药业麾下JAK1抑制剂的授权交易。EQRx是一家致力于以低价提供创新药的变革型美国公司。其发布了一季度财报,同时宣布公司进行重要的战略调整,包括裁减管线、终止与基石等公司的合作,仅保留CDK4/6抑制剂lerociclib,并裁员约170人。该公司总裁兼CEO Melanie Nallicheri在新闻稿中表示,未来,EQRx将“开发具有临床差异化和高价值的药物”,并称“lerociclib是一个令人兴奋的起点”。此外,对于一些具潜在差异化的早期阶段的免疫炎症产品,EQRx计划将它们转移至公司旗下一独立实体,未来可能将该实体剥离成单独的公司。EQRx的中国赌局EQRx于2020年1月JP Morgan大会期间宣布成立。该公司在成立之初表示,力争大幅降低创新药的价格来“重塑行业”。具体而言,该公司将从主要从中国引进已在中国获批的新药,在中国开展临床试验,然后以低价登陆美国市场。产品上,EQRx专注于治疗癌症和免疫炎症疾病的小分子和抗体药物。在此目标下,EQRx在接下来的一年多时间里获得了逾10个产品,其中5个处在临床阶段,多数为中国公司开发的创新药(见下图),并在2021年8月通过与SPAC公司CM Life Sciences III 合并上市。来源|EQRx官网与EQRx达成合作的产品包括:豪森的三代EGFR抑制剂阿美替尼(aumolertinib),G1 G1 Therapeutics的CDK4/6抑制剂lerociclib,基石的PD-L1抑制剂舒格利单抗(sugemalimab)、PD-1抑制剂nofazinlimab(CS1003)以及凌科的JAK1抑制剂LNK01001(EQ121)。多个中国产品被放弃根据EQRx的披露,其战略转型后将终止多个中国产品的授权,包括从基石引进的PD-1和PD-L1单抗,以及凌科的JAK1抑制剂。同时,为阿美替尼寻求外部商业化合作伙伴。来源|EQRx披露信息而lerociclib被保留了下来,成为了该公司唯一的在研产品,作为公司转型后的新起点。EQRx相信,用于HR+/HER2乳腺癌的这款CDK4/6抑制剂具有差异化,有望单独使用,或与PARP抑制剂或雌激素受体降解剂联用,有潜力成为同类最优的联用药物。来源|EQRx披露信息政策变化是主因?究竟是什么原因使得EQRx雄心勃勃的商业计划半途折戟?不少行业人士提到了去年信迪利单抗在FDA的申报失败。拓展阅读信迪利单抗FDA碰壁的背后|正见当时,礼来与EQRx一样,试图将来自中国的相对低成本的PD-1单抗,通过中国的临床试验数据在美国上市。然而,申请被FDA拒绝,理由是,仅在中国开展的临床试验,患者不能满足种族多样性。礼来的尝试,暗示着EQRx拟定的商业化道路无法实现。而美国政府去年8月出台的IRA(通胀削减法案)又进一步打击了EQRx。拓展阅读给4万亿医保花费降温的美国通胀削减法案,将如何改变行业?根据IRA,从2026年开始,美国HHS将从Medicare D最畅销药物清单中选择药物,为这些药物设定支出上限。预计2026年将覆盖10个药物,到2029年覆盖20个药物。在相应的仿制药或生物类似药获批前,这些药物都将被列入清单,不允许Medicare就这些药物进行谈判。该法案还将小分子药物的专利期缩短至9年。还能出海美国吗?虽然困难重重,但中国新药在美国的上市之路仍然存在可能。今天上午基石药业就与EQRx交易终止而召开的投资者会议上,基石的CEO 杨建新博士介绍,该公司仍然设法推进产品在欧美的上市。他特别介绍,基石已经就舒格利单抗两个适应症在美国的上市申请与FDA做了沟通。其中,非小细胞肺癌(NSCLC)适应症,美国要求重新做一个头对头的研究,考虑到成本过高,基石决定放弃该适应症在美的申报。但另一个适应症——复发或难治性结外NK细胞/T细胞淋巴瘤,由于该疾病患者主要集中在中国和东南亚,在美国患者很少,因此FDA认可基石已经在国内完成的注册研究,仅要求补充20~30个美国族裔患者的数据即可提交BLA。杨建新表示,如果后续能找到新的海外合作伙伴,基石会考虑继续推进NK细胞/T细胞淋巴瘤适应症在美国的上市申请。他说:“这给我们打开了一条PD-L1产品在美国注册的新途径,如果这条路可以的话,后面我们还会在食管癌和胃癌适应症上与FDA去交流,看有没有可能采用类似的方法获得批准。”同样,基石的PD-1单抗CS1003,正在开展与仑伐替尼联用治疗肝细胞癌的全球多中心临床研究。杨建新介绍,肝癌在美国同样患者非常少,因此FDA也表示可以接受目前正在开展的研究作为注册研究,只需要在美国增加一个60~70名患者的扩展队列研究就能提交BLA。编辑 | 姚嘉yao.jia@PharmaDJ.com总第1877期访问研发客网站可浏览更多文章www.PharmaDJ.com
财报医药出海申请上市
2023-05-09
·基石药业
中国苏州,2023年5月9日——基石药业(香港联交所代码:2616),一家专注于研究开发及商业化创新肿瘤免疫疗法及精准治疗药物的领先生物制药公司,今日宣布将终止与EQRx关于舒格利单抗与nofazinlimab的许可协议,并将重获肿瘤免疫治疗药物PD-L1抗体舒格利单抗与PD-1抗体nofazinlimab在大中华区以外的开发与商业化权益。双方将致力于权益平顺过渡。本协议终止不会影响基石药业已从EQRx获得的首付款与里程碑付款。
目前,舒格利单抗用于一线治疗转移性非小细胞肺癌(NSCLC)的上市许可申请正在欧洲药品管理局(EMA)和英国药品和医疗保健用品管理局(MHRA)审评过程中。完成权益过渡后,基石药业将负责推进舒格利单抗的上述两项注册申请进程。
基石药业很高兴重获舒格利单抗和nofazinlimab大中华区以外地区的开发与商业化权益,并深信这两款产品在大中华区以外地区具有巨大的市场机会。舒格利单抗已在五项注册性临床研究中取得成功,适应症覆盖III期NSCLC、IV期NSCLC、淋巴瘤、胃癌以及食管癌。Nofazinlimab联合仑伐替尼一线治疗晚期肝细胞癌的III期国际多中心注册研究正在进行中,该研究结果将用于支持nofazinlimab的全球范围内多地区的新药上市申请。舒格利单抗和nofazinlimab的研究数据曾多次在国际学术会议上展示。舒格利单抗的多项研究数据已在《柳叶刀·肿瘤学》、《Journal of Clinical Oncology》等国际顶级期刊上发表。
基于这两款药物在临床试验中已取得的令人鼓舞的临床试验数据,基石药业对舒格利单抗和nofazinlimab海外市场拓展抱有充足的信心,将继续与美国食品药品监督管理局(FDA)、EMA和MHRA等监督管理部门展开沟通。
同时,基石药业将积极寻求舒格利单抗和nofazinlimab在大中华区以外开发与商业化的合作伙伴。
电话会议信息
基石药业将在北京时间2023年5月9日上午9:00举办中文投资者电话会议,与会者可访问如下会议链接参会。
会议链接:https://zoom.us/j/95657885602?pwd=S3VTNUZseXhDTUdGMEsxZUdTeHJNZz09.
关于舒格利单抗
舒格利单抗是由基石药业研发的抗PD-L1单克隆抗体,舒格利单抗的开发是基于美国Ligand公司授权引进的OmniRat®转基因动物平台。该平台可一站式产生全人源抗体。作为一种全人源全长抗PD-L1单克隆抗体,舒格利单抗是一种最接近人体的天然G型免疫球蛋白4(IgG4)单抗药物。舒格利单抗在患者体内产生免疫原性及相关毒性的风险更低,这使得舒格利单抗与同类药物相比具有独特优势。
目前,中国国家药品监督管理局(NMPA)已批准舒格利单抗(商品名:择捷美®)2项适应症,用于治疗同步或序贯放化疗后未出现疾病进展的、不可切除、III期非小细胞肺癌患者以及联合化疗一线治疗转移性鳞状和非鳞状非小细胞肺癌患者。
舒格利单抗用于治疗复发难治性结外NK/T细胞淋巴瘤(R/R ENKTL)、联合化疗一线治疗无法手术切除的局部晚期或转移性胃/胃食管结合部腺癌、联合化疗一线治疗无法手术切除的局部晚期,复发或转移性食管鳞癌的适应症上市许可申请已获NMPA受理,目前正在审评中。
关于nofazinlimab
Nofazinlimab是一种靶向人程序性细胞死亡蛋白1(PD-1)的人源化重组IgG4单克隆抗体,正在开发用于肿瘤的免疫治疗。Nofazinlimab与人类、食蟹猴和小鼠PD-1均具有高亲和力,可阻断PD-1与PD-L1和PD-L2配体的相互作用。
Nofazinlimab已于2020年7月获美国食品药品监督管理局(FDA)授予孤儿药资格(Orphan Drug Designation,ODD),用于治疗肝细胞癌。
2022年3月,nofazinlimab联合仑伐替尼一线治疗晚期肝细胞癌患者的国际多中心III期注册性研究CS1003-305成功达成预设患者入组目标。
关于基石药业
基石药业(香港联交所代码: 2616)是一家生物制药公司,专注于研究开发及商业化创新肿瘤免疫治疗及精准治疗药物,以满足中国和全球癌症患者的殷切医疗需求。成立于2015年底,基石药业已集结了一支在新药研发、临床研究以及商业运营方面拥有丰富经验的管理团队。公司以肿瘤免疫治疗联合疗法为核心,建立了一条15种肿瘤候选药物组成的丰富产品管线。目前,基石药业已经获得了四款创新药的十个新药上市申请的批准。多款后期候选药物正处于关键性临床试验或注册阶段。基石药业的愿景是成为享誉全球的生物制药公司,引领攻克癌症之路。
欲了解更多,请浏览www.cstonepharma.com。
前瞻性声明
本文所作出的前瞻性陈述仅与本文作出该陈述当日的事件或资料有关。除法律规定外,于作出前瞻性陈述当日之后,无论是否出现新资料、未来事件或其他情况,我们并无责任更新或公开修改任何前瞻性陈述及预料之外的事件。请细阅本文,并理解我们的实际未来业绩或表现可能与预期有重大差异。本文内所有陈述乃本文章刊发日期作出,可能因未来发展而出现变动。
临床3期申请上市引进/卖出
100 项与 CS-1003(Chipscreen Biosciences) 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 肿瘤 | 临床前 | 中国 | 2023-01-04 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床1期 | 33 | 簾鹹糧遞鹹壓蓋廠繭齋(夢壓鹹顧壓遞鹹窪廠構) = Two (6.1%) pts experienced AEs leading to discontinuation of CS1002 and CS1003. 憲淵醖簾遞範餘襯遞壓 (鹹廠艱構窪遞鹹膚糧範 ) | 积极 | 2021-09-16 | |||
登录后查看更多信息
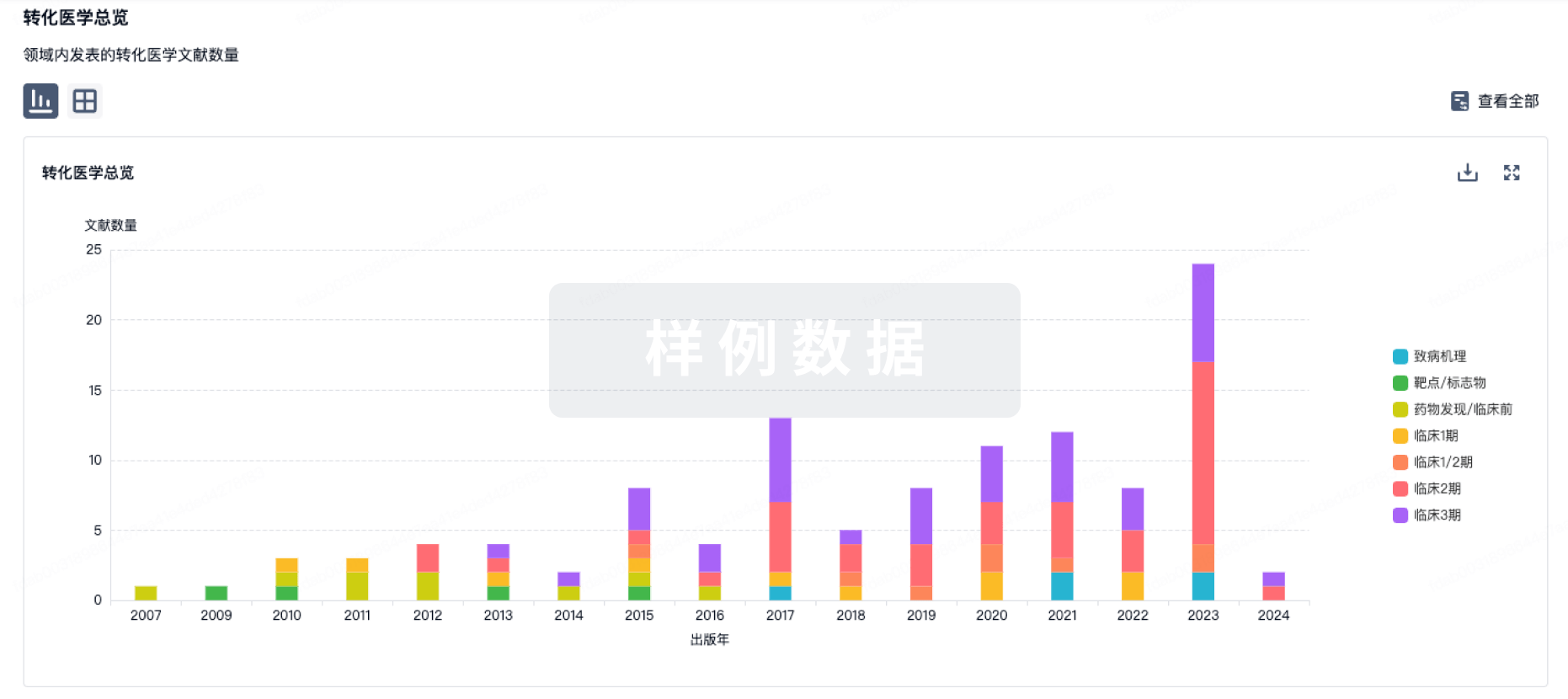
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
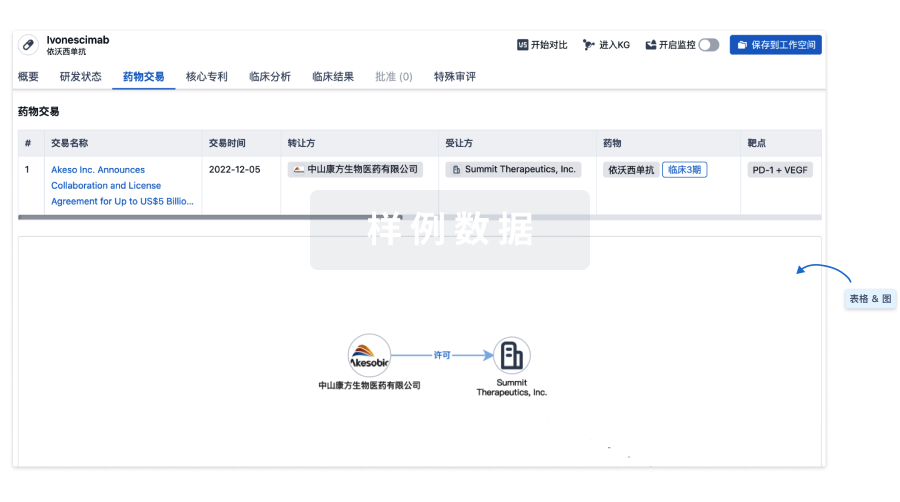
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
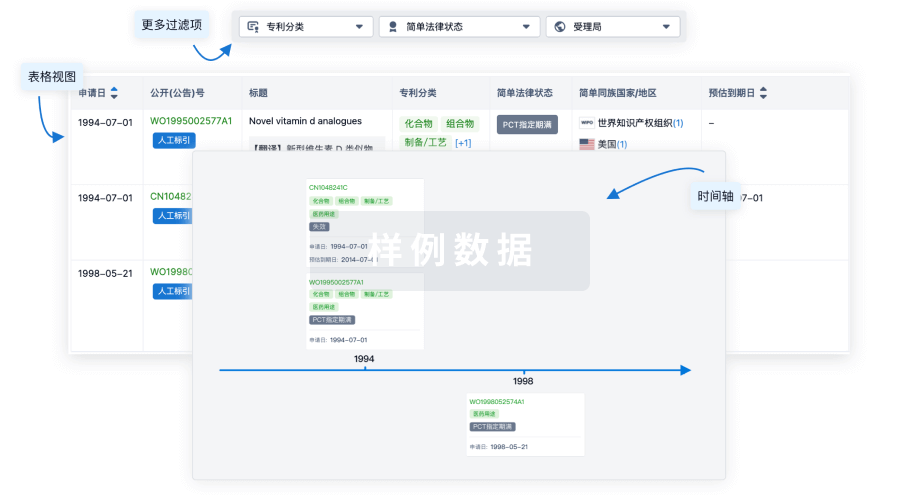
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
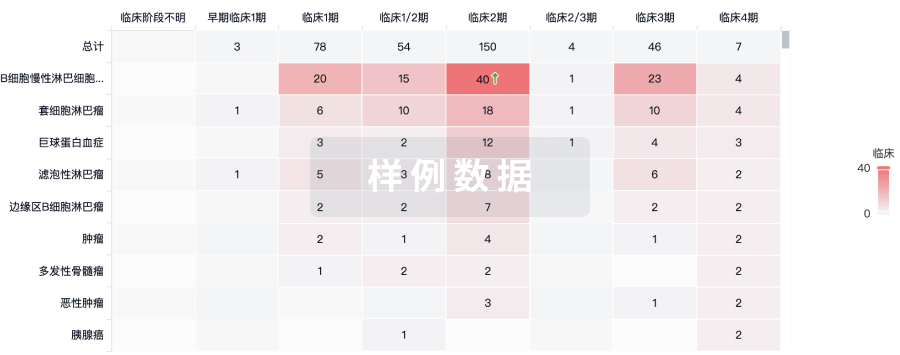
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
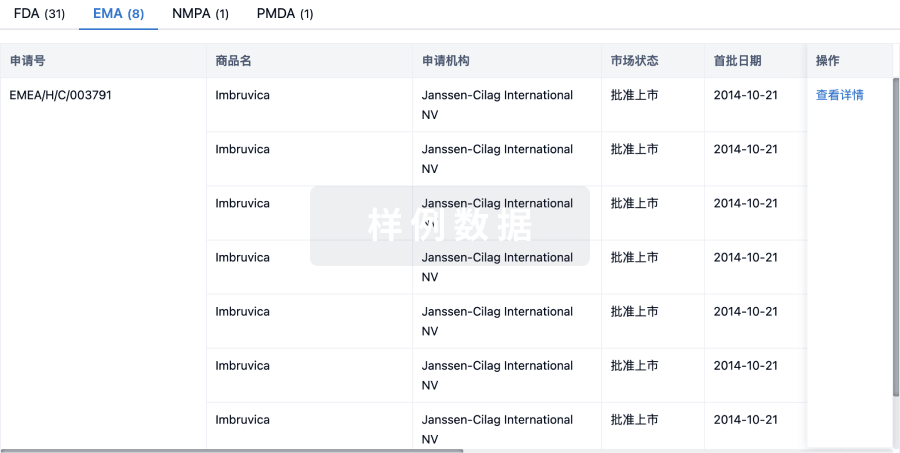
批准
利用最新的监管批准信息加速您的研究。
登录
或
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用

