更新于:2024-06-20
Omalizumab biosimilar (Reliance Life Sciences )
奥马珠单抗生物类似药 (Reliance Life Sciences)
更新于:2024-06-20
概要
基本信息
非在研机构- |
最高研发阶段临床前 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
序列信息
Sequence Code 81670L

当前序列信息引自: *****
Sequence Code 143601H

当前序列信息引自: *****
关联
100 项与 奥马珠单抗生物类似药 (Reliance Life Sciences) 相关的临床结果
登录后查看更多信息
100 项与 奥马珠单抗生物类似药 (Reliance Life Sciences) 相关的转化医学
登录后查看更多信息
100 项与 奥马珠单抗生物类似药 (Reliance Life Sciences) 相关的专利(医药)
登录后查看更多信息
3
项与 奥马珠单抗生物类似药 (Reliance Life Sciences) 相关的新闻(医药)2024-03-12
·药研发
「 本文共:16条资讯,阅读时长约:3分钟 」今日头条科伦广谱抗耐药新药获快速通道资格。科伦药业第二代选择性RET抑制剂A400(EP0031,KL590586)获FDA授予的快速通道资格,用于治疗RET融合阳性非小细胞肺癌(NSCLC)。A400对常见的RET基因融合和突变具有广泛活性,具有克服第一代选择性RET抑制剂耐药的潜力。去年11月,该新药已获得FDA授予治疗RET融合阳性实体瘤的孤儿药资格。值得一提的是,科伦博泰已将该产品在欧美等区域的权益独家授权给Ellipses公司。国内药讯1.恒瑞JAK1抑制剂湿疹Ⅲ期临床成功。恒瑞医药JAK1抑制剂艾玛昔替尼(SHR0302)在AAD2024年会上公布了用于治疗中重度特应性皮炎(AD)的Ⅲ期临床长期结果。该项试验在第16周时已达到共同主要终点。52周数据显示,SHR0302(4mg和8mg)治疗患者的研究者总体评估(IGA)应答率(42.3%和40.2%)与湿疹面积和严重度指数改善75%应答率(EASI-75,60.6%和55.9%)持续保持;患者WI-NRS应答率也维持稳定(59.6%和45.1%)。此外,16周-52周期间,未出现新的安全信号。2.和黄妇科肿瘤新药拟纳入优先审评。和黄医药VEGFR抑制剂呋喹替尼胶囊与信达生物PD-1抑制剂信迪利单抗构成的组合方案,获CDE拟纳入优先审评,用于既往系统性抗肿瘤治疗后疾病进展且不适合进行根治性手术治疗或根治性放疗的晚期pMMR或non MSI-H子宫内膜癌患者。去年7月,这一组合用于治疗既往至少一线含铂治疗失败的pMMR晚期子宫内膜癌患者已被CDE纳入突破性治疗品种。3.华东GLP-1R/GIPR激动剂获批IND。华东医药旗下杭州中美华东1类化药HDM1005注射液获国家药监局临床许可,拟开发用于2型糖尿病和超重或肥胖人群体重管理。HDM1005是一款GLP-1R/GIPR双靶点激动剂,可通过激活GLP-1受体和GIP受体,促进胰岛素释放,抑制食欲,具有降糖和减重的潜力。临床前研究数据也显示,HDM1005具有良好的成药性和安全性。4.先声中美双报三抗获批临床。先声药业自主研发的GPRC5D/BCMA/CD3三特异性抗体SIM0500获FDA临床许可,即将在美国开展用于治疗复发或难治性多发性骨髓瘤的新药研究。在临床前研究中,SIM0500已显示出比GPRC5D/CD3双抗以及BCMA/CD3双抗有更好的肿瘤杀伤效果,可潜在克服现有治疗手段所导致的耐药。今年1月,该新药的临床试验申请已获得CDE受理。5.上海健信两款双抗获批临床。健信生物自主研发的核心产品注射用重组抗PD1/TIM3人源化双特异抗体(Bis5,LB1410)和注射用LB4330(Bis2)的联合治疗方案获国家药监局临床默示许可,拟开展用于治疗晚期/转移性实体瘤的Ib/II期临床试验。这两款新药均已完成单药I期临床爬坡研究,正在进行多种肿瘤疗效扩展研究。Bis2是一款靶向肿瘤CD8+T细胞和CLDN18.2的双功能免疫治疗产品。6.捷思英达引进肿瘤抑制剂获批IND。捷思英达1类化药Aurora A抑制剂VIC-1911片获国家药监局临床默示许可,将开展VIC-1911单药/联合奥拉帕利治疗晚期乳腺癌的临床研究。VIC-1911最初由日本Taiho公司开发(TAS-119),捷思英达美国子公司VITRAC拥有该药在肿瘤领域的全球独家权益。在美国,VIC-1911已处于I/II期开发阶段,并已被证明没有明显的骨髓抑制毒副作用。国际药讯1.首款奥马珠单抗生物类似药报产。Celltrion USA公司奥马珠单抗生物类似药CT-P39已向FDA提交上市申请(BLA),作为Xolair(奥马珠单抗)的可互换生物类似药,用于治疗哮喘、慢性鼻-鼻窦炎伴鼻息肉(CRSwNP)、IgE介导的食物过敏(仅限美国)和慢性自发性荨麻疹(CSU)。在国际III期CT-P39 3.1研究中,与Xolair相比,CT-P39组患者的每周瘙痒严重程度评分(ISS7)较于基线变化的疗效相当(-9.21 vs. -9.98)。2.强生引进银屑病口服多肽长期疗效积极。强生与Protagonist公司开发的IL-23R拮抗多肽JNJ-2113治疗中重度斑块状银屑病(PsO)的Ⅱb期临床扩展研究FRONTIER 2结果积极。数据显示,JNJ-2113治疗组的缓解率从第16周维持到第52周,其中JNJ-2113(每天两次100mg)队列保持PASI 75应答的患者比例达到76.2%(第16周为78.6%)。临床中未发现新的安全性信号。目前,JNJ-2113也在Ⅱb期ANTHEM-UC研究中评估治疗中重度活动性溃疡性结肠炎的潜力。3.礼来创新单抗湿疹Ⅲ期临床积极。礼来IL-13抑制剂lebrikizumab治疗中重度特应性皮炎的Ⅲ期试验达到主要终点。第16周时,lebrikizumab治疗实现湿疹面积和严重程度指数相对基线降低75%(EASI-75)的患者比例达到68%;有56%患者的瘙痒数字评定量表[PNRS]的评分改善≥4分。研究中,没有观察到新的安全信号与严重的不良事件,详细结果将在医学会议上公布。4.银屑病关节炎拮抗剂Ⅱb/Ⅲ期临床积极。ACELYRIN公司IL-17A融合蛋白拮抗剂izokibep治疗银屑病关节炎(PsA)的国际Ⅱb/Ⅲ期临床达到复合主要终点。第16周时,izokibep(160mg Q2W、160mg QW)治疗患者达成美国风湿病学会(ACR)50应答标准的比例显著高于安慰剂(43%和40%,vs15%);达成银屑病面积与严重程度指数(PASI)改善100%(PASI100)的患者比例也更高(47%和51%,vs12%)。此外,izokibep耐受性良好,与已知研究结果一致。5.Incyte公司痒疹性结节新药Ⅱ期临床成功。Incyte公司口服JAK1抑制剂povorcitinib治疗痒疹性结节(PN)的Ⅱ期临床达到主要和次要终点。与安慰剂相比,povorcitinib(15mg、45mg和75mg)治疗患者第16周时瘙痒数字评估量表(NRS4)评分改善≥4点的比例更高(36.1%、44.4%和54.1%,vs8.1%);达到研究者总体评估治疗成功(IGA-TS)得分为0或1,且从基线起改善≥2级的患者比例更多(13.9%、30.6%和48.6%,vs5.4%)。Povorcitinib总体耐受性良好。6.MoonLake公司纳米抗体Ⅱ期临床积极。MoonLake公司靶向IL17A/F三特异性纳米抗体sonelokimab治疗银屑病关节炎(PsA)的Ⅱ期临床ARGO达到主要终点。第24周时,sonelokimab治疗达成美国风湿病学会(ACR)50应答的患者比例超过60%,有40%的患者达到ACR70应答;达到ACR50+PASI 90标准的患者比例高达59%,ACR50+PASI 100高达52%,ACR70+PASI 100高达48%。Sonelokimab由三个抗体重链可变区蛋白域共价连接而成。医药热点1.中疾控原主任高福加盟浙大。根据浙江大学公开资料显示,中国疾病预防控制中心原主任高福院士已出任浙江大学大健康学院院长。3月14日,高福院士将于浙江大学大健康学院为本科生开讲“求是大讲堂”通识课程第六课。除浙江大学大健康学院院长外,高福目前还是中国科学院病原微生物与免疫学重点实验室主任、中国生物工程学会理事长、中华医学会副会长。2.广东省中医院又一临床科室成立。3月8日,广东省中医院举行康复科大科成立大会。康复科大科涵盖大学城医院康复科、大德路总院康复科、语言认知中心、理疗科、珠海医院康复科,由2个住院部和5个门诊部组成,开放床位84张。拥有医护治人员共148人。欧海宁任康复科大科主任。康复科大科旨在构建从“急性期-恢复期-后遗症期”全程康复立体诊疗模式,为各种功能障碍患者提供最优最及时的中西医结合综合康复方案。3.韩国向4944名拒绝复工医生发吊销执照通知。据韩联社等媒体11日报道,政府已向近5000名拒绝复工的医生发送吊销执照通知,并决定从当天起向20家医院派遣20名军医官、138名公共卫生医师,以解燃眉之急。截至8日,韩国保健福祉部共向4944名拒绝复工的实习和住院医师发送吊销医师执照的预告通知,并正在向其余罢工医生逐一发送该通知。此外,为协助已复职或有意复职的医生,韩国政府将于12日起设立运营“保护与举报中心”,并开通电话和短信举报热线。评审动态 1. CDE新药受理情况(03月12) 2. FDA新药获批情况(北美03月11日)股市资讯上个交易日 A 股医药板块 +1.58%涨幅前三 跌幅前三长药控股+20.08% *ST 太安-5.03%佐力药业+20.00% 羚锐制药-4.80%香雪制药+19.95% 海 思 科 -3.41%【百奥泰】于近日收到国家药品监督管理局核准签发的《药物临床试验批准通知书》,公司在研药品BAT8008联合BAT1308治疗晚期实体瘤的临床试验申请获得批准。【新华制药】收到国家药品监督管理局核准签发的布洛芬缓释胶囊《药品注册证书》。【兴齐眼药】公司收到了国家药品监督管理局重新签发的硫酸阿托品滴眼液《药品注册证书》,药品批准文号由国药准字H20240320更正为国药准字 H20243320。- The End -戳“阅读原文”,了解更多医药研发及股市资讯。
临床3期优先审批快速通道突破性疗法孤儿药
2024-03-11
·医药魔方
3月10日,Celltrion USA宣布已向FDA提交CT-P39的生物制品许可申请(BLA),用于治疗哮喘、慢性鼻-鼻窦炎伴鼻息肉(CRSwNP)、IgE介导的食物过敏(仅限美国)和慢性自发性荨麻疹(CSU)。该产品是Xolair(奥马珠单抗)的可互换生物类似药。此次BLA主要是基于全球性III期CT-P39 3.1研究的结果。该研究评估了CT-P39对比参照药Xolair在CSU患者中的疗效、安全性和药代动力学。结果显示,CT-P39组和Xolair组患者的每周瘙痒严重程度评分(ISS7)相比于基线的变化的疗效差异(-9.21 vs. -9.98)在[-2.0, 2.0]的等效置信区间内。安全性方面,两组之间的治疗期间不良事件(TEAE)发生率也相似(25.6% vs. 26.3%)。根据罗氏和诺华财报,2023年Xolair的全球销售额为38.95亿美元。奥马珠单抗的化合物专利已经到期,其配方专利将于2025年11月在美国到期。目前,全球范围内已有3款奥马珠单抗生物类似药获批上市,其中1款来自迈博太科。此外,石药集团的奥马珠单抗生物类似药SYN008也已申报上市。 推荐阅读第2款托珠单抗生物类似药在美申报上市石药集团「奥马珠单抗」申报上市济民可信获得迈博药业奥马珠单抗药物中国市场独家推广权Copyright © 2024 PHARMCUBE. All Rights Reserved.欢迎转发分享及合理引用,引用时请在显要位置标明文章来源;如需转载,请给微信公众号后台留言或发送消息,并注明公众号名称及ID。免责申明:本微信文章中的信息仅供一般参考之用,不可直接作为决策内容,医药魔方不对任何主体因使用本文内容而导致的任何损失承担责任。↑长按识别二维码 / 扫码即可报名↑
财报生物类似药专利到期临床3期
2024-02-29
·同写意
为打造全球ADC/RDC未来产业高地,成都医学城拟于2024年4月18日-19日举办首届未来XDC新药大会!大会以“共创偶联药物产业未来”为主题,由同写意策划,安排一场主论坛和九场主题论坛,邀请“政、产、学、研、金、媒”各领域专家,通过“成果发布、主题演讲、热点对话、表彰颁奖、展览展示”五位一体的多元化的组织形式,迸发更多XDC产业新科技、新业态、新模式,构建XDC产业全新生态,触摸医药产业未来脉动。凭借石药集团的资本加码,新诺威投资者喜迎泼天富贵,2023年股价暴涨320%,市值一度超过560亿元。石药集团虽然知名度没有恒瑞医药高,但整体营收已经超越恒瑞,坐稳国内药企第一梯队。如此一家老牌头部制药公司,为何会选择如今这个时间点进行大手笔资本操作?一番操作过后,新诺威又将成为一家怎样的公司?这将是本文探讨的两个核心问题。1“借尸还魂”中国医药产业正处于前所未有的寒冬之中。伴随资本市场中医药公司市值的不断下降,投资者情绪已经到了崩溃边缘。新年之后,证监会紧急召开系列座谈会,就加强资本市场监管、防范化解风险、推动资本市场高质量发展广泛听取各方面意见建议。最终形成了未来工作的七大发力点:严把IPO准入关,全方位立体式追责,鼓励上市公司加大分红力度,完善退市制度,引导中长期资金入市,完善行业机构监管模式,加快权益类产品注册节奏。这些动作中,IPO收紧无疑是影响最为深远的。自2007年以来,A股市场的股票数量从1459家猛增到5200家,尤其是科创板四年发新股546家,增加市值供应6.41万亿。IPO过量发行,俨然成为投资者诟病的重点。如此背景下,IPO收紧自然是预料之中的事。极端行情下,创新企业生存压力倍增,融资难度飙升,整个产业都陷入悲观情绪。不过希望往往就孕育在绝望之中,寒冬的另一面则是极具性价比的管线价格。换句话说,中国医药产业都正在进入BD交易黄金期。当大多数企业无法获得融资时,融资能力就成为企业核心竞争力。虽然A股IPO渠道正在关闭,但老谋深算的石药集团早已埋下新诺威这个“种子”,这也使得其能够规避IPO政策,转而选择一条独特的“幽径”。借助早已上市的子公司新诺威,石药集团可以将体内极具价值的热门资产转移回A股,从而获得更高的市场关注度与估值水平,最终实现吸引投资的目的。2023年8月底,新诺威公告正在筹划对巨石生物实施现金增资,以取得巨石生物51%以上的股权,并实现对其控股;9月,新诺威公布增资方案,以现金方式增资,总金额18.71亿元,其中10.41亿元计入巨石生物注册资本,8.3亿元计入巨石生物资本公积。消息一经落地,新诺威市值便开启爬坡模式。以8月30日12.78元/股的收盘价,至12月6日股价创下历史最高的48.74元/股计算,两个月时间,新诺威股价暴涨281%。注入巨石生物后,新诺威由原来的保健品和原料药制造商摇身一变成为Biotech(生物科技)潜力新星,公司名称也迫不及待变更为“石药创新制药股份有限公司”。然而这还并非石药集团的全部操作。1月10日,新诺威再次发布公告,筹划发行股份及支付现金购买资产并募集配套资金,因构成重大资产重组而停牌。这次收购的对象又是石药集团旗下资产——石药百克100%股权。根据公布的交易预案,此项收购交易中现金支付比例不超过10%,其余部分以发行股份方式支付。两次收购案之后,新诺威早已换了另外一副面貌。2怎样的资产?在石药集团注入资产之前,新诺威仅是一家以功能性原料及保健食品为主的大健康公司。虽然公司也拥有二十亿级别营收及数亿元利润,但其本质还是一家想象空间有限的原料公司。因此在资本市场中,新诺威股价始终不温不火。经过石药集团的“闪转腾挪”,新诺威“高大威猛”的形象逐渐开始浮现。巨石生物虽未能独立IPO,但单论目前的战绩丝毫不逊色于一些明星Biotech公司,其中最耀眼的成绩便是成功斩获国内首款新冠mRNA疫苗。除新冠mRNA疫苗外,巨石生物在研项目20余个,有8款产品在国内开展不同阶段临床试验或正在申报上市,其中2款处申报上市阶段,3款处于临床II/III期,5款处临床I期。聚焦巨石生物研发管线布局,可谓鳞次栉比。首先,PD-1和一众生物类似药是巨石生物的根基,有望凭借短期上市预期,成为护城河。具体来看,PD-1恩朗苏拜单抗已经递交上市申请,有望于今年获批上市,首发适应症为宫颈癌,目前国内获批该适应症的厂家有誉衡生物。生物类似药中,奥马珠单抗已递交上市申请,预计2024年获批,有望斩获首款国产奥马珠单抗生物类似药;后续管线中还有乌司奴单抗类似药、帕妥珠单抗类似药,均已进入临床III期。图:巨石生物在研单抗管线,来源:华泰证券其次,巨石生物还有ADC管线作为X因素。巨石生物的ADC技术平台采用酶法定点偶联的技术,目前已有四款ADC产品进入临床阶段,分别涉及HER2、Nectin4、CLDN18.2、EGFR靶点,此外还包括三款临床前管线,涉及ROR1、HER3、HER2分子胶靶点。进展最快的HER2 ADC目前已处于临床III期,有望在2025年批准上市。图:巨石生物的ADC在研管线,来源:华泰证券自2022年以来,巨石生物的两款处于I期临床的ADC药物已经实现license-out出海。其中CDLN18.2靶点ADC药物SYSA1801为公司带来2700万美元首付款,11.5亿美元的里程碑付款;Nectin4靶点ADC药物SYS6002为公司带来750万美元首付款,6.85亿美元里程碑付款。最后,巨石生物还拥有mRNA这个长期布局的技术平台。短期内,mRNA并不能实现商业化目的,但也留下了炒作空间。巨石生物主要拥有7款mRNA疫苗品种,在新冠mRNA疫苗后,在研重磅仍有狂犬、呼吸道合胞病毒、带状疱疹、HPV治疗苗等,其中狂犬/呼吸道合胞病毒疫苗已申报临床。图:巨石生物mRNA管线一览,来源:华泰证券研报此外,并购石药百克则多了更多概念标签。石药百克是石药集团最大的生物医药产业基地之一,已上市产品“津优力”(聚乙二醇化重组人粒细胞刺激因子注射液)是国家生物1类新药,也是石药集团原有的三大核心产品之一。根据药渡数据显示,2021-2023年上半年,津优力销售额分别为23.31亿元(市占率38.16%)、25.99亿元(市占率40.12%)和13.6亿元(市占率38.74%)。石药百克拥有7个以上在研管线,而且主要布局方向为减肥药方向的GLP-1。在研产品包括处于临床III期的TG103(GLP-1 Fc融合蛋白注射液)和2.2类新药司美格鲁肽(化学合成法)、处于临床前的长效司美格鲁肽(流体晶剂型)、口服司美格鲁肽、GLP-1双靶/三靶候选药物等。新诺威集PD-1、ADC、mRNA、GLP-1等诸多热门概念于一身,都说贪多嚼不烂,因此能否兑现需要长期观察,作为医药投资者切不可一时上头。 — 总结 — 回归A股一直都是石药集团的夙愿,早在2020年10月,石药集团就进行上市辅导备案,筹划进军A股,但却始终未能如愿。如今石药集团将各项核心资产装入新诺威,本质是利用新诺威,以及A股的高估值,实现其创新资产的曲线上市。石药“借尸还魂”,是否意味着“创新药一哥”恒瑞医药将在A股迎来最强对手了 ?这个问题,大可见仁见智。近期直播推荐:
IPO抗体药物偶联物
100 项与 奥马珠单抗生物类似药 (Reliance Life Sciences) 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 哮喘 | 临床前 | 印度 | - |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
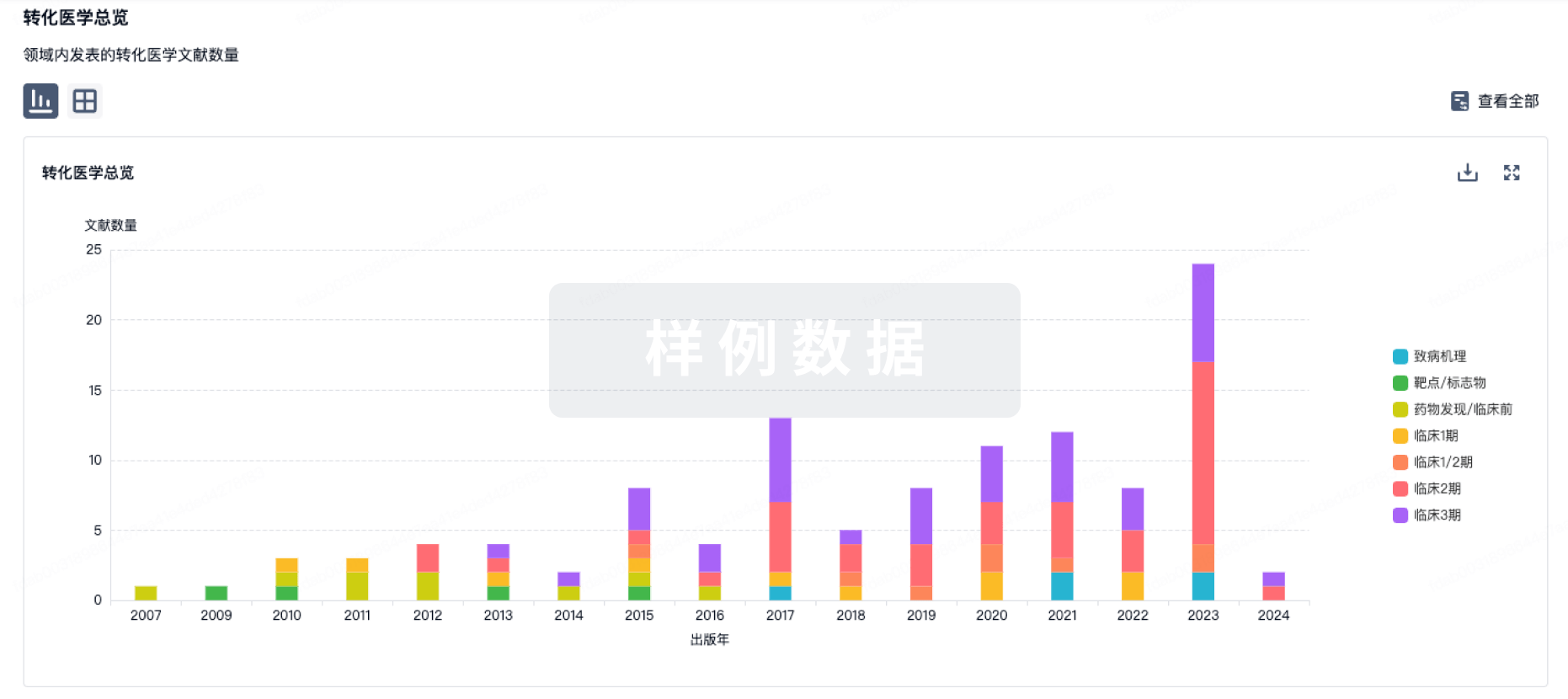
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
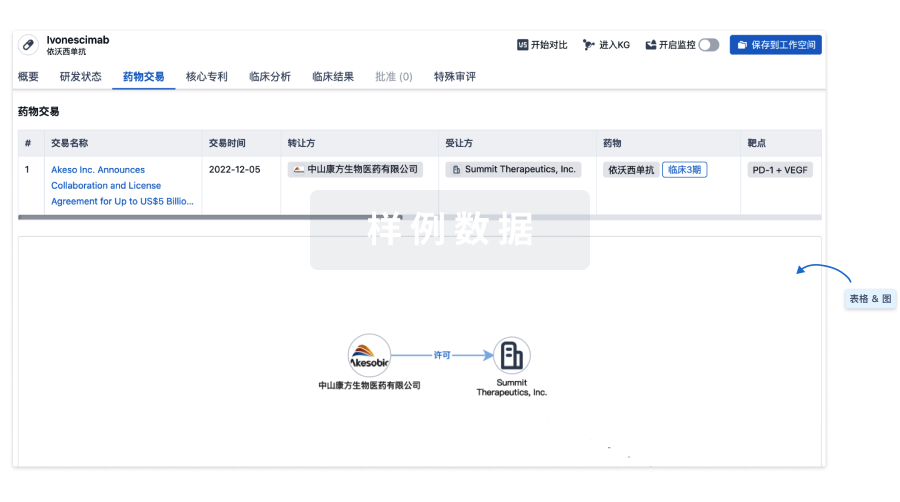
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
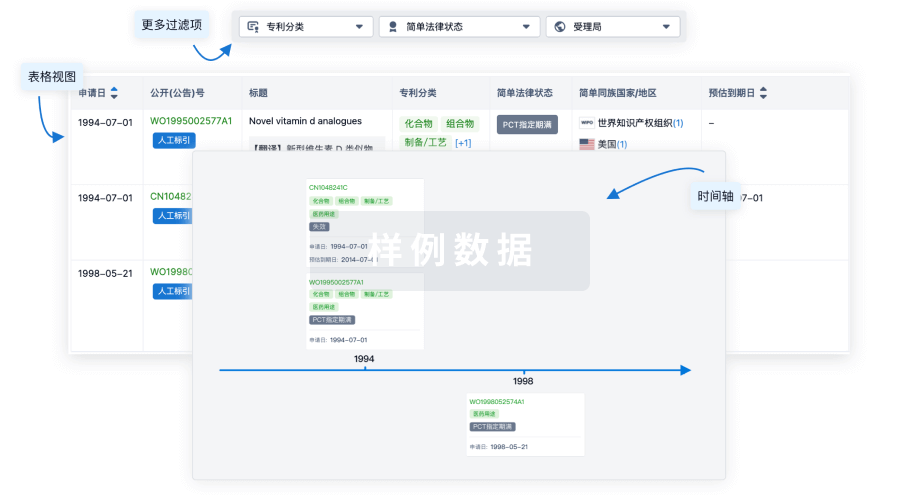
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
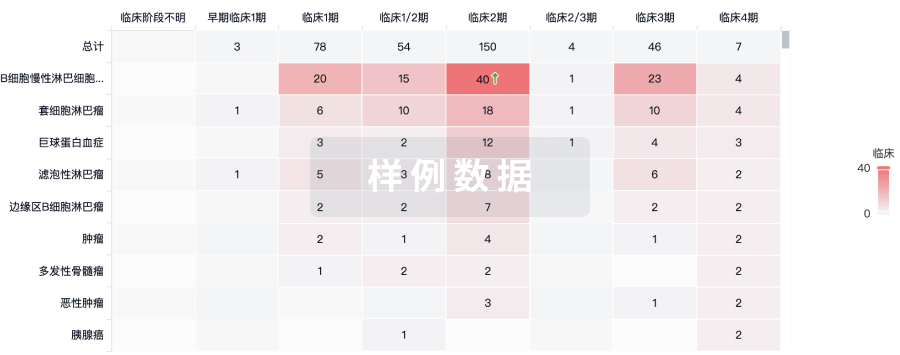
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
批准
利用最新的监管批准信息加速您的研究。
登录
或
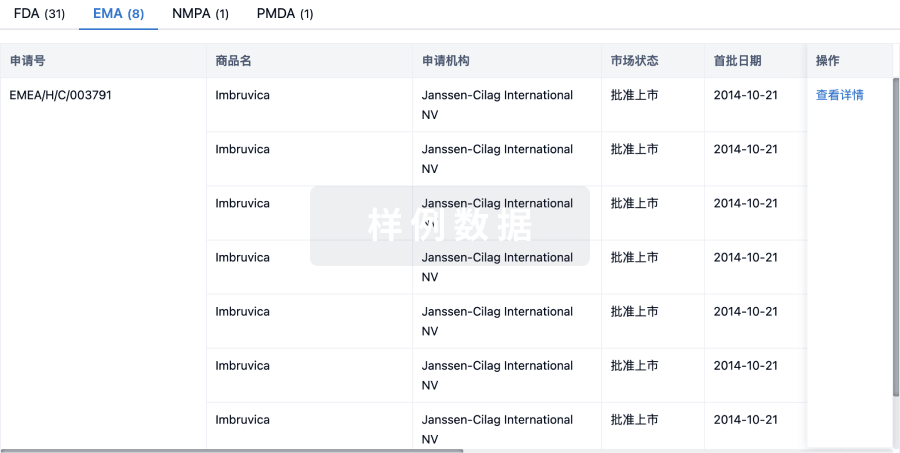
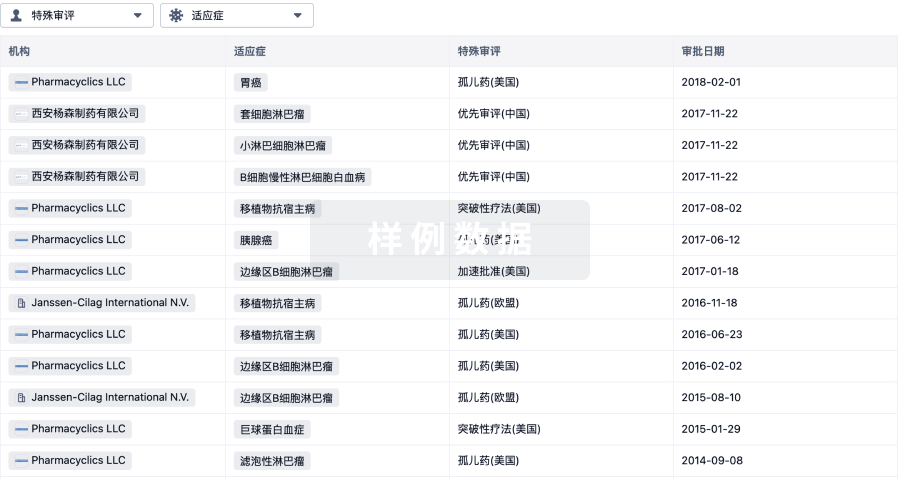
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
