预约演示
更新于:2025-01-23
ISRIB
更新于:2025-01-23
概要
基本信息
在研机构- |
最高研发阶段无进展临床前 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
关联
100 项与 ISRIB 相关的临床结果
登录后查看更多信息
100 项与 ISRIB 相关的转化医学
登录后查看更多信息
100 项与 ISRIB 相关的专利(医药)
登录后查看更多信息
134
项与 ISRIB 相关的文献(医药)2025-02-01·Brain Research
Neurotranscriptomic and behavioral effects of ISRIB, and its therapeutic effects in the traumatic brain injury model in zebrafish
Article
作者: Demin, Konstantin A. ; De Abreu, Murilo S ; Boyko, Galina A. ; Ikrin, Aleksey N. ; Yang, LongEn ; Boyko, Galina A ; De Abreu, Murilo S. ; Demin, Konstantin A ; Katolikova, Nataliia V. ; Katolikova, Nataliia V ; Ikrin, Aleksey N ; Yenkoyan, Konstantin B. ; Lim, Lee Wei ; Yenkoyan, Konstantin B ; Kalueff, Allan V. ; Ilyin, Nikita P. ; Kolesnikova, Tatiana O. ; Ilyin, Nikita P ; Kalueff, Allan V ; Chekrygin, Sergei A ; Shevlyakov, Anton D ; Kolesnikova, Tatiana O ; Galstyan, David S ; Chekrygin, Sergei A. ; Moskalenko, Anastasia M ; Moskalenko, Anastasia M. ; Galstyan, David S. ; Shevlyakov, Anton D.
2024-11-01·International Journal of Pharmaceutics
Enhancing topical delivery of ISRIB: Optimizing cream formulations with chemical enhancers and pH adjustment
Article
作者: Banga, Ajay K. ; Radmard, Ariana ; Banga, Ajay K ; Shrestha, Nisha ; Kumar Srivastava, Ritesh ; Athar, Mohammad ; Muzaffar, Suhail ; Khan, Jasim
2024-11-01·International Immunopharmacology
Epigallocatechin gallate induces apoptosis in multiple myeloma cells through endoplasmic reticulum stress induction and cytoskeletal disruption
Article
作者: Jiang, Wen ; Zhang, Xunqi ; Han, Yanxiao ; Fan, Chenliu ; Jiang, Yang ; Zheng, Chengyun
11
项与 ISRIB 相关的新闻(医药)2025-01-08
近日(1月6日),Denali Therapeutics公布了该公司eIF2B激活剂DNL343在肌萎缩侧索硬化(ALS)II/III期临床失败,主要终点和次要终点均为达到。
Denali这家公司一直有着挖掘ALS市场的野心,隔壁Amylyx仅仅只是上市后又因为临床验证失败撤市Relyvrio,就可以大赚特赚,也说明了这一市场大有可为。
不过,现在看来,这已经是这家公司第二次败走ALS适应症,上一次失败来源于另外一款管线DNL788。2024年2月时,该公司宣布DNL788这款与赛诺菲合作研发的RIPK1抑制剂未达到临床终点。10月该管线被赛诺菲“退货”。
如今DNL343的失败意味着Denali Therapeutics基本失去了所有关于ALS的资产布局,虽然还有事后分析的一线希望,但市场的反应不会骗人。公告发布后,在该公司盘后交易中,股价下跌了8.2%。
冷门靶点eIF2B
DNL343是一种可跨越血脑屏障的真核起始因子2B(eIF2B)小分子激动剂。从机制上来看,eIF2B是一种鸟苷酸交换因子,也是一种参与真核翻译起始的重要蛋白质,在ALS等神经退行性疾病中,神经元会经历应激状态。这种应激状态会抑制eIF2B的活性,导致蛋白质合成受损,并促使应激颗粒的形成。
应激颗粒是TDP-43蛋白的前体,而TDP-43在绝大多数ALS患者以及很多其他神经退行性疾病患者的细胞质中会异常聚集,成为ALS的标志性病理特征。
而Denali认为通过DNL343激活eIF2B以恢复蛋白质合成、驱散TDP-43聚集并改善神经元活性。
当然,Denali并不是第一个认为这一机制可以治疗神经退行性疾病的。
2013年Walter实验室发现的eIF2B小分子激动剂ISRIB就在早期临床前研究中发现具有抗衰老和保护神经元的功效。
然而由于理化性质不佳,ISRIB并没有得到更多开发,而后Denali的研究人员就在ISRIB的基础上进行对化学结构进行了优化,从而获得了现在的DNL343。
Denali的未来
对于Denali来说,目前账面上的现金还是相当充裕的,在ALS领域的失利短期内可能无法影响该公司运营,用于MPS II的酶替代疗法DNL310的也预计会在2025年提交上市申请,该公司的下一个要点里程碑可能是LRRK2抑制剂BIIB122/DNL151以及外周RIPK1抑制剂AR443122/DNL758的II期临床数据。
这决定了这家公司未来的发展方向。
参考来源:
Craig RA 2nd, De Vicente J, Estrada AA, Feng JA, Lexa KW, Canet MJ, Dowdle WE, Erickson RI, Flores BN, Haddick PCG, Kane LA, Lewcock JW, Moerke NJ, Poda SB, Sweeney Z, Takahashi RH, Tong V, Wang J, Yulyaningsih E, Solanoy H, Scearce-Levie K, Sanchez PE, Tang L, Xu M, Zhang R, Osipov M. Discovery of DNL343: A Potent, Selective, and Brain-Penetrant eIF2B Activator Designed for the Treatment of Neurodegenerative Diseases. J Med Chem. 2024 Apr 11;67(7):5758-5782. doi: 10.1021/acs.jmedchem.3c02422. Epub 2024 Mar 21.
临床2期临床终止临床1期引进/卖出
2024-12-20
·抗体圈
前言
内质网(ER)是分泌和跨膜蛋白合成、折叠和修饰的中心细胞器。ER中的蛋白质处理、修饰和折叠是决定细胞功能、命运和生存的严格调控过程。在几种肿瘤类型中,不同的致癌、转录和代谢异常协同作用,产生不利的微环境,破坏肿瘤细胞和间质细胞的内质网稳态,以及浸润淋巴细胞。
这些变化引发了持续的内质网应激状态,已经证明这种应激状态控制着癌细胞的多种促肿瘤属性,同时动态地重新编程固有免疫细胞和适应性免疫细胞的功能。ER应激传感器及其下游信号通路的异常激活已成为肿瘤生长和转移以及对化疗、靶向治疗和免疫治疗反应的关键调节因子。
TME中ER应激的常见驱动因素
内质网蛋白质折叠和修饰是一个高度调控的过程。然而,各种内源性和外源性应激可以破坏细胞器中的蛋白质稳态,导致内质网应激。未折叠蛋白反应(UPR)是一种高度保守的适应性机制,有三个分支协调对未折叠或错误折叠蛋白质的有害累积的反应。它们包括:需肌醇酶1α(IRE1α)、类PRKR ER激酶(PERK)和激活转录因子6(AFT6)。
TME中丰富的多种应激源动态地干扰了恶性细胞和间质细胞内质网的蛋白质折叠能力。
缺氧:缺氧是TME的一个常见特征,它扰乱内质网的稳态。蛋白质合成过程中二硫键的形成可以在没有氧气的情况下发生,但翻译后折叠或异构化是氧依赖的过程。此外,缺氧限制了氧依赖性内质网局部氧化还原酶ERO1α的功能,这是形成二硫键和蛋白质折叠所必需的。
营养:与正常能量需求相比,代谢应激以营养供应不足或过量为特征,很容易破坏内质网的稳态。葡萄糖和谷氨酰胺的有效性与内质网应激密切相关。
活性氧:内质网中的蛋白质折叠很大程度上依赖于这个细胞器的氧化还原状态。细胞内活性氧(ROS)的积累对外界条件的反应或由不同的信号事件引起,可以极大地扰乱内质网蛋白表达。
低pH:癌细胞利用有氧糖酵解作为中心代谢途径,从而产生乳酸,降低周围微环境的pH值。
肿瘤细胞内质网应激反应
UPR在肿瘤转化和肿瘤生长中的作用
致癌转化是一个多步骤的过程,它利用UPR来克服各种障碍。正常上皮细胞中MYC的过度激活会产生大量的蛋白毒性应激,并导致细胞存活率下降。然而,在包括淋巴瘤、神经母细胞瘤、前列腺癌和乳腺癌在内的多种人类癌症中,经受MYC诱导应激的细胞表现出UPR活性的增强。因此,完全激活的UPR对于适应由MYC驱动的癌基因转化引起的压力至关重要。
突变体RAS是另一个与UPR相互作用的致癌驱动因素。获得性耐药使KRAS突变型肺癌细胞能够绕过典型的KRAS效应器,但需要过度活跃的AXL/eIF4E,增加ER中的蛋白质周转,以及ER应激缓解UPR生存途径的适应性激活,HSP90维持其完整性。HSP90抑制剂可以协同增强MTA和trametinib的抗肿瘤作用。
分子伴侣结合免疫球蛋白(BiP)在多种人类癌症中过度表达,并通过多种机制促进肿瘤生长,如促进生长因子成熟和分泌、抑制细胞凋亡和促进血管生成。因此,BiP被认为是治疗人类癌症的一个有吸引力的靶点。
PERK利用各种机制来调节肿瘤的进展。首先,它的一个关键功能是通过增加抗氧化剂谷胱甘肽的生物合成来控制氧化应激。第二,PERK–eIF2α轴减弱整体转录并增强自噬作用,以促进MYC驱动的淋巴瘤中的细胞保护性UPR功能。第三,PERK和GCN2都被MYC激活以磷酸化eIF2α并诱导ATF4。
UPR在转移和休眠中的作用
一些研究表明PERK–eIF2α轴抑制失巢,是肿瘤侵袭和转移所必需的。PERK在经历上皮-间充质转化(EMT)的细胞中也被选择性激活,其分泌能力增强。在原发性肿瘤中,转移细胞在循环和远处组织中的氧化应激水平高于癌细胞。代谢适应,如抗氧化剂的合成,对于癌细胞在远处的生存和最终的生长是必不可少的。PERK分支通过ATF4和NRF2促进抗氧化反应,因此,可能通过减轻氧化应激而有益于转移细胞。
最近的研究还表明,来自病人和小鼠癌症模型的休眠恶性细胞的UPR反应增加,包括乳腺癌、鳞癌、结直肠癌和胰腺导管腺癌(PDAC)。UPR可能诱导休眠,作为在远端器官的不利微环境中生存的一种适应。
肿瘤细胞ER应激对肿瘤免疫微环境的调节
大量研究表明,肿瘤细胞内在的ER应激反应可以通过改变共存于TME中的免疫细胞的功能来影响肿瘤进展。
早期研究表明,ER应激的诱导和UPR的激活可能通过XBP1s和ATF6过度表达抑制主要组织相容性复合体I类(MHC-I)分子的表面表达。
肿瘤细胞ER应激反应被认为可以改变自然杀伤细胞(NK)介导的肿瘤识别。研究表明,在经历药物性ER应激的黑色素瘤细胞中,激活UPR的PERK–eIF2α轴可以诱导B7H6的表达,B7H6是NK细胞受体NKp30的配体。
ER应激的肿瘤细胞可以释放额外的因子来招募或改变肿瘤中髓系细胞的功能。
肿瘤细胞ER应激还可以调节T细胞介导的肿瘤生长、转移和对免疫治疗的反应。在接受抗CTLA-4治疗的各种黑色素瘤患者队列中,XBP1s、ATF4和BiP的表达减少与改善疗效和延长生存期相关。
肿瘤内免疫细胞的UPR
肿瘤细胞的高代谢需求和无限制的增殖能力极大地改变了肿瘤环境的营养成分,而肿瘤浸润性免疫细胞对蛋白质折叠和产生有效抗癌反应所需的关键营养素的获取有限。因此,肿瘤浸润的淋巴细胞持续激活ER应激反应,除了触发典型的UPR外,还以免疫细胞特异的方式调节主要的转录和代谢程序。
靶向内质网应激传感器或其相关的UPR反应途径,可能有助于增强免疫检查点阻断和过继性T细胞免疫治疗对目前这些方法难以治疗的实体瘤的效果。
靶向UPR的药物研究
将标准疗法与UPR调节剂相结合的方法已在临床前癌症模型中显示出显著的疗效,因此值得在癌症患者中进一步研究。
IRE1α抑制剂:IRE1α有两个可靶向的酶结构域:激酶结构域和内啡肽酶结构域。IRE1α激酶抑制剂在多发性骨髓瘤异种移植模型中显示出显著的体内疗效。IRE1α激酶抑制剂KIRA8或AMG-18,抑制多发性骨髓瘤生长,并增强这些肿瘤对已建立的一线药物,蛋白酶体抑制剂硼替佐米和免疫调节药物来那度胺的反应。
IRE1αRNase抑制剂,包括B-I09、STF083010、MKC3946和MKC8866,已在乳腺癌、前列腺癌、黑色素瘤、淋巴瘤、多发性骨髓瘤和CLL的小鼠模型中进行了广泛的试验。B-I09已被证明是一种安全和选择性的IRE1αRNase抑制剂,适合在体内使用。B-I09抑制CLL小鼠模型中的白血病生长而不引起全身毒性,并与FDA批准的Bruton酪氨酸激酶(BTK)抑制剂ibrutinib协同作用,诱导B细胞白血病、淋巴瘤和多发性骨髓瘤的人类细胞系的凋亡。
PERK抑制剂:PERK抑制剂GSK2606414和GSK2656157抑制不同癌症的人类异种移植模型中的肿瘤生长。GSK2656157还可使结肠癌细胞对5-氟尿嘧啶(5-FU)化疗药物敏感。有趣的是,在免疫原性肉瘤小鼠模型中,GSK2606414可激活T细胞功能并增强对PD-1阻断的反应。尽管疗效显著,但PERK抑制对胰腺产生严重的毒性作用,并显著抑制胰岛素的生成。
基于结构的设计和优化使化合物AMG44和AMG52被认为是有效和高度选择性的PERK抑制剂。这两种化合物在体内具有良好的药代动力学特性和耐受性,需要进一步的临床前和临床研究来评估它们与细胞毒性药物或靶向治疗相结合的抗肿瘤疗效和潜在副作用。
eIF2α抑制剂:ISRIB是一种有效的eIF2α抑制剂,通过激活eIF2B来抑制eIF2α磷酸化的影响。当作为一种单一的药物使用时,ISRIB能显著抑制PTEN缺陷和MYC过度表达的前列腺癌进展,延长带瘤小鼠的生存期。重要的是,单用ISRIB可在治疗3周后导致晚期前列腺肿瘤消退,而无明显副作用。
BiP抑制剂:在各种小鼠肿瘤模型中,BiP抑制剂KP1339诱导大范围ER应激和免疫原性细胞死亡。KP1339的I期研究显示,38例转移性神经内分泌肿瘤、非小细胞肺癌(NSCLC)或结肠癌患者中有10例疾病稳定,并且具有可接受的耐受性。
HA15是另一种以BiP为靶点的化合物,在黑色素瘤的异种移植模型中,HA15诱导了显著的抗肿瘤作用,并且有效地减缓了BRAF抑制剂耐药的黑色素瘤,没有主要的副作用。
展望
持续性内质网应激是肿瘤的一个新特征,它是由TME中的多种代谢和致癌异常因素引起的,这些异常扰乱了肿瘤细胞和浸润性免疫细胞的蛋白质折叠稳态。活跃的内质网应激反应使肿瘤细胞适应致癌和环境挑战,同时协调不同的免疫调节机制,促进肿瘤进展。
以内质网应激反应为靶点可以在增强抗肿瘤免疫的同时破坏肿瘤细胞的某些攻击性特质。越来越多的证据表明,对内质网应激传感器或UPR反应的调节,会使侵袭性肿瘤对细胞毒性药物、靶向治疗和免疫治疗更加敏感。更大规模的临床前研究以及对临床试验样本的回顾性分析,有助于发现有效的UPR靶向联合治疗,以获得防止癌症进展和/或复发的持久反应。
参考文献:
1.Endoplasmic reticulum stress signals in the tumour and itsmicroenvironment. Nat Rev Cancer. 2020 Nov 19.
2. HSP90/AXL/eIF4E-regulated unfolded protein response as an acquiredvulnerability in drug-resistant KRAS-mutant lung cancer. Oncogenesis. 2019 Sep; 8(9): 45.
3. Stress relief for cancer immunotherapy: implications for the ERstress response in tumor immunity. Cancer Immunol Immunother. 2020 Oct 26.
识别微信二维码,添加抗体圈小编,符合条件者即可加入抗体圈微信群!
请注明:姓名+研究方向!
本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观点,不代表本站立场。
免疫疗法
2024-12-18
·梅斯医学
一年一度的中国十大医学研究评选活动拉开帷幕,2024年我国科学家在医学领域取得了丰硕的成果,这些成就不仅彰显了我国科研实力的显著提升,也为世界医学的发展做出了巨大的贡献。
梅斯医学已经连续7年发布了年度十大医学研究进展。今年我们依旧通过线上评选的方式,评出“2024年度最受瞩目的中国十大医学研究”,这些研究具有原创性、突破性和引领性,在推进医疗实践、改善医疗质量方面具有重要的意义。
回顾这一年,中国科学家在中医药领域取得了众多令人瞩目的研究成果。那么,究竟有哪些研究能够荣登年度十大医学之列呢?
梅斯医学诚邀您一起票选出年度十大研究,投下您宝贵的一票
1. 评选活动中,须本着公开、公平、公正的原则,保持正常的心态参与投票。
2. 禁止任何人采用任何形式进行刷票,投票以后台实时监测的真实数据为准,恶意刷票数据将做无效处理。
3. 本次投票按照投票结果及专家评分,评选出的“2024年度中国中医药领域的十大医学研究”。
4. 评选结果将陆续发布在“梅斯医学”公众号,敬请关注!
投票截止时间
2024年12月27日 00:00
— 01 —
Lancet:宋莉莉/郭建文教授发表关于传统中药中风醒脑方治疗急性脑出血研究:一项多中心随机、安慰剂对照的双盲临床研究
doi: 10.1016/S0140-6736(24)02261-X
急性自发性脑出血是最严重的脑卒中类型,但有效治疗手段十分匮乏,且局限在发病早期以减少血肿体积为目的。中药FYTF-919(中风醒脑液)是一种由4种中草药制成的口服制剂,在中医理论上被认为具有促进血肿吸收和调节免疫的作用,在中国有多年应用于治疗脑出血的临床经验。CHAIN研究旨在采用标准的随机对照试验方法评估FYTF-919在中重度脑出血患者中的临床有效性和安全性。
为了评估“中风醒脑方”的临床有效性和安全性,研究团队在中国26家医院开展了一项历时三年的前瞻性、大规模、多中心随机安慰剂对照双盲试验。
研究团队纳入了在症状发生后48小时内被诊断为有症状的自发性脑出血(经脑影像学证实)并导致中度至重度神经功能缺损的成年人(年龄≥18岁),神经功能缺损的定义为美国国立卫生研究院卒中量表(National Institute of Health Stroke Scale)评分至少为8分或格拉斯哥昏迷量表(Glasgow Coma Scale)评分为7-14分。试验表明,传统中药复方“中风醒脑方”对中度至重度脑出血患者的功能恢复、生存期和健康相关生活质量的影响,与安慰剂并无差别。
发表期刊:Lancet. 2024 Nov 30;404(10468):2187-2196
通讯作者/关键作者:宋莉莉;郭建文
主要作者单位:复旦大学类脑智能科学与技术研究院;广东省中医院
— 02 —
JAMA Internal Medicine:贾振华教授团队揭秘,中医药复方降低糖尿病风险高达41%!
doi: 10.1001/jamainternmed.2024.1190
糖尿病是一种由胰岛素绝对或相对分泌不足以及利用障碍引发的,以高血糖为标志的慢性疾病。前期阶段,具体表现为空腹血糖受损(IFG)、糖耐量受损(IGT)及其合并状态。据美国糖尿病协会所发布的报告揭示,高达50%的糖尿病前期患者在短短五年内即会进展为糖尿病。
相较于IFG,IGT与糖尿病及心血管疾病(CVD)的风险增加之间,存在显著的相关性。尤为引人关注的是,当IGT与肥胖、血脂异常及高血压等其他危险因素并存时,个体罹患糖尿病的风险将进一步攀升,而患CVD的风险更已被确凿的证据表明增加了34%。
中医药复方能否预防糖尿病?研究团队就中医药复方“津力达颗粒”开展了研究。津力达颗粒是在络病理论指导下研发的创新中药,由17种中药成分组成,于2005年获得中国国家药品监督管理局批准,用于治疗2型糖尿病,既往临床研究发现,津力达可改善糖脂代谢紊乱,降低血糖和糖化血红蛋白,改善血糖波动,促进血糖达标。
结果显示,津力达颗粒能够通过针对性地改善多种代谢异常,有效降低IGT患者进展为糖尿病的风险。在此过程中,津力达颗粒的安全性及有效性得到了充分证实,因此,其作为一种极具潜力的干预手段,为那些患有多种代谢紊乱的IGT患者提供了预防糖尿病发病的新途径。
发表期刊:JAMA Intern Med. 2024 Jul 1;184(7):727-735
通讯作者/关键作者:贾振华;仝小林院士;连凤梅
主要作者单位:中国中医科学院广安门医院
— 03 —
JAMA Network Open:董强教授团队揭示大型临床试验证实通心络显著改善脑卒中预后
doi: 10.1001/jamanetworkopen.2024.33463
通心络作为一种中药复方制剂,其组方基于中医理论中“活血化瘀”的核心理念。该方由12味中药组成,包括檀香、降香、土鳖虫、水蛭、全蝎、赤芍、苏木、冰片、蜈蚣、穿山甲、麝香和红花。在中医理论中,这些药物共同发挥活血化瘀、通络止痛的功效,特别适用于治疗由血瘀引起的各种疾病,包括中风。
现代药理学研究揭示,通心络具有多靶点、多途径的作用机制,包括保护血脑屏障、促进神经可塑性、抑制炎症反应、减轻氧化应激等。这种多重作用机制与中医整体观和辨证论治的理念高度契合,也为其在复杂疾病如脑卒中中的应用提供了科学基础。
此次TISS试验采用了最严格的随机、双盲、安慰剂对照设计,共纳入2007名急性缺血性脑卒中患者。患者在发病72小时内被随机分配接受通心络或安慰剂治疗,疗程为90天。这种设计不仅符合国际最高标准的临床试验要求,也充分考虑了中医药的特点,为评估中药复方的长期疗效提供了可能。结果显示,对于发病72小时内的轻中度急性缺血性中风患者,在标准治疗的基础上,与安慰剂相比,加用通心络可显著改善90天功能预后,且年龄<60岁、发病48小时内的患者以及糖尿病患者似乎更有可能从中获益。
发表期刊:JAMA Netw Open. 2024 Sep 3;7(9):e2433463
通讯作者/关键作者:董强
主要作者单位:复旦大学附属华山医院
— 04 —
Journal of Advanced Research:吴迪炯/开国银教授揭秘中药有效成分逆转白血病BCL-2抑制剂耐药
doi: 10.1016/j.jare.2024.10.003
急性髓系白血病(AML)作为一种恶性克隆性疾病,其特征是骨髓原始细胞增殖伴扩增和分化阻滞,导致正常造血作用失效,并导致危及生命的血细胞减少和输血依赖。
中药应用治疗白血病具有悠久的历史,研究人员于上个世纪70年代研发了抗AML的一线用药“高三尖杉酯碱”。“抗白延年汤”是浙江省中医院血液科治疗白血病的经验方,研究团队前期对其进行了相应方药组份的筛选,发现其中的一个有效成分松萝酸可能具有特殊的抗耐药机制。
结果显示:松萝酸在低细胞毒性水平下,成功恢复了对产生ABT-199耐药性的AML细胞系对ABT-199的敏感性,并在小鼠异种移植模型中显著增加了ABT-199的抗白血病活性。从机制上讲,松萝酸和ABT-199的联合通过血红蛋白调节的抑制激酶(HRI)协同提高了综合应激反应(ISR)相关基因ATF4、CHOP和NOXA的表达,同时促进了抗凋亡蛋白MCL-1的降解。ISRIB,一种阻断ISR的化合物,能够逆转联合给药引起的AML细胞生长抑制和凋亡,以及ISR相关基因表达的增加和MCL-1蛋白的抑制。此外,ISR介导的MCL-1的下调与MCL-1在丝氨酸159位点的磷酸化增加以及随后蛋白酶体降解有关。上述研究为复发或难治性白血病患者提供了新的治疗选择,未来的研究有必要进一步验证这些初步发现,并探索这种联合方法的临床潜力。
发表期刊:J Adv Res. 2024 Oct 9:S2090-1232(24)00436-3
通讯作者/关键作者:吴迪炯;开国银;李曼;晋李;洪耀南
主要作者单位:浙江省中医院;浙江中医药大学
— 05 —
Adv Sci:华茜/梁兴杰教授团队揭秘中医复方“君-臣-佐-使”配伍理论
doi: 10.1002/advs.202306140
中医以其独特理论体系及丰富临床实践广泛应用于多种疾病治疗。方剂是在中医“君-臣-佐-使”配伍理论指导下的一种内服治疗手段。中药复方多成分的特性,使其物质基础阐释受到阻碍。近年研究表明中药汤剂中存在的自组装纳米结构可能是其发挥药效的主要组分。
研究者通过纳米技术,以中药复方芪银三两三(QY305)为例,阐释方剂发挥药效物质基础。研究人员提出:方剂煎煮过程中,中药多成分自组装产生的纳米结构为“君”,是方剂发挥药效的重要物质基础。研究通过临床观察及不同动物模型明确QY305方剂(T-QY305)改善EGFRIs相关皮肤不良反应和腹泻药效,基于良好效果,进一步制备QY305纳米颗粒(N-QY305),对其进行表征、鉴定,并通过动物模型证明N-QY305为其发挥药效的关键组分。
发表期刊:Adv Sci (Weinh). 2024 Feb;11(5):e2306140
通讯作者/关键作者:华茜;梁兴杰
主要作者单位:北京中医药大学;国家纳米科学中心
— 06 —
Nature:王卫庆/王计秋教授团队揭示“脑肠轴”调控体重新机制,中药葛根素或可用于减肥
doi: 10.1038/s41586-024-07929-5
肥胖问题日益严峻,全世界患有肥胖症的儿童、青少年和成年人总数已超过10亿。全世界范围内的高脂肪和高热量食品的消费激增,是导致持续蔓延的肥胖症和代谢紊乱的重要原因。虽然脂肪是饮食中重要的能量来源,但摄入过多会导致肥胖。一般认为,肠道内的脂肪吸收是通过扩散的方式实现器官自主吸收。然而,这一过程是否由脑-肠轴控制,目前仍不清楚。
研究者通过调控迷走神经运动背核(DMV)神经元的活动来揭示它们在控制小肠脂肪吸收中的作用。研究团队发现,通过抑制GABAA受体α1亚基(GABRA1)阳性的DMV神经元的活动,可以增强脂肪从粪便中排出并体重减轻。这些发现揭示了一个以前未知的脑-肠轴,控制着肠道的脂肪吸收。同时,该研究还展示了来自中药葛根的天然化合物葛根素(puerarin)可以靶向抑制这一“脑-肠轴”,帮助实现排油减肥。
发表期刊:Nature. 2024 Oct;634(8035):936-943
通讯作者/关键作者:王卫庆;王计秋
主要作者单位:上海交通大学医学院附属瑞金医院
— 07 —
Nature Medicine:李新立/张海锋/贾振华教授团队探讨芪苈强心胶囊在双盲临床试验中改善心力衰竭患者结局
doi: 10.1038/s41591-024-03169-2
中医作为补充医学的一个主要分支,在过去几十年中,在亚洲和西方国家的受欢迎程度都有所增加,并且有可能补充目前用于治疗慢性心力衰竭的疗法。通过弥补常规治疗的不足,中医可能为心力衰竭的治疗提供一种整体方法,有可能改善患者的预后和生活质量。然而,随机对照试验和严格的科学证据尚未证明中医在既定疗法之外改善心力衰竭患者临床结局的能力。
芪苈强心胶囊是一种中药配方,研究团队之前的初步研究显示,其在针对射血分数降低的心力衰竭(HFrEF)患者的既定心力衰竭治疗中显示出了良好效果。患者在治疗后N末端B型钠尿肽前体(NT-proBNP,心力衰竭的重要生物标志物)水平降低,心力衰竭症状、功能分级和6分钟步行距离得到改善,生活质量也有所提高。尽管治疗组的死亡率和再入院率低于安慰剂组,但样本量过小,因此无法得出明确结论。
为此,研究团队进行了一项随机、双盲、安慰剂对照临床试验评估了中药芪苈强心胶囊对射血分数降低的心力衰竭(HFrEF)患者的疗效和安全性,结果表明,在常规治疗的基础上加用芪苈强心胶囊可能会改善HFrEF患者的临床结局,与安慰剂相比,芪苈强心胶囊使患者心血管原因死亡和/或心力衰竭住院的主要结局降低了22%。
发表期刊:Nat Med. 2024 Aug;30(8):2295-2302
通讯作者/关键作者:李新立;张海锋;贾振华
主要作者单位:南京医科大学第一附属医院;河北医科大学附属以岭医院
— 08 —
JAMA Network Open:邢雁伟教授团队揭示太极拳比有氧运动的降血压效果更好
doi: 10.1001/jamanetworkopen.2023.54937
高血压前期(Prehypertension)是一种导致高血压的疾病,即慢性高血压。之前的研究表明,有氧运动(能够增加呼吸和心率的运动)可以阻止高血压前期患者发展为高血压。此外,也有研究表明太极拳具有同样的效果。在这项新研究中,研究团队希望了解更多关于这两种活动(有氧运动和太极拳)在一整年中的影响。
这项随机临床试验采用了严格的设计来测试太极拳和有氧运动在降低高血压前期患者血压的有效性。研究结果显示,太极拳在降低血压方面比有氧运动更有效。具体而言,经过一年的联系后,在办公室环境和跑步机上测试时,太极拳组的志愿者血压变化为-7.01 mmHg,而有氧运动组为-4.61 mmHg。太极组的24小时动态收缩压和夜间动态收缩压均显著低于有氧运动组。此外,在研究结束后对志愿者的后续监测显示,太极拳组的志愿者进展为高血压的人数比有氧运动组的更少。
发表期刊:JAMA Netw Open. 2024 Feb 5;7(2):e2354937
通讯作者/关键作者:邢雁伟
主要作者单位:中国中医科学院广安门医院
— 09 —
Adv Sci:覃江江/张卫东/程向东教授发现天然小分子,诱导胃癌铁死亡
doi: 10.1002/advs.202307899
胃癌是全球健康领域的重要挑战,是全球第五大最常见癌症和第三大癌症相关死亡原因。胃癌患者的预后通常较差,五年生存率低于30%,作为标准治疗方案的传统化疗疗效有限,且存在显著副作用。尽管靶向治疗和免疫治疗等治疗方法取得了进展,但这些疗法在胃癌仍然面临挑战。靶向治疗往往面临耐药性且疗效有限,而免疫治疗并非对所有胃癌患者都有效。因此,迫切需要创新和有效的治疗策略来改善患者的预后。
研究团队通过计算机筛选,确定了可用作中药的旋覆花中的一种半萜内酯化合物——DHPO,是一种有效的USP7抑制剂,可用于胃癌治疗。DHPO在体外表现出显著的抗肿瘤活性,抑制细胞活力和克隆形成能力,并防止肿瘤迁移和侵袭。在原位胃肿瘤小鼠模型中进行的体内研究验证了DHPO在抑制肿瘤生长和转移方面的疗效,且无显著毒性作用。
研究揭示了DHPO的抗肿瘤作用机制,DHPO对USP7的抑制引发了铁死亡,表现为线粒体改变、脂质活性氧、丙二醛的积累和铁过载。
发表期刊:Adv Sci (Weinh). 2024 May;11(18):e2307899
通讯作者/关键作者:覃江江;张卫东;程向东
主要作者单位:中国科学院杭州医学研究所,上海中医药大学
— 10 —
Adv Sci:高安博教授团队为芦荟大黄素在心脏损伤中保护作用的调节机制提供了新的见解
doi: 10.1002/advs.202406026
芦荟大黄素是传统中药单体蒽醌,在心血管疾病中起保护作用。但芦荟大黄素在保护放射性心脏损伤(RIHD)中的调控机制尚不清楚。乳酸化作为一种新型的翻译后修饰,被认为是炎症级联和心脏损伤的关键介质。
研究者通过差异组学和4D无标记乳酸化组学的交叉,确定蛋白质二硫键异构酶(P4HB)是乳酸化的新靶点,芦荟大黄素抑制乳酸与P4HB的K311位点的结合。芦荟大黄素通过抑制受损线粒体上天冬氨酸转氨酶(GOT2)的积累来稳定犬尿氨酸代谢。从机制上看,芦荟大黄素抑制细胞核内磷酸化糖原合酶激酶3B(p-GSK3B)的转录,从而抑制前列腺素G/H合酶2(PTGS2)与含有SH3结构域的GRB2样蛋白B1(SH3GLB1)的SH3结构域相互作用,从而破坏线粒体复合物的功能,减少SH3GLB1介导的线粒体ROS积累,最终抑制钙结合和卷曲螺旋结构域蛋白2(NDP52)诱导的线粒体自噬。
本研究揭示了芦荟大黄素通过PTGS2/SH3GLB1/NDP52轴在缓解RIHD中的调节作用,表明芦荟大黄素通过P4HB乳酸化稳定GOT2介导的犬尿氨酸代谢。
发表期刊:Adv Sci (Weinh). 2024 Nov 4:e2406026
通讯作者/关键作者:高安博
主要作者单位:南华大学
— 11 —
Adv Sci:胡德胜教授团队揭示中草药提取物苦豆碱抗肿瘤作用的机理
doi: 10.1002/advs.202308307
Aloperine (苦豆碱,ALO)是一种从天然中草药中分离出来的喹诺齐啶类生物碱,具有良好的抗肿瘤作用。然而,其共同作用机制和具体作用靶点尚不明确。研究团队在Advanced Science在线发表了一项研究,表明ALO在体外抑制非小细胞肺癌细胞系的增殖和迁移,并在体内抑制几种小鼠肿瘤模型的肿瘤发展。在机制上,ALO抑制自噬体与溶酶体的融合及自噬通量,导致sequestoome -1 (SQSTM1)的积累和活性氧(ROS)的产生,从而诱导肿瘤细胞凋亡,阻止肿瘤生长。
细胞中SQSTM1的敲低抑制ROS的产生并逆转ALO诱导的细胞凋亡。此外,VPS4A被鉴定为ALO的直接靶点,VPS4A的氨基酸F153和D263被确认为ALO的结合位点。敲除H1299细胞中的VPS4A显示出与ALO处理相似的生物学效应。此外,ALO增强了抗PD-L1 /TGF-β双特异性抗体抑制LLC源性皮下肿瘤模型的功效。因此,ALO首次被鉴定为一种新的晚期自噬抑制剂,通过靶向VPS4A触发肿瘤细胞死亡。
发表期刊:Adv Sci (Weinh). 2024 Aug;11(31):e2308307
通讯作者/关键作者:胡德胜
主要作者单位:华中科技大学
— 12 —
EHJ:贾振华/黄鹤教授揭示射频消融后口服参松养心胶囊能够减少持续性房颤患者的房颤复发
doi: 10.1093/eurheartj/ehae532
参松养心胶囊是在络病理论指导下研发的治疗心律失常的创新药物,由人参、麦冬、山茱萸、丹参、酸枣仁(炒)、桑寄生、赤芍、土鳖虫、甘松、黄连、南五味子、龙骨等12味中药组成,于2003年获得中国国家食品药品监督管理局(SFDA)批准上市,为中国国家医保甲类品种、国家基药目录品种。基础研究显示,参松养心胶囊可通过多种机制发挥抗心律失常的作用。
为进一步评价参松养心胶囊对Per房颤患者接受RFCA后的影响,研究人员在中国24个省/直辖市的66家医院开展,共纳入2019年11月至2021年10月期间920例首次RFCA后的Per房颤患者,结果显示,与对照组相比,参松养心胶囊可显著降低射频消融术(RFCA)后持续性(Per)房颤患者的房颤复发率,同时改善患者生活质量。
SS-AFRF研究结果不仅为心血管领域的国际难题提供了具有中国特色的解决方案,也为中医药的全球化发展提供了有力循证。这标志着我国传统中医药在传承创新和国际化发展方面迈出了坚实的一步,是中医药现代化和国际化进程中的重大突破。
发表期刊:Eur Heart J. 2024 Oct 21;45(40):4305-4314
通讯作者/关键作者:贾振华;黄鹤
主要作者单位:武汉大学人民医院;河北以岭医院
— 13 —
Mol Cancer:唐海林/侯少贞/蔡铭升教授发现中药成分牡荆素可减轻慢性肠道炎症向结直肠癌的转变
doi: 10.1186/s12943-024-02108-6
结直肠癌(CRC)是全球癌症相关死亡的主要原因之一,超过20%的病例与慢性炎症有关。与炎症性肠病(IBD)相关的结直肠癌(CAC)是结直肠癌的一种特别具有侵袭性的亚型,发生在长期处于慢性炎症环境中的IBD患者中。患有CAC的患者通常在晚期被诊断出并预后不佳。到目前为止,癌症的管理遇到了巨大的挑战,特别是由于针对该疾病的治疗中出现耐药性。
先前研究已经证明牡荆素能够有效缓解CAC,但其确切的作用机制有待进一步探索。本研究发现,维生素D受体(VDR)的缺失会加速从慢性结肠炎到结直肠癌的进程。牡荆素能够特异性地靶向VDR蛋白,促进其进入细胞核并发挥转录活性。此外,通过巨噬细胞和癌细胞的共培养模型,观察到牡荆素能够促进巨噬细胞向M1表型极化,这一过程依赖于VDR。
此外,ChIP-seq分析显示,牡荆素通过VDR调控吩嗪生物合成样结构域蛋白(PBLD)的转录激活。并证实了VDR/PBLD通路对牡荆蛋白介导的巨噬细胞极化调控至关重要。
发表期刊:Mol Cancer. 2024 Sep 13;23(1):196
通讯作者/关键作者:唐海林;侯少贞;蔡铭升
主要作者单位:中山大学;广州中医药大学;广州医科大学
— 14 —
EMBO Molecular Medicine:陈思禹/刘畅/张雯翔教授发现木犀草素能够解除小鼠DEHP毒性并预防肝损伤
doi: 10.1038/s44321-024-00160-9
邻苯二甲酸二(2-乙基己基)酯(DEHP)是一种环境污染物,广泛存在于环境和临床样本中,对内分泌系统稳态构成严重威胁DEHP在肝脏中的积聚非常明显,可导致肝损伤。高通量筛选系统的缺乏阻碍了对特异性靶向并消除DEHP有害影响的药物的发现。
研究团队开发了一种Cy5修饰的靶向DEHP的单链DNA适配体,确定木犀草素是一种潜在治疗药物,它通过促进小鼠原代肝细胞和肝脏中DEHP的排出,表现出强大的DEHP解毒功效。从机制上讲,木犀草素通过靶向肝尿酸水合酶1(Uroc1)的Ala270和Val272位点来增强蛋白质降解。更重要的是,反式尿酸(trans-UCA)作为Uroc1的底物,通过抑制ERK1/2信号级联调节溶酶体胞吐作用,具有类似于木犀草素的特性。总之,木犀草素是一种有效的治疗剂,通过调节UCA/Uroc1轴有效地解毒肝脏中的DEHP。
发表期刊:EMBO Mol Med. 2024 Nov;16(11):2699-2724
通讯作者/关键作者:陈思禹;刘畅;张雯翔
主要作者单位:中国药科大学
— 15 —
Small:陈瑞教授团队合作研究制备白藜芦醇仿生纳米药调节肿瘤干细胞活性以抑制结直肠癌转移
doi: 10.1002/smll.202407191
抑制肿瘤转移是提高结直肠癌(CRC)患者生存率的关键,癌症干细胞(CSCs)是转移的主要驱动因素。当前,尚不清楚相关分子机制,且针对CSCs的治疗方法有限。
为应对上述挑战,作者开发了一种仿生纳米颗粒递送系统CMD-BHQ3-PTL/DOX@RBCM,用于递送干细胞调节剂白皮杉醇(PTL)。
CMD-BHQ3-PTL/DOX@RBCM使用羧甲基葡聚糖(CMD)和淬灭基团Black Hole Quencher 3(BHQ3)将PTL和细胞毒性药物阿霉素(DOX)封装在红细胞膜(RBCm)内,增强稳定性和生物相容性,同时响应低氧条件逐渐释放药物。分子生物学实验、质粒构建和高通量测序研究了PTL对CSCs的影响,并阐明了该仿生纳米颗粒递送系统的分子作用机制。在组织水平上使用人源和鼠源的皮下和转移性肿瘤模型验证了PTL的治疗效果。
结果表明,CMD-BHQ3-PTL/DOX@RBCM有效解决了体内特异性和生物相容性问题,显著抑制了CSC相关肿瘤转移,该抑制作用与Hippo/YAP1/SOX9通路密切相关。该研究强调了pH响应仿生纳米颗粒系统CMD-BHQ3-PTL/DOX@RBCm将PTL递送到肿瘤部位的有效性,发现SOX9及其上游Hippo/YAP1通路是潜在的作用机制。
发表期刊:Small. 2024 Nov 10:e2407191
通讯作者/关键作者:陈瑞,梁凤霞,张红星
主要作者单位:华中科技大学,湖北中医药大学
注:排名不分先后
点击下方「阅读原文」 立刻下载梅斯医学APP!
抗体药物偶联物临床研究
100 项与 ISRIB 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 唐氏综合征 | 临床前 | 美国 | 2019-11-15 | |
| 唐氏综合征 | 临床前 | 美国 | 2019-11-15 | |
| 唐氏综合征 | 临床前 | 美国 | 2019-11-15 | |
| 唐氏综合征 | 临床前 | 美国 | 2019-11-15 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
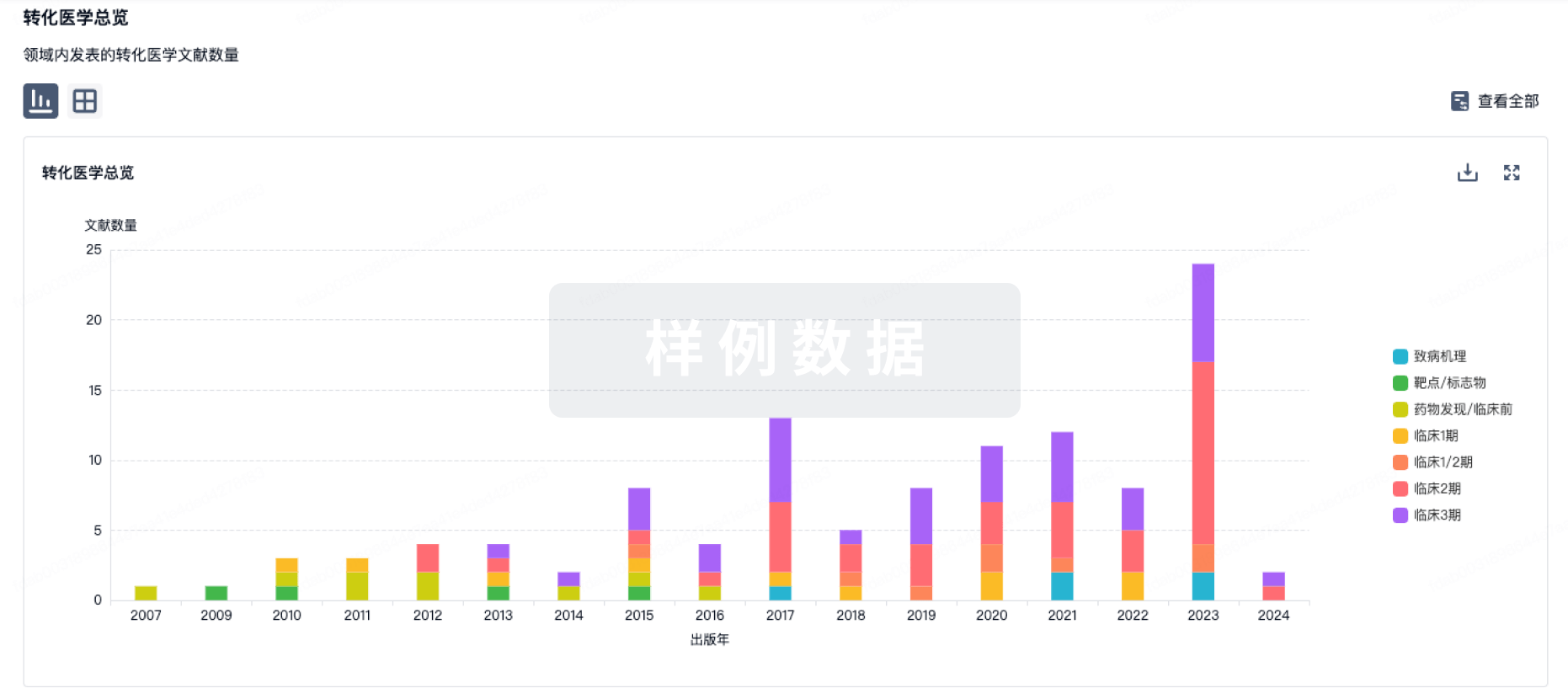
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
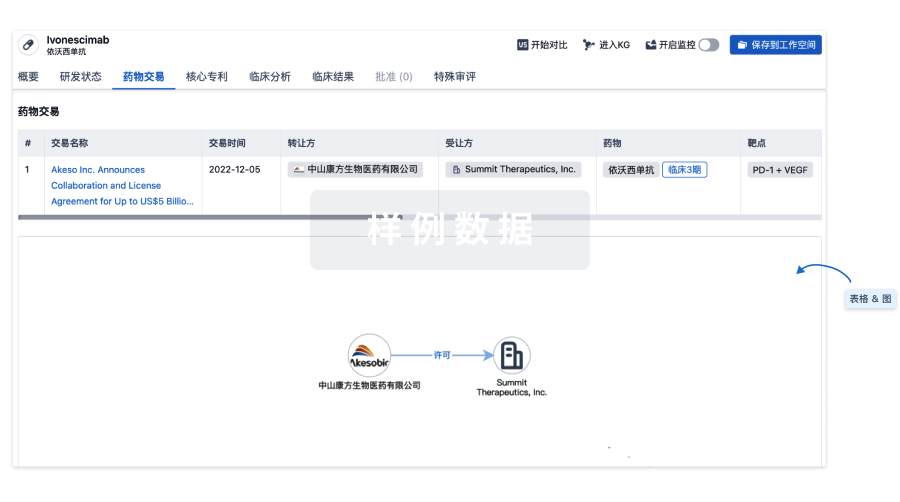
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
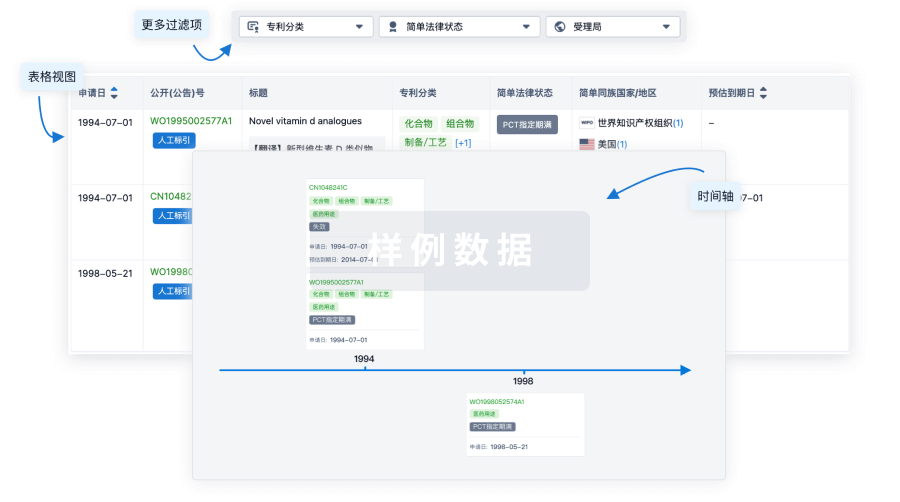
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
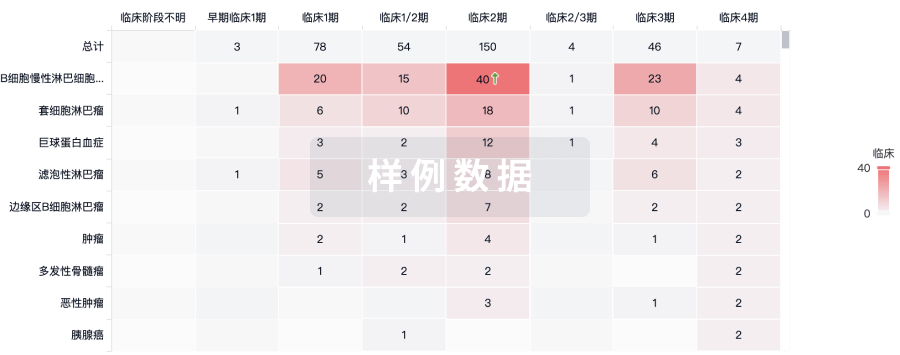
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
批准
利用最新的监管批准信息加速您的研究。
登录
或
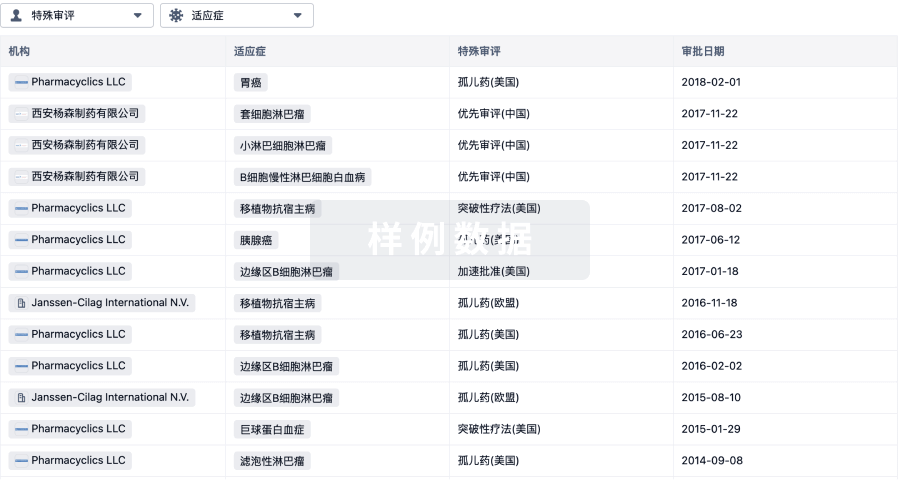
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用



