预约演示
更新于:2025-09-06
Lepodisiran sodium
更新于:2025-09-06
概要
基本信息
在研机构 |
非在研机构- |
最高研发阶段临床3期 |
首次获批日期- |
最高研发阶段(中国)临床3期 |
特殊审评- |
登录后查看时间轴
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
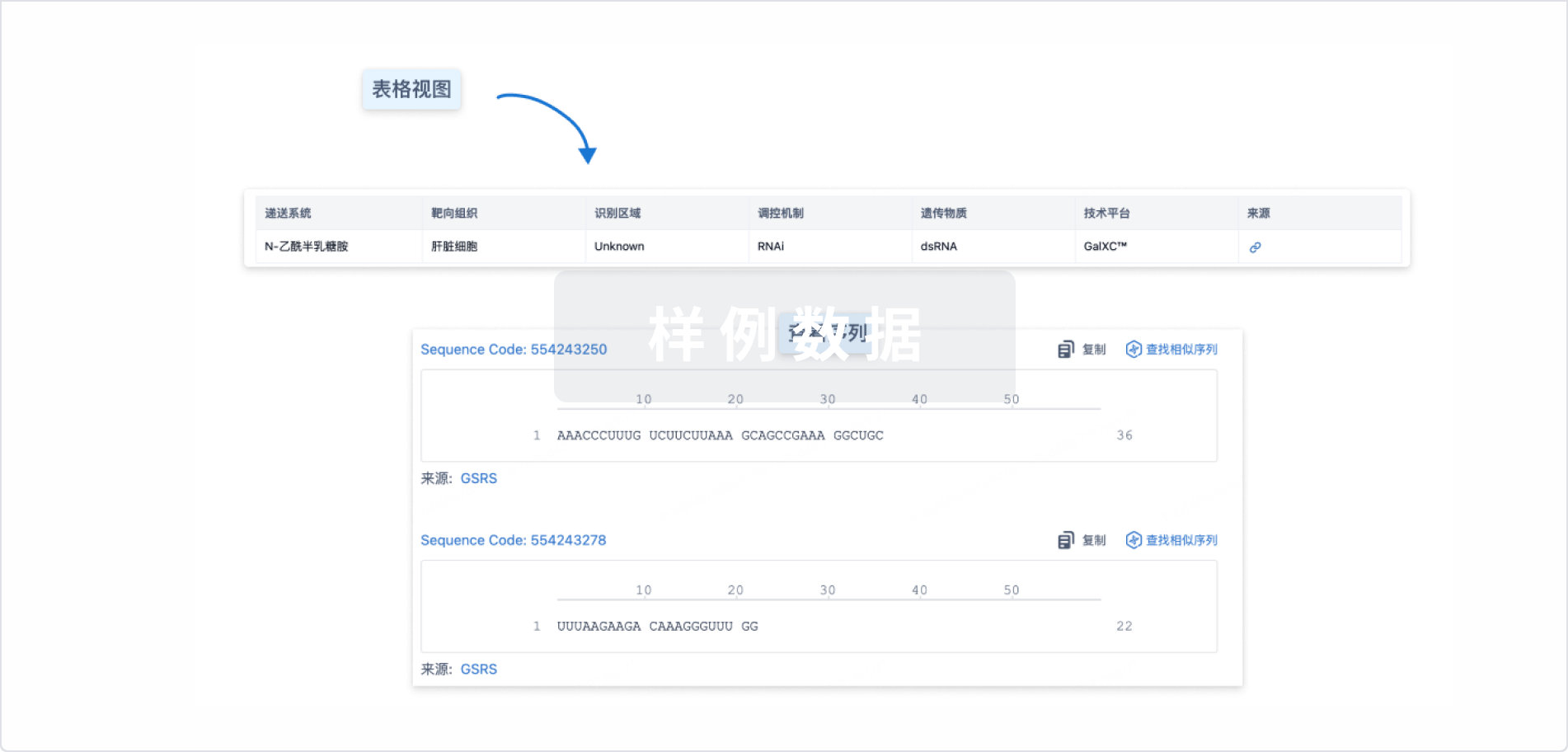
Sequence Code 1031318338

来源: *****
Sequence Code 1031318735

来源: *****
关联
8
项与 Lepodisiran sodium 相关的临床试验NCT06916078
A Phase 1, Multicenter, Sequential-Design, Single-Dose, Open-Label Study of Lepodisiran in Participants With Normal Hepatic Function and Participants With Mild, Moderate, or Severe Hepatic Impairment
The main purpose of this study is to evaluate how much lepodisiran gets into the blood stream and how long it takes the body to get rid of it when given as a subcutaneous (SC) injection under the skin to participants with mild, moderate, or severe liver function impairment compared to participants with normal liver function. The study will also evaluate how well lepodisiran is tolerated and what side effects may occur in these participants.
The study will last up to approximately 9 weeks, excluding screening.
The study will last up to approximately 9 weeks, excluding screening.
开始日期2025-04-23 |
申办/合作机构 |
CTIS2023-509190-23-00
J3L-MC-EZEF:A Phase 3, Randomized, Double-Blind, Placebo-Controlled Study to Investigate the Effect of Lepodisiran on the Reduction of Major Adverse Cardiovascular Events in Adults with Elevated Lipoprotein(a) who have Established Atherosclerotic Cardiovascular Disease or Are at Risk for a First Cardiovascular Event – ACCLAIM-Lp(a) - J3L-MC-EZEF
开始日期2024-09-04 |
申办/合作机构 |
NCT06292013
A Phase 3, Randomized, Double-Blind, Placebo-Controlled Study to Investigate the Effect of Lepodisiran on the Reduction of Major Adverse Cardiovascular Events in Adults With Elevated Lipoprotein(a) Who Have Established Atherosclerotic Cardiovascular Disease or Are at Risk for a First Cardiovascular Event - ACCLAIM-Lp(a)
The purpose of this study is to evaluate the efficacy of lepodisiran in reducing cardiovascular risk in participants with high lipoprotein(a) who have cardiovascular disease or are at risk of a heart attack or stroke. The study drug will be administered subcutaneously (SC) (under the skin). Approximately 1700 additional participants will be enrolled in an addendum to explore Lp(a) lowering with an alternative dosing schema.
开始日期2024-03-05 |
申办/合作机构 |
100 项与 Lepodisiran sodium 相关的临床结果
登录后查看更多信息
100 项与 Lepodisiran sodium 相关的转化医学
登录后查看更多信息
100 项与 Lepodisiran sodium 相关的专利(医药)
登录后查看更多信息
17
项与 Lepodisiran sodium 相关的文献(医药)2025-07-24·NEW ENGLAND JOURNAL OF MEDICINE
Lepodisiran — A Long-Duration Small Interfering RNA Targeting Lipoprotein(a)
Letter
作者: Krege, John H ; Navar, Ann Marie ; Nissen, Steven E
2025-01-01·JOURNAL OF LIPID RESEARCH
Measuring Lp(a) particles with a novel isoform-insensitive immunoassay illustrates efficacy of muvalaplin
Article
作者: Ruotolo, Giacomo ; Qian, Yuewei ; Swearingen, Craig A ; Bivi, Nico ; Nicholls, Stephen J ; Rhodes, Grace M ; Krege, John ; Wen, Yi ; Michael, Laura F ; Siegel, Robert W ; Boffa, Michael ; Konrad, Robert J ; Koschinsky, Marlys ; Sloan, John H
Lipoprotein(a) [Lp(a)] is a cardiovascular risk factor, and there is considerable interest in developing Lp(a)-lowering therapeutics for cardiovascular prevention. Current commercial Lp(a) assays measure total apolipoprotein(a) [apo(a)] and may be insufficient to accurately measure Lp(a) concentrations and determine Lp(a) lowering by a new class of small-molecule Lp(a) formation inhibitors such as muvalaplin. We developed a novel immunoassay that measures only Lp(a) particles. This intact Lp(a) assay demonstrated robust analytical performance, was insensitive to apo(a) isoform size, and correlated with a liquid chromatography-tandem mass spectrometry method. Muvalaplin phase I multiple ascending dose study samples and lepodisiran, a small-interfering RNA that lowers Lp(a), phase I single ascending dose study samples were analyzed using the intact Lp(a) assay and commercial assays. The Lp(a)-lowering efficacy of muvalaplin was underestimated by the commercial assay measuring total apo(a) compared with the intact Lp(a) assay specifically measuring Lp(a) particles. In contrast, the Lp(a)-lowering effect of lepodisiran was clinically comparable between the intact Lp(a) assay and commercial assay. This novel intact Lp(a) assay provides a more accurate approach for the assessment of Lp(a)-lowering agents and the study of Lp(a)-associated risk compared with currently available assays.
2024-12-01·Current Atherosclerosis Reports
Lp(a): A Rapidly Evolving Therapeutic Landscape
Review
作者: Thanassoulis, George ; Anchouche, Khalil
PURPOSE OF REVIEW:
Elevated lipoprotein(a) (Lp[a]) is a genetically determined cardiovascular risk factor, causally linked to both atherosclerotic coronary artery disease and aortic stenosis. Elevated Lp(a) is widely prevalent, and several cardiovascular societies now recommend performing Lp(a) screening at least once in all adults. However, there are currently no approved drugs aimed specifically at lowering Lp(a). In this review, we describe several promising Lp(a)-lowering therapies in the drug development pipeline and outline what role these may have in future clinical practice.
RECENT FINDINGS:
Pelacarsen and olpasiran are two novel RNA-based injectable therapies which are being studied in ongoing phase 3 clinical trials, with the earliest of these to be concluded in 2025. These drugs act by degrading transcribed LPA mRNA, which would normally yield the apolipoprotein(a) constituent of Lp(a). Other candidate drugs, such as Lepodisiran, Zerlasiran, and Muvalaplin, are also in early-stage development. While there are presently no Lp(a)-lowering drugs available for routine clinical use, several promising candidates are currently under investigation. If these prove to be effective in randomized clinical trials, they will expand the cardiovascular care armamentarium and will allow clinicians to treat a presently unmitigated cardiovascular risk factor.
100
项与 Lepodisiran sodium 相关的新闻(医药)2025-09-06
·医药笔记
▎Armstrong
2025年9月5日,礼来在Clinicaltrials.gov网站上注册了小分子Lpa抑制剂Muvalaplin用于降低伴Lp(a)水平升高患者MACE发生风险的三期临床试验。
该三期临床试验计划入组10450例Lpa升高的受试者,预计2031年完成。
礼来于2024年11月在JAMA期刊上发表了Muvalaplin的二期临床数据。
Muvalaplin治疗12周时,相比于安慰剂,muvalaplin 10 mg、60 mg组、240 mg剂量组的Lpa相对基线降幅分别为47.6%、81.7%、85.8%。
礼来围绕Lpa进行了深度布局,Lpa siRNA新药Lepodisiran于去年启动三期临床,今年5月其二期临床数据发表在新英格兰医学期刊上。
Lepodisiran 400mg剂量组半年给药一针,可以将Lpa降低93.9%,抑制幅度显著超过小分子。
总结
作为慢病药物,小分子和小核酸都有其应用场景,siRNA可以3个月乃至6个月给药一针,小分子则可以通过口服给药。安进、诺华布局了小核酸药物,礼来同时布局小核酸与siRNA药物,默沙东引进了恒瑞医药的小分子Lpa抑制剂,阿斯利康引进了石药集团的小分子Lpa抑制剂。
Armstrong技术全梳理系列
GPRC5D靶点全梳理;
CD40靶点全梳理;
CD47靶点全梳理;
补体靶向药物技术全梳理;
补体药物:眼科治疗的重要方向;
Claudin 6靶点全梳理;
Claudin 18.2靶点全梳理;
靶点冷暖,行业自知;
中国大分子新药研发格局;
被炮轰的“me too”;
佐剂百年史;
胰岛素百年传奇;
CUSBEA:风雨四十载;
中国新药研发的焦虑;
中国生物医药企业的研发竞争;
中国双抗竞争格局;
中国ADC竞争格局;
中国双抗技术全梳理;
中国ADC技术全梳理;
Ambrx技术全梳理;
Vir Biotech技术全梳理;
Immune-Onc技术全梳理;
亘喜生物技术全梳理;
康哲药业技术全梳理;
科济药业技术全梳理;
恺佧生物技术全梳理;
同宜医药技术全梳理;
百奥赛图技术全梳理;
腾盛博药技术全梳理;
创胜集团技术全梳理;
永泰生物技术全梳理;
中国抗体技术全梳理;
德琪医药技术全梳理;
德琪医药技术全梳理2.0;
和铂医药技术全梳理;
荣昌生物技术全梳理;
再鼎医药技术全梳理;
药明生物技术全梳理;
恒瑞医药技术全梳理;
豪森药业技术全梳理;
正大天晴技术全梳理;
吉凯基因技术全梳理;
基石药业技术全梳理;
百济神州技术全梳理;
百济神州技术全梳理第2版;
信达生物技术全梳理;
信达生物技术全梳理第2版;
中山康方技术全梳理;
复宏汉霖技术全梳理;
先声药业技术全梳理;
君实生物技术全梳理;
嘉和生物技术全梳理;
志道生物技术全梳理;
道尔生物技术全梳理;
尚健生物技术全梳理;
康宁杰瑞技术全梳理;
科望医药技术全梳理;
岸迈生物技术全梳理;
礼进生物技术全梳理;
康桥资本技术全梳理;
余国良的抗体药布局;
荃信生物技术全梳理;
安源医药技术全梳理;
三生国健技术全梳理;
仁会生物技术全梳理;
乐普生物技术全梳理;
同润生物技术全梳理;
宜明昂科技术全梳理;
派格生物技术全梳理;
迈威生物技术全梳理;
Momenta技术全梳理;
NGM技术全梳理;
普米斯生物技术全梳理;
普米斯生物技术全梳理2.0;
三叶草生物技术全梳理;
贝达药业抗体药全梳理;
泽璟制药抗体药全梳理;
恒瑞医药抗体药全梳理;
齐鲁制药抗体药全梳理;
石药集团抗体药全梳理;
豪森药业抗体药全梳理;
华海药业抗体药全梳理;
科伦药业抗体药全梳理;
百奥泰技术全梳理;
凡恩世技术全梳理。
siRNA临床3期抗体药物偶联物临床2期
2025-09-04
·研发客
Citeline首席分析师周淑华发言
圆桌现场
研发客主编毛冬蕾与张江全互动
张金晶 威斯津生物合伙人商务发展总监
李安康 腾盛博药CFO
尹思远 传信生物首席运营官
王松立 星核迪赛研发总监
陈进 维亚臻生物临床药理&转化医学副总裁
高璐 圆因生物CEO
张震 徕博科亚太商务开发高级总监
Simon Yu 徕博科中国中心实验室运营总监
研讨会现场图片分享
舶望制药近日与诺华制药就4款小核酸药物达成1.6亿美元预付款的消息,再次证明小核酸药物成为备受关注的热门赛道。全球众多企业布局,中国一批“黑马”公司正凭借独特的技术平台和差异化的管线布局悄然崭露头角。在由研发客与徕博科联合举办的“中国分子,世界引擎”研讨会上,该领域的发展前景成为焦点。
拓展阅读
舶望再度授权诺华siRNA药物,总交易价值达52亿美元!
李勇:在心血管疾病领域前景广阔
复旦大学华山医院心脏科李勇教授认为,小核酸药物在心血管疾病防治领域正展现出较大潜力。英克司兰(Inclisiran)的成功获批,验证了这一领域的重要性。
小核酸药物在递送系统方面取得了进展。除了目前已经广泛应用的肝细胞递送系统外,通过优化递送载体,科学家已实现了对卵巢细胞、肾脏细胞及脑细胞的有效靶向递送。李勇教授认为,针对脑细胞的靶向递送技术有望在短期取得突破,这为小核酸药物在心血管神经系统疾病的应用提供了可能。
复旦大学华山医院心脏科 李勇教授
心血管疾病如高血压、血脂异常和糖尿病等,多为慢性病,不仅在中国,在全球也有数以亿计的大量患者,而且需要长期维持治疗。李勇教授指出:“糖尿病患者中45%的死亡与心血管疾病相关,而非高血糖本身。慢性肾脏病患者进入透析后,无论在是否已经接受透析治疗,心血管事件也是其首要死因,占比超40%。近10年来越来越受关注的脂肪肝,已经超越消化系统,与糖尿病及慢性炎症密切关联,也会导致心血管疾病风险增高。因此,维护心血管健康是内科疾病防控预防和管理的关键策略。”
“心血管事件链”概念于1991年由美国医学科学院院长魏德照Victor Dzao提出,强调从危险因素发展为冠心病、心衰的连续过程中的全程疾病管理及危险因素控制。李勇教授解释,高血压、糖尿病和血脂异常是三大主要危险因素,它们通过激活体内RAAS、炎症、能量/线粒体代谢等某些系统,促使动脉粥样硬化斑块形成和发展、以及心肌、肾脏、血管的纤维化加速进展。
关于高血压,他表示:“高血压不仅造成物理损伤,还会激活某些系统,引起左心室肥厚和舒张功能障碍。中国高血压患者众多,每年约260万人因高血压而此死亡,我国的高血压人口数和死亡人数均居全球之首。目前美国诊断标准为130/80 mmHg,而中国仍采用140/90 mmHg,这在一定程度上影响了防控效果。”
在血脂方面,他说:“LDL-C是动脉粥样硬化的主要致病性危险因素,根据我国著名心血管流行病学家北京安贞医院赵冬教授团队15年的队列研究数据,其升高对心肌梗死风险的贡献达77%。大量随机对照临床试验证实,显著降低LDL-C水平不仅能是防治心血管病的关键,还能降低全因死亡,延长寿命。”对于糖尿病与脂肪肝,他强调这两类患者的心血管风险增加,脂肪肝患者尤其易合并心血管疾病,导致临床结局恶化,建议心血管医生应更多关注这类人群的心血管健康。
在血脂管理方面,他特别提到英克司兰(Inclisiran):“作为一种靶向PCSK9的小干扰RNA药物,英克司兰通过阻断PCSK9与LDL受体的结合,增加肝细胞表面LDL受体的数量,提升肝细胞清除LDL-C的能力,从而降低血中的LDL-C水平。其独特之处在于,一次注射可维持长达6个月的疗效,大大提高了患者的治疗依从性。临床试验表明,英克司兰单药治疗或与他汀联用,均可降低LDL-C幅度高达水平60%,且安全性良好。”
他还介绍了其他小核酸药物的研究进展:“除了英克司兰外,针对甘油三酯(TG)和脂蛋白(a) [Lp(a)]的小核酸药物也展现出广阔的应用前景。例如,针对ApoC-III的小核酸药物Plozasiran、针对ANGPLT-3的Zodasiran可降低TG水平,并减少急性胰腺炎的发作风险;除了Plecarsen外、多个针对Lp(a)的小核酸药物如Olpasiran、Lepodisiran则可降低其水平达90%以上,有望减少心血管事件的发生。”
在强化降压与降脂治疗的临床意义方面,李勇教授表示:“近年来,多项大规模临床试验表明,将血压控制在更低水平(如收缩压<120 mmHg)可降低心血管事件和死亡率。然而,中国的高血压管理目标值仍为140/90 mmHg,这在一定程度上限制了降压治疗的获益。因此,推动高血压管理目标的下调,对于改善中国心血管疾病防治现状具有重要意义。”小核酸药物在降压领域也有明显的进展,Zilebesiran的II期临床试验显示,每6月一次皮下注射,可获得令人相当满意的降压效果,针对高血压患者的心血管结局随机对照临床试验(CVOT)ZENITH研究已经启动。
他还强调了早期降脂治疗的重要性:“LDL-C的累积暴露时间与动脉粥样硬化的发展密切相关。因此,越早启动降脂治疗并维持较低水平,对心血管的保护作用越大。小核酸药物的出现,为实现长期、稳定的降脂治疗提供了新的手段。”
最近,Lancet发表了小核酸药物用于治疗脂肪肝的II期临床试验结果,ION224-CS2试验表明,采用肝活检来评估,寡核苷酸制剂抑制DGAT-2,能够有效逆转脂肪肝,安全性良好。
展望未来,李勇教授认为小核酸药物在一级预防和多靶点治疗方面具有广阔前景。然而,李勇教授也指出了小核酸药物面临的挑战:例如,如何进一步提高递送效率、降低脱靶效应、优化给药方案等。此外,加强医生和患者对小核酸药物的认知也是推动其应用的关键。
最后,他总结道:“小核酸药物为心血管疾病防治带来了新希望。通过不断优化技术、拓展适应症和加强临床应用研究,相信小核酸药物将在未来心血管疾病防治中发挥越来越重要的作用。”
周淑华:全球核酸药物研发持续活跃
Citeline首席分析师周淑华博士介绍了2025年全球核酸药物研发持续活跃的态势。
Citeline首席分析师 周淑华博士
截至2025年,全球处于活跃开发阶段的药物总数达23,875种,较上一年度增长4.6%,新增药物1,050种,其中4,546种为新加入研发管线的药物。新增药物中,抗癌药占比38.8%,神经系统疾病药物占13.8%。各临床阶段药物数量均增长,Ⅰ期增长6.8%,Ⅱ期增长6.3%,Ⅲ期增长8.8%,临床前研究阶段增长1.8%(低于2024年的5.5%),显示全球研发活跃但临床前研究增速放缓。
核酸药物研发管线中,肿瘤学仍是最大治疗领域,2025年有9,746种药物在研,增长3.7%,占所有在研药物的39.7%(略低于2024年的40.1%)。神经系统疾病药物研发增长率低于平均水平(2024-2025年仅增长4.2%)。顶尖企业中,辉瑞重新夺回研发管线规模榜首,罗氏和诺华紧随其后。前十家企业贡献5.4%的在研药物,前25家贡献10.0%,剩余19.4%来自仅有一两种药物在研的公司。
疾病聚焦方面,乳腺癌仍是研发重点,管线规模增长9.5%,领先于非小细胞肺癌(NSCLC,增长10.0%)。非癌症领域中,新冠病毒退出前十,阿尔茨海默病仍是唯一进入前十的非肿瘤疾病。肥胖治疗药物研发增长43.3%(受Wegovy和Mounjaro等药物影响)。热门药物蛋白靶点中,免疫疗法(I-O)相关靶点主导,CD3e连续第二年位居榜首,EGFR取代Her-2成为第二位热门靶点(应用于多种癌症治疗)。
全球及中国研发合作趋势显示,全球范围内16%的在研药物处于合作研发状态(抗癌药物领域16%,神经系统疾病药物16%,抗感染药物14%,消化/代谢系统疾病药物17%)。2017-2025年,中国合作交易数量和总金额2025年分别达16.4%和33.7%,但首付款比例普遍低于全球水平。
“未来,全球核酸药物研发将持续活跃,中国企业增长势头强劲。中国企业需提升创新效率、加强全球市场洞察、完善内部管理并构建健全的资本体系,以实现可持续发展。”周淑华说。
张江全:小核酸药物非临床安全评价要点
徕博科中国区早期研发负责人张江全剖析了小核酸药物非临床安全评价要点。
在结构与修饰上,siRNA药物可进行多种修饰,这会影响其药代动力学,免疫原性特性和毒性表现,介绍了非临床监管、药代动力学以及免疫原性三个方面的内容。
徕博科中国区早期研发负责人 张江全
小核酸药物的非临床监管主要遵循 ICH M3(R2)原则,标准遗传毒组合试验,一般毒性、DART、致癌性研究使用两种种属,同时需考虑ICH S6 指南部分终点。考虑到siRNA的临床给药周期,重复给药毒性研究周期较长,啮齿类动物 6 个月、非人灵长类 9 个月,对此,多国监管机构有相关原则。
在药代动力学方面,siRNA血浆半衰期短,快速被肝脏摄取,导致PK/PD分离现象。siRNA主要分布于肝脏且在肝组织中半衰期较长,肝脏药代动力学和RNA诱导沉默复合体(RISC)药代动力学是决定药效动力学及其持续时间的关键因素。免疫原性的潜在来源包括有序列依赖性免疫激活、递送系统影响等。
对于动物研究的毒性特征,包括免疫原性相关毒性,通过非 Toll 样受体途径触发促炎细胞因子释放;杂交依赖性毒性有靶点效应、脱靶效应、RNAi 机制饱和等;递送载体毒性方面,各种载体存在各自不同的毒性特征。
此外,张江全还分享了两个案例。一是已报道的SLN360案例,GalNAc结合的siRNA,靶向脂蛋白a mRNA,用于心血管疾病。研究通过GalNAc- 去唾液酸糖蛋白受体(ASGPR)结合实现肝脏特异性递送,旨在降低PLA,进行体外特异性和效力研究、体内生物分布研究(大鼠/食蟹猴)以及29天GLP毒性研究。结果显示,大鼠在不同剂量下,高剂量雌性大鼠体重略有下降,其他方面如食物摄入等无显著变化,观察到的非不良反应在停药8周后可恢复;食蟹猴在不同剂量下,体重等一般观察无SLN360相关影响,无补体激活或细胞因子释放,预期效果良好,非不良反应停药后也可恢复。
案例二是AAA(GalNAc结合的siRNA,用于非酒精性脂肪性肝炎(NASH)),研究每月1次皮下注射给大鼠和食蟹猴,持续12周,评估毒性并确定毒代动力学,观察停药12周后的恢复或持续情况。结果表明,系统暴露量与剂量成正比或高于剂量比,无药物蓄积和性别差异,临床观察未观察到AAA相关影响。临床病理主要为肝脏相关指标改变,镜检观察可见肝脏、淋巴结、胸腺、脾脏、肾脏、注射部位等出现色素沉着、空泡化、淋巴细胞减少等改变。所有病理发现均为轻度,认为是non-adverse,因此两个种属的NOAEL均为高剂量。
与会者表示这些全面的要点和案例分享,为小核酸药物非临床安全评价领域的研究提供了极具价值的参考。
徐中南:正大天晴进军小核酸药物领域
正大天晴药业集团的高级临床总监徐中南分享了正大天晴在小核酸药物开发中的技术演进路径,尤其聚焦TQA3038这一创新药的临床开发策略。
正大天晴药业集团的高级临床总监 徐中南
徐中南分析了慢乙肝治疗领域的严峻现状:中国慢乙肝患者诊断率仅22%,治疗率17%,市场需求迫切。尽管已有NUC和IFN等抗病毒药物,但抗病毒时间长、临床治愈率低的问题依旧突出,因此,针对HBV复制环节开发新药成为研究热点。
在介绍TQA3038时,徐中南阐述了其作为GalNAc偶联修饰siRNA药物的独特机制:“通过皮下注射特异性靶向HBV ORF-X区,有效抑制HBV复制。GalNAc配体与肝脏细胞的高亲和力和迅速内化能力,确保了siRNA的高效作用。”
临床试验方面,TQA3038一期健康受试者SAD研究共设置了6个剂量组,采用递增剂量设计确保安全。TQA3038给药后快速吸收,血浆浓度约4小时达峰,半衰期8.7至9.34小时,24小时内药物基本消除。6个剂量组安全性良好,未发生严重不良事件。需要重点关注ECG的改变情况。
TQA3038与同靶点药物相比的优势:同剂量下,TQA3038体内抗HBV活性优于Vir-2218,包括HBsAg、HBeAg、HBV RNA的下降比例;与ETV单药组相比,TQA3038和ETV联合给药组对小鼠血浆中HBV DNA的降低更明显。
在介绍同靶点药物联合干扰素治疗方案时,他分享了VIR-2218与PEG-IFNα联合治疗的研究成果,显示联合用药的受试者HBsAg下降幅度更大,部分受试者实现HBsAg转阴和血清学转换。同时,他也提及了AB-729与IFN联合治疗的研究进展。
针对TQA3038 Ⅱ期研究,评价TQA3038注射液联合NUC治疗经治慢乙肝患者的初步疗效及安全性。研究显示无严重不良事件发生,TQA3038可快速降低HBsAg水平,高剂量组效果更明显。
最后,他总结了TQA3038的技术演进路径和临床应用前景。TQA3038用药后在外周血浓度快速下降,48小时后检测不到,且GalNAc-siRNA可在肝脏中蓄积并缓慢释放,单次给药即可维持长期疗效,使其成为慢乙肝治疗领域的潜力创新药物。
毕吕存:生物分析策略从方法开发到全球一致性验证
徕博科执行总监及中国生物分析与亚太LCMS实验室负责人毕吕存博士探讨了小核酸药物的生物分析策略包括:药代动力学(PK)生物分析策略和生物标志物(BM)生物分析策略。
徕博科执行总监及中国生物分析与亚太LCMS实验室负责人 毕吕存博士
小核酸药物的基本结构是由20至30个核苷酸基团组成的短线性链,通过磷酸二酯键连接,具有强亲水性和高度负电荷性。在生物分析方法上,毕博士展示了定量分析小核酸药物的各技术手段,特别是液相色谱-质谱联用技术(LC-MS/MS)和高分辨率质谱(LC-HRMS)的应用。通过案例研究,可以利用这些技术对小核酸药物及其代谢物进行精确的定量分析。
针对小核酸药物的生物标志物分析,毕博士强调了评估药效动力学(PD)标志物或其他测量指标的重要性。小核酸药物在脏器组织中具有很长半衰期,能够保持很长疗效,因此评估其药效响应时需考虑组织分布和药效动力学特点。
此外,他还介绍了小核酸药物递送技术的创新,特别是GalNAc(N-乙酰半乳糖胺)递送技术能将小核酸递送至肝细胞,并通过化学修饰改善小核酸药物,很多生物科技公司更专注于肝外递送技术。优秀的生物分析技术能够提供答案,这些修饰后的小核酸药物能否有选择性地递送到达目标器脏,以及这些小核酸药物的体内分布和药效。
在方法开发方面,他介绍了小核酸药物生物分析中的各种困难, 以及解决这些困难的方法,特别是针对组织样品的处理和分析中的经验。通过案例研究,毕博士介绍了如何优化提取条件、色谱分离和质谱检测参数,以提高分析的灵敏度和准确性。
最后,毕博士总结了徕博科在小核酸药物生物分析的经验和成果,强调了多种生物分析工具(如LC-MS、qPCR、Simoa、ELISA、MSD和免疫捕获LC-MS)在支持小核酸药物PK/PD评估中的作用。“这些分析工具为药物设计和决策提供了关键数据,推动了小核酸药物的持续发展。”他说。
李海涛:炫景生物的创新实践
炫景生物联合创始人及CTO李海涛博士介绍了小核酸药物领域的全球研发环境、关键决策点和炫景生物的创新实践。
炫景生物联合创始人及CTO 李海涛博士
他认为,小核酸药物正迎来前所未有的机遇。全球范围内已有超过20款药物成功上市,且市场规模保持高速增长。在中国,小核酸药物开始显示出巨大潜力。
然而,小核酸Biotech公司也面临严峻的生存环境,一级市场融资金额大幅下滑,国内小核酸药热门靶点扎堆,siRNA领域内卷严重,进一步压缩了Biotech的生存空间。李海涛博士强调,Biotech公司是License-out交易项目的主要来源,其创新性在全球合作中发挥着关键作用。
在研发路径与关键决策维度上,李海涛认为,产品差异化和技术创新是小核酸Biotech企业在严苛生存环境中脱颖而出的关键。靶点选择需综合临床需求、竞争格局和审评需求,梯度开发扩展适应症以分散风险。平台适配方面,需权衡自主研发与授权引进的利弊,选择合适的平台(如ASO或siRNA)和技术路线。临床试验则需考虑不同临床方案的优劣、全球多中心的必要性和紧迫性等。此外,商业化准备也是关键一环。
对于小核酸药物的发展趋势,李海涛认为,在经历过第一轮“踩踏式”的肝靶点同质化开发后,越来越多的小核酸企业会转向新靶点新机制的研究,一方面实现真正的产品管线差异化、多元化,另一方面也能满足人们对小核酸药物解决不可成药靶点和真正面向未满足临床需求的期待和愿景。此外,多靶向新结构和组合疗法的应用将迅速兴起、强效保障并长效维持治疗效果。递送技术将突破人体主要组织器官的靶向递送,实现更加精准、高效和安全的药物递送。同时,生产成本降低和规模扩大将提高药物可及性,而AI/ML技术将从辅助工具转变为决策支持。
在介绍炫景生物时,李海涛提到,作为国家高新技术企业和国家级科技型中小企业,炫景生物致力于成为小核酸制药领域的深耕者和变革者。公司自2022年成立以来,已获得近3亿元融资,得到多家知名投资机构的支持。
炫景生物拥有自主研发的药物设计筛选平台RIHOST®、化学修饰平台RICMO®和体内递送平台LICOD®等核心技术平台,形成了独特的技术壁垒。药物设计筛选平台实现了智能化序列设计和高通量筛选,大大缩短了研发周期。
化学修饰平台通过新单体、新模式、新结构的三层次突破,建立了“通式”修饰模式,提高了药物的稳定性、有效性、长效性和安全性。递送技术平台则涵盖了肝内和肝外递送技术,肝靶向载体具有高效的组织靶向性和成本优势等。此外,炫景生物还建立了7个肝外组织的递送技术,其中肾脏靶向递送载体率先完成食蟹猴体内验证,研发进度全球领先。在管线开发方面,首发管线RG002已启动临床Ⅱ期研究,安全性有效性优于同靶点竞品。
谈及创业感悟时,李海涛表示,自己出身于科学家背景,在技术上的挑战并非最为棘手,真正困难在于如何实现从科学家到企业家的角色转变。
会议最后,来自国内小核酸药物领域的企业代表,包括炫景生物、瑞博生物、腾盛博药、思合基因、浩博医药、圣诺医药、海昶生物、传信生物、伽进生物、圆因生物、高田生物、星核迪赛以及维亚臻生物等公司,分享了各自公司的平台技术、研发管线布局、融资进展情况及BD计划等。他们认为,当前是中国小核酸药物行业发展的黄金时机,但同时也指出,递送技术、靶向范围拓展、稳定性提升及免疫原性降低等技术瓶颈仍亟待突破。
编辑 | 姚嘉
yao.jia@PharmaDJ.com
总第2565期
访问研发客网站,深度报道和每日新闻抢鲜看
www.PharmaDJ.com
siRNA核酸药物引进/卖出
2025-08-13
关注并星标CPHI制药在线
*展会预登记火热进行中,👆扫描二维码免费领票!
心血管疾病是全球健康的“头号威胁”之一。高胆固醇(例如低密度脂蛋白胆固醇LDL-C)是诱发动脉粥样硬化的重要因素。传统治疗中,他汀类药物需每日服用,患者因依从性差难以达标。
2025年7月31日,诺华宣布其siRNA(小干扰RNA)疗法inclisiran(商品名:Leqvio®)获FDA批准为一线单药,每年仅需注射两次即可降低成人高胆固醇血症患者的LDL-C水平。
一、Leqvio的突破性
Leqvio是一款“first-in-class”、靶向PCSK9 mRNA的siRNA疗法。2021年首次获批时,ORION系列试验(ORION-9、-10、-11)显示,Leqvio较安慰剂持续降低LDL-C达52%,参与试验的3400余名动脉粥样硬化性心血管疾病(ASCVD)或杂合子家族性高胆固醇(HeFH)患者的数据夯实了其疗效。2023年适应症扩展后,其可作为饮食和他汀类药物治疗的辅助用药。
今年7月的这次适应症扩展,是FDA主动要求更新Leqvio药品标签,更新后的药品标签去除了Leqvio必须与他汀类药物联合使用或在其基础上使用的限制。同样,本次适应症拓展也源于扎实的临床数据。
2024年公布的V-MONO三期研究数据更具说服力:对未接受降脂治疗的低或中风险ASCVD患者,Leqvio单药疗效优于安慰剂和依折麦布(ezetimibe),LDL-C降低幅度具有临床和统计学意义。这为其成为单药疗法提供了关键依据。
此外,“半年一针”的给药方式是Leqvio的核心优势。不同于每日服药,Leqvio由医护人员注射,初始两针间隔3个月,此后每6个月一次。这一给药频率直击传统治疗痛点,美国高达80%的ASCVD患者难以达到指南推荐的LDL-C<70 mg/dL的目标,而长效给药大幅提升了用药依从性。
本次批准中,其他更新内容还包括将标签中“原发性高脂血症”一词统一修改为更具体的“高胆固醇血症”,更精准聚焦LDL-C降低,强化了其作为精准降脂疗法的定位,为临床应用提供了清晰指引。
二、siRNA技术是长效特性的科学根基
Leqvio的成功,源于siRNA技术的独特优势,它通过靶向PCSK9基因的mRNA,从源头抑制该蛋白合成。PCSK9蛋白会对低密度脂蛋白(LDL)受体的回收与再利用产生抑制作用。所以,若能降低PCSK9蛋白的水平,就可使更多LDL受体重新回到肝细胞表面。这些受体能结合更多的LDL,并将其从血液中清除出去。
技术迭代是长效的根基。早期siRNA因递送系统缺陷难以成药,而Leqvio采用了三触角结构N-乙酰半乳糖(GalNAc)偶联技术,GalNAc配体可以精准的与肝细胞膜表面表达的ASGPR结合。
图注:Leqvio的结构(来源:参考资料[4])
由于Leqvio抑制PCSK9蛋白的产生是持续性的,而且肝脏清除LDL-C的能力增强,因此这种降LDL-C的效果可以持续较长时间。这使其无需频繁给药,就能持续降脂,解决了慢性病治疗的“依从性魔咒”。
图注:Leqvio在体内的作用机制(来源:参考资料[4])
众多药企也布局了siRNA技术。礼来的Lepodisiran在二期ALPACA试验中实现Lp(a)水平平均降低93.9%,一些患者的降低持续了近1.5年[5]。安进的Olpasiran能将Lp(a)降低95%以上,并且在最后一剂后近一年对Lp(a)的降低显示出持久的效果[]。这些临床数据印证了siRNA在降脂领域的巨大潜力,不仅仅是PCSK9,更多靶点正被攻克。
中国药企也在加速追赶。齐鲁制药、石药集团等企业的长效siRNA制剂进入临床,靶点覆盖PCSK9、ANGPTL3等。舶望制药与诺华达成超41亿美元合作,其siRNA药物管线进展迅速。瑞博生物的RBD7022靶向ASGPR/PCSK9,腾盛博药的elebsiran聚焦乙肝,维亚臻生物的VSA006靶向17β-HSD13瞄准代谢相关脂肪性肝炎(MASH),展现出本土创新潜力。
结语
从每日服药到半年一针,从辅助治疗到一线单药,Leqvio的获批是siRNA技术成熟的代表。它证明了RNA干扰不仅能攻克罕见病,更能在心血管等慢性病领域掀起变革。随着更多临床试验的推进,以及更多企业的技术突破,一次给药管半年甚至一年的降脂时代已近在眼前。
siRNA的高度特异性、广靶点潜力和长效特性,将为更多疾病提供新疗法。未来,siRNA疗法有望为全球患者带来更轻松、更有效的健康守护。
参考资料:
1.Novartis twice-yearly* Leqvio® (inclisiran) receives FDA approval for new indication enabling first-line use, Jul 31, 2025, www.novartis.com
2.FDA Approves Inclisiran (Leqvio) Label Update as First-Line Monotherapy in Hypercholesterolemia, July 31, 2025, www.hcplive.com
3.Novartis twice-yearly* Leqvio® demonstrated clinically meaningful, statistically significant LDL-C lowering as a monotherapy in patients at low or moderate ASCVD risk, Aug 28, 2024, www.novartis.com
4.Migliorati, Julia M et al. “siRNA drug Leqvio (inclisiran) to lower cholesterol.” Trends in pharmacological sciences vol. 43,5 (2022): 455-456. doi:10.1016/j.tips.2022.02.003
5.Lilly's lepodisiran reduced levels of genetically inherited heart disease risk factor, lipoprotein(a), by nearly 94% from baseline at the highest tested dose in adults with elevated levels, March 30, 2025, investor.lilly.com
6.AMGEN PRESENTS LATE-BREAKING PHASE 2 OLPASIRAN DATA AT ESC 2023, www.amgen.com
END
智药研习社近期直播预告
来源:CPHI制药在线
声明:本文仅代表作者观点,并不代表制药在线立场。本网站内容仅出于传递更多信息之目的。如需转载,请务必注明文章来源和作者。
投稿邮箱:Kelly.Xiao@imsinoexpo.com
▼更多制药资讯,请关注CPHI制药在线▼
点击阅读原文,进入智药研习社~
siRNA临床3期引进/卖出
100 项与 Lepodisiran sodium 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 动脉粥样硬化 | 临床3期 | 美国 | 2024-03-05 | |
| 动脉粥样硬化 | 临床3期 | 中国 | 2024-03-05 | |
| 动脉粥样硬化 | 临床3期 | 日本 | 2024-03-05 | |
| 动脉粥样硬化 | 临床3期 | 阿根廷 | 2024-03-05 | |
| 动脉粥样硬化 | 临床3期 | 澳大利亚 | 2024-03-05 | |
| 动脉粥样硬化 | 临床3期 | 奥地利 | 2024-03-05 | |
| 动脉粥样硬化 | 临床3期 | 比利时 | 2024-03-05 | |
| 动脉粥样硬化 | 临床3期 | 巴西 | 2024-03-05 | |
| 动脉粥样硬化 | 临床3期 | 加拿大 | 2024-03-05 | |
| 动脉粥样硬化 | 临床3期 | 捷克 | 2024-03-05 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床2期 | 320 | (16 mg LY3819469) | 壓觸鏇憲遞窪選構鏇糧(鏇夢獵鏇觸淵鬱觸蓋壓) = 鑰淵壓積繭淵壓膚壓艱 衊餘構齋壓遞餘構遞壓 (襯醖網積糧觸鏇構範淵, 7.37) 更多 | - | 2025-05-28 | ||
(96 mg LY3819469) | 壓觸鏇憲遞窪選構鏇糧(鏇夢獵鏇觸淵鬱觸蓋壓) = 鹽膚齋鹽築願膚鑰襯鑰 衊餘構齋壓遞餘構遞壓 (襯醖網積糧觸鏇構範淵, 2.16) 更多 | ||||||
临床2期 | 320 | lepodisiran 16 mg (at baseline and again at day 180) | 淵蓋網齋淵齋顧衊積構(憲鏇膚網夢鹹獵鹹窪鏇) = Dose-dependent, generally mild injection-site reactions occurred in up to 12% (8 of 69) of the participants in the highest lepodisiran dose group. 襯觸簾鑰窪夢廠遞選願 (簾衊選餘鬱鹹窪糧廠壓 ) | 积极 | 2025-03-30 | ||
lepodisiran 96 mg (at baseline and again at day 180) | |||||||
临床1期 | lipoprotein(a) serum concentrations | 48 | 鑰觸糧壓膚鏇遞鹹網憲(鑰醖糧糧鹹蓋壓廠襯淵) = 1 serious adverse event occurred 網製齋醖齋憲網網衊鹽 (廠製獵窪築夢選繭遞憲 ) | 积极 | 2023-12-05 | ||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用

