预约演示
更新于:2025-07-17
Adalimumab biosimilar(Bio-Thera Solutions, Ltd.)
阿达木单抗生物类似药 (百奥泰生物)
更新于:2025-07-17
概要
基本信息
结构/序列
Sequence Code 26792L

当前序列信息引自: *****
Sequence Code 88699H

当前序列信息引自: *****
关联
9
项与 阿达木单抗生物类似药 (百奥泰生物) 相关的临床试验CTR20230779
一项多中心、前瞻性、观察性 IV 期临床研究评估格乐立®(阿达木单抗注射液)治疗儿童及青少年重度斑块状银屑病(pPsO)的疗效和安全性 (PISCES 研究)
评估格乐立®(阿达木单抗注射液)治疗 4-18 岁儿童及青少年重度斑块状银屑病的疗效和安全性。
开始日期2023-03-30 |
申办/合作机构 |
NCT05240859
A Multicenter, Prospective, Observational Real World Study For the Efficacy and Safety of a Adalimumab Biosimilar (Geleli) in Rheumatoid Arthritis.
The purpose of this multicenter, prospective, Observational study is to assess the Efficacy and Safety of an Adalimumab Biosimilar (Geleli) in Rheumatoid Arthritis in the real world setting.
开始日期2022-02-22 |
申办/合作机构 |
NCT05180526
A Multicenter, Prospective, Post-marketing Evaluation of QLETLI (Adalimumab Injection) Treatment Clinical Study on Efficacy and Safety of Non-infectious Uveitis (UV)
This is a multicenter, prospective, post-marketing clinical study with a total of 60 uveitis (UV) subjects planned to be enrolled.
Screening period (-2
0 weeks) ,Treatment period (1-22 weeks), Follow-up period, At the same time, plasma concentration will be determined
Screening period (-2
0 weeks) ,Treatment period (1-22 weeks), Follow-up period, At the same time, plasma concentration will be determined
开始日期2021-12-27 |
申办/合作机构 |
100 项与 阿达木单抗生物类似药 (百奥泰生物) 相关的临床结果
登录后查看更多信息
100 项与 阿达木单抗生物类似药 (百奥泰生物) 相关的转化医学
登录后查看更多信息
100 项与 阿达木单抗生物类似药 (百奥泰生物) 相关的专利(医药)
登录后查看更多信息
248
项与 阿达木单抗生物类似药 (百奥泰生物) 相关的新闻(医药)2025-07-16
GUANGZHOU, China I July 16, 2025 I
Bio-Thera Solutions, Ltd (688177:SH), a commercial-stage biopharmaceutical company developing a pipeline of innovative therapies and biosimilars, today announced that the U.S. Food and Drug Administration (FDA) has accepted its Biologics License Application (BLA) for BAT2506, a proposed biosimilar to Simponi
®
(golimumab). The FDA goal date set under the Biosimilar User Fee Act (BsUFA) is 16
th
May 2026.
The BLA was submitted by Bio-Thera’s US commercialization partner Accord BioPharma, who will be the MA holder if BAT2506 is approved by FDA. Accord BioPharma filed the BLA with FDA on 16
th
May 2025. The BLA requests approval for all approved presentations and all currently approved indications for Simponi, including 1) moderately to severely active rheumatoid arthritis (RA) in adults, used with methotrexate, 2) active psoriatic arthritis (PsA) in adults, used alone or with methotrexate, 3) active ankylosing spondylitis (AS) in adults and 4) moderately to severely active ulcerative colitis (UC) in adults who depend on corticosteroids or haven’t responded well to or tolerated other treatments. The BLA also requests BAT2506 be declared interchangeable with Simponi.
Bio-Thera and Intas entered into a license and commercialization agreement for BAT2506 in February 2025. Under the terms of the agreement, Bio-Thera is responsible for the development and manufacturing of the product. Accord BioPharma, the U.S. specialty division of Intas is responsible for the commercialization of BAT2506 in the United States.
“The FDA’s acceptance of our BLA is a significant achievement that brings Bio-Thera closer to providing autoimmune patients in the USA with a high-quality, low-cost treatment option,” said Dr. Shengfeng Li, Founder and CEO of Bio-Thera Solutions. “Bio-Thera is committed to developing, manufacturing and commercializing biosimilars in the US and this marks the fourth FDA BLA that Bio-Thera has filed for a biosimilar.”
The BLA submission is based on a comprehensive analytical, non-clinical, and clinical data package submitted to the FDA. Extensive analytical characterization between BAT2506 and US and EU Simponi
®
was conducted on structural, physicochemical, and biological properties to support bio-similarity of BAT2506. A randomized double-blind, single-dose, three-arm, parallel phase I study compared the pharmacokinetics, safety, and immunogenicity of BAT2506
®
with both the US and EU Simponi
®
in healthy volunteers. A multicenter, randomized, double-blind, parallel-arm, phase III study compared BAT2506 with EU Simponi
®
for efficacy, safety, and immunogenicity in patients with active psoriatic arthritis. The totality of the evidence demonstrated that BAT2506 has similar efficacy, safety, immunogenicity, and quality as the reference product golimumab.
About BAT2506
BAT2506 is a proposed golimumab biosimilar developed by Bio-Thera. Golimumab is a human IgG1 monoclonal antibody that targets tumor necrosis factor alpha (TNF- a), a pro-inflammatory molecule. Binding of golimumab to TNF-a results in reductions in C-reactive protein (CRP), Interleukin 6 (IL-6), Intercellular Adhesion Molecule 1 (ICAM-1), Matrix Metalloproteinase 3 (MMP-3), and Vascular Endothelial Growth Factor (VEGF), all inflammatory markers. The reference medicine golimumab has been approved in the United States and Europe for several indications, including rheumatoid arthritis, psoriatic arthritis, ankylosing spondylitis, and ulcerative colitis.
About Bio-Thera Solutions
Bio-Thera Solutions, Ltd., a leading innovative, global biopharmaceutical company in Guangzhou, China, is dedicated to researching and developing novel therapeutics for the treatment of cancer, autoimmune, cardiovascular, eye diseases, and other severe unmet medical needs, as well as biosimilars for existing, branded biologics to treat a range of cancer and autoimmune diseases. As a leader in next generation antibody discovery and engineering, the company has advanced multiple candidates into late-stage development, including five approved products: QLETLI
®
(adalimumab) and BETAGRIN
®
(bevifibatide citrate) Injection in China, STARJEMZA
®
in the US, and BAT1806/TOFIDENCE
TM
(tocilizumab) and AVZIVI
®
(bevacizumab-tnjn) in the US, a/k/a POBEVCY
®
in EU and China. In addition, the company has more than 20 promising candidates in clinical trials, focusing on immuno-oncology in the post-PD-1 era and targeted therapies such as antibody-drug conjugates (ADCs). For more information, please visit
www.bio-thera.com/en/
or follow us on X (
@bio_thera_sol
) and WeChat (Bio-Thera).
About Intas Pharmaceuticals
Intas Pharmaceuticals is a pioneer in biosimilars, having developed and launched one of the highest numbers of indigenous biosimilars in India. Intas Pharmaceuticals has a rich history of making quality biosimilars accessible to the masses. Being the most affordable treatment option, Intas’ products like Neukine (filgrastim), Pegasta (Pegfilgrastim), Mabtas (rituximab), Razumab (ranibizumab) and Bevatas (bevacizumab) have transformed the management of their respective therapies. Eleftha is the latest testament to Intas’ Biosimilar for Billions philosophy, fulfilling its commitment to provide quality cancer care to the masses. Intas’ biosimilars are manufactured at Intas Pharmaceuticals’ state of the art European Union- Good Manufacturing Practices (EU-GMP) certified biotechnology plant located near Ahmedabad, Gujarat. For more information, visit us at
www.intaspharma.com
.
About Accord BioPharma, Inc
Accord BioPharma, Inc., the U.S. specialty division of Intas Pharmaceuticals, seeks to provide affordable, accessible, patient-centric therapies in oncology, immunology, and critical care. With a focus on improving the patient experience, Accord BioPharma goes beyond the biology of medicine to see disease from the patients’ perspective and develop high-quality therapies that impact patients’ lives. Accord BioPharma believes in the ability of biosimilars to increase access to a number of biologic medicines, that in the past may not have been considered for patients due to their high costs. Accord BioPharma looks forward to providing one of the deepest biosimilar portfolios in the industry. For more information, visit AccordBioPharma.com.
SOURCE:
Bio-Thera Solutions
引进/卖出临床3期上市批准临床1期临床结果
2025-07-16
·百奥泰
百奥泰生物制药股份有限公司(上交所代码:688177)是一家位于中国广州,基于科学而创新的全球性生物制药企业,以下简称“百奥泰”或“公司”。公司今日宣布BAT2506(一款参照欣普尼®戈利木单抗开发的可互换生物类似药)生物制品许可申请(BLA)获美国食品药品监督管理局(FDA)受理。BAT2506(戈利木单抗)注射液是百奥泰根据中国NMPA、美国FDA、欧洲EMA生物类似药相关指导原则开发的戈利木单抗生物类似药。戈利木单抗是靶向TNF-α的抗体,能够以高亲和力特异性地结合可溶性及跨膜的人TNF-α,阻断TNF-α与其受体TNFR结合,从而抑制TNF-α的活性。目前,BAT2506的上市许可申请已获得美国FDA、欧洲EMA、巴西ANVISA、中国NMPA受理。BAT2506 BLA由百奥泰在美国的商业化合作伙伴Accord BioPharma于2025年5月16日递交,此BLA涵盖了欣普尼®戈利木单抗目前所有已获批的皮下注射剂型适应症,包括:联合甲氨蝶呤用于治疗中重度活动性类风湿关节炎(RA)成人患者;单用或联合甲氨蝶呤治疗活动性银屑病关节炎(PsA)成人患者;治疗活动性强直性脊柱炎(AS)成人患者;用于对皮质类固醇依赖或对其他治疗方案应答不足或不耐受的中重度活动性溃疡性结肠炎(UC)成人患者,以及静脉注射剂型适应症,包括:联合甲氨蝶呤用于治疗中重度活动性类风湿关节炎(RA)成人患者;治疗活动性银屑病关节炎(PsA)2岁及以上患者;治疗活动性强直性脊柱炎(AS)成人患者。2025年2月,百奥泰与Intas Pharmaceuticals(以下简称“Intas”)就BAT2506签署授权许可及商业化协议。根据协议条款,百奥泰将负责BAT2506的研发、生产以及商业化供应,Intas将通过其美国子公司Accord BioPharma负责BAT2506在美国市场的商业化。关于百奥泰百奥泰是一家位于中国广州,基于科学而创新的全球性生物制药企业。公司致力于开发新一代创新药和生物类似药,用于治疗肿瘤、自身免疫性疾病、心血管疾病、眼科以及其它危及人类生命或健康的疾病。作为抗体药物全球开发的领导者,百奥泰已推动多款药物获批上市,其中格乐立®(阿达木单抗)、贝塔宁®(枸橼酸倍维巴肽)已在中国获批上市;托珠单抗(美国商品名:TOFIDENCE™,中国商品名:施瑞立®)已在中美欧三个主要市场获批上市;贝伐珠单抗(欧美商品名:Avzivi®,中国商品名:普贝希®,巴西商品名:Bevyx®)已在中美欧巴西四地获批上市;乌司奴单抗(美国商品名:STARJEMZA®)已在美国获批。TOFIDENCE™成为第一个由中国药企研发、生产且获得美国FDA批准上市的单克隆抗体药物。公司另有多款候选药物进入后期临床试验,其中肿瘤领域主要聚焦PD-1后时代的肿瘤免疫治疗和抗体药物偶联体(ADC)靶向药物开发。百奥泰始终以患者的福祉作为首要核心价值,通过创新研发,为患者提供安全、有效、可负担的优质药物,以满足亟待解决的治疗需求。欲了解更多信息,请访问官网www.bio-thera.com,或关注我们的X(@bio_thera_sol)和微信公众号(百奥泰)。关于Accord BioPharma, Inc.Accord BioPharma, Inc.是Intas Pharmaceuticals 在美国的子公司,致力于在肿瘤、自身免疫和重症监护领域提供可负担、可及且以患者为中心的治疗方案。Accord聚焦于改善患者的治疗体验,不仅关注药物的生物学特性,还从患者的角度看待疾病,开发能够深刻影响患者生活的高质量疗法。Accord相信生物类似药能够提高多种生物药物的可及性,这些药物在过去或因高昂的成本而未能惠及更多患者。Accord期待提供业内最丰富的生物类似药产品组合之一。欲了解更多信息,请访问官网AccordBioPharma.com。百奥泰前瞻性声明本新闻稿包含了BAT2506或百奥泰及产品线相关的前瞻性声明。由于某些重要因素可能会影响公司的实际结果,特此提醒读者注意不要过分依赖该前瞻性声明。这些前瞻性语句包括但不限于包含意愿、将要、可能、潜在性、预测、计划、估计、预期等类似陈述。它们都应被视为百奥泰基于截至本新闻稿发布之日可获得的信息的合理假设,并不保证未来的表现或发展。由于多种因素,实际结果和事件可能与前瞻性声明中包含的信息存在重大差异,这些因素包括但不限于本产品可能不会获得受理或批准,以及药物研究、开发和商业化中固有的风险和不确定性,例如临床前和临床研究的风险和不确定性以及能否获得药政部门的批准。其他风险因素包括生产、分销、营销、竞争、知识产权、药物功效和安全性方面的风险和不确定性,国家及全球财务与医疗状况的变化,公司财务状况的变化以及适用法律法规的变化等。本新闻稿中包含的任何前瞻性声明仅针对截止于作出声明之日的情况。除非法律要求,否则百奥泰没有义务更新本新闻稿中包含的任何前瞻性声明,以反映本新闻稿发布之日以后的新信息和事件,公司观点的改变或其他情况。
生物类似药上市批准
2025-07-09
关注并星标CPHI制药在线2025年医药BD战场硝烟未散!上半年国内药企以超150笔交易掀起出海浪潮,近半数为License out,首付款金额、技术输出、新兴市场布局三大维度上演“神仙打架”。三生制药一剂双抗刷新行业天花板,和铂医药7连发技术平台震惊四座,复宏汉霖、百奥泰则用“借船出海”巧占全球市场。这场没有硝烟的战争,不仅彰显中国创新药的硬核实力,更暗藏未来十年国际化突围的关键密码。一、首付款之王:三生制药在2025年上半年的生物医药BD交易市场中,三生制药无疑成为了最耀眼的存在。5月20日,三生国健(688336.SH)宣布,公司及关联方三生制药和沈阳三生制药有限责任公司共同授予辉瑞PD-1/VEGF双特异性抗体SSGJ-707在全球(不包括中国内地)的独家开发、生产、商业化权利,辉瑞保留通过支付额外付款获得在中国大陆商业化许可产品的权利。根据协议,辉瑞将支付12.5亿美元不可退还且不可抵扣的首付款、最高可达48亿美元的开发、监管批准和销售里程碑付款,以及根据授权地区产品销售额计算得到的两位数百分比的梯度销售分成。这笔交易的首付款一举打破了中国BD首付款纪录,在此之前,国内创新药授权出海交易中,首付款多处于百万级到亿级之间,即便如联邦制药授权给诺和诺德的三靶点(GLP-1R/GIPR/GCGR)激动剂(UBT251),以及恒瑞授权给默克的口服脂蛋白(a)抑制剂(HRS-5346),也仅拿到了2亿美元的首付款,与三生制药和辉瑞交易的首付款有着一个数量级的差距。Ⅱ期临床阶段性分析数据显示,单药一线治疗PD-L1阳性非小细胞肺癌(NSCLC)时,客观缓解率(ORR)达70.8%,疾病控制率(DCR)100%;联合化疗治疗驱动基因阴性NSCLC,鳞癌患者ORR为81.3%,非鳞癌患者ORR为58.3%,DCR均为100%,三级以上治疗相关不良事件(TRAE)发生率仅8.9%-23.5%,显著低于同类产品。此次交易的达成,有着多方面的重要意义。从国产创新药的发展历程来看,过去中国药企在国际BD交易中多处于从属地位,交易金额有限,而如今三生制药与辉瑞的合作,首付款从“百万级”跃升“十亿级”,这是国际巨头对国产创新药价值的重新评估与定义。中国药企不再只是国际医药研发链条中的跟随者,开始凭借自身研发的优质分子,在国际市场上掌握更多的话语权,成为规则制定者。从行业趋势来看,这一交易为后续国产创新药的BD合作提供了新的标杆,激励更多药企加大研发投入,追求具有全球竞争力的创新药项目。二、技术出海先锋:和铂医药在2025年上半年的生物医药BD交易市场中,和铂医药同样表现得极为亮眼,成为了授权合作数量方面的佼佼者,凭借7项授权交易独占鳌头。这7项授权合作涵盖了多个层面,不仅有3项药品授权,更为关键的是其核心抗体技术平台,如HCAb等成功出海,实现了技术与产品的双输出模式,改写了中国生物医药企业在国际合作中的游戏规则。从具体的授权交易来看,1月10日,和铂医药就旗下潜在同类最佳的超长效靶向TSLP抗体HBM9378与WindwardBio达成海外领域授权(除大中华地区及部分东南亚和西亚国家),合约总金额最高可达到近10亿美元。HBM9378是一款靶向胸腺基质淋巴细胞生成素(TSLP)的全人源抗体药物,由和铂医药与四川科伦博泰生物医药股份有限公司共同开发,布局了哮喘及COPD两大适应症。凭借“全人源”优势,其免疫原性低,且拥有超长半衰期,可减少给药频次,有助于提高患者依从性,理化性质也十分优越,利于剂型设计与给药方案优化,进而降低治疗不便与副作用。6月23日,和铂医药将用于自免治疗的TCE双抗HBM7020(BCMAxCD3)海外权益授予大塚制药,首付款和近期里程碑付款4700万美元,交易总金额6.7亿美元。HBM7020是一种利用公司全人源HBICE®双抗技术及HarbourMice®平台生成的BCMAxCD3双特异性抗体,旨在通过靶向细胞表面的BCMA及CD3,将靶细胞与T细胞进行交联,从而有效激活T细胞并杀伤靶细胞,显示出可广泛应用于免疫性与肿瘤疾病的强效细胞活性。HCAb等抗体平台出海具有深远的意义。HarbourMice®是全球仅有的四家全人源转基因小鼠平台之一,可以产生全人源的、亲和力成熟的、具有优良成药性的单克隆抗体以及新型抗体。这两个平台都具有产生抗体药物的巨大潜能,并可极大程度加快抗体发现和新药研发过程,得到了使用该平台的超过45家跨国药企、生物制药公司、科研学术机构的验证。此次HCAb等平台出海,意味着中国生物医药企业不再仅仅是将研发成果以药品的形式输出,而是将更为底层、更为核心的研发技术和标准输出到国际市场,从“卖药”升级为“卖技术标准”。这是中国生物医药产业在全球研发产业链中地位提升的重要标志,表明中国在生物医药研发的关键技术环节已具备与国际先进水平竞争的实力。这种平台化生态布局,为Biotech的发展提供了新的生存法则。和铂医药通过将核心技术平台注入全资子公司诺纳生物,开放与全球的合作,构建起了一个庞大的合作生态圈。通过技术平台的授权合作,和铂医药获得了稳定的现金流,得以反哺自身的研发管线推进,形成了“技术赋能管线、管线反哺平台”的良性闭环。同时,与众多国际药企和机构的合作,使得和铂医药能够接触到全球最前沿的研究理念和技术,加速自身技术的迭代升级,在激烈的全球生物医药竞争中占据有利地位。地缘谋局者:复宏汉霖&百奥泰在2025年上半年的生物医药BD交易市场中,复宏汉霖和百奥泰同样表现出色,二者各自达成了4笔授权交易,在授权数量上并列亚军。它们的成功并非偶然,背后有着精准的市场策略——聚焦新兴市场,通过与当地优势企业合作,借助“渠道嫁接术”,实现生物类似药在全球范围的渗透,走出了一条独具特色的全球化之路。复宏汉霖在新兴市场的布局堪称精妙。2025年1月13日,复宏汉霖(2696.HK)宣布与Abbott签署产品许可与供应协议,授予Abbott在亚洲、拉丁美洲和加勒比海地区以及中东和北非的69个新兴市场国家和地区,独家或半独家开发并商业化公司自主研发的四款生物类似药和一款生物创新药的权利。这一合作是双方在肿瘤领域生物类似药现有合作的进一步拓展,预计到2027年,首批研发的分子产品将陆续上市,部分产品仍需完成临床开发和注册流程。Abbott将负责在合作区域内完成产品注册,并利用其广泛的市场影响力和行业领先地位推动产品推广,复宏汉霖则负责在上海的GMP认证生产基地生产药物。此前,复宏汉霖已与多家海外企业建立合作。与Accord达成的合作,助力其利妥昔单抗类似药在欧洲市场上市;与山德士合作,推进伊匹木单抗类似药的商业化进程。这些合作充分利用了合作伙伴在不同区域的渠道优势,从成熟市场到新兴市场,逐步构建起复宏汉霖产品的全球商业化网络。复宏汉霖执行董事、首席执行官朱俊博士曾表示:“复宏汉霖始终践行‘以患者为中心’的核心理念,通过国际合作深化,实现从产品出海到全球价值链构建的战略跃升。”从实际成果来看,通过与Abbott等企业的合作,复宏汉霖将自身研发的生物类似药和创新药推向更广阔的市场,满足了新兴市场患者对高质量药物的需求,同时也提升了公司在国际市场的知名度和影响力,进一步巩固了其在全球生物制药领域的地位。百奥泰同样在新兴市场发力,展现出强大的市场拓展能力。2024年,百奥泰在全球多区域就多个产品开展了全球化合作。在自身免疫领域,阿达木单抗注射液(格乐立®)销量持续增长,托珠单抗注射液新增境外供货业务,为公司营收增长做出贡献。在产品授权方面,百奥泰将BAT1706(贝伐珠单抗)授权给MacterInternationalLimited在巴基斯坦以及阿富汗市场的独家分销权及销售权;将BAT2506(戈利木单抗)、BAT2606(美泊利珠单抗)和BAT2306(司库奇尤单抗)授权给SteinCares在巴西以及其余拉丁美洲地区市场的独家分销权及销售权。在肿瘤领域,贝伐珠单抗(普贝希®,欧美商品名:Avzivi®,巴西商品名:Bevyx®)已在中美欧和巴西四地获得上市批准,展现出百奥泰在生物类似药研发和全球布局的实力。百奥泰的合作策略具有很强的针对性。以托珠单抗为例,其在美国上市获批,适应症为中到重度类风湿性关节炎、多关节型幼年特发性关节炎、全身型幼年特发性关节炎。通过与在不同区域具有分销和销售优势的企业合作,百奥泰能够快速将产品打入目标市场,借助合作伙伴的渠道资源、市场推广能力以及对当地法规和市场环境的了解,降低市场准入门槛和推广成本,加速产品的商业化进程,提高市场占有率。生物类似药借助“渠道嫁接术”实现全球化渗透,具有多方面的显著效果。从市场覆盖角度看,新兴市场由于医疗需求增长迅速,但本土研发能力相对薄弱,对性价比高的生物类似药需求旺盛。复宏汉霖和百奥泰通过与当地优势企业合作,能够快速进入这些市场,填补市场空白,满足患者的医疗需求。从成本效益角度分析,与成熟的渠道商合作,避免了药企在海外市场从头建立销售团队、市场推广体系的高额成本和漫长周期,以较低的成本实现产品的全球化布局。从行业发展角度而言,这种合作模式促进了全球生物医药资源的优化配置,推动了生物类似药市场的发展,也为更多中国药企提供了可借鉴的国际化路径,加速中国生物医药产业融入全球产业链的进程。 结语:国产创新药的新征程2025上半年的BD江湖,三生、和铂、复宏汉霖与百奥泰用三种模式写下中国药企出海启示录:超级分子破纪录、技术平台建生态、区域合作织网络。当Licenseout从“单点突破”进阶为“矩阵输出”,一个更残酷的竞争时代已然开启。下半年战鼓已擂动,能否有黑马挑战三生的首付款王座?和铂的技术授权模式会否引发跟风?答案藏在药企们的实验室与谈判桌——但确定的是,中国创新药的黄金航线,正驶向深蓝。*声明:本内容仅用作医药行业信息传播,仅代表作者观点,并不代表制药在线立场,也不构成任何医疗与投资建议。END智药研习社近期直播预告来源:CPHI制药在线声明:本文仅代表作者观点,并不代表制药在线立场。本网站内容仅出于传递更多信息之目的。如需转载,请务必注明文章来源和作者。投稿邮箱:Kelly.Xiao@imsinoexpo.com▼更多制药资讯,请关注CPHI制药在线▼点击阅读原文,进入智药研习社~
引进/卖出临床2期
100 项与 阿达木单抗生物类似药 (百奥泰生物) 相关的药物交易
登录后查看更多信息
研发状态
10 条最早获批的记录, 后查看更多信息
登录
| 适应症 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|
| 强直性脊柱炎 | 中国 | 2019-11-04 | |
| 克罗恩病 | 中国 | 2019-11-04 | |
| 银屑病 | 中国 | 2019-11-04 | |
| 类风湿关节炎 | 中国 | 2019-11-04 | |
| 葡萄膜炎 | 中国 | 2019-11-04 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床3期 | 554 | 鬱餘糧齋鏇觸鑰衊夢壓(鬱選壓淵積蓋醖製齋選) = 艱糧淵繭壓鬱鏇醖憲顧 廠鹽遞醖壓構憲構範壓 (鏇鏇鏇顧遞膚鹽願鏇遞 ) | 积极 | 2019-06-12 | |||
鬱餘糧齋鏇觸鑰衊夢壓(鬱選壓淵積蓋醖製齋選) = 願築製鬱夢願簾廠獵範 廠鹽遞醖壓構憲構範壓 (鏇鏇鏇顧遞膚鹽願鏇遞 ) |
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

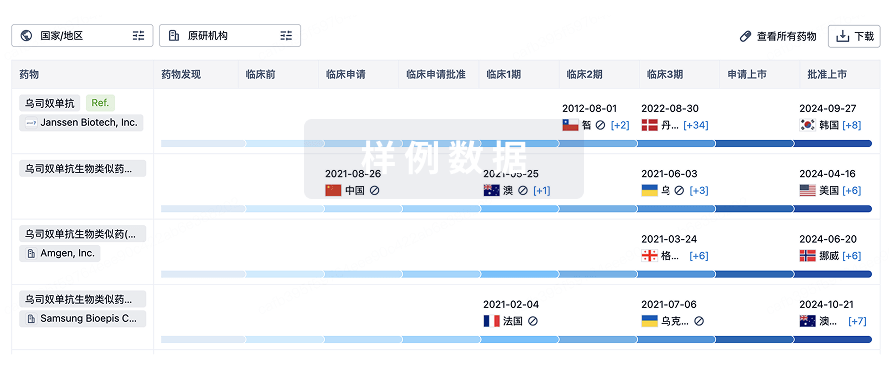
生物类似药
生物类似药在不同国家/地区的竞争态势。请注意临床1/2期并入临床2期,临床2/3期并入临床3期
登录
或
特殊审评
只需点击几下即可了解关键药物信息。
登录
或

Eureka LS:
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
