预约演示
更新于:2025-01-23
MASP2 x TACI
更新于:2025-01-23
关联
1
项与 MASP2 x TACI 相关的药物作用机制 MASP2抑制剂 [+1] |
非在研适应症- |
最高研发阶段临床前 |
首次获批国家/地区- |
首次获批日期1800-01-20 |
100 项与 MASP2 x TACI 相关的临床结果
登录后查看更多信息
100 项与 MASP2 x TACI 相关的转化医学
登录后查看更多信息
0 项与 MASP2 x TACI 相关的专利(医药)
登录后查看更多信息
1
项与 MASP2 x TACI 相关的文献(医药)International Journal of Molecular Sciences
Genomic Landscape of Susceptibility to Severe COVID-19 in the Slovenian Population
Article
作者: Vokač Križaj, Hana ; Kovanda, Anja ; Šelb, Julij ; Rituper, Boštjan ; Korošec, Peter ; Čižek Sajko, Mojca ; Maver, Aleš ; Lukežič, Tadeja ; Peterlin, Borut ; Bitežnik, Barbara ; Rijavec, Matija ; Bidovec-Stojković, Urška
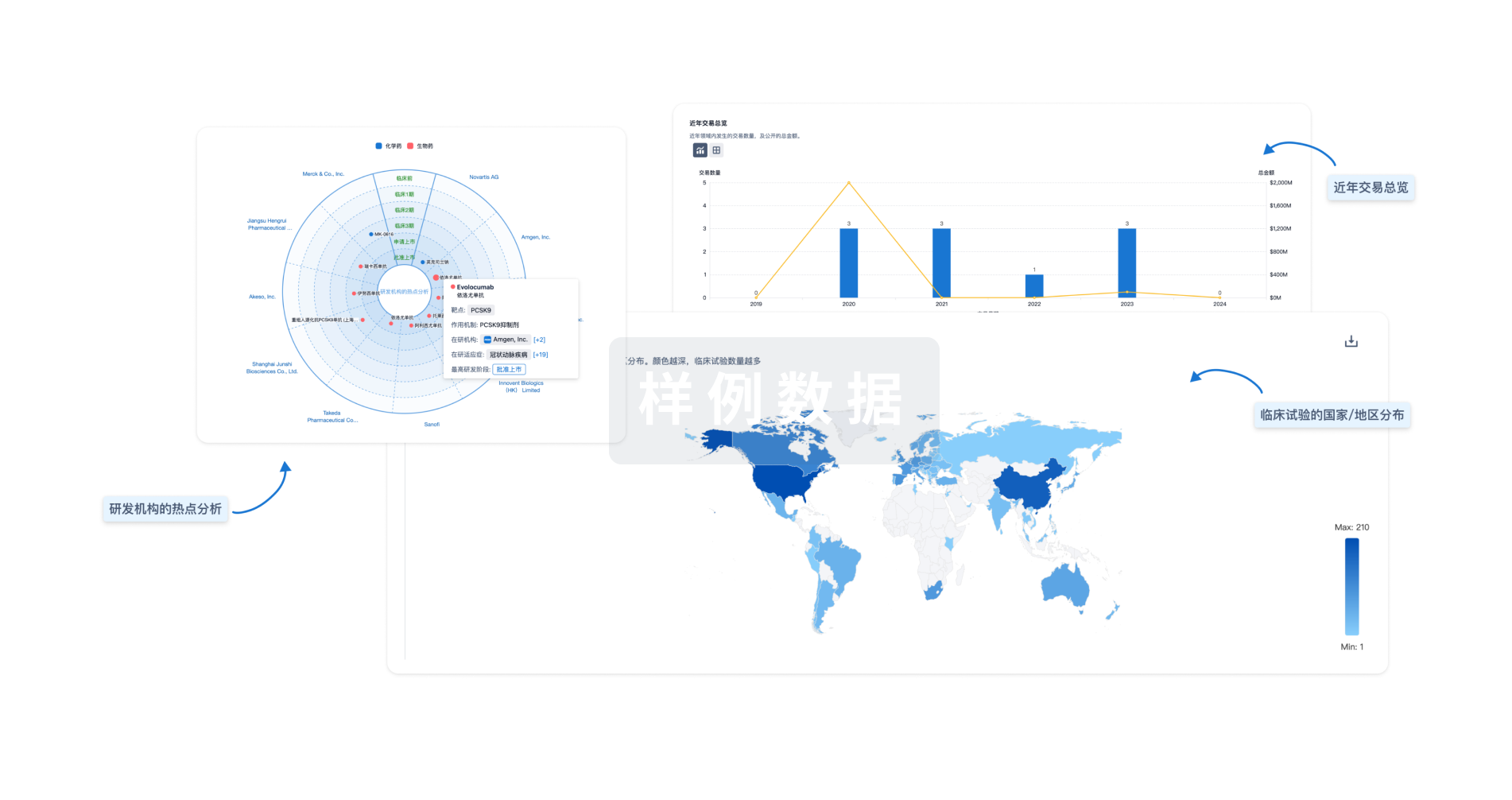
分析
对领域进行一次全面的分析。
登录
或
来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用