预约演示
更新于:2025-01-23
ROR1 x DNA
更新于:2025-01-23
关联
1
项与 ROR1 x DNA 相关的药物作用机制 DNA嵌入剂 [+2] |
在研机构  VelosBio, Inc.初创企业 VelosBio, Inc.初创企业 |
原研机构  VelosBio, Inc.初创企业 VelosBio, Inc.初创企业 |
非在研适应症- |
最高研发阶段临床前 |
首次获批国家/地区- |
首次获批日期1800-01-20 |
100 项与 ROR1 x DNA 相关的临床结果
登录后查看更多信息
100 项与 ROR1 x DNA 相关的转化医学
登录后查看更多信息
0 项与 ROR1 x DNA 相关的专利(医药)
登录后查看更多信息
4
项与 ROR1 x DNA 相关的新闻(医药)2024-10-09
摘要:化学免疫疗法和细胞疗法是复发/难治性(R/R)淋巴瘤治疗的主要手段。这些治疗中出现的耐药性和常见毒性限制了它们在实现期望的响应率和持久缓解方面的作用。抗体-药物偶联物(ADC)是一种新型靶向疗法,已证明在治疗包括淋巴瘤在内的各种癌症中具有显著的疗效。迄今为止,已有三种ADC药物被批准用于不同类型的淋巴瘤,这标志着该领域取得了重大进展。在本文中,我们旨在回顾ADC的概念及其在淋巴瘤治疗中的应用,分析目前批准的药物,并讨论ADC开发正在进行的进展。
1.引言
淋巴瘤是一组来自不同类型淋巴细胞(B细胞、T细胞或自然杀伤(NK)细胞)在不同成熟阶段的克隆性增殖的恶性肿瘤。过去几十年来,不同类型淋巴瘤的发病率一直在增加。化学免疫疗法和细胞疗法仍然是不同亚型淋巴瘤常用的治疗手段。大多数化疗方案的治疗效果指数较窄,导致广泛的毒性。此外,耐药性的出现是最常见的原因之一,阻碍了它在复发和难治性(R/R)情况下的使用。针对表面抗原的单克隆抗体,如利妥昔单抗和奥比妥珠单抗,已经彻底改变了淋巴瘤的治疗。抗体-药物偶联物(ADCs)是一种高度靶向的药物,将针对特定表面抗原的单克隆抗体(mAb)与细胞毒素分子连接起来。毒素只传递给表达表面抗原的细胞,具有高度的肿瘤特异性和有限的系统暴露。美国食品药品监督管理局(FDA)已经批准了三种用于治疗淋巴瘤的ADC药物,分别是本妥昔单抗、波拉图单抗和洛卡图单抗。
在本文中,我们将回顾ADC的概念,重点关注它们的结构、工程和在淋巴瘤治疗中的作用。此外,我们将提供目前批准的ADC在这一设置中的综合分析,以及正在进行的进展的概述。这包括突出来自临床前和临床试验的有希望的结果,以及讨论下一代ADC开发的未来方向。
2.ADC的基本结构
ADC由抗体、药物(有效载荷或细胞毒素)和连接子组成。抗体结合恶性细胞表面表达的特定抗原。一旦结合,ADC被内化,细胞毒素有效载荷释放到细胞内,导致细胞周期终止和凋亡。在周围目标阴性细胞中也可以看到细胞毒性效应,当药物扩散到它们中并引起“旁观者杀伤”时,这是一种当有效载荷从被内化和降解的ADC释放或当药物释放到细胞外空间后从目标细胞释放时发生的细胞死亡。值得注意的是,为了获得更好的结果和更少的副作用,抗原和抗体之间的结合需要尽可能特异性。有效载荷的内化率、连接子的稳定性和相应抗体的选择是影响ADC在临床实践中使用的一些变量。
2.1. 单克隆抗体
选择合适的抗体是ADC工程中的关键步骤;它通常被设计为特异性结合癌细胞表面表达的目标抗原。理想的单克隆抗体应具有低免疫原性、低交叉反应性、长的血浆半衰期,以及对肿瘤细胞表面抗原的高结合亲和力。最常用的类别是免疫球蛋白G(IgG),更具体地说是IgG1亚型,因其血清稳定性。在ADC开发的早期阶段,主要使用小鼠来源的抗体。然而,这些抗体报告有很高的失败率,可能归因于它们缺乏临床效益,同时引起严重的免疫原性相关的不良效应。这些ADC也被人类抗小鼠抗体迅速清除,限制了它们的疗效。此外,这些早期ADC中使用的连接子在人体循环中不稳定,导致有效载荷过早释放,大大降低了效果并增加了毒性。自从出现显著降低免疫原性的人源化小鼠单克隆抗体以来,已经取代了小鼠抗体,导致更优化的设计,如2000年FDA批准的针对CD33阳性急性髓系白血病患者的首个ADC药物吉妥单抗奥佐米星。迄今为止,已有十四种ADC获得FDA市场批准,其中三种如前所述已获批准用于治疗淋巴瘤。其中,只有本妥昔单抗使用嵌合抗体。嵌合抗体是通过融合不同物种的域(例如,整个小鼠或兔的可变区与人类来源的恒定域)设计的。相比之下,人源化抗体含有嵌入人类来源的Fab区和恒定区的外来氨基酸段。因此,它们较少免疫原性,是更安全的选择。在全人抗体中,没有一部分是小鼠来源的,与人类化抗体相比,它们在免疫反应中的发生率更低;例如FDA批准的enfortumab vedotin。
2.2. 有效载荷
ADC的理想有效载荷应具有低免疫原性、长半衰期、小分子量、在抗体的水性环境中良好的溶解度、在循环和溶酶体中的高稳定性、体外亚纳摩尔半最大抑制浓度(IC-50)以及有助于与抗体结合的官能团,同时保持ADC的内化特性。每个抗体平均结合两到四个强效的细胞毒素分子。目前,ADC设计中最受欢迎的两类有效载荷是微管破坏剂和DNA靶向剂(图1)。
图1. 设计ADC时常用的十种不同有效载荷的分子结构
微管抑制剂可以根据它们的作用机制分为两大类。第一组包括微管稳定剂。这些药物通过抑制微管解聚和促进聚合来增强丝状体的稳定性,使丝状体功能降低。第二组由破坏微管的物质组成,阻止微管蛋白组装和成熟微管的发展。在ADC开发中使用和研究的主要微管抑制剂包括长春碱类、紫杉醇类、auristatins、美登素类、隐孔菌素、海葵素和圆盘菌素。auristatins如单甲基auristatin E (MMAE)通过阻止α-和β-微管蛋白单体聚合并触发凋亡来破坏微管并阻止细胞分裂。结合区域位于两个纵向排列的微管二聚体的β1-微管蛋白和α2-微管蛋白亚基之间。根据体外研究结果,auristatin-微管蛋白键合形成环状或螺旋形聚集体,改变微管的功能。长春碱类如长春新碱或长春碱,以及隐孔菌素和多拉斯他汀,诱导微管形成类似的弯曲结构构象。
在细胞周期的任何阶段,DNA损伤剂通过双链断裂、烷基化、插入和交联四种主要机制可以杀死癌细胞。最常用的DNA损伤有效载荷是卡利烯胺、二酮霉素、吡咯并苯并二氮杂环(PBD)、多柔比星和喜树碱类似物。针对BCL-2抑制剂、剪接体抑制剂和针对RNA聚合酶II的转录抑制剂等靶向药物是具有不同作用机制的额外有效载荷。
值得注意的是,根据FDA对15种含有PBD有效载荷的ADCs的肿瘤学分析,PBD有效载荷的毒性概况更高,这表明常见的不良事件包括可能的血管渗漏综合征、转氨酶升高、骨髓抑制、胃肠事件、代谢效应、肌肉骨骼事件、神经病变、呼吸困难和肾损伤,所有这些都源于PBD的非靶向输送;该分析表明,2013年至2017年间47%的PBD偶联ADCs的新药申请被中止。这些高效ADCs发生危及生命的毒性的更高发生率是一个限制。
目前减轻PBD毒性的机制包括药物-连接子组分的聚乙二醇化,这显著提高了ADC的耐受性。另一种机制是使用对氨基苄氧羰基(PABC)自毁间隔基,在连接臂-药物中;该间隔基具有稳定的二硫键,允许在细胞内快速释放自由有效载荷,从而实现更好的血浆稳定性和与可裂解连接臂相比提高的毒性。后一项研究认为,肽连接的和二硫键连接的PBD ADC在两种不同的淋巴瘤模型中提供了相似的疗效,并且二硫键连接的PBD ADC具有更好的安全性。第三种机制是通过减少PBD结构中的一个亚胺官能团进行化学修饰,从而将DNA交联的PBD二聚体转变为DNA烷基化代谢物,称为吲哚喹喔啉二聚体(IGN),这在小鼠肿瘤模型中实现了更有效的载荷释放,其中小鼠能够耐受更高剂量的IGN偶联ADC。
近期在有效载荷方面也取得了进展。主要的进展是免疫调节ADC,如干扰素基因刺激剂(STING)激动剂、Toll样受体(TLR)激动剂和使用蛋白酶体靶向嵌合体(PROTAC)策略的目标蛋白降解剂(TPD)。STING激动剂激活干扰素和其他细胞因子的产生,从而增强免疫和抗肿瘤反应。将STING激动剂作为有效载荷纳入ADC可以实现其向肿瘤目标的传递,具有更高的疗效和由于免疫激活导致的过度炎症反应而减少的毒性。STING激动剂的例子包括DMXAA、c-di-AMP、c-di-GMP、cGAMP、ADU-S100、MK-1454、SB11285、BMS-986301、E7766、MSA-1和MSA-2;它们主要在乳腺癌中被探索。TLR激动剂通过增强肿瘤微环境中抗原呈递细胞的抗原呈递,改善先天和适应性抗肿瘤免疫,从而促进更多细胞毒性T细胞的促进和活性。它们在局部癌症中发挥作用,例如,BCG(TLR2/4激动剂)用于膀胱非浸润性癌,AS04(TLR4激动剂)用于宫颈癌,以及咪喹莫特(TLR7激动剂)用于表皮基底细胞癌。目前,许多TLR激动剂正在作为ADC中的有效载荷在癌症免疫疗法中进行研究。一个例子是BDC-1001(TLR7/TLR8激动剂与抗HER2抗体偶联的ADC),在临床前模型中显示出有希望的结果。目前正在进行一项I/II期临床试验,该试验正在招募表达HER2的晚期实体瘤患者(NCT04278144)。PROTAC是一种催化作用于小剂量的催化剂,它通过泛素化介导的蛋白水解作用靶向特定的蛋白质。当PROTAC有效载荷与抗体偶联时,它会产生PROTAC催化行为和抗体的组织特异性的新型组合,具有更好的疗效和更少的限制。在表达HER2的细胞中存在成功的例子。这些在ADC设计中的微妙改进具有巨大的潜力,通过不断的研究可以为肿瘤学带来更好的结果,并为包括淋巴瘤在内的其他癌症类型的发展打开大门。
2.3. 化学连接臂
连接臂是成功开发ADC的最重要和最复杂的部分,因为它们形成了治疗和抗体之间的联系。它们的结合机制、稳定性和化学性质对于防止意外释放药物进入血流以及在癌细胞内吞后促进容易裂解至关重要,允许有效载荷仅在预期的地点释放。它们在确定ADC的药代动力学、药效学和治疗窗口方面至关重要。目前FDA批准的ADC使用两类连接臂,它们在有效载荷释放机制上有所不同:可裂解和不可裂解连接臂。最常用的四种可裂解连接臂是β-葡萄糖醛酸酶敏感连接臂、谷胱甘肽(GSH)敏感二硫键连接臂、卡他蛋白B敏感连接臂和腙连接臂。前面描述的旁观者效应,它影响肿瘤微环境中的正常细胞和没有或低目标表达的肿瘤细胞,更有可能发生在使用可裂解连接臂的ADC中。
不可裂解连接臂与可裂解连接臂相比,具有更好的血浆稳定性、较低的非目标毒性和抗蛋白水解降解的能力,因为它们与抗体的氨基酸残基具有不可还原的键。通常,不可裂解连接臂由硫醚或马来酰亚胺己酰基团形成。附着在由降解的抗体衍生的氨基酸残基上的不可裂解连接臂必须在ADC内化后,由细胞质和溶酶体蛋白酶完全分解抗体部分才能释放有效载荷。图2展示了一般的基本结构。
图2. ADC的一般基本结构。ADC由一个嵌合或人源化(免疫原性较低)的抗体组成,该抗体对淋巴瘤癌细胞表面表达的抗原具有强烈的结合活性。抗体应在循环中具有较高的半衰期,以便被输送到目标细胞表面。抗体与不同结构的有效载荷(主要是微管抑制剂或DNA相互作用)相连,这些是具有理想药物/抗体比例的高效药物。抗体与有效载荷之间的连接是通过可裂解或不可裂解的连接臂实现的,这些连接臂应具有精确的结合、在循环中的稳定性,并确保在目标处有效分配有效载荷。
3.FDA批准用于淋巴瘤的ADC
截至2023年,已有三种ADC获得了FDA对各种类型淋巴瘤的批准,分别是Brentuximab Vedotin(BV)、Polatuzumab Vedotin(PV)和Loncastuximab Tesirine(LT),如表1所示。
Brentuximab Vedotin(BV)由针对CD30的IgG1嵌合单克隆抗体“cAC10”和细胞毒素MMAE组成,它们通过一个稳定的连接臂(Cathepsin可裂解连接臂和对氨基苄基-羰基间隔基)结合在一起。嵌合单克隆抗体cAC10与CD30结合,随后通过内吞作用和随后与溶酶体的囊泡融合,在溶酶体中,溶酶体半胱氨酸蛋白酶裂解连接臂,释放MMAE直接进入癌细胞内,从而导致癌细胞毒性。抗体和MMAE之间的连接系统设计为在循环中稳定,由马来酰亚胺己酰基间隔基、蛋白酶敏感的二肽Val-Cit、自毁PABC基团以及二肽和药物之间的附加间隔基组成。后者具有自裂解的能力,并有助于卡他蛋白B进入其裂解序列。马来酰亚胺部分与抗体重链和轻链中的半胱氨酸残基的末端硫醇形成硫醚键,将连接臂连接到抗体。由蛋白酶裂解Cit-PABC酰胺键产生的不稳定PABC取代的MMAE中间体,通过自发的1,6-消除反应,产生自由的MMAE分子、CO2和对氨基苄基醇。值得注意的是,CD30在恶性淋巴瘤细胞上表达非常强,在正常组织上表达较少。与单独的抗体相比,BV可以使CD30+细胞系的生长停滞高达340倍。BV的结构和作用机制如图3所示。cHL的恶性Reed-Sternberg细胞以表达CD30为特征,CD30是肿瘤坏死因子超家族的成员,鉴于其对一小部分活化的B细胞、T细胞和嗜酸性粒细胞的表达限制,它代表了单克隆抗体治疗的理想靶点。BV在未经治疗的cHL患者和R/R疾病中表现出显著的活性,导致在这些情况下获得FDA批准。
图3. BV的结构和作用机制。它由一个针对淋巴瘤细胞上CD30抗原的单克隆抗体组成。结合后,整个ADC-抗原复合物被细胞内运输到溶酶体,在那里释放MMAE(有效载荷),干扰细胞核中的微管结构,导致细胞周期停滞和凋亡。
ECHELON-1 III期试验将1334名未经治疗的III期或IV期cHL患者随机分配接受BV-AVD(Brentuximab Vedotin、Adriamycin、Vinblastine、Dacarbazine)或ABVD(Adriamycin、Bleomycin、Vinblastine、Dacarbazine)。试验显示BV-AVD组的2年修正无进展生存期(PFS)为82%,而ABVD组为77%,风险比(HR)为0.77,6年总生存期(OS)分别为93.9%和89.4%,HR为0.59。基于ECHELON-1的结果,FDA批准BV与化疗联合用于成人未经治疗的III期或IV期cHL的治疗。最近,SWOG S1826试验被开发出来,比较BV-AVD与N-AVD(Nivolumab、Adriamycin、Vinblastine、Dacarbazine)对儿童和成人新诊断的晚期cHL(III期或IV期)患者的疗效。S1826研究表明,Nivo-AVD的1年PFS(94%)优于BV-AVD(86%),HR为0.48,并且两组的不良事件(AE)概况相当,因此它目前是未经治疗的cHL的一线治疗的首选方案。
尽管年轻患者更容易耐受多药化疗方案,但由于多种因素,包括合并症、身体状况差、无法耐受全剂量化疗以及治疗相关AEs增加,老年cHL人群的治疗结果较差。一项多中心II期研究评估了60岁及以上患者的序贯BV方案,随后进行AVD化疗,并在随后进行BV维持治疗。研究报告了84%的2年PFS率和93%的2年OS率。这种序贯方法提高了这一脆弱人群中cHL的治愈率,是新诊断cHL老年人的首选方案。
在R/R cHL环境中,BV最初在自体造血干细胞移植(ASCT)失败的患者中进行了研究。BV单药治疗显示总响应率(ORR)为75%,完全缓解(CR)为34%,中位无进展生存期(mPFS)为5.6个月。值得注意的是,CR患者的中位持续响应时间(mDOR)为20.5个月。这些结果导致BV首次获得FDA批准,用于治疗ASCT失败或至少两个先前的多药化疗方案失败的cHL患者。随后,AETHERA III期试验包括了接受过ASCT并具有以下不利风险之一的cHL复发难治性疾病患者,例如原发性难治性HL、初次缓解<12个月的复发HL,或一线治疗后复发时的结外受累。AETHERA研究表明,ASCT后早期巩固使用BV将mPFS提高到42.9个月,而对照组为24.1个月,HR为0.57。基于AETHERA试验,FDA随后扩大了BV的批准范围,用于治疗ASCT巩固后有高复发或进展风险的cHL患者。
除了前述的FDA批准外,BV还根据CheckMate 744 II期研究的结果,被国家综合癌症网络(NCCN)指南推荐与Nivolumab联合用于复发或难治性cHL患者的二线或后续治疗。该研究评估了涉及Nivolumab加BV,随后对次优反应患者使用BV加Bendamustine的风险分层响应适应方法。CheckMate 744研究表明,59%接受BV和Nivolumab治疗的患者,以及94%随后接受BV和Bendamustine治疗的患者,实现了完全分子反应(CMR)。这些结果明显优于历史上60至70%的CMR率,为R/R环境中的更高治愈率奠定了基础。
正在进行的BV在cHL的试验如图2所示。
BV在CD30阳性T细胞淋巴瘤中的作用
系统性间变性大细胞淋巴瘤(sALCL)中CD30的普遍表达,以及在外周T细胞淋巴瘤-未另行指明(PTCL-NOS)、血管免疫母细胞性T细胞淋巴瘤(AITL)和成人T细胞白血病或淋巴瘤(ATLL)等亚型中的高表达,为在T细胞淋巴瘤中靶向CD30提供了强有力的理由。
一项针对至少一种联合化疗方案失败后的R/R ALCL患者的II期研究显示,86%的患者实现了客观反应,其中57%为CR,mDOR为12.6个月。这项研究的结果导致FDA批准BV用于R/R PTCL。ECHELON-2试验旨在比较BV与环磷酰胺、多柔比星和泼尼松(A+CHP)联合使用与标准CHOP(环磷酰胺、多柔比星、长春新碱和泼尼松)治疗未经治疗的CD30阳性PTCL患者的疗效和安全性。A+CHP显示出48.2个月的mPFS,与CHOP的20.8个月相比,具有可比的安全性概况。5年PFS分别为A+CHP的51.4%和CHOP的43%(HR 0.7),5年OS分别为A+CHP的70.1%和CHOP的61%(HR 0.72),两组之间的安全性概况相当。随后的亚组分析显示,S-ALCL主要从A+CHP中受益,而AITL和PTCL-NOS亚组的益处尚不明确。
除了PTCL,BV在皮肤T细胞淋巴瘤(CTCL)中的作用也得到了探索。ALCANZA III期试验包括了接受过一线系统治疗的原发性皮肤间变性大细胞淋巴瘤(pcALCL)或表达CD30的蕈样真菌病(MF)的患者。在平均45.9个月的随访中,试验偏爱BV组,ORR为54.7%对12.5%,mPFS为16.7对3.5个月。同样,与医生选择相比,BV组的下一次治疗的中位时间显著更长(14.2对5.6个月;HR 0.27)。基于ALCANZA试验的结果,FDA批准BV用于治疗接受过先前系统治疗的pcALCL或表达CD30的MF患者。目前,BV正在许多早期阶段的试验中进行评估,这些试验包括在表2中。
波拉图珠单抗(PV)由一种抗CD79B的人源化IgG1单克隆抗体组成,通过一个可被蛋白酶裂解的马来酰亚胺己酰基-缬氨酸-PABC肽段连接臂与MMAE结合。一旦波拉图珠单抗与CD79b结合,它就会被内吞并通过内质网运输到溶酶体,在那里发生连接臂裂解,导致有效载荷释放到细胞内诱导凋亡。PV的结构和作用机制如图4所示。
图4. PV的结构和作用机制。PV由一个针对淋巴瘤细胞上的CD79b抗原的单克隆抗体组成。结合后,整个ADC-抗原复合物被内吞到内质体,并与溶酶体融合。然后连接臂被裂解以释放MMAE(有效载荷),这反过来导致细胞核中的有丝分裂停止和细胞死亡。
5.1. PV在弥漫大B细胞淋巴瘤中的应用
弥漫大B细胞淋巴瘤(DLBCL)是非霍奇金淋巴瘤(NHL)最常见的形式。虽然利妥昔单抗的加入显著提高了CHOP化疗的治愈率,但大约40-50%的患者最初反应后会出现难治性疾病或复发。
POLARIX是一项具有里程碑意义的III期研究,评估了PV加入R-CHP(利妥昔单抗、环磷酰胺、多柔比星、泼尼松)在DLBCL一线治疗中的疗效,并与R-CHOP进行了比较。POLARIX证明了pola-R-CHP组2年PFS为76.7%对70.2%,(分层HR 0.73)。两组的整体安全性概况相似。值得注意的是,pola-R-CHP的益处在60岁以上的患者、国际预后指数(IPI)在3到5之间的患者以及具有活化B细胞样亚型的DLBCL患者中观察到。相反,在60岁或以下的患者、有大量疾病、较低IPI评分或滤泡中心B细胞样亚型的DLBCL患者中没有明显益处。基于POLARIX试验,pola-R-CHP是第一个在DLBCL一线治疗中证明比R-CHOP具有更好PFS的方案,并获得了FDA对先前未经治疗的DLBCL、未另行指明(NOS)、高级别B细胞淋巴瘤(HGBL)或IPI评分为2或更高的患者的批准。
POLAR BEAR III期试验比较了mini-R-CHOP与pola-mini-R-CHP作为老年DLBCL患者的一线治疗。初步安全性数据显示,两种方案在老年人(69%在80至90岁之间)和脆弱人群中(16%脆弱,12%的ECOG表现状态为3)都是可耐受的,用波拉图珠单抗替代长春新碱并没有导致3到4级血液学毒性或神经病变的发生率更高。值得注意的是,pola-mini-R-CHP组的胃肠道不良事件频率更高(31%对16%)。基于POLARIX试验的结果,人们倾向于假设pola-mini-R-CHP可能显示出比mini-R-CHOP更好的PFS。因此,这项研究的结果备受期待。
在R/R DLBCL环境中,评估PV安全性和有效性的第一项试验是Ib/II期试验,该试验比较了PV与利妥昔单抗(R)和苯达莫司汀(B)联合使用与单独BR对不适合移植的R/R DLBCL的疗效。pola-BR组显示更高的CR(40%对17.5%),更长的mPFS(9.5对3.7个月,HR 0.36),以及更高的mOS(12.4对4.7个月,HR 0.42)。然而,它导致了更高比例的3到4级中性粒细胞减少症(46.2%对33.3%)、贫血(28.2%对17.9%)和血小板减少症(41%对23.1%),尽管3到4级感染的发生率相似(23.1%对20.5%)。与PV相关的周围神经病变在43.6%的患者中观察到,但大多数是1到2级并解决了。这项试验导致了2019年6月pola-BR的初步批准及其在这种情况下的广泛使用。
波拉图珠单抗的另一个有希望的组合在Ib/II期试验中得到证明,该试验结合了Mosunetuzumab,一种针对CD20和CD3的人源化IgG1双特异性抗体,在R/R DLBCL、HGBCL、转化的FL或3b级FL中。在平均23.9个月的随访中,59.2%的患者对波拉图珠单抗加Mosunetuzumab有反应,45.9%的患者达到了CR。mPFS为11.4个月,mOS为23.3个月。这种方案被良好耐受,最常见的AE是25%患者的中性粒细胞减少症。总的来说,这些结果表明波拉图珠单抗和Mosunetuzumab的组合可以在不适合移植的R/R LBCL中带来具有临床意义的反应和有利的安全性概况。
5.2. PV在其他B细胞非霍奇金淋巴瘤(B-NHL)中的应用
除了DLBCL,包括PV的联合疗法也在惰性B-NHL中进行了探索。在Ib/II期试验中,评估了波拉图珠单抗、奥比妥珠单抗(G)和来普尼(Len)联合治疗R/R FL的安全性和有效性。在平均27个月的随访后,结果显示ORR为76%,CR率高达63%,尽管没有达到预先设定的活性阈值。在平均43.3个月的随访后,mPFS和mOS尚未达到,而4年的里程碑PFS为53%。这些结果与R/R FL的现有标准化疗选择相当,并支持在FL中进一步研究Pola-G-Len方案。
PV的疗效也在套细胞淋巴瘤(MCL)中进行了研究。在一项针对R/R MCL的II期研究中,PV与Mosunetuzumab联合用于先前接受过两线或以上治疗的患者,包括布鲁顿酪氨酸激酶抑制剂(BTKi),并显示出75%的高ORR和70%的CR。然而,需要更多的结果数据来评估其在MCL中的作用,对于对化疗免疫疗法和BTKi耐药的患者迫切需要新的方案。
6.隆卡图珠单抗
CD19是一种在B细胞分化的最早阶段直到浆细胞发育过程中表达的表面糖蛋白。除了正常的B细胞,CD19也在大多数B细胞淋巴瘤中表达。与CD20相比,CD19表现出更均匀的表达,并在抗CD20靶向治疗后的小部分CD20阴性肿瘤中保留,使其成为免疫疗法和联合疗法的选择性靶点。隆卡图珠单抗(LT,ADCT-402)是一种ADC,由一种人源化抗CD19单克隆抗体组成,通过一个可被卡他蛋白裂解的连接臂与高度细胞毒性的DNA小沟交叉链接吲哚喹喔啉二聚体毒素(PBD二聚体)结合。由于其快速的内吞动力学、运输到溶酶体和在循环中的稳定性,LT是针对CD19最有效的ADC。LT的结构和作用机制如图5所示。
图5. LT的结构和作用机制。LT由单克隆抗体Loncastuximab通过可裂解连接臂(统称为Tesirine)与PBD二聚体(有效载荷)相连。该抗体与淋巴瘤细胞上的CD19抗原结合,之后整个复合物被内吞并合并到溶酶体中。接着,PBD被释放到细胞质中,它移动到细胞核,在那里发生DNA交叉链接,导致细胞死亡。
6.1. LT在弥漫大B细胞淋巴瘤中的应用
LT在人体I期研究中显示出对R/R NHL具有临床意义的活性,这导致了LOTIS-2研究,该研究评估了其在R/R DLBCL中的疗效。LT显示出48.3%的ORR,其中50%的应答者达到了CR。虽然mPFS为4.9个月,但达到CR者的mDOR为13.4个月。它展示了通常被良好耐受的安全概况,中性粒细胞减少症是最常见的3级AE(26%),其次是血小板减少症(18%)和γ-谷氨酰转移酶升高(17%)。显著的抗肿瘤活性、持久的反应和可接受的安全概况导致了2021年FDA批准用于治疗经过两线或以上系统治疗后的R/R大B细胞淋巴瘤。批准包括那些有DLBCL NOS、由低级别淋巴瘤引起的DLBCL和HGBL。
在具有里程碑意义的LOTIS-2研究之后,LT与其他靶向疗法的组合,如LOTIS-3中的ibrutinib和LOTIS-5中的单克隆抗CD20抗体rituximab对R-GemOX(利妥昔单抗、吉西他滨和奥沙利铂)进行了评估,但目前尚不清楚这些组合是否会进入临床应用(表2)。
6.2. LT在滤泡性淋巴瘤中的应用
LT在复发/难治性非霍奇金淋巴瘤(R/R NHL)的I期研究中进行了评估,其中在滤泡性淋巴瘤(FL)中显示了78.6%的客观反应率(ORR)。在2023年美国血液学会(ASH)会议上,最近展示了将LT与利妥昔单抗联合应用于R/R FL的II期试验的非常鼓舞人心的结果。该试验显示了95.2%的客观反应率,其中包括66.7%的完全缓解(CR)和28.6%的部分缓解(PR)的比率。
7.其他正在研究、开发和评估用于治疗淋巴瘤的抗体药物偶联物
7.1 针对CD19的抗体药物偶联物
7.1.1 科尔图珠单抗拉伐坦辛
科尔图珠单抗拉伐坦辛(SAR3419)是一种IgG1抗体(huB4),通过二硫键交联剂SPDB与细胞毒素药物DM4相连,靶向CD19。CD19是一种在血液形成分化过程中的B淋巴细胞系高度表达的蛋白,从早期B细胞到成熟B细胞,并在大多数B细胞恶性肿瘤中保持表达。两项II期试验已经研究了科尔图珠单抗拉伐坦辛作为单药或联合用药的使用。一项正在进行的试验正在检查其在R/R DLBCL患者中单药治疗的使用,初步数据显示ORR为44%;然而,mPFS、mOS和DOR尚未得出。它具有可接受的安全性概况,药物在41名患者中有4名因不良事件而中断。另一项试验检查了科尔图珠单抗拉伐坦辛与利妥昔单抗联合用于DLBCL患者,显示出ORR为31.1%,在复发疾病患者中疗效最高(ORR 58.3%),与难治疾病(ORR 43%)或一线治疗(ORR 15.4%)形成对比。总体而言,它显示出mPFS为3.9个月,mOS为9个月,DOR为8.6个月。
7.1.2 德尼珠单抗马佛多汀
德尼珠单抗马佛多汀(SGN-19A或SGN-CD19A)是另一种针对CD19的ADC。它是一种抗体(hBU12-491),通过不可裂解的马来酰亚胺己酰基连接臂与MMAF偶联。一项主要纳入了B-ALL患者(n = 59)的I期试验,以及侵袭性B细胞淋巴瘤(n = 6)和伯基特白血病/淋巴瘤(n = 6),显示DOR为27个月。每3周给药一次,在B-ALL中显示CRc(CR+CRi+CRp)为35%。在六名伯基特白血病/淋巴瘤患者和六名B-LBL患者中,每组只有一名达到CR。最常见的AEs是发热(54%)和恶心(52%)。另一项主要纳入了R/R DLBCL(n = 53),以及MCL(n = 5)和FL(n = 3)的I期试验,与前一次试验相比,在DLBCL中显示出略高的活性,ORR为33%,CR为22%,复发病例的DOR为39周,难治病例为41周。最常见的AEs与眼睛相关:视力模糊(65%)和干眼(52%)。德尼珠单抗马佛多汀在两项II期试验中进一步与化疗联合研究,一项将其与RICE化疗联合用于R/R DLBCL或3B级FL,与单独RICE进行比较,而另一项研究了其与R-CHOP或R-CHP联合对照R-CHOP单独作为DLBCL或3B级FL的一线治疗;然而,这两项试验都被赞助商终止。
7.2 针对CD22的抗体药物偶联物
7.2.1 伊诺珠单抗奥佐加霉素
CD22是一种135 kDa的I型跨膜糖蛋白,是一种在未成熟和成熟B细胞上表达的B细胞系特异性蛋白。它在B细胞恶性肿瘤包括大多数淋巴瘤和白血病中上调表达。目前有两种针对CD22的ADC正在淋巴瘤中进行研究。第一种是伊诺珠单抗奥佐加霉素(CMC-544),一种IgG4 kappa单克隆抗体,带有N-乙酰-γ-卡利奇霉素二甲基肼,一种卡利奇霉素的半合成衍生物,通过4'-乙酰苯氧基丁酸连接,于2017年8月获得FDA批准用于R/R B细胞ALL。一项I期试验研究了其在R/R B细胞NHL患者中的应用,显示79名入组患者的ORR为39%,在FL中为68%,在DLBCL中为15%。然而,DOR很短,DLBCL的mPFS为10.4个月,FL为49天。患者中有90%出现最常见的AE,即血小板减少。一项针对顽固性B细胞NHL(n = 81)的II期试验显示了类似的结果,ORR为67%,CR为31%,mPFS为12.7个月。
7.2.2 匹那珠单抗韦德汀
匹那珠单抗韦德汀(Pina,DCDT2980S,RG-7593)是一种抗CD22的单克隆IgG1抗体,通过可裂解的马来酰亚胺己酰基-缬氨酸-PABC连接臂与MMAF偶联。一项I期试验显示,与利妥昔单抗联合使用相比,作为单药治疗使用时显示出更高的疗效,DLBCL组的ORR分别为25%和17%。在慢性淋巴细胞性白血病(CLL)中未见客观反应。在II期试验ROMULUS中进一步检查了其与利妥昔单抗的联合使用,与R-pola相比,在DLBCL患者中显示出更优越的反应,但在FL患者中没有;DLBCL队列在R-Pina(n = 42)上显示ORR为60%,CR为26%,而R-Pola(n = 39)上为ORR 54%,CR 21%。在这项试验中,两者的AEs相当,R-pina组DLBCL队列的3-5级AEs为79%,R-Pola为77%。在FL队列中,AEs略低,R-Pina和R-Pola的3-4级AEs分别为62%和50%。
7.3 针对CD25的抗体药物偶联物
卡米达卢单抗特西林
CD25是一种I型跨膜蛋白,是白细胞介素-2受体α链,是一种在活化的B细胞、活化和调节性T细胞以及髓系前体上表达的蛋白,在包括淋巴瘤和白血病在内的各种肿瘤中过度表达。卡米达卢单抗特西林(ADCT-301,HuMax-TAC)是一种IgG1单克隆抗体,通过可被卡他蛋白裂解的缬氨酸-丙氨酸二肽连接臂与PBD二聚体弹头(SG3199)偶联。一项I期试验检查了其在R/R cHL(n = 133)和R/R NHL(n = 56)中的疗效,其中在cHL患者中显示出71%的优越ORR和42%的CR,与R/R NHL相比(ORR 38%和CR 9%)。3级及以上AEs包括GGT水平升高(15%)、皮疹(12%)和贫血(11%)。更重要的是,3.8%的患者出现了严重的神经系统事件,包括吉兰-巴雷综合征(GBS)/多神经根病变,27.4%的患者因不良反应而中断治疗。尽管研究报告的CR令人鼓舞,但FDA建议不要提交用于治疗R/R HL的批准文件,因此其未来仍不明朗。
7.4 针对CD37的抗体药物偶联物
纳拉图珠单抗艾美曲辛
CD37是一种参与细胞膜组织和共刺激信号的跨膜蛋白,主要在成熟B细胞上表达,在T细胞、巨噬细胞/单核细胞和粒细胞上表达较少。它在成熟的B细胞恶性肿瘤中高度表达,如CLL,在DLBCL中表达不一,CD37阳性范围从40%到90%的病例,而在急性淋巴细胞性白血病(ALL)和HL中低表达或缺失。纳拉图珠单抗艾美曲辛(IMGN529)是一种IgG1单克隆抗体,通过硫醚连接臂N-succinimidyl-4-(N-maleimidomethyl) cyclohexane-1-carboxylate (SMCC)与美登木素DM1偶联,靶向CD37。
纳拉图珠单抗艾美曲辛最初在R/R B细胞淋巴瘤的I期试验中研究,结果显示最小的效果,总有效率(ORR)为13%。然而,纳拉图珠单抗艾美曲辛与利妥昔单抗联合的II期试验结果显示,在DLBCL中ORR更高,达到44.7%,完全缓解(CR)为31.6%,在FL中的响应率略高,ORR为57%,CR为36%。在中位随访15个月和21.8个月时,DLBCL和FL亚组的中位持续缓解时间(mDOR)尚未达到。治疗总体上被良好耐受,如在FACT-Lym QoL的淋巴瘤子量表上平均提高了三点的生命质量(QoL)测量所示。总体而言,目前尚不清楚它是否会进入III期研究。
7.5 针对CD70的抗体药物偶联物
Vorsetuzumab Mafodotin
CD70是一种共刺激分子,也是肿瘤坏死因子超家族的成员,它在抗原激活的B细胞、T细胞、NK细胞和成熟的树突状细胞上短暂表达。它在实体瘤和血液学恶性肿瘤中异常表达。Vorsetuzumab Mafodotin (SGN-75)是一种ADC,靶向CD70分子和微管毒素分子,连接到单甲基奥瑞斯他汀F(MMAF)。在R/R CD70+ NHL的I期试验中显示出不可接受的毒性,主要是血小板减少症。此外,SGN-CD70A是一种通过稳定、可被蛋白酶裂解的肽基连接臂与PBD二聚体偶联的工程半胱氨酸单克隆抗体(EC-mAb),靶向CD70。同样,它也与不可接受的毒性相关,并且只有适度的活性。
7.6 针对ROR1的抗体药物偶联物
7.6.1. Zilovertamab Vedotin
ROR1是一种酪氨酸激酶跨膜受体,表达在未成熟的B淋巴细胞、内分泌腺和小肠上。它在血液学恶性肿瘤中高度表达,尤其是B细胞淋巴瘤。Zilovertamab Vedotin (MK 2140或VLS-101)是一种针对ROR1的人源化IgG1单克隆抗体,通过可被蛋白酶裂解的连接臂与MMAE偶联。在一项具有里程碑意义的I期试验中,Zilovertamab Vedotin在R/R MCL患者中显示出47%的ORR,CR为20%,在R/R DLBCL患者中ORR为60%。II期waveLINE-004研究,将Zilovertamab Vedotin作为R/R DLBCL的单药治疗,显示出略低的疗效,ORR为30%,有10%的患者实现了CR。最常见的3-4级AEs是中性粒细胞减少症(18%),其次是贫血(15%)。目前有额外的研究正在进行招募;一项是将Zilovertamab Vedotin与R-CHP联合用于DLBCL的前线治疗的II期试验,另一项是评估其与R-GemOX联合对照R-GemOX单独用于R/R DLBCL的II/III期研究。
7.6.2. Cirmtuzumab-ADC-7
另一种针对ROR1的ADC是Cirmtuzumab,一种针对ROR1的单克隆抗体,通过UC-961连接臂与MMAE偶联。在I/II期,Cirmtuzumab与ibrutinib联合用于R/R MCL或治疗未经验(TN)或R/R CLL的管理。在MCL队列中,Cirmtuzumab显示出80%的ORR,35%的患者实现了CR。值得注意的是,在中位随访14.9个月时,mPFS尚未达到。在CLL队列中,结果随着成熟仍然令人鼓舞,TN和R/R CLL患者的mPFS在中位随访14个月和7个月时也未达到。总体而言,该研究正在进行中,结果看起来很有希望。
7.7 临床前开发中的ADCs
7.7.1. 新型CD30靶向ADC:SGN-35C
SGN-35C在组成上与BV相似,都是抗CD30抗体,但在连接臂上有所不同,它连接的是一种新型的喜树碱衍生的拓扑异构酶1抑制剂有效载荷。在CD30阳性ALCL和HL细胞系上进行的体外和体内研究,包括那些对BV有抗性的细胞系,显示出治疗诱导的细胞毒性。值得注意的是,这种效果扩展到了CD30阴性细胞,表明了旁观者效应。非人灵长类动物模型也证实了其安全性。下一步是人类临床试验,目前正在计划中。
7.7.2. CD19靶向ADC:IKS03
IKS03由一种针对CD19的人源化抗体组成,设计用于位点特异性结合PBD前药有效载荷。它通过生物结合激活,产生一种药物与抗体比率为2的偶联物。体外和体内研究已经证明了其在多种CD19阳性淋巴瘤细胞系中的有效细胞毒性,最值得注意的是在含有经常在R/R NHL中观察到的遗传异常的MCL和DLBCL异种移植模型中,如CCND1 t(11;14)易位和三重打击淋巴瘤,涉及BCL-2、BCL-6和c-MYC的基因重排。此外,与其他使用PBD前药的ADC相比,它展示了更低的非特异性有效载荷从偶联物中的释放率,包括LT。目前正在进行I期临床试验NCT05365659,以评估其在晚期B细胞NHL患者中的安全性。
7.7.3. CXCR5靶向ADC:VIP924
VIP924是一种首创的ADC,靶向CXCR5,由一种可被legumain裂解的连接臂和一种微管蛋白抑制剂(KSPi)有效载荷组成。CXCR5是一种趋化因子受体,在B细胞和T细胞来源的淋巴瘤上高度表达,并参与调节肿瘤细胞侵袭、生长和迁移的途径。一项体内研究比较了VIP924与PV和LT在MCL的人性化小鼠模型中的效果。结果表明VIP924在抑制肿瘤生长、提高存活率和耐受性方面的优势。值得注意的是,与LT不同,VIP924组的动物没有经历细胞减少症。这些有希望的结果支持在人类临床试验中进行进一步研究的需求。
8.ADCs的未来发展方向
最近在设计位点特异性ADCs、利用双特异性抗体以及修改可裂解连接臂方面取得了进展,以期使ADCs更有效、更高效,同时最小化毒性。一种新颖的偶联化学方法涉及位点特异性附着,其中一些技术利用抗体中的天然链间二硫键,而其他技术则需要生物工程将酶促偶联标签整合到抗体序列中。尽管在淋巴瘤中尚未探索,但位点特异性偶联已在实体恶性肿瘤(如乳腺癌、卵巢癌和胰腺癌)中得到评估。其中一种应用是ThioMab技术,它涉及使用工程化半胱氨酸进行位点特异性偶联。使用这种技术生产的ADC包括抗MUC16 ADC,它由在曲妥珠单抗的轻链和重链的特定位置插入半胱氨酸残基组成,然后与MMAE上的硫醇基团结合。此外,pClick技术提供位点特异性偶联;然而,它使用天然抗体和近距离激活的交联剂,不涉及任何生物工程。ThioBridge技术包括一种可裂解的连接臂,也使用天然抗体,并由三碳桥接附着提供增强的稳定性。此外,最近创新的AJICAP第二代技术通过利用硫酯化学的选择性裂解反应,实现了无聚集挑战的位点特异性ADC的生产,并有望成为无需抗体工程的位点特异性ADC。最后,通过不同的方法(如糖基重塑、转谷氨酰胺酶或脂酸连接酶方法)对天然抗体进行无标签酶促修饰,作为推进ADC发展的潜在工具具有潜力。
一类有前景的ADCs由双价双特异性抗体组成,如在HER-2靶向ADC中所示。双特异性抗体靶向两个不重叠的表位,随后诱导受体聚集和内化。这类ADCs已在乳腺癌中显示出疗效,并且在临床前研究中检查了MET过表达肿瘤,提供了有效的细胞毒性。
关于连接臂的最新进展,工作集中在制造稳定以避免非目标有效载荷释放的连接臂,但也容易在目标部位裂解以有效传递。这导致制造具有pH和微环境依赖性裂解的连接臂,允许ADCs在细胞内释放有效载荷。
这些进展正处于开发或临床前阶段研究中,有望提高下一代ADCs在包括淋巴瘤在内的各种癌症中的治疗效果。
9.结论
ADCs是革新了霍奇金和非霍奇金淋巴瘤治疗的新方法。抗体、连接臂和有效载荷的进步将导致ADCs的进一步发展,对淋巴瘤具有更高的特异性和细胞毒性。虽然获得抗性将是一个限制因素,但与其他新型药物的联合疗法,如单克隆抗体、分子靶向疗法和双特异性抗体,将为新的突破性治疗铺平道路。我们迫切需要创新的I期研究,以更好地理解ADCs在不同疾病环境中的作用,因为我们的目标是提高淋巴恶性肿瘤的治愈率。
抗体药物偶联物免疫疗法细胞疗法
2023-12-04
产品推荐:ACROBiosystems百普赛斯发布多种高质量、高亲和力的抗Payload抗体,包括抗PBD/ PTX/ MMAE/ DXD/SN38/DM1的抗体,可用于ADC进行临床前及临床阶段的PK检测以及DAR值分析,为提高ADC药物PK分析的准确性和可靠性提供了有力的支持和保障。扫码申请试用装ADC有效载荷在药物疗效中起着关键作用。理想的有效载荷应具有良好的细胞毒性、低免疫原性、高稳定性和可改构的官能团。常见的ADC有效载荷主要包括微管蛋白抑制剂、DNA损伤剂、转录抑制剂等。然而,由于传统有效载荷具有效率有限及耐药性产生等局限性,需要开发具有靶向不同靶标和减少副作用的新型高效有效载荷。本文总结了当前ADC有效载荷研究的进展,为开发高效、低毒性、稳定性强且能克服耐药性的新型ADC有效负荷提供了参考。常见ADC药物使用的细胞毒素载荷第一代ADC细胞毒性不足第一代ADC使用传统化疗药物(如甲氨蝶呤、长春碱和阿霉素)作为细胞毒性有效载荷,但由于第一代ADC对肿瘤细胞的细胞毒性不足、缺乏选择性和低摄取率,其临床效果有限。第二代ADC微管蛋白抑制剂成中流砥柱为了提高疗效,第二代ADC采用了比传统化疗药物效力更强的高细胞毒性化合物作为有效载荷,其中微管蛋白抑制剂成为主要选择。微管蛋白是细胞骨架的主要成分。微管蛋白抑制剂通过破坏微管蛋白,干扰细胞分裂来杀死肿瘤细胞。目前最广泛使用的微管蛋白抑制剂是Auristatin和DM1。01奥瑞他汀(Auristatin)Auristatin中应用最广泛的是MMAE和MMAF。MMAE存在于两种上市药物Adcetris和Polivy中。MMAF与游离微管蛋白的结合亲和力比MMAE增加了近5倍。02艾日布林(Eribulin)以Eribulin为有效载荷的ADC具有较强的“旁观者效应”,临床效果较好。MORAb-202(FRα ADC)使用Eribulin为有效载荷,其在临床试验中展现出良好的耐受性。MORAb-202结构03微管溶素(Tubulysins)Tubulysin能抑制微管蛋白聚合,诱导细胞凋亡。AstraZeneca/MedImmune开发的靶向HER-2两个不同表位的双特异性ADC MEDI4276,其抗体与Tubulysin衍生物AZ13599185通过不可切割的Linker连接,MEDI4276在临床前研究中表现出了良好的抗肿瘤活性。AZ13599185结构04美登素(Maytansinoids)及其衍生物美登素及其衍生物均为强力的微管组装抑制剂,可诱导细胞的有丝分裂停止。DM1和DM4是美登素C-3位被改造的硫代衍生物,是当前常用的美登素类有效载荷。使用DM1的ADC包括已商业化的Kadcyla®及用于治疗卵巢癌的FRα ADC药物Mirvetuximab Soravtansin等。此外,科学家还在尝试将其他类型的微管蛋白抑制剂用于ADC。例如,紫杉醇(Paclitaxel)、长春新碱(Vincristine)和秋水仙碱(Colchicine)的衍生物。紫杉醇已在ADC药物领域进行了一些研究,研究人员使用带有聚乙二醇连接子构建了基于紫杉醇的ADC药物,具有较高的药物负载和良好的水溶性,但距离临床试验还有一段距离。第三代ADC微管蛋白抑制剂对处于分裂期的肿瘤细胞非常有效,但对静态癌细胞的效果有限。因此,第三代ADC使用能够靶向整个细胞周期的DNA损伤剂作为有效载荷,通过双链断裂、烷基化、嵌合和交联来破坏DNA结构,杀死肿瘤细胞。DNA损伤剂因机制不同分为DNA双链破坏剂、DNA插入剂和DNA烷基化剂。具有代表性的包括拓扑异构酶抑制剂(DNA插入剂)和吡咯苯二氮卓类药物(PBD)。01拓扑异构酶Ӏ抑制剂DNA拓扑异构酶Ӏ抑制剂是目前最具前景的有效荷载之一,可裂解单链DNA、抑制拓扑异构酶修复机制,使得DNA损伤,细胞凋亡。分为喜树碱和非喜树碱类。目前已用于商业化ADC药物有效载荷的喜树碱类拓扑异构酶 I 抑制剂包括DXd和SN-38。ADC药物常用有效载荷的作用浓度范围比较❖ DXd为依喜替康衍生物,可克服p-糖蛋白介导的耐药。DXd与GGFG连接子组成德鲁替康(deruxtecan)连接子-载荷被用于多个ADC设计,例如DAR为8的Enhertu®、U3-1402和DS-6157a,以及DAR为4的DS-1062a和DS-7300a。❖ SN-38是伊立替康(Irinotecan)的活性形式,是一种半合成的喜树碱。被FDA批准用于治疗TNBC和转移性尿路上皮癌的抗TROP-2 ADC Trodelvy®即使用SN-38为有效载荷。其他基于SN-38的ADC还包括靶向CEACAM5的IMMU-130(Labetuzumab govitecan)和靶向HLA-DR的IMMU-140等。02吡咯并苯二氮杂䓬(PBD)PBD是一种序列特异性的DNA烷化剂,PBD二聚体通过与DNA小沟相结合,形成有效的细胞毒性DNA链间交联,导致细胞凋亡,表现出强大的细胞毒性作用。以PBD为有效载荷设计的ADC如靶向ROR1的CS5001,其在多种血液和实体瘤异种移植物小鼠模型中显示出显著的体内抗肿瘤活性。拓扑异构酶Ⅱ抑制剂等其他DNA抑制剂也被应用于ADC领域。例如,蒽环类药物PNU-159682被用NBE-002(ROR1 ADC)的有效载荷。目前ADC药物仍不断更新迭代,其他各类作用机制的毒素也被逐步应用于ADC药物开发中,包括RNA抑制剂、Bcl-xL抑制剂、NAMPT抑制剂和蛋白酶体抑制剂卡霉素等。有效载荷的体外和体内药代动力学研究考量有效载荷(payload)的多样性是ADC药物未来开发的关键一环。表征生物药物是整个药物从开发到临床评估过程的关键步骤。ADC结构复杂多样,偶联小分子药物导致ADC异质性增加。结合《抗体偶联药物非临床研究技术指导原则(征求意见稿)》,需要对ADC进行深入的表征分析,揭示其药代动力学/药效学特征,以确保药物的安全性。影响ADC质量的一个重要属性是DAR值和载药量分布,因此是PK方法开发的重点。为了解决ADC药物PK分析中的挑战和难点,ACROBiosystems百普赛斯发布多种高质量、高亲和力的抗Payload抗体,包括抗PBD/ PTX/ MMAE/ DXD/SN38/DM1的抗体,可用于ADC进行临床前及临床阶段的PK检测以及DAR值分析,为提高ADC药物PK分析的准确性和可靠性提供了有力的支持和保障。产品特点✔ 高纯度:纯度经SDS-PAGE及SEC-MALS验证>95%;✔ 高灵敏度:经ADC药物结合验证;✔ 高特异性:可特异性识别小分子毒素;✔ 售后完善:提供完善的售后技术支持满足客户的技术指导需求。产品列表验证数据● 高纯度经SEC-MALS验证The purity of Monoclonal Anti-SN38 Antibody (Cat. No. SN8-S223) is more than 95% and the molecular weight of this protein is around 135-160 kDa verified by SEC-MALS.● 抗PTX抗高亲和力经PTX-ADC验证Immobilized ADC-PTX at 1 μg/mL (100 μL/well) can bind Mouse Anti-PTX Antibody, Mouse IgG2a (MALS verified) (Cat. No. PTX-S343) with a linear range of 0.106-6.767 ng/mL (QC tested).● 抗MMAE&MMAF抗体高亲和力结合MMAE ADCImmobilized Disitamab Vedotin (RC48) at 0.2 μg/mL (100 μL/well) can bind Mouse Anti-MMAE&MMAF Antibody, Mouse IgG1 (Cat. No. MME-M5252) with a linear range of 0.1-2 ng/mL (QC tested).● 抗MMAE&MMAF抗体高亲和力结合MMAF ADCImmobilized ADC-MMAF at 2 μg/mL (100 μL/well) can bind Mouse Anti-MMAE&MMAF Antibody, Mouse IgG1 (Cat. No.MME-M5252) with a linear range of 0.5-1.56 ng/mL (Routinely tested).● 抗SN38抗体高亲和力结合SN38-ADCImmobilized ADC-SN38 at 2 μg/mL (100 μL/well) can bind Monoclonal Anti-SN38 Antibody (Cat. No. SN8-S223) with a linear range of 0.05-1.56 ng/mL (QC tested).ACROBiosystemsinquiry@acrobiosystems.com15117918562(备注:姓名+公司)
抗体药物偶联物
2023-02-13
ADC药物已成为治疗越来越多癌症适应症的重要组成部分。目前已有十几种ADC药物获批上市,数百项临床试验正在进行中,以探索新的靶点和适应症。ADC领域取得的巨大进步主要得益于为特定靶标量身定做的设计。这要归功于几项成就,包括:(1)探索和验证越来越多的靶标;(2)筛选专用于ADC的抗体,重点是交叉反应,利用pH变化有助于与肿瘤的优先结合,促进内吞和FcRn循环;(3)偶联技术的改进,药物与抗体的比更高;(4)有效载荷的多样化(图1)。图1. 微管和DNA烷化剂以外的ADC有效载荷示意图多年来,微管抑制剂和DNA烷化剂一直占据ADC 有效载荷的主导地位。这些有效载荷已使得8个ADC药物获得批准。然而,最近两种基于拓扑异构酶1抑制剂的ADC药物--trastuzumab deruxtecan (Enhertu®)和saituzumab govitecan(Trodelvy®)的批准和临床成功显示了具有不同的作用机制的非传统有效载荷的潜力。这得益于ADC结构的重大突破,通过改进的连接子设计以允许更高的DAR值、更稳定的有效载荷附着和增强的旁观者杀伤活性。在ADC领域的未来发展中,有效载荷多样化有望发挥关键作用,越来越多的处于临床前和临床阶段非传统有效载荷偶联的ADC就是例证。本文就具有不同作用机制的新开发的、有效的、进入临床阶段的非传统有效载荷做一个简要介绍。成功的有效载荷家族:拓扑异构酶1抑制剂拓扑异构酶1抑制剂是FDA批准的最新的抗体-药物结合有效载荷家族,最先批准的是trastuzumab deruxtecan,紧接着是sacituzumab govitecan 。拓扑异构酶位于细胞核内。它们的作用是控制和修复在DNA打开、上游转录和复制过程中发生的DNA超螺旋和缠绕。拓扑异构酶分为两个家族:拓扑异构酶I裂解单链DNA,拓扑异构酶II裂解双链DNA。拓扑异构酶抑制剂特异性地结合到DNA-拓扑异构酶复合体的界面上,从而抑制拓扑异构酶修复机制,导致DNA损伤,从而导致细胞凋亡。然而,最有效的拓扑异构酶抑制剂的效力比微管抑制剂maytansines或DNA烷化剂calicheamicin低100到1000倍,这解释了为什么在最初的ADC设计中对这种有效载荷类别缺乏兴趣。该有效载荷类别包括基于喜树碱和非喜树碱的化合物。喜树碱(CPT)是一种由五个化学环组成的天然植物生物碱,不易溶于水。几种具有更好生物利用度的衍生物已获得监管当局的批准,如topotecan, irinotecan 和 belotecan。这些药物已经被批准用于几种适应症,包括卵巢癌、肺癌、宫颈癌和结肠癌。Irinotecan的脂质体制剂也已被批准用于治疗晚期胰腺癌。其他几种CPT衍生物也已被合成,例如gimatecan,目前正处于治疗卵巢癌、输卵管癌或腹膜癌的II期评估(NCT04846842)。基于CPT的分子最显著的严重不良事件包括严重水样腹泻、中性粒细胞减少和血小板减少。CPT衍生物最近被用作ADC有效载荷,因为它们具有中等的细胞毒性效力,IC50值在纳摩尔范围内。它们的效力介于非常有效的抗微管/DNA靶向药物(皮摩尔IC50)和传统化疗药物(微摩尔IC50)之间,后者最初用于最初的ADC,但因缺乏疗效而失败(甲氨蝶呤和阿霉素)。到目前为止,已有两个CPT衍生物成功地与抗体偶联并获得批准:DXd和irinotecan的活性代谢物SN-38。Exatecan及其衍生物与CPT相比,exatecan具有更高的活性和更好的溶解性,并且不是ABCC2或ABCG1底物。未偶联的exatecan在几个临床试验中进行了评估,但其糟糕的治疗窗口,具有剂量限制性的中性粒细胞减少和血小板减少以及强烈的胃肠道毒性限制了其应用。在初步尝试中,exatecan与抗体的生物偶联取得了部分成功,但偶联物显著聚集。Daiichi Sankyo的科学家通过使用一种名为DXd的exatecan的略微修改的乙醇酸衍生物解决了这个问题。结果发现,这种新化合物保留了exatecan的效力,同时使每个抗体成功地偶联了多达8个DXd分子,而且没有明显的聚集。这种deruxtecan 药物-连接子已被用于多个的ADC药物(图2),例如DAR8的DS-8201a(Enhertu®)、U3-1402和DS-6157a,以及在DAR的DS-1062a和DS-7300a,以限制它们的毒性。这些ADC药物中,DS-8201a因为卓越疗效已得到FDA的批准上市,其他的还正在进行临床评估。虽然DXd有效载荷表现出比exatecan甲磺酸盐更低的被动膜渗透性,但它的骨髓毒性较小,因此也因其改善的安全性而被选中。图2. 基于deruxtecan 药物-连接子的ADC药物最近,exatecan已被作为潜在的ADC有效载荷进行临床前探索,这要归功于亲水性可切割连接子的开发,这些结构能够绕过化合物的疏水和聚集特性。这使得exatecan可以在较高的DAR值下偶联,而不会干扰ADC的药代动力学特性。这些ADC在肿瘤移植瘤中表现出很强的抗肿瘤活性,与deruxtecan为基础的ADC相比,其表现出更强的旁观者杀伤效应,这要归功于与DXd相比,exatecan的被动细胞渗透性改善。使用这种药物-连接子的策略已开发了两种ADC药物:PRO1184和PRO1160 , DAR均为8。最近的体内研究也表明,exatecan不需要氟环功能来发挥其抗肿瘤活性,从而扩大了分子的官能化以产生可连接的衍生物。使用这种策略开发的最有前途的ADC(mAbE21a,derivative 11, DAR7.5)在EGFR+模型中显示出优异的抗肿瘤活性,在0.25 mg/kg时即可完全缓解。一种新的特有exatecan衍生物AZ’0132最近被披露,目前已作为ADC 药物AZD8205的有效载荷进行I/II期临床研究(NCT05123482),靶标是B7-H4(图3)。图3. AZD8205结构示意图IrinotecanIrinotecan已被FDA批准用于治疗各种实体肿瘤,如胃肠道恶性肿瘤、胶质母细胞瘤和宫颈癌,是拓扑异构酶1抑制剂SN-38的前体药物。SN-38不溶于水,会导致严重的毒性,包括强烈的骨髓抑制和重度腹泻。因此,开发Irinotecan是为了提高生物利用度并获得可接受的治疗指数。IMMU-132(Trodelvy®)是一种TROP2抗体与基于SN-38的药物连接子相偶联的ADC药物。该ADC已于2020年被FDA批准用于治疗三阴性转移性乳腺癌和转移性尿路上皮癌,目前正在进行治疗HR+/HER2-、前列腺癌和子宫内膜癌的临床试验(NCT03725761和NCT04251416)。使用这种基于SN-38的连接子也已经开发了其他ADC药物,包括分别以CEACAM5和HLA-DR为靶点的IMMU-130和IMMU-140(图4)。图4. 基于SN-38的代表ADC药物结构示意图最近,A7R-SN-38 ADC已被开发用于治疗自身免疫性疾病,以避免类固醇耐药性。Belotecan 衍生物另一种拓扑异构酶1抑制剂KL610023是FDA批准的Belotecan分子的衍生物,正在作为ADC有效载荷进行研究。基于这种拓扑异构酶I抑制剂开发了抗TROP2 ADC药物SKB-264,DAR为7.4(图5)。目前正处于I/II期临床试验(NCT04152499)中,用于治疗各种实体肿瘤患者。图5.SKB264结构示意图其他拓扑异构酶1抑制剂以喜树碱为基础的衍生物作为ADC有效载荷的限制之一是分子中缺乏可连接的化学胺基团。已经合成了其他CPT衍生物,以在不改变其抗肿瘤特性的情况下在有效载荷内插入可连接的功能团。在这些衍生物中,cAC10是一种CD30抗体与8个AMDCPT分子连接的ADC药物,临床前研究显示出优异的效果有希望的结果。最近已经开发了几个非CPT衍生物,包括吲哚异喹啉,二苯并萘酮和氟吲哚异喹啉(图6)。与CPT衍生物相比,这些分子表现出几个优点,包括更高的细胞毒性、更好的稳定性或更长的活性,目前正处于早期临床试验阶段。图6. 下一代拓扑异构酶I抑制剂作为ADC的潜在有效载荷已进入临床试验的其他有效载荷:希望与挑战并存虽然拓扑异构酶1抑制剂已经深刻地改变了ADC的有效载荷格局,但其他一些有效载荷已经在临床试验中进行了评估,主要包括拓扑异构酶2抑制剂、RNA聚合酶抑制剂、Bcl-xL抑制剂和免疫刺激剂。拓扑异构酶2抑制剂拓扑异构酶2抑制剂广泛应用于血液系统恶性肿瘤和实体瘤的抗癌治疗。它们的作用机制复杂,不仅可能直接抑制拓扑异构酶2的活性,还可能涉及DNA嵌入、ROS诱导和线粒体破坏。它们的毒性包括骨髓抑制、胃肠道毒性,在某些情况下还会出现严重的心脏毒性。目前已有多种拓扑异构酶2抑制剂ADC药物进入临床阶段(图7)。第一个含有拓扑异构酶2抑制剂的ADC 药物SGN-15(BMS-182248)是由阿霉素偶联到小鼠BR-96抗体上,靶向Le-Y抗原。其I期临床试验显示出可接受的耐受性,但II期由于连接子的不稳定和Le-Y靶标在正常组织中的表达而导致靶外毒性而终止。阿霉素后来被连接到CD74靶向抗体Milatuzumab(IMMU-110)上,用于治疗多发性骨髓瘤。但疗临床效令人失望,于2013年停止(NCT01101594)。图7. 拓扑异构酶2抑制剂示意图考虑到阿霉素作为ADC有效载荷的局限性,后来又开发了另一种细胞毒性比阿霉素高100倍的蒽环类药物PNU-159682。除了比其他拓扑异构酶2抑制剂更有效之外,PNU-159682也不是外排底物。2020年,一种基于PNU-159682的新型ADC 药物NBE-002,靶向ROR1,进入了I/II期临床试验(NCT04441099)。另外,NBE-002还诱导了长期的免疫保护,这使得它可以成功地与免疫检查点抑制剂组合治疗。SOT102是另一款基于PNU-159682的ADC药物,靶标是CLDN18.2。SOT102在低表达肿瘤中显示出很大的治疗窗口,并已于2022年4月进入I期临床试验。转录抑制物转录在细胞发育、活性和增殖中起着重要作用,因此可以构成ADC有效载荷的创新和原始靶点。转录由直接与DNA结合的RNA聚合酶II(RNApolII)调控,涉及与RNApolII形成复合体启动转录(如TFIIH)的转录因子和调节染色质结构和可及性的辅助调节因子(如组蛋白脱乙酰酶,HDAC)。虽然一些HDAC抑制剂已获得批准,但由于RNApolII抑制剂耐受性较差,目前还没有批准。Amanitin是一种天然的、高效的RNApolII抑制剂,来源于鹅膏菌。α-Amanitin和β-Amanitin与其他七个大环衍生物一起构成鹅膏毒素家族。尽管它们被广泛用作实验室试剂来探索转录机制,但事实证明,α-Amanitin毒性太大,特别是对肝脏,不能作为抗癌剂进一步开发。然而,这种分子作为一种潜在的ADC有效载荷呈现出许多优点,包括细胞内靶点、良好的物理化学性质(包括亲水性)、它对外排泵的不敏感性,以及它在静止的癌细胞中产生细胞毒性的能力。β-Amanitin于1973年首次与白蛋白偶联,显示出对巨噬细胞的选择性杀伤。该衍生物后来与抗MUC1和抗PSMA抗体偶联,并在临床前模型中显示出强烈的选择性细胞毒性。2021年5月,首个Amanitin抗体偶联物(ATAC®) HDP-101进入早期临床试验(图8)。HDP-101是一种针对BCMA的ADC,目前正在多发性骨髓瘤和浆细胞疾病患者中进行评估(NCT04879043)。ATAC最近被发现可以是一种免疫激活药物,它们被发现可以诱导免疫原性细胞死亡(ICD),并与ICI表现出协同作用,这为临床环境中联合应用的可能性开辟了新的视野。许多针对其他靶点(EpCAM、HER2、PSMA、CD19)的α-Amanitin ADC在体外和体内也都已显示出强大的抗肿瘤活性。图8. HDP-101结构示意图其他高效的RNApolII抑制剂在20世纪90年代已被偶联应用,如鬼臼毒素,霉菌毒素毛霉烯、疣草素A和大蒜素A。这些化合物在各种细胞系中具有纳摩尔细胞毒性,有望是未来几年进一步研究的对象。另一种阻止DNA转录的策略是抑制转录因子(TFs)。TF对于RNApolII在起始步骤中与DNA的连接至关重要。TF抑制剂(TFi)已经在水溶性前药minnelide的临床试验中证明了其抗肿瘤活性,目前处于II期评估(NCT04896073)。雷公藤甲素是一种来源于中草药“雷神藤”的天然化合物,具有很高的细胞毒性,但也是疏水性的,生物利用度低,毒性高。因此,正在努力开发具有更好药物化学性质的类似物。另一种策略是将这种分子与靶向实体偶联,从而绕过这些问题。雷公藤甲素最近首次与CD26抗体偶联靶向间皮瘤和淋巴瘤,这种不可切割的ADC有效地阻止了靶细胞中mRNA的合成,并表现出优异的体外和体内抗肿瘤活性。HDACs(组蛋白脱乙酰酶)影响转录因子,因此参与包括转录在内的各种细胞过程。已发现它们在癌细胞中过度表达或过度活化,并被认为与增殖、迁移和侵袭的增加有关。Vorinostat和dacinostat是FDA批准的HDAC抑制剂(HDACi)的两个例子。然而,这些分子存在很大的全身副作用风险,如血小板减少症和胃肠道毒性,以及较差的PK特性。自2018年以来,它们一直在ADC设计中进行研究:ST74612AA1是第一个生物偶联HDAC抑制剂。这种相对无毒的分子是第二代pan-HDACi。这种分子已与西妥昔单抗和曲妥珠单抗成功偶联,产生的两种ADC都比未偶联的HDACi更安全,同时在CDX和PDX模型中均具有活性。2020年,vorinostat和dacinostat也与西妥昔单抗和曲妥珠单抗偶联,并在体外显示抗肿瘤活性。Bcl-xL抑制剂Bcl-2家族成员可以是pro (Bad,Bim,PUMA,Bik,Bak,Bax)或抗凋亡蛋白(Bcl-2、Bcl-xL、Bcl-w、Mcl-1)。在癌细胞中,这些蛋白质之间的平衡更通常倾向于存活,使得抗凋亡蛋白质成为创新ADC有效载荷的靶标。Bcl-xL和Bcl-2抑制剂根据其化学功能分为4大类:N-酰基磺酰胺类(navitoclax,venetoclax),吲哚类(obatoclax),醋酸棉酚(AT-101,sabutoclax)和苯并噻唑腙类(如WEHI-539)。Bcl-xL的抑制与严重的血小板减少症有关,证明了寻找高度特异性的Bcl-2抑制剂如venetoclax的必要性。目前,venetoclax被批准用于慢性淋巴细胞性白血病和急性髓细胞性白血病患者。ABBV-155 (mirzotamab clezutoclax)是B7-H3抗体与Bcl-xL抑制剂clezutoclax偶联的创新ADC药物,其在2018年进入了I/II期临床试验,用于治疗晚期非小细胞肺癌和乳腺癌患者的晚期实体肿瘤(NCT03595059)。单药I期队列中的前31名患者中未报告剂量限制性毒性,严重副作用包括贫血、淋巴细胞数减少、疲劳和腹泻。21%的患者在紫杉醇联合治疗组中观察到部分反应。激酶抑制剂人类基因组包含超过500种激酶,其中超过150种与包括癌症在内的各种疾病相关。蛋白激酶是催化磷酸化的酶,分为3类:丝氨酸、苏氨酸或酪氨酸激酶。在癌症中,多种激酶家族参与细胞周期进程、细胞增殖、运动和血管生成。虽然蛋白激酶抑制剂在癌症治疗方面得到了广泛研究,但作为ADC的有效载荷尚未得到广泛研究,可能是因为它们的效力较低。抗CD19抗体B43已经与木黄酮偶联,发现木黄酮可通过抑制酪氨酸激酶受体表皮生长因子受体(EGFR)从而诱导细胞凋亡和细胞增殖抑制。体外和体内临床前研究表明,累积剂量为100 mg/kg时无毒性,且在小鼠模型中比标准化疗具有更强的抗肿瘤效果。这些有优异的结果使得其在1999年对ALL和NHL患者进行了临床研究。其在人体内呈现良好的药代动力学特征外,没有毒性,且有优异的抗肿瘤活性。然而,这种ADC药物的进展还没有进一步的报告(NCT00004858)。最近,其他激酶抑制剂作为ADC有效载荷也进行了评估。包括neolymphostin (一种PIKK抑制剂),以及dasatinib 和staurosporine(多激酶抑制剂)。但总体而言,ADC形式的酪氨酸激酶抑制剂的疗效目前被发现是有限的,该家族很难在晚期患者中获得成功。免疫刺激抗体偶联物针对适应性免疫系统的免疫检查点抑制剂的成功极大地刺激了研究人员利用先天免疫系统刺激的抗肿瘤研究。然而,最有效的药物如STING和TLR激动剂的全身给药与严重的全身毒性有关,这是由细胞因子释放综合征引起的,从而将当前的研究限制在肿瘤内注射。因此,它们与抗体的结合似乎是一种在改善耐受性的同时开发其强大的抗肿瘤潜力的有希望的手段。免疫刺激抗体偶联物代表了一种新的抗体-药物偶联物,目前有两个ADC已进行临床试验 (NJH395,BDC1001),另外一个SBT6050其临床评估因战略决定而终止 (图9)。图9. 免疫刺激抗体偶联物结构示意图小编小结有效载荷是ADC的重要组成部分,在ADC领域的未来发展中,有效载荷多样化将发挥关键作用,其有望将ADC的治疗武器库开放给其他尚未受益于靶向治疗的癌症。开发这些新型有效载荷的一个关键问题是减轻它们的副作用。目前批准的ADC已表明,它们具有预期的(骨髓抑制、神经毒性)或意想不到的(如眼或肺)毒性。因此,获得令人满意的治疗指数将是创新ADC有效载荷未来发展的关键。参考文献1.Payload diversification: a key step in the development of antibody–drug conjugates.2.Strategies and challenges for the next generation of antibody-drug conjugates.
抗体药物偶联物上市批准引进/卖出临床结果多肽偶联药物
分析
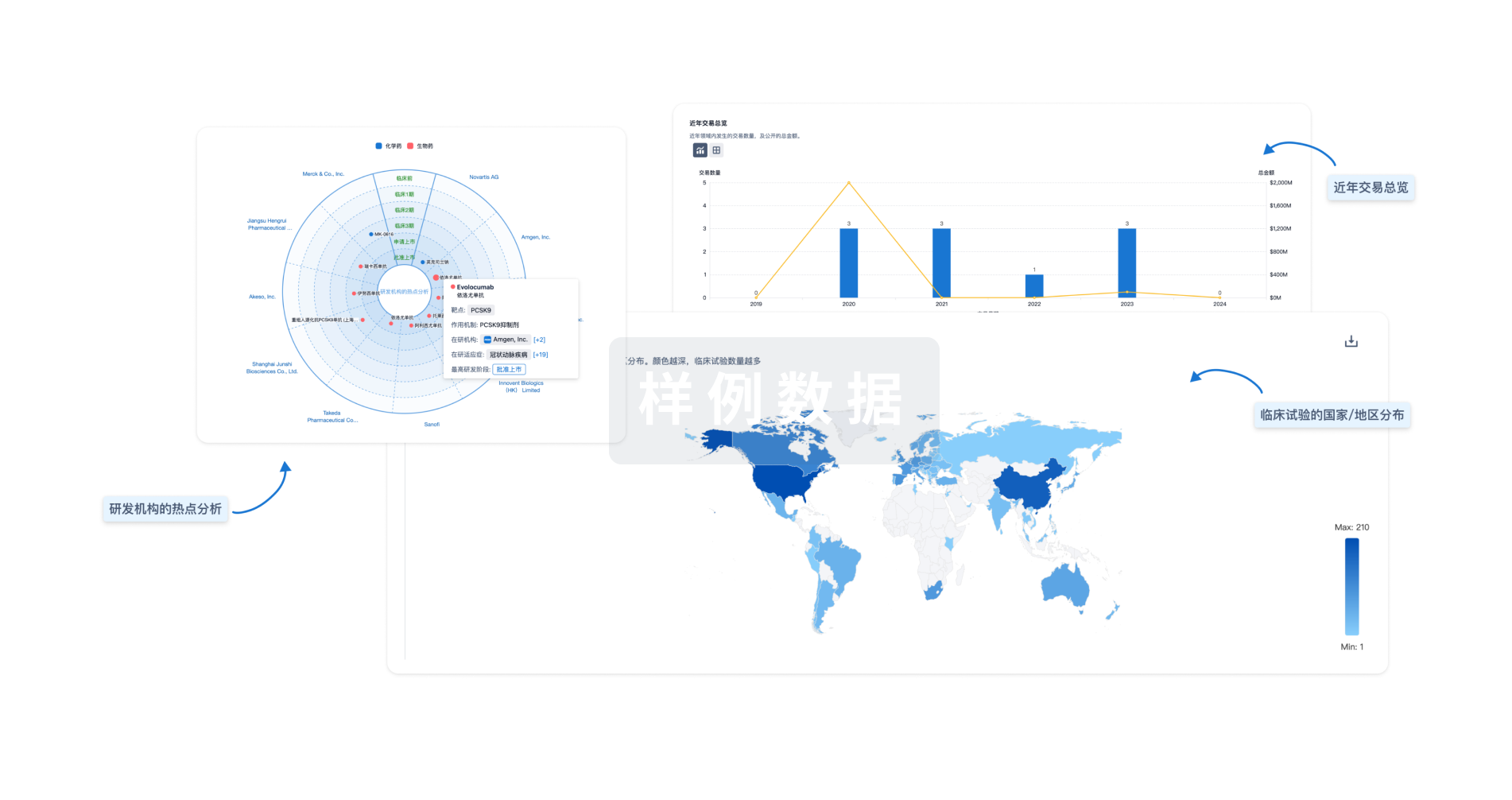
对领域进行一次全面的分析。
登录
或
来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用