预约演示
更新于:2025-01-23
Xinyao Biology (Shanghai) Co., Ltd.
私营公司|
2021|
中国上海市
私营公司|
2021|
中国上海市
更新于:2025-01-23
概览
关联
2
项与 Xinyao Biology (Shanghai) Co., Ltd. 相关的临床试验NCT06026748
A Phase I Study to Evaluate the Safety, Tolerability, Pharmacokinetics and Immunogenicity of XJ103 in Chinese Healthy Subjects
This is a randomized, double-blind, placebo-parallel intervention clinical study that will include approximately 38 healthy subjects based on inclusion and exclusion criteria. Subjects will be assigned to one of four different dosage cohorts. Subjects in each cohort will randomly be given experimental drug or a placebo.
开始日期2023-09-12 |
NCT06014736
A Phase I Study to Evaluate the Safety, Tolerability, Pharmacokinetics and Immunogenicity of XJ101 in Chinese Healthy Subjects
This is a randomized, double-blind, placebo-parallel intervention clinical study that will include approximately 38 healthy subjects based on inclusion and exclusion criteria. Subjects will be assigned to one of four different dosage cohorts. Subjects in each cohort will randomly be given experimental drug or a placebo.
开始日期2023-08-15 |
100 项与 Xinyao Biology (Shanghai) Co., Ltd. 相关的临床结果
登录后查看更多信息
0 项与 Xinyao Biology (Shanghai) Co., Ltd. 相关的专利(医药)
登录后查看更多信息
2
项与 Xinyao Biology (Shanghai) Co., Ltd. 相关的新闻(医药)2024-04-09
·药研网
PD-1/PD-L1作用于人体免疫系统,被认为是抗肿瘤治疗的“杀手锏”,更被誉为广谱抗癌药,也是药企之间竞争最为激烈的市场之一。国内多家企业均有所布局。今年的AACR,与PD-(L)1相关的单/双/三抗、ADC产品可谓百花齐放。AACR会议期间,至少有13家中国Biotech公司带来了PD-(L)1相关成果展示,其中4款单/双抗产品已上市,4款PD-(L)1在研单抗、双/三抗组合产品,5款处于临床前PD-(L)1双抗、ADC产品,足以证明该赛道竞争的火热态势。2024年AACR展示的国产PD-(L)1药物01PD-(L)1药物市场规模弗若斯特沙利文报告指出,全球PD-1/PD-L1单抗市场预计于2025年达到626亿美元。其中,中国PD-1/PD-L1市场规模预计将于2025年达到519亿元。巨大的市场下,国内多家企业均有所布局。据 Insight 数据库显示,在国内已获批上市以及处于申报上市阶段的 PD-(L)1 单抗高达22款,目前临床试验多以拓展适应症或者联合用药为主,涉及企业超百家,处在III期临床阶段的管线也超百条。近期各家企业年报披露的国内PD-1业绩排名浮出水面。从已上市产品销售额来看,百济神州以38亿销售额遥遥领先,复宏汉霖作为后起之秀,在2023年实现了11亿元的销售额,并成功反超君实生物的特瑞普利单抗,成为国产PD-1领域的一匹黑马。毫无疑问,在产品的竞争上,PD-1/L1依旧是药企之间竞争最为激烈的市场之一。2023国内PD-1销售额排名|来源财经网医药吉满生物为了满足广大用户需求,可以提供PD-1/PD-L1稳定过表达细胞系、报告基因检测细胞系、抗体和蛋白现货产品;旨在加快药物研发进程,助力临床申报。具体咨询吉满客服电话(同微信):18916119826。02PD-(L)1双抗荣昌生物在AACR上展示的是自研PD-1/VEGF双抗RC148,RC148为荣昌生物首款双抗新药。去年8月29日,荣昌生物在Clinicaltrials.gov网站上注册了RC148的一期临床试验。RC148是一种新型的人源化IgG1沉默双特异性抗体,靶向VEGF和PD-1。在临床前研究中,RC148阻断VEGF与VEGFR和PD-1与PD-L1的结合,阻止人脐静脉内皮细胞的生长和迁移,实现有效的T细胞活化,在啮齿动物模型中表现出协同抗肿瘤作用,并在非人灵长类动物研究中显示出安全性。开拓药业一项临床前研究PD-1/ALK-1双特异性抗体Nivo813也在此次AACR大会入选。临床前数据表明,Nivo813是一种双阻断抗PD-1/ALK-1双特异性抗体,同时显示出与细胞表面PD-1和ALK-1的结合效力,在体外表现出剂量依赖性的抗血管生成和强大的抗肿瘤疗效,支持其治疗人类癌症的临床潜力。目前国内PD-1/VEGF双抗赛道已打的火热。康方生物AK112为全球首款PD-1/VEGF双抗,并与Summit达成50亿美元合作开发协议,首付款即高达5亿美元。此外,君实生物也申报了PD-1/VEGF双抗,荣昌生物、开拓药业的加入无疑为此靶点双抗的竞争又加了一把火。03PD-(L)1三抗嘉和生物的GB268,宏成药业的HC010,这两款均为PD-1/CTLA-4/VEGF三抗。此外还有烁星生物带来的PD-L1/EGFR/CD28三抗SM2275。嘉和生物的GB268是同类首创的抗PD-1/CTLA-4/VEGF三特异性抗体,设计创新。临床前数据表明,GB268在引发抗肿瘤反应方面非常有效。同时,免疫相关的不良事件得到缓解。上海宏成药业自主研发的1类生物制品创新药注射用HC010是一款针对晚期实体瘤的注射用冻干制剂,靶向人PD-1、CTLA-4和VEGF的三特异性抗体,属于全球首创。其设计目的是用于阻断PD-1与其配体PD-L1/L2、CTLA-4与其配体CD80/CD86以及VEGF与其受体VEGFR2之间的相互作用,同时抑制两个免疫检查点和血管新生,从而促进抗肿瘤免疫和血管正常化。该项目已于2023年12月正式获国家药监局批准开展临床试验。结合临床前疗效和安全性数据,HC010在治疗抗PD-1抗体耐药NSCLC患者方面显示出潜在的益处。烁星生物的SM2275是使用 StarMab 专有的 Quadbody 多功能 VHH 抗体平台开发的。M2275是一种新型双 EGFR 和 PD-L1 靶向、条件性 CD28 激动抗体。它通过独特的作用机制在临床前研究中验证了良好功效和安全性。值得一提的是,烁星生物成立于2019年,是一家以创新为驱动力的生物制药公司,利用自创的纳米多抗生物药平台技术,开发创新的纳米抗体药物。04PD-(L)1ADC药物与非特异性小分子细胞毒性药物相比,ADC显示出更好的疗效和靶点选择性。康源久远是全球唯一一家开发基于PEG的双抗ADC的公司,其利用聚乙二醇双抗ADC(P-BsADC)技术平台开发的CD47/PD-L1双抗ADC JY207在AACR上展示最新研究成果。研究表明,JY207在体外和体内均具有良好的抗肿瘤作用,其作用机制已得到充分认识。这些发现为JY207作为CD47/PD-L1双阳性癌症患者的临床疗效提供了证据。05结语进入「后 PD-(L)1 时代」,各大药企为了延续 PD-(L)1 单抗的生命周期,或拓展差异化适应症,或探索联合疗法。无论PD-(L)1 单抗还是ADC,单药治疗难免力所不及,而PD-(L)1联合用药能发挥出「1+1>2」的疗效。AACR上的”百花齐放”的国产PD-(L)1组合药物预示着一个崭新时代来临了。细胞系产品查询投稿丨商务合作转载丨加交流群往期推荐视角 | 纸面之外的药明康德2023年报Claudin18.2ADC赛道群雄逐鹿:3家率先进入III期临床下一个10亿美元重磅炸弹选手"裁员潮”仍在加剧:2月多家药企裁员点击下方“药研网”,关注更多精彩内容
AACR会议临床3期临床结果临床1期抗体药物偶联物
2023-06-28
·药创客
近日,星济生物(苏州)有限公司(简称“星济生物”或“Starmab”)宣布,公司自主研发的1.1类单克隆抗体新药---XJ103注射液的新药临床试验申请(IND)获得国家药品监督管理局(NMPA)批准。XJ103注射液为重组抗肺炎链球菌人源化单克隆抗体,临床拟用于重症肺炎链球菌感染治疗及高危人群的预防。肺炎链球菌(Streptococcus pneumoniae,Spn)广泛定植在人类鼻咽部,当机体免疫功能下降时能够穿透黏膜形成各种类型的感染(包括菌血症性肺炎、脑膜炎等重症感染及其导致的脓毒症),其中儿童和老年人是肺炎链球菌感染的高危人群。肺炎链球感染是全球最严重的公共卫生问题之一,呈现高发病率和死亡率。据报道全球每年有370万例5岁以下儿童患肺炎链球菌感染,导致约30万例死亡,平均每2分钟就有一个儿童死于肺炎链球菌感染。我国每年5岁以下儿童肺炎球菌感染例数位列全球第二。随着抗菌药物的长期使用,肺炎链球菌的耐药性日益严重,世界卫生组织将耐药肺炎链球菌定义为急需开发新型药物的病原体。近年来,非疫苗血清型肺炎链球菌感染流行也呈现上升趋势,尤其是在免疫功能低下人群中发生的感染显著升高。所以,目前的小分子抗菌药物和疫苗均不能完全解决肺炎链球菌性疾病高发病率、高死亡率的临床问题,临床上急需更加有效的药物用于预防和治疗严重的肺炎链球菌感染。XJ103注射液是星济生物自主研发的全球首款肺炎链球菌中和抗体药物。临床前研究表明:XJ103注射液体外具有较强的肺炎链球菌中和活性,对肺炎链球菌感染动物模型具有显著的药效学作用;食蟹猴体内的毒理学试验证明XJ103注射液具有很好的安全性。星济生物期望XJ103注射液早日在患者体内确证临床疗效,为重症肺炎链球菌感染的治疗和预防提供创新疗法,并将于近期启动I期临床试验研究,在人体内评价XJ103注射液的安全、耐受性及药代动力学。关于星济生物:星济生物(苏州)有限公司于2020年6月由复星医药旗下复健新药基金、重庆药友制药携手安毛毛博士及李博华博士共同投资创建。是一家专注于抗感染大分子药物(抗体药物、长效融合蛋白药物等)研究与开发的公司,产品线布局涉及细菌、真菌和病毒等多种病原体,产品适应症主要聚焦医院内超级耐药菌感染和严重危害公共安全的病毒和真菌感染,解决现有小分子抗感染药物所不能解决的临床问题,为严重威胁人类生命的感染性疾病提供创新疗法。识别微信二维码,添加小编,符合条件者即可申请加入微信群!请注明:姓名+研究方向!声明:本文旨在传递更多信息,版权归原作者所有。原创文章转载均需经过授权并注明来源,如涉及内容、版权或其他问题请时联系小编删除!文章仅代表作者个人观点,并不代表公众号立场。本公众号拥有对此声明的最终解释权!投稿邮箱:yck19876@163.com
临床申请疫苗临床1期
100 项与 Xinyao Biology (Shanghai) Co., Ltd. 相关的药物交易
登录后查看更多信息
100 项与 Xinyao Biology (Shanghai) Co., Ltd. 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2025年04月06日管线快照
无数据报导
登录后保持更新
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
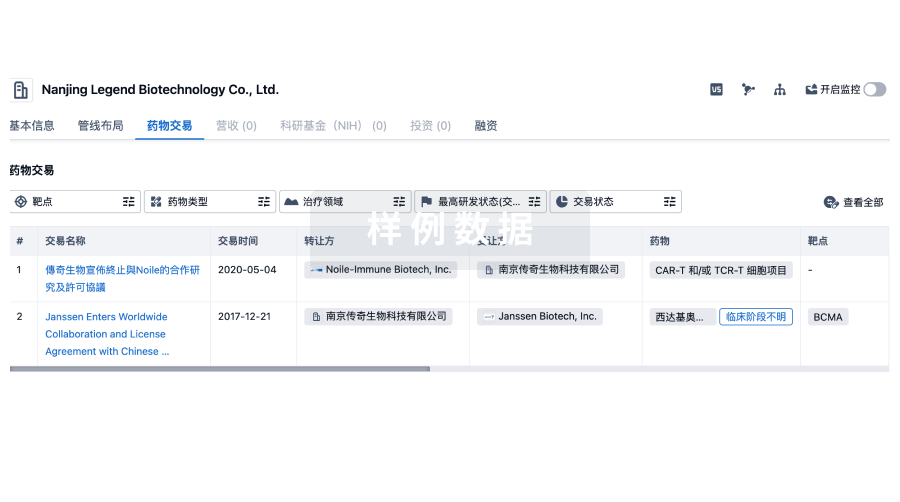
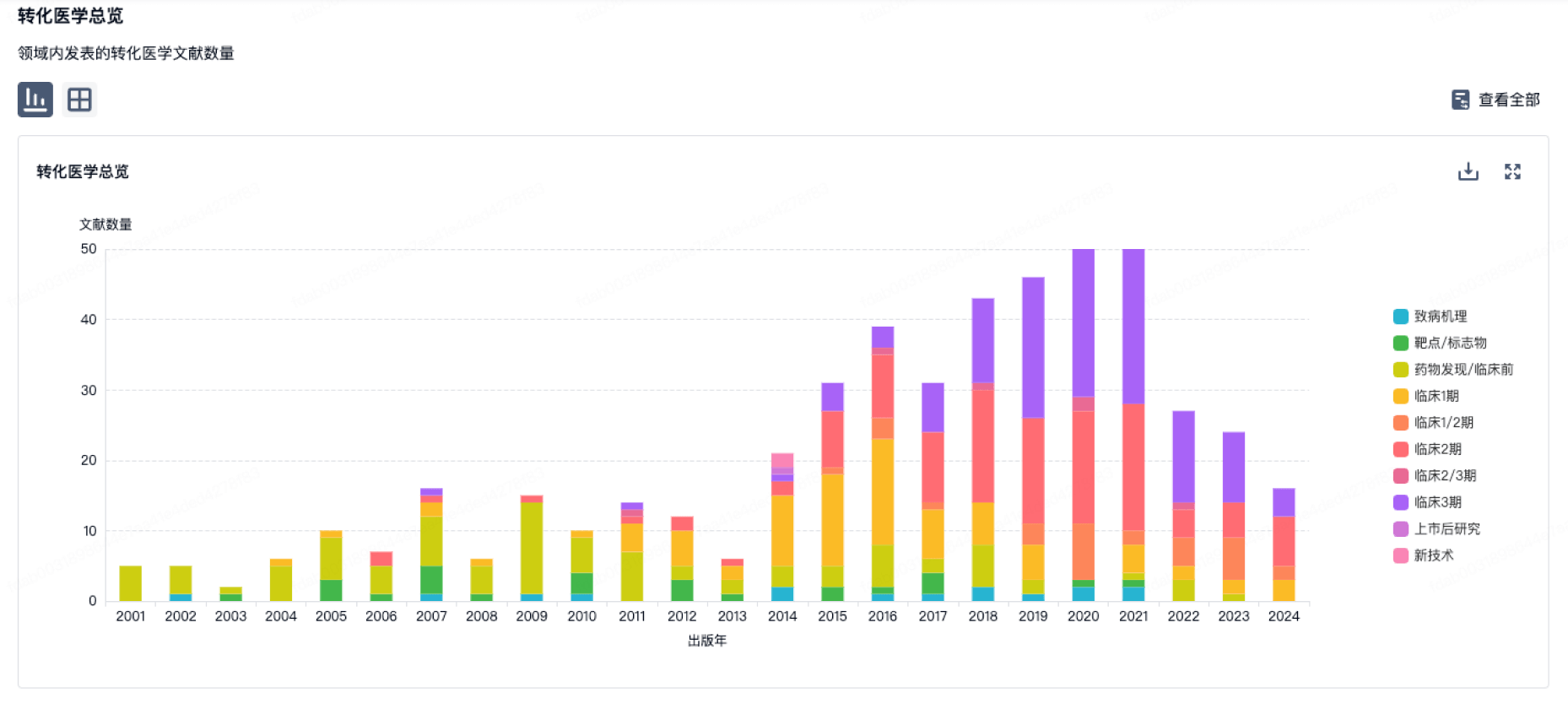
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
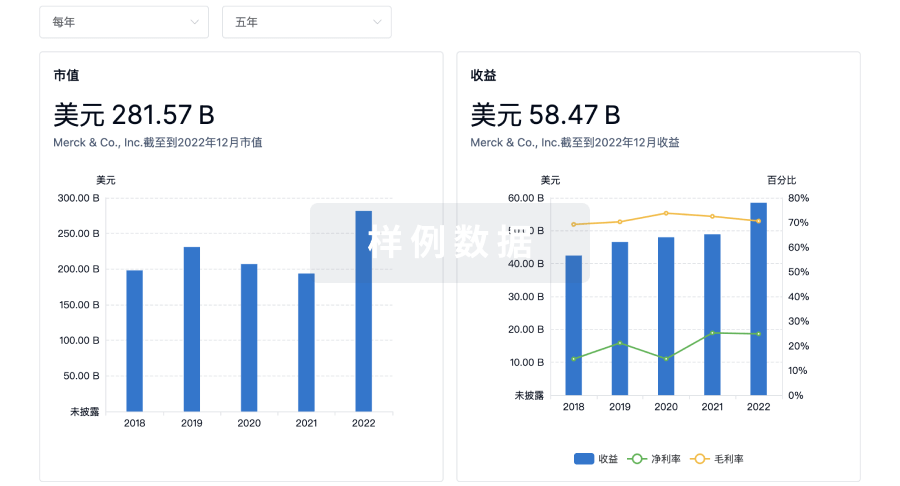
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
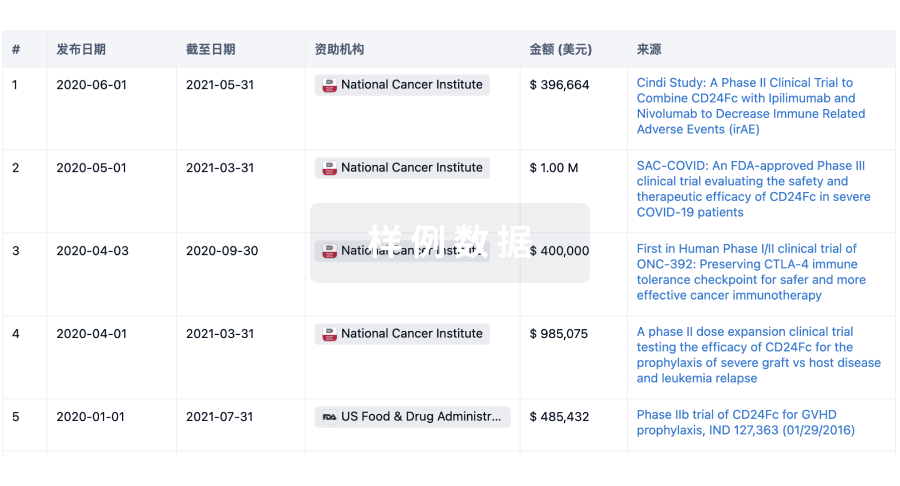
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
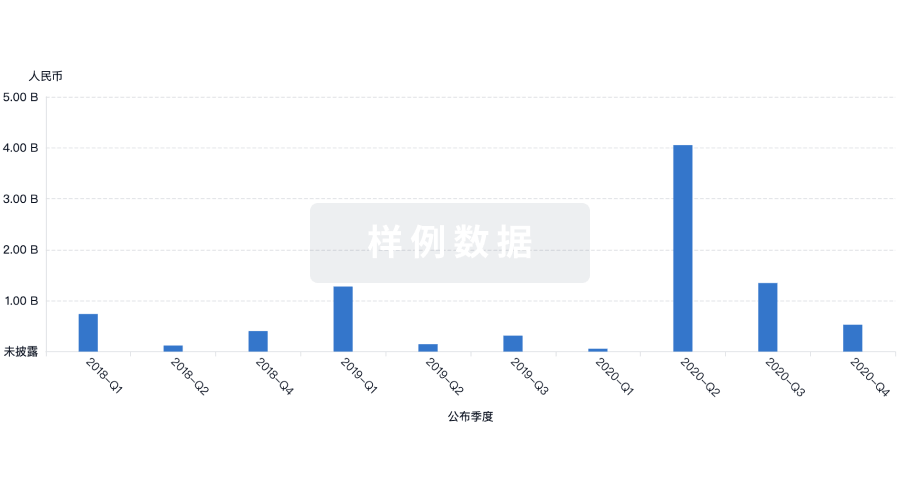
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
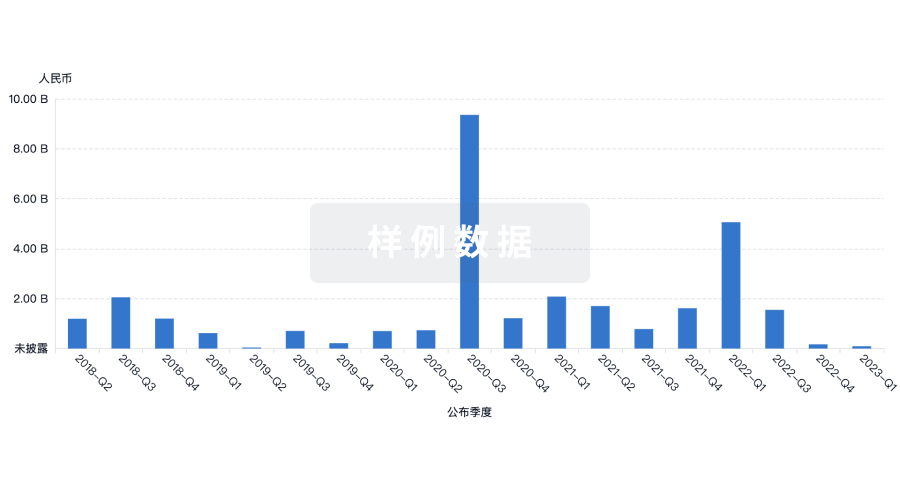
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用