预约演示
更新于:2025-08-29

EpiDestiny, Inc.
更新于:2025-08-29
概览
关联
5
项与 EpiDestiny, Inc. 相关的临床试验NCT07006025
Phase 1 Study of Oral Tetrahydrouridine-Decitabine to Treat Relapsed or Refractory Myelodysplastic Syndromes
The goal of this clinical trial is to learn about the safety and effectiveness of the combination drug Tetrahydrouridine (THU) and decitabine (DEC) to treat patients with relapsed or refractory myelodysplastic syndrome. The main questions it aims to answer are:
* Does the combination drug exhibit hematological and nonhematological toxicity?
* Does the combination drug improve health status and reduce the number of days of hospitalization?
Participants will:
* Take tetrahydrouridine and decitabine once a week for 24 weeks
* Visit the clinic once every 4 weeks for checkups and tests
* Keep a diary of their symptoms
* Does the combination drug exhibit hematological and nonhematological toxicity?
* Does the combination drug improve health status and reduce the number of days of hospitalization?
Participants will:
* Take tetrahydrouridine and decitabine once a week for 24 weeks
* Visit the clinic once every 4 weeks for checkups and tests
* Keep a diary of their symptoms
开始日期2025-06-03 |
申办/合作机构 |
NCT05816356
An Open Label, Randomized, Single Dose, Two Way Crossover, Bioavailability Study of a Combination Formulation of Decitabine/Tetrahydrouridine (2.5 mg/100 mg) Modified Release Capsules in Healthy, Fasting, Male Adults
This is an open-label, randomized, single-dose per period, two-period, crossover study to evaluate the relative bioavailability of decitabine and tetrahydrouridine ingested as a modified-release combination formulation compared to THU and decitabine ingested as immediate-release capsules
开始日期2023-03-24 |
申办/合作机构  EpiDestiny, Inc. EpiDestiny, Inc. [+1] |
NCT04055818
Proof-of-concept Study of Nicotinamide and Oral Tetrahydrouridine (THU) and Decitabine to Treat High Risk Sickle Cell Disease
A randomized control trial in 20 subjects with sickle cell disease comparing oral THU-decitabine to nicotinamide and in combination (THU, decitabine and nicotinamide).
开始日期2020-01-24 |
申办/合作机构  EpiDestiny, Inc. EpiDestiny, Inc. [+2] |
100 项与 EpiDestiny, Inc. 相关的临床结果
登录后查看更多信息
0 项与 EpiDestiny, Inc. 相关的专利(医药)
登录后查看更多信息
3
项与 EpiDestiny, Inc. 相关的新闻(医药)2022-09-05
关注并星标CPHI制药在线2022年9月,诺和诺德和Forma Therapeutics宣布双方已达成一项最终协议。据协议,诺和诺德将以每股20美元的现金收购Forma Therapeutics,总股本价值为11亿美元。 Forma Therapeutics是一家专注于镰状细胞病(SCD)和罕见血液疾病业务的临床阶段生物制药公司,其进展较快的两款产品为Etavopivat和Olutasidenib。其中Etavopivat是一种选择性丙酮酸激酶-R(PKR)激活剂,被开发用于治疗SCD,目前正在开展一项随机、安慰剂对照、双盲、多中心的2/3期临床试验。Olutasidenib是一款口服IDH1 酶抑制剂,可透过血脑屏障,开发用于治疗胶质母细胞瘤、复发/难治型急性髓系白血病、骨髓增生异常综合征和其它IDH1突变实体瘤。 诺和诺德是糖尿病领域的佼佼者,同时在血友病、生长激素治疗以及激素替代疗法等领域处于先进地位。目前诺和诺德罕见病部门的主要关注点是生长激素缺乏症和血友病,且在这两个领域有多种产品上市销售,如每日一次生长激素注射剂Norditropin和重组FVII NovoSeven。此外,罕见病研发管线中concizumab、nedosiran、Mim8和EPI01也已进入临床。 • Concizumab 是一种抗组织因子途径抑制剂(TFPI)单抗,经皮下注射用于预防所有血友病亚型,其作用独立于 FVIII 和 FIX,通过增加 FXa 的产生增强凝血起始阶段,从而产生足够的凝血酶 (TG) 以防止出血。已公布的3期临床实验结果显示:使用concizumab预防性治疗患者的自发性与外伤性出血情形降低 86%,平均年出血率(ARB)为1.7,相比未经concizumab 治疗的对照组平均ABR 为11.8,达到主要研究终点。公司预计将在2022年下半年在美国、日本提交监管申请。 • Mim8是一款针对FIXa和FX的下一代双特异性抗体,是用于有/无抑制物血友病A患者的皮下注射预防治疗药物,目前处于1/2期临床研究阶段。 • Nedosiran是利用Dicerna专有的RNAi技术平台GalXC开发的一款RNAi药物,通过与mRNA结合抑制肝乳酸脱氢酶(LDH)的表达,被开发用于治疗原发性高草酸尿症(PH)。去年11月,该药一项关键性临床试验达到主要终点:与安慰剂相比,nedosiran使PH1亚型患者的尿液中的草酸盐排泄(Uox)表现出具有统计学显著性的持续降低。据悉,今年Nedosiran将递交监管申请。2021年12月,诺和诺德斥资约33亿美元收购了Dicerna。 • EPI01是一种口服复方药,由固定剂量的DNA甲基转移酶1抑制剂地西他滨(DAC)和胞嘧啶核苷脱氨酶抑制剂四氢尿苷(THU)组成,具有潜在的增加胎儿血红蛋白(HbF)的量来取代SCD患者中存在的有缺陷的血红蛋白,从而防止红细胞变形并提高血液中的血氧水平,目前该项目即将进入2期临床。2018年4月,诺和诺德与EpiDestiny达成一项全球独家授权协议,获得EPI01项目。 据公司财报,诺和诺德2022上半年糖尿病和肥胖症业务收入727.15亿丹麦克朗,同比增长13%,罕见病业务营收105.81亿丹麦克朗,同比增长6%。整体来看,诺和诺德罕见病业务占比较小,有待继续挖掘。在今年3月举办的资本市场日(CMD)上,诺和诺德正式宣布加大对罕见病领域的投资力度,此次收购Forma Therapeutics也进一步证明了诺和诺德布局罕见病领域的决心。 而且,此前诺和诺德已在罕见病领域与多家企业达成合作,如2019年10月,诺和诺德与bluebird bio达成一项为期3年的研究协议,联合开发下一代体内基因组编辑疗法,治疗严重遗传性疾病,而合作的重点在于为A型血友病患者开发出替代注射凝血因子的新型疗法。2021年7月,诺和诺德和Prothena宣布两家企业达成收购协议,以最高达12亿美元的开发和销售里程碑付款获得后者在研抗体PRX004和转甲状腺素蛋白淀粉样变性(ATTR)研发项目。2021年11月,诺和诺德斥资33亿美元收购Dicerna,引进Dicerna 先进的 RNAi 药物引擎和细胞内递送系统。 据Frost&Sullivan资料,全球罕见病药物市场规模将由2020年的1351亿美元增至2030年的3833亿美元,年复合增长率高达11%。目前罕见病已成为继肿瘤、自身免疫疾病之后跨国药企斥巨资布局的又一赛道。据不完全统计,围绕罕见病赛道,近年来跨国药企先后达成多项大型收购交易,其中多项收购交易总额高达百亿美元。 ► 2022年8月,安进以约 37 亿美元现金收购 ChemoCentryx。 ► 2022年8月,辉瑞以54亿美元的价格收购Global Blood Therapeutics(GBT)。 ► 2021年12月,默克宣布收购Chord Therapeutics。 ► 2021年9月,默沙东以110亿美元收购制药公司Acceleron。 ► 2021年9月,阿斯利康以3亿美元价格收购Caelum Biosciences。 ► 2020年12月,阿斯利康以390亿美元的价格收购Alexion。 ► 2018年3月,武田以630亿美元收购夏尔。 ► 2018年1月,赛诺菲以116亿美元的价格收购Bioverativ。 ► 2017年2月,强生以300亿美元收购Actelion Pharmaceuticals。 【企业展示】点击下图,投票选出您喜爱的制药文章智药研习社近期研习会报名来源:CPHI制药在线声明:本文仅代表作者观点,并不代表制药在线立场。本网站内容仅出于传递更多信息之目的。如需转载,请务必注明文章来源和作者。投稿邮箱:Kelly.Xiao@imsinoexpo.com▼更多制药资讯,请关注CPhI制药在线▼点击阅读原文,进入智药研习社~
并购免疫疗法抗体合作信使RNA
2022-09-01
Novo Nordisk announced a big purchase on Thursday to augment its rare disease portfolio.
The Danish pharmaceutical giant is shelling out $20 per share in cash to acquire clinical-stage biotech Forma Therapeutics, which focuses on rare hematologic diseases. The deal represents a total equity value of $1.1 billion, about $425 million more than Forma’s current market cap. The transaction is expected to close before the end of the year.
Forma made its market debut in 2020 with a $278 million initial public offering. The Massachusetts-based company’s lead drug candidate is etavopivat, a once-daily selective pyruvate kinase-R activator designed to improve anemia and red blood cell health in patients with sickle cell disease (SCD).
SCD is an inherited disease that causes hemoglobin, the oxygen-carrying protein in red blood cells, to become rigid and misshapen. This makes normally round and flexible red blood cells rigid, and they take on a sickle shape. The clogging of these sickle-shaped blood cells impedes blood flow, as well as the delivery of oxygen to tissues. The condition leads to complications including vaso-occlusive crisis, which occurs when sickled red blood cells block blood flow to tissues thereby depriving them of oxygen.
In a Phase 1 trial, etavopivat was shown to increase hemoglobin in SCD patients, improve their red blood cell health and decrease vaso-occlusive crises.
The drug is currently being studied in a global Phase 2/3 trial involving patients with SCD, as well as a Phase 2 involving patients with transfusion-dependent SCD or another inherited hemoglobinopathy called thalassemia. The first interim data release for the Phase 2/3 is slated to take place before the end of the year.
The acquisition is “by no means out of the blue,” Ludovic Helfgott, Novo’s executive vice president and head of rare disease, said in an interview. The deal signals Novo’s commitment to developing more products to treat hematological disorders, which Helfgott identified as an area with a large unmet need.
Novo was attracted to etavopivat for a few reasons. The drug has demonstrated a good safety profile and efficacy during its clinical testing, and it is convenient for patients given that it needs to be taken only once daily. Novo also liked how flexible the drug can be — it can be used alone or in combination with other treatments, and it is currently being developed for use in pediatric patients as well as adults, according to Helfgott.
This is not the first time Novo has made an acquisition to strengthen its SCD portfolio. In 2018, the company paid $400 million for Ohio-based EpiDestiny’s early stage SCD program. Together, Novo and EpiDestiny have built NDec — an oral, fixed-dose formulation of decitabine and tetrahydrouridine for the treatment of SCD. The compound is currently in clinical development, Helfgott said.
Novo’s acquisition of Forma is the second billion-dollar SCD deal the pharmaceutical industry has seen in the last 30 days. Pfizer forked over $5.4 billion in August to buy Global Blood Therapeutics, a company with one commercialized therapy for sickle cell disease and a pipeline of additional drugs in various stages of development for the blood disorder.
IPO并购
2018-04-06
A Novo Nordisk flag flies in the wind/Courtesy jor
Danish pharma giant Novo Nordisk tied up a sickle cell and beta-thalassemia program in a $400 million deal with Ohio-based EpiDestiny.
Danish pharma giant
Novo Nordisk
tied up a sickle cell and beta-thalassemia program in
a $400 million deal
with Ohio-based EpiDestiny.
Novo Nordisk will acquire the gene control therapy EPI01, which recently finished Phase I testing for sickle cell disease. Phase I testing of EPI01, which is a combination of tetrahydrouridine and decitabine, in a small group of patients showed that EPI01 increased levels of fetal hemoglobin. An increase in fetal hemoglobin is important to both sickle cell and beta-thalassemia patients. Elevated HbF correlated with increased red blood cell half-life, reduced number of pain crises and increased life expectancy, Novo Nordisk said in its announcement.
“This is a great opportunity for Novo Nordisk to enter into a new therapeutic area closely related to our existing biopharmaceutical business and thereby utilize our core R&D and commercial capabilities to make a significant difference for patients living with a serious chronic disease. We are looking forward to working closely with EpiDestiny and their great network among sickle cell disease experts and the sickle cell community. We are confident that together we can make a significant difference for SCD patients and their families globally,” Novo Nordisk Chief Science Officer Mads Krogsgaard Thomsen said in a statement.
Under terms of the deal, the $400 million paid to EpiDestiny will include upfront fees, as well as developmental and commercial milestone payments. The companies did not disclose a breakdown in the way the money will be paid out. The two companies will collaborate on the development of EPI01 for both sickle cell disease and beta-thalassemia.
With Phase I data in hand the Danish company is looking to take orally-administered EPI01 to the next stage of clinical testing. If the drug continues to impress it’s likely to be a contender with hydroxyurea, a standard sickle cell drug. That standard care though does have some toxicity issues. There is currently no treatment for sickle cell disease that targets the cause. Sickle cell disease can cause blood vessels to become blocked. That blockage can damage organs and cause death.
Following the small Phase I trial EpiDestiny said
EPI01 provided an effective way
of controlling gene expression, without causing the toxicity problems of hydroxyurea.
The acquisition of the EpiDestiny product comes at a time when Novo Nordisk, known for its diabetes products, is looking to boost its hematology program. Last year Novo snagged approval from the U.S. Food and Drug Administration for
Rebinyn
, a hemophilia B treatment for adults and children.
临床1期并购上市批准基因疗法引进/卖出
100 项与 EpiDestiny, Inc. 相关的药物交易
登录后查看更多信息
100 项与 EpiDestiny, Inc. 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2025年09月03日管线快照
管线布局中药物为当前组织机构及其子机构作为药物机构进行统计,早期临床1期并入临床1期,临床1/2期并入临床2期,临床2/3期并入临床3期
其他
1
登录后查看更多信息
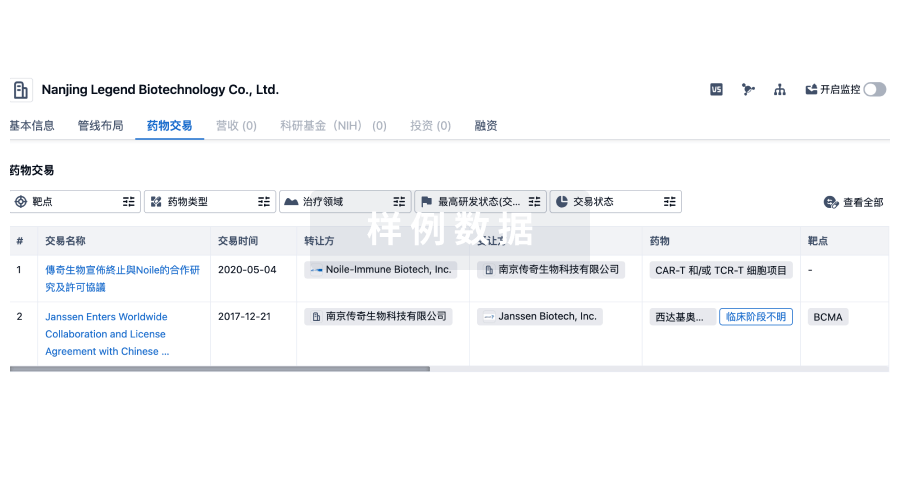
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
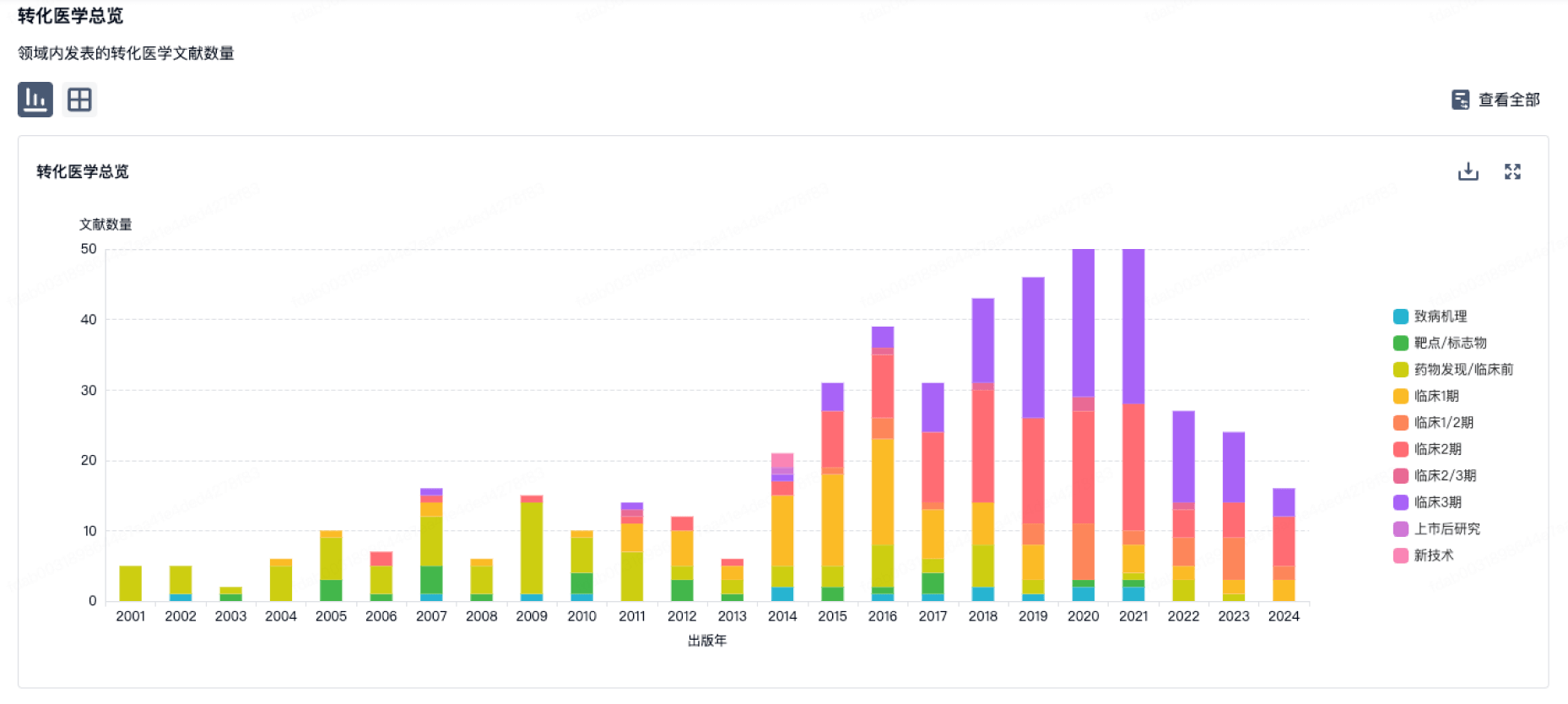
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
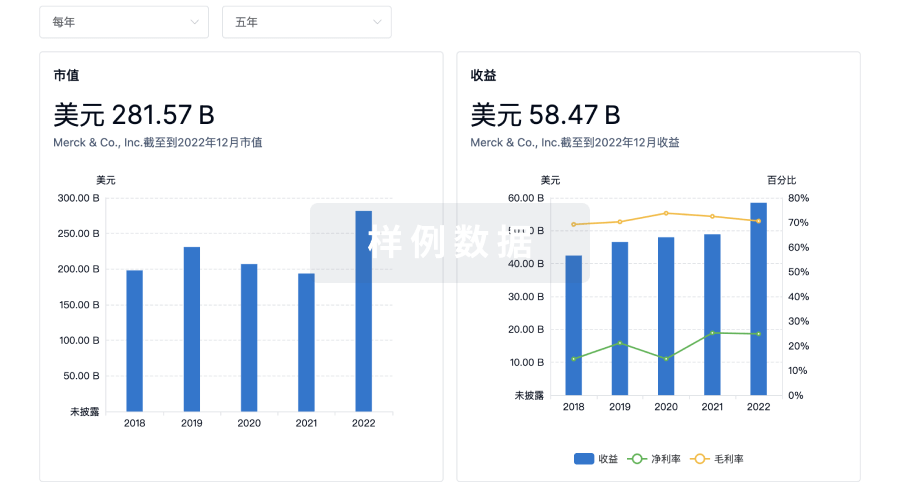
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
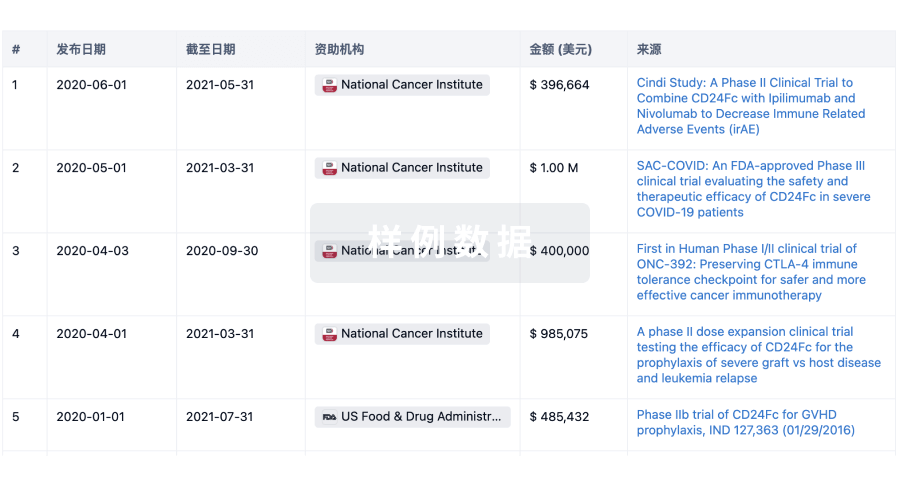
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
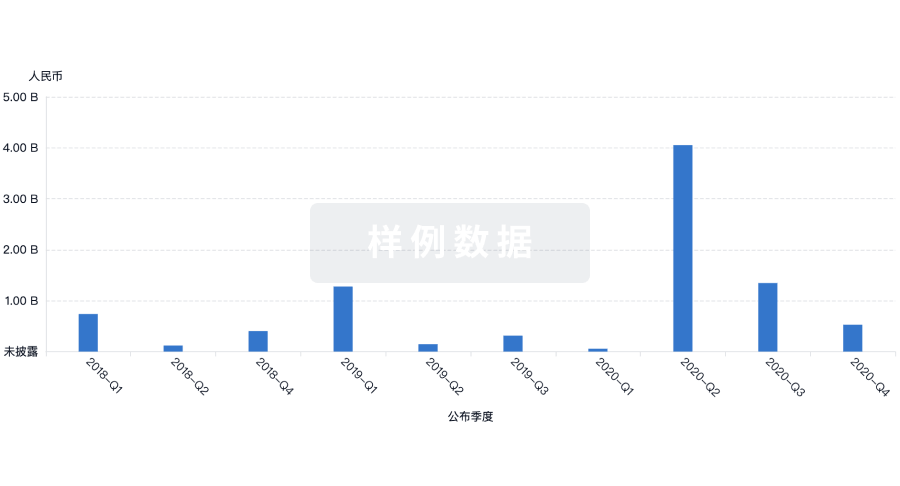
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
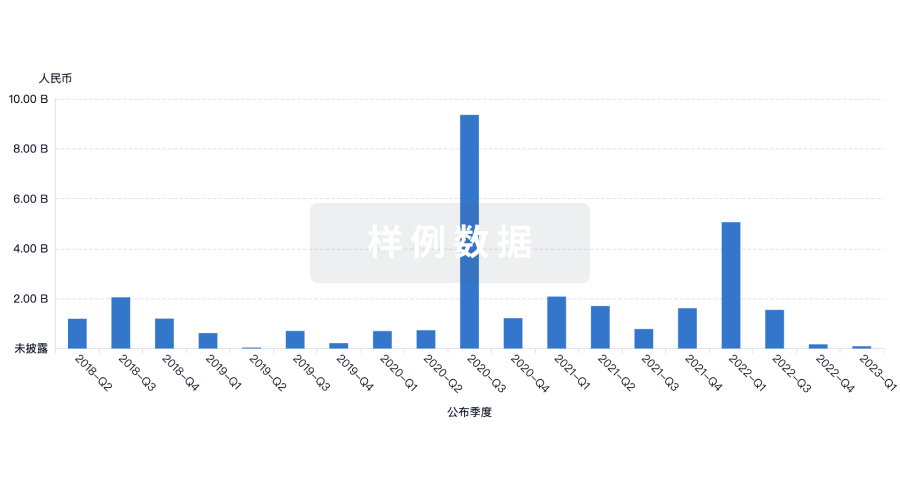
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
Eureka LS:
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用