更新于:2024-09-19
汉氏药业(北京)股份有限公司
私营公司|
2021|
中国北京市
私营公司|
2021|
中国北京市
更新于:2024-09-19
概览
标签
心血管疾病
神经系统疾病
免疫系统疾病
间充质干细胞疗法
关联
2
项与 汉氏药业(北京)股份有限公司 相关的药物靶点- |
作用机制 干细胞替代物 |
在研机构 |
原研机构 |
非在研适应症- |
最高研发阶段临床1/2期 |
首次获批国家/地区- |
首次获批日期- |
靶点- |
作用机制 干细胞替代物 |
在研机构 |
原研机构 |
在研适应症 |
非在研适应症- |
最高研发阶段临床1期 |
首次获批国家/地区- |
首次获批日期- |
7
项与 汉氏药业(北京)股份有限公司 相关的临床试验注射用间充质干细胞(脐带)治疗急性缺血性脑卒中(AIS)患者安全性、耐受性及
初步疗效的单臂、开放探索期临床研究
主要目的 评价注射用间充质干细胞(脐带)治疗急性缺血性脑卒中的耐受性和安全性,确定临床用药的范围。
次要目的 初步探索注射用间充质干细胞(脐带)治疗急性缺血性脑卒中患者的有效性,并为后续确证阶段临床试验试验药物剂量的选择提供依据。
探索目的 进一步探索注射用间充质干细胞(脐带)治疗急性缺血性脑卒中患者药代动力学特征及可能的分子机制。
开始日期2024-08-08 |
申办/合作机构 |
A Single Arm, Open Label Exploratory Clinical Study on the Safety, Tolerability, and Preliminary Efficacy of Mesenchymal Stem Cells (Umbilical Cord) Injection in the Treatment of Acute Ischemic Stroke (AIS) Patients
The goal of this clinical trial is to learn if drug mesenchymal stem cells (umbilical cord) injection works to treat acute ischemic stroke in adults. It will also learn about the safety and efficacy of drug mesenchymal stem cells (umbilical cord) injection . The main questions it aims to answer are:
Identify the dose-limiting toxicity (DLT) of drug mesenchymal stem cells (umbilical cord) injection in acute ischemic stroke patients.
Dose the drug mesenchymal stem cells (umbilical cord) injection improves the mRS score, NIHSS score, Fugl-Meyer score and and Barthel index of acute ischemic stroke patients? What is the pharmacokinetic characteristics and immunogenic response of mesenchymal stem cells (umbilical cord) injection in the treatment of acute ischemic stroke patients.
What is the the possible molecular mechanisms of mesenchymal stem cells (umbilical cord) injection in the treatment of acute ischemic stroke patients.
Participants will:
Take drug drug mesenchymal stem cells (umbilical cord) injection once or once a week for three consecutive weeks.
After receiving the corresponding dose of mesenchymal stem cells (umbilical cord) injection, the subjects entered a 6-month safety, efficacy observation and further safety evaluation period. Long term efficacy and survival follow-up up to 2 years.
Identify the dose-limiting toxicity (DLT) of drug mesenchymal stem cells (umbilical cord) injection in acute ischemic stroke patients.
Dose the drug mesenchymal stem cells (umbilical cord) injection improves the mRS score, NIHSS score, Fugl-Meyer score and and Barthel index of acute ischemic stroke patients? What is the pharmacokinetic characteristics and immunogenic response of mesenchymal stem cells (umbilical cord) injection in the treatment of acute ischemic stroke patients.
What is the the possible molecular mechanisms of mesenchymal stem cells (umbilical cord) injection in the treatment of acute ischemic stroke patients.
Participants will:
Take drug drug mesenchymal stem cells (umbilical cord) injection once or once a week for three consecutive weeks.
After receiving the corresponding dose of mesenchymal stem cells (umbilical cord) injection, the subjects entered a 6-month safety, efficacy observation and further safety evaluation period. Long term efficacy and survival follow-up up to 2 years.
开始日期2024-08-01 |
申办/合作机构 |
注射用间充质干细胞(脐带)治疗外伤性脊髓损伤单臂、开放、多中心探索性临床研究
主要目的
评价注射用间充质干细胞(脐带)治疗外伤性脊髓损伤患者的耐受性和安全性,确定临床用药的范围。
次要目的
初步探索注射用间充质干细胞(脐带)治疗外伤性脊髓损伤患者的有效性,并为后续确证阶段临床试验试验药物剂量的选择提供依据。
探索目的
进一步探索注射用间充质干细胞(脐带)治疗外伤性脊髓损伤患者药代动力学特征、免疫原性、可能的分子机制及fMRI和神经电生理检测的变化情况。
开始日期2024-03-15 |
申办/合作机构 |
100 项与 汉氏药业(北京)股份有限公司 相关的临床结果
登录后查看更多信息
0 项与 汉氏药业(北京)股份有限公司 相关的专利(医药)
登录后查看更多信息
12
项与 汉氏药业(北京)股份有限公司 相关的文献(医药)2023-09-01·Heart, Lung and Circulation
Comment on: Bone Marrow Mesenchymal Stem Cells for Heart Failure Treatment: A Systematic Review and Meta-Analysis
Review
作者: Sun, Qian ; Gu, Jundong ; Li, Qiuhan
2023-09-01·Journal of clinical neuroscience : official journal of the Neurosurgical Society of Australasia
Comment on: Autologous hematopoietic stem cell transplantation in neuromyelitis optica spectrum disorder: A systematic review and meta-analysis.
Review
作者: Gu, Jundong ; Xie, Qiong ; Sun, Tianze
2023-09-01·European journal of neurology
Comment on: Prognostic significance of the clinical and radiological haemorrhagic transformation subtypes in acute ischaemic stroke: a systematic review and meta-analysis.
Review
作者: Sun, Jingchen ; Xie, Qiong ; Gu, Jundong
4
项与 汉氏药业(北京)股份有限公司 相关的新闻(医药)2023-06-21
·生物谷
综述
综述
当前我国细胞行业真实业态多样,细胞领域临床研究、研发、生产产能及市场需求均有较大释放空间;另一方面,从主要监管部门到各地地方政府,或在具体监管案例中谨慎处理,为日后完善监管留白预留充分政策空间,或积极探索细胞行业发展模式和监管路径。
本文拟通过全景梳理经市场化机制催生的细胞领域实际业态(而非从产业链角度),及各地司法、监管实践案例,并基于监管的底层逻辑和依托要素,分析研判我国细胞行业未来发展模式和监管路径,以供业界参考。除非明确写明“干细胞”或“免疫细胞”,本文所称“细胞”包含体细胞、免疫细胞、干细胞等。
一、我国细胞行业当前业态及典型投建模式
(一)当前细胞行业主要业态
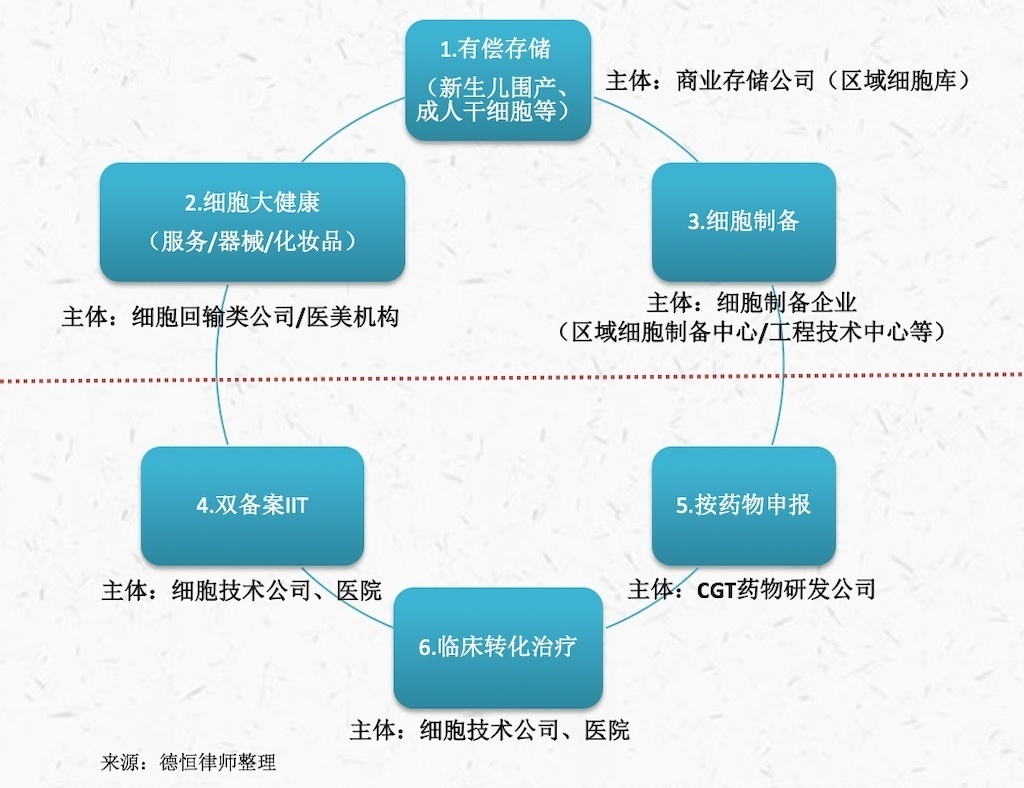
根据市场公开信息,目前我国细胞行业主要业态包括细胞商业存储、细胞生产与制备、细胞医美大健康、按药物申报、双备案的干细胞临床试验、临床转化治疗等实际业态,整体如下图:
1.细胞商业存储现状
目前我国细胞存储业务分为公共血库造血干细胞存储和商业有偿存储,涉及的组织样本主要包括新生儿脐带、脐带血和胎盘样本、骨髓液样本、牙齿样本、脂肪组织、滑膜组织等。
公共库主要系原卫生部依据《脐带血造血干细胞库设置管理规范(试行)》等规定,以公益为目的进行采集和存储,供有需求的患者配型使用而先后批准设立的北京、天津、上海、浙江、山东、广东、四川等7个脐带血造血干细胞库。
商业存储则由相关企业面向社会公众从事有偿细胞存储和制备,以新生儿自体围产组织干细胞和成人自体细胞为主。目前各省基本均有细胞有偿存储业务业态,且呈现头部企业虹吸效应。如中源协和(600645)在2022年报中披露其已在全国20 个省市建立细胞资源库,开展脐带血造血干细胞、脐带间充质干细胞、胎盘亚全能干细胞、脂肪干细胞及免疫细胞的检测、制备与存储服务,构建了全国性细胞资源存储网络。
2.细胞生产与制备现状
除细胞药物研发制备企业及相关CDMO企业外,当前细胞制备业务主要指细胞企业为临床研究医院、科研及企事业单位提供细胞制品。如天晴股份(832035)年报披露,公司的制备服务项目“主要集中在省内及东三省的专业的肿瘤医院及综合性医院的肿瘤科、普通外科等产生肿瘤病人的科室,公司为他们的生物治疗癌症临床研究提供高效 NK细胞”。截止2022年底,我国获得中检院干细胞质量检验报告机构的数量约50家。近年,随着诱导多能干细胞(IPSC)技术及其应用的不断成熟和拓展,IPSC来源的种子细胞、前体细胞制剂制备的市场需求不断扩容。
在各地政府鼓励发展细胞与基因治疗背景下,头部细胞企业多被当地科技、发改等部门认定为当地“工程技术中心”、“工程研究中心”、“区域细胞制备中心”等。如赛莱拉(831049)曾在信披文件中披露,广东省(赛莱拉)区域细胞制备中心即是广东省发改委、省科技厅、省卫计委、省食药监局联合发函批复,由赛莱拉承担建设的省级区域细胞制备中心。
3.细胞医美与大健康业务现状
细胞大健康业务常见的有干细胞、免疫细胞回输及相关医美制品或服务。如冠昊生物(300238)在2021年报中即披露,公司“扎根大健康前沿领域,适时推出免疫增强方案、牙髓干细胞储存等新技术服务,借助产品线扩充升级,自建中医养生保健馆--天佑延年堂、高端综合门诊--广州百尼夫等技术落地运营机构,完善产品应用闭环”。
值得一提的是,由于人源细胞因子尚未列入国家药监局化妆品原料药目录,目前国内尚无获批的干细胞化妆品。国家药监局曾在2021年9月发文强调“干细胞化妆品”属于伪概念。当前合规化生产、销售的化妆品也并非是以“人源细胞”作为原料的化妆品。如赛莱拉曾披露“公司依托掌握的干细胞核心技术,延伸到动植物细胞提取物技术研发,将自主研发、自主生产的包含专利技术的动植物细胞提取物原料转化为功能性护肤品”。
4.按药物进行申报
随着2021年两款CAR-T产品在我国批准上市,细胞治疗产品按照药品监管的路径全面打通。根据CDE官网信息,截至2023年2月28日,国内共有42家企业的62款干细胞药物临床试验申请(IND)获得受理,30家企业的47款获得临床默示许可,主要为来源脐带、胎盘、骨髓、脂肪、牙髓、宫血等间充质干细胞药物。同时,IPSC类干细胞药物IND申请也逐渐增多。目前在该方面较活跃的企业包括安徽中盛溯源、南京艾尔普、浙江霍得生物、呈诺医学、武汉睿健医药等。
值得一提的是,今年4月西比曼生物科技正式宣布启动公司旗下“异体人源脂肪间充质祖细胞注射液AlloJoin”的 III 期临床试验。这也标志着我国干细胞药物研发进入III期临床时代。
5.双备案的临床试验现状
双备案即非注册临床研究(IIT)的研究机构、研究项目双备案。
经检索,目前全国已有137家研究机构(含军队医院22家)在卫健委、药监局或后勤保障部卫生局完成临床研究机构备案,共有112个干细胞临床研究项目备案。相关适应症涉及循环系统(如急性心梗、心衰)、神经系统(如帕金森病、缺血性卒中)、泌尿生殖系统(如宫颈粘连、卵巢早衰)、免疫系统(如狼疮性肾炎)、运动系统(如膝骨关节炎、半月板损伤等)等多系统疾病的治疗。
6.临床转化治疗现状
尽管监管政策前后有所变化,在医疗实践中,医院或企业通过多种方式尝试或实施细胞临床转化治疗的行为从未终止。许多地方政府或自贸区也积极探索,希望打通细胞临床转化治疗的支付路径。如中源协和在2021年报中披露,“2021 年 6 月,血研所与公司等主体合作建设中国(天津)自由贸易试验区联动创新示范基地,该基地计划依托国家干细胞工程产品产业化基地细胞存储、研发、生产制备、临床转化应用等全闭环管理环境,探索在细胞治疗临床试验同情用药、进口国外已上市国内未上市药品与医疗器械、细胞治疗按照医疗技术准入开展临床收费应用等方面实现突破”。
(二)当前细胞企业典型投建模式
鉴于细胞治疗药品研发周期长、资本密集的特点,国内多数细胞企业同时布局多种业态,以构建细胞产业全闭环。以国内上市或挂牌的细胞企业为例,其业态布局情况如下:
再如,根据市场公开资料,北京汉氏联合生物技术股份有限公司同时布局汉氏生物、汉氏药业、汉氏医学、希诺神州四个产业板块,其中汉氏生物负责细胞存储、制备和CXO服务;汉氏医学承担集团精准医疗大健康产业的建设运营任务,主要包括三级医院、综合门诊部、高端体检中心、第三方医学检验中心、互联网医院、医美护肤中心、医疗旅游等业务;汉氏医药则以细胞类新药研发为主,现有多个干细胞1类新药临床试验申请获得批准。
二、现有业态的法律评价与司法监管实践
(一)当前司法监管实践的整体特征
目前我国细胞领域的司法裁判以零星案例为主,尚未形成体系化的裁判标准,针对同类型案例,不同法院裁判口径不一;行政监管实践以相关主体投诉、举报等发起的被动型监管为主,主动研判型、体系化监管相对偏少。
值得一提的是,为应对行业发展带来的监管挑战,部分地方开始加强主动型监管的研究。如2021年9月深圳市坪山区人民法院发布《生物医药产业全流程法律风险及司法应对研究》专项调研课题投标公告,2022年12月深圳坪山区发布《深圳市坪山区生物医药企业刑事合规工作指引》,均系主动构建当地裁判或监管体系。
(二)各业态典型司法、监管案例及执行口径
1.商业存储业务的法律评价与裁判
(1)商业存储合约效力认定
泰州中院(2017)苏12民终570号一案中,在案由上,法院将脐带血存储纠纷界定为消费者权益纠纷;在合约效力上,针对上述人(存储脐带血的自然人)提出的“案涉合同违反法律、行政法规的强制性规定应当无效”的诉请,法院认为,上诉人 “既是脐带血造血干细胞的提供者,也是脐带血造血干细胞的所有者,脐带血造血干细胞仅仅供本人或者近亲属使用,并不涉及其他公民,亦不会对公共安全造成影响”,故“被上诉人接受上诉人委托制备、存储脐带血造血干细胞并不违反《中华人民共和国献血法》等法律、行政法规的强制性规定”,最终判决脐带血有偿存储合约有效。
经笔者在裁判文书网检索,尚未发现人遗条例颁布后的商业存储纠纷判例。
(2)商业存储与保藏审批的监管实践
目前的从事细胞商业存储的企业多将存储行为定位成基于“未来临床治疗目的”,未申请保藏许可。部分企业因兼有未来科学研究目的或承担了特定平台职能,则申请并获得了保藏审批,如河南省华隆生物技术有限公司河南省人类干细胞资源库等。
目前尚无商业存储方因未取得保藏许可而被人遗监管部门处罚的案例。
2.细胞回输协议效力的司法实践
在已有的细胞回输相关纠纷案例中,针对细胞回输协议的效力,出现“有效”和“无效”两种不同的裁判结果。
(1)协议有效的案例
在烟台中院(2020)鲁06民终1331号一案中,上述人(接受回输方)提出“被上诉人在未获得国家批准情况下,直接将‘干细胞回输液’注射到上诉人体内,并向上诉人收取费用,违反上述管理办法及《中华人民共和国药品管理法》、《医疗机构管理条例》等法律规定,被上诉人以‘免疫细胞保健’名义向上诉人有偿提供的‘干细胞套餐’服务依法应当认定无效。二审法院最终认为,“本案双方签订的‘干细胞套餐’服务合同,系双方真实意思表示,且双方在签订合同时,该合同并未违反法律或行政法规的强制性规定”,即判决细胞保健合同有效。
(2)协议无效的案例
在上海一中院(2020)沪01民终4321号一案中,法院认为 “与干细胞相关的管理规范具有公共利益属性,虽然《干细胞临床研究管理办法(试行)》不属于法律、行政法规,在法律规范的效力位阶上属于部门规章,但是该管理办法系依据《中华人民共和国药品管理法》《医疗机构管理条例》等法律、行政法规而制定,旨在规范和促进干细胞临床研究健康、有序发展”,因此,“聚仁公司销售‘干细胞’给他人直接用于人体回输,违反了《干细胞临床研究管理办法(试行)》第五十二条关于禁止干细胞直接进入临床应用的规定的同时,严重违背了伦理规范,破坏国家医疗监管制度,危及不特定个体生命健康安全,进而损害社会公共利益”,最终判决协议无效。
综上,对于细胞医美和细胞大健康服务的法律评价,司法实践中尚无统一认定标准。
3.“细胞化妆品”的监管实践
国家市场监督管理总局广告监督司《关于加强干细胞广告监管的工作提示》(广函字(2021)187号)、国家药监局《关于开展化妆品“线上净网、线下清源”专项行行动的通知》(国药监妆(2021)47号)等文件均明确不得违规宣称相关产品含有干细胞且存在美容、抗衰等功效,多地亦出现行政处罚案例。
因此,针对“细胞化妆品”的监管口径比较清晰。
4.临床转化治疗的司法监管实践
一直以来,国内因临床转化治疗涉刑案件较少,较有代表性的是(2020)沪0101刑初76号许某等人非法经营罪案。该案判决书载明,2016年12月至2017年4月期间,许某以上海某高校转化医学研究院名义对外招揽病患,汪某负责在涉案公司办公地制作干细胞注射液,最终在涉案医院肿瘤科或公司办公地为患有渐冻症、脑溢血等不同病症的患者有偿注射干细胞。
该案的审理过程颇有看点。最初,上海市黄浦区法院一审判决许某等人犯生产、销售假药罪,公诉机关及原审被告人均不服,分别提出抗诉、上诉。上海三中院以“涉案干细胞是否假药以及各被告人在共同犯罪中的地位、作用等事实尚需进一步查明”为由,裁定发回重审。2020年1月,黄浦区法院重审立案,黄浦区检察院变更指控罪名为非法经营罪。最终,黄浦区法院判决被告人许某等“违反国家药品专营、专卖管理法律法规,未经许可经营药品”,构成非法经营罪。许某的刑罚从生产销售假药罪项下的有期徒刑11年,变更为非法经营罪项下的有期徒刑6年。
同时,针对细胞临床转化治疗,近两年典型行政处罚案件如下:
截止目前,上述案件相关方均未涉及刑事处罚。
5.与细胞领域相关的其他司法实践
目前与细胞行业关联的刑事罪名主要包括销售假药罪、诈骗罪以及走私、妨碍检验检疫等进出口类犯罪,其中以诈骗罪案例居首,这也与我国当前细胞治疗知识普及度和监管留白有关。近年来典型案件如下:
综上,尽管仅有少量司法裁判和监管处罚案例,但亦能看出,相关法院和监管部门在处理具体案件时,为行业发展预留政策空间的谨慎克制,在司法裁判上也似有轻刑化趋势。
三、我国细胞行业监管趋势研判与分析
(一)研判分析的基准
1.基于国外监管模式的共同底层逻辑或最大公约数
我们认为,无论是基于《公共卫生服务法案》将人体细胞和组织分为低风险产品(PHS ACT 351章节)和高风险产品(PHS ACT 361章节)而构建监管体系的美国“单轨制”(欧盟与之类似),还是将再生细胞治疗产品与药物、医疗器械平行立法的日本“双轨制”,均具有共性的底层逻辑和要素支撑。主要体现在以下两点:
(1)依托完善的风险分级制度
FDA依据细胞和组织产品风险的高低,将产品分为如下两大类,并明确界定“最小操作”和“同源性使用”的含义:
来源:《中国食品药品监管》
日本则由厚生劳动省(MHLW)按照三级风险对细胞治疗进行申报备案管理的,如下:
来源:《中国食品药品监管》
(2)依托完备的细胞制备体系和市场
针对细胞制备体系,美国FDA制定了较为完备的指南,包括工艺相关指南、临床前期相关指南、针对特定疾病或特定细胞的指南、有效性和安全性指南等。日本细胞治疗指导文件也涵盖不同的疾病领域、细胞类型,聚焦细胞采集、细胞制备、质量评价、疗效安全评估以及运输和存储标准等环节,基本实现细胞制备标准化。
关于细胞制备与流通市场,以干细胞为例,根据市场公开资料,日本在2020年底发放细胞制备许可证已超过2700家。
2.基于我国细胞行业监管模式的沿革逻辑
未来的监管模式即是对过去、当前现状的延伸和完善。
我国曾实行一段时间的“双轨制”,2016年“魏则西事件”之后,原国家卫计委终止细胞治疗收费,药监部门则逐渐强化、明晰和完善按药品监管的路径和体系。根据当前法律法规、规范体系,我国细胞基因治疗领域的“正清单”如下:
“正清单”之外领域的监管暂时留白,但趋势逻辑却在相关表征中有所体现。如2019年国家卫健委曾发布《生物医学新技术临床应用管理条例(征求意见稿)》《体细胞治疗临床研究和抓华应用管理办法(试行)》(征求意见稿),虽至今仍未颁布,但被业界认为是“双轨制”回归的信号。2023年5月9日卫健委发布的《体细胞临床研究工作指引(征求意见稿)》,即进一步体现了体细胞IIT与干细胞IIT监管模式逐渐趋同的趋势。
3.基于我国细胞领域政策趋势和立法逻辑
政策方面,继纳入十三五、十四五规划、健康中国 2030 后,2022年初,工信部、发改委、科技部、卫健委等九部门联合发布《“十四五”医药工业发展规划》,提出重点发展细胞治疗等新型生物药的产业化制备技术。2022年5月,发改委发布《“十四五”生物经济发展规划》,提出发展基因诊疗、干细胞治疗、免疫细胞治疗等新技术,加快相关技术产品转化和临床应用,推动形成再生医学和精准医学治疗新模式,并推动政策先行先试。
立法方面,我国在科技进步、生物安全、人遗资源管理、数据安全、科学伦理、外商投资、技术进出口等领域密集立法或修订,构建更符合当前国内外经济、科技发展形势的法律体系。
我们认为,我国针对细胞治疗等生物科技行业的政策和立法基本逻辑整体为“鼓励发展、守住红线”,具体如下:
(二)监管趋势与中国版“双轨制”分析
1.商业存储的监管趋势分析
我们认为,一段时间内将商业存储自体库纳入保藏审批监管的可能性不大。对于“存储”行为,仍将根据“存储目的”进行区分监管,即仅对基于科学研究目的的样本库要求保藏资质,具体如下图:
特别指出的是,无论是否取得保藏许可,从事干细胞存储的企业和机构均应无差别遵守《生物安全法》、人遗条例、《刑法》等法律法规中关于人遗资源出境、国际合作、人遗信息对外提供等监管的规定。
2.细胞医美与大健康的监管趋势分析
一方面,部分地方政府将干细胞医美作为地方特色经济来支持。如昆明市于2022年8月发布的《昆明市细胞产业发展规划(2021-2035年)》,在“近期重点推进”部分提出,“以临床技术(疾病治疗、医美应用)为行业突破点,打通临床应用环节和支付环节,实现临床技术在多病种上的突破”;在“重点任务”部分明确,“积极发展干细胞美容制品,引进一批拥有核心技术的医美制造企业;推进昆明医疗机构整形美容科室建设,推动干细胞研发等多方向研究及在修复重建、组织再生、创伤修复等的治疗应用;发挥昆明旅游胜地的流量优势,开发以干细胞医疗美容服务为主题的旅游产品”。
另一方面,2021年国家药监局修订发布的《已使用化妆品原料目录》中,并未收录“干细胞”作为化妆品原料。我国当前备案的干细胞临床研究中,也少有干细胞在美容、抗衰方面的研究。
我们认为,长远来看,细胞技术在医美和大健康领域的应用将分别纳入低风险临床转化细胞项目或保健品、化妆品等渠道监管。但因我国细胞制备体系和市场相对滞后、干细胞临床研究“双备案”门槛较高等现实因素,将“干细胞制品”纳入化妆品、保健品原料,或按照风险分级原则调整“双备案”门槛,在短期内落地的可能性不大,因此,未来一段时间内该领域大概率仍处于监管留白。但相关探索不会停止,如2021年1月,《中国美容整形外科杂志》即刊发《干细胞在整形修复美容领域研究和临床试验的专家共识》,旨在为干细胞在整形修复美容领域的研究与未来临床转化提供参考与支持。
3.细胞治疗的中国版“双轨制”模式分析
针对是否支持细胞治疗临床转化应用,不同地方政府表现出不同的态度,代表性的地方政策包括:
鉴于当前多数备案医院均不具备细胞制备能力,我国细胞制备工艺成熟度和市场容量也无法满足全面放开IIT项目临床转化的需求,因此完全按实施主体性质进行分类监管的可能性不大;同时,若仅依风险分级进行监管,将封闭现有多数“双备案”项目的临床转化通路,使得现有IIT研究的价值大打折扣,可行性亦受限。二种模式的优劣如下:
与之对应,我国细胞行业研发、生产产能和市场需求容量又亟需释放。
综上,我们认为,我国对细胞治疗的监管大概率将出现如下变化或趋势(各项内容或同步推进):
(1)对体细胞、干细胞临床研究的监管日渐趋同,即均施行“双备案”;
(2)率先在“双备案”项目中开展风险分级管理,并尝试放开低风险项目临床转化应用与收费;
(3)分类型、分病种完善细胞制备体系,统一或趋同不同监管通道的同类型细胞制备标准,扩容细胞制备市场和第三方检验检测市场;
(4)加强IIT与IST并轨管理,完善和优化IIT数据用于新药注册申请的路径和机制,进一步打通“双备案”项目成果转化通路;
(5)利用区域创新试点机制,择较成功区域扩大试点。
具体如下图
结语
尽管我国细胞行业的监管存在一定不确定性,但基于影响监管模式选择的底层逻辑和要素分析,我们仍能捕捉较多的确定性。对于不同的组织或机构,宜提前布局应对。如从事细胞医美的机构,积极推动细胞在美容、抗衰方面的IIT研究与转化,逐步将细胞医美大健康项目纳入各级、各类医疗机构经营范围,或是其合规化发展趋势。再如,对于地方政府,积极进行主动型管理布局,或是提高当地营商监管环境,促进当地细胞产业发展的有力措施。
参考文献
[1]山东省烟台市中级人民法院(2020)鲁06民终1331号民事判决书;
[2]上海市第一中级人民法院(2020)沪01民终4321号民事判决书;
[3]江苏省泰州市中级人民法院(2017)苏12民终570号民事判决书;
[4]《注释刑法全书》陈兴著,2022版;
[5]《细胞和基因治疗产品监管科学研究进展和展望》,国家药品监督管理局药品审评中心高建超,韦薇,张旻,高晨燕,《中国新药杂志》2022年第31卷
[6]《国际细胞和基因治疗制品监管比较及对我国的启示》,虞淦军等,《中国食品药品监管》,2019年08期;
[7]冠昊生物科技股份有限公司2021、2022年度报告;
[8]中源协和细胞基因工程股份有限公司2021、2022年度报告;
[9]广州赛莱拉干细胞科技股份有限公司2021、2022年度报告;
[10]《诱导多能干细胞(IPSC)技术及转化、应用核心法律机制与问题研究》德恒律师,左玉杰等。
本文作者
左玉杰
左玉杰,德恒重庆办公室合伙人;主要执业领域为证券上市、并购重组。
细胞疗法免疫疗法上市批准医药出海核酸药物
2023-06-05
·动脉网
干细胞技术突飞猛进的发展,给人类健康带来了新的解决方案。从理论上来说,干细胞能够治疗各类难治疾病,从修复、替代衰老损伤的角度为解决重大疾病带去新希望,在神经系统、分泌系统、细血管系统、免疫系统等领域均有发挥空间。另一方面,由于我国干细胞研究起步较晚,市场鱼龙混杂,不乏有用干细胞概念“唬人”的各类企业,具体到健康管理领域更是良莠不齐,使人们对干细胞技术的安全性和可靠性产生怀疑。“尽管干细胞已经成为未来的一大趋势,但人们对干细胞的误解仍然很深:或是认为它无所不能,或是认为它只是‘神话’,与此同时干细胞市场无序、健康管理方式五花八门,且人们也因不了解而对技术服务持有怀疑。”希诺神州CEO韩之海提到。希诺神州CEO 韩之海基于这种考虑,创办于2007年的北京汉氏联合生物技术股份有限公司(以下简称“汉氏联合”)将旗下事业部进行平行拆分,聚焦推进干细胞在各领域中的应用。具体包括以细胞存储和CDMO等为主要方向的汉氏生物、以研发干细胞新药和细胞外泌体产品为主要方向的汉氏药业、搭建各类联合医院及体检中心的汉氏医学,以及承接汉氏联合大健康事业部十多年深耕基础的上海希诺神州生命健康科技股份有限公司(以下简称“希诺神州”)。希诺神州集团总部基地 受访者供图经过一年的发展,希诺神州已经发展成为与汉氏联合齐头并进的集团之一。依托创新技术服务平台、生物信息大数据等技术基础,希诺成立上海汉氏方舟生物科技有限公司(以下简称“汉氏方舟”)及北京希诺赛尔健康科技推广有限公司两家全资子公司,共同致力于将生物科学技术工程化、工艺化、标准化,最终达到规模产业化及应用普及化,并普及到大健康未病先防和疾病治疗产业中,现业务涵盖美丽健康、生物信息大数据和生命工厂等。据了解,希诺神州已成立近150个以“汉氏方舟”为载体的科普中心,涵盖包括北京、上海杭州等一线城市及贵阳、青海等二三线城市。 法国两院院士坐镇,超30年干细胞研究经验1989年,韩忠朝来到法国医学科学院150研究所做博士后研究,自此投身于再生医学领域研究。之后的三十年,韩忠朝共发表论文500余篇,在《Lancet》《Nature Medicine》《Nature Communications》《Blood》等刊物发表300余篇SCI(H-index:58),获授权发明专利20余项,荣获国内科技奖30项。法国国家技术科学院院士、法国国家医学科学院外籍通讯院士 韩忠朝韩忠朝院士是法国国家技术科学院院士、法国国家医学科学院外籍通讯院士,受聘为国家干细胞工程技术中心主任、细胞产品国家工程研究中心主任及实验血液国家重点实验室学委主任。2007年,韩忠朝院士就踏上了科研转化之路,创办汉氏联合集团,致力于让研究成果惠及更多人。汉氏联合以细胞治疗和再生医学技术为核心,专注细胞科技产业领域的创新及发展。据QYResearch数据,2020-2026 年,中国干细胞医疗产业市场规模复合增长率约为15%,未来几年,中国干细胞医疗产业市场规模在全球市场规模中的占比将进一步上涨。机会巨大,但干细胞科研转化仍然面临五大问题。在韩忠朝院士看来,“首先是伦理方面,这关系到干细胞制备标准,如胚胎干细胞的获取和使用需要遵循伦理道德原则;二是技术,干细胞研究在我国起步较晚,又需要高度复杂的技术支持,目前仍然存在许多技术难题待攻克;三是安全性,我国从2017年开始受理干细胞新药审批,积累的真实世界实验数据还不足,细胞的致瘤性、免疫原性和异质性等需要科学评估监测;四是法律法规问题,需要遵循国家和地方法律法规,加强监督管理。”。“最后一个则是市场化问题,如果我们能够将科普工作提前,让百姓了解干细胞是什么、有何用、如何用,那么一旦在研发上取得新突破,就会缩短百姓的接收期,使更多人更快受益。”韩忠朝院士说。每一个新兴的事物都要遵循发展的逻辑,如何将科研结果成功转化、如何进行推广和普及等都是需要考虑的问题,这也是汉氏集团孵化希诺神州的一大原因。聚焦健康管理,以汉氏方舟为载体实现多种功能近年来,以个性化健康检测评估、养生咨询、疾病康复等为切入点的健康管理服务势头正猛。《健康中国2030规划纲要》中也明确提到,要持续推进覆盖全生命周期的预防、治疗、康复和自主管理一体化的国民健康信息服务。老龄化社会的加深、慢病发病率提高、人们健康意识的不断提高,伴随着人工智能、大数据、生物科技等新科技不断推陈出新,健康管理领域发展也迎来了前所未有的好时机。据动脉橙数据库显示,2022年至今,健康管理领域一级市场共发生76起投资事件。另据普华永道数据,中国为全球第二大健康产业市场,大健康市场规模在过去的数年中正以高达13%的年复合增长率增长。健康管理领域与所有人息息相关,但同样存在缺乏行业标准、公众认知度低、尚未形成完整服务链等痛点,使得像干细胞一类的新兴技术难以为公众知晓使用。因此,在韩忠朝院士看来,让希诺神州从市场化角度切入健康管理领域,不断普及干细胞知识和开发应用,对促进形成健康管理行业标准、推广干细胞使用惠及更多百姓等有重要作用。希诺神州通过快速收集和分析数据,不断加快产品升级和多元化体验,促使形成行业标准,最终实现健康管理体系的优化和提升;同时,希诺神州利用场景化定制满足不同需求,推动细胞服务向数字化、自动化迈进。具体而言,希诺神州具有三大业务板块,包括汉氏方舟、希诺赛尔(包含imcell健康美学空间、大健康产业园)及赛尔须弥。汉氏方舟汉氏方舟集科普、护肤、健康管理、休闲和鉴赏于一体,以人的生命健康为研究对象,布局大健康全产业链,打造出高定制型的全生命周期健康管理平台,为用户提供更系统便捷的健康管理服务。汉氏方舟创新技术服务平台包括健康指数评估平台、美丽健康技术项目和平台搭建CDM服务,同时搭建“我的细胞中心(MCC)”、“Life-GPS精准健康干预体系”及“IMCELL健康美学空间”,覆盖全生命周期健康管理。目前,汉氏方舟已在北京、上海、杭州、贵阳、青海等城市布局,“目前约有150个汉氏方舟科普中心,未来三年,我们将全面实现全国范围内五百家科普中心及健康美学空间的规模。”希诺神州CEO韩之海说。希诺赛尔希诺赛尔由imcell健康美学空间和大健康产业园构成。健康美学空间概念具有前瞻性,从产品导向跨越到健康生活服务。“健康美”不仅是一种积极的健康观念,也是未来抗衰老的新意识,新方法。健康美学空间依托高定制生物干预技术,打造出衰老辅助干预技术和产品,包括IMCELL、生物护肤技术产品、海曦谜语及口服健康技术产品等。大健康产业园以大健康生物医疗为依托,是集生物医药、医疗器械、医药研发、大健康数据、康养护理、技术交流、城市医疗科技、生物医药人才、智能制造和健康产业配套服务企业于一体的高品质创新型、大健康产业专业型科技产业园。基地项目建设一期用地97亩,建设体量为14万平方米,定位为“区域地标式科技产业园区”。赛尔须弥赛尔须弥(Sumi big data)是希诺神州集团基于须弥-ERP、须弥-Saas、须弥-健康管理等平台收集到的具有数据量大、数据多样性、真实有价值、处理速度快、长期持续性等特点的健康大数据。通过收集到的须弥大数据,希诺神州不断加快产品升级和优化,有望推动形成行业标准。希诺神州具有领先的研发优势,完备的研发生产平台,可提供研发生产一站式服务;拥有产业集群的细胞谷生态系统及高精尖研发团队,为企业提供创新性的工艺研发及生产服务。企业以高附加值技术输出取代单纯的产能输出,内容酒盖细胞产品CRO和CMO服务、临床研究、完整干细胞技术体系建立的解決方案。深入研究与成果转化两手抓,寻找志同道合伙伴共建健康管理新范式目前,全球范围内已经有十几种干细胞产品成功获批上市,对比来看,我国多数产品处于在研阶段。从应用角度来看,间充质干细胞适应症覆盖更为广泛,但由于价格昂贵、难以大规模商业化、应用范围有限等原因,已有产品难以大规模推广。另一方面,作为新兴产业的干细胞,受政策影响较深,且因为起步较慢,与国外领先研究有相当一段距离。无论是从研究、推广还是应用等方面来说,我们仍然有很长一段路要走。通过希诺神州可以在继续深入研究干细胞的同时,加快成果转化,使领先的技术能够快速惠及更多人群。希诺神州核心团队在大健康领域深耕数十年,具备健康、医疗、生物技术等领域相关知识,同时具备催化市场成熟的资深经验。总经理韩之海具备超十年的生命健康领域工作经验,参与了多项技术工程开发和产业转化工作,获得多项发明专利;同时聘请瑞典Uppsala university肿瘤生物学博士王家伦担任首席科技官,外籍大数据专家Raymond ASTRI担任首席技术官。“干细胞领域企业在成果转化中更要夯实基础研究,关键技术是要不来、买不来、讨不来的,必须要加强基础研究,催生颠覆性创新成果,攻克核心技术加强成果转化。围绕领域内关键核心技术,扑下身子、攥紧拳头,坚持不懈做下去,快速推进成果转化。加强领域内高科技人才储备,重视人才自主培养,培养高素质技术技能人才及能工巧匠。”韩忠朝院士说。“外部压力巨大,市场相对混沌,我们同时更需要志同道合的伙伴加入,共同面对具有挑战性的未来。”希诺神州CEO韩之海说。未来,希诺神州将继续完善布局,将各项业务合规化,启动“健康美学空间”项目布局,推进建设信息化平台,加速细胞产业化,赋能细胞药物智能智造。近期推荐声明:动脉网所刊载内容之知识产权为动脉网及相关权利人专属所有或持有。未经许可,禁止进行转载、摘编、复制及建立镜像等任何使用。动脉网,未来医疗服务平台
细胞疗法
2023-05-29
·生物谷
5月27日,第一届细胞生物医药技术与产业发展论坛活动在上海宝山高新区举行,此次论坛以“打造细胞科技新驱力,全面助力宝山北转型”为主题,汇聚政、学、研、医、商五个领域领导及专家学者,共话细胞行业研发进展,共探未来细胞产业发展新趋势。法国两院院士、国家干细胞工程技术研究中心主任、汉氏联合首席科学家韩忠朝,中国工程院院士、美国国家工程院外籍院士、解放军总医院生命科学院院长、全国政协委员付小兵,法国医学科学院院士、法国医学科学院972所研究所所长Georges UZAN,欧洲科学院院士、江苏省干细胞与生物医用材料重点实验室主任时玉舫,宝山区相关委办局、宝山高新区管委会出席论坛。大会现场开幕致辞宝山高新区管委会主任刘惠斌表示,园区多年来深耕生物医药产业,初步构建了医药器械、生物技术和新型医疗健康服务等特色产业集群,在上海乃至全国形成了品牌效应,产业竞争力逐步凸显。细胞生物医药是生物技术最前沿也是关乎人民健康的关键技术,园区将以此次论坛为契机,把握细胞生物这一细分赛道,以有力的政策支持、高效的创新服务和完善的创新体系,将生物医药产业不断做大做强。刘惠斌主任致辞法国国家技术科学院院士、法国国家医学科学院外籍通讯院士、国家干细胞工程技术研究中心主任韩忠朝教授表示:汉氏联合多年来在细胞再生医学领域做出了很多喜人的成果,近几年已经从研发、生产到终端服务形成了完整的生态链条,希诺神州集团作为根源于汉氏的一家全生命健康管理及产业园运营的新星企业,立足宝山,辐射全国,面向世界,正在尽全力践行北转型的使命。韩忠朝院士致辞宝山区推介丁建平主任推介区科创委主任丁建平介绍了宝山区的产业发展情况及招商政策。生物医药产业一直是宝山重点发展的战略性新兴产业。欢迎更多企业家朋友选择宝山、建设宝山、深耕宝山,与宝山共同成长、共赢未来。基地签约仪式借助第一届细胞生物医药技术与产业发展论坛的良好平台,现场举行了驻产业基地签约仪式,推动更多企业入驻国际综合性细胞生物医药产业基地,促进共同发展。天津昂赛细胞基因工程有限公司、北京汉氏联合生物技术股份有限公司代表与宝山高新区管委会进行签约。上海希诺神州生命健康科技股份有限公司,分别与华东理工大学商学院心脑科学实验室、上海工程技术大学材料工程学院、上海师范大学、中科睿极、工商银行宝山支行进行产学研及金融合作项目签约。院士专家讲堂来自学术界、产业界、医疗界、资本界、法律界等专家齐聚一堂,聚焦生物医药与智慧诊断领域,共同探讨行业面临的机遇和挑战,未来产业布局与投资方向,为科创宝山贡献智慧,为与会来宾呈现了一场细胞生物医药的学术盛宴。韩忠朝院士作《间充质干细胞产品的研发与应用》分享付小兵院士作《初心与使命:中国特色创面修复学科体系构建的回顾与展望》分享Georges UZAN院士作《循环肿瘤细胞分析对临床肿瘤学的价值》分享时玉舫院士作《组织炎症微环境与再生》分享活动现场,嘉宾们围绕《干细胞与再生医学》和《异基因移植与免疫治疗》展开主题演讲。陶勇教授作《外泌体用于眼部疾病的治疗研究》分享韩英教授作《肝病的干细胞治疗思考》分享周斌教授作《谱系示踪与干细胞研究》分享郭全义教授作《干细胞治疗骨关节疾病研究进展》分享李宗金教授作《间充质干细胞来源的外泌体囊泡在组织损伤修复中的治疗应用》分享李银萍教授作《间充质干细胞衍生物对脑缺血的治疗作用》分享Jean François Henri ROSSI教授作《Immune precision medicine from allogeneic transplantation》分享Stéphane BREZILLON教授作《Differential MMP-14 targeting by Biglycan, Decorin, Fibromodulin and Lumican Unraveled by In Silico Approach》分享孙锋先生作《近期中国细胞基因治疗行业投融资情况回顾及未来展望》分享Céline GIGANT教授作《Immune properties of umbilical cord mesenchymal stromal cells in cell therapy context》分享Martin VILLALBA GONZÁLEZ教授作《Non-genetically modified,CAR-like,NK cells》分享张君总监作上海宝山高新技术产业园区推介汪英颖教授主持《细胞产业创新与临床转化》何志旭教授作《CAR-NK免疫细胞疗法研发及应用进展》分享韩之波教授作《围产期干细胞药物研发与转化》分享管峥教授作《脱细胞牙髓涂层壳聚糖支架对牙髓干细胞成骨分化的体内外实验研究》分享Loïc REPPEL教授作《Targeting disialoganglioside GD2 with chimeric antigen receptor-redirected T cells in lung cancer》分享张智勇教授作《干细胞/外泌体的数字化、自动化、规模化、封闭化、活性化(DASEA)生物智造平台的研发及转化——从实验室研究到临床应用》分享【圆桌论坛一】韩之波教授、曹晓沧教授、张磊教授、李宗金教授、张智勇教授、何志旭教授、张磊升教授共同参加《产学研合作助力细胞药物转化》论坛汤红明教授作《加快干细胞产业高质量发展打造生物经济新引擎》分享张磊教授作《中国基因治疗的现状与未来》分享华国强教授作《机理图解:如何通过使用创新的联合治疗法来避免由骨替代物的矿物块阻止的新形成的血管》分享吴朝晖教授作《干细胞来源合规的思考与应对》分享Rana SMAIDA教授作《Development of an innovative advanced therapy medicinal product combining stem cells and an implantable medical device for regenerative medicine》分享周芙玲教授作《脐带血微移植治疗老年AML患者》分享【圆桌论坛二】以《中国细胞医药产业的突围》为主题,由王家伦教授、郑杨副主任、傅大煦会长、许敬东律师、沈俊先生、吴朝晖副理事长、韩之海先生参与讨论。最后,希诺神州集团总经理韩之海先生以《立足上海,面向全国建立生命科学科普中心全国网络》为题,从生物医药技术创新研究、成果转化、希诺神州集团责任和愿景,以及全球网络布局等方面进行了阐述,为与会嘉宾在相关领域的发展带来了不同视角的新观念。展位展示及会场盛况大会闭幕式希诺神州集团副总经理、IMCELL健康美学空间创始人杨女士在论坛闭幕仪式上表示:“短暂的两天,我们相聚在宝山这块宝地,见证了宝山的“起步即是冲刺”的奋斗姿态,以及支持科创之花”结出更多产业之果,形成蓬勃姿态的决心和毅力。两天的会议内容更是务实、全面,我们看到了再生医学行业的蓬勃发展和可期的未来。大会结束之际,让我们共同祝愿,细胞产业的领先技术和未病先防的新服务,能够走进千家万户,造福更多的老百姓”。大会合影留念“第一届细胞生物医药技术与产业发展论坛”与宝山高新区的战略定位高度契合。细胞与基因产业近年来高速发展,细胞治疗技术日臻完善,发展细胞与基因产业,不仅是经济发展的需要,更是人民健康生活、幸福生活的需要。把握时机、抓住机遇,宝山区和希诺神州集团将为创业者提供更广阔的发展空间和更优质的服务,让他们在创业的道路上走得更远、更稳、更成功。END希诺神州上海宝山基地汉氏方舟是希诺神州集团根据人类健康需求而构建的健康科普及细胞技术服务的平台。设置线上体验平台和线下科普中心,通过线上+线下的全方位模式,为用户提供全面的健康管理服务,提供多样化、一站式健康管理方案。从现代预防医学,结合传统中医治未病理念,融合细胞再生医学,汉氏方舟从生命健康出发,维护人体细胞的健康,延缓细胞衰老,保障全身心健康,守护您与家人的健康。
细胞疗法高管变更
100 项与 汉氏药业(北京)股份有限公司 相关的药物交易
登录后查看更多信息
100 项与 汉氏药业(北京)股份有限公司 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2024年10月06日管线快照
管线布局中药物为当前组织机构及其子机构作为药物机构进行统计,早期临床1期并入临床1期,临床1/2期并入临床2期,临床2/3期并入临床3期
临床1期
1
1
临床2期
登录后查看更多信息
当前项目
| 药物(靶点) | 适应症 | 全球最高研发状态 |
|---|---|---|
脐带间充质干细胞注射液(天津昂赛) | 成人呼吸窘迫综合征 更多 | 临床2期 |
Umbilical Cord Mesenchymal Stem Cells(Tianjin Amcellgene Engineering) | 急性缺血性卒中 更多 | 临床1期 |
登录后查看更多信息
药物交易
使用我们的药物交易数据加速您的研究。
登录
或

转化医学
使用我们的转化医学数据加速您的研究。
登录
或

营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或

科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或

投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或

融资
发掘融资趋势以验证和推进您的投资机会。
登录
或

标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
