预约演示
更新于:2025-05-07
Beijing Xuanzhu Combio Co., Ltd.
北京轩竹康明生物科技有限公司|私营公司|2021|中国北京市
北京轩竹康明生物科技有限公司|私营公司|2021|中国北京市
更新于:2025-05-07
概览
关联
3
项与 北京轩竹康明生物科技有限公司 相关的临床试验CTR20230726
评价KM501双抗ADC在HER2表达、扩增或突变的晚期实体瘤受试者中的安全性、耐受性、药代动力学特征和有效性的单臂、开放、多中心的I期临床研究
Ia期:
主要目的:
评价KM501在HER2表达、扩增或突变的晚期实体瘤受试者中的安全性和耐受性。
确定KM501的最大耐受剂量(MTD)(如有),以及II期临床推荐剂量(RP2D)。
次要目的:
评价KM501在HER2表达、扩增或突变的晚期实体瘤受试者中的药代动力学特征。
评价KM501在HER2表达、扩增或突变的晚期实体瘤受试者中的有效性。
评价KM501在HER2表达、扩增或突变的晚期实体瘤受试者中的免疫原性。
Ib期:
主要目的:
评价KM501单药治疗在HER2表达、扩增或突变的特定类型肿瘤受试者中的有效性。
次要目的:
评价KM501单药治疗在HER2表达、扩增或突变的特定类型肿瘤受试者中的安全性和耐受性。
评价KM501单药治疗在HER2表达、扩增或突变的特定类型肿瘤受试者中的药代动力学特征。
评价KM501单药治疗在HER2表达、扩增或突变的特定类型肿瘤受试者中的免疫原性。
探索性目的:
探索HER2表达、扩增或突变与KM501抗肿瘤疗效之间的关系。
开始日期- |
申办/合作机构 北京轩竹康明生物科技有限公司 [+1] |
CTR20230600
评估KM602在晚期实体瘤患者中的安全性、耐受性、药代动力学特征和初步疗效的开放、多中心I期临床研究
主要目的:评价KM602在晚期实体瘤患者中的安全性和耐受性,确定KM602的最大耐受剂量(MTD)(如有)以及II期临床推荐剂量(RP2D);
次要目的:初步评估KM602在晚期实体瘤患者中的抗肿瘤活性,研究KM602在晚期实体瘤患者中的药代动力学特征,以及KM602的免疫原性;
探索性目的:探索研究与KM602治疗相关药效学及预测性生物标志物。
开始日期2023-04-06 |
申办/合作机构 北京轩竹康明生物科技有限公司 [+1] |
CTR20220774
评价KM257在HER2阳性或表达的晚期实体瘤患者中的安全性、耐受性、药代动力学特征和有效性的单臂、开放、多中心的I期临床研究
Ia期
主要目的:
1. 评价KM257在HER2阳性或表达的晚期实体瘤患者中的安全性和耐受性。
2. 确定KM257的最大耐受剂量(MTD)(如有),以及II期临床推荐剂量(RP2D)。
次要目的:
1. 确定KM257在HER2阳性或表达的晚期实体瘤患者中的药代动力学特征。
2. 评价KM257在HER2阳性或表达的晚期实体瘤患者中的有效性。
3. 评价KM257在HER2阳性或表达的晚期实体瘤患者中的免疫原性。
探索性目的:
1. 探索HER2阳性或表达的晚期实体瘤患者中细胞因子血液浓度水平。
Ib期
主要目的:
1. 评价KM257单药或联合治疗在HER2表达或扩增的特定类型肿瘤受试者中的有效性。
次要目的:
1. 评价KM257单药或联合治疗在HER2表达或扩增的特定类型肿瘤受试者中的安全性和耐受性。
2. 评价KM257单药或联合治疗在HER2表达或扩增的特定类型肿瘤受试者中的药代动力学特征。
3. 评价KM257单药或联合治疗在HER2表达或扩增的特定类型肿瘤受试者中的免疫原性。
开始日期2022-05-12 |
申办/合作机构 北京轩竹康明生物科技有限公司 [+1] |
100 项与 北京轩竹康明生物科技有限公司 相关的临床结果
登录后查看更多信息
0 项与 北京轩竹康明生物科技有限公司 相关的专利(医药)
登录后查看更多信息
2
项与 北京轩竹康明生物科技有限公司 相关的新闻(医药)2023-10-30
关注并星标CPHI制药在线——10.31-11.1月线下会议论坛推荐—— 10月27日,中国国家药品监督管理局药品审评中心(CDE)官网公示,由石药集团全资附属公司津曼特生物和康宁杰瑞共同申请的重组人源化抗HER2双特异性抗体注射液(KN026)拟纳入突破性治疗品种,拟定适应症为联合化疗药物用于一线标准化疗(曲妥珠单抗联合化疗)失败的HER2阳性局部晚期、复发或转移性的胃癌(包括胃-食管结合部腺癌)。 图片来源:CDE官网 KN026是康宁杰瑞采用具有Fc异二聚体平台技术(CRIB)开发的抗HER2双特异性抗体,可同时结合HER2的两个非重叠表位,导致HER2信号阻断。研究显示,该产品展示出较高的亲和力,在HER2阳性肿瘤细胞株中具备优效的肿瘤抑制作用。同时,KN026对HER2中低表达肿瘤和曲妥珠单抗抗性细胞株也有抑制作用。 2021年8月,康宁杰瑞与石药集团全资附属公司津曼特生物就KN026签订了在中国内地的开发及商业化授权协议。根据协议条款,津曼特生物将获得KN026在中国内地(不包括中国香港、中国澳门及中国台湾地区)在乳腺癌、胃癌适应症上的排他性开发与独占性商业化许可权。为此,康宁杰瑞有权收取最高人民币10亿元的预付款及里程碑付款。 此前,KN026已在二线治疗HER2表达晚期胃癌或胃食管结合部癌的Ⅱ期临床研究中取得积极结果,并在国际肿瘤领域知名期刊European Journal of Cancer上发表。本研究共入组了45例患者,25例患者接受过至少一次肿瘤影像学评估,其中14例评估为部分缓解(PR),5例评估为疾病稳定(SD),5例评估为疾病进展(PD),1例无法评估,客观缓解率(ORR)高达56%,且能够获得长期的疾病缓解;中位缓解持续时间(DOR)为9.7个月,中位无进展生存期(PFS)和总生存期(OS)分别高达8.3个月和16.3个月。对于既往接受过曲妥珠治疗后进展的14例患者,仍然有较好的治疗效果。 目前,KN026正在中国、美国开展多项不同阶段临床试验,适应症包括乳腺癌、胃癌/胃食管结合部癌等。2022 SABCS公布了KN026联合多西他赛一线治疗HER2阳性复发/转移性乳腺癌的Ⅱ期临床研究数据,客观缓解率(ORR)为76.4% ,中位缓解持续时间(mDoR)为24.0个月,疾病控制率(DCR)为100%。今年5月,KN026联合注射用多西他赛(白蛋白结合型)用于一线治疗HER2 阳性复发转移性乳腺癌的Ⅲ期临床试验申请,在中国获批。 非重叠表位HER2双抗 HER2是一个在实体瘤治疗领域,特别是胃癌和乳腺癌治疗领域相当热门的靶点,已有多款靶向药物上市,最知名的就是罗氏的曲妥珠单抗和帕妥珠单抗,其中赫赛汀(曲妥珠单抗)是1998年上市的全球首款HER2抗体。但随着研究的进展,人们发现,曲妥珠单抗通过抗体依赖细胞介导的细胞毒性作用(ADCC)杀伤HER2阳性癌细胞,不足以完全消灭癌细胞和阻断下游信号通路。HER2蛋白在体内的作用机制很特殊,它是一个"孤儿受体",也就是说,HER2没有与它相应的配体,它通过和自己或其他HER家族成员形成二聚体,从而激活下游信号发挥作用。 HER2二聚体激活的下游信号通路 图片来源:参考来源2 HER2蛋白由胞外结构域、跨膜结构域及含有酪氨酸蛋白激酶(RTK)活性的胞内结构域三部分组成。胞外部分又包含I~IV 4个结构域。曲妥珠单抗可以结合结构域IV,而帕妥珠单抗结合的是于HER2二聚体形成息息相关的结构域II。这两款单抗的结合位点不同,为开发联用方案提供了可能。到2017年,在证实了曲妥珠单抗+帕妥珠单抗+化疗方案的长期疗效优越性后,FDA批准上市了这一治疗方案。在靶向HER2不同位点的可行的背景下,非重叠表位HER2双抗登上了舞台。从目前 HER2 双抗的临床表现看,针对 HER2 表达的晚期实体瘤,双特异性抗体的临床药效有望优于单抗。2020 年全球 HER2 靶点的单抗治疗药物市场规模超过 110 亿美元,预计未来 HER2 双抗药物上市后,有望在这超百亿美元的市场中迅速放量,市场潜力巨大。 HER2双抗全球研发情况 HER2双特异性抗体作为HER2靶点的下一代药物,是国内外各大药企研发的重点,全球尚无HER2/HER2双特异性抗体药物上市,均处于临床阶段。Zymeworks/百济神州的ZW25是首 个进入到Ⅲ期临床阶段的HER2双抗,康宁杰瑞/石药集团的 HER2 双抗 KN026 紧随其后,也已经进入Ⅲ期临床。除此之外,国内天广实的 MBS301和轩竹生物的KM257 也已经进入 I 期临床阶段。目前HER2双抗有广泛的适应症布局包括乳腺癌、胃癌、胆管癌和表达HER2的实体瘤。 进入临床阶段的HER2双抗 Zanidatamab(ZW25) Zanidatamab(泽尼达妥单抗)是Zymeworks的主要候选产品,且基于该公司特有的双特异性抗体开发平台Azymetric进行开发。该药物是一种可以同时结合HER2靶点上两个非重叠的抗原表位的双特异性抗体,从而可以双重阻断HER2信号、增强结合并去除细胞表面的HER2蛋白以及导致抗肿瘤活性增强的强效效应器功能。 值得一提的是,美国FDA已经授予了Zanidatamab突破性疗法认定(BTD),用于治疗既往治疗过的HER2基因扩增性胆管癌(BTC)患者,还授予了Zanidatamab 2个快速通道资格(BTD),一个是单药治疗难治性BTC,另一个是联合标准护理化疗一线治疗胃食管腺癌(GEA)。此外,美国FDA还授予了Zanidatamab治疗胆管癌、胃癌和卵巢癌的孤儿药资格(ODD)。在欧盟,EMA也授予了Zanidatamab治疗胆管癌和胃癌的ODD。 2018年11月,百济神州与Zymeworks公司就两款在研HER2靶向双特异性抗体药物ZW25和ZW49的临床开发和推广达成合作。这项授权合作涉及金额高达约4.3亿美元,百济神州也由此获得这两款候选药物在亚洲(日本除外)、澳大利亚和新西兰的开发和推广的独家授权。 百济神州在今年ASCO大会上口头报告了泽尼达妥单抗治疗胆管癌和乳腺癌的Ⅱ期研究结果。泽尼达妥单抗治疗既往经治的HER2扩增性胆道癌的关键性Ⅱb期HERIZON-BTC-01研究数据显示,在HER2阳性患者中,总体的疾病控制率为68.8%。客观缓解率(ORR)为41%,中位缓解持续时间(DOR)为12.9个月。Zanidatamab联合多西他赛作为晚期HER2阳性乳腺癌患者的一线治疗的Ib/II期研究结果显示,在33例可评估疗效的患者中,经证实的ORR达到了90.9%,6个月PFS率达90%以上,一年PFS率达73%。 据 Insight 数据库,目前 ZW25 已经启动了全球多中心 III 期临床,其中国部分由百济启动。 MBS301 MBS301是天广实基于其独有的ADCC增强抗体平台及多特异性抗体平台自主研发的HER2/HER2双表位双特异性抗体,也是全球首个岩藻糖全敲除的双功能抗体,能够同时结合HER2抗原的D2和D4结构域,从而起到帕妥珠和曲妥珠两个单抗药物联用的效果。而岩藻糖敲除又进一步增强了其ADCC抗肿瘤活性。独特的作用机制使得MBS301成为目前全球临床开发阶段针对HER2阳性乳腺癌和胃癌实验药物中的最优品种。 天广实将MBS301的临床开发重点放在胃癌和胃肠道肿瘤上,目前正在中国进行I期临床试验,以评估MBS301对HER2阳性转移性胃癌、胆管癌、胰腺癌及其他实体瘤的疗效,尚无临床结果公布。 KM257 KM257 为重组抗 HER2 结构域 II 和结构域 IV 双特异性抗体,是轩竹生物依托于旗下大分子创新药公司轩竹康明自主研发的 Mebs-lg(抗体编辑的双特异性抗体)平台和 Mab-Edit(抗体编辑)技术平台诞生的 HER2/HER2 双特异性抗体,机制创新,靶向 HER2 的两个不同结构域(结构域 II 和结构域 IV)的双特异性抗体,拥有极强的创新性。其通过阻碍 HER2 蛋白与其他 HER 家族成员的异源二聚化,从而阻止信号的有效传递,达到抑制肿瘤细胞的增殖或诱导其凋亡的作用。据四环医药官方信息,KM257 具有稳定性强、有效性高的特点,具备成为 Best-In-Class 药物的潜质。 KM257开展用于HER2+中高表达的晚期实体瘤治疗的临床试验申请已成功获得中国国家药品监督管理局的批准,目前KM257已进入临床I期阶段。 参考来源: 1. CDE官网 2. Iqbal N, Iqbal N. Human Epidermal Growth Factor Receptor 2 (HER2) in Cancers: Overexpression and Therapeutic Implications. Mol Biol Int. 2014 3. Results from the pivotal phase (Ph) 2b HERIZON-BTC-01 study: Zanidatamab in previously-treated HER2 amplified biliary tract cancer (BTC). 4. Jiong Wu, et al. KN026 in combination with docetaxel as neoadjuvant treatment for HER2-positive early or locally advanced breast cancer: A single arm, multicenter, phase 2 study. SABCS, 2022. OT2-16-04. 5. Qingyuan Zhang, et al. Efficacy and safety results of KN026, a HER2-targeted bispecific antibody combined with docetaxel in first-line treatment of HER2-positive recurrent/metastatic breast cancer. SABCS, 2022. PD18-08. 来源:CPHI制药在线声明:本文仅代表作者观点,并不代表制药在线立场。本网站内容仅出于传递更多信息之目的。如需转载,请务必注明文章来源和作者。投稿邮箱:Kelly.Xiao@imsinoexpo.com▼更多制药资讯,请关注CPHI制药在线▼点击阅读原文,进入智药研习社~
引进/卖出突破性疗法临床3期临床2期
2023-03-11
·医药地理
扫描二维码即可下载《数图药讯》2023年第11期目 录政策解读1. 国家药监局:印发2023年药品检验能力验证计划2. 国家医保局:2022年全国通过省级医药集中采购平台网采订单总金额10615亿元,同比增275亿元3. 国家医保局:医保部门对患者住院天数无限制性政策4. 浙江杭州市医疗保障管理服务中心发布:关于2023年第一季度集中受理浙江省、杭州市医疗保障医药机构协议定点申请的通告5. 江西省药监局:制定《江西省药物非临床安全性评价机构与药物临床试验机构监督管理办法》6. 云南省科技厅:关于2023年生物医药领域第一批科技计划拟立项项目的公示7. 陕西药监局:产创融合 赋能“秦药”秦创原创新药品医疗器械成果转化路演活动在西安举办行业动态1. 药讯动态:重磅获批和重磅临床2. 药企动态:市场动态零售品类数据洞见1. 甲地孕酮零售样本市场销售分析2. 甲地孕酮零售放大市场销售分析政策解读1、国家药监局:印发2023年药品检验能力验证计划3月9日,根据《国务院办公厅关于全面加强药品监管能力建设的实施意见》(国办发〔2021〕16号)和《国家药监局综合司关于加强和改进药品检验检测能力验证工作的通知》(药监综科外〔2020〕67号)要求,为提升新形势下药品、医疗器械、化妆品检验检测机构能力和水平,国家药监局制定了2023年药品检验能力验证计划,该计划由中国食品药品检定研究院负责组织实施。药品检验能力验证是有效提高实验室能力的重要手段、是药品安全考核工作重要组成部分。请各省级局积极组织、协调、指导所属行政区域内国家药监局重点实验室和省、市、县级检验检测机构、实验室参加能力验证计划;同时组织、指导行政区域内省级检验检测机构加强对市县级检验检测机构的业务指导,提升参加药品检验能力验证的参与率和满意率。2、国家医保局:2022年全国通过省级医药集中采购平台网采订单总金额10615亿元,同比增275亿元3月9日,国家医保局发布2022年医疗保障事业发展统计快报。2022年,全国通过省级医药集中采购平台网采订单总金额10615亿元,比2021年增加275亿元。其中,西药(化学药品及生物制品)8618亿元,比2021年增加303亿元;中成药1997亿元,比2021年减少28亿元。医保目录内药品网采订单金额为7945亿元,占网采订单总金额74.8%。3、国家医保局:医保部门对患者住院天数无限制性政策近日,有患者曾反映“部分医院为提高病床周转率而规定患者15天必须出院的问题”。国家医保局关于大病医保患者病床周转率的政策做出回应。国家医保局在此次回应中明确,国家医保局和各级医保部门对参保患者住院天数无限制性政策,享受医保待遇也与患者住院天数没有关系。国家医保局表示,大病保险在基本医保报销基础上,对大病患者发生的高额医疗费用给予进一步保障。各地普遍采取分段阶梯式报销,费用越高,大病保险报销比例越高。各地普遍将大病患者年度内发生的政策范围内住院、门诊大额医疗费用累计计算,再按政策规定计算报销金额。4、浙江杭州市医疗保障管理服务中心发布:关于2023年第一季度集中受理浙江省、杭州市医疗保障医药机构协议定点申请的通告3月9日,根据《医疗机构医疗保障定点管理暂行办法》(国家医疗保障局令第2号)、《零售药店医疗保障定点管理暂行办法》(国家医疗保障局令第3号)、《浙江省医疗保障局关于印发浙江省医疗保障定点医疗机构和定点零售药店确定评估细则的通知》(浙医保发〔2021〕46号)文件要求,结合杭州市医疗保障定点协议管理有关规定,杭州市医疗保障管理服务中心发布了2023年第一季度集中受理浙江省省级、杭州市医保协议定点医疗机构及零售药店申请的相关事宜通告。5、江西省药监局:制定《江西省药物非临床安全性评价机构与药物临床试验机构监督管理办法》3月8日,为更好贯彻落实属地监管责任,加强江西省药物研究机构监督管理,提升江西省药品注册研发能力,保障药品“设计”质量,江西省药监局制定印发了《江西省药物非临床安全性评价机构与药物临床试验机构监督管理办法》(以下简称《办法》)。《办法》强化了风险管理理念和机构主体责任意识,明确了研究机构监督管理适用范围、各部门职责,细化了监管要求,从监管形式、监管内容、现场检查流程、检查结果处理等方面明确了程序和要求。《办法》明晰了省市药监部门和卫生健康主管部门对药物临床试验机构的监管职责。《办法》还专门配套了各相关监督检查标准及其评定标准,增强了检查的规范性和实操性。6、云南省科技厅:关于2023年生物医药领域第一批科技计划拟立项项目的公示3月7日,根据《云南省科技厅科技计划项目管理办法》、《云南省科技厅科技计划项目库管理办法》等规定,经省科技厅2023年3月7日厅务会议和厅党组会议审议通过,现将2023年生物医药领域第一批科技计划拟立项项目进行公示。表:2023年生物医药领域第一批科技计划拟立项项目7、陕西药监局:产创融合 赋能“秦药”秦创原创新药品医疗器械成果转化路演活动在西安举办3月9日,由陕西省药监局与西咸新区开发建设管理委员会主办,西咸新区市场监管局(药监分局)和秦创原创新促进中心承办的秦创原创新药品医疗器械成果转化路演活动在西咸新区举办。此次活动主题为“产创融合 赋能‘秦药’”,采取线上直播和现场参与的方式举行,旨在探索建立研发端与生产端的创新合作模式,以“创新链”赋能“产业链”,助推生产企业药物研究产创融合,促进我省医药产业高质量发展。大会首先对创新药械相关政策发布作了介绍,主要包括《药品注册金钥匙》项目、西咸新区医药协同研发服务平台建设情况及新区医药产业扶持政策、秦创原立体联动孵化器总基地,以及第六届中国医疗器械创新创业大赛有关情况等。行业动态1、药讯动态:重磅获批和重磅临床最近重磅获批1. 赛诺菲(SNY.US)度普利尤单抗新适应症的上市申请获中国药监局受理。2. 中科院上海药物所与海和药物研发的用于治疗具有间质-上皮转化因子(MET)外显子14跳跃突变(METex14跳变)的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者的抗肿瘤1类新药谷美替尼片通过中国药监局附条件获批上市。3. 合源生物科技(天津)有限公司用于治疗成人复发或难治性B细胞型急性淋巴细胞白血病(r/r B-ALL)的赫基仑赛注射液(CNCT19细胞注射液,Inaticabtagene Autoleucel)IND申请已获美国食品药品监督管理局(U.S.FDA)许可。4. 先声诊断的CYP2C19试剂盒获得国家药品监督管理局(NMPA)第三类医疗器械注册证,这也是国内首个基于飞行时间质谱技术进行药物基因组(PGx)检测的获证试剂盒,可用于指导心脑血管疾病常用药物(如氯吡格雷)的临床精准用药。最近重磅临床1. 华东医药自主研发的GLP-1R激动剂HDM1002片向CDE申报临床。HDM1002是第7款申报临床的国产小分子GLP-1R激动剂。2. 北京轩竹康明生物科技有限公司研发的适用于治疗HER2阳性/表达、扩增或突变的局部晚期/转移性实体瘤,包括HER2低表达的相关晚期肿瘤的双抗ADC药物KM501获得临床试验批件)。3. 礼来宣布Solanezumab用于治疗有淀粉样斑块但无疾病临床症状(又称为阿尔茨海默病临床前阶段)患者的III期A4研究未达主要终点和关键次要终点,即Solanezumab不能减缓阿尔茨海默病(AD)引起的认知衰退或降低其进展为症状性AD的风险,也无法清除斑块或阻止淀粉样蛋白积聚。4. 上海华奥泰生物药业股份有限公司与华博生物医药技术(上海)有限公司自主研发的创新候选药物HB0025注射液近日获国家药监局(NMPA)批准开展多项针对晚期实体瘤的临床试验。2、药企动态:市场动态1. 3月7日,康方生物宣布,公司旗下康方药业有限公司将与上海医药集团股份有限公司(简称“上海医药”)携手,共同推进公司自主开发的全球首创PD-1/CTLA-4双特异性抗体新药开坦尼®(卡度尼利单抗注射液)联合上海医药自主开发的靶向CDK4/6抑制剂SPH4336片,针对高分化脂肪肉瘤(WDLS)/去分化脂肪肉瘤(DDLS)等肿瘤适应症的联合疗法开发。2. 3月7日,F-star宣布,美国外国投资委员会(“CFIUS”)批准中国生物制药全资附属公司invoX以现金约1.61亿美元收购F-star公司。通过收购,中国生物制药获得该公司新一代双特异性抗体平台以及3款处于临床阶段的双特异性抗体(FS118、FS222和FS120)。其中,FS118是一种靶向PD-L1及LAG-3的双检查点抑制剂,目前正在Ⅱ期临床中用于治疗头颈部癌症患者;FS222是一款靶向CD137(4-1BB)及PD-L1的双抗药物;FS120是一款靶向OX40及CD137的双重激动剂。零售品类数据洞见1、甲地孕酮零售样本市场销售分析图1:甲地孕酮零售(样本市场)销售额图2: 甲地孕酮零售(样本市场)地区销售额*数据来源:中国医药工业信息中心 中国药品零售数据库RPDB 样本药店数据 2、甲地孕酮零售放大市场销售分析图3: 甲地孕酮零售(放大市场)销售额图4: 甲地孕酮零售(放大市场)企业销售分析*数据来源:中国医药工业信息中心 中国药品零售数据库RPDB 样本药店数据来源:医药地理、中国政务网、国家药监局、网易、新浪、澎湃等。END如需获取更多数据洞察信息或公众号内容合作,请联系医药地理小助手微信号:pharmadl001
带量采购并购申请上市一致性评价
100 项与 北京轩竹康明生物科技有限公司 相关的药物交易
登录后查看更多信息
100 项与 北京轩竹康明生物科技有限公司 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2025年08月20日管线快照
无数据报导
登录后保持更新
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
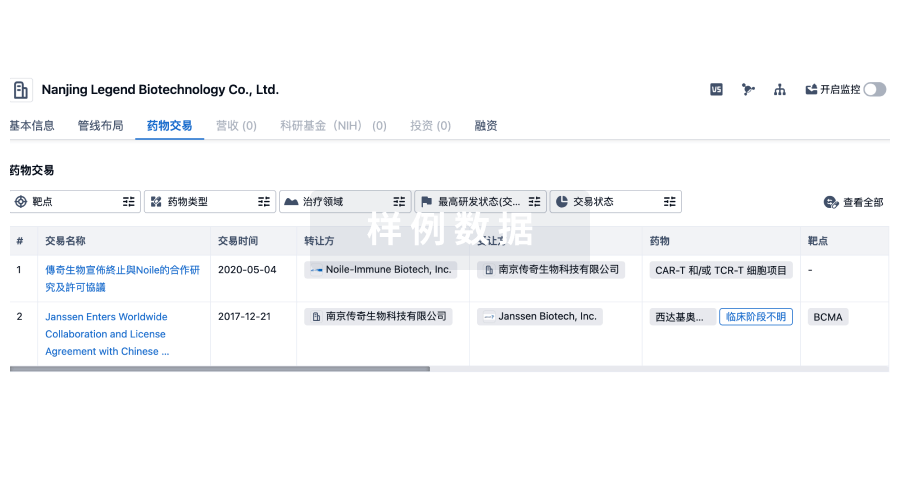
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
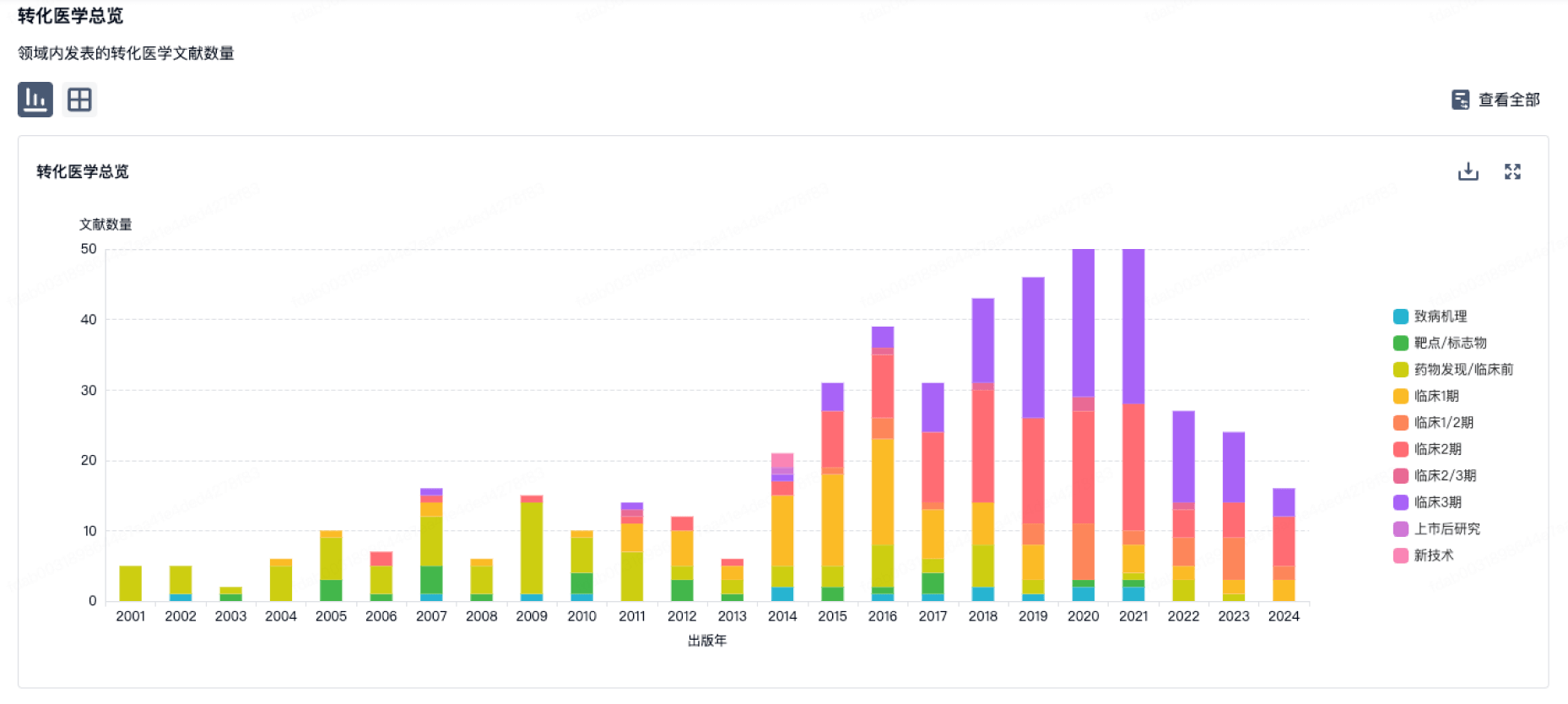
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
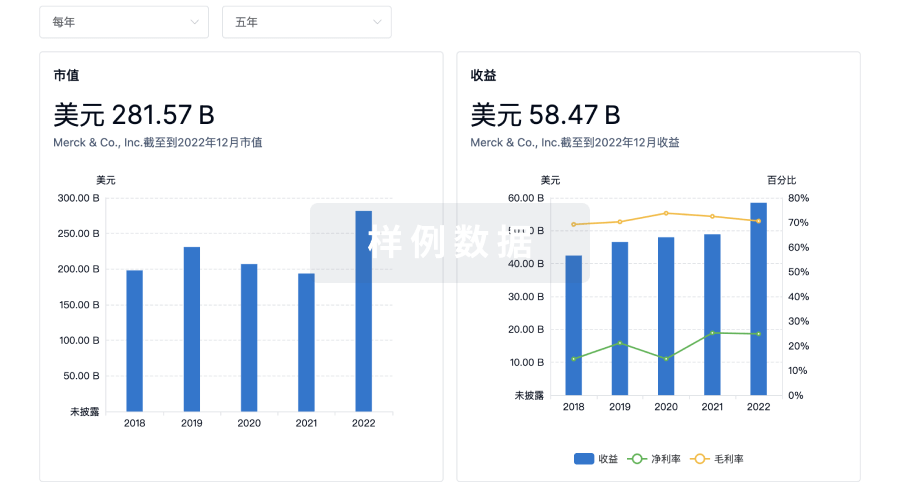
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
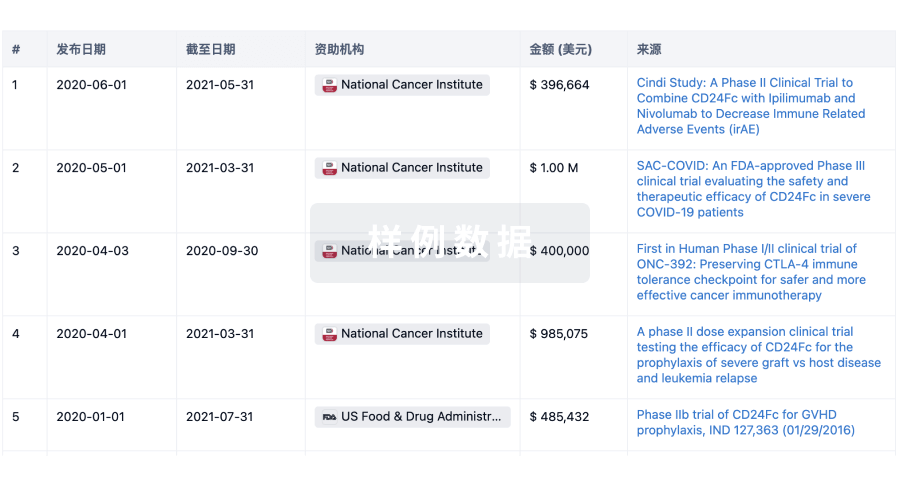
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
Eureka LS:
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用