靶点- |
作用机制- |
|
|
|
非在研适应症- |
最高研发阶段临床前 |
首次获批国家/地区- |
首次获批日期- |
靶点- |
作用机制- |
|
|
|
非在研适应症- |
最高研发阶段临床前 |
首次获批国家/地区- |
首次获批日期- |
靶点- |
作用机制- |
|
|
|
非在研适应症- |
最高研发阶段临床前 |
首次获批国家/地区- |
首次获批日期- |
一项多中心、单臂、开放性设计的验证性临床研究评价异硫蓝注射液用于早期乳腺癌患者前哨淋巴结示踪的有效性和安全性
主要目的:评价异硫蓝注射液用于早期乳腺癌患者前哨淋巴结示踪的有效性
次要目的:评价异硫蓝注射液用于早期乳腺癌患者前哨淋巴结示踪的安全性
100 项与 广东和博制药有限公司 相关的临床结果
0 项与 广东和博制药有限公司 相关的专利(医药)
广东和博制药有限公司于今年2月获批上市的异硫蓝注射液——博林兰®近期主动下调价格,由8860元/支的挂网价格下调到5980元/支,降幅近30%。
据悉,异硫蓝注射液是一种示踪剂,用于淋巴造影的辅助,最早于1981年美国上市,国内无厂家获批。
广东和博制药有限公司(下称“和博制药”)于2022年3月启动3类仿制申报,产品获批后填补国内市场空白。为响应国家让医疗资源造福患者号召,和博制药于近期主动下调价格,这也是自该药物上市以来首次调价。
值得关注的是,8月27日,国家医保局正式公布《2024年国家基本医疗保险、工伤保险和生育保险药品目录调整通过形式审查的申报药品名单》。249个目录外药品通过形式审查,广东和博制药自主研发的异硫蓝注射液在列。
根据2022年10月在《中华医学杂志》英文版上发表的《临床评价国产首仿异硫蓝注射液对早期乳腺癌前哨淋巴结示踪的有效性和安全性:一个多中心、单臂、开放性验证试验(CSBrS-024)》,认为国产首仿异硫蓝注射液“用于中国早期乳腺癌患者前哨淋巴结活检安全有效”。
相关研究显示,博林兰®前哨淋巴结示踪成功率为94%,前哨淋巴结示踪准确率为96%,淋巴管示踪成功率98%,研究中未发生与研究药物相关的不良反应,亦未发生注射部位坏死现象。作为前哨淋巴结活检的理想示踪剂,博林兰®将创造巨大的医疗价值。
和博制药于2013年落户中山火炬开发区国家健康基地,在上海张江科学城建有研发中心,并与中山大学建立战略合作关系。和博制药坚持产学研一体发展模式,以首仿药推动创新药双轮驱动发展。主要聚焦国内“首仿”药品、二类新药及创新药,掌握糖类药物制备及质量控制关键技术和手性药物制备关键技术,多次上榜粤港澳大湾区生物科技创新50强,累计获得国内外发明专利授权20余项。
据了解,通过形式审查的药品即代表该药品符合相应的申报条件,获得参加下一步评审的资格。
接下来,国家医保局将按照《基本医疗保险用药管理暂行办法》和《2024年国家基本医疗保险、工伤保险和生育保险药品目录调整工作方案》的要求,按程序组织开展专家评审等工作。
摘要abstract2024年2月有5个1类新药、7个改良型新药申请上市;225个品种按新分类仿制申请申报,其中49个品种暂无国内仿制获批,二羟丙茶碱注射液申报企业最多;51个存量品种有企业申报一致性评价,其中9个品种为首次申报。3款1类新药获批上市,4个品种获批新适应症,8个品种首家过评,其中4个为首仿。创新药品种申报情况2024年2月,132个创新药品种(药品注册分类为“1”的品种)获CDE承办。有5个品种申请上市:TQB2450注射液(正大天晴南京顺欣制药)、夫那奇珠单抗注射液(苏州盛迪亚生物医药)、玛赛洛沙韦片(南京征祥医药)、玛仕度肽注射液(信达生物制药(苏州))、小儿黄金止咳颗粒(北京东方运嘉药业)。2024年2月创新药上市申请承办情况2024年2月创新药临床申请承办情况改良型新药品种申报情况2024年2月,31个改良型新药品种获CDE承办,7个品种申请上市,其中HY22017胶囊(长春海悦药业)为新复方制剂,特立帕肽注射液(深圳翰宇药业)和盐酸氨溴索口服冻干片(华润三九医药)为新剂型。2024年2月改良型新药上市申请承办情况2024年2月改良型新药临床申请承办情况新分类仿制药品种申报情况2024年2月,225个品种仿制申请获CDE承办,49个品种目前暂无国内仿制药获批。二羟丙茶碱注射液共有5家企业申报,目前二羟丙茶碱注射液存量批准文号有13个,在审申请有39个,尚无企业过评,米内网数据显示,2022年中国公立医疗机构终端二羟丙茶碱注射液销售额超过7亿元。2024年2月新分类仿制药品种申报情况存量品种一致性评价申报情况2024年2月,51个品种的一致性评价补充申请获CDE承办。丁二磺酸腺苷蛋氨酸肠溶片、丁溴东莨菪碱注射液、复方电解质注射液(Ⅴ)、硫酸特布他林注射液、头孢泊肟酯片、头孢呋辛酯干混悬剂、盐酸普萘洛尔注射液、药用炭胶囊、注射用厄他培南钠等9个品种为首次申报。2024年2月存量品种一致性评价申报情况获批情况2024年2月有3款1类新药获批上市,富马酸泰吉利定注射液(江苏恒瑞医药)、九味止咳口服液(卓和药业集团)、可伐利单抗注射液(罗氏)。1个新复方制剂获批:阿达帕林克林霉素凝胶(兆科(广州)眼科药物)。4个品种获批新适应症:帕博利珠单抗注射液(默沙东)、注射用重组人TNK组织型纤溶酶原激活剂(石药集团明复乐药业(广州))、恩曲替尼胶囊(罗氏)、尼妥珠单抗注射液(百泰生物药业)。78个品种按新分类仿制申请获批并视同通过一致性评价,40个品种按存量品种一致性评价补充申请过评。8个品种为首家过评,首家过评品种中夫西地酸乳膏(福元药业)、呋塞米口服溶液(成都倍特得诺药业)、美沙拉秦肠溶缓释片(上海宣泰医药科技)、异硫蓝注射液(广东和博制药)等4个品种为国内首仿。2024年2月主要注册类型品种获批情况数据来源:米内网中国申报进度数据库(MED)、CDE、NMPA;相关统计字段按药品名称统计,时间截至2024年2月29日;获批品种按NMPA发布时间统计;药物作用靶点以及适应症整理自公开资料。本文为原创稿件,转载请注明来源和作者,否则将追究侵权责任。投稿及报料请发邮件到872470254@qq.com稿件要求详询米内微信首页菜单栏商务及内容合作可联系QQ:412539092【分享、点赞、在看】点一点不失联哦
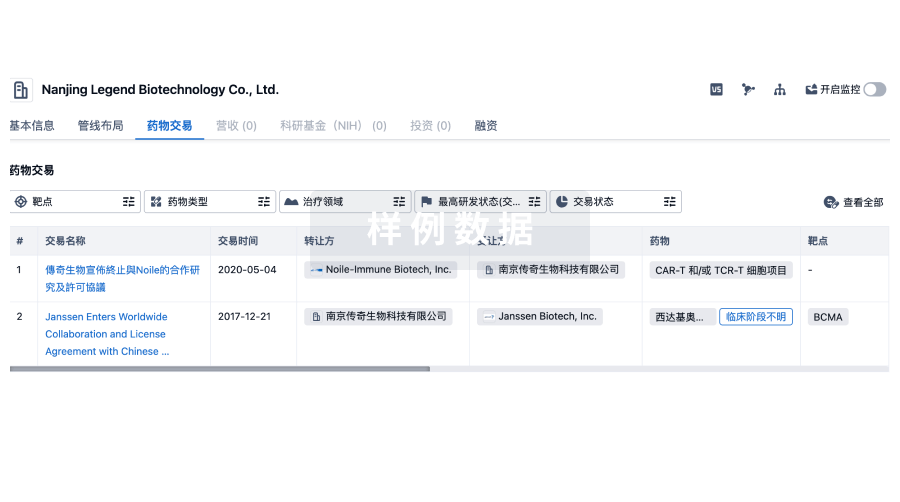
100 项与 广东和博制药有限公司 相关的药物交易
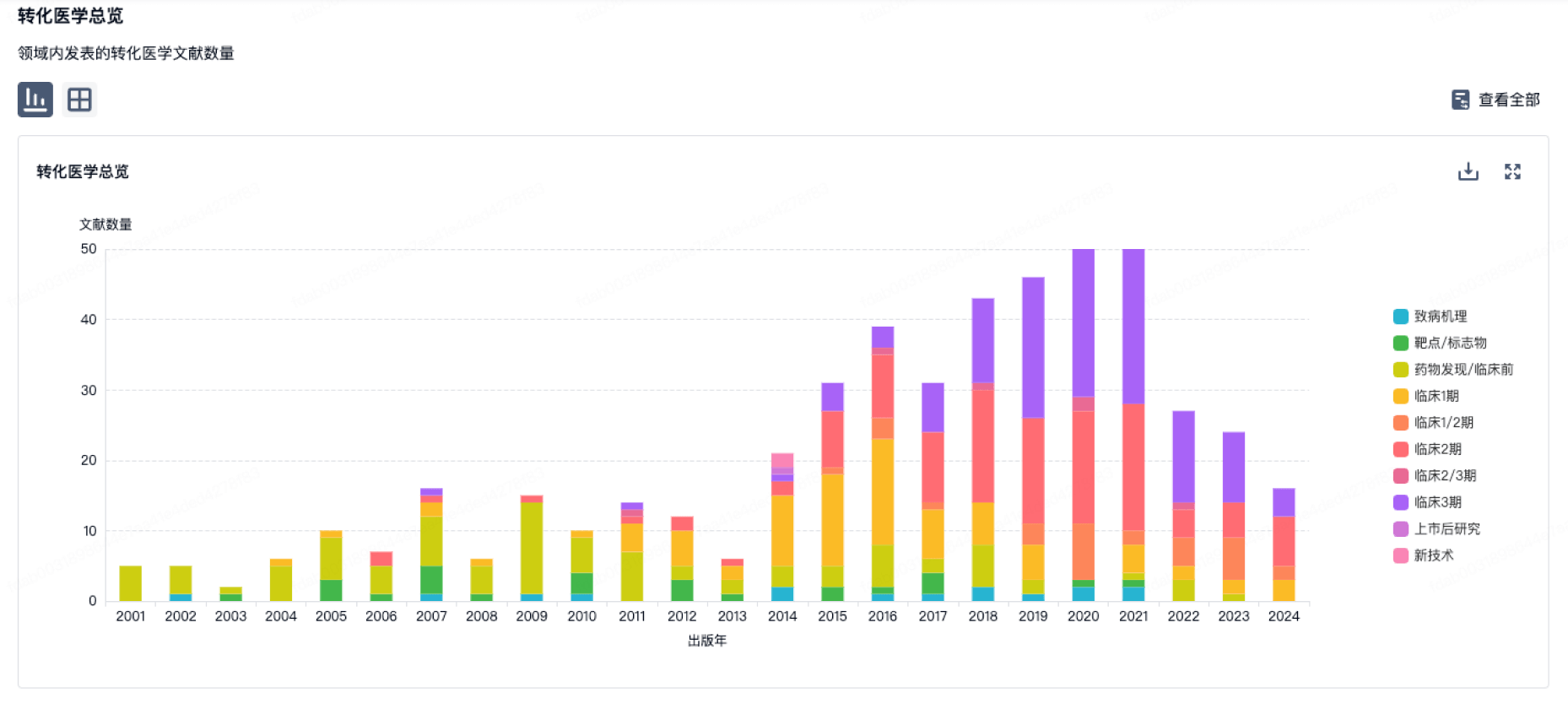
100 项与 广东和博制药有限公司 相关的转化医学