预约演示
更新于:2025-08-29
Hangzhou Shengyu Biomedical Technology Co., Ltd.
更新于:2025-08-29
概览
标签
肿瘤
泌尿生殖系统疾病
皮肤和肌肉骨骼疾病
小分子化药
化学药
疾病领域得分
一眼洞穿机构专注的疾病领域
暂无数据
技术平台
公司药物应用最多的技术
暂无数据
靶点
公司最常开发的靶点
暂无数据
| 排名前五的药物类型 | 数量 |
|---|---|
| 小分子化药 | 6 |
| 化学药 | 2 |
| 排名前五的靶点 | 数量 |
|---|---|
| PARG(聚ADP-核糖水解酶) | 2 |
| POLQ(DNA polymerase theta) | 2 |
关联
8
项与 杭州圣域生物医药科技有限公司 相关的药物靶点 |
作用机制 PARG抑制剂 |
在研机构 |
原研机构 |
在研适应症 |
非在研适应症- |
最高研发阶段临床1期 |
首次获批国家/地区- |
首次获批日期- |
靶点 |
作用机制 POLQ抑制剂 |
在研机构 |
原研机构 |
在研适应症 |
非在研适应症- |
最高研发阶段临床1期 |
首次获批国家/地区- |
首次获批日期- |
靶点- |
作用机制- |
在研机构 |
原研机构 |
在研适应症 |
非在研适应症- |
最高研发阶段临床申请 |
首次获批国家/地区- |
首次获批日期- |
3
项与 杭州圣域生物医药科技有限公司 相关的临床试验NCT07088588
A First-in-Human Phase 1 Study to Evaluate the Safety, Tolerability, Pharmacokinetics, and Preliminary Antitumor Activity of SYN608, a Poly ADP-ribose Glycohydrolase (PARG) Inhibitor in Patients With Locally Advanced or Metastatic Solid Tumors
This interventional study will evaluate the safety, tolerability, pharmacokinetics, pharmacodynamics and preliminary efficacy of SYN608 as monotherapy in adult patients with advanced solid tumors
开始日期2025-07-31 |
申办/合作机构 |
NCT06666270
A First-in-human, Phase I Study to Evaluate the Safety, Tolerability, Pharmacokinetics, Pharmacodynamics and Preliminary Anti-tumor Activity of SYN818, a DNA Polymerase Theta (POLQ) Inhibitor Alone in Patients With Locally Advanced or Metastatic Solid Tumors
This interventional study will evaluate the safety, tolerability, pharmacokinetics, pharmacodynamics and preliminary efficacy of SYN818 as monotherapy in adult patients with advanced solid tumors
开始日期2024-11-21 |
申办/合作机构 |
CTR20253189
一项评价SYN818(一种DNA聚合酶θ[POLQ]抑制剂)与奥拉帕利联合给药在携带乳腺癌易感基因(BRCA)突变和/或同源重组修复(HRR)通路缺陷的局部晚期或转移性实体瘤患者中的安全性、耐受性、药代动力学和初步抗肿瘤活性的Ib期研究
评价SYN818与奥拉帕利联合给药在携带BRCA突变和/或HRR通路缺陷的局部晚期或转移性实体瘤受试者中的安全性和耐受性,可能包括确定最大耐受剂量(MTD)和/或II期推荐剂量(RP2D),以及评价SYN818与奥拉帕利联合给药的初步疗效。
开始日期- |
申办/合作机构 |
100 项与 杭州圣域生物医药科技有限公司 相关的临床结果
登录后查看更多信息
0 项与 杭州圣域生物医药科技有限公司 相关的专利(医药)
登录后查看更多信息
22
项与 杭州圣域生物医药科技有限公司 相关的新闻(医药)2025-08-10
·信狐药迅
每周药品注册获批数据,分门别类呈现,一目了然。(8.4-8.10)
新药上市申请药品名称企业注册分类受理号磷酸奥司他韦口腔崩解片北京星昊医药股份有限公司2.2CXHS2400027磷酸奥司他韦口腔崩解片北京星昊医药股份有限公司2.2CXHS2400026马来酸噻吗洛尔凝胶上海奥全生物医药科技有限公司2.4;2.2CXHS2400111
新药临床申请药品名称企业注册分类受理号HRS-6093片江苏恒瑞医药股份有限公司1CXHL2500550HRS-6093片江苏恒瑞医药股份有限公司1CXHL2500549HRS-4508片江苏恒瑞医药股份有限公司1CXHL2500541HRS-4508片江苏恒瑞医药股份有限公司1CXHL2500540QL-H118片南京芩领医药科技有限公司1CXHL2500538SZ2001片苏中药业集团股份有限公司1CXHL2500524SZ2001片苏中药业集团股份有限公司1CXHL2500523HSK47388片海思科医药集团股份有限公司1CXHL2500521HSK47388片海思科医药集团股份有限公司1CXHL2500522BGB-16673片百济神州(苏州)生物科技有限公司1CXHL2500526BGB-16673片百济神州(苏州)生物科技有限公司1CXHL2500525RO7840734罗氏(中国)投资有限公司1CXHL2500519RO7840734罗氏(中国)投资有限公司1CXHL2500518SYN818片杭州圣域生物医药科技有限公司1CXHL2500511SYN818片杭州圣域生物医药科技有限公司1CXHL2500510HW241045片武汉人福创新药物研发中心有限公司1CXHL2500498HW241045片武汉人福创新药物研发中心有限公司1CXHL2500497DC411151胶囊杭州民生药业股份有限公司1CXHL2500487DC411151胶囊杭州民生药业股份有限公司1CXHL2500486HEC20002胶囊广东东阳光药业股份有限公司2.2CXHL2500527KEM2417缓释干混悬剂深圳珐玛易药品科技有限公司2.2CXHL2500515KEM2417缓释干混悬剂深圳珐玛易药品科技有限公司2.2CXHL2500514盐酸奥洛他定口服液海南万玮制药有限公司2.2CXHL2500504MZ-01吸入溶液成都米子生物医药科技有限公司2.2;2.4CXHL2500513注射用多西他赛(白蛋白结合型)石药集团中奇制药技术(石家庄)有限公司2.4CXHL2500537氟[18F]阿洛夫定注射液江苏华益科技有限公司2.4CXHL2500485重组带状疱疹疫苗(CHO细胞)桓科(河北)生物技术有限公司1.3CXSL2500371注射用LM-24C5礼新医药科技(上海)有限公司1CXSL2500457注射用SHR-A1811苏州盛迪亚生物医药有限公司1CXSL2500455SIBP-A10注射液上海生物制品研究所有限责任公司1CXSL2500449注射用YL201苏州宜联生物医药有限公司1CXSL2500441注射用BAT8008百奥泰生物制药股份有限公司1CXSL2500440BAT1308注射液百奥泰生物制药股份有限公司1CXSL2500438注射用YL202苏州宜联生物医药有限公司1CXSL2500437注射用YL201苏州宜联生物医药有限公司1CXSL2500436注射用BL-B01D1成都百利多特生物药业有限责任公司1CXSL2500424注射用IMD303亲合力(成都)药业有限公司1CXSL2500422SHR-7782注射液苏州盛迪亚生物医药有限公司1CXSL2500416注射用TJ101一线医药(杭州)有限公司1CXSL2500413注射用LB4330上海健信生物医药科技有限公司1CXSL2500407注射用重组抗PD1/TIM3人源化双特异抗体上海健信生物医药科技有限公司1CXSL2500404注射用MHB042C明慧医药(杭州)有限公司1CXSL2500409注射用BC3195无锡智康弘义生物科技有限公司1CXSL2500398CM512注射液康诺亚生物医药科技(成都)有限公司1CXSL2500391ABO2102注射剂苏州艾博生物科技有限公司1CXSL2500388NW-101C注射液新景智源生物科技(苏州)有限公司1CXSL2500386NW-101C注射液新景智源生物科技(苏州)有限公司1CXSL2500385SENL103自体T细胞注射液河北森朗生物科技有限公司1CXSL2500382SYS6026注射液石药集团巨石生物制药有限公司1CXSL2500376EXG202注射液杭州嘉因生物科技有限公司1CXSL2500375自体天然肿瘤浸润淋巴细胞注射液上海君赛生物药业有限公司1CXSL2500374人脐带间充质干细胞注射液天津华域药业有限公司1CXSL2500373替雷利珠单抗注射液广州百济神州生物制药有限公司2.1CXSL2500447贝伐珠单抗注射液苏州盛迪亚生物医药有限公司2.2CXSL2500450阿得贝利单抗注射液上海盛迪医药有限公司2.2CXSL2500448BAT4706注射液百奥泰生物制药股份有限公司2.4CXSL2500439
仿制药申请药品名称企业注册分类受理号西格列汀二甲双胍缓释片杭州和泽坤元药业有限公司3CYHS2403955盐酸纳美芬注射液广州市联瑞制药有限公司3CYHS2403434阿糖胞苷注射液吉斯美(武汉)制药有限公司3CYHS2403402阿糖胞苷注射液吉斯美(武汉)制药有限公司3CYHS2403404盐酸纳美芬注射液成都明德至远医药科技有限公司3CYHS2403300注射用乳糖酸红霉素广东金城金素制药有限公司3CYHS2403305盐酸纳美芬注射液江苏安必生制药有限公司3CYHS2403223氯化钙注射液海南倍特药业有限公司3CYHS2403093布瑞哌唑口腔崩解片成都康弘药业集团股份有限公司3CYHS2402954小儿复方氨基酸注射液(19AA-I)湖北民康药业集团有限公司3CYHS2400829奥贝胆酸片正大天晴药业集团股份有限公司3CYHS2400425奥贝胆酸片正大天晴药业集团股份有限公司3CYHS2400424度拉糖肽注射液山东博安生物技术股份有限公司3.3CXSS2400054度拉糖肽注射液山东博安生物技术股份有限公司3.3CXSS2400053度拉糖肽注射液山东博安生物技术股份有限公司3.3CXSS2400052度拉糖肽注射液山东博安生物技术股份有限公司3.3CXSS2400051阿达木单抗注射液武汉生物制品研究所有限责任公司3.3CXSS2300100乙酰半胱氨酸注射液嘉实(湖南)医药科技有限公司4CYHS2502336硫酸艾沙康唑胶囊福安药业集团庆余堂制药有限公司4CYHS2502230溴芬酸钠滴眼液盈科瑞(珠海金湾)制药有限公司4CYHS2502224磷酸芦可替尼片齐鲁制药有限公司4CYHS2501525磷酸芦可替尼片齐鲁制药有限公司4CYHS2501524磷酸芦可替尼片齐鲁制药有限公司4CYHS2501523噻托溴铵吸入喷雾剂天津信达制药有限公司4CYHS2404343洛索洛芬钠凝胶贴膏广东恒健制药有限公司4CYHS2403666地屈孕酮片浙江美迪深生物医药有限公司4CYHS2403641右旋糖酐羟丙甲纤维素滴眼液宏越科技(湖州)有限公司4CYHS2403233多巴丝肼片上海理想制药有限公司4CYHS2403254富马酸贝达喹啉片中诺凯琳健康产业(海南)有限公司4CYHS2403134熊去氧胆酸口服混悬液海南斯达制药有限公司4CYHS2402608丙酸氯倍他索搽剂江苏知原药业股份有限公司4CYHS2401668盐酸氨溴索注射液多多药业有限公司4CYHS2401261丙戊酸钠口服溶液浙江赛默制药有限公司4CYHS2400631盐酸特比萘芬喷雾剂浙江赛默制药有限公司4CYHS2303349培哚普利氨氯地平片(III)宁波科尔康美诺华药业有限公司4CYHS2303149培哚普利氨氯地平片(I)宁波科尔康美诺华药业有限公司4CYHS2303148培哚普利氨氯地平片(I)宁波科尔康美诺华药业有限公司4CYHS2303147吸入用复方异丙托溴铵溶液深圳大佛药业股份有限公司4CYHS2200587国;CYHS2200587苯磺顺阿曲库铵润都制药(荆门)有限公司CYHS2460216维生素D口服溶液厦门紫旭医药科技有限公司3CYHL2500105氨苯砜凝胶深圳珐玛易药品科技有限公司3CYHL2500101艾考糊精腹膜透析液仁合益康集团有限公司4CYHL2500093注射用SIM0692山东先声生物制药有限公司3.3CXSL2500417
进口申请药品名称企业注册分类受理号埃万妥单抗注射液Janssen-Cilag International NV2.2JXSS2400004GIREDESTRANTGenentech, Inc.1JXHL2500122CHF1535-IICHIESI FARMACEUTICI SPA2.2JXHL2500110TAR-210Janssen Research & Development, LLC2.2;2.4JXHL2500125匹妥布替尼片Eli Lilly and Company2.4JXHL2500113PF-08046047Pfizer Inc.1JXSL2500085Depemokimab注射液GlaxoSmithKline Research & Development Limited1JXSL2500080SAR402663注射液Sanofi-Aventis Recherche & Developpement1JXSL2500074Mosunetuzumab Injection (Subcutaneous Injection)F. Hoffmann-La Roche Ltd.2.1JXSL2500084Mosunetuzumab Injection (Subcutaneous Injection)F. Hoffmann-La Roche Ltd.2.1JXSL2500083
中药相关申请药品名称企业注册分类受理号紫英颗粒广东方盛融科药业有限公司1.1CXZL2500030
注:橙色字体部分结论为不批准或收到通知件;
申请上市疫苗临床申请
2025-07-12
·医药观澜
根据中国国家药监局药品审评中心(CDE)官网以及公开资料梳理,本周(7月7日~7月12日),有12款1类创新药首次在中国获得临床试验默示许可(IND)。这些产品涵盖了小分子药物、多肽、CAR-T细胞疗法、碱基编辑疗法、疫苗、ADC等类型。怡豪生物:MSLN-CAR-T细胞注射液作用机制:MSLN靶向CAR-T细胞治疗药物适应症:间皮素阳性卵巢癌怡豪生物申报的MSLN-CAR-T细胞注射液获批临床,拟开发治疗复发或难治间皮素阳性卵巢癌。MSLN(间皮素)是一种在多种实体瘤中高度表达的抗原,尤其是间皮瘤、卵巢上皮癌和胰腺癌,研究发现MSLN过表达与患者较低的存活率相关,是一个颇具潜力的靶点。科锐克医药:CRG-B191注射液作用机制:基因治疗药物适应症:nAMD科锐克医药1类新药CRG-B191注射液获批临床,拟开发治疗湿性(新生血管性)年龄相关性黄斑变性(nAMD)。公开资料显示,该产品是采用 “新一代共价封闭端DNA基因组构型” 的AAV(cceAAV)基因治疗药物,经视网膜下注射后,可在视网膜细胞中稳定、持续、高效表达经氨基酸序列优化的抗VEGF蛋白,有望实现一次注射长期有效,解决传统治疗中反复眼内注射带来的风险及患者依从性差等问题。荃信生物:QX029N注射液作用机制:生物制品1类新药适应症:成人中度至重度特应性皮炎荃信生物生物制品1类新药QX029N注射液获批临床,拟开发治疗成人中度至重度特应性皮炎。英脉德医疗:IMD101注射液作用机制:生物制品1类新药适应症:晚期恶性实体瘤英脉德医疗申报的生物制品1类新药IMD101注射液获批临床,拟开发治疗晚期恶性实体瘤(拟用于包括但不限于黑色素瘤、肾细胞癌、尿路上皮癌等)。宜联生物:注射用YL242作用机制:靶向VEGF的ADC适应症:晚期实体瘤宜联生物1类新药注射用YL242获批临床,拟用于治疗晚期实体瘤,包括但不限于结肠直肠癌、胃腺癌或胃食管结合部腺癌、非小细胞肺癌、肝细胞癌等。公开资料显示,这是一款靶向VEGF的抗体偶联药物(ADC)。VEGF是已经充分验证的肿瘤治疗靶点,但无法通过传统ADC技术而开发。VEGF富集于肿瘤组织附近,并在血管生成中发挥重要作用,其表达与多种癌症的进展相关。YL242是一款靶向可溶性VEGF的非内化型ADC,旨在结合靶向VEGF的抗血管生成作用和肿瘤微环境释放的细胞毒载荷来发挥抗肿瘤活性。该产品此前已在澳洲和美国获批临床试验。瑞宏迪医药、瑞领医药:注射用RGL-232作用机制:针对KRAS靶点的肿瘤疫苗适应症:携带KRAS突变的恶性实体肿瘤由瑞宏迪医药和其全资子公司瑞领医药申报的1类新药注射用RGL-232获批临床,拟用于治疗携带KRAS突变(G12C、G12D、G12V或G13D)的恶性实体肿瘤。公开资料显示,这是一款针对KRAS靶点的肿瘤疫苗。KRAS肿瘤疫苗主要通过增强免疫应答、克服耐药性及调节肿瘤微环境来提升疗效,具有与其他药物联用的多模式联合治疗潜力。同时KRAS疫苗利用MHC呈递抗原,可以绕过直接结合KRAS蛋白的需要,从而解决小分子药物面临的结构难题。此外,免疫激活还可能产生记忆T细胞,实现对肿瘤的长期监控,降低耐药发生的风险。圣域生物:SYN608片作用机制:PARG抑制剂适应症:晚期实体瘤圣域生物1类新药SYN608片获批临床,拟开发治疗晚期实体瘤。公开资料显示,SYN608是一款创新小分子化合物,属于新型强效、高选择性PARG(聚ADP核糖水解酶)抑制剂,能有效抑制肿瘤细胞的DNA损伤修复功能,从而特异性诱导具同源重组修复缺陷(HRD)特征的肿瘤细胞死亡,有望为肿瘤患者(尤其是对现有疗法如PARP抑制剂不敏感的患者)带来全新的治疗希望。圣域生物基于对DNA损伤修复机制的深入理解和原创研究,验证了除HRD之外的新型生物标志物,将指导SYN608精准地运用在差异化的肿瘤适应症,为临床概念验证打下坚实的基础。尧唐生物、信立泰药业:YOLT-101注射液作用机制:靶向PCSK9基因的体内碱基编辑药物适应症:杂合子型家族性高胆固醇血症(HeFH)尧唐生物和信立泰药业共同申报的1类新药YOLT-101注射液的临床试验申请获得受理。公开资料显示,这是一款靶向PCSK9基因的体内碱基编辑药物。其能在DNA单碱基水平精准编辑并沉默PCSK9基因,下调血液中的PCSK9蛋白水平,抑制PCSK9介导的低密度脂蛋白受体(LDLR)降解,从而增强LDLR对低密度脂蛋白的摄取,有效清除血液中的LDL-C,最终延缓和治愈家族性高胆固醇血症。该产品在研究者发起的临床研究(IIT)中已经取得积极结果,单次给药即可实现低密度脂蛋白胆固醇(LDL-C)的显著且持久降低,这一效果已持续观察超过6个月。信立泰此前与尧唐生物签订协议,获得YOLT-101于中国大陆区域的独家许可权益。多米瑞生物:DMR2301注射液作用机制:多肽药物适应症:代谢功能障碍相关脂肪性肝炎多米瑞生物申报的1类新药DMR2301注射液获批临床,拟开发治疗代谢功能障碍相关脂肪性肝炎。公开资料显示,上海多米瑞生物技术有限公司成立于2015年,为国药医工总院所属,前身为2007年成立的上海医工院多肽与蛋白质药物课题组,多米瑞始终聚焦多肽药物赛道,从事创新药研发与临床急需多肽药物的产业化成果转化。炎明生物:PTT-621片作用机制:化药新药适应症:成人炎症性肠病(IBD)炎明生物申报的1类新药PTT-621片获批临床,拟开发治疗炎症性肠病。公开资料显示,这是一款化药新药,具体靶点尚未披露。BioPhoenix:BPC2001注射液作用机制:化药新药适应症:预防急性移植物抗宿主病三福生醫(BioPhoenix)申报的1类新药BPC2001注射液获批临床,拟开发用于预防急性移植物抗宿主病。公开资料显示,这是一款化药新药,具体靶点尚未披露。杉竹曜生物:BBT001注射液作用机制:四价双抗适应症:中重度特应性皮炎杉竹曜生物1类新药BBT001注射液获批临床,拟开发治疗中重度特应性皮炎。公开资料显示,这是一款靶向IL4Ra和IL31的四价双特异性抗体。期待这些在研新药后续临床研发进程顺利,早日为患者带来新的治疗选择。参考资料:[1]中国国家药监局药品审评中心(CDE)官网. Retrieved July 12 , From https://www.cde.org.cn/main/xxgk/listpage/4b5255eb0a84820cef4ca3e8b6bbe20c[2]各公司官网及公开资料版权说明:本文欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权或其他合作需求,请联系wuxi_media@wuxiapptec.com。免责声明:本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
免疫疗法细胞疗法疫苗抗体药物偶联物临床申请
2025-07-10
·氨基观察
氨基观察-创新药组原创出品作者 | 黄恺CXO一哥公布最新成绩单。7月10日,药明康德露业绩预告,公司预计2025年半年度实现营业收入约207.99亿元,同比增长约20.64%,其中持续经营业务收入同比增长约24.24%。公司预计本期实现经调整非《国际财务报告准则》下归属于本公司股东的净利润(经调整归母净利润)约63.15亿元,同比增长约44.43%。Biotech技术平台出海。7月9日,维泰瑞隆宣布,诺华获得维泰瑞隆专有 “脑递送模块(BDM)平台” 的独家收购选择权,而 Sironax 将可获得最高1.75亿美元的预付款及近期付款,同时保留部分基于 BDM 平台开发的自有治疗资产(如针对特定神经退行性疾病的候选药物)的开发权。复宏汉霖PD-L1 ADC药物HLX43火速推进。7月9日,复宏汉霖宣布,HLX43获多国批准开展NSCLC国际多中心II期临床。全球尚无同类靶向PD-L1的ADC产品获批上市,HLX43为全球首个进入临床II期的PD-L1 ADC。在过去的一天里,国内外医药市场还有哪些热点值得关注?让氨基君带你一探究竟。/ 01 /市场速递1)维泰瑞隆出售脑递送模块平台7月9日,维泰瑞隆宣布,诺华获得维泰瑞隆专有 “脑递送模块(BDM)平台” 的独家收购选择权,而 Sironax 将可获得最高1.75亿美元的预付款及近期付款,同时保留部分基于 BDM 平台开发的自有治疗资产(如针对特定神经退行性疾病的候选药物)的开发权。/ 02 /资本信息1)药明康德上半年归母净利润同比增长约44%7月10日,药明康德露业绩预告,公司预计2025年半年度实现营业收入约207.99亿元,同比增长约20.64%,其中持续经营业务收入同比增长约24.24%。公司预计本期实现经调整非《国际财务报告准则》下归属于本公司股东的净利润(经调整归母净利润)约63.15亿元,同比增长约44.43%。/ 03 /医药动态1)复宏汉霖HLX43获多国批准开展NSCLC国际多中心II期临床7月9日,复宏汉霖宣布,PD-L1 ADC药物HLX43获多国批准开展NSCLC国际多中心II期临床。全球尚无同类靶向PD-L1的ADC产品获批上市,HLX43为全球首个进入临床II期的PD-L1 ADC。2)圣域生物SYN608片获临床许可7月10日,据CDE官网,圣域生物SYN608片获临床许可,拟开展治疗晚期实体瘤的研究。3)复融生物FL115注射液获临床许可7月10日,据CDE官网,复融生物FL115注射液获临床许可,拟联合PD-1单抗用于治疗晚期实体瘤。4)旺山旺水司美那非获批上市7月10日,据NMPA官网,旺山旺水司美那非获批上市。根据公开资料和临床试验进展,适应症为治疗男性勃起功能障碍(ED)。5)亚盛医药Bcl-2抑制剂获批上市7月10日,亚盛医药宣布,Bcl-2抑制剂利沙托克拉片获批上市,用于治疗既往经过至少包含BTK抑制剂在内的一种系统治疗的成人慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(CLL/SLL)患者。PS:欢迎扫描下方二维码,添加氨基君微信号交流。
引进/卖出临床2期财报并购抗体药物偶联物
100 项与 杭州圣域生物医药科技有限公司 相关的药物交易
登录后查看更多信息
100 项与 杭州圣域生物医药科技有限公司 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2025年09月02日管线快照
管线布局中药物为当前组织机构及其子机构作为药物机构进行统计,早期临床1期并入临床1期,临床1/2期并入临床2期,临床2/3期并入临床3期
药物发现
3
2
临床前
临床申请
1
2
临床1期
其他
1
登录后查看更多信息
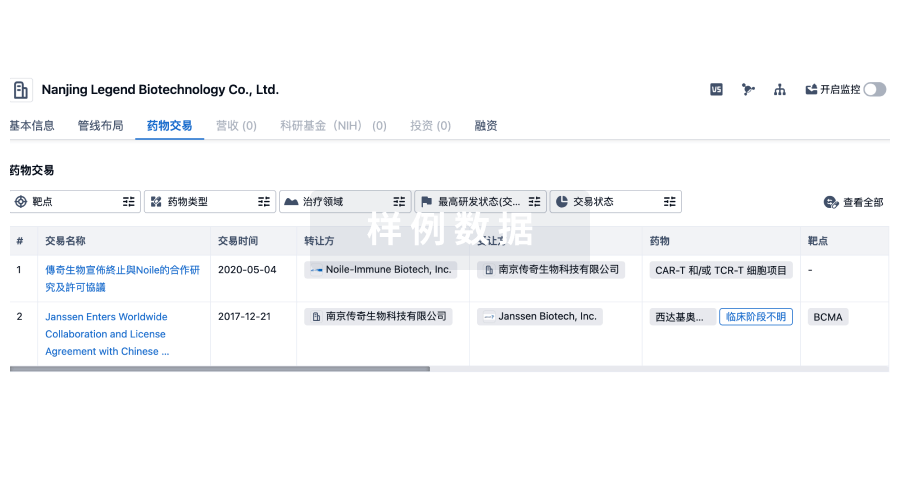
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
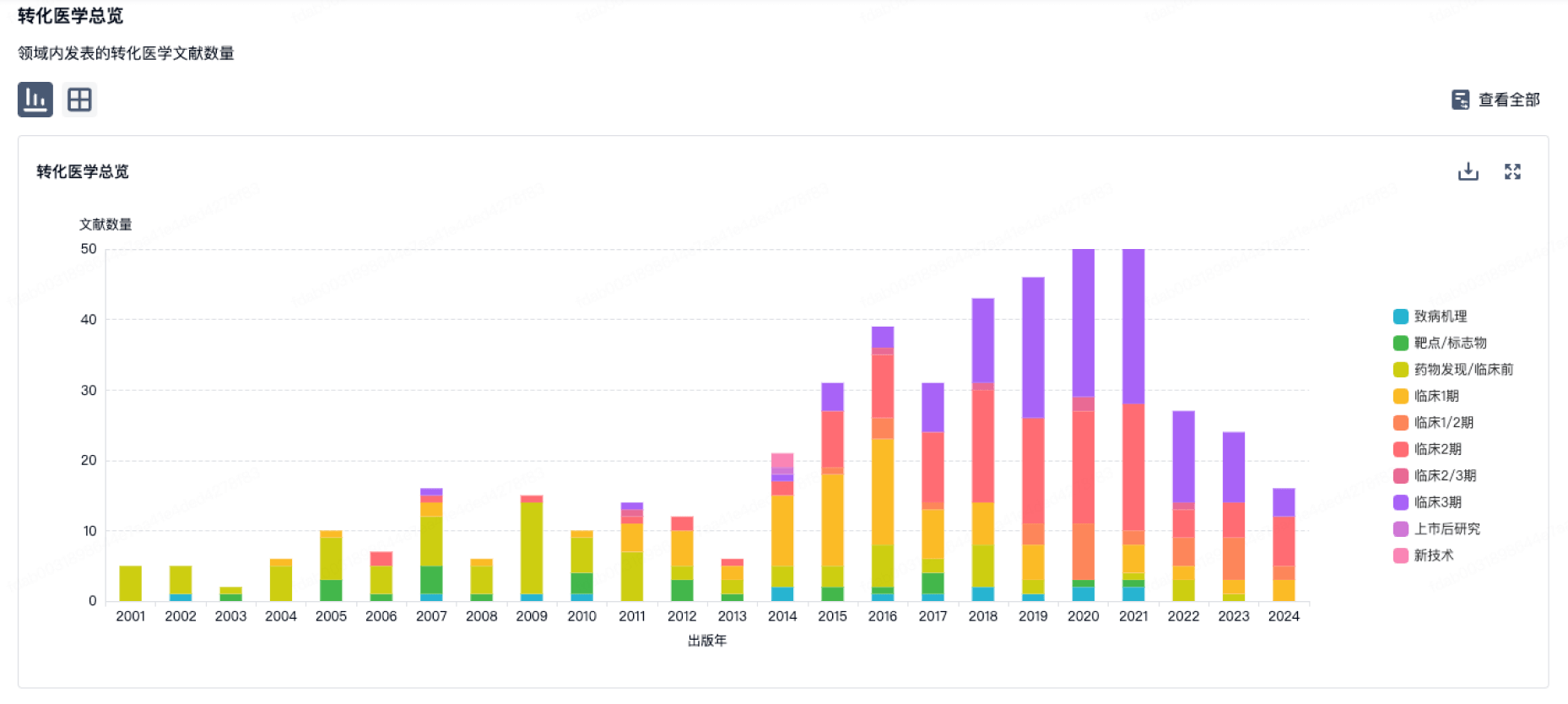
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
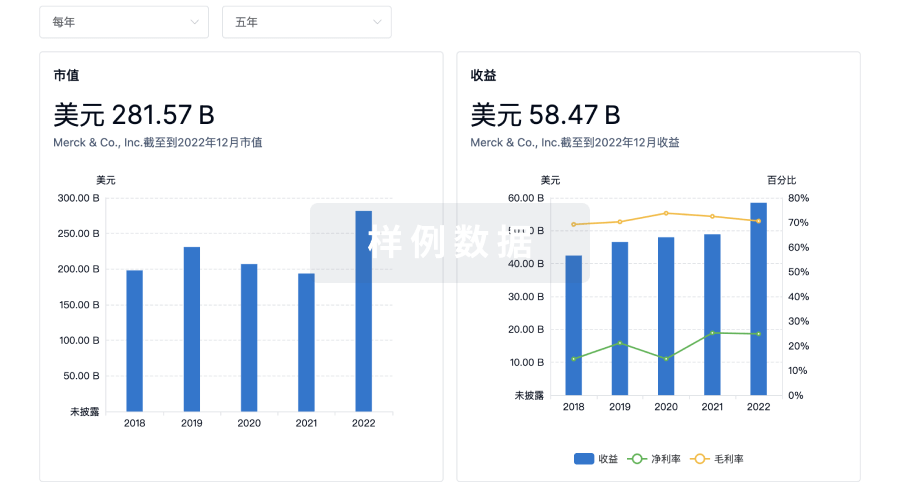
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
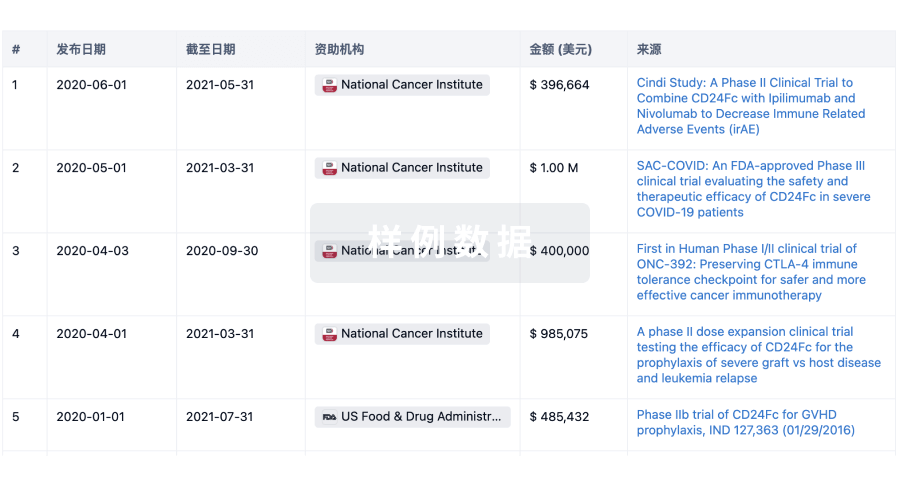
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
Eureka LS:
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用