预约演示
更新于:2025-01-23
Zhejiang Younuojin Bioengineering Co., Ltd.
更新于:2025-01-23
概览
标签
内分泌与代谢疾病
其他疾病
神经系统疾病
激素
生长因子
Fc片段
疾病领域得分
一眼洞穿机构专注的疾病领域
暂无数据
技术平台
公司药物应用最多的技术
暂无数据
靶点
公司最常开发的靶点
暂无数据
| 排名前五的药物类型 | 数量 |
|---|---|
| 激素 | 5 |
| 生长因子 | 1 |
| Fc片段 | 1 |
| 排名前五的靶点 | 数量 |
|---|---|
| GHR(生长激素受体) | 4 |
| IGF-1R(胰岛素样生长因子-I受体) | 1 |
关联
7
项与 浙江优诺金生物工程有限公司 相关的药物靶点 |
作用机制 GHR激动剂 |
在研机构 |
原研机构 |
非在研适应症- |
最高研发阶段临床3期 |
首次获批国家/地区- |
首次获批日期- |
靶点 |
作用机制 GHR激动剂 |
在研机构 |
原研机构 |
在研适应症 |
非在研适应症- |
最高研发阶段临床前 |
首次获批国家/地区- |
首次获批日期- |
靶点- |
作用机制- |
在研机构 |
原研机构 |
在研适应症 |
非在研适应症- |
最高研发阶段临床前 |
首次获批国家/地区- |
首次获批日期- |
3
项与 浙江优诺金生物工程有限公司 相关的临床试验CTR20241643
一项在生长激素缺乏患儿中评估注射用HSA-rhGH治疗儿童生长障碍的疗效和安全性的随机、开放标签、阳性药对照的Ⅲ期临床试验
主要目的:
评价试验药物注射用HSA-rhGH对比对照药品rhGH注射液治疗青春期前生长激素缺乏症儿童的安全性和有效性,为注射用重组人血白蛋白-生长激素融合蛋白的获批上市提供依据。
次要目的:
1)评价包括胰岛素样生长因子-1(IGF-1)、胰岛素样生长因子结合蛋白-3(IGFBP-3)水平及其标准差分值在内的药效学(PD)参数的变化。
2)评价注射用重组人血白蛋白-生长激素融合蛋白在儿童生长激素缺乏症受试者中的免疫原性。
3)评价注射用重组人血白蛋白-生长激素融合蛋白在儿童生长激素缺乏症群体药代动力学特征。
探索性目的:
评价注射用重组人血白蛋白-生长激素融合蛋白是否通过以下方式对目标人群产生的有益影响:
1)减轻受试者的疾病家庭负担。
2)提高受试者的治疗依从性。
开始日期2024-06-20 |
申办/合作机构 |
CTR20213096
注射用重组人血白蛋白-生长激素融合蛋白治疗因内源性生长激素缺乏所造成的儿童生长障碍的多中心、开放、阳性药对照的Ⅱ期临床试验
主要目的:
探索不同剂量注射用HSA-rhGH治疗因内源性生长激素缺乏所造成的儿童生长障碍的有效性、安全性、耐受性和群体药代动力学,确定Ⅲ期临床试验用法、用量。
次要目的:
1)评价注射用HSA-rhGH在儿科患者体内的免疫原性;
2)评价注射用HSA-rhGH在儿科患者体内的PK/PD特征;
3)比较rhGH注射液和注射用HSA-rhGH的有效性、安全性、PK/PD特征和免疫原性。
开始日期2022-02-27 |
申办/合作机构 |
CTR20201721
一项双盲、单剂量、剂量递增、安慰剂对照、序贯设计试验,合并开放、多剂量、平行试验评估健康男性受试者单次皮下注射递增剂量的注射用重组人血白蛋白-生长激素融合蛋白后的耐受性和安全性的I期临床试验 。
主要目的: 评估健康男性受试者单次皮下注射递增剂量的注射用重组人血白蛋白-生长激素融合蛋白后的耐受性和安全性。 次要目的: 研究健康男性受试者单次皮下注射递增剂量的注射用重组人血白蛋白-生长激素融合蛋白后的药代动力学和药效学动力学; 比较健康男性受试者单次皮下注射注射用重组人血白蛋白-生长激素融合蛋白与多次皮下注射注射用重组人生长激素后的药代动力学和药效学动力学。
开始日期2020-09-18 |
申办/合作机构 |
100 项与 浙江优诺金生物工程有限公司 相关的临床结果
登录后查看更多信息
0 项与 浙江优诺金生物工程有限公司 相关的专利(医药)
登录后查看更多信息
9
项与 浙江优诺金生物工程有限公司 相关的新闻(医药)2024-08-09
各位领导、专家和行业同仁:
与传统的小分子药物和抗体药物相比,核酸药物具有设计简便、研发周期短、靶向特异性强、治疗领域广泛和长效性等优点,在治疗遗传性疾病、病毒感染、肿瘤等领域展现出巨大潜力,有望成为继小分子药物和抗体药物后的第三大类药物。据报道,目前全球已有19款小核酸药物获批上市,中国也有2款核酸药物已获批上市。面对核酸药物崛起这个不可多得的战略性发展机遇,中国创新药产业迎来了新的发展契机。
产业发展需要科技创新,创新的归宿是产业化,创新的水平也体现在产业化。自2008年起,由核酸药物领域科学家及产业精英指导召开的中国小核酸技术与应用学术系列会议已成功举办七届。以此为基础,为更充分发挥国家级行业协会平台功能,推进中国核酸药物产业创新体系进一步完善,提升产业创新能力与核心竞争力,中国生化制药工业协会拟定于2024年9月25-26日在天津组织召开“第八届中国(天津)核酸药物大会”。大会拟邀院士、产业界、学术界、药监药审药检、临床医生、投融资分析等专家共同搭建汇集“产学研用管投”六方面的合作交流平台,探索我国核酸药物产业创新发展的新机会,共筑核酸药物产业生态圈!
现将具体事项通知如下:
一、会议时间、地点
会议时间:2024年9月25-26日,9月24日全天报到
会议地点:天津万丽泰达酒店(天津市滨海新区第二大街29号)
二、会议组织
主办单位:
中国生化制药工业协会
承办单位:
天津国际生物医药联合研究院
天津经济技术开发区核酸产业联盟
博蕴生物
协办单位:
天津市药品检验研究院
媒体支持:
生物制品圈、药时空、细胞基因研究圈
三、会议主题
核酸药物:引领发展融合,共筑产业生态
四、大会组委会
名誉主席:张礼和院士、陈润生院士
主 席:谭蔚泓院士
委 员:白海娇、陈春麟、陈宁、范钟允、洪晓鸣、胡晓敏、胡新辉、黄震、贾晖、江伟、金新亮、孔繁圃、李彬、李九远、梁子才、刘艺锦、陆阳、邵宁生、石平、司端运、宋相容、宋艳民、苏晓晔、孙涛、汤新景、汪群杰、王海盛、王均、王升启、席真、杨朝勇、杨振军、尹正、英博、宇学峰、喻建华、张立云、张林琦、张佩琢、赵宣、赵志刚、朱涛(以上专家均按姓氏拼音排序,持续更新中......)
秘书长:胡文言、荀标
五、会议内容(拟定)
(一)开幕式、颁发“核酸药物终身成就奖”
(二)主题报告
(1) 核酸药物的创新与发展
l 从核酸药物谈基础研究和源头创新
l 从大数据、精准医学到核酸药物
l 靶向核药临床研究
l 核酸制药的关键挑战与研发进展
l 反义寡核酸药物靶向精准治疗原发性肝细胞
l 反义寡核酸药物设计与开发
l 新型重组小RNA生物合成技术及小RNA药物研发
l 寡核苷酸药物在罕见病领域的探索和开发策略
(2) 核酸药物的临床/非临床评价
l 治疗用单链寡核苷酸药物的非临床研究评价
l 核酸药物非临床评价策略与考量点
l 国内外上市核酸药物的临床应用与评价
(3) 核酸药物工艺技术与质量控制
l mRNA技术挑战与工艺方案
l mRNA制品的质量控制分享
l 寡核苷酸药物质量研究要点
l RNA靶向药物设计策略与生产工艺优化
l 核酸药物研发及生产中核心物料的布局策略
(4) 核酸的递送系统与修饰
l 核酸疫苗的微针递送
l 新型LNP核酸递送系统研究及质量标准探讨
l 靶向递送LNP技术在RNA药物中的应用
l 新型核酸药物制剂体内靶向递送研究
l 可电离脂质的理性设计与RNA药物递送
l 基于脂质的纳米载体设计及其在RNA药物研发的探索
l VLP-mRNA递送技术的应用前景
l 小核酸药物的肝外递送
l 小核酸药物口服递送系统的研发
l 小核酸药物递送技术-偶联递送平台探索
l 优化双递送技术平台,拓展核酸干扰药物临床适应症
l 解析siRNA药物递送平台技术的研发思路
(5) 核酸适配体在疾病治疗中的应用
l 核酸适配体-药物偶联物的研究进展
l 修饰核酸适配体筛选技术
l 核酸适配体PET现象策略
l 双特异性适配体对于抗肿瘤免疫的增强作用
l 适配体药物研发前景
(6) 小核酸药物CMC策略与产业化展望
l 小核酸药物的开发与监管考量
l 寡核苷酸药物的高效合成和持续性流程改进
l 新型高效经济寡核苷酸固相合成载体
l 双靶点小核酸技术平台和应用
l 小核酸大规模商业化生产线的系统设计思考
l 临床阶段创新小核酸公司进展分享
(7) 核酸药物的前沿探索
l 小核酸干扰药开发的黄金时代
l 小核酸药物开发的国内外机会
l 小核酸药物临床前研究的创新与应用
l 立足全新核苷修饰,打造创新的小核酸药物研发平台
l 核酸药物领域专利审查标准
l 核酸药物投资分析与案例分享
(8) 人工智能在核酸药物研发中的应用
l 人工智能驱动肿瘤个体化免疫治疗(mRNA疫苗)
l RNAi生物智造
l 人工智能预测RNA和DNA结合位点,加速核酸药物发现
l 优化mRNA设计算法提高稳定性和免疫原性
六、参会人员
核酸药物及其产业链企业的研发、生产、质量及高层管理人员;核酸药物相关大专院校、科研院所的研究人员;核酸药物领域药监、药检、药审人员;对核酸药物领域感兴趣的其他人士。
七、合作及展览展示
本次会议同期设置交流展示展位,企业专场研讨会、卫星会等各种商务合作,欢迎相关企业积极参与。
八、会议事项
(一)注册参会
识别下方二维码,点击马上报名,按提示填写注册信息并提交完成。
(二)收费标准
协会及分会专家免费参会;协会及分会副会长(副理事长)单位3个免费参会名额,常务理事、理事单位2个免费参会名额,普通会员单位1个免费参会名额。
8月30日前报名并转账:会员单位代表800元/人;非会员单位代表1200元/人;学生代表600元/人(凭学生证)。
8月30日后报名并转账:会员单位代表1200元/人,非会员单位代表1600元/人;学生代表800元/人(凭学生证)。
费用包含:会议场地费、会议期间餐费及资料费。注册参会代表交通住宿需自理。
(三)收款账号
账户名称 :中国生化制药工业协会
开 户 行 :工商银行北京市长安支行
账 号 :0200003309014418333
(四)发票
参会代表注册费由中国生化制药工业协会开具增值税电子普通发票,内容为会议费,参会代表注册时请务必准确填写开票信息,电子发票发送至报名人邮箱,发票一经开出,不可更改。
(五)住宿
本次会议的协议酒店也是会议酒店为天津万丽泰达酒店,酒店大/双床房(含双早):600元/天;酒店行政套房(含双早):900元/天。
联系方式:预订部:(8622) 65709000(周一至周六)
酒店房间紧张,可提前电话预留,需提前三天付费确认预定
【地址】:天津市滨海新区第二大街29号
【停车】:自驾可停酒店停车场(路面停车场)
拟邀请参会嘉宾名单
持续更新中……
1. 张礼和院士 中国科学院院士、北京大学药学院教授、天然药物及仿生药物国家重点实验室学术委员会主任
2. 陈润生院士 中国科学院院士、中国科学院生物物理研究所研究员
3. 谭蔚泓院士 中国科学院院士、中国科学院杭州医学研究所所长、浙江省肿瘤医院院长、上海交通大学分子医学研究院院长
4. 邵明立 中国药品监管研究会创会会长、原卫生部副部长、原国家食品药品监督管理局局长
以下嘉宾按姓氏拼音排序
1. 白海娇 天津市药品检验研究院院长、书记
2. 曹跃琼 上海吉凯基因医学科技股份有限公司董事长
3. 陈 璞 加拿大工程院院士、加拿大纳米生物制造首席教授、纳肽得(青岛)生物医药有限公司创始人
4. 陈 宁 天津科技大学生物工程学院教授
5. 陈春麟 上海美迪西生物医药股份有限公司创始人兼CEO
6. 陈建新 传信生物医药(苏州)有限公司创始人、董事长兼CEO
7. 陈振昌 瑞博奥科技有限公司总经理
8. 程 强 星锐医药联合创始人、北京大学研究员
9. 杜新平 天津市第五中心医院执行院长
10. 范晓光 天津科技大学生物工程学院教授
11. 范钟允 天津国际生物医药联合研究院副总经理
12. 冯 红 旭和(天津)医药科技有限公司副总经理
13. 顾景凯 吉林大学生命科学学院教授
14. 郭万成 奥锐特药业(天津)有限公司总经理
15. 贺慧宁 天津医科大学药学院教授
16. 洪晓鸣 海河生物医药科技集团董事长
17. 侯丽强 诺泰诺和生物医药科技有限公司总经理
18. 胡晓敏 原国家药品监督管理局药品审评中心高级审评员
19. 胡新辉 凯莱英医药集团CTO&CBO
20. 华益民 苏州安天圣施科技有限公司创始人
21. 黄 震 四川大学生命科学学院教授、硒核酸国际研究院院长、邵斯达克(诺奖)成都高新大核酸研究院院长
22. 黄金宇 大睿生物医药科技(上海)有限公司联合创始人兼副总裁
23. 黄渊余 北京理工大学教授、苏州炫景生物科技有限公司创始人
24. 黄泽傲 悦康药业集团药物研究院寡核苷酸开发负责人
25. 纪雪峰 北京安理(天津)律师事务所主任
26. 冀群升 靖因药业(上海)有限公司CEO兼执行董事
27. 贾 晖 天津国际生物医药联合研究院总经理
28. 江 伟 上海兆维科技发展有限公司执行董事
29. 金新亮 江苏汉邦科技股份有限公司副总经理
30. 孔繁圃 清华大学首席研究员、国家药品监督管理局药品审评中心原主任
31. 孔素东 苏州贝信生物技术有限公司执行总监
32. 李 彬 天津兴博润生物制药有限公司总经理
33. 李 高 齐鲁制药创新药物研究院助理院长
34. 李 和 艾斯拓康生物医药(天津)有限公司首席运营官
35. 李安平 瀚盟测试科技(天津)有限公司总经理
36. 李剑光 浙江海昶生物医药技术有限公司首席科学家
37. 李金亮 奥锐特药业(天津)有限公司总经理
38. 李九远 宏科百世投资管理有限公司合伙人
39. 李林鲜 深圳深信生物科技有限公司创始人
40. 李龙承 中美瑞康核酸技术(南通)研究院有限公司董事长
41. 李守军 天津瑞普生物技术股份有限公司董事长
42. 梁子才 苏州瑞博生物技术有限公司董事长
43. 林殿海 浙江优诺金生物工程有限公司董事长
44. 林金钟 上海蓝鹊生物医药有限公司联合创始人兼CSO
45. 刘 沛 国家药品监督管理局政策法规司原司长
46. 刘克良 军事医学研究院毒物药物研究所研究员、中国生化制药工业协会多肽分会专家委员会主任委员
47. 刘艺锦 南开大学药物化学生物学国家重点实验室教授
48. 刘岳琪 天津博创合成生物科技有限公司董事长助理
49. 陆 阳 苏州圣诺医药技术有限公司董事长
50. 逯晓云 天津中合基因科技有限公司CEO
51. 马玉新 天津南开和成科技有限公司董事长
52. 孟凡宏 金杜律师事务所合伙人
53. 孟庆斌 军事医学研究院毒物药物研究所研究员、中国生化制药工业协会多肽分会秘书长
54. 彭育才 珠海丽凡达生物技术有限公司创始人
55. 邵宁生 军事医学科学院基础医学研究所研究员
56. 施 扬 天津博纳艾杰尔科技有限公司总经理
57. 施章杰 北京欧凯纳斯科技有限公司董事长
58. 石 平 芜湖华仁科技有限公司总经理
59. 舒东旭 上海舶望制药有限公司联合创始人兼CEO
60. 司端运 天津有济医药科技发展有限公司CEO
61. 宋相容 四川大学华西医院生物治疗全国重点实验室研究员
62. 宋艳民 天津全合诚科技有限责任公司董事长
63. 苏晓晔 石药集团有限公司核酸药物研究院院长
64. 孙 涛 南开大学药物化学生物学国家重点实验室教授
65. 孙春光 天津奥瑞芙生物医药有限公司总经理
66. 汤新景 北京大学药学院教授、天然药物及仿生药物全国重点实验室PI
67. 万金桥 成都先衍生物技术有限公司董事长、总经理
68. 汪 云 中国生化制药工业协会会长
69. 汪群杰 天津博蕴纯化装备材料科技有限公司董事长
70. 王海盛 思合基因(北京)生物科技有限公司创始人兼CEO
71. 王 均 华南理工大学医学院和生命科学研究院教授
72. 王升启 军事科学院军事医学研究院研究员
73. 王为民 苏州圣因生物医药有限公司创始人兼CEO
74. 王晓稼 中国科学院大学附属肿瘤医院(浙江省肿瘤医院)乳腺肿瘤内科主任
75. 王泽峰 中国科学院上海营养与健康研究所研究员
76. 魏文胜 北京大学教授、圆因(北京)生物科技有限公司科学创始人
77. 吴 芩 中国科学院杭州医学所特聘研究员
78. 席 真 南开大学化学学院教授、农药国家工程研究中心主任
79. 徐嵘松 广东威立特尔生物医药科技有限公司创始人兼CEO
80. 徐胜平 上海创诺医药集团有限公司董事长
81. 徐增军 艾斯拓康生物医药(天津)有限公司总裁
82. 荀 标 天津经开区核酸产业联盟特聘专家
83. 杨 赟 上海合全药业有限公司联合创始人兼CTO
84. 杨朝勇 厦门大学化学化工学院教授
85. 杨宪斌 圣诺医药大中华区CSO
86. 杨永胜 浙江海昶生物医药技术有限公司副总裁兼核酸创新研究院院长
87. 杨玉龙 法尔玛国际健康管理有限公司总经理
88. 杨振军 北京大学药学院教授、制能(北京)生物科技有限公司创始人
89. 姚庆佳 斯芬克司药物研发(天津)股份有限公司董事长
90. 尹 正 三一创新(北京)投资管理有限公司创始人与管理合伙人
91. 英 博 苏州艾博生物科技有限公司创始人兼CEO
92. 于涵洋 南京大学现代工程与应用科学学院教授
93. 余 蓉 四川大学华西药学院教授、中国生化制药工业协会专家委员会委员
94. 宇学峰 康希诺生物股份有限公司董事长兼首席执行官
95. 喻建华 凯莱英医药集团副总经理
96. 袁 铭 Cytiva中国基因药物运营公司总经理
97. 袁洪雨 天津辰欣药物研究有限公司总经理
98. 袁旭东 艾康药业创始人&CEO
99. 詹濮源 天津创业投资有限公司总经理助理、党办主任
100. 张 丹 俄罗斯工程院外籍院士、昆翎医药联合创始人兼首席战略官、兴湾生物首席科学家
101. 张必良 中科院广州生物医药与健康研究院研究员、广州市锐博生物科技有限公司董事长、阿格纳生物制药有限公司董事长
102. 张华伟 四面体(天津)化学试剂有限公司总经理
103. 张立云 南开大学药物化学生物学国家重点实验室教授
104. 张林琦 清华大学医学院教授
105. 张佩琢 苏州吉玛基因股份有限公司董事长
106. 章金刚 原军事医学科学院野战输血研究所研究员
107. 赵 海 苏州欧利生物医药科技有限公司董事长
108. 赵 宣 天津键凯科技有限公司董事长
109. 赵孝斌 浙江海昶生物医药技术有限公司创始人兼总裁
110. 赵志刚 北京天坛医院主任药师
111. 郑 伟 天津津亚电子有限公司研发总监
112. 朱 涛 康希诺生物股份公司首席技术官
识别微信二维码,添加生物制品圈小编,符合条件者即可加入
生物制品微信群!
请注明:姓名+研究方向!
版
权
声
明
本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观点,不代表本站立场。
核酸药物上市批准
2024-03-13
关注并星标CPHI制药在线3月8日,维昇药业(VISEN Pharmaceuticals)宣布中国国家药品监督管理局(NMPA)已受理隆培促生长素(lonapegsomatropin,Skytrofa)的上市许可申请(BLA)。隆培促生长素是第一个在欧美获批上市的长效生长激素,每周注射一次,用于治疗儿童生长激素缺乏症。 隆培促生长素是采用全球极具创新性的TransConTM(Transient Conjugation, 暂时连接)专利技术平台设计的人生长激素前药,能够以可控的方式在体内缓慢释放未经修饰的生长激素,血浆半衰期可达30.7(±12.7)小时,支持每周一次给药。 已公布的隆培促生长素针对中国生长激素缺乏症(GHD)儿童患者的3期临床试验数据显示:治疗52周时,隆培促生长素治疗组儿童生长激素缺乏症患者的年化生长速率(AHV)显著高于生长激素日制剂组(10.66厘米/年Vs 9.75厘米/年),达到研究主要终点。 此外,在52周治疗期间,隆培促生长素治疗组和生长激素日制剂组患者的平均胰岛素样生长因子-1(IGF -1)标准差积分(SDS)均增加至正常范围内,且隆培促生长素组相对较高。IGF -1是肝脏对生长激素反应时产生的一种多肽,可刺激软骨细胞增殖、分化和胶原的合成。而且,隆培促生长素耐受性良好,安全性与生长激素日制剂相当。 隆培促生长素由Ascendis Pharma开发,维昇药业拥有其在大中华区的独家开发、制造和商业化权益。2021年8月,该药被FDA用于治疗年龄在一岁及以上、体重至少11.5公斤、因内源性生长激素分泌不足而导致生长迟缓的儿童患者。2022年1月,该药在欧盟被批准用于治疗因内源性生长激素分泌不足而导致的3-18岁儿童和青少年生长迟缓。据公司财报,隆培促生长素2022年、2023年销售额分别为35百万欧元和179百万欧元,预计2024年将达到320-340百万欧元。 生长激素药物的发展迭代 生长激素缺乏症(GHD),又称垂体性侏儒,因下丘脑-垂体轴的器质性病变或是功能性异常导致生长激素缺乏引起,患者不仅表现为身材矮小,还存在代谢异常、心理社会挑战、认知缺陷和生活质量差等问题。据公开资料,我国儿童患矮小症的比例约为3%,其中GHD最为常见,占比约三分之一。补充生长激素是目前公认治疗儿童GHD最有效方法之一。 生长激素是人脑垂体前叶嗜酸性细胞分泌的一种长度为191个氨基酸的肽类 激素,通过刺激肝脏等组织产生胰岛素样生长因子(IGF -1)发挥生理功能,促进骨骼生长,促进蛋白质合成,调节脂肪、糖、矿物质代谢等,在人体生长发育过程中发挥重要作用。 根据制备技术的迭代,生长激素药物的研发经历了五代更替。其中第一代生长激素从人脑垂体中提取,存在来源受限、传递传染性疾病的风险,且会引起慢性脑部海绵样变性导致死亡,世界各国已相继停用。第二代生长激素是利用大肠杆菌包涵体技术合成的基因重组人生长激素(rhGH),与天然生长激素结构不同,由192个氨基酸组成,但容易产生抗体影响疗效,目前已淘汰。第三代生长激素是利用普通大肠杆菌以及哺乳动物真核表达系统,表达合成的含有191个氨基酸的 rhGH ,结构与hGH还有差异,存在易产生抗体、成本高和易污染等缺点。第四代生长激素是利用哺乳动物细胞重组DNA技术合成的含有191个氨基酸的生长激素,其结构和天然的生长激素结构更为接近,目前仅被极少数生产厂家沿用。第五代生长激素是利用分泌型大肠杆菌表达技术合成,其氨基酸含量、序列和蛋白质结构与人垂体生长激素完全一致,因此生物活性高、免疫原性低、副作用少。 剂型上,目前市面上的生长激素产品包括短效粉针、短效水针和长效水针,其中粉针粉针和短效水针在疗效上没有显著差异,但针粉临床使用繁琐,注射前需抽取抑菌水注入冻干粉容器中重新配制,不过其稳定性较水针好。 金赛药业领跑,国内多款生长激素产品获批上市 目前,国内已批准多款生长激素产品,详见下表。整体来看,国内生长激素持有企业比较集中,主要为金赛药业、安科生物等。其中金赛药业是国内生长激素的领军企业,且是国内唯一实现短效粉针、短效水针、长效水针三种剂型全部上市的企业。 据米内网数据,2022年中国城市公立医院、县级公立医院、城市社区中心以及乡镇卫生院(简称中国公立医疗机构)终端生长激素销售规模约为67亿元,其中金赛药业是行业老大,市场占比超80%:在粉针剂市场,金赛药业市场份额占比超50%;在水针剂市场,金赛药业市场份额高达99%;金赛增是国内唯一获批的长效水针,2022年销售额超7亿元。 对比国外,国内批准的长效生长激素水针有限,仅金赛药业的金赛增。目前,国外已批准多款长效生长激素水针,即Ascendis Pharma的Skytrofa、诺和诺德的Sogroya和辉瑞的Ngenla。 上述四款长效生长激素的长效作用机制还不太一样。其中Skytrofa是凭借TransCon技术,该技术可使其给药后以可控方式在一周内缓慢释放未经修饰的活性生长激素,从而发挥作用。Sogroya是一种hGH的长效类似物,由天然的hGH经过修饰以增强其与血浆白蛋白的结合,使其适合每周一次给药。Ngenla也是一种长效hGH类似物,利用OPKO专有的C末端肽段(CTP)长效技术在一段天然生长激素序列的C和N末端分别加上了2个和1个来自人类绒毛膜促性腺激素(HCG)β亚基的CTP拷贝,使其半衰期得以延长。金赛增是全球首支上市的聚乙二醇(PEG)化长效生长激素注射液,其利用天然肽键连接了惰性PEG和天然结构的生长激素,从而降低其被肾脏过滤的速度和蛋白酶对它的降解作用,进而提高其在人体内的稳定性。 此外,微球技术也被开发用长效生长激素领域,如基因泰克的Nutropin Depot、韩国LG Life Sciences的 Declage。其中Nutropin Depot是全球第一个上市的长效生长激素,其采用PLGA缓释微球技术,缓释效果显著,1999年获批上市,但后续因注射局部疼痛,4年后退市。Declage采用的是透明质酸技术,2007年在韩国上市。 长效生长激素有哪些后备军 长效生长激素是儿童GHD生长激素替代疗法研发的热门方向,目前全球药企已研发出多款在研长效生长激素,详见下表。我国药企也积极布局长效生长激素,其中特宝生物的怡培生长激素已于今年1月在国内报产。 怡培生长激素由特宝生物自主研发,其采用40kD Y型分支聚乙二醇(YPEG)分子对rhGH进行单分子修饰,优选高生物学活性、非N-末端位点为主的修饰组分,在保证疗效的同时,旨在降低给药剂量,获得更佳的长期药物安全性。已公布的2/3期研究数据显示:儿童GHD患者接受12周治疗后,怡培生长激素100、120、140μg/kg/周组和重组人生长激素35μg/kg/天组(对照组)的身高增长速度分别为7.07、10.39、12.27厘米/年和11.58厘米/年。 天境生物的伊坦生长激素进展也相对较快,其治疗儿童GHD的3期研究已达到非劣效性主要终点,今年将递交上市申请。该药是基于Genexine的专利hyFc®技术开发,hyFc部分由人 免疫球蛋白D(IgD)和G4(IgG4)的一部分组成。前者包含一个柔性铰链,后者可通过新生儿Fc受体(FcRn)介导的代谢调控延长半衰期。已公布的3期临床试验结果显示:伊坦生长激素组患者的年化身高生长速率(AHV)为10.76厘米/年,而Norditropin(诺泽)组患者的AHV为10.28厘米/年。 值得一提的是,围绕伊坦生长激素药企间达成数项交易。该药由Genexine开发,2015年10月天士力子公司Tasgen(被天境生物收购)与Genexine达成协议,获得伊坦生长激素的中国权益。2021年11月,天境生物将伊坦生长激素的商业化权益授权给济川药业。 安科生物、优诺金的长效生长激素处于2期临床,其中AK2017通过采用Fc融合蛋白结合技术延长半衰期,是重组人GH同源二聚体与通过突变的人IgG4-Fc的融合蛋白。 此外,除了皮下注射生长激素,儿童GHD患者还有望迎来口服疗法。2023年11月,Lumos Pharma生长激素促分泌素受体(GHSR)激动剂LUM-201治疗儿童GHD的两项2期研究(OraGrowtH210研究和OraGrowtH212研究)达到了所有主要终点及次要终点。 总结 生长激素药物的问世给儿童生长激素缺乏症(GHD)患者带来了希望。历经60多年的发展,生长激素药物的研发取得巨大成功,已从每日一次给药实现每周一次给药的跨越。全球儿童GHD的治疗规模也随之扩大,Frost & Sullivan数据显示其2030年有望达到60亿美元。目前,我国也已批准多款生长激素药物,但长效制剂相对国外较少,而且生长激素药物的市场渗透率也比较低。不过随着生长激素纳入集采,我国将有更多的儿童GHD患者接受生长激素治疗。期待未来有更多的新型生长激素药物获批上市,造福众多儿童GHD患者。 参考资料: 1.《生长激素行业深度:长效剂型快速放量,产品出海未来可期》.青山医药笔记.2024-02-07 2.《洞察o创新|慎思而笃行:生长激素发展历程带来的挑战与风险》.全球健康产业创新观察.2023-07-20 3.《临床需求决定研发方向:生长激素的不断进步史》.医学界儿科频道.2022-10-14 【智药研习社近期直播预告】来源:CPHI制药在线声明:本文仅代表作者观点,并不代表制药在线立场。本网站内容仅出于传递更多信息之目的。如需转载,请务必注明文章来源和作者。投稿邮箱:Kelly.Xiao@imsinoexpo.com▼更多制药资讯,请关注CPHI制药在线▼点击阅读原文,进入智药研习社~
财报临床3期
2024-01-31
·药智网
生物制品行业,以大单品为尊。例如智飞生物代理的9价HPV疫苗、华兰疫苗的四价流感疫苗、特宝生物的长效干扰素,都是这一行业里响当当的“黄金大单品”。正是凭借“黄金大单品”派格宾(长效干扰素)快速放量,特宝生物再次交出了亮眼成绩单:预计2023年实现归母净利润5.3亿元到5.8亿元,同比增长84.66%到102.08%。3年卖24亿元,特宝生物如何崛起?下一个增长点又在哪里?01业绩亮眼,源自拳头产品“接力赛”特宝生物成立于1996年,主要专注重组蛋白质药物及其长效修饰领域,公司第二大股东是胰岛素龙头之一的通化东宝。截至2023年底,特宝生物已有5款产品获批上市,包括2005年以前获批的特尔立(人粒细胞巨噬细胞刺激因子)、特尔津(人粒细胞刺激因子)和特尔康(人白介素-11),以及2016年获批的派格宾(国内首款长效产品聚乙二醇干扰素α2b)、2023年6月获批的珮金(长效人粒细胞刺激因子)。其中,2005年以前获批的3款产品,上市时间均超过18年,市场竞争格局已相对成熟,对公司业绩贡献有限;派格宾的竞争格局较优,且处于快速放量期,成为拉动特宝生物业绩增长的主力产品。据业绩预告显示,特宝生物2023年度经营业绩同比实现较大增长的主要原因在于,“随着乙肝临床治愈研究的不断深入,派格宾作为慢性乙肝抗病毒治疗的一线用药,对于提高乙肝患者临床治愈率、降低肝癌风险的作用进一步得到专家和患者的认可,产品持续放量。”图片来源:首创证券研报2023年前三季度,特宝生物实现总营收14.6亿元,同比增长27.69%,归母净利润3.69亿元,同比增长84.08%。其中,第三季度单季业绩表现靓丽,实现收入5.56亿元,同比增长29.86%,归母净利润1.67亿元,同比大幅增长149.78%。究其原因,得益于“公司积极开拓市场,深化核心产品的市场渗透,派格宾的市场需求不断增加,营业收入和盈利水平持续增长”。这也使得公司2023年前三季度实现经营活动产生的现金流量净额3.83亿元,同比增长68.87%。023年卖近24亿,长效干扰素的「隐形冠军」对于生物制品公司,大单品地位关键,是公司发展的核心支柱。作为贡献特宝生物业绩的“黄金大单品”,派格宾自2016年上市后快速爬坡,实现收入占公司总营收比重不断攀升。以近三年数据为例。2020-2022年,特宝生物实现总营收分别为7.94亿元、11.32亿元、15.27亿元,其中派格宾实现收入4.58亿元、7.70亿元、11.61亿元,占公司总收入的比重分别为57.74%、68.02%、76.01%。究其原因,一方面在于派格宾是国内首个自研的长效干扰素产品,在慢乙肝治疗领域保持着领先优势,且疗效显著。针对慢性乙肝患者,传统核苷酸类药物单用仅能实现3%左右的治愈率,而序贯/联用长效干扰素48周可达到超过30%的治愈率(NAs经治优势人群)。另一方面,国内获批的慢乙肝治疗药物类型较少,且患者人数庞大。据《慢性乙型肝炎防治指南(2022年版)》显示,我国慢乙肝感染者约8600万例,其中慢乙肝患者为2000万-3000万例,现有抗病毒治疗人群约500万-600万。相关统计数据显示,我国乙肝的诊断率和治疗率相对较低。尤其在外资竞争对手罗氏退出国内市场后,我国长效干扰素α市场从2023年起由派格宾占据。此前,罗氏宣布自2022年12月31日起与歌礼制药终止派罗欣在中国大陆地区市场的推广合作,同时也表明不会在中国大陆地区开展派罗欣的商业推广。这意味着,派格宾未来销售收入仍有望维持高速增长态势。图片来源:华泰证券研报除派格宾外,特宝生物也在培育潜在大单品,2023年6月新上市的拓培非格司亭注射液(珮金)就是其中之一。珮金为Y型聚乙二醇(PEG)修饰的人粒细胞刺激因子,适用于降低肿瘤患者化疗后的感染发生率,与已上市的同类长效产品相比,具有较长的药物半衰期、较低的药物剂量,药物剂量约为已上市同类长效产品的三分之一,与公司现有上市产品特尔津为长短效产品组合。销售策略上,特宝生物将珮金在中国大陆地区的权益(不含港澳台)授予复星医药全资子公司江苏复星,将获得不低于7300万元的首付款和里程碑款项,后续有望借助复星强大的商业化能力,实现快速放量。03下一个“黄金大单品”,长效生长激素?沿着“打造大单品”这个逻辑,特宝生物在聚焦乙肝主业的同时,向更多疾病领域拓展,其中已申报上市的长效生长激素便深受市场关注。据2023年半年度报告显示,特宝生物正在积极推进长效人生长激素、Y型聚乙二醇重组人促红素(YPEG-EPO)、AK0706和ACT50、ACT60等多个临床研究项目。其中,AK0706是一种全新结构的小分子化合物,用于治疗慢性乙型肝炎。2024年1月11日,特宝生物提交的怡培生长激素上市申请获国家药监局受理,拟用于治疗内源性生长激素分泌不足所致的儿童生长障碍。2023年半年度报告披露,特宝生物已针对怡培生长激素累计投入研发费用1.33亿元。从市场空间看,据药智数据统计,2022年我国生长激素类药物市场规模超过50亿元,逐年增加,有望很快突破百亿大关。可与此同时,生长激素又是一个竞争较为激烈的赛道。我国生长激素赛道呈现出一家独大的局面,长春高新子公司金赛药业凭借上市全部三种剂型(短效粉针剂、短效水针剂和长效水针剂),占据绝大部分市场份额。仅长效水针剂而言,目前国内仅有金赛药业一家获批上市,但后来者来势汹汹,包括安科生物(已申报上市)、天境生物(已完成III期研究)、维昇药业(III期)、诺和诺德(III期),另外还有优诺金、亿一生物和千红药业等已开展临床研究。这意味着,特宝生物面临的竞争压力不小。在慢乙肝治疗领域,特宝生物也在探索不同机制新疗法,采取开放合作的策略,选择在各个技术路线与合作伙伴开展技术合作。2023年5月,特宝生物与Aligos就治疗肝炎的核酸技术合作研发寡核苷酸化合物(siRNA)。特宝生物将获得在中国区域内对该核酸技术进行开发和商业化的独家选择权,Aligos将获得700万美元预付款和研究合作资金,分阶段支付的产品开发、上市销售里程碑费用(最高不超过1.09亿美元)以及按净销售额的一定比例计算的特许权使用费。近年来,核酸药物在乙肝功能性治愈上体现出了治疗优势,已有一些创新药企开展了临床试验,包括罗氏、GSK、腾盛博药、瑞博生物和齐鲁制药等。在其他适应症领域,特宝生物表示将继续围绕免疫相关的细胞因子上下游开发产品,布局的主要方向聚焦在免疫和代谢领域。其中,在研管线中,ACT50是一种PEG化的针对全新机制靶向V3的新型蛋白质药物,用于治疗肿瘤等相关疾病;ACT60是一种糖皮质激素及IL-2类激动剂的联合药物组合,用于治疗过敏等相关呼吸道疾病;Y型聚乙二醇重组人促红素(YPEG-EPO)用于慢性肾功能不全导致的贫血。04结语生物制品行业以大单品为尊,这一点在特宝生物的发展历程中得到了充分体现。通过打造核心大单品,特宝生物实现了业绩的快速增长,并在市场中获得了广泛的认可。未来,随着公司研发管线的不断推进和新产品的陆续上市,特宝生物或将有望保持强劲的发展势头。参考资料:1.特宝生物财报、公告、官网2.首创证券、华泰证券研报声明:本内容仅用作医药行业信息传播,为作者独立观点,不代表药智网立场。如需转载,请务必注明文章作者和来源。对本文有异议或投诉,请联系maxuelian@yaozh.com。责任编辑 | 绿色转载开白 | 马老师 18996384680(同微信)商务合作 | 张武龙 13368443108(同微信) 阅读原文,是受欢迎的文章哦
财报疫苗
100 项与 浙江优诺金生物工程有限公司 相关的药物交易
登录后查看更多信息
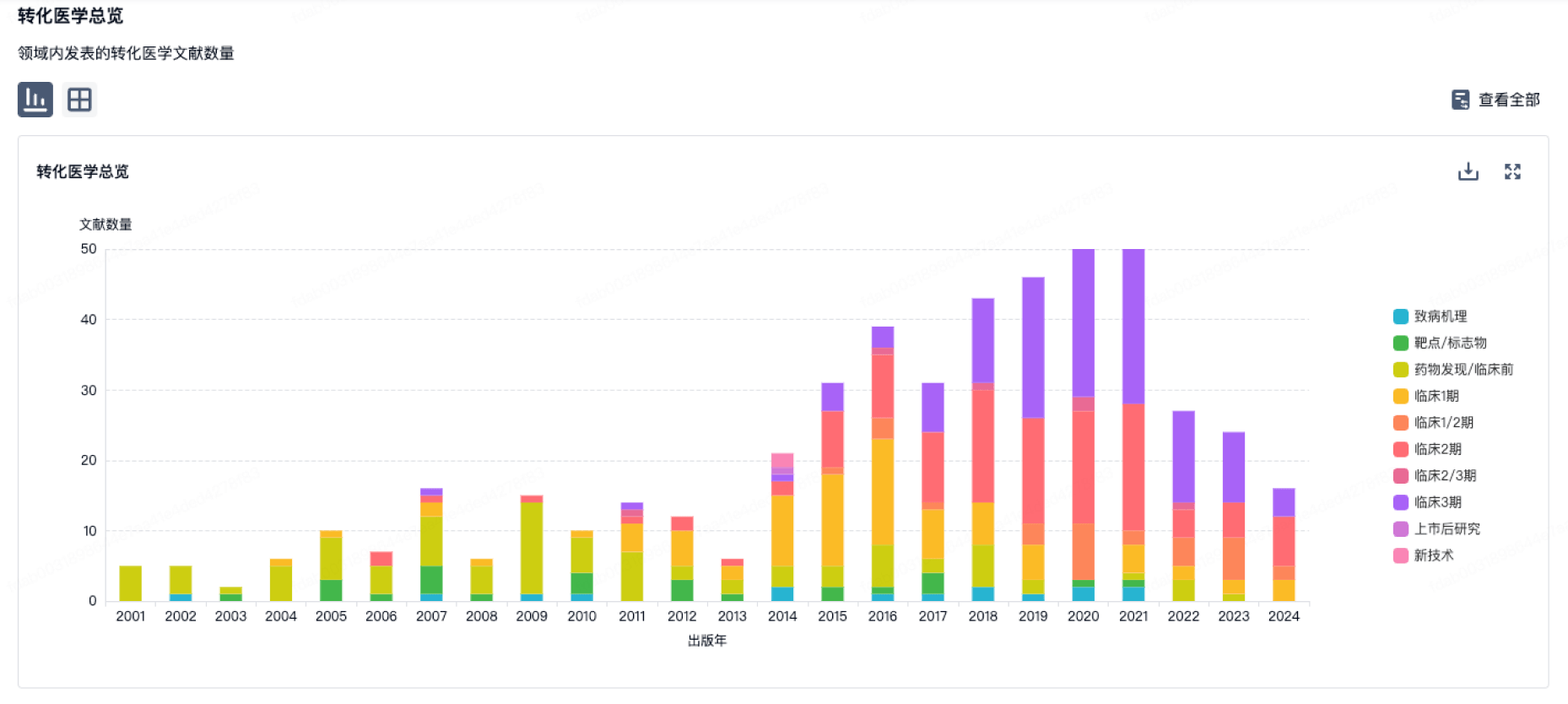
100 项与 浙江优诺金生物工程有限公司 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2025年02月17日管线快照
管线布局中药物为当前组织机构及其子机构作为药物机构进行统计,早期临床1期并入临床1期,临床1/2期并入临床2期,临床2/3期并入临床3期
临床前
6
1
临床3期
登录后查看更多信息
当前项目
| 药物(靶点) | 适应症 | 全球最高研发状态 |
|---|---|---|
人血白蛋白-生长激素融合蛋白(浙江优诺金生物工程有限公司) ( GHR ) | 生长激素缺乏症 更多 | 临床3期 |
YDK-01 ( GHR ) | 生长激素缺乏症 更多 | 临床前 |
YDK-06 | 骨质疏松症 更多 | 临床前 |
YDK-03 ( IGF-1R ) | 胰岛素样生长因子I缺乏症 更多 | 临床前 |
YDK-04 ( GHR ) | 生长激素缺乏症 更多 | 临床前 |
登录后查看更多信息
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
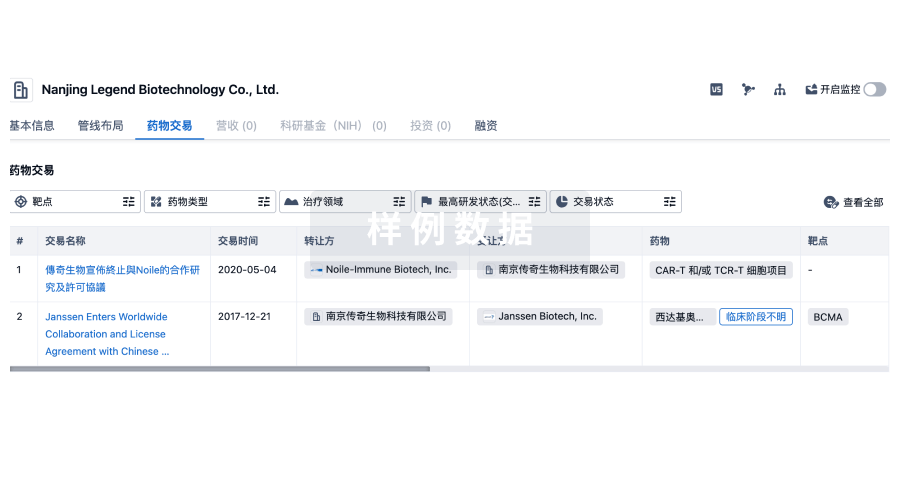
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
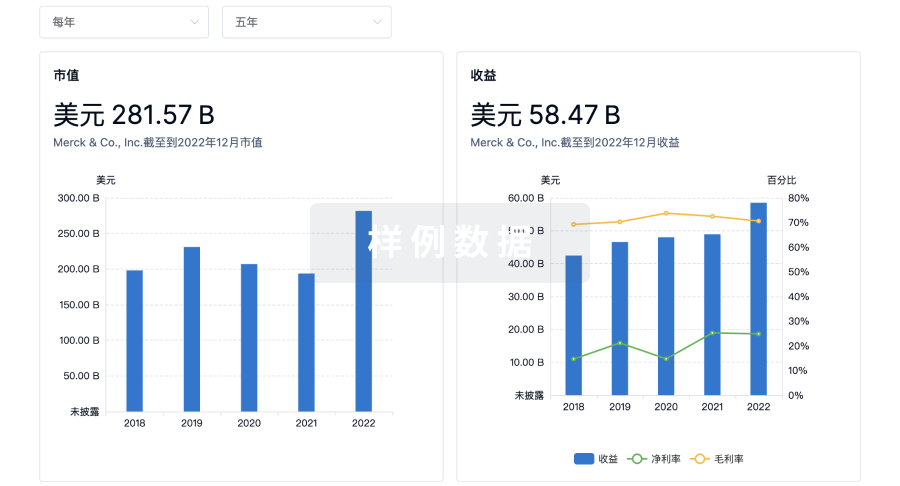
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
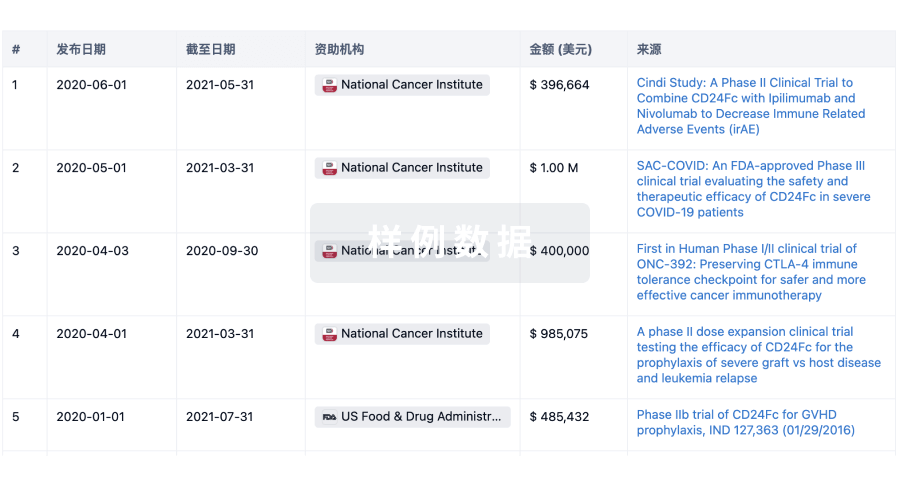
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
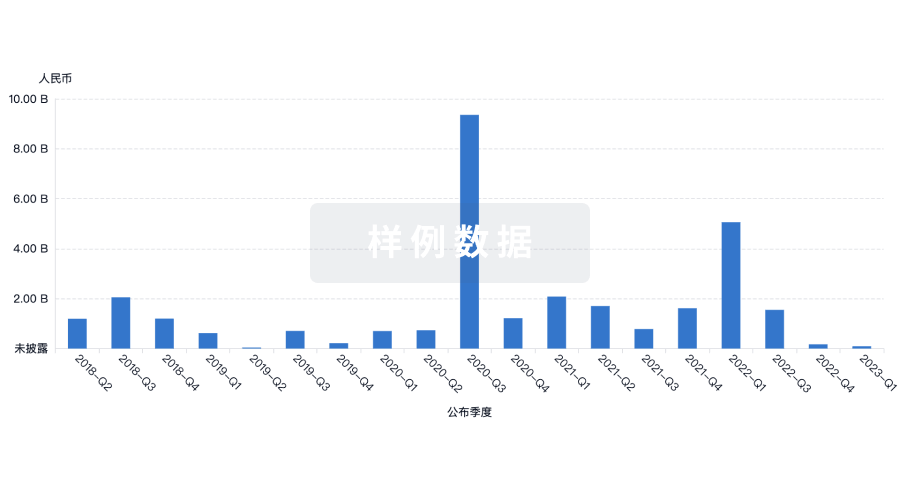
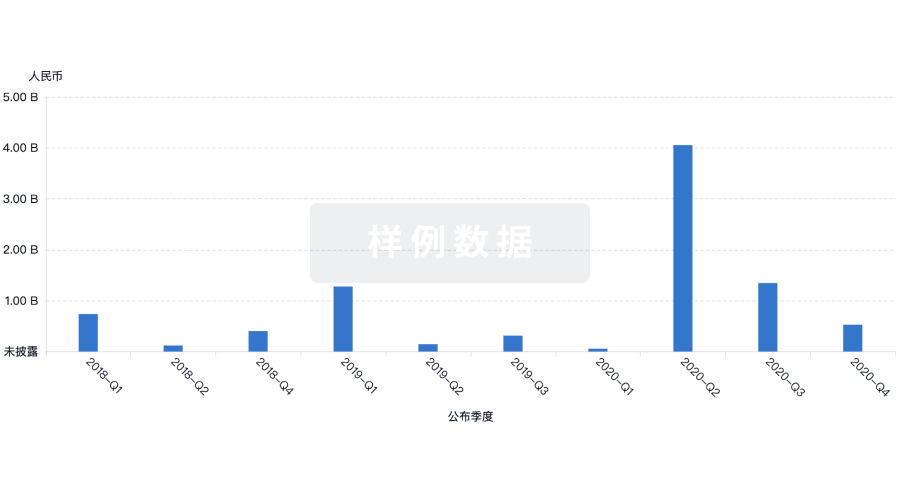
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用