预约演示
更新于:2025-01-23

Beijing Children's Hospital.Captital Medical University
首都医科大学附属北京儿童医院|
中国北京市
首都医科大学附属北京儿童医院|
中国北京市
更新于:2025-01-23
概览
关联
10
项与 首都医科大学附属北京儿童医院 相关的临床试验NCT06489951
Efficacy and Safety of Short-term High-dose Vitamin D Supplementation Combined With Standard Behavioral Therapy for the Treatment of Dry Overactive Bladder in Children: a Prospective, Randomized Controlled, Multicentre Clinical Study
The aim of this study is to give children with dry OAB: (1) Standard behavioral therapy combined with classical anticholinergic drugs (Solinaxine), or (2) standard behavioral therapy combined with short-term high-dose exogenous vitamin D supplementation are used to compare the outcomes of lower urinary tract symptoms in children with dry OAB during follow-up. To provide more robust supporting evidence for the broader promotion of short-term high-dose exogenous vitamin D supplements in combination with standard behavioral therapy as an effective treatment for dry OAB treatment in children.
开始日期2024-12-01 |
申办/合作机构  重庆医科大学附属儿童医院 重庆医科大学附属儿童医院 [+2] |
CTR20233531
巯嘌呤微片在餐后条件下相对生物利用度研究
本试验旨在研究单次餐后口服华润双鹤药业股份有限公司研制、生产的巯嘌呤微片(5 mg)的药代动力学特征;以Quinn Pharmaceuticals持证的巯嘌呤片(50 mg)为参比制剂,比较两制剂中药动学参数Cmax、AUC0-t、AUC0-∞,评价两制剂的人体药代动力学差异。
探索性分析:评价两制剂的人体生物等效性。
开始日期2023-11-13 |
申办/合作机构 |
NCT06078969
The Efficacy of Oral Prednisone in Treating Langerhans Cell Histiocytosis of Bone in Childhood and Adolescence: A Multi-center, Open-label, Randomized-controlled, Phase II Study
Langerhans cell histiocytosis (LCH) of bone is a benign-tumor-like osteolytic lesion in childhood and adolescence, which is characterized by the aberrant activation of antigen presenting cells. Rather than the multi-system involvements of LCH, no standard or widely-accepted therapeutic regimens were established for LCH of bone. In the previous clinical practice, several LCH patients obtained remarkable pain relief after taking prednisone. Therefore, the investigators aim to conducting a multi-center, open-labelled, randomized-controlled, Phase II study to investigate the efficacy and safety of oral prednisone in treating LCH of bone in children and adolescents. The enrolled patients will be randomly recruited to the following groups: (1) Oral prednisone [Test group); (2) Regular observation [Control group].
开始日期2023-11-04 |
申办/合作机构 上海长征医院 [+11] |
100 项与 首都医科大学附属北京儿童医院 相关的临床结果
登录后查看更多信息
0 项与 首都医科大学附属北京儿童医院 相关的专利(医药)
登录后查看更多信息
107
项与 首都医科大学附属北京儿童医院 相关的新闻(医药)2025-01-16
流感药、报案、利润下跌、新股东,为关键词
图/视觉中国
No.1
今冬还囤“流感药”?
工信部的回答来了
2025年的第一周,全国流感病毒阳性率较上周上升了3.8%。中国疾控中心数据显示,流感仍处于季节性流行期。
同时,工信部重点监测了两款抗病毒流感药,分别是玛巴洛沙韦和磷酸奥司他韦。
在1月12日国家卫健委召开新闻发布会上,工业和信息化部消费品工业司副司长王孝洋回答《财经》提问,目前玛巴洛沙韦总体库存充足,干混悬剂剂型的主要对医疗机构保持常态化供应,线上渠道正在组织企业进一步加大投放规模。
玛巴洛沙韦是一种进口药,分为片剂和干混悬剂两种剂型,其中干混悬剂主要用于吞咽困难的儿童。
已经过了专利期的磷酸奥司他韦,则有多家国产药企生产。由于往年的流感季中,曾经出现过抢购磷酸奥司他韦的现象,工信部在2024年10月专门到国内龙头生产企业调研,组织企业加强生产供应。
目前,磷酸奥司他韦在中国有生产批件100多个,生产企业60余家,实际在产的企业30多家。全国日产能达到了156万人份、库存超过4700万人份,其中儿童用的颗粒剂型库存超过1600万人份。
王孝洋强调,其实磷酸奥司他韦的需求量与往年同期相比是在下降的,目前产能产量充足。
这两款抗病毒药物都是处方药,首都医科大学附属北京儿童医院主任医师徐保平提醒,“如果怀疑得了流感以后,应该及时到医院就诊,根据医生的处方使用抗流感病毒药物。不建议自己使用处方药。”
除了抗病毒药物,解热镇痛、抗生素、中药等需求也都有所增加。应对市场需求,连花清瘟的日产能达到了1.2亿颗、库存超过了8600万盒;布洛芬日产能达到1.5亿片,这些品类都具备增产和扩产的能力。
此类药物也都纳入中央和地方的医药储备中,可随时紧急调用,中央医药储备还存有磷酸奥司他韦的中间体,能够用于紧急扩产。
更关键的是,流感高峰即将过去,人们也不必急于“囤药”。中国疾病预防控制中心数据显示,流感检测阳性率上升趋势已经减缓,随着中小学校的陆续放假,预计在1月中下旬,流感活动水平可能会逐步下降。
No.2
医保基金
启动对医疗机构即时结算改革
自2025年1月1日起,实行医保基金结算改革新模式。
过去,医保基金对医疗机构结算一直是“后付制”,即:参保患者出院时只缴纳个人自付费用,医保报销部分需要当月进行逐笔汇总,于次月15日前向医保经办机构申请支付;医保经办机构受理后,再在30个工作日内完成审核、拨付等流程。
这种基金拨付方式存在滞后性,一笔医保应付费用,自患者出院后一般需要60天才能到医院账户上。如遇到异常结算需要沟通复议等情况,有时需要更长时间才能到账,不利于医院资金流转。
住院医保基金即时结算新模式,如安徽省模式——“日拨付、月结算、年清算”的医保基金结算机制,即:患者办理出院结算时,医保信息平台业务子系统实时抓取患者的医保结算信息,自动按照医保基金支付金额的60%予以拨付。
这意味着医保基金拨付时限由通常60天左右压缩至一天,大大缩短医保基金对医疗机构的回款周期,缓解医疗机构垫付资金压力,提高医保基金使用效率。以2024年全省住院医保基金支出额测算,将有170多亿元医保基金提前2个-3个月支付给定点医院。
“实施即时结算改革后,医院每天都能按比例收到上一天发生的住院医保基金,这些真金白银缓解了医院垫付资金的压力,为医院可持续发展赋能助力。”安徽省人大代表、淮北市人民医院刘永刚院长说。
No.3
国药集团报案称
药材股份伪造印章
1月10日、11日连续两天,国药集团及全资子公司中国中药有限公司(下称“国药中药”)先后在官网发布声明,直指国药药材股份有限公司(下称“药材股份”)冒用前两者名义,涉嫌侵害两者商标权、不正当竞争,以及伪造印章等行为。
国药集团声明称,自2016年11月起,国药集团及国药中药在药材股份的持股比例为25%。对药材股份,国药集团、国药中药既非控股股东,也非实际控制人。
国药集团表示,从未授权药材股份及其所属企业以“中国医药集团有限公司”“中国医药集团”“国药集团”“国药集团成员企业”等名义开展宣传、投资等行为,也未授权其使用国药集团注册商标。
药材股份于2000年10月成立,重点业务领域包括中草药育种研发与育种基地建设、中草药种养殖基地建设运营、中草药交易市场(线上+线下)建设运营、中草药材仓储与物流、中药饮片加工与销售等
据前述声明,对药材股份涉嫌侵害国药集团、国药中药商标权和不正当竞争行为,以及虚构股东大会会议,伪造股东大会决议、伪造国药中药董事签字、伪造变造公司章程等违法行为,国药集团、国药中药已依法提起诉讼并获法院支持;对药材股份伪造印章等涉嫌犯罪行为,已向公安机关依法报案。
实际上,国药集团、国药中药与药材股份之间的“纠葛”由来已久。2022年7月至2025年1月,国药集团在官网发布过近20次关于未授权、冒名的声明、公告,其中至少六次涉及药材股份。
No.4
118亿元
招商局拟成为人福医药控股股东
2025年1月15日晚间,人福医药(600079.SH)发公告称,其控股股东武汉当代科技产业集团股份有限公司(下称“当代科技”)的重整投资协议已正式签署,招商局创新科技(集团)有限公司(下称“招商创科”)成为当代科技的重整投资人。
此前,当代科技因陷入债务困境,于2024年9月30日被湖北省武汉市中级人民法院裁定受理重整,并指定清算组担任管理人。在公开招募重整投资人的过程中,共有六家投资人通过形式审查并缴纳报名保证金,成为合格报名重整投资人。最终,招商创科在2025年1月15日与当代科技及管理人签署了重整投资协议。
根据协议内容,招商创科将作为重整投资人参与当代科技的重整。其将在武汉市东湖新技术开发区全资设立招商局生命科技(武汉)有限公司(暂定名,下称“招商生科”),并计划投资总额达118亿元。通过一系列安排,招商生科将合计控制当代科技持有的人福医药23.70%股票的表决权,其中包括直接持有6%公司股票、通过新设有限合伙企业持有6%公司股票以及持有信托计划的优先受益权份额并获得11.70%公司股票表决权委托等。
投资款的支付将分两期进行。第一期投资款占投资总额的60%,即70.80 亿元,在满足一系列先决条件后支付;第二期投资款占投资总额的40%,即47.20亿元,支付条件包括第一期投资款先决条件的满足或豁免、相关股票过户以及有限合伙企业和信托计划的成立等。
No.5
万泰生物预计
2024年净利润跌超九成
1月15日,万泰生物(603392.SH)披露2024年年度业绩预减公告:预计2024年年度实现归母净利润为8600万元-1.2亿元,同比减少93.11%-90.38%;扣非净亏损2.2亿元-1.55亿元,同比减少120.4%-114.38%。
对于本期业绩变动的原因,万泰生物在公告中指出,由于报告期内公司疫苗板块受市场调整、政府集采及九价HPV疫苗扩龄等影响,销售不及预期,疫苗板块收入及利润出现大幅下降,导致净利润出现亏损。同时,公司通过多方式、多渠道推动国际市场销售,海外营业收入较去年同期实现55%的增长。
万泰生物的主营业务分为疫苗和体外诊断两大板块。最重要的疫苗板块,该公司占据了先发优势,在2019年获批首个国产宫颈癌疫苗,其上市后疫苗业务逐渐成为万泰生物最主要的收入来源,万泰生物的归母净利润迅速上涨,2019年-2022年,分别为2.089亿、6.770亿、20.21亿和47.36亿,2020年-2022年同比增速分别为224.13%、198.59%和134.28%。
不过,目前,这款国产二价HPV疫苗已不具市场独占性,在沃森生物进入战场后,马上开启了价格战模式。而价格战下,万泰生物和沃森生物的业绩均受到拖累。2024年,一则沃森生物二价HPV疫苗采购价降至27.5元/支的消息震惊行业,从最初的300元降价至几十元,有媒体称其将价格打到了“一杯奶茶钱”。
而整体市场需求疲弱。从签发情况来看,西南证券的数据显示,2024年上半年共签发了97批次HPV疫苗,同比下降72%。其中,双价HPV疫苗签发33批次,其中万泰生物签发了25批次,同比下降89%;沃森生物签发了六批次,同比下降74%。
被业内认为或成为万泰生物新的利润增长点是九价HPV疫苗。不过,九价HPV疫苗后续的竞争环境同样激烈,除了万泰生物,康乐卫士、上海博唯、瑞科生物、沃森生物都已进入三期临床。
往期 · 推荐
别错过优质内容,记得设置星标或在看哟
并购专利到期
2025-01-15
·动脉网
眼下正值流感高发季,很多人不免焦虑。
人们比以往更关注自己呼吸道的异常反应,更急于找到病因,希望赶在黄金治疗窗口期用上药,尽量缩短病程。而这种扑面而来的焦虑,激发出对药物和检测的需求,往往异乎寻常的大。
在2023年的冬春之交,困扰3亿人的流感焦虑,就曾引爆呼吸道多联检市场。2023年末,美团和京东的互联网医疗板块相继上线呼吸道病原的居家快检。通过互联网平台,消费者可以在家下单,由骑手上门取样,随后平台上的医生会根据检测结果,给出处方或者用药建议。这种在院外形成的从检验到就医、用药闭环,在患者挤爆医院的流感高发季,一上线就颇受追捧。
根据美团买药在2024年世界流感大会上提供的数据,从2023年8月至2024年5月间,呼吸道多病原居家检测数量超50万人次,几乎相当于全国哨点医院全年的流感样样本送检量。这也引爆了2024年呼吸道多联检的开发热潮。
据动脉网统计,2024年,国内共13款呼吸道多联检试剂获批上市,创下历史新高,更多的检验企业,也通过样本外送的方式,加入这样流感焦虑引发的激战。而上一次如此密集的检测产品开发,还是在HPV检测流行之初,但此番产品上线之迅速、技术迭代之频繁,远超以往。
01
呼吸道感染风再起
自2023年初开始,呼吸道感染的风似乎就没有停过。
根据北京疾控中心统计,2023年全年,各种病原体交替爆发。2月至3月间,流感病毒肆虐全国。进入4月后,呼吸道合胞病毒开始传播,并在5月至6月间升级为国内呼吸道感染的主要病原体。到了7月,肺炎支原体、副流感病毒开始流行,主导了此后4个月间高发的呼吸道感染。11月,尽管肺炎支原体感染仍处于高位,呼吸道合胞病毒、流感病毒又卷土重来。
这样的流行趋势,在2024年几乎被复刻。从目前的监测数据看,呼吸道病原体交替爆发的风波,2025年还会持续,程度可能超过2023年的极致水平。根据国家疾控中心的流感监测周报,2024年12月23日至2024年12月29日间,南方省份哨点医院报告的流感样病例占总门诊人数的比例为 5.7%,高于前一周和2021年同期水平。同时,北方省份哨点医院报告的这一数据为7.2%,同样高于前一周水平,甚至超出2021年至2023年间的同期水平。
当然,大多数情况下,呼吸道感染并不会造成太严重的后果。但这类疾病的及时、正确处置,却让医院和患者都十分棘手。
一方面,呼吸道感染人数多、分布广、病程短,并且具有传染性。早在2019年,因呼吸道感染而就诊的人数,就达到3.08亿人。如果患者样本在传统实验室完成检测,需要等待较长时间后出结果,从而延长门急诊患者在医疗服务场所的等待时间,增加呼吸道传染病院内传播的风险。
另一方面,也是更重要的一点,呼吸道疾病中混合感染的比例较高。根据国家疾控中心的数据,23.3%的急性呼吸道患者合并感染超过两种病毒或细菌,如果只检测单一病原体,容易导致漏诊误诊,影响治疗效果。
从这个意义上讲,快速、易于普及的检测工具,成为呼吸道感染亟待满足的临床需求。2024 年 2 月,国家卫生健康委在2024年各专业质控工作改进目标中明确提出,提高抗流感病毒药物使用前流感病原学诊断阳性率,提高住院患者抗菌药物治疗前病原学送检率。次月,国家感染病质控中心发布《发热门诊患者就诊指引》,要求医疗机构应结合传染病流行特点,配置多种病原体的抗原检测和抗原多联检项目,并建议有条件的医疗机构在发热门诊开展对常见病原的即时检验和多联检项目,以进一步提高检测效率。
正是在临床需求和监管引导的双重推动下,国内呼吸道多联检市场迎来了快速发展的周期。
02
跨界者将产品卷出新高度
一直以来,针对呼吸道感染的经验用药广受诟病,但改变这种现状的过程,却缓慢而曲折。这与呼吸道感染的病原体本身复杂多样,相应的工具体系相对落后不无关系。
通常,在呼吸道感染进程的不同阶段,可以采用病原体培养、抗原检测、炎症标志物检测、核酸检测、抗体检测等方式,来实现病原学诊断,或者感染类型评价、疗效检测等。临床上,传统的血常规、炎症标志物检测等手段,仍是呼吸道疾病检测的主流工具。但这种方式只能判断是否存在细菌或病毒感染,无法确认具体病原体,而作为呼吸道病原体检测“金标准”的病原体培养,则由于操作复杂、耗时较长,在基层临床实践中已经不常见。
2023年,国家卫健委发布《国家医疗质量安全改进目标》,明确要求提高呼吸道病原体核酸检测覆盖率和呼吸道感染性疾病核酸检测百分比,以及要求提高住院患者抗菌药物治疗前病原学送检率,为医疗机构开展非新冠呼吸道分子检测、报新项目提供了政策支持
近年来,医院的住院部和高等级门引入了分子检测,操作更便捷的胶体金检测也开始在基层医院门诊中铺开。其中,分子检测准确度高、覆盖病程长,随着自动化、检测速度方面等技术要素不断优化,已经展示初完成住院和医院门急诊大规模呼吸道病原体筛查的潜力。也是从2023年开始,沉寂多时的呼吸道病原检测试剂开发进入高潮。到了2024年,国内呼吸道多联检试剂获批数量更是创下历史新高,全年共13款相关试剂获批上市,几乎相当于2015年以来各年度同类试剂获批数量的总和。
值得注意的是,2024年有呼吸道病原检测试剂获批上市的多家企业,此前在这一领域鲜少有布局。比如,基蛋生物、新产业生物此前主要聚焦传统院内体外诊断项目的化学发光试剂开发,他们在2024年获批上市的甲型/乙型流感病毒及呼吸道合胞病毒核酸联合检测试剂盒、呼吸道合胞病毒IgM抗体检测试剂盒,均为该领域获批的首款产品。再如,由于拿下超10重病原的呼吸道检测产品而备受关注的宝创生物、创澜生物,在这一领域的积淀也并不算厚重。由此可见,呼吸道多联检大热的辐射范围,已经超出英诺特生物、圣湘生物等深耕该领域多年的企业,而为更多体外诊断厂商构建新的增长曲线,提供了可能。
2024年国内呼吸道病原检测试剂开发的另一重特点在于,单一产品能够检测的呼吸道病原体数量大大增加。此前,无论基于抗体、抗原,还是核酸做检测,呼吸道病原检测主要针对单一病原体。在2023年海尔施基因的13种呼吸道病原体多重检测试剂盒获批上市前的很长一段时间,英诺特生物覆盖9种病原体的呼吸道感染病原体抗体IgM检测试剂盒,是市场上能够同时检测呼吸道病原体数量最多的试剂。
而在2024年获批的13款试剂种,近半纳入了5种及以上的呼吸道病原体,尤其是到了2024年末,10重及以上呼吸道病原检测试剂成为主流。据了解,已经有企业尝试开发覆盖近30种呼吸道病原体的检测试剂。有意思的是,这些开发多重、超多重呼吸道病原检测试剂的企业,多为该领域的新面孔。比如前面提到的宝创生物、创澜生物,及爱科睿特等,均是如此,他们纷纷通过功能更强大的产品,来开辟自身并不具备先发优势的市场。
此外,在定价层面,性能不断突破天花板的呼吸道多联检试剂,性价比却不断走高。动脉网查询公开信息发现,包括目前呼吸道病原体组合最大的检测试剂在内,各类呼吸道多联检产品的终端销售价格均在1000元以内。并且伴随呼吸道病原体数量的增加,对应的单个病原体检测费用呈下降趋势。比如,6重呼吸道病原体检测的均价约300元,而9重病原体检测试剂的价格则约420元,对应单个病原体检测费用为约50元和46元。
更强的检测能力、更低的产品定价,无疑为呼吸道多联检试剂在临床普及,奠定了重要基础。
03
还能火多久?
呼吸道多联检试剂扎堆上市的背后,是这类试剂销售带来的业绩暴涨,几乎贯穿了整个呼吸道感染流行周期。
首先发力的是圣湘生物。在呼吸道疾病领域,圣湘生物提供单检、多联检、 免疫抗原、耐药基因筛查、病原体二代测序等多种组合方案,相继上线60多种产品。其中,2021年获批上市的六项呼吸道病原体核酸检测试剂盒,覆盖甲型流感病毒、乙型流感病毒、呼吸道合胞病毒、腺病毒、人鼻病毒、肺炎支原体等6种高发的呼吸道病原体,更是成为2023年的明星产品。根据圣湘生物的财务报告,2023年,呼吸道类产品营业收入超4亿元,同比增长达680%。
值得注意的是,圣湘生物还率先尝试数字化的居家监测,直接将C端的呼吸道病原检测推向高潮。2023年圣湘生物与美团、京东等第三方购物平台合作,推出了“居家快检”业务。从京东平台的信息来看,C端业务已经在北京、上海、广州、深圳、苏州、成都、重庆、天津、武汉、杭州等城市展开。文章开头提到的50万人次呼吸道多病原居家检测,就是在这项合作启动后。根据最新财务报告,2024年上半年,圣湘生物营业收入增长和净利润分别增长67.6%、49.1%,呼吸道多联检带来的业绩拉动力,仍在持续。
此外,专注于POCT产品的英诺特生物,也在呼吸道感染大爆发中,挖到了金子。根据最近财务报告,2024年上半年,实现营业收入4.21亿元,同比增长88.3%,其中,净利润2.06亿元,同比增长166.4%,成为国内同期业绩增长最快的IVD企业之一。而在2024年上半年,呼吸道感染检测收入占英诺特生物营业收入比例达98%。
早在2019年,英诺特生物就成为国内呼吸道病原快检市场份额第一厂家。2023年下半年,国内多地出现肺炎支原体感染高峰,英诺特生物儿童急门诊作为切入点,快速将呼吸道多联检产品推向院内。据报道,包括首都儿科研究所附属儿童医院、首都医科大学附属北京儿童医院、上海市儿童医学中心、复旦大学附属儿科医院等在内的国内顶级儿童医院,都引入了英诺特生物的相关产品。其中,英诺特生物2021年获批上市的呼吸道感染病原体抗体IgM检测试剂盒,覆盖肺炎支原体、肺炎衣原体、甲型流感病毒、乙型流感病毒、副流感病毒、呼吸道合胞病毒、腺病毒、柯萨奇病毒、嗜肺军团菌等当季主要的呼吸道病原体,成为主力产品。
不过,在已经杀成一片红海的呼吸道多联检市场,特定的产品和企业想要复制这样的业绩暴涨,似乎并不容易。
一方面,圣湘生物和英诺特生物踩准呼吸道病原感染交替爆发的节奏,有一定的偶然性。
在呼吸道感染爆发之初的2023年,市场上可选择的包含流汗病毒检测的试剂有限,多以呼吸道合胞病毒为靶标,为圣湘生物的六项呼吸道病原体核酸检测试剂盒脱颖而出创造了条件。而英诺特生物除了压中肺炎支原体外,提前聚焦检测需求密集的儿科场景,也策略上推动了相应试剂销售的增长。
另一方面,呼吸道多联检试剂院内应用本身,还处于初期探索阶段,在临床落地、上量方面还有很多亟待解决的问题。
比如收费和医保问题,当前,大多数呼吸道多联检试剂在院内没有独立的收费项目,只能通用病原体DNA、RNA来进行组合收费,这就可能出现医保报销中套收、重复收费的问题。再如,呼吸道多联检的临床价值问题一直存在争议,现阶段,除了部分流感和呼吸道合胞病毒感染已经有特效药上市外,大量呼吸道感染都只能对症治疗,对于是否有必要对用越来越大的靶点组合,来区分病原,尚无定论。而如果多重或者超多重呼吸道病原检测试剂的临床价值被否定,企业就不能通过扩大靶点范围来确保纳入未来流行的病原体,从而产品商业价值将存在极大不确定性。
当然,被流感焦虑加速的呼吸道病原精准检测,极大提升了这种疾病的诊疗效率。但作为一门赚钱的生意,这个赛道的成长还需要时间。
*封面图片来源:123rf
如果您认同文章中的观点、信息,或想进一步讨论,请与我们联系;也可加入动脉网行业社群,结交更多志同道合的好友。
近
期
推
荐
声明:动脉网所刊载内容之知识产权为动脉网及相关权利人专属所有或持有。未经许可,禁止进行转载、摘编、复制及建立镜像等任何使用。
动脉网,未来医疗服务平台
上市批准
2025-01-08
·梅斯医学
“2024年度中国儿科&罕见病领域十大医学研究”正式揭晓。回望2024,我国科学家在儿科&罕见病领域取得了丰硕的研究成果,为世界医学的发展做出了巨大的贡献。
梅斯医学已连续7年发布了年度十大医学进展,研究内容面向中国学者在医学领域取得的重大科学进展和标志性成果,这些研究展现了我国研究实力和学术水平,同时在推进医疗实践、改善医疗质量方面具有重大意义。
在儿科&罕见病领域,今年我们依旧甄选出15项研究进入终选,采取网络投票的方式进行评选,得票数排名前10位入选“2024最受瞩目的中国十大医学研究"。(注:本次排名顺序根据线上票选数量进行排名,若出现总分相同的情况,将按照投票序号前后顺序进行依次排列。)
— 01 —
JAMA Network Open:张惠文教授团队开展中国6种溶酶体贮积症新生儿筛查
doi: 10.1001/jamanetworkopen.2024.10754
溶酶体贮积症(LSDs)是一类由基因突变导致溶酶体水解酶或转运蛋白异常导致其底物在细胞内外堆积所引起的疾病。LSDs包含近60种类型,大部分为常染色体隐性遗传,部分为X染色体连锁遗传。
研究者利用串联质谱法(MS/MS)筛查6种LSDs,包括戈谢病、尼曼匹克病A/B型、克拉贝病、黏多糖贮积症I 型、法布雷病和庞贝病,较准确地评估了上海市6种LSDs发病率情况并判断了患儿的临床分型。该项研究成果为中国溶酶体贮积症发病率及疾病分型提供了重要的数据支撑,这是目前较大规模的关于溶酶体贮积症新生儿筛查的研究成果。
研究表明, MS/MS新生儿酶活性筛查联合基因检测和生物标志物检测及临床分析,成功确认了患儿的临床亚型。上海市常见LSDs综合发病率a高达1/1 856,晚发型占比相对较高。中国人群部分基因存在热点突变,导致对应疾病发病率相对较高,比如GALC 基因c.1901T>C(p.Leu634Ser)变异,SMPD1基因c.995C>G (p.Pro332Arg) 变异,GAA基因c.2238G>C (p.Trp746Cys)变异,GBA1基因c.1448T>C (p.Leu483Pro) 变异。
发表期刊:JAMA Netw Open . 2024 May 1;7(5):e2410754
通讯作者/关键作者:张惠文
主要作者单位:上海交通大学医学院附属新华医院
— 02 —
Nature Medicine:李华伟/舒易来/王武庆/陈正一教授团队终结“无声世界”,迎接耳聋基因治疗新时代
doi: 10.1038/s41591-024-03023-5
耳聋是较为常见的出生缺陷之一。近年来,基因疗法的快速发展给耳聋儿童带来了重获听力的希望。近日,复旦大学附属眼耳鼻喉科医院的李华伟教授、舒易来教授、王武庆教授以及哈佛大学医学院陈正一教授合作团队在《自然-医学》(Nature Medicine)发表了基因疗法(AAV1-hOTOF)治疗双耳遗传性耳聋的临床研究结果。
研究结果显示,所有患儿(5例)双耳听力均得到恢复,言语感知和声源定位能力改善,且未引起剂量限制性毒性或严重不良事件。此研究结果为遗传性耳聋的双耳基因治疗提供了有效性和安全性证据。目前,该研究仍在进行中,将随访观察明确基因疗法的长期安全性和有效性。
此前,该研究团队在《柳叶刀》(The Lancet)发表了全球首个遗传性耳聋单耳基因治疗的研究结果,83%(5/6例)的常染色体隐性遗传性耳聋9(DFNB9)患儿在接受同一基因疗法(AAV1-hOTOF)治疗后听力获得明显改善,并被选为封面导读,获得《柳叶刀》杂志同期点评,被国际同行称为“耳聋治疗的范式转变”、“标志着基因治疗听觉障碍乃至更广泛疾病的新时代开启”。
发表期刊:Nat Med . 2024 Jul;30(7):1898-1904
通讯作者/关键作者:李华伟,舒易来,王武庆,陈正一
主要作者单位:复旦大学附属眼耳鼻喉科医院,哈佛大学医学院
— 03 —
双重磅 Nat Med&Lancet:我国科学家在基因治疗遗传性耳聋取得进展
01 Nat Med:王武清、李华为等教授发布常染色体隐性遗传性耳聋 9 型儿童的双侧基因治疗的单臂试验结果
doi: 10.1038/s41591-024-03023-5
基因治疗是治疗遗传性耳聋的一种有前景的方法。我们最近表明,使用携带人 OTOF 转基因的双腺相关病毒(AAV)血清型 1 进行单侧 AAV1 - hOTOF 基因治疗在常染色体隐性遗传性耳聋 9 型(DFNB9)患者中是安全的,并与功能改善相关。随后该方案被修订并获批允许进行双侧基因治疗。在此我们报告一项单臂试验的中期分析,该试验研究双侧治疗在 5 名 DFNB9 儿童患者中的安全性和有效性。主要终点是 6 周时的剂量限制性毒性,次要终点包括安全性(不良事件)和有效性(听觉功能和言语感知)。共发生 36 例不良事件。最常见的不良事件是淋巴细胞计数增加(36 例中有 6 例)和胆固醇水平升高(36 例中有 6 例)。
所有患者双侧听力均恢复。所有患者基线时右(左)耳的平均听性脑干反应阈值均 > 95 dB(>95 dB),在 26 周时患者 1 右(左)耳的平均听性脑干反应阈值恢复到 58 dB(58 dB),患者 2 为 75 dB(85 dB),患者 3 为 55 dB(50 dB);在 13 周时患者 4 为 75 dB(78 dB),患者 5 为 63 dB(63 dB)。所有 5 名患者的言语感知和声源定位能力均恢复。这些结果为双侧 AAV 基因治疗遗传性耳聋的安全性和有效性提供了初步见解。该试验正在进行中,将进行更长时间的随访来验证其安全性和有效性。
发表期刊:Nat Med . 2024 Jul;30(7):1898-1904
通讯作者/关键作者:王武清,李华为
主要作者单位:复旦大学眼耳鼻喉医院
02 Lancet:舒宜来、李华为教授团队开展AAV1-hOTOF基因治疗常染色体隐性遗传性耳聋 9 型的一项单臂试验
doi: 10.1016/S0140-6736(23)02874-X
由 OTOF 基因突变引起的常染色体隐性遗传性耳聋 9 型,其特征为先天性或语前性、重度至极重度双侧听力损失。然而,目前尚无针对先天性耳聋的药物治疗方法。在本文中,我们报告了使用携带人 OTOF 转基因的腺相关病毒(AAV)血清型 1(AAV1 - hOTOF)进行基因治疗对常染色体隐性遗传性耳聋 9 型儿童的安全性和有效性。
在 2022 年 10 月 19 日至 2023 年 6 月 9 日期间,我们筛选了 425 名受试者的入组资格,并招募了 6 名儿童进行 AAV1-hOTOF 基因治疗(1 名儿童接受了 9×10¹¹ 载体基因组 [vg] 的剂量,5 名儿童接受了 1.5×10¹² vg 的剂量)。所有受试者均完成了直至 26 周的随访。总共观察到 48 例不良事件;46 例(96%)为 1-2 级,2 例(4%)为 3 级(1 名受试者中性粒细胞计数减少)。5 名儿童听力恢复,表现为 0.5-4.0 kHz 平均听性脑干反应(ABR)阈值降低 40 - 57 dB。在接受 9×10¹¹ vg 剂量的受试者中,平均 ABR 阈值从基线时的大于 95 dB 改善至 4 周时的 68 dB、13 周时的 53 dB 和 26 周时的 45 dB。在接受 1.5×10¹² AAV1 - hOTOF 的受试者中,4 名听力恢复的儿童在 26 周时平均 ABR 阈值从基线时的大于 95 dB 变为 48 dB、38 dB、40 dB 和 55 dB。听力恢复的受试者言语感知能力得到改善。
发表期刊:Lancet . 2024 May 25;403(10441):2317-2325
通讯作者/关键作者:舒宜来,李华为
主要作者单位:复旦大学眼耳鼻喉医院
— 04 —
NEJM:倪鑫团队打破“无药可治”困境!齐瑞索韦迈向呼吸道合胞病毒感染治疗的第一步
doi: 10.1056/NEJMoa2313551
儿童呼吸道合胞病毒(RSV)感染疾病负担重。根据《柳叶刀》报告,2019年全球5岁以下儿童RSV相关急性下呼吸道感染病例高达3300万例,住院患儿约360万例,死亡病例逾10万例,其中近一半死亡(近4.6万例)发生在6个月以下的儿童中。
儿童RSV感染的治疗主要依赖于支持和对症治疗,包括畅通气道、辅助氧疗、液体管理、营养支持等,但全球范围内尚无抗RSV病毒的特效药物获批上市。本研究的新型抗RSV药物齐瑞索韦在3期临床试验中显示出积极结果,能够显著降低RSV感染婴幼儿的病毒载量,改善临床症状,这标志着在RSV感染治疗领域取得了突破性进展,将为临床提供了一种新的、有效的治疗方法。
发表期刊:N Engl J Med . 2024 Sep 26;391(12):1096-1107
通讯作者/关键作者:赵顺英;倪鑫,刘瀚旻
主要作者单位:北京儿童医院,首都医科大学附属北京儿童医院,四川大学华西第二医院
— 05 —
JAMA Neurology:赵重波教授团队发布中国首个重症肌无力治疗的III期临床研究
doi: 10.1001/jamaneurol.2024.0044
重症肌无力是一种以骨骼肌无力为特征的慢性自身免疫性神经肌肉疾病,其核心机制在于自身抗体对神经肌肉接头的破坏。为了寻求更有效的治疗方法,研究人员发现新生儿片段结晶化受体(FcRn)拮抗剂efgartigimod和rozanolixizumab具有显著潜力。这两种拮抗剂均通过降低血液循环中的免疫球蛋白G(IgG)水平,成功减轻了全身型重症肌无力患者的症状,为这一疾病的治疗开辟了新的途径。
在这一背景下,来自复旦大学附属华山医院神经内科赵重波教授团队开展了Batoclimab的一项III期临床研究,旨在评估单克隆IgG1抗体batoclimab在全身型重症肌无力患者中的疗效和安全性,验证batoclimab是否能够成为治疗重症肌无力的有效药物,以期为患者提供更安全、更可靠的治疗选择。
结果显示,在成年全身型重症肌无力患者中,batoclimab显著提高了MG-ADL评分的持续改善,同时患者对其的耐受性良好。其临床疗效以及IgG降低程度与先前报道的efgartigimod和rozanolixizumab药物相当。然而,为了进一步了解batoclimab的安全性,未来需要开展更大样本量的研究。
发表期刊:JAMA Neurol . 2024 Mar 4;81(4):336-345
通讯作者/关键作者:赵重波
主要作者单位:复旦大学附属华山医院
— 06 —
JAMA Pediatrics:王海俊教授团队助力儿童肥胖率下降27%!适合中国儿童的全方位干预
doi: 10.1001/jamapediatrics.2021.4375
《中国居民营养与慢性病状况报告(2020年)》数据显示:中国儿童青少年的体重管理不容乐观,6-17岁儿童青少年中,超重率为11.1%,肥胖率为7.9%;6岁以下儿童超重率为6.8%,肥胖率为3.6%。儿童期肥胖会增加成年期肥胖、心脑血管疾病和糖尿病等慢性病发生的风险,给个人、家庭和社会带来沉重负担。既往研究报道,儿童肥胖干预的效果不一致,很难在人群中推广。那么,有没有适合中国儿童的肥胖预防有效策略?
中国学者在JAMA Pediatrics发表一项重磅研究,介绍了有效预防中国儿童肥胖的多中心整群随机对照试验(cluster-RCT)研究成果。这是一项设计严谨的整群随机对照干预研究。研究者纳入了来自北京、山西长治和新疆乌鲁木齐的24所小学中的1392名8-10岁(平均年龄为9.6岁)的儿童。其中12所小学的儿童被随机分配至干预组,12所小学的儿童被随机分配至对照组。
面向干预组儿童,研究者开发了一套基于社会生态模型的综合干预措施,其中包括三大项针对儿童的干预,以促进儿童养成健康的饮食和体力活动习惯,以及两大项针对儿童环境的干预,让学校和家庭支持儿童的行为改变。结果显示,干预组儿童平均体重指数(BMI)相比于对照组降低0.46kg/m2,与研究开始相比,干预组儿童肥胖率相对下降27.0%,明显高于对照组(5.6%)。该研究结果为今后在中国推广儿童肥胖干预措施提供了重要的科学依据。
发表期刊:JAMA Pediatr . 2022 Jan 1;176(1):e214375
通讯作者/关键作者:刘峥;王海俊
主要作者单位:北京大学公共卫生学院
— 07 —
Lancet Oncol:胡锡春、罗志国等教授团队探讨90 基因表达分析指导的部位特异性治疗与经验性化疗对原发部位不明的癌症患者的影响(复旦 CUP-001):一项随机对照试验
doi: 10.1016/S1470-2045(24)00313-9
经验性化疗仍然是原发不明肿瘤(cancer of unknown primary, CUP)患者的标准治疗方法。尽管基因表达谱检测已被用于推断CUP患者的肿瘤组织起源,但其在指导临床治疗中的价值尚未得到证实。该随机对照临床研究旨在评估90基因检测指导的部位特异性治疗对比经验性化疗在CUP患者中的疗效和安全性。
这项单中心随机对照临床研究表明,90基因检测指导的部位特异性治疗相比经验性化疗能够显著改善初治CUP患者的无进展生存期。90基因检测提示的肿瘤组织起源可为CUP患者提供更多的疾病信息并增加治疗选择。
发表期刊:Lancet Oncol . 2024 Aug;25(8):1092-1102
通讯作者/关键作者:胡锡春;罗志国
主要作者单位:复旦大学附属肿瘤医院
— 08 —
Cell Rep Med:瞿介明教授、左为教授合作研究开发肺前体细胞治疗支气管扩张症临床新策略
doi: 10.1016/j.xcrm.2024.101819
支气管扩张症(bronchiectasis,以下简称“支扩”)是一种由各种病因引起的支气管异常和持久性扩张的慢性呼吸道疾病,表现为频繁感染和持续的肺部炎症,肺组织结构破坏不可逆,患者生活质量下降,造成巨大的社会经济负担。目前,针对支扩的治疗方法主要是以抗感染为主的对症治疗,未能真正有效的再生修复受损的肺组织或改善疾病进展。因此,研究者们积极探索基于干细胞的新型再生医学方法,以期为支扩患者提供新的治疗选择。
为了进一步评价自体P63+肺前体细胞治疗支扩的安全性与疗效,研究团队设计开展了一项随机、单盲、对照临床试验。研究对象为确诊支扩且弥散功能指标(DLCO)小于80%的患者,研究入组了37例受试者,最终共35例受试者完成了治疗,随机分为接受气管镜下气道廓清治疗(B-ACT)的受试者18例(对照组)和接受B-ACT+自体肺前体细胞移植治疗的受试者17例(细胞治疗组),两组受试者的基线期数据无统计学差异。其中,细胞治疗组受试者的自体肺前体细胞通过支气管镜刷检取样,在GMP车间培养扩增后,经过一系列严格质控,经纤维支气管镜以1~3×10^6细胞/kg体重的剂量移植到患者自身肺部。
自体P63+肺前体细胞可能为支气管扩张症提供一种有前景的治疗方法,为肺再生医学带来了新视角,未来将进一步探索该技术在肺部疾病中的应用,期待为更多患者带来突破性的治疗手段。
发表期刊:Cell Rep Med . 2024 Nov 19;5(11):101819
通讯作者/关键作者:左为;瞿介明,周敏
主要作者单位:同济大学医学院/附属东方医院;上海交通大学医学院附属瑞金医院
Lancet:王昕教授团队揭示2019年早产儿呼吸道合胞病毒急性下呼吸道感染全球疾病负担和风险因素
doi: 10.1016/S0140-6736(24)00138-7
随着各国政府开始考虑将 RSV 疫苗纳入国家免疫计划,了解早产儿 RSV 相关 ALRI 的全球疾病负担和风险因素,对于制定最佳的 RSV 预防策略至关重要。
研究团队在Lancet杂志上发表了一项研究,旨在评估妊娠 37 周前出生的婴幼儿中 RSV 相关 ALRI 的全球疾病负担和风险因素。研究揭示胎龄<32周早产婴儿比所有婴儿平均发病率和住院率高1.7-3.8倍,并且2岁时住院风险仍是同年龄平均水平的2.3倍 。胎龄32-<37周早产儿出生6月内住院风险是同年龄所有婴儿平均水平的1.9倍。在所有婴儿RSV下呼吸道感染住院负担中,早产婴儿住院负担占25%(早产婴儿人口数约占10%)。RSV下呼吸道感染发病与围产期和社会人口学相关,而重症结局与基础疾病如先天性心脏病、支气管肺发育不良、其他慢性肺病或唐氏综合症等有关(OR=1.40~4.23)。
此外,研究表明中低收入与高收入国家间发病-住院比的差距缩小且住院病死率相近,这一结果反映了中低收入国家早产儿对医院资源有较好的可及性,以及由医疗资源可及性和质量差异所导致的幸存者效应,即高收入国家患基础疾病的早产儿更易幸存(基础疾病患病率是中低收入国家的1.5倍),易罹患重症和死亡。研究还发现发展中国家RSV急性下呼吸道感染发病率、住院率和住院病死率均随时间下降,这一结果反映了风险因素暴露减少、医疗资源可及性和医疗质量的提升。
发表期刊:Lancet . 2024 Mar 30;403(10433):1241-1253
通讯作者/关键作者:王昕,李有
主要作者单位:南京医科大学
— 09 —
Orphanet Journal of Rare Diseases:刘杰教授团队探讨罕见病肺淋巴管肌瘤病中国人群接种COVID-19疫苗的安全性和有效性
doi: 10.1186/s13023-024-03260-4
淋巴管肌瘤病(lymphangioleiomyomatosis,LAM)是一种罕见的多系统肿瘤性疾病,主要特征是肺部弥漫性囊性病变。据最新研究估计,LAM在普通人群中的发病率为每百万成年女性中有5例。由于其罕见性和复杂性,LAM的治疗选择非常有限。目前,主要治疗方法是使用雷帕霉素靶蛋白(mTOR)抑制剂,能稳定部分LAM患者肺功能,改善生活质量。
在新冠疫情背景下,接种疫苗已成为预防COVID-19重症和死亡的关键措施。然而,对于LAM患者来说,接种COVID-19疫苗的安全性和有效性仍然存在不确定性。这主要是由于LAM患者的特殊病情以及他们常用的mTOR抑制剂可能对免疫系统产生影响。因此,研究LAM患者接种疫苗的反应具有重要的临床意义。
本研究通过问卷调查的方式,于2022年12月1日到2023年1月期间收集了来自全国各地181名LAM患者和143名年龄匹配的健康参与者的信息。结果表明,尽管22.7 %的LAM患者对COVID - 19疫苗接种存在犹豫,LAM患者的疫苗接种率低于普通人群。然而,研究也显示LAM患者接种COVID - 19疫苗的安全性与健康人群相当,且疫苗接种可以降低LAM患者COVID - 19症状的发生率。此外,mTOR 抑制剂似乎不会增加 LAM 患者在 COVID-19 期间出现并发症的风险。这些数据将有助于我们更好地理解LAM患者在疫苗接种中的表现,并为他们的疫苗接种策略提供科学依据。
发表期刊:Orphanet J Rare Dis . 2024 Jul 3;19(1):247
通讯作者/关键作者:刘杰,江梅,王蔚林
主要作者单位:广州医科大学附属第一医院,国家呼吸医学中心罕见病与间质性肺疾病专业组
Signal Transduct Target Ther:魏文斌、杨丽萍研究团队探索Bietti 结晶性角膜视网膜营养不良症的基因替代疗法:一项开放标签、单臂、探索性试验
doi: 10.1038/s41392-024-01806-3
Bietti 结晶样角膜视网膜营养不良是一种由 CYP4V2 基因突变引起的遗传性视网膜疾病,可导致劳动年龄人群失明,目前尚无有效治疗方法。在此,我们报告 Bietti 结晶样角膜视网膜营养不良基因治疗的首次人体临床试验(NCT04722107)结果,包括 12 名随访 180 - 365 天的受试者。这项开放标签、单臂探索性试验旨在评估一种编码人 CYP4V2 蛋白的重组腺相关病毒血清型 2/8 载体(rAAV2/8 - hCYP4V2)的安全性和有效性。受试者接受单次单侧视网膜下注射 7.5×10¹⁰个 rAAV2/8 - hCYP4V2 载体基因组。总体而言,报告了 73 例治疗中出现的不良事件,其中大多数(98.6%)为轻度或中度强度,被认为与手术或皮质类固醇相关;未观察到治疗相关的严重不良事件或局部 / 全身免疫毒性。
与基线测量值相比,77.8% 的治疗眼在第 180 天最佳矫正视力(BCVA)有所改善,在分析的 9 只眼中平均 ± 标准差增加了 9.0±10.8 个字母(p = 0.021)。到第 365 天,80% 的治疗眼 BCVA 增加,在评估的 5 只眼中平均增加 11.0±10.6 个字母(p = 0.125)。重要的是,通过多焦视网膜电图、微视野计和视觉功能问卷 - 25 观察到的患者改善进一步支持了该治疗的有益效果。
发表期刊:Signal Transduct Target Ther. 2024 Apr 24;9(1):95
通讯作者/关键作者:魏文斌;杨丽萍
主要作者单位:北京同仁眼科中心
EHJ:夏家红教授团队发文激动PIEZO1分子治疗马凡综合征胸主动脉瘤的新机制
doi: 10.1093/eurheartj/ehae786
马凡综合征(Marfan syndrome, MFS)是一种基因突变引起的遗传性结缔组织疾病。其主要心血管表现为胸主动脉瘤(TAA),严重时引起夹层破裂可危及生命,且有较高的死亡率。目前缺乏有效的药物治疗,手术治疗仍然是目前唯一的治疗方法。因此,深入探究参与马凡综合征TAA的信号通路和有效治疗靶点对于该疾病的治疗至关重要。
MFS TAA的主要病理变化是血管中层平滑肌细胞(VSMC)的表型转换导致的细胞外基质降解重塑、弹性纤维减少、变形断裂,胶原过度分泌。机械敏感离子通道PIEZO1是机体重要的力感应传感器,分布于血管平滑肌细胞上,调控多种心血管系统生理过程,如血压调节、血管发育等。
研究团队首次发现PIEZO1在TAA血管组织中表达减少。在马凡模型小鼠中,tamoxifen诱导的平滑肌细胞PIEZO1特异性缺失(Fbn1C1041G/+; Piezo1flox/flox; Sm22-CreERT2)显著促进了动脉瘤的形成和加重疾病严重程度。血管紧张素II诱导的主动脉瘤模型也展现了相同的效果。该研究国际上首次揭示了PIEZO1在马凡综合征胸主动脉瘤的作用及详细机制,为未来马凡综合征TAA治疗靶点的探究提供了可能性。
发表期刊:Eur Heart J . 2024 Nov 25:ehae786
通讯作者/关键作者:夏家红
主要作者单位:华中科技大学
The Lancet :宋逸/马军教授发文优化方案,应对中国儿童青少年不断变化的健康需求
doi: 10.1016/S0140-6736(23)02894-5
中国正处于人口结构高速转变时期,儿童青少年人口位居世界第二。随着社会经济的发展,中国儿童青少年面临着疾病谱的转变和社会文化压力的加剧。为了全面促进儿童青少年的健康和福祉,政府需要综合考虑儿童青少年人口减少、老龄化、经济增长和环境可持续发展等因素。
本研究综合了全国性调查数据、文献证据和政策文献,并通过多领域学者的合作和青年人参与,深入分析中国儿童青少年的主要健康问题、健康风险、健康决定因素和相关政策(图1),为政府制定和优化儿童青少年健康政策提供科学依据,并提供了可行的政策建议,旨在促进中国儿童青少年的健康和福祉。
过去三十年,中国儿童青少年整体健康状况得到了极大改善,但也面临着新的健康问题和社会挑战。从1990年到2019年,中国5~19岁儿童青少年全因死亡率从每10万人口77.63人下降到27.79人,下降了64.2%。儿童青少年主要疾病负担由传染性疾病转向伤害和慢性非传染性疾病,非传染性疾病成为伤残损失寿命年的主要原因。1995~2019年,7~18岁儿童青少年超重肥胖率从 5.0%上升到 24.2%,视力不良率(包括近视、远视和其他视力问题) 从 41.2%上升到 60.7%。不健康生活行为方式普遍存在,心理健康问题高发,青少年性成熟年龄不断提前,而性教育、咨询和治疗服务却无法满足其日益增长的需求。
发表期刊:Lancet . 2024 May 4;403(10438):1808-1820
通讯作者/关键作者:宋逸,马军;陈天娇,董彬,董彦会
主要作者单位:北京大学公共卫生学院,北京大学儿童青少年卫生研究所,北京大学公共卫生学院
Jama Pediatrics:潘海峰/侯胜平教授团队研究极端环境温度下的青少年全球疾病负担
doi: 10.1001/jamapediatrics.2024.4392
气候变化导致的温度极端化已成为全球儿童和青少年健康的重大威胁。极端环境温度暴露(EHCE)不仅对成年群体产生严重健康影响,对身体更脆弱、调节机制尚未成熟的儿童和青少年尤甚。EHCE会引发一系列生理应激反应,导致自主神经失调、心血管负担增加,甚至导致严重的健康损害。
研究团队使用全球疾病负担研究2019(GBD 2019)数据库,涵盖1990至2019年期间204个国家和地区的0-19岁儿童和青少年数据进行了一项研究,旨在全面了解1990~2019年儿童和青少年EHCE相关疾病的全球负担并分析其时间趋势。结果表明,自1990~2019年,儿童和青少年EHCE相关疾病的全球负担总体呈上升趋势,并且其在不同性别、年龄和社会发展水平方面均存在差异。
发表期刊:JAMA Pediatr . 2024 Nov 4:e244392
通讯作者/关键作者:潘海峰,侯胜平;何义胜,曹凡,王鹏,胡晓
主要作者单位:安徽医科大学公共卫生学院,首都医科大学附属北京同仁医院,北京市眼科研究所,安徽医科大学第一附属医院
— 10 —
Cell Stem Cell:蔡玉佳,李士奇教授团队开展改良慢病毒珠蛋白基因治疗儿童β(0)/β(0)输血依赖性β地中海贫血:一项单中心、单臂试点试验
doi: 10.1016/j.stem.2024.04.021
β0/β0 地中海贫血是输血依赖性 β 地中海贫血(TDT)中最严重的类型,并且仍然是慢病毒基因治疗面临的一个挑战。在此,本团队报告一项单中心、单臂初步试验(NCT05015920)的中期分析,该试验评估一种 β 珠蛋白表达优化且带有绝缘子的慢病毒修饰细胞产品(BD211)在 β0/β0 TDT 中的安全性和有效性。两名女童入组,接受了 BD211 输注,并平均随访了 25.5 个月。两名患者的基因修饰造血干细胞和祖细胞均成功且持续植入。在预处理期间或输注后未出现意外的安全问题。两名患者均实现了超过 22 个月的输血独立性。该治疗将红细胞的寿命延长了超过 42 天。对基因修饰细胞的动态变化、转基因表达和癌基因激活进行的单细胞 DNA/RNA 测序分析显示无显著不良影响。优化的慢病毒基因治疗可能安全有效地治疗所有 β 地中海贫血。
发表期刊:Cell Stem Cell . 2024 Jul 5;31(7):961-973.e8
通讯作者/关键作者:蔡玉佳 ;李士奇
主要作者单位:上海系统生物医学研究中心;中国人民解放军联勤保障部队第920医院
本文仅仅是2024年我国科学家发表的部分重磅级研究成果,相信2025年我国科学家会再创辉煌,取得更多重要的研究成果!
点击下方「阅读原文」 立刻下载梅斯医学APP!
基因疗法临床研究
100 项与 首都医科大学附属北京儿童医院 相关的药物交易
登录后查看更多信息
100 项与 首都医科大学附属北京儿童医院 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2025年04月27日管线快照
无数据报导
登录后保持更新
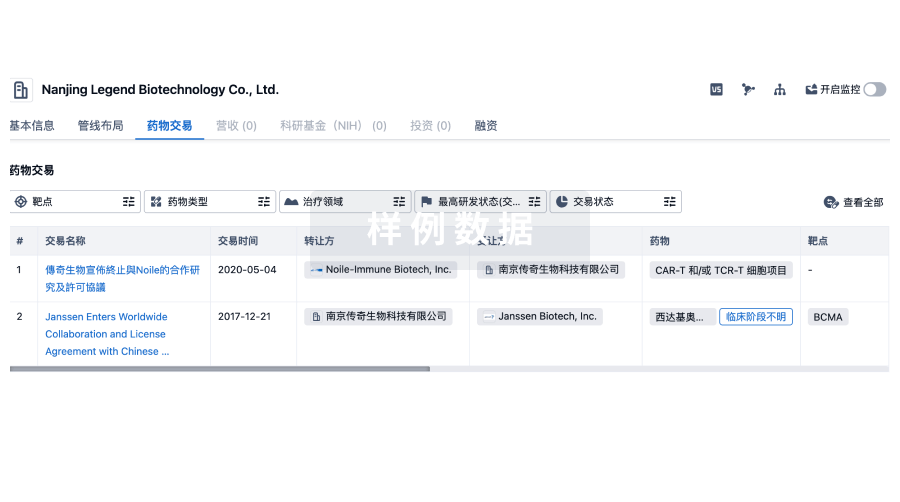
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
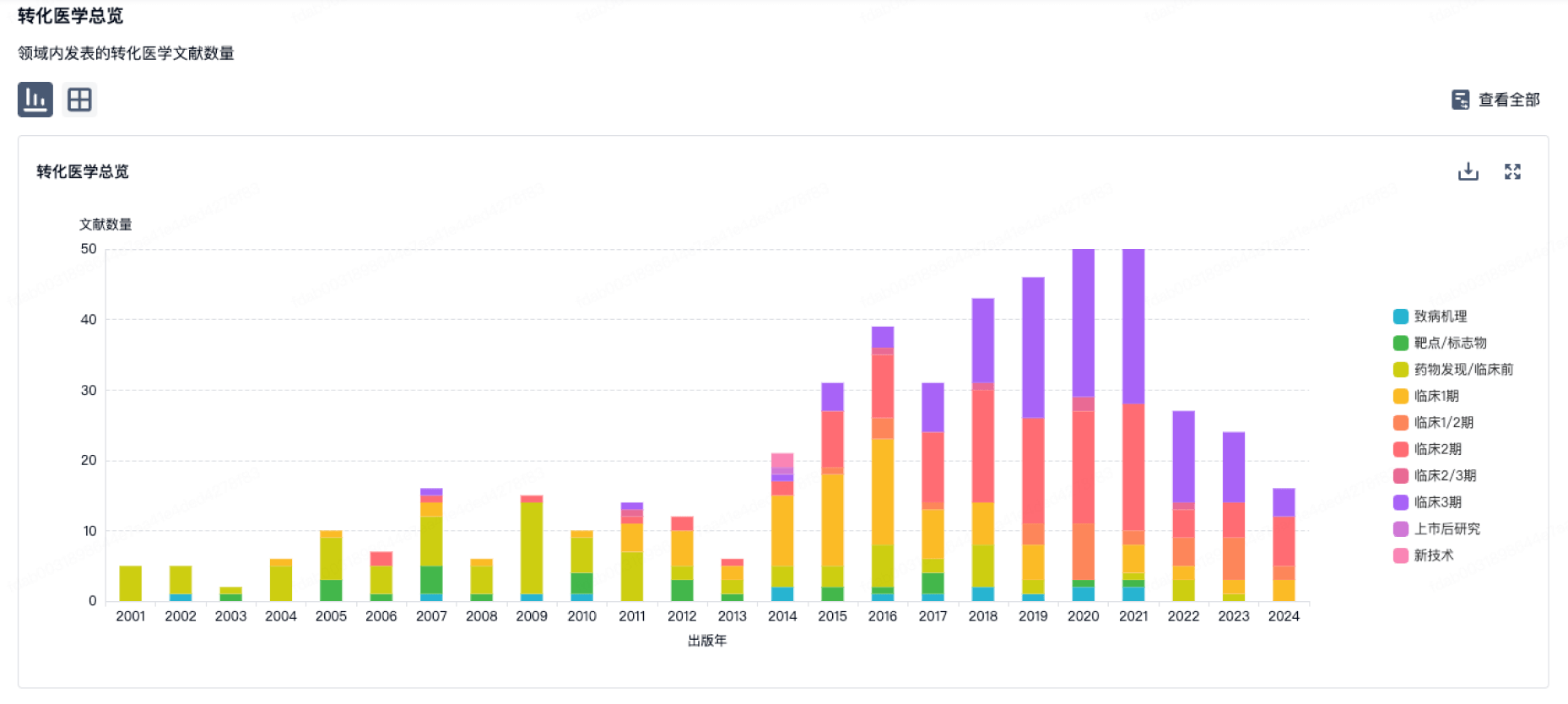
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
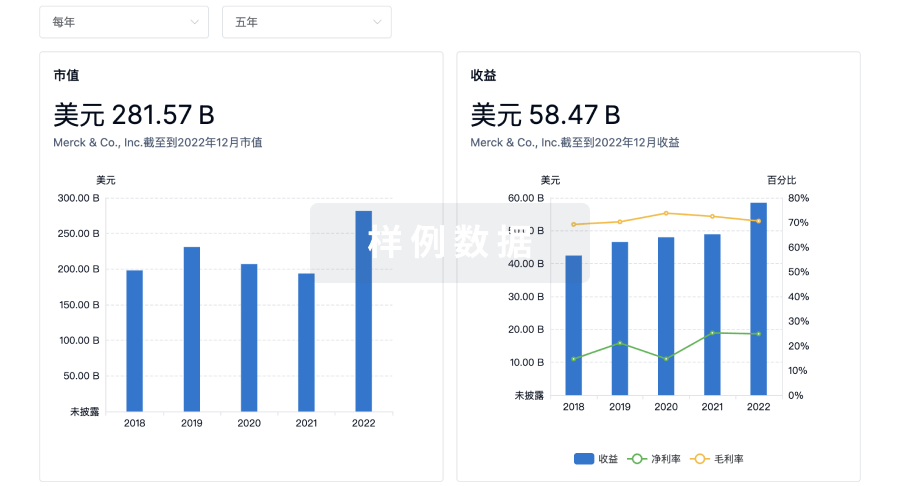
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
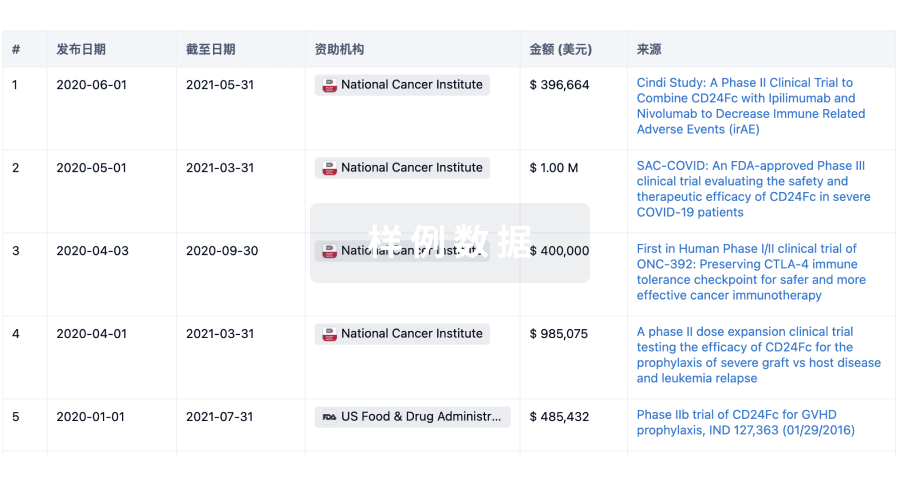
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
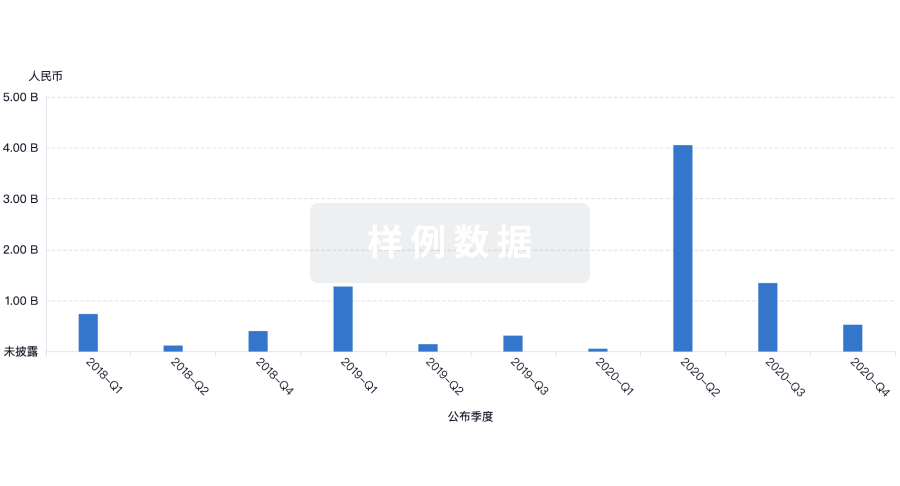
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
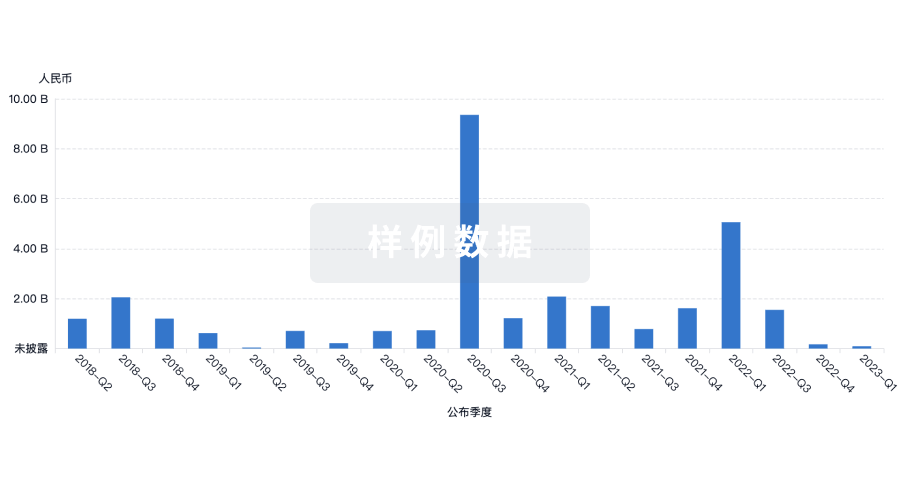
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
来和Eureka LS聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用