新靶点DDR1:实体肿瘤的“双刃剑”
2022-12-20
免疫疗法细胞疗法
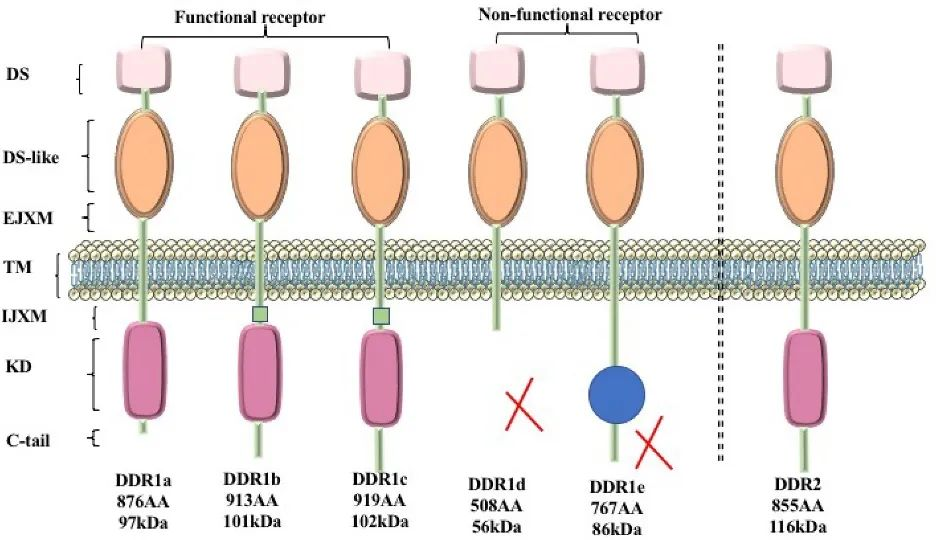
DDR结构和正常功能
DDR是在20世纪90年代发现的一种胶原激活RTK,DDR2仅有一种亚型。DDR的分子结构由细胞内激酶结构域、跨膜结构域和细胞外结构域组成。DDR与胶原(细胞外基质中最丰富的蛋白之一)结合,并刺激DDR磷酸化以激活激酶活性。
Preview
来源: 生物制药小编
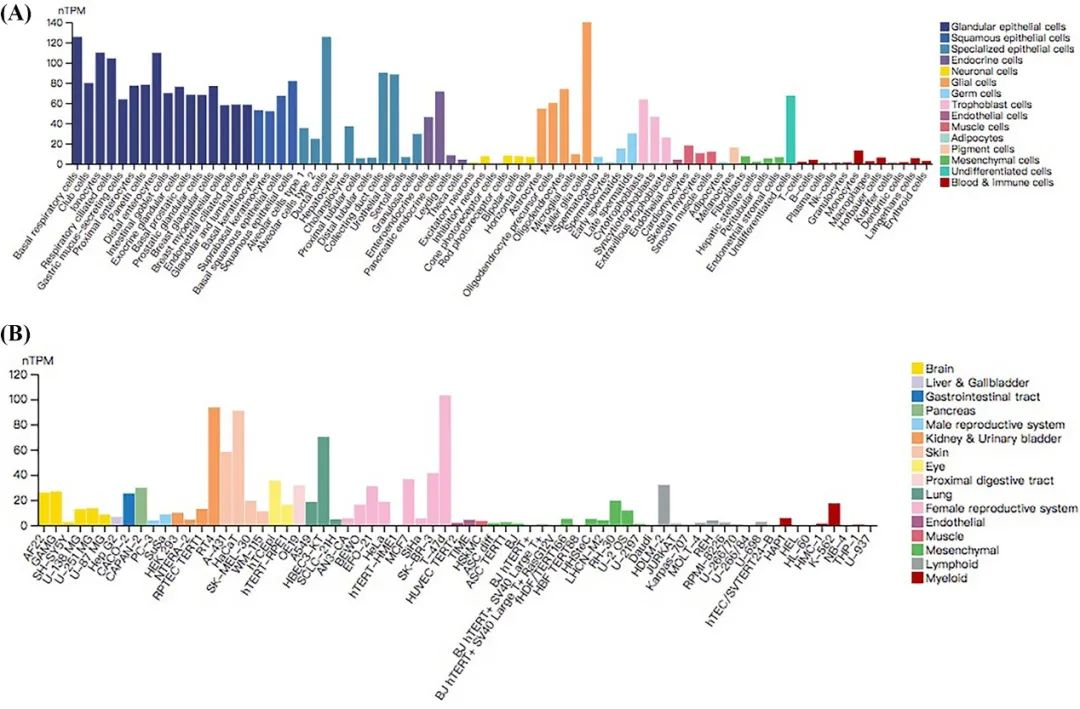
DDR1在人组织中的表达谱
Preview
来源: 生物制药小编
图2.DDR1在人单细胞中的分布
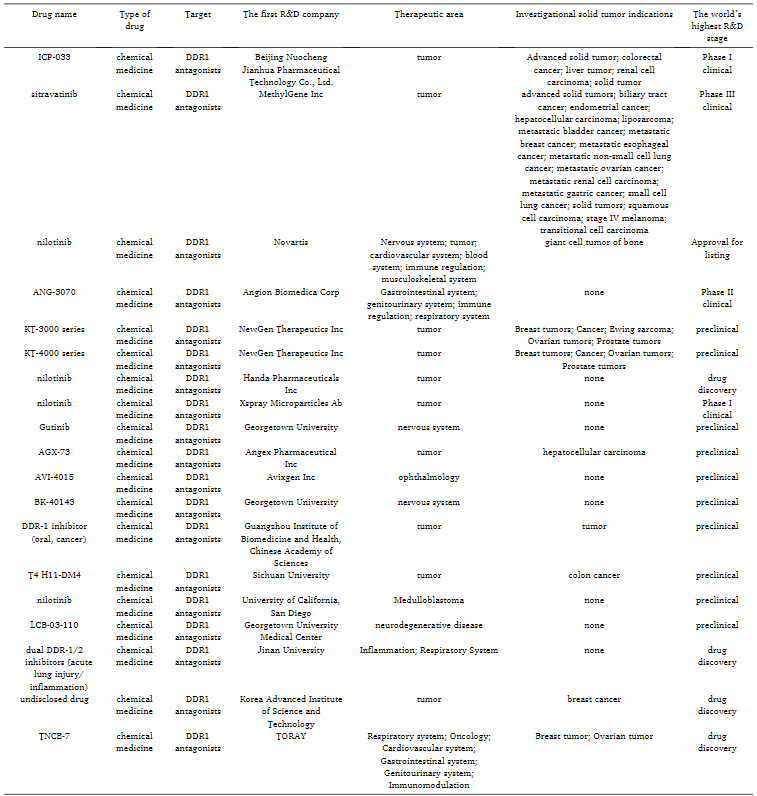
靶向DDR1的药物
表1. 针对DDR1的全球药物研发
Preview
来源: 生物制药小编
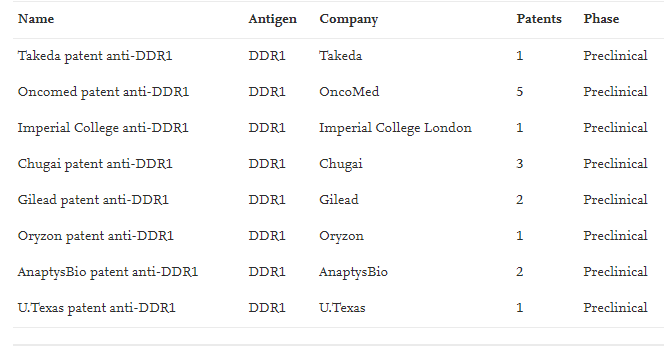
表2:靶向DDR1的抗体的开发
Preview
来源: 生物制药小编
随着人工智能的飞速发展和深度学习,越来越多的DDR1激酶抑制剂被快速鉴定出来,这将大大促进DDR1激酶抑制剂在实体瘤中发挥更大的作用。此外,之前的一项研究发现抗DDR1单抗可以抑制实体瘤的免疫排斥反应,为肿瘤免疫基质治疗开辟了一条新的途径。除了上述针对DDR1的药物和抗体外,此前已有大量研究证实CAR-T细胞已经完全改变了血液系统恶性肿瘤的治疗格局,但CAR-T细胞在实体瘤的治疗方面仍面临诸多挑战。其中寻找高特异性的肿瘤抗原是克服上述挑战的策略之一。在此,基于DDR1在实体瘤发生发展中的独特作用以及CAR-T细胞在实体瘤治疗中所面临的挑战,未来我们可以通过释放细胞毒性因子来杀死癌细胞,制备靶向DDR1的CAR-T细胞,而开发靶向DDR1的CAR-T细胞治疗实体瘤将是一项非常有趣且具有挑战性的任务。基于DDR1在肿瘤中的独特作用,很可能发挥强大的抗肿瘤作用。
Preview
来源: 生物制药小编
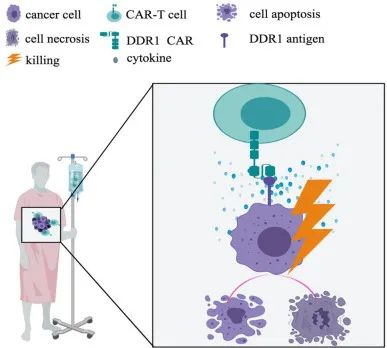
图:靶向DDR1-CAR-T细胞杀死癌细胞
结论
参考文献:
Tian Y, Bai F, Zhang D. New target DDR1: A "double-edged sword" in solid tumors. Biochim Biophys Acta Rev Cancer. 2022 Nov 7;1878(1):188829. doi: 10.1016/j.bbcan.2022.188829. Epub ahead of print. PMID: 36356724
内容来源于网络,如有侵权,请联系删除。
机构
-药物
-热门报告
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。


