预约演示
更新于:2025-05-24
Targeting GPC3 Chimeric Antigen Receptor Autologous T Cell (OriCell Therapeutics)
靶向GPC3嵌合抗原受体自体T细胞(原启生物)
更新于:2025-05-24
概要
基本信息
原研机构 |
在研机构 |
非在研机构- |
权益机构- |
最高研发阶段临床1/2期 |
首次获批日期- |
最高研发阶段(中国)临床1/2期 |
特殊审评- |
登录后查看时间轴
关联
1
项与 靶向GPC3嵌合抗原受体自体T细胞(原启生物) 相关的临床试验NCT05652920
A Phase Ib/II, Open-Label, Multi-Center Study to Investigate the Safety, PK, and Efficacy of Ori-C101 in Advanced Hepatocellular Carcinoma (HCC) Patients (BEACON)
This is a Phase I, open-label, multi-center study to assess the safety, pharmacokinetics, and preliminary efficacy of GPC3-directed chimeric antigen receptor modified T cells injection (Ori-C101) in Advanced Hepatocellular Carcinoma(HCC).
开始日期2022-12-15 |
申办/合作机构 |
100 项与 靶向GPC3嵌合抗原受体自体T细胞(原启生物) 相关的临床结果
登录后查看更多信息
100 项与 靶向GPC3嵌合抗原受体自体T细胞(原启生物) 相关的转化医学
登录后查看更多信息
100 项与 靶向GPC3嵌合抗原受体自体T细胞(原启生物) 相关的专利(医药)
登录后查看更多信息
25
项与 靶向GPC3嵌合抗原受体自体T细胞(原启生物) 相关的新闻(医药)2025-02-25
·药研网
2025年2月21日,浙江时迈药业有限公司自主研发的I类治疗用生物制品注射用CMD011获得FDA临床试验默示许可,本品为全人源抗GPC3×CD3双特异性抗体,拟用于晚期肝细胞癌治疗。
此为全球第三个获得FDA临床试验批准的GPC3×CD3双特异性抗体。由于GPC在肝细胞癌以及其他多种肿瘤类型中的显著上调,该靶点在肿瘤细胞中的特异性表达受到了广泛关注。
肝细胞癌
肝癌是全球第二大癌症死因(占总数的 8.2%),而肝细胞癌(HCC)是最常见的肝癌类型。
尽管在诊断和治疗方面都取得了重大进展,但只有 40% 的 HCC 能在早期确诊,而且治疗效果往往令人失望。手术仍然是首选的治疗方法。然而,只有 5%-10%的 HCC 肿瘤适合切除,大多数患者(50%-70%)在手术后五年内肿瘤复发。虽然肝移植是一种选择,但合适的供肝数量极其有限,在等待供肝的过程中,肿瘤可能会进展,这可能导致失去手术机会或术后预后恶化。
尽管目前的治疗方法取得了进展,但有效系统治疗HCC的方案仍然有限。因此,其五年生存率仅为18%。因此,鉴定特异性分子标记物和靶点将有助于早期诊断和靶向治疗。
GPC3靶点简介
01
结构
GPC3是一种细胞膜表面的糖基磷脂酰肌醇(GPI)锚定蛋白,属于Glypican家族,由约60-70 kDa的蛋白质核心组成。其结构包括:
GPI锚:将GPC3固定在细胞膜上。
14个保守的半胱氨酸残基:参与蛋白质折叠和稳定性。
硫酸肝素(HS)侧链:修饰羧基末端的最后50个残基,参与信号传导和分子相互作用。
GPC3与其他Glypican家族成员(GPC1-6)具有相似的结构,但在功能和表达模式上存在差异。
磷脂酰肌醇蛋白聚糖-3 (GPC3) 蛋白示意图
02
功能
胚胎发育:GPC3在胚胎发育过程中调控细胞生长、分化和迁移,尤其是通过Wnt、Hedgehog和FGF等信号通路发挥作用。
肿瘤相关功能:
在正常成人组织中,GPC3表达极低或几乎不表达。
在多种癌症中,GPC3表达显著上调,尤其是在肝细胞癌(HCC)、卵巢癌和黑色素瘤中。
GPC3通过促进细胞增殖、抑制凋亡和增强侵袭性,参与肿瘤的发生和发展。
GPC3靶点作为癌症治疗策略
01
诊断标志物
GPC3可通过免疫组化(IHC)或血液检测(如ELISA)用于HCC的早期诊断和鉴别诊断。其高特异性和敏感性使其成为HCC的理想生物标志物。
02
治疗靶点
(1)抗体疗法:
针对GPC3的单克隆抗体(如Codrituzumab)可通过抗体依赖性细胞毒性(ADCC)和补体依赖性细胞毒性(CDC)杀死癌细胞。
抗体药物偶联物(ADC)将抗体与细胞毒性药物结合,进一步提高疗效。
(2)CAR-T细胞疗法:
靶向GPC3的CAR-T细胞在临床试验中显示出对HCC的抗肿瘤活性。
03
疫苗
GPC3肽疫苗在HCC患者中诱导特异性免疫反应,显示出一定的临床获益。
04
小分子抑制剂
针对GPC3相关信号通路(如Wnt、Hedgehog)的小分子药物。
GPC3靶点研发格局
现阶段靶向GPC3的主要研究方向包括CD3型双抗、CAR-T等疗法,同时也有单克隆抗体和其他新型免疫疗法的研发,适应症主要集中在肝细胞癌等实体瘤。
据不完全统计,全球处于在研阶段的靶向GPC3的药物有70余个,最高临床阶段为二期。目前全球还没有GPC3靶向药获批上市,不过已有多款在研药物进入临床试验阶段。国内药企,如科济药业、原启生物、康诺亚等也积极布局GPC3靶点。
吉满生物根据市场需求和研究现状,推出稳定表达细胞系以及阳性对照抗体,可用于GPC3相关药物的体外效果评价,助力药物临床申报。
01
CMD011
CMD011是时迈药业基于自主开发的抗体筛选文库和完全自主知识产权的双抗平台构建的肿瘤细胞靶点+免疫细胞靶点组合的全人源双抗药物。
CMD011具有明确的抗肿瘤机制,通过共结合GPC3阳性肿瘤细胞和CD3阳性T细胞诱导T细胞活化并杀伤肿瘤细胞。它的设计基于时迈药业自主研发的HBiTE双抗平台,优化了对GPC3和CD3的亲和力,从而实现更高的肿瘤选择性和更低的毒副作用。
2025年2月21日,浙江时迈药业有限公司自主研发的GPC3×CD3双抗CMD011获得FDA临床试验默示许可,拟用于晚期肝细胞癌治疗。
CMD011作用机制
02
AZD9793
AZD9793是出自阿斯利康平台,其在GPC3抗体的铰链区加入了CD8和TCR激动性纳米抗体,以起到特异性激活CD8 细胞的作用。
近期,Clinical trials网站显示,阿斯利康在登记了GPC3/TCR/CD8药物AZD9793,和多种实体瘤患者中,启动一项1期临床试验NCT06795022,该临床预计于2025年2月底启动,入组人数为304例。
03
PRS-342
PRS-342是一种4-1BB/GPC3临床前免疫肿瘤双特异性融合蛋白。此前Pieris Pharmaceuticals公布了其研发的双特异性抗体候选药物PRS-342的研究数据展示,该候选药物能够导致NF-κB活化,刺激T细胞激活,IL-2的表达量增加并具有剂量依赖性关系。PRS-342还能诱导人源化肝细胞癌异种移植小鼠模型中肿瘤浸润淋巴细胞(TIL)水平局部增加,所呈现的数据表明PRS-342具有潜在抗肿瘤活性。
Pieris认为PRS-342可能对肝细胞癌、Merkel细胞癌和黑色素瘤有效。
04
Ori-C-101
Ori-C101是一款靶向GPC3嵌合抗原受体自体T细胞注射液,Ori-C101拥有高特异性、高亲和力的靶向GPC3全人源抗体序列,能够精准识别并结合肝癌细胞表面的GPC3靶点。该药物还包含独特的信号激活元件Ori,能够成倍提升记忆性免疫细胞的扩增效率,有效突破肿瘤微环境中的细胞外基质的物理屏障,抵御肿瘤微环境的免疫抑制。通过上述机制,Ori-C101能够显著增强CAR-T细胞在体内的抗肿瘤活性和持久性,具有更好的防止复发潜力。
Ori-C101(靶向GPC3嵌合抗原受体自体T细胞注射液)目前正在进行Ib/Ⅱ期临床研究,该研究旨在评估其在二线后GPC3阳性晚期肝细胞癌(HCC)受试者中评估的安全性、药代动力学和初步疗效。
总结
目前,越来越多的证据表明GPC3是肿瘤药物开发的一个潜力靶点,尤其是在肝细胞癌领域。作为生物标志物,GPC3在肝细胞癌的早期诊断、预后判断和免疫治疗中的价值已经逐步显现。未来,深入研究GPC3的机制和应用,将有助于推动肝细胞癌的诊疗方式发展,改善患者的临床结果。
吉满生物
吉满生物提供与GPC3靶点相关的功能细胞系和抗体等产品,能够支持GPC3相关药物的活性验证和体外效果评价。
产品列表
数据展示
GM-C15633
H_GPC3 HEK-293 Cell Line使用Anti-GPC3 hIgG1 Antibody(Codrituzumab)流式验证结果
联系我们
吉满生物(Genomeditech)成立于2011年,是专业从事生物科技服务和前沿技术研发的高新技术企业。吉满生物专注为生物药开发赋能,自主创立了国内知名的细胞系品牌-DDXCELL,目前已布局近400个热门靶向药靶点,超1000株现货单克隆细胞系,涵盖GPCR、细胞因子、免疫检查点、TAA等多领域,做到进口细胞的国产替代。此外,吉满生物还可在药物研发进程中提供一系列抗体、蛋白产品,旨在为客户提供高效的研发工具和解决方案!
扫码咨询
扫码找现货
抗体药物偶联物
2024-07-19
·药智网
又一家专注CAR-T疗法的biotech掀起热度。
近日,原启生物宣布,美国FDA已授予公司靶向GPRC5D的CAR-T细胞注射液OriCAR-017快速通道资格,用于治疗复发/难治性多发性骨髓瘤(RRMM)。
前有传奇生物并购消息满天飞,后有原启生物OriCAR-017商业化进程加快,CAR-T疗法的普及程度,正在悄然加快。
何方神圣?
原启生物原名原能医学,成立于2015年,2019年进入大众视野。那一年,原能医学获得了启明创投将近亿元的pre-A轮融资。
随后在2020年,原启生物完成了沂景资本、张科创投领投的A轮融资;一直到2023年,原启生物已经融到了B+轮,领投方也从上海本地的知名VC到外资风投机构。
该公司目前知名管线主要是两条:Ori-C101和OriCAR-017。
图1 原启生物管线
图片来源:原启生物官网
2021年,它的核心管线Ori-C101登陆ASCO,获得公开发表,是一个重要的里程碑。Ori-C101是一款靶向GPC3的肝癌适应症药物,也是其CAR-T疗法的得意之作。GPC3在肝癌细胞表面是过度表达的,根据相关研究,GPC3在超过70%的肝细胞癌中高表达,并且其表达水平随着HCC恶性程度的增加而升高,因此其可以作为肝癌药物的理想靶点而存在。而这个靶点也不止CAR-T一种疗法在卷,乐普生物和智康弘义的巴靶点GPC3的ADC药物皆已申报临床。
Ori-C101作为CAR-T疗法治疗肝癌,算是HCC领域的重大突破。根据其初步临床研究数据,在10例可评估受试者中,6例达到部分缓解(PR),3例达到疾病稳定(SD),1例疾病进展(PD),达到了60%客观缓解率,90%疾病控制率。在14例安全性可评估受试者中,仅4例出现了细胞因子释放综合征(CRS)等级3,其余均为1-2级CRS,并且未见神经毒性和剂量限制性毒性。
目前,Ori-C101正在进行Ib/II期临床试验,受试者至少进行了二线治疗。
OriCAR-017则是该公司另一款主打产品。虽然与传奇生物的Carvykti适应症以及疗法相同,但靶点并不相同,Carvykti的靶点为BCMA,而OriCAR-017的靶点为GPRC5D。
它是中国首个、全球第二个靶向GPRC5D治疗复发难治多发性骨髓瘤的CAR-T产品。
该药的临床研究数据在2022年的ASCO年会和2022年的EHA年会进行了口头报告,根据ACSO公布的临床I期结果,10名患者全部对OriCAR-017治疗反应良好。总体的客观缓解率(ORR)为100%,严格完全缓解率(sCR)为80%,非常好的部分缓解率(VGPR)为20%。此外,所有患者在第28天均达到了100%的微小残留病灶阴性率。
此外,此次临床的中位缓解持续时间(DOR)为10.43个月,中位无进展生存期(PFS)为11.37个月。
该药的安全性非常不错,仅有一名患者出现二级细胞因子释放综合征(CRS),其余全为一级CRS。目前该药已于中美双地开展临床研究。
两条核心管线之外,其余管线均处于临床前阶段,而治疗实体瘤的各管线也暂时没有确认具体的适应症。
国内CAR-T单品梳理
CAR-T作为新兴疗法,拥有值得肯定的疗效,也受到许多争议比如严重不良反应,此外,成本昂贵也是其显著的特点。
但也正是因为昂贵,给了该药市场非常可观的复合增长率,根据Frost&Sullivan预测,2024年全球CAR-T市场将达到约66亿美元(2019年~2024年的复合年增长率为55.0%);2030年将达至218亿美元(2024年~2030年的复合年增长率为22.1%)。
国内最负盛名的CAR-T疗法代表,自然是传奇生物,以及它的代表单品——Carvykti。该药自从liscense out后,强生也一直给它进行背书和商业推广,给它的销售额峰值为50亿美金。该药目前在适应症拓展上也不负众望,不断向前线治疗推进。今年2月,该药在欧洲获批二线治疗;4月,FDA批准其用于二线治疗。
很有意思的是,Carvykti目前并没有在中国获批。
目前国内获批的CAR-T疗法药物有5款,分别是:复星凯特旗下的阿基仑赛注射液、药明巨诺旗下的瑞基奥仑赛注射液、信达生物与驯鹿生物合作研发的伊基奥仑赛注射液、合源生物旗下的纳基奥仑赛注射液及科济药业研发的泽沃基奥仑注射液。
表1 中国CAR-T获批上市药物
数据来源:据公开资料整理
如表格所示,目前上市的药物适应症皆为血液瘤或白血病,靶点为CD19或BCMA,这也是CAR-T疗法面临的局限性之一。
价格方面,阿基仑赛是我国第一个获批的CAR-T疗法药物,原研方为吉利德。吉利德财报显示,2023年其总销售额达到15亿美元。该药在中国的售价为120万元,而后期上市的药物,例如合源生物的纳基奥仑赛已经把价格打到了百万以下,为99.9万元。不过科济药业的新药泽沃基奥仑赛依然较高,为115万元左右。
拓展适应症上,已经上市的药物正在积极向自身免疫病适应症拓展,例如信达和驯鹿合研的伊基奥仑赛,今年1月获得了肌无力适应症的临床试验批准。但靶向CD19的药物由于靶点原因,很难取得B细胞疾病以外的突破。
从血液瘤到实体瘤的飞跃
在已经商业化的CAR-T药物中,靶点主要是BCMA和CD19,后者由于靶点原因拓展适应症较为困难,前者还有自身免疫疾病的想象空间。
不过,CAR-T药物,大家更关注的是从血液瘤到实体瘤的突破。
其中非常典型的,自然是上文提到的原启生物的Ori-C101治疗肝癌。而相比原启生物,科济药业的CT011起源更早:2017年12月28日,该药获得了国家药监局的IND许可,为GPC3靶向CAR-T候选产品中全球首个IND,不过目前该管线尚未突破I期试验阶段。
Claudin18.2是CAR-T在实体瘤领域炙手可热的靶点,该靶点针对的适应症则是经典的消化道癌症:胃癌,胰腺癌等。代表产品则是科济药业的CT041,目前该药已经进入了临床II期阶段。
间皮素也是目前实体瘤领域正在研发的新兴靶点。间皮素是一种肿瘤相关抗原,在上皮样间皮瘤、胰腺癌、卵巢癌、胆管癌和胃癌等多种恶性肿瘤细胞上过表达,而在大多数正常组织中几乎没有表达。不过,目前该靶点的管线近两年并未看到巨大突破。
而此外,一些比较经典的靶点上,例如肺癌的EGFR,前列腺癌的PSMA上,CAR-T疗法也均有涉及。
CAR-T成为主流疗法值得期待。
参考来源:原启生物官网、科济药业官网
声明:本内容仅用作医药行业信息传播,为作者独立观点,不代表药智网立场。如需转载,请务必注明文章作者和来源。对本文有异议或投诉,请联系maxuelian@yaozh.com。
责任编辑 | 史蒂文
转载开白 | 马老师 18996384680(同微信)
商务合作 | 王存星 19922864877(同微信)
阅读原文,是昨天最受欢迎的文章哦
免疫疗法细胞疗法ASCO会议临床1期临床结果
2024-05-17
嘉宾简介曾任生物药无菌制剂商业化生产质量负责人和放行人曾任中国首个CAR-T细胞治疗产品的质量负责人和质量受权人。参与上海医药行业协会组织起草的团体标准《细胞和基因治疗产品快速无菌检查法的验证技术要求》(T/SHPPA 012-2022)(2022年6月28日发布)参与新版《GMP实施指南 无菌分册》(2023年5月)中相关细胞治疗产品的质量管理章节的编写现任原启生物(Biotech company)质量VP及质量负责人一职,负责公司细胞治疗产品从研发至上市的全生命周期的质量风险控制体系的搭建,负责产品IND及NDA阶段的质量风险策略制订及控制。原启生物原启生物是一家临床阶段的生物技术公司,致力成为创新驱动的全球领先肿瘤免疫疗法开拓者,目前专注开发创新型细胞疗法,以解决全球肿瘤学和免疫学领域未被满足的医疗需求。通过自主创新的Ori®Ab抗体筛选和工程平台、Ori®CAR结构平台以及在CMC领域积累的专识,原启生物开发了多条治疗血液肿瘤和实体肿瘤的产品管线,并在探索性临床研究中验证出良好的安全性和有效性,相关临床研究数据分别在2021 ASCO,2022 ASCO,2022 EHA以及2023《柳叶刀血液学》等会议以及国际学术期刊发布。公司自成立来总融资金额超2亿美元,有启明创投、泉创资本、RTW、QIA等生命科学领域专业投资人参与投资,最新一轮融资为2023年2月完成的B1轮融资,由全球知名的生命科学领域投资人RTW和QIA领投。欲了解更多信息,请访问:www.oricell.com发展历程20185月与北京艺秒神州医疗科技有限公司签署战略合作协议201912月获启明创投独家Pre-A轮投资20206月上海市科委“科技创新行动计划”科技型中小企业技术创新资金项目承担、单位自主研发的双特异性抗体与德琪医药(6996.HK)达成一项潜在交易额为1.42亿美金全球开发协议20215月原能细胞医学技术有限公司正式更名为“原启生物科技(上海)有限责任公司”20223月原启生物授权许可给德琪医药的PD-L/4-1BB的双特异性抗体OriBS-001(ATG101)获得CDE的默示许可9月Ori-C101注射液一类新药临床试验(IND)申请正式获国家药品监督管理局(NMPA)批准10月GPRC5D CAR-T获美国FDA授予“孤儿药”资格认定11月于第五届进博会与Cytiva签署战略合作协议技术平台▐ Ori®Ab抗体发现技术平台公司利用创新方法构建了大容量的1011全人源噬菌体展示抗体库与1010合成纳米抗体库,用于筛选不同类型抗原的候选抗体。▐ Ori®CAR高记忆性高活力CAR-T技术平台公司设计引入了一系列的OriCAR信号原件,通过多重机制增强CAR-T对于血液瘤及实体瘤的杀伤,从而有效提高CAR-T对于肿瘤的杀伤及减少复发和耐受。产品管线目前,原启生物已有超过10个针对肿瘤治疗的细胞药物管线。重点关注肝癌、多发性骨髓瘤、胃癌、胰腺癌、胆管癌、卵巢癌、非小细胞肺癌等具有广泛临床治疗需求的适应症。原启生物将不断通过自主创新的技术平台,探索开发疗效好、差异化、成本可及的创新型肿瘤细胞免疫治疗药物。新闻速递2024年3月21日,中国上海—原启生物宣布,德琪医药和原启生物为共同通讯单位的关于PD-L1/4-1BB双特异性抗体ATG-101(原启产品代码YN051)的临床前研究论文“ATG-101 is a tetravalent PD-L1×4-1BB bispecific antibody that stimulates anti-tumor immunity through PD-L1 blockade and PD-L1-directed 4-1BB activation”在国际权威期刊Cancer Research上发表。这款具有突破性的PD-L1/4-1BB双特异性抗体由原启生物自主研发,并于2020年与德琪医药达成license out合作,由德琪进行后续开发和商业化。质量源于设计,又贯穿始终。QbD大会历经四载,在行业同仁的持续关注和支持下,2024第五届QbD生物药质量科学大会(QbD2024)将于7月26-27日在北京悠唐皇冠假日酒店再次召开。将重点围绕创新生物药的质控、分析、法规等内容展开讨论。从案例、实践去解读创新药质量研究管理的进程,持续深化QbD理念。原启生物质量副总裁陶铜静将在大会会场二:免疫细胞药物质量专场为大家带来主题为“CGT药物CMC质量控制策略”的报告,诚邀各位专家莅临指导!药企福利-享免费观摩门票
细胞疗法免疫疗法临床申请ASCO会议高管变更
100 项与 靶向GPC3嵌合抗原受体自体T细胞(原启生物) 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 晚期肝细胞癌 | 临床2期 | 中国 | 2022-12-08 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
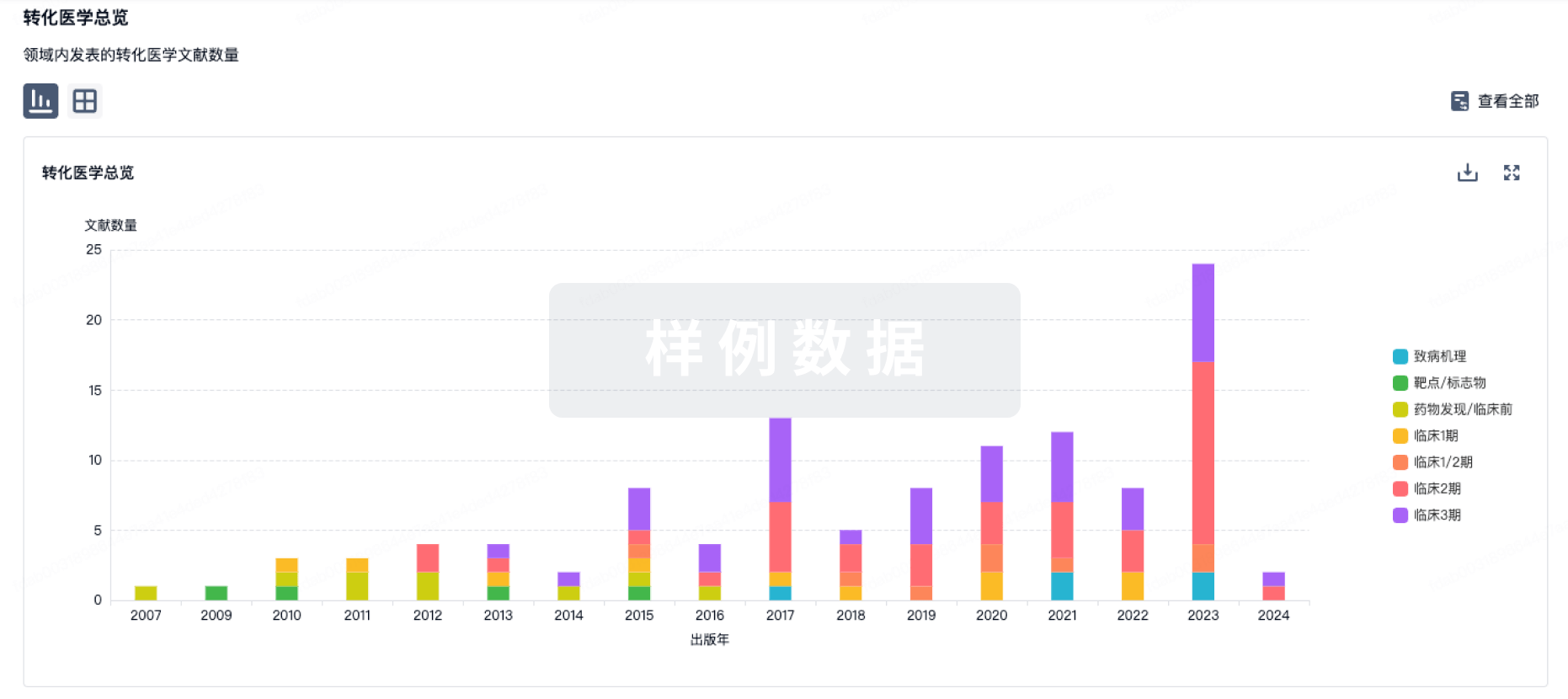
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
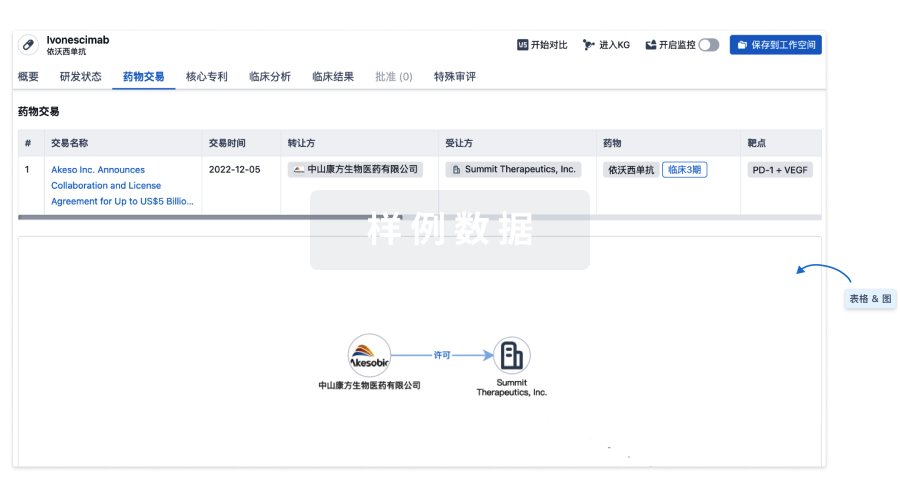
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
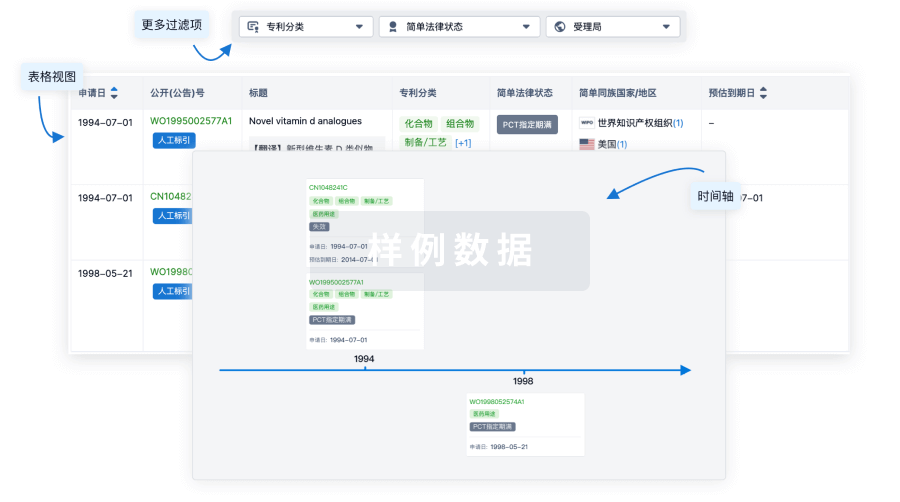
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
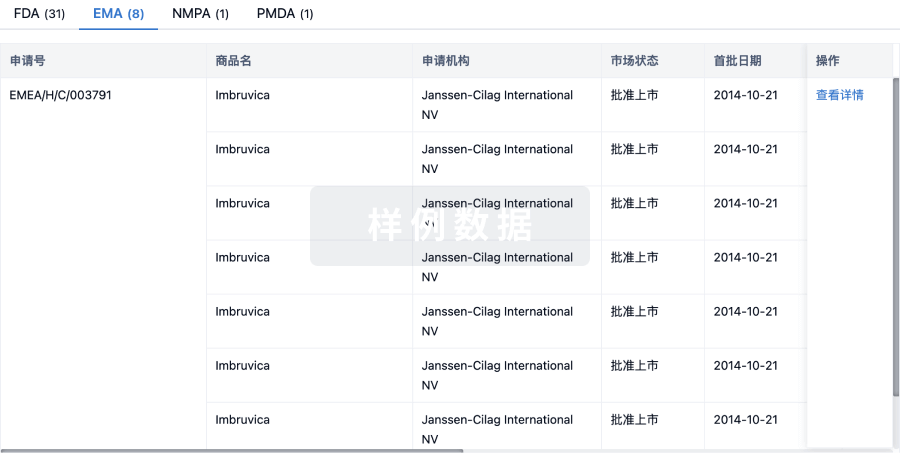
临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或
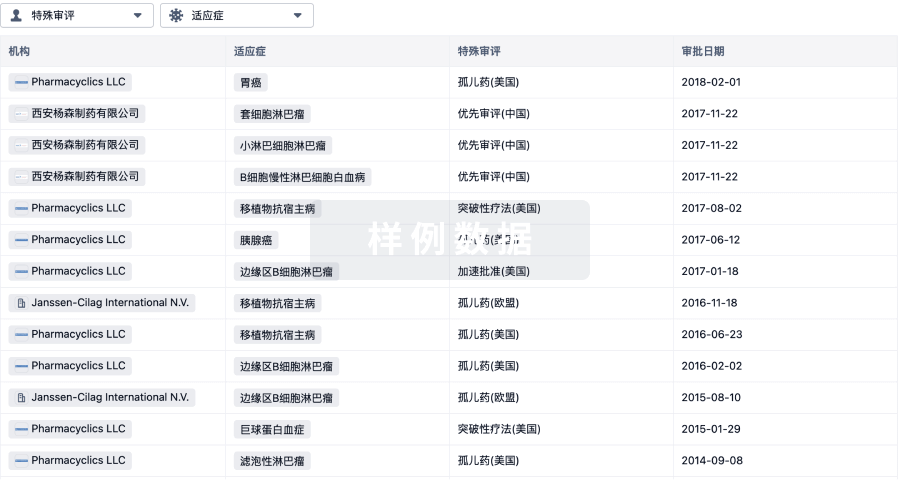
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
Eureka LS:
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
