预约演示
更新于:2025-06-19
Cugrastomig
更新于:2025-06-19
概要
基本信息
药物类型 双特异性抗体 |
别名 AK 129、AK-129、AK129 |
作用方式 抑制剂 |
作用机制 LAG3抑制剂(淋巴细胞活化基因3蛋白抑制剂)、PD-1抑制剂(细胞程序性死亡-1抑制剂) |
在研适应症 |
非在研适应症- |
原研机构 |
非在研机构- |
权益机构- |
最高研发阶段临床1/2期 |
首次获批日期- |
最高研发阶段(中国)临床1/2期 |
特殊审评- |
登录后查看时间轴
结构/序列
Sequence Code 1099010698

来源: *****
Sequence Code 1116814767

来源: *****
关联
5
项与 Cugrastomig 相关的临床试验NCT06943820
A Phase Ib/II Study of Anti-PD-1/LAG-3 Bispecific Antibody AK129 Combinations in Advanced Solid Tumors
This is an open, multicenter phase Ib/II clinical study. The goal of this study is to confirm the Phase II recommended dose (RP2D) of AK129 combinations for advanced solid tumors and evaluate the safety and efficacy of AK129 combinations for non-small cell lung cancer (NSCLC), head and neck squamous cell carcinoma (HNSCC), colorectal adenocarcinoma (CRC), and other advanced solid tumors.
开始日期2025-05-21 |
申办/合作机构 |
CTR20251054
抗PD-1和LAG-3双特异性抗体AK129联合治疗晚期实体瘤的Ⅰb/Ⅱ期临床研究
主要目的:
Ⅰb期
评价AK129联合化疗治疗晚期实体瘤的安全性和耐受性;
确定AK129联合化疗治疗晚期实体瘤的Ⅱ期推荐剂量(RP2D)。
Ⅱ期
评价AK129单药或联合治疗晚期实体瘤的安全性和有效性。 次要目的:
Ⅰb期:根据实体瘤疗效评价标准(RECIST v1.1)确定AK129联合化疗治疗晚期实体瘤的初步抗肿瘤活性;
评价AK129单药或联合治疗晚期实体瘤的药代动力学(PK)特征;
评价AK129单药或联合治疗晚期实体瘤的免疫原性(ADA)。 探索性目的:
探索肿瘤组织样本中与抗肿瘤疗效相关的潜在生物标志物。
开始日期2025-05-13 |
申办/合作机构 |
NCT06642792
A Phase I/II Study of AK129 (Bispecific Antibody Targeting LAG-3 and PD-1) Monotherapy or in Combination With AK117 (Anti-CD47 Monoclonal Antibody) in Relapse or Refractory Classic Hodgkin Lymphoma With PD-1/L1 Inhibitor Treatment Failure
This is a phase I/II study. All subjects are patients diagnosed with relapse or refractory (R/R) classic Hodgkin lymphoma (cHL) and has progressed on treatment with PD-1/L1 inhibitor therapy. The purpose of this study is to evaluate the safety and efficacy of AK129 (bispecific antibody targeting LAG-3 and PD-1) monotherapy or in combination with AK117 (anti-CD47 monoclonal antibody) in R/R cHL with PD-1/L1 inhibitor treatment failure.
开始日期2025-01-17 |
申办/合作机构 |
100 项与 Cugrastomig 相关的临床结果
登录后查看更多信息
100 项与 Cugrastomig 相关的转化医学
登录后查看更多信息
100 项与 Cugrastomig 相关的专利(医药)
登录后查看更多信息
21
项与 Cugrastomig 相关的新闻(医药)2025-04-01
4月1日,康方生物股价再度飙升,开盘后一度涨近16%。如此积极正面的市场反馈,很大程度源自其31日发布的2024年财报。财报显示,尽管这家药企因没有高额的授权收入,导致2024年营收同比腰斩53.08%至21.24亿元,净亏损约为5亿元,但其核心产品商业化能力正悄然破局。2024年,康方生物销售收入再创历史新高,同比增长约25%至20.02亿元。而两款全球首创双抗药物卡度尼利与依沃西于2024年成功被纳入国家医保目录,更是让市场对其医保放量预期充满想象。从自研产品依沃西头对头击败全球“药王”帕博利珠单抗(即K药)那一刻,不仅康方生物在国际上一战成名,也为中国创新药赢来了“DeepSeek时刻”,全球顶级投行高盛更是对其尤为看好。凭借依沃西的全球临床开发、市场潜力及竞争格局,高盛在近日一份报告中给出了2041年销售峰值将达到530亿美元的预期。而这一数字,近乎是K药2024年销售额(294.82亿美元)的2倍。可以说,康方生物双抗产品商业化的含金量还在不断上升。与此同时,叠加年报中的其他“利好”消息,截至今日收盘,康方生物股价上涨12.86%至86港元/股,市值为771.91亿港元。20亿,商业销售再创新高作为全球迄今唯一拥有2个肿瘤免疫双抗新药的制药公司,康方生物在2024年迈上了商业化新台阶。其2024年扣除分销成本后的商业销售收入达20.02亿元,同比增长24.88%,再创了新高。康方生物商业销售的增长主要得益于卡度尼利销售持续增长和依沃西在2024年5月获批上市后带来的积极销售贡献。2022年6月,康方生物全球首创的PD-1/CTLA-4双抗卡度尼利获批上市,成为全球首个获批的肿瘤免疫治疗双抗新药,也是中国第一个双特异性抗体新药。2024年5月,康方生物另一全球首创双抗新药依沃西获批上市,用于EGFR-TKI治疗进展的局部晚期或转移性nsq-NSCLC,是全球首个获批的“肿瘤免疫+抗血管生成”机制双抗新药。2024年12月,卡度尼利和依沃西均通过医保谈判被纳入国家新版医保目录。康方生物业绩会上披露,这两款药在2025年年初已完成所有挂网工作(西藏除外),纳入30+省份的双通道目录,实现1000余家医院准入,预计2025年底实现2000+医院覆盖。康方生物董事会主席夏瑜对此表示:“2025年是公司产品进入医保的元年,‘入院’是今年第一二季度主要聚焦的工作。到目前为止,还在非常快速放量起量的过程之中。”虽然康方生物2024年的营收和净利相较于2023年有所减少,但来自于产品商业销售的收入增长对创新药企来说更为重要。2022年12月,康方生物以50亿美金+2位数百分比销售提成的方案,将依沃西部分海外权益许可给美国Summit公司,该合作创下了彼时中国新药对外许可的最高交易金额记录。2023年度康方生物收到Summit公司首付款,2024年度来源于Summit公司的商业授权收入有所减少。而从商业销售成本可以看出,康方生物正在重金部署下一阶段。2024年度,康方生物销售成本为2.89亿元,同比增长116.92%。这些销售成本也主要用在了卡度尼利和依沃西的获批上市销售上。逆势增员,顺势扩能裁员砍管线、降本增效是药企正常的运营方式,但如果一家公司在行业仍处资本寒冬时期不断增员,扩大产能,至少对于行业来说,是一个正向消息。截止2024年12月31日,康方生物雇员总人数达到3035名,相较于2023年的2778人,增长了257人。不同于大多数公司一段时间内集中扩张某一职能岗位人员,康方生物的增员更加稳定和全面。具体来看,2024年度康方生物临床前研发岗位增加了9人,达329人;临床研发岗位增加了21人,达700人;生产、质量保证和质量控制岗位增加了127人,达814人;销售及营销岗位增加28人,达816人;一般及行政岗位增加72人,达376人。从岗位增长人数可以看出,生产、质量保证和质量控制是康方生物重点布局环节,而这也是一家创新药企从临床研发阶段迈入商业化阶段最重要的链接点之一。同样,康方生物也确实建立起了强大的生产能力。截至目前,康方生物现有产能为94000升,可以保障大规模产能供应。康方生物也在业绩报告中透露,有持续和稳定的产能扩张计划,以满足未来的临床及商业化需求。康方生物对此表示:“我们符合GMP要求的生产设施是根据美国FDA、EMA和NMPA的规章设计和验证的,可支持从药物发现到工艺开发、GMP合规试点和商业生产的整个药物开发过程,将有效地支撑本公司临床及商业化发展。”在集生物医药研究、开发、生产和销售于一体的中山翠亨康方湾区科技园中,康方生物总规划产能超100,000升,已配备一系列全球最先进的生物制药设施设备。截至2025年3月,该园区已运行产能55000升,包含了40000升不锈钢反应器以及全球先进的灌装联动系统,和15000升一次性生物反应器。此外,康方生物的中新广州知识城生物制药基地已运行产能36000升;国家健康科技产业基地园区(中山)已运行产能3000升。迎接IO +ADC 2.0时代卡度尼利和依沃西这两款全球first-in-class产品,既是康方生物的核心产品,也作为基石性药物奠定了康方生物在IO(肿瘤免疫)治疗上的1.0时代。随着这两款重磅药物纳入医保,一线适应症陆续获批,康方生物正全面开启商业化新征程。对于下一阶段的目标,康方生物表示,将以卡度尼利和依沃西为基石产品,持续巩固肿瘤免疫(IO)双抗作为基石产品的先发优势和广谱效应,多模式联用公司自研平台或行业领先的ADC药物或其他创新疗法,拓宽在不同适应症上的布局和开发。在研发投入方面,康方生物2024年度研发开支为11.87亿元,同比减少5.29%。主要原因是康方生物近年加强了临床团队建设,原委托外部临床服务供应商开展的研发服务目前基本由公司自营,这一举措使其能够在临床能力增长的情况下进一步控制研发开支。目前,康方生物总计有50多个在研创新项目,涵盖肿瘤、自身免疫及代谢性疾病等多个领域。24个处于临床试验及商业化阶段,其中15个为潜在全球首创(first-in-class)或同类最佳(best-in-class)双抗/多抗/双抗ADC。康方生物管线图肿瘤免疫治疗是康方生物重点专注的治疗领域之一。目前正在进行临床试验的产品包括已获批上市的卡度尼利、依沃西、派安普利以及莱法利(AK117,CD47)、佐斯利(AK119,CD73)、普络西(AK109,VEGFR-2)、AK115(NGF)、AK127(TIGIT)、AK129(PD-1/LAG-3)、AK130(TIGIT/TGF-β)、AK131(PD-1/CD73)、AK132(CLDN18.2/CD47),以及于近期推进至临床阶段的AK135(IL1RAP)、AK137(CD73/LAG-3)、AK138D1(HER3 ADC)和AK146D1(Trop2/Nectin4 ADC),覆盖了包含实体瘤、血液瘤领域等广泛的适应症。值得注意的是,康方生物正在加速ADC平台成果转化。AK138D1(HER3 ADC)用于治疗晚期恶性肿瘤的全球I期临床试验已启动,AK146D1(Trop2/Nectin4 ADC)的IND申请已递交。康方生物也将持续推进多款ADC候选产品到临床阶段,通过联合其核心双抗产品拓展到更多实体瘤治疗。在代谢类疾病治疗领域,康方生物的创新产品伊喜宁®(伊努西,PCSK9)已于2024年9月获批上市。在自身免疫性疾病领域,康方生物也拥有丰富的产品管线,其中爱达罗®(依若奇,IL-12/IL-23)和古莫奇(AK111,IL-17)的NDA正处于审评阶段。此外,康方生物也在积极推进包括曼多奇(AK120,IL-4R)和AK139(IL-4Rα/ST2)在内的其他产品的临床研究和探索。展望未来,康方生物表示,将立足“商业化”与“国际化”双轮驱动战略,持续加大研发投入,推动一系列具有全球竞争力的创新候选药物进入临床研究阶段,加速推进新药产品在全球范围内的临床开发、生产及商业化进程,为患者带来更多安全有效的创新治疗方案。推荐阅读恒瑞医药2024年报:研发投入82.28亿元创新高,创新药临床批准3天一个收入大增342%,亚盛医药按下全球化加速键Copyright © 2025 PHARMCUBE. All Rights Reserved.欢迎转发分享及合理引用,引用时请在显要位置标明文章来源;如需转载,请给微信公众号后台留言或发送消息,并注明公众号名称及ID。免责申明:本微信文章中的信息仅供一般参考之用,不可直接作为决策内容,医药魔方不对任何主体因使用本文内容而导致的任何损失承担责任。
财报上市批准
2025-01-22
·求实药社
来源:生物药大时代
1月20日,国家药品监督管理局药品审评中心(CDE)官网显示,康方生物旗下康方汇科(上海)生物有限公司自主研发的LAG-3/PD-1双特异性抗体“AK129注射液”获批临床默示许可,拟适应症为抗PD-1和LAG-3双特异性抗体AK129联合治疗晚期实体瘤,这是AK129注射液获批临床的第四项适应症。
此前曾获批临床的适应症包括:AK129联合化疗联合或不联合卡度尼利单抗(研发代号:AK104)治疗一线HER2-胃癌/胃食管结合处腺癌,AK129单药或联合AK117治疗PD-1/L1抑制剂治疗失败的复发或难治性经典型霍奇金淋巴瘤,晚期恶性肿瘤。
AK129是康方生物自主研发的靶向人PD-1和LAG3的双特异性抗体。已发布于AACR 2022年会的临床前研究结果显示,与PD-1和LAG-3抗体联合疗法相比,AK129可介导更强的免疫激活。AK129不仅具有优越的抗原结合性,有效阻滞PD-1/LAG-3信号通路,还可促进PBMC中IL-2和IFN-γ产生。此外,AK129在动物实验中显示了强大的抗肿瘤活性。
值得一提的是,2022年3月,百时美施贵宝联合疗法Opdualag(PD-1抗体+LAG-3抗体)首次获得美国FDA批准上市。AK129可同时靶向两个免疫抑制性受体PD-1和LAG-3,协同抑制抗肿瘤免疫反应,解除肿瘤微环境中的免疫抑制。AK129不仅可阻断LAG-3,提高T细胞免疫应答,同时还可阻断PD-1可促发免疫反应协同性增强,进一步提高免疫细胞的活性,增强抗肿瘤免疫反应,有望表现出更佳的治疗效果。
免责声明:
文章内容仅供参考,不构成投资建议。投资者据此操作,风险自担, 关于对文中陈述、观点判断保持中立,不对所包含内容的准确性、可靠性或完整性提供任何明示或暗示的保证。请读者仅作参考,并请自行承担全部责任。本公众号发布的各类文章重在分享,如有侵权请联系我们,我们将会删除。
联系我们
ABC 2025
展位火热预定中!
扫码立即咨询
电话:13816031174
(同微信)
赞助形式包括但不仅限于演讲席位、会场展位、会刊彩页、晚宴赞助、会议用品宣传等。
点击此处“阅读全文”咨询更多精彩!
AACR会议上市批准
2025-01-20
·氨基观察
氨基观察-创新药组原创出品
作者 | 黄凯
艾力斯业绩继续飙升。
1月20日,艾力斯发布2024年业绩预告,预计全年营业收入35.5亿元,同比增长75.9%;净利润14.3亿元,同比增长122%。那么,艾力斯的增长,会持续到什么时候呢?
同日,百利天恒公告,预计2024年度实现营业收入为58亿元左右,同比增加932.27%左右;预计实现归属于母公司所有者的净利润36亿元左右,将实现扭亏为盈。
国内CXO接手海外企业工厂。
1月20日,昭衍生物宣布,成功以资产交易的方式收购广州知识城龙沙大分子CDMO工厂。昭衍生物表示,此次在大湾区增加服务能力的布局,是进一步完善国际化布局的重要一步。昭衍生物,能否如愿?
在过去的一天里,国内外医药市场还有哪些热点值得关注?让氨基君带你一探究竟。
/ 01 /
市场速递
1)君实生物与利奥制药签署分销与商业化协议
1月20日,君实生物宣布,全资子公司拓普艾莱与利奥制药签署《分销与商业化协议》,授予利奥制药在欧盟、欧洲经济区所有现有成员国和未来成员国以及瑞士、英国内储存、分销、推广、营销和销售特瑞普利单抗的独占权利。利奥制药将向拓普艾莱支付1500万欧元首付款,并根据销售情况支付销售分成。
2)诺诚健华CD20×CD3双抗出海
1月20日,诺诚健华宣布,与Prolium达成重要许可协议,将其CD20×CD3双抗ICP-B02全球非肿瘤领域以及除亚洲以外的全球肿瘤领域的独占性权利,授予Prolium。作为回报,诺诚健华将获得总计1,750万美元的首付款,以及高达5.025亿美元的里程碑付款机会。此外,诺诚健华还将获得产品未来销售的特许权使用费以及Prolium公司的少数股权。
3)昭衍生物收购龙沙广州大分子CDMO工厂
1月20日,昭衍生物宣布,成功以资产交易的方式收购广州知识城龙沙大分子CDMO工厂。昭衍生物表示,此次在大湾区增加服务能力的布局,是进一步完善国际化布局的重要一步。
/ 02 /
资本信息
1)步长制药2024年度最高亏损8.08亿元
1月20日,步长制药发布2024年年度业绩预告,预计2024年度实现归属于母公司所有者的净利润约为-8.08亿元到-4.28亿元,与上年同期相比,将出现亏损。
2)沃森生物2024年度净利润同比下降57%-67%
1月20日,沃森生物发布2024年年度业绩预告,预计2024年归属于上市公司股东的净利润盈利1.4亿-1.8亿元,比上年同期下降57%-67%;扣除非经常性损益后的净利润盈利1.1亿-1.5亿元,比上年同期下降74%-81%。
3)甘李药业2024年净利润同比增长76.44%到91.14%
1月20日,甘李药业发布2024年年度业绩预告,预计2024年年度实现归属于母公司所有者的净利润为6亿元到6.5亿元,同比增加76.44%到91.14%。
4)通化东宝2024年净利润同比预减约96.53%
1月20日,通化东宝发布2024年年度业绩预告,预计2024年年度实现归属于上市公司股东的净利润约为4052.77万元,与上年同期相比减少约11.27亿元,同比减少约96.53%。
5)艾力斯预计2024年净利润14.3亿元
1月20日,艾力斯医药发布2024年业绩预告,预计全年营业收入35.5亿元,同比增长75.9%;净利润14.3亿元,同比增长122%。
6)百利天恒预计2024年净利润36亿元
1月20日,百利天恒公告,预计2024年度实现营业收入为58亿元左右,同比增加932.27%左右;预计实现归属于母公司所有者的净利润36亿元左右,将实现扭亏为盈。
/ 03 /
医药动态
1)百济神州BG-60366片获临床许可
1月20日,据CDE官网,百济神州BG-60366片获临床许可,拟开展治疗EGFR突变型非小细胞肺癌的研究。
2)康方汇科AK129注射液获临床许可
1月20日,据CDE官网,康方汇科AK129注射液获临床许可,拟开展治疗晚期实体瘤的研究。
3)海思科HSK44459片获临床许可
1月20日,据CDE官网,海思科HSK44459片获临床许可,拟开展治疗白塞病的研究。
4)弼领生物BL0175注射液获临床许可
1月20日,据CDE官网,弼领生物BL0175注射液获临床许可,拟用于绝经后激素受体阳性的局部晚期或转移性乳腺癌患者的治疗。
5)科伦博泰注射用SKB445获临床许可
1月20日,据CDE官网,科伦博泰注射用SKB445获临床许可,拟开展治疗晚期实体瘤的研究。
6)辛夷尚德生物ACT001胶囊拟获突破性疗法认定
1月20日,据CDE官网,辛夷尚德生物ACT001胶囊拟获突破性疗法认定,用于经过一线治疗或一线治疗中出现脑部新发病灶或原脑转移病灶进展的小细胞肺癌脑转移患者。
7)舒泰神血友病新药IIb期研究成功
1月20日,舒泰神宣布,取得关于凝血因子X(FX)激活剂STSP-0601的IIb期临床研究总结报告。鉴于IIb期临床数据达到了预设的主要有效性终点,舒泰神计划基于已有数据推进附条件上市申报准备工作,并在后续阶段尽快向CDE提交附条件上市申请。
8)智翔金泰抗IL-17单抗获批第二项适应症
1月20日,据NMPA官网,智翔金泰IL-17A单抗赛立奇第二项适应症获批,用于治疗放射学阳性中轴型脊柱关节炎(强直性脊柱关节炎)。
/ 04 /
器械跟踪
1)加奇生物输送型球囊扩张导管获注册许可
1月20日,据NMPA官网,加奇生物输送型球囊扩张导管获注册许可。
2)励楷科技一次性使用血栓抽吸负压吸引泵获注册许可
1月20日,据NMPA官网,励楷科技一次性使用血栓抽吸负压吸引泵获注册许可。
3)恒瑞宏远体外心肺支持辅助设备获注册许可
1月20日,据NMPA官网,恒瑞宏远体外心肺支持辅助设备获注册许可。
/ 05 /
海外药闻
1)安进KRAS抑制剂再获FDA批准
日前,安进宣布,美国FDA已批准其KRAS G12C抑制剂Lumakras与EGFR抑制剂Vectibix联合,用于治疗经FDA批准检测确认携带KRAS G12C突变的转移性结直肠癌成人患者,这些患者曾接受过基于氟嘧啶类、奥沙利铂和伊立替康的化疗。
PS:欢迎扫描下方二维码,添加氨基君微信号交流。
并购财报
100 项与 Cugrastomig 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 大肠腺癌 | 临床2期 | 中国 | 2025-05-21 | |
| 非小细胞肺癌 | 临床2期 | 中国 | 2025-05-21 | |
| 非小细胞肺癌IIIA期 | 临床2期 | 中国 | 2025-05-21 | |
| 头颈部鳞状细胞癌 | 临床2期 | 中国 | 2025-05-21 | |
| 晚期恶性实体瘤 | 临床2期 | 中国 | 2025-05-13 | |
| 难治性经典霍奇金淋巴瘤 | 临床2期 | 中国 | 2025-01-17 | |
| 典型霍奇金淋巴瘤 | 临床2期 | 中国 | 2025-01-03 | |
| 典型霍奇金淋巴瘤 | 临床2期 | 中国 | 2025-01-03 | |
| HER2阴性胃癌 | 临床2期 | 中国 | 2024-09-26 | |
| HER2阴性胃癌 | 临床2期 | 中国 | 2024-09-26 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

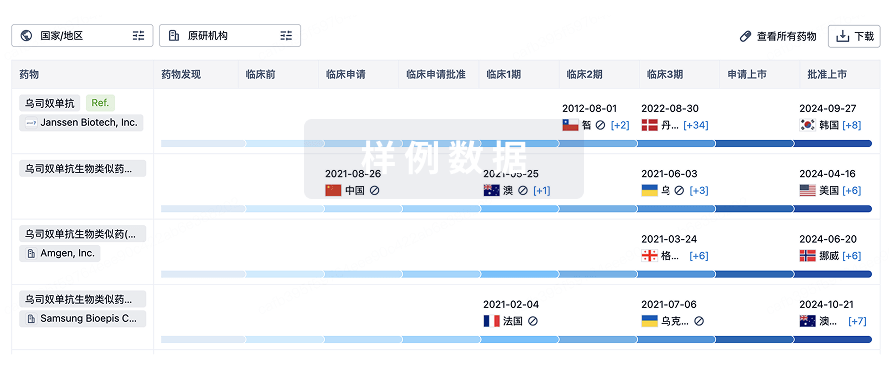
生物类似药
生物类似药在不同国家/地区的竞争态势。请注意临床1/2期并入临床2期,临床2/3期并入临床3期
登录
或
特殊审评
只需点击几下即可了解关键药物信息。
登录
或

Eureka LS:
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
