更新于:2024-07-06
BGB-R046
更新于:2024-07-06
概要
基本信息
原研机构 |
非在研机构- |
最高研发阶段临床1期 |
首次获批日期- |
最高研发阶段(中国)临床1期 |
特殊审评- |
关联
2
项与 BGB-R046 相关的临床试验一项评价BGB-R046单药及其联合替雷利珠单抗在选定的晚期或转移性实体瘤受试者中的安全性和初步抗肿瘤活性的多中心、开放性、1a/1b 期研究(目前仅开展1a期间单药试验)
1. 评估BGB-R046单药治疗和与替雷利珠单抗联合治疗在选定的晚期或转移性实体瘤受试者中的安全性和耐受性;
2. 确定BGB-R046单药治疗和与替雷利珠单抗联合治疗的最大耐受剂量(MTD)或最大给药剂量(MAD)以及扩展期推荐剂量(RDFE)
开始日期- |
申办/合作机构 |
A Multicenter Open-Label Phase 1a/1b Study to Evaluate the Safety and Preliminary Antitumor Activity of BGB-R046 as Monotherapy and in Combination With Tislelizumab in Participants With Selected Advanced or Metastatic Solid Tumors
This is a first-in-human (FIH) study that will evaluate the safety, tolerability, pharmacokinetics (PK), pharmacodynamics, and preliminary antitumor activity of BGB-R046 as a single agent and in combination with tislelizumab (BGB-A317) in participants with advanced or metastatic immune-sensitive solid tumors.
开始日期- |
申办/合作机构 |
100 项与 BGB-R046 相关的临床结果
登录后查看更多信息
100 项与 BGB-R046 相关的转化医学
登录后查看更多信息
100 项与 BGB-R046 相关的专利(医药)
登录后查看更多信息
2
项与 BGB-R046 相关的新闻(医药)2024-06-16
yuan
Bio·News
药
监
资
讯
1、国务院办公厅| 印发《深化医药卫生体制改革2024年重点工作任务》
2024年6月6日,国务院办公厅印发关于《深化医药卫生体制改革2024年重点工作任务》的通知。(相关阅读点击查看)
(来源:中央人民政府官网、蒲公英Biopharma)
2、国家药监局 | 发布三个与血液制品相关的文件
2024年6月11日,国家药监局发布了三个与血液制品相关的文件。(相关阅读点击查看)
1)药品生产质量管理规范(2010年修订)血液制品附录修订稿,自发布之日起实施。其中,对于附录第25条和35条,企业信息化建设工作需要一定周期,应在2027年1月1日前符合相关要求;新建车间或者新建生产线应符合上述要求。
2)血液制品生产智慧监管三年行动计划(2024—2026年)
按照率先实施、分批推进的原则,通过三年行动,2026年底前基本实现血液制品生产企业信息化管理,切实提高血液制品监管效能,有力保障血液制品质量安全。
3)血液制品生产检验电子化记录技术指南(试行)
《血液制品生产检验电子化记录技术指南(试行)自发布之起实施。实现血液制品生产、检验信息的电子化记录,并对关键生产、检验环节进行可视化监控,促进血液制品产业高质量发展。
(来源:国家药品监督管理局、蒲公英Biopharma)
3、CDE|征求意见:《儿童临床试验药物警戒技术指导原则》
2024年6月7日,CDE发布公开征求《儿童临床试验药物警戒技术指导原则(征求意见稿)》意见的通知。(相关阅读点击查看)
指导原则分为五部分,主要内容包括:背景、总体考虑、儿童临床试验药物警戒需特殊关注的安全风险和儿童临床试验期间安全性评估与报告。
(来源:国家药品监督管理局药品审评中心、蒲公英Ouryao)
受
理
情
况
CDE受理情况
2024年6月6日-6月12日期间,中国国家药监局药品审评中心(CDE)共受理药品申请260个,其中生物制品41个(新药14个和进口2个,见下图)。
(来源:国家药品监督管理局药品审评中心)
企
业
动
态
1、GSK | 5000 万美元!收购一家寡核苷酸公司
2024年6月6日,葛兰素史克(GSK)宣布以5000万美元收购西海岸生物技术公司 Elsie Biotechnologies,这项收购协议是在GSK花了11个月时间了解 Elsie公司的寡核苷酸平台之后达成的。
该协议不受成交条件限制,收购已经完成。此次收购使GSK整合了Elsie的寡核苷酸发现、合成和递送技术,以增强自身平台的研发能力。在此之前,GSK曾于2023年7月与Elsie达成过研究合作。
(来源:GSK官网)
2、勃林格殷格翰|Survodutide获CDE突破性疗法认定
2024年6月11日,勃林格殷格翰近日宣布,胰高血糖素受体/胰高血糖素样肽-1受体(GCGR/GLP-1R)双重激动剂survodutide(BI 456906)获得中国国家药品监督管理局(NMPA)药品审评中心(CDE)突破性疗法认定,拟用于代谢功能障碍相关脂肪性肝炎 (MASH) 的治疗。
Survodutide是一种具有独特作用机制的胰高血糖素受体/胰高血糖素样肽-1受体(GCGR/GLP-1R)双重激动剂。此前,survodutide于2021年被美国食品药品管理局 (FDA) 授予快速审评资格,并于去年11月,被欧洲药品管理局 (EMA)授予优先药物(PRIME)资格。
(来源:勃林格殷格翰中国官微)
3、百济神州|「抗肿瘤1类新药」获批临床
2024年6月11日,据CDE官网显示,广州百济神州生物制药有限公司(以下简称“百济神州”)的1类新药“注射用BGB-R046”获得临床试验默示许可,适应症为晚期获转移性实体瘤。BGB-R046是百济神州开发的一款抗肿瘤1类新药,目前尚未公开具体成分,其临床试验申请于今年4月获得CDE受理。
今年开年以来,百济神州多款抗肿瘤新药在国内申报临床;此外,HER2双抗“泽尼达妥单抗”的新药上市申请也于6月7日获得了CDE受理。
(来源:国家药品监督管理局药品审评中心、医药魔方)
4、礼来 | Donanemab 11:0全票通过生物制品许可申请,支持获益大于风险
2024年6月10日,FDA外周和中枢神经系统药物咨询委员会(PCNS)就Donanemab用于治疗早期症状性阿尔茨海默病(AD)的生物制品许可申请(BLA)召开的会议结果出炉,委员会以11:0的票数一致赞同该药物的有效性,并一致赞同其获益大于风险。
Donanemab是礼来开发的一款新一代Aβ单抗,可与β淀粉样蛋白亚型N3pG结合,从而促进患者大脑中淀粉样蛋白斑块的清除。
图片来源:PCNS会议礼来PPT
(来源:Bioshanghai)
5、再生元/赛诺菲|IL-6受体靶向单抗再获FDA批准!
2024年6月12日,再生元(Regeneron Pharmaceuticals)宣布,美国FDA批准其和赛诺菲(Sanofi)共同开发的Kevzara(sarilumab),用于治疗体重63公斤或以上的活动性多关节型幼年特发性关节炎(pJIA)患者,这是一种同时影响多个关节的关节炎。
(来源:Regeneron Pharmaceuticals官网)
END
编辑:芝麻核桃
声明:本文仅代表作者个人观点,不代表任何组织及本公众号立场,如有不当之处,敬请指正。如需转载,请注明作者及来源:蒲公英Biopharma。
佳课推荐
、
1、6月20日19:00-20:00 制药企业MES实施合规重点
2、6月25日19:00-20:30 理论与操作:细菌内毒素检测深度分享
并购高管变更寡核苷酸
2024-04-22
·医药笔记
▎Armstrong2024年4月20日,百济神州第2款自主研发双抗BGB-B2033的临床试验申请获得NMPA受理。此前,百济神州首款自主研发双抗CEA/4-1BB双抗BGB-B167于2022年申报临床。2023年研发日上,百济神州系统介绍了其创新布局情况,其中肺癌为其布局重点,7大重点即覆盖了小分子、ADC、双抗、免疫治疗等多重要药物形式。核心的2款双抗为MUC1/CD16a双抗、Claudin6/CD3双抗。双抗以T cell engager和NK cell engager为主。MUC1/CD16a双抗测差异化在于更高的CD16a亲和力,CD16a与MUC1臂空间距离近,将于2024年进入临床阶段。Claudin6/CD3双抗的差异化设计在于对Claudin9具有高选择性,Fab/scFv格式缩短Claudin6和CD3的空间距离,通过低抗原依赖性和旁观者效应的设计克服抗原异质性,将于2024年进入临床阶段。总结百济神州计划从2024年起每年申报至少10款新分子,以2024年为例,目前已经申报了BGB-R046(成分未公开,应为新药物形式)、BGB-B2033(双抗,Claudin6/CD3或MUC1/CD16a)。Armstrong技术全梳理系列GPRC5D靶点全梳理;CD40靶点全梳理;CD47靶点全梳理;补体靶向药物技术全梳理;补体药物:眼科治疗的重要方向;Claudin 6靶点全梳理;Claudin 18.2靶点全梳理;靶点冷暖,行业自知;中国大分子新药研发格局;被炮轰的“me too”;佐剂百年史;胰岛素百年传奇;CUSBEA:风雨四十载;中国新药研发的焦虑;中国生物医药企业的研发竞争;中国双抗竞争格局;中国ADC竞争格局;中国双抗技术全梳理;中国ADC技术全梳理;Ambrx技术全梳理;Vir Biotech技术全梳理;Immune-Onc技术全梳理;亘喜生物技术全梳理;康哲药业技术全梳理;科济药业技术全梳理;恺佧生物技术全梳理;同宜医药技术全梳理;百奥赛图技术全梳理;腾盛博药技术全梳理;创胜集团技术全梳理;永泰生物技术全梳理;中国抗体技术全梳理;德琪医药技术全梳理;德琪医药技术全梳理2.0;和铂医药技术全梳理;荣昌生物技术全梳理;再鼎医药技术全梳理;药明生物技术全梳理;恒瑞医药技术全梳理;豪森药业技术全梳理;正大天晴技术全梳理;吉凯基因技术全梳理;基石药业技术全梳理;百济神州技术全梳理;百济神州技术全梳理第2版;信达生物技术全梳理;信达生物技术全梳理第2版;中山康方技术全梳理;复宏汉霖技术全梳理;先声药业技术全梳理;君实生物技术全梳理;嘉和生物技术全梳理;志道生物技术全梳理;道尔生物技术全梳理;尚健生物技术全梳理;康宁杰瑞技术全梳理;科望医药技术全梳理;科望医药技术全梳理2.0;岸迈生物技术全梳理;礼进生物技术全梳理;康桥资本技术全梳理;余国良的抗体药布局;荃信生物技术全梳理;安源医药技术全梳理;三生国健技术全梳理;仁会生物技术全梳理;乐普生物技术全梳理;同润生物技术全梳理;宜明昂科技术全梳理;派格生物技术全梳理;迈威生物技术全梳理;Momenta技术全梳理;NGM技术全梳理;普米斯生物技术全梳理;普米斯生物技术全梳理2.0;三叶草生物技术全梳理;贝达药业抗体药全梳理;泽璟制药抗体药全梳理;恒瑞医药抗体药全梳理;齐鲁制药抗体药全梳理;石药集团抗体药全梳理;豪森药业抗体药全梳理;华海药业抗体药全梳理;科伦药业抗体药全梳理;百奥泰技术全梳理;凡恩世技术全梳理。
抗体药物偶联物引进/卖出
100 项与 BGB-R046 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 实体瘤 | 临床1期 | 中国 | 2024-07-03 | |
| 转移性实体瘤 | 临床1期 | - | 2024-07-01 | |
| 晚期恶性实体瘤 | 临床申请批准 | 中国 | 2024-06-08 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
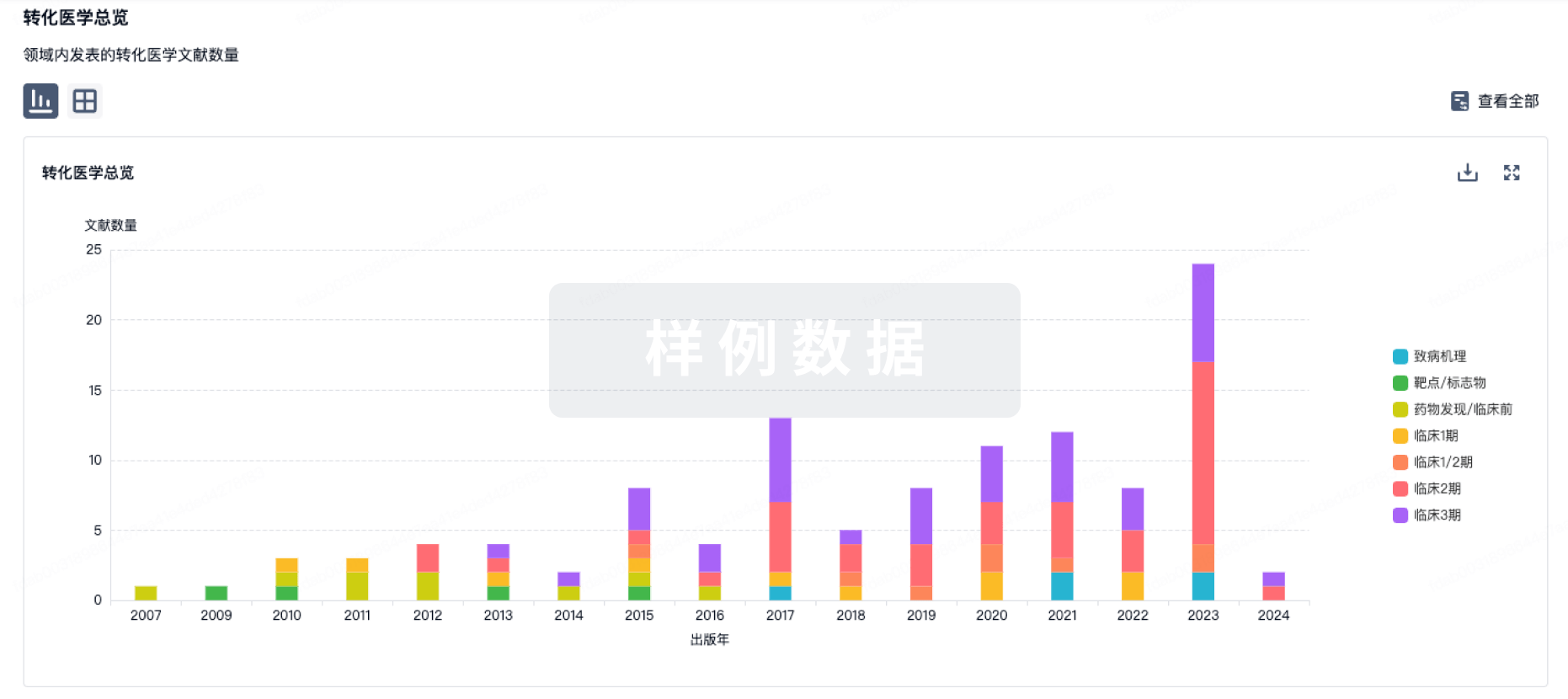
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
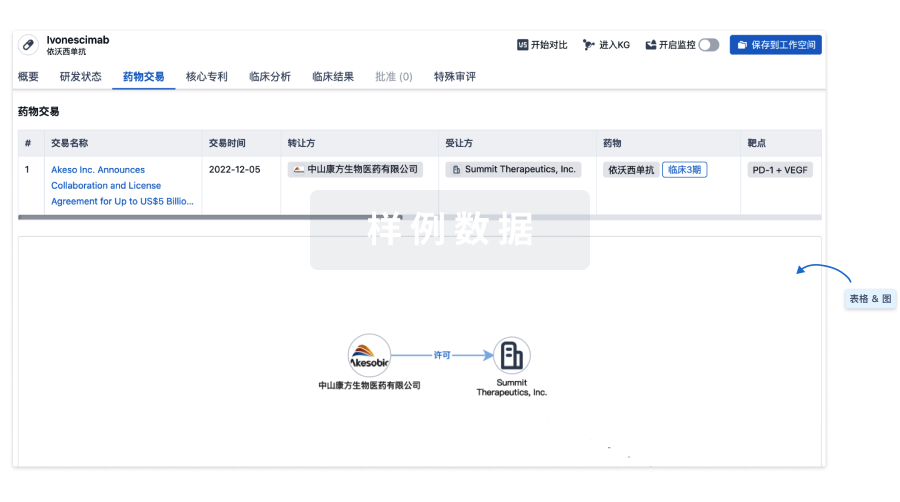
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
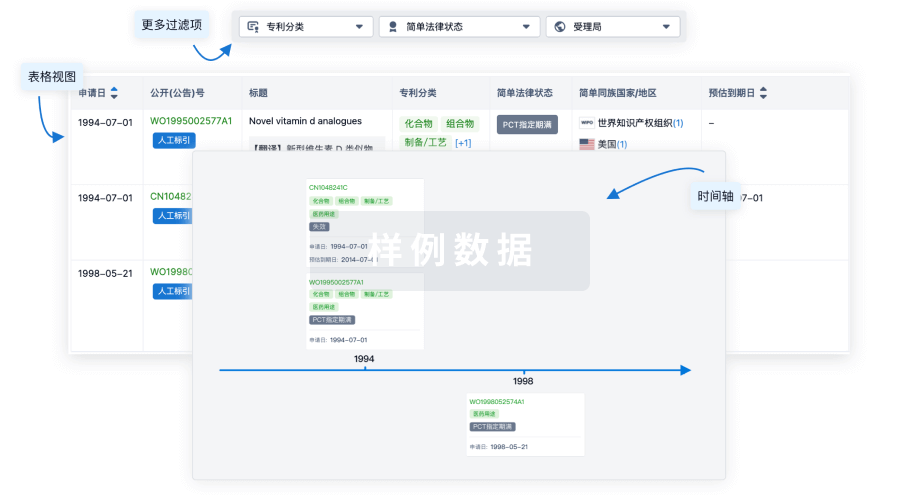
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
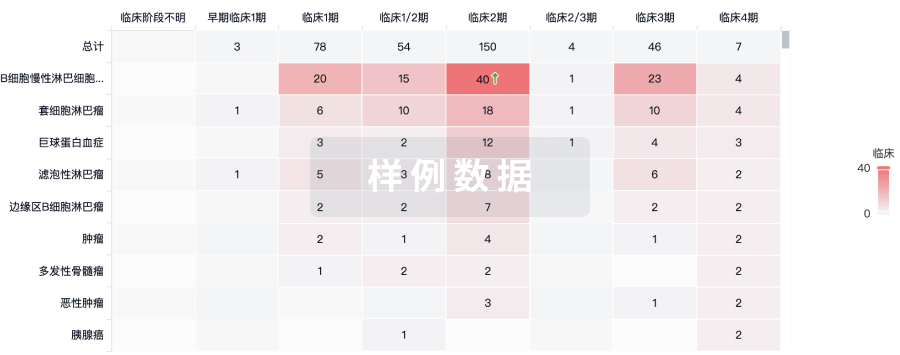
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
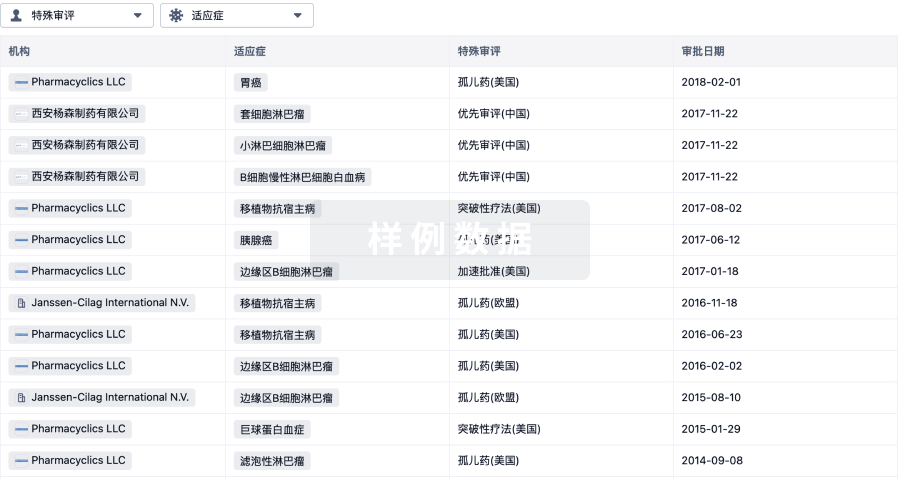
批准
利用最新的监管批准信息加速您的研究。
登录
或
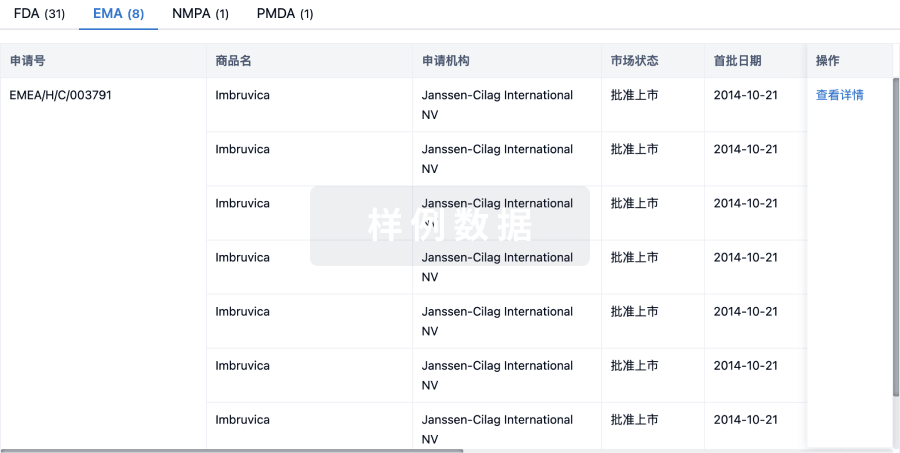
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
