更新于:2024-09-19
SOLVx-COVID-19
更新于:2024-09-19
概要
基本信息
非在研机构- |
最高研发阶段临床前 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
关联
100 项与 SOLVx-COVID-19 相关的临床结果
登录后查看更多信息
100 项与 SOLVx-COVID-19 相关的转化医学
登录后查看更多信息
100 项与 SOLVx-COVID-19 相关的专利(医药)
登录后查看更多信息
7
项与 SOLVx-COVID-19 相关的新闻(医药)2022-11-17
导 读RNA疗法是一种使用基于RNA分子来治疗或预防特定疾病的新疗法。随着mRNA COVID-19疫苗获得紧急授权并正式投入使用,RNA药物成为了研发新热点。纯化和细胞传递方面的进步使mRNA疗法得以广泛应用。与传统药物相比,RNA疗法具有成本效益高、易生产等优势。目前主要的 RNA 疗法包括:反义寡核苷酸、小干扰RNA(siRNA)、mRNA以及核酸适配体。本文将利用IQVIA Pipeline Intelligence数据库,回顾RNA疗法的最新进展。1RNA疗法在肿瘤治疗中的运用随着科学家对以寡核苷酸或siRNA为基础的靶向非编码RNA展现出越来越多的兴趣,RNA疗法在癌症领域的探索再度兴起。非编码RNA的优势在于其具有肿瘤特异性,即只在肿瘤中具有活性。Sirnaomics的cotsiranib (STP 705)是一种抑制TGF-Beta1和COX-2基因表达的双重靶点siRNA治疗方法,用于非黑色素瘤皮肤癌,包括鳞状细胞癌,基底细胞癌和肝癌的治疗。2022年2月,Sirnaomics公布了cotsiranib治疗皮肤基底细胞癌II期临床试验的中期数据。数据显示,剂量范围在30至90微克之间的患者,其剂量反应实现了完全应答,且无明显的皮肤不良反应。研发人员也在积极探索将mRNA疫苗技术应用于癌症的治疗干预,并设计为肿瘤相关抗原的表达,用于诱导细胞介导的免疫反应,以摧毁癌细胞。目前有两种mRNA疫苗正处于Ⅱ期临床试验阶段。默克和Moderna合作研发的mRNA 4157是一种基于mRNA的个性化癌症疫苗,通过引导患者的细胞表达选定的新表位,刺激免疫系统更好地识别并消灭癌细胞。该疫苗正处于Ⅱ期临床试验,验证与pembrolizumab联合用于治疗高风险的黑色素瘤患者,预计将于2023年12月完成。基因泰克和BioNTech研发的基于mRNA的个体化癌症疫苗autogene cevumeran(RG 6180;BNT 122)编码了20个来自患者的特异性肿瘤新抗原,以诱导针对肿瘤的强大免疫反应。该疫苗正作为一线治疗药物与pembrolizumab联合使用,对未经治疗的晚期黑色素瘤患者进行II期临床试验。同时,对将其作为替代II期(高风险)或III期手术切除结直肠癌的治疗模式的II期试验正在进行中。2RNA疗法在传染性疾病治疗中的运用BioNTech/辉瑞和Moderna的COVID-19疫苗是最早进入市场的两种mRNA疫苗。2020年12月11日,美国FDA紧急授权使用辉瑞和BioNTech共同研发的mRNA新冠疫苗tozinameran。Tozinameran采用LNP递送技术,由编码SARS-CoV-2的突变针刺蛋白的核苷修饰的mRNA组成,并于2021年8月23日被FDA正式批准用于预防16岁及以上人群的新冠肺炎。该疫苗随后在全球范围获得了100多个监管机构的批准。Moderna公司的elasomeran(SPIKEVAX;mRNA 1273)是一种由脂质纳米粒子包裹的RNA链组成的mRNA疫苗,编码一种预融合稳定形势的刺突SARS-CoV-2蛋白,已在美国、英国、欧盟、澳大利亚、加拿大、韩国和瑞士获批用于预防18岁及以上人群的新冠肺炎。该疫苗获得了韩国的附条件批准,并获得了多个国家的紧急使用授权,包括美国、日本和印度。3RNA疗法在心血管代谢性疾病治疗中的应用在过去十年中,研究人员已发现,部分RNA有助于调控心血管疾病,抑制胆固醇的形成、胆固醇斑块的堆积和心脏病发作后导致的细胞死亡。RNA疗法正作为一种治疗心血管代谢疾病的方法迅速崛起。Alnylam公司的patisiran(ONPATTRO)是一种针对转甲状腺素(TTR)的RNAi疗法,利用Arbutus公司专有的脂质纳米粒子技术,是第一个获得美国FDA批准的RNAi疗法,于2018年上市,用于治疗遗传性转甲状腺素介导的(hATTR)淀粉样变性引起的多发性神经病。Patisiran旨在通过抑制TTR蛋白的合成来使TTR mRNA沉默,并防止TTR淀粉样蛋白在组织中进一步积累。Patisiran也已在加拿大、欧盟和巴西获得批准。4RNA疗法在眼科疾病领域的应用眼科疾病领域是RNA疗法的另一个发展领域,基因沉默疗法在该领域中显示出良好表现。ProQR的ultevursen (QR 421a)是一种基于RNA的寡核苷酸药物,旨在治疗USH2A基因13号外显子突变引起的Usher综合征Ⅱ型和非综合征性视网膜色素变性。Ultevursen与突变的USH2A RNA结合,并通过外显子跳转方法将13号外显子从RNA中排除,使视网膜细胞能够产生一种略微缩短但功能正常、且对视觉至关重要的usherin蛋白的表达。目前,针对这些适应症的II/III期临床试验正在进行中。此外,还有两个项目的Ⅱ期试验也在进行中。Ionis的IONIS-FB-LRx是一种使用Ionis LICA技术设计的反义药物,旨在减少补体先天免疫系统中的关键蛋白补体因子B的产生。Ribomic的RBM 007是一种基于寡核苷酸的抗FGF2(成纤维细胞生长因子2)适体,能够同时抑制血管生成及视网膜中的瘢痕形成。 总 结 RNA疗法已成为治疗多种疾病的有效方式,为靶向致病基因表达模式提供了更多选择,具有可高效生产、可提供长期疗效,可降低基因毒性风险的特点,2020年首次获批用于预防COVID-19的mRNA疫苗就是一个成功案例。技术创新有助于扩大RNA疗法的应用范围,推进mRNA等复杂核酸模板的使用,造福更多患者。
信使RNA临床2期siRNA疫苗寡核苷酸
2022-11-04
·生物谷
Vaxzevria是一种“病毒载体”疫苗,使用了基于普通感冒病毒(腺病毒)的弱化版本的复制缺陷型黑猩猩病毒载体。
图片来源:摄图网
2022年11月03日讯 /生物谷BIOON/ --阿斯利康(AstraZeneca)近日宣布,其COVID-19疫苗Vaxzevria(ChAdOx1-S[重组],前称AZD1222)已获得欧洲药品管理局(EMA)授予完全上市许可(full marketing authorization)。
在欧盟,由于新型冠状病毒肺炎(COVID-19)的紧迫性,Vaxzevria最初被授予附条件上市许可(cMA)。由于继续有足够的安全性和有效性证据证实Vaxzevria的益处,EMA现已授予其完全上市许可(MA)。这一决定遵循了EMA人类使用药品委员会(CHMP)关于完全MA的积极建议。
完全MA涵盖了Vaxzevria在基础免疫(Primary series)中的使用,以及作为异源(与一种已批准的mRNA新冠肺炎疫苗接种)或同源(相同的疫苗)第三剂加强针的使用。
临床研究和现实证据表明,Vaxzevria对从轻度症状到严重疾病(包括住院和死亡)的所有形式的COVID-19都有效。其中包括对52项现实世界研究数据的专家审查,这些研究表明,Vaxzevria与可用的mRNA COVID-19疫苗相比,在三次注射后针对COVID-19住院和死亡可提供同等有效的保护。也有大量证据支持,在迄今为止测试的所有基础免疫计划之后使用Vaxzevria作为加强针接种。
阿斯利康疫苗和免疫治疗执行副总裁Iskra Reic表示:“Vaxzevria从附条件上市许可转变为完全上市许可,是EMA对Vaxzevria安全性和有效性的重要确认,表明其益处继续大于潜在风险。据估计,在疫苗接种的第一年,Vaxzeviria已帮助挽救了600多万人的生命,这反映了Vaxzevaria对新冠肺炎引起的严重疾病和死亡具有保护作用的证据强度。”
Vaxzevria(ChAdOx1-S[重组],前称AZD1222)由牛津大学发明。它使用基于普通感冒病毒(腺病毒)的弱化版本的复制缺陷型黑猩猩病毒载体,该病毒在黑猩猩中引起感染,并包含新型冠状病毒(SARS-CoV-2)刺突蛋白的遗传物质。接种疫苗后,会产生表面刺突蛋白,激发免疫系统攻击SARS-CoV-2病毒。
Vaxzevria是一种“病毒载体”疫苗,这意味着一种不会导致疾病的病毒版本被用作疫苗的一部分,让机体知道如果以后暴露在真正的病毒中如何对抗它。在过去的40年里,科学家们已使用这种疫苗技术来对抗其他传染病,如流感、寨卡病毒、埃博拉病毒和艾滋病毒。
截至目前,阿斯利康及其全球合作伙伴已向180多个国家分发了超过30亿剂Vaxzevria,其中约三分之二的疫苗已交付给中低收入国家。据估计,在其推出的第一年,Vaxzevria已经帮助拯救了全球600多万人的生命。
根据临床研究和全球数千万人的真实证据,Vaxzevria具有可接受的安全性。根据数百万接种Vaxzevria疫苗的人群,报告的常见不良反应包括:头痛、恶心、肌痛、关节痛、注射部位压痛/疼痛/发热/瘙痒、疲劳、不适、发热和寒战。大多数不良反应的严重程度为轻度至中度,通常在接种疫苗后几天内消失。(生物谷Bioon.com)
原文出处:Vaxzevria receives full Marketing Authorisation in the EU for the prevention of COVID-19

疫苗信使RNA免疫疗法合作
2022-10-20
国内稀缺的质粒-mRNA-LNP-成品端到端产业化服务平台楷拓速度- 4.5个月完成设计、施工与验证华中地区首条mRNA GMP产线,符合中美临床申报标准国际先进的mRNA技术平台,资深专业团队一站式服务10月20日,楷拓生物武汉mRNA GMP基地落成典礼在武汉光谷生物城正式举办。东湖高新区管委会副主任冯立,东湖高新区一级调研员、武汉国家生物产业基地建设服务中心建设融资处处长严兴春等政府、园区企业、合作伙伴和投资人嘉宾代表受邀参加典礼。楷拓生物联合创始人、CEO王潇博士,楷拓生物联合创始人、总经理任科云博士出席典礼。典礼现场,任科云博士代表楷拓生物团队向与会领导、嘉宾致欢迎辞,并分享了公司发展情况。2021年8月,楷拓生物落户武汉光谷生物城并建立基地,现拥有4700㎡研发中心及产业化产线,其中GMP厂房总面积3000㎡,配有技术转移场地、GMP车间、质控实验室,全套功能区实现质粒-mRNA-LNP-成品全覆盖,加速项目转移孵化效率。其中,质粒DNA GMP生产线已于2022年初投产,楷拓生物凭借强大的质粒DNA工艺开发和制造能力,完成多个客户的不同级别质粒需求的交付。此次投产的全新的mRNA和LNP GMP生产线实现了从质粒、mRNA合成、LNP递送、成品灌装端到端生产工艺流程,可为国内外mRNA疫苗和药物提供符合中美临床申报标准的GMP生产服务。东湖高新区管委会副主任冯立登台致辞并为楷拓生物武汉mRNA GMP基地正式启动剪彩。参与剪彩的嘉宾还有,东湖高新区一级调研员、武汉国家生物产业基地建设服务中心建设融资处处长严兴春,人福医药集团总裁邓霞飞先生,楷拓生物联合创始人、CEO王潇博士,楷拓生物联合创始人、总经理任科云博士,元生资本副总裁陆庭麟博士,楷拓生物质量管理部副总裁段成才先生。楷拓生物董事、元生资本副总裁陆庭麟博士,中信银行武汉东湖支行行长翟洲先生先后登台致辞,向楷拓生物武汉mRNA GMP基地落成表示祝贺。mRNA领域资深专家、前复星医药全球研发中心总裁回爱民博士在落成典礼上进行了《mRNA - COVID-19 疫苗和未来》主题分享,深入剖析行业趋势。楷拓生物致力于打造先进的工艺技术平台,建立稳定优质的上下游生态合作。落成典礼上,楷拓生物与Precision NanoSystems(PNI)、多宁生物、糖智医药、百林科制药装备达成战略合作。未来,楷拓生物将持续输出高质量服务,以专业精神、创新理念实现互信共赢的伙伴关系,加速核酸和基因治疗领域技术发展,助力先进疗法惠及社会大众。扫码加入BiG生物创新社读者交流群,分享、交流纯粹的行业知识,非诚勿扰!BiGScientific Driven, Making Impact!创新生态丨医药论坛丨行业分析媒体公关丨BiG Webinar联系我们商务:Max 18662346610媒体:Kathy 17621909690
信使RNA疫苗合作
100 项与 SOLVx-COVID-19 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 新型冠状病毒感染 | 临床前 | 美国 | - |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
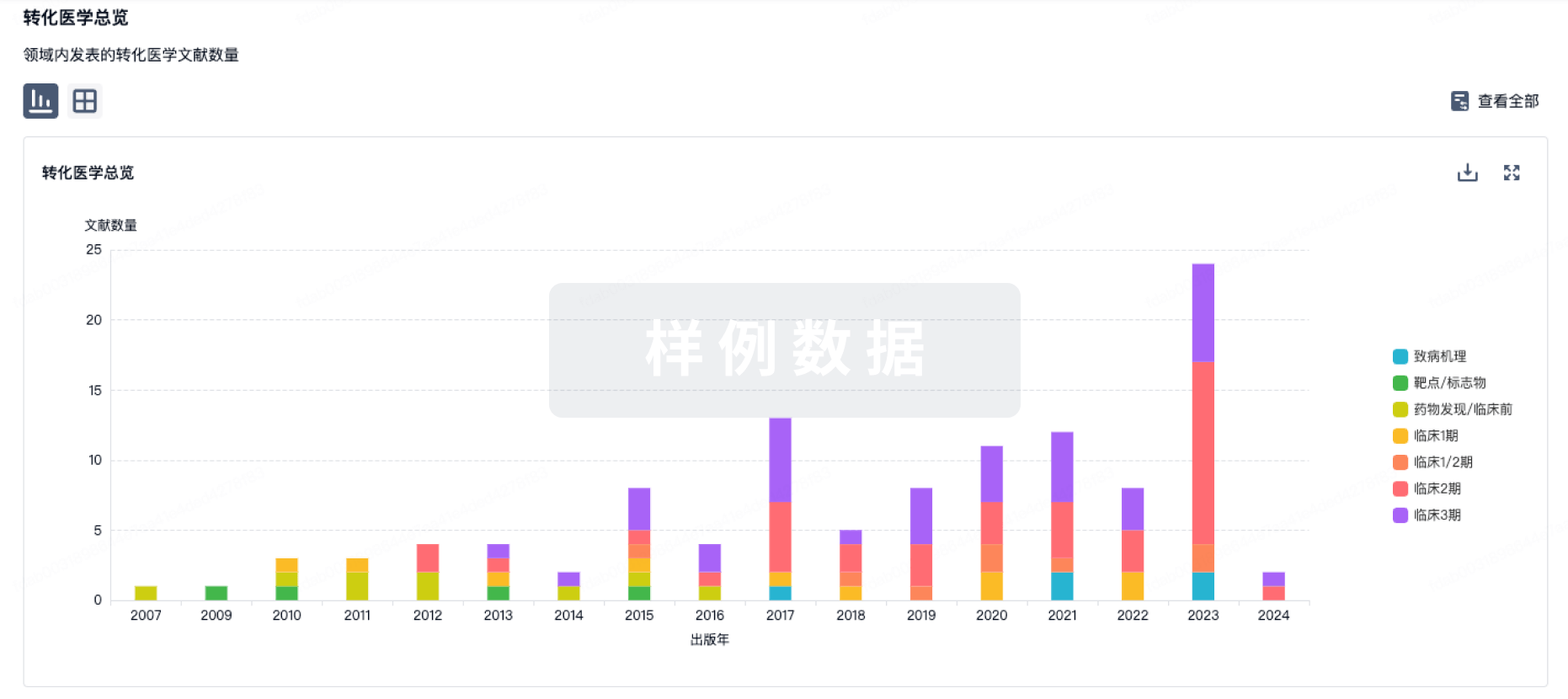
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
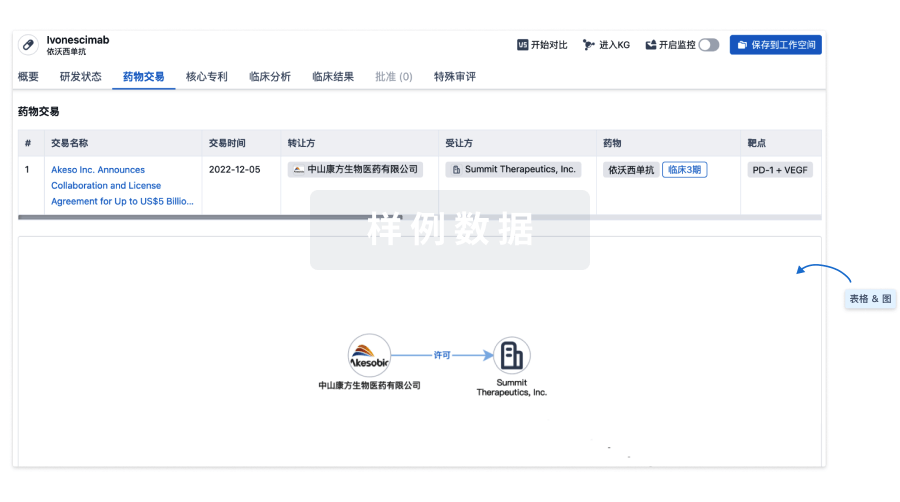
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
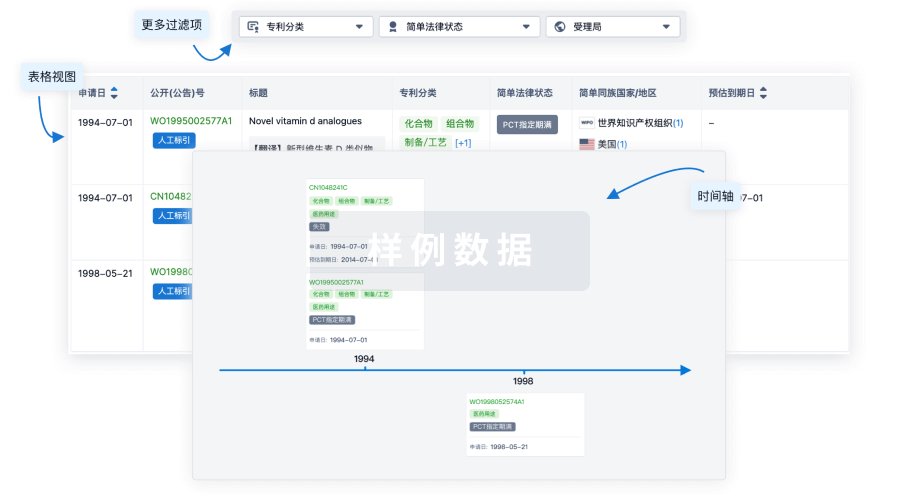
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
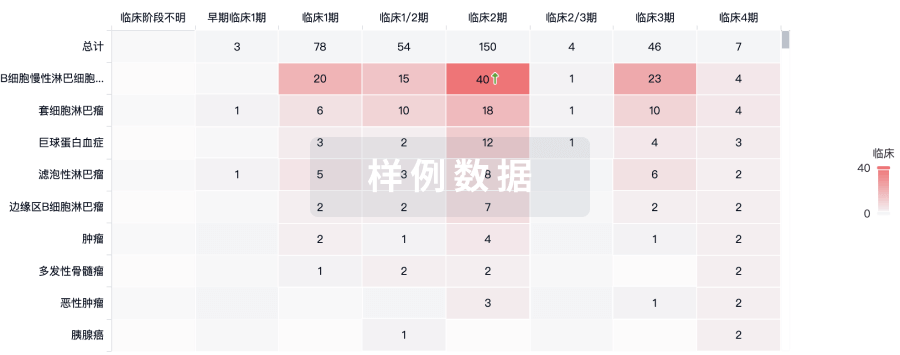
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
批准
利用最新的监管批准信息加速您的研究。
登录
或
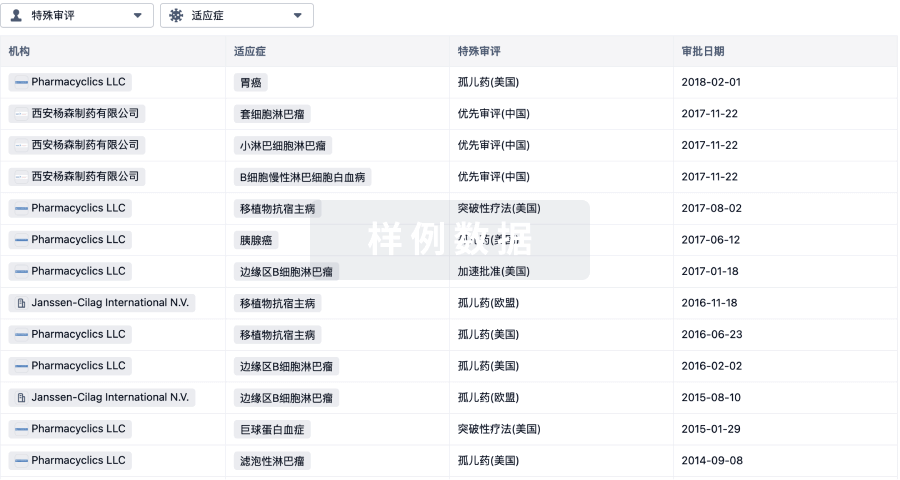
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用