预约演示
更新于:2025-05-26
SLC-391 (SignalChem)
更新于:2025-05-26
概要
基本信息
药物类型 小分子化药 |
别名 SLC-0211、SLC-391、SLC391 + [1] |
作用方式 抑制剂 |
作用机制 AXL抑制剂(AXL受体酪氨酸激酶抑制剂)、TYRO3抑制剂(TYRO3蛋白酪氨酸激酶抑制剂) |
在研适应症 |
非在研机构- |
最高研发阶段临床1/2期 |
首次获批日期- |
最高研发阶段(中国)临床1期 |
特殊审评- |
登录后查看时间轴
关联
5
项与 SLC-391 (SignalChem) 相关的临床试验NCT05860296
An Open-Label, Phase 1b/2a Study of SLC-391, an AXL Inhibitor, in Combination with Pembrolizumab in Subjects with Advanced or Metastatic Non-Small Cell Lung Cancer (NSCLC)
SLC-391 is a novel, potent and specific small molecule inhibitor of receptor tyrosine kinase AXL with desirable potency and pharmaceutical properties.
The study is being done to evaluate the safety and pharmacokinetic (PK) profile of SLC-391 in combination with pembrolizumab in participants with non-small cell lung cancer (NSCLC).
Each treatment cycle lasts 21 days. Participants will swallow SLC-391 pills two times every day. Participants will get pembrolizumab intravenously (IV) from the study site staff on the first day of every cycle.
This study has 2 parts. The first part will determine the recommended dose of SLC-391 in combination with pembrolizumab. The second part wants to find out if the combination of SLC-391 and pembrolizumab can help stop NSCLC tumours from growing or spreading.
The study is being done to evaluate the safety and pharmacokinetic (PK) profile of SLC-391 in combination with pembrolizumab in participants with non-small cell lung cancer (NSCLC).
Each treatment cycle lasts 21 days. Participants will swallow SLC-391 pills two times every day. Participants will get pembrolizumab intravenously (IV) from the study site staff on the first day of every cycle.
This study has 2 parts. The first part will determine the recommended dose of SLC-391 in combination with pembrolizumab. The second part wants to find out if the combination of SLC-391 and pembrolizumab can help stop NSCLC tumours from growing or spreading.
开始日期2023-05-31 |
申办/合作机构 |
NCT05772455
A Phase I, Open-label, Dose-escalation Study of the Safety, Pharmacokinetics and Efficacy of the XZB-0004 in Patients With Solid Tumours
XZB-0004 is a novel and potent small molecule inhibitor of receptor tyrosine kinase AXL.
This is an open-label, multicentre phase I study of XZB-0004 in patients with solid tumors. Part 1 is a dose-escalation study to evaluate the safety, pharmacokinetic (PK), and pharmacodynamic profile of XZB-0004, and then to identify a safe and pharmacologically active dose for evaluation in subsequent cohorts or clinical studies. Part 2 is a study to evaluate the efficacy and safety of XZB-0004 combined with Penpulimab in patients with NSCLC or advanced solid tumors.
This is an open-label, multicentre phase I study of XZB-0004 in patients with solid tumors. Part 1 is a dose-escalation study to evaluate the safety, pharmacokinetic (PK), and pharmacodynamic profile of XZB-0004, and then to identify a safe and pharmacologically active dose for evaluation in subsequent cohorts or clinical studies. Part 2 is a study to evaluate the efficacy and safety of XZB-0004 combined with Penpulimab in patients with NSCLC or advanced solid tumors.
开始日期2023-03-24 |
申办/合作机构 |
NCT05740917
A Multicenter, Open Phase I Clinical Study to Evaluate the Safety, Tolerability, Pharmacokinetics, Pharmacodynamics, and Initial Efficacy of XZB-0004 in the Treatment of Relapsed/Refractory Acute Myeloid Leukemia or Myelodysplastic Syndrome
This is an open-label, multicenter Phase I study that will enroll patients with relapsed/refractory AML or MDS. Stage Ia and stage Ib are included in this study. Phase Ia is a single-agent dose-escalation study that enrolling R/R AML subjects to identify XZB-0004 monotherapy MTD (if any) and RP2D and evaluate its safety and pharmacokinetic profile. Phase Ib will be an expanded study in R/R AML patients (group 1) and R/R MDS patients (group 2) at RP2D doses to further evaluate and determine the efficacy and safety of XZB-0004 in R/R AML or R/R MDS patients.
开始日期2023-02-01 |
申办/合作机构 |
100 项与 SLC-391 (SignalChem) 相关的临床结果
登录后查看更多信息
100 项与 SLC-391 (SignalChem) 相关的转化医学
登录后查看更多信息
100 项与 SLC-391 (SignalChem) 相关的专利(医药)
登录后查看更多信息
4
项与 SLC-391 (SignalChem) 相关的新闻(医药)2025-03-06
With increasing biomarker-driven cancer treatments, TEPMETKO benefits from growing adoption in precision oncology. Competition from other MET inhibitors like TABRECTA (capmatinib) exists, but TEPMETKO's once-daily dosing and efficacy profile offer differentiation.
LAS VEGAS, March 6, 2025 /PRNewswire/ -- DelveInsight's "
TEPMETKO Market Size, Forecast, and Market Insight Report" highlights the details around TEPMETKO, a kinase inhibitor indicated for the treatment of adult patients with metastatic NSCLC harboring MET exon 14 skipping alterations. The report provides product descriptions, patent details, and competitor products (marketed and emerging therapies) of TEPMETKO. The report also highlights the historical and forecasted sales from 2020 to 2034 segmented into 7MM [the United States, the EU4 (Germany, France, Italy, and Spain), the United Kingdom, and Japan].
EMD Serono's TEPMETKO (tepotinib) Overview
TEPMETKO is a kinase inhibitor prescribed for adult patients with metastatic non-small cell lung cancer (NSCLC) carrying MET exon 14 skipping alterations. The active component is Tepotinib (as hydrochloride monohydrate), administered orally. Patients should be cautioned about the heightened risk of severe or fatal interstitial lung disease/pneumonitis, liver toxicity, and potential embryo-fetal toxicity, necessitating effective contraception during and shortly after treatment.
Tepotinib specifically targets MET, including variants with exon 14 skipping mutations. It blocks HGF-dependent and independent MET phosphorylation, disrupting MET-driven signaling pathways. Additionally, at clinically relevant concentrations, Tepotinib inhibits melatonin 2 and imidazoline 1 receptors. In vitro studies show that it suppresses tumor cell proliferation, anchorage-independent growth, and migration of MET-dependent cancer cells. In mouse models with MET-driven tumors, including those with MET exon 14 skipping alterations, Tepotinib reduced tumor growth, sustained MET phosphorylation inhibition, and, in one case, decreased metastasis formation.
The recommended dose of TEPMETKO is 450 mg taken orally once daily until disease progression or intolerable toxicity occurs. Patients should take it at the same time each day, swallowing tablets whole without chewing, crushing, or splitting them. If a dose is missed and less than eight hours remain until the next scheduled dose, patients should skip it. In cases of vomiting after taking TEPMETKO, the next dose should be taken at the usual time.
Learn more about TEPMETKO projected market size for NSCLC @
TEPMETKO Market Potential
Non-small cell lung cancer (NSCLC) is the most common type of lung cancer, accounting for 81% of all diagnosed cases. Early detection greatly improves outcomes, but diagnosing NSCLC and other lung cancers is challenging because their symptoms are often mistaken for common illnesses or the long-term effects of smoking. Consequently,
80% of NSCLC cases are already at advanced stages by the time they are identified, making treatment more difficult. Around
80% of EGFR mutations in NSCLC involve either exon 19 deletions or the exon 21 L858R substitution, both of which are classified as sensitizing mutations.
Until the last decade, chemotherapy was the primary treatment for advanced and metastatic lung cancer. However, this changed in 2015 with the approval of the first immune checkpoint inhibitor (ICI),
KEYTRUDA (pembrolizumab), as a second-line therapy for advanced cases. This was followed by
TECENTRIQ (atezolizumab) in 2016. Both therapies were later approved for first-line treatment, broadening their use to a larger patient population. In 2020, the combination of
OPDIVO (nivolumab) and ipilimumab also received approval as a first-line treatment for metastatic NSCLC.
According to DelveInsight, the NSCLC market size across the 7MM is projected to grow from
USD 30 billion in 2024, with a substantial CAGR through 2034. This growth is largely driven by the introduction of emerging therapies during the forecast period (2025–2034).
Discover more about the NSCLC market in detail @
Non-small Cell Lung Cancer Market Report
Emerging Competitors of TEPMETKO
The NSCLC pipeline is very robust with the promising therapies such as
Telisotuzumab vedotin (AbbVie),
Patritumab deruxtecan (Daiichi Sankyo/AstraZeneca),
Datopotamab deruxtecan (Daiichi Sankyo/AstraZeneca),
Eftilagimod alpha (Immutep),
BNT311/GEN1046 (acasunlimab) (Genmab),
V940 (mRNA-4157) + Pembrolizumab (Moderna Therapeutics/Merck),
Plinabulin + Docetaxel (BeyondSpring),
Olomorasib (LY3537982) (Eli Lilly and Company),
Zipalertinib (Cullinan Oncology/Taiho Pharma),
Ceralasertib (AZD6738) (AstraZeneca),
TEDOPI (EP-2101; IDM 2101; OSE-2101) (OSE Immuno-therapeutics),
Sigvotatug vedotin
(PF08046047) (Pfizer),
ANKTIVA (N-803) (ImmunityBio),
Aumolertinib/Almonertinib/HS-10206 (Jiangsu Hansoh Pharmaceutical),
Niraparib (GSK),
Savolitinib (AstraZeneca/Hutchison MediPharma),
TRODELVY (Gilead Sciences),
Pyrotinib (Jiangsu HengRui Medicine),
Ociperlimab (BGB-A1217) (BieGene),
Volrustomig (AstraZeneca),
Gotistobart (BNT316/ONC-392) (OncoC4/BioNTech),
Ivonescimab (AK112/SMT112) (Akeso Biopharma/Summit Therapeutics),
ZYNYZ (retifanlimab/INCMGA00012) (Incyte/Macrogenics),
Divarasib (GDC-6036) (Roche/Genentech),
Tiragolumab (RG6058) (Roche),
Sacituzumab Tirumotecan (Merck and Kelun-Biotech),
JEMPERLI (dostarlimab/TSR-042) (GSK and AnaptysBio),
Zongertinib (BI-1810631) (Boehringer Ingelheim),
BAY 2927088 (Bayer),
Serplulimab (HLX10) (Shanghai Henlius Biotech),
Rilvegostomig (AZD2936) (AstraZeneca),
MK-1084 (Merck, Taiho Pharmaceutical, and Astex),
Domvanalimab (Arcus Biosciences and Gilead Sciences),
OPDUALAG (nivolumab and relatlimab) (Bristol-Myers Squibb),
Belrestotug + JEMPERLI (iTeos Therapeutics and GSK),
Firmonertinib (ArriVent BioPharma),
Sunvozertinib (DZD9008) (Dizal Pharmaceutical),
Cobolimab (GSK),
Livmoniplimab (AbbVie),
Fianlimab (REGN3767) (Regeneron Pharmaceuticals),
BNT327/PM8002 (Biotheus/BioNTech),
HS-20117 (Hansoh BioMedical),
IO102-IO103 + Pembrolizumab (IO Biotech),
Naptumomab estafenatox (NeoTX Therapeutics/Active Biotech),
FF-10832 (FUJIFILM Corporation),
BNT116 (BioNTechSE/Regeneron Pharmaceuticals),
CAN-2409 (Candel Therapeutics),
Mecbotamab Vedotin (BA3011/CAB-AXL-ADC) (BioAtla),
Bemcentinib (BGB 324/BGB-3234/R-428) (BerGenBio/Rigel Pharmaceuticals),
DOVBLERON (taletrectinib/AB-106/IBI-344) (Nuvation Bio/Innovent Biologics/Daiichi Sankyo/Nippon Kayaku),
Lifileucel (Iovance Biotherapeutics),
IBI363 (Innovent Biologics),
Sotevtamab (AB-16B5) (Alethia Biotherapeutics),
Avutometinib (VS6766) (Verastem Oncology),
Vebreltinib (APL-101) (Apollomics),
LP-300 (Lantern Pharma),
JNJ-90301900 (Johnson & Johnson Innovative Medicine),
AMG 193 (Amgen),
Luveltamab tazevibulin (Sutro Biopharma),
PRT3789 (Prelude Therapeutics),
Disitamab vedotin (Seagen),
PADCEV (enfortumab vedotin) (Astellas Pharma),
RP1 (Replimune),
TIVDAK (tisotumab vedotin) (Seagen),
Zanidatamab (Jazz Pharmaceuticals),
Utidelone injectable
(UTD1) (Beijing Biostar Pharmaceuticals),
REGN5093-M114 (Regeneron Pharmaceuticals),
SLC-391 (SignalChem Lifesciences),
fulzerasib (GenFleet),
Davutamig (REGN5093) (Regeneron Pharmaceuticals),
TAS3351 (Taiho Oncology),
H002 (RedCloud Bio),
JIN-A02 (J INTS BIO),
FWD1509 (Forward Pharma),
Sabestomig (AZD7789) (AstraZeneca),
Sasanlimab (Pfizer),
Selvigaltin (GB1211) (Galecto Biotech),
Vepafestinib Helsinn (Healthcare/Taiho Pharmaceutical),
EP0031 (A400/ KL590586) (Ellipses Pharma/Kelun-Biotech),
Pamvatamig (MCLA-129) (Merus),
Zidesamtinib (NVL-520) (Nuvalent),
NVL-655 (Nuvalent),
RMC-4630 (Revolution Medicines),
REQORSA (quaratusugene ozeplasmid) (Genprex),
PDC*lung01 (PDC*line Pharma),
Evalstotug (BA3071) (BioAtla and BeiGene),
PT-112 (Promontory Therapeutics),
MRT-2359 (Monte Rosa Therapeutics),
GAIA-102 (GAIA BioMedicine),
Rigosertib (Traws Pharma),
HMBD-001 (Hummingbird Bioscience),
PLB1004 (Avistone Biotechnology),
ANS03 (Avistone Biotechnology),
MYTX-011 (Mythic Therapeutics),
A166 (Sichuan Kelun-Biotech Bio-pharmaceutical),
Atamparib (BN-2397) (Ribon Therapeutics),
DELTACEL (KB-GDT-01) (Kiromic BioPharma),
Carotuximab (ENV-105) (Kairos Pharma),
YL202 (MediLink Therapeutics), and others.
To know more about the number of competing drugs in development, visit @
TEPMETKO Market Positioning Compared to Other Drugs
Key Milestones of TEPMETKO
In
February 2024, the FDA granted traditional approval to TEPMETKO for adult patients with metastatic NSCLC harboring MET exon 14 skipping alterations.
In
February 2022, the EC approved TEPMETKO as monotherapy for the treatment of adult patients with advanced NSCLC harboring alterations leading to METex14 skipping who require systemic therapy following prior treatment with immunotherapy and/or platinum-based chemotherapy.
In
February 2021, Merck announced that the US FDA has approved TEPMETKO following priority review for the treatment of adult patients with metastatic NSCLC harboring MET exon 14 skipping alterations. This indication was approved under accelerated approval based on ORR and DOR.
In
October 2020, TEPMETKO received ODD for treating NSCLC with MET genomic tumor aberrations
In
March 2020, EMD Serono (the biopharmaceutical business of Merck KGaA), announced that the MHLW approved TEPMETKO for the treatment of patients with unresectable, advanced, or recurrent NSCLC with METex14 skipping alterations.
In
September 2019, the US FDA granted BTD for tepotinib in patients with metastatic NSCLC harboring METex14 skipping alterations who progressed following platinum-based cancer therapy
Discover how TEPMETKO is shaping the NSCLC treatment landscape @
TEPMETKO NSCLC
TEPMETKO Market Dynamics
TEPMETKO competes in a growing but highly specialized market where MET-targeted therapies are gaining traction due to their
efficacy in addressing MET-altered tumors. The market for MET inhibitors is expanding as precision oncology advances and molecular diagnostics become more widely available,
enabling better identification of patients who would benefit from targeted treatments like TEPMETKO.
A key factor shaping TEPMETKO's market dynamics is competition. It directly competes with
Novartis' TABRECTA (capmatinib), another MET inhibitor approved for the same indication. While TEPMETKO offers the advantage of
once-daily dosing compared to TABRECTA's
twice-daily regimen, both drugs have similar efficacy profiles, making physician and patient preference an important differentiator. Additionally,
broader competition from next-generation MET inhibitors and combination therapies in clinical trials could impact TEPMETKO's long-term market position.
Regulatory approvals and market access play a crucial role in TEPMETKO's adoption. The drug has been approved in multiple regions, including the U.S., Europe, and Japan, but
reimbursement and pricing strategies vary by market. Payer policies, along with the
cost-benefit analysis of MET inhibitors compared to other targeted therapies, influence prescription trends. Furthermore,
real-world evidence and post-marketing studies will be critical in demonstrating TEPMETKO's sustained effectiveness and safety, which could support expanded indications and increased market penetration.
Looking ahead, the MET inhibitor market is expected to grow with advances in biomarker-driven therapy, further refining patient selection. TEPMETKO's success will depend on
continued clinical development, potential label expansions, and strategic partnerships to strengthen its competitive edge. As new entrants emerge, Merck KGaA's ability to differentiate TEPMETKO through combination strategies or enhanced formulations may determine its long-term sustainability in this evolving landscape.
Dive deeper to get more insight into TEPMETKO's strengths & weaknesses relative to competitors @
TEPMETKO Market Drug Report
Table of Contents
Related Reports
Non-small Cell Lung Cancer Market
Non-small Cell Lung Cancer Market Insights, Epidemiology, and Market Forecast – 2034 report deliver an in-depth understanding of the disease, historical and forecasted epidemiology, as well as the market trends, market drivers, market barriers, and key NSCLC companies including
Daiichi Sankyo, AstraZeneca, Gilead Sciences, BieGene, AbbVie, Roche, Merck, Novartis, Pfizer, Takeda Pharmaceuticals, Eli Lilly, BerGenBio, GlaxoSmithKline, Duality biologics, among others.
Non-small Cell Lung Cancer Pipeline
Non-small Cell Lung Cancer Pipeline Insight – 2025 report provides comprehensive insights about the pipeline landscape, pipeline drug profiles, including clinical and non-clinical stage products, and the key non-small cell lung cancer companies, including
BridgeBio Pharma, Daiichi Sankyo, EMD Serono, Merck, BridgeBio Pharma, Abbvie, Pfizer, Eli Lilly and Company BioNTech SE, Shenzhen TargetRx, Taiho Pharmaceutical, Chong Kun Dang, Bristol Myers Squibb, Innovent Biologics, Xuanzhu Biopharmaceutical, Bayer, GeneScience Pharmaceuticals, InventisBio, Apollomics, Imugene, Ono Pharmaceutical, Pierre Fabre, Jiangsu Hengrui Medicine Co., Bristol-Myers Squibb, Surface Oncology, Inhibrx, Sinocelltech, Mirati Therapeutics, REVOLUTION Medicines, Yong Shun Technology Development, Iovance Biotherapeutics, Galecto Biotech, among others.
C-MET Metastatic Non-small Cell Lung Cancer Market
C-MET Metastatic Non-small Cell Lung Cancer Market Insights, Epidemiology, and Market Forecast
– 2034 report deliver an in-depth understanding of the disease, historical and forecasted epidemiology, as well as the market trends, market drivers, market barriers, and key C-MET mNSCLC companies, including
Novartis, Merck, EMD Serono, AbbVie, Regeneron Pharmaceuticals, Mythic Therapeutics, Apollomics, Johnson & Johnson Innovation, Haihe Biopharma, among others.
C-MET Non-small Cell Lung Cancer Pipeline
C-MET Non-small Cell Lung Cancer Pipeline Insight – 2025 report provides comprehensive insights about the pipeline landscape, pipeline drug profiles, including clinical and non-clinical stage products, and the key C-MET non-small cell lung cancer companies, including
AbbVie, Janssen Research & Development, Beijing Pearl Biotechnology Limited Liability Company, Novartis, among others.
About DelveInsight
DelveInsight is a leading Business Consultant and Market Research firm focused exclusively on life sciences. It supports pharma companies by providing comprehensive end-to-end solutions to improve their performance. Get hassle-free access to all the healthcare and pharma market research reports through our subscription-based platform PharmDelve
.
Contact Us
Shruti Thakur
[email protected]
+14699457679
Logo:
SOURCE DelveInsight Business Research, LLP
WANT YOUR COMPANY'S NEWS FEATURED ON PRNEWSWIRE.COM?
440k+
Newsrooms &
Influencers
9k+
Digital Media
Outlets
270k+
Journalists
Opted In
GET STARTED
上市批准免疫疗法优先审批
2022-12-28
·赛柏蓝
来源 | 药智网作者 | 中华小吃01国内化药1类新药新增IND品种227个国内1类新药新增品种数量,是衡量2022年全年我国创新药研发进展的重要数据之一。在2019年化药1类新药注册新增品种首次超过100个以后,2020、2021两年内几乎是以近50%的速度快速增长,2021年全年的化药1类IND新增品种数量为243个。在新药开发迎来井喷式势头之后,开发的节奏正在逐渐减缓,并趋向平稳。截至2022年12月26日(全文以此时间统计),通过对国内新药注册申报1类品种(化药)进行统计并对数据进行逐一确定,2022年全年国内化药1类品种新增数量应为227个。 关注赛柏蓝,回复关键词“IND”查看完整名单。图1 2019-2022全年中国化药1类IND首次申报-受理品种统计02恒瑞领跑,一骑绝尘申办方维度,仅从注册的申报企业来看(不关联子母公司),2022年国内注册申报IND新增品种数量最多的企业为山东盛迪,共7个品种。紧随其后的申报企业依次为齐鲁制药、江苏恒瑞、东阳光药业、中美华世通生物、盛世泰科生物、广州必贝特医药、江苏恩华等等。而进一步关联,恒瑞医药成绩突出,本年度恒瑞(包括广东恒瑞、江苏恒瑞、山东盛迪、成都盛迪)大约有14个品种首次申报IND,应为本年度化药IND新增品种数量最多的企业。图2 2022年国产1类化药新药IND申请数量较多的企业032022全年首次申报-受理的IND品种新药IND阶段品种,基于申办方的开发策略不同,对外披露信息的程度也不同。通过查询,将部分新增品种的重点信息进一步摘录如下(以时间排序)。➣NO.1:GNP开发公司为广州雷恩康亚生物医药科技有限公司,临床适应症应为肺动脉高压以及心衰合并肺动脉高压。GNP是由17个氨基酸组成,并通过半胱氨酸二硫键相连的环状结构,来自于东非绿曼巴蛇的毒腺组织。➣NO.2:HSK36273开发公司为海思科医药集团股份有限公司,静脉给药,临床拟用于血液透析及术中患者的全身抗凝。作为一种小分子高选择XIa因子抑制剂,HSK36273具有高效、起效快、解离快等特点。已有研究表明,其疗效与肝素相当,同时安全性更好。➣NO.3:SCR-6920开发公司为江苏先声药业有限公司,是一款口服蛋白精氨酸甲基转移酶5(PRMT5)抑制剂,为合成致死领域抗肿瘤药物,临床适应症为晚期恶性肿瘤。该品种具有PRMT5高抑制活性和高选择性,药代证实其易分布于肿瘤内,肿瘤内药物浓度与血浆药物浓度比值是其他在研PRMT5抑制剂的10倍左右,有望降低靶点相关的血液毒性。➣NO.4:AC682开发公司为冰洲石生物科技(上海)有限公司,作用靶点为ER,是一款PROTAC产品。该品种已获得美国FDA的临床批准,适应症为ER+/HER2-局部晚期/转移性乳腺癌。➣NO.5:FHND5071开发公司为江苏正大丰海制药有限公司,为一种RET选择性抑制剂,具更优的体内药效特点、更高的肿瘤组织分布以及更低的有效剂量,同时还可以透过血脑屏障,对于原发或转移至中枢神经系统的肿瘤具有潜在的疗效。➣NO.6:DAJH-1050766开发公司为成都地奥九泓制药厂,是一款四代EGFR抑制剂。结构上同二代ALK抑制剂布加替尼和四代EGFR抑制剂BPI-361175的结构具有一定的相似性。➣NO.7:SMP-100开发公司为科岭源生物科技(深圳)有限公司,是一种选择性5-羟色胺3(5-HT3)受体部分激动剂。该品种可与5-HT3受体有高亲和性和高选择性,口服药代动力学特性较好,与其他药物相互作用低。➣NO.8:QR056251开发公司为武汉朗来科技发展有限公司,该品种为ROCK抑制剂,临床拟用于特发性肺纤维化(IPF)的治疗。➣NO.9:ABSK043开发公司为上海和誉生物医药科技有限公司,为一种PD-L1抑制剂,具有选择性高、生物利用度较好的特点,临床前数据证实了该品种的强效抑制效果,以及在多个临床前模型中的抗肿瘤效果。➣NO.10:DC05F01开发公司为北京双鹤润创科技有限公司,是一种Fascin蛋白抑制剂,为抗肿瘤口服品种。同时该品种是华润双鹤通过创新事业部从美国NOVITA引进的跨境创新药合作项目。据报道该品种的相关研发项目累计已至少投入研发费用1.49亿元。➣NO.11:ASC60开发公司为歌礼生物科技(杭州)有限公司,是一款强效、高选择性、安全的口服小分子脂肪酸合成酶抑制剂,拟用于治疗晚期实体瘤。➣NO.12:HHT120开发公司为上海华汇拓医药科技有限公司,是一款靶向凝血酶抑制剂,拟口服用于预防骨科大手术术后的静脉血栓栓塞症。目前,公司在该项目上已合计至少投入研发费用约人民币2898万元。➣NO.13:QY101开发公司为启元生物(杭州)有限公司,是一款磷酸二酯酶4(PDE4)抑制剂,以软膏剂临床拟用于特应性皮炎的治疗。临床前试验已初步显示了良好的PK特性,较好的药效和安全性。➣NO.14:H002开发公司为南京红云生物科技有限公司,是一款四代EGRF抑制剂,具有针对多种EGFR突变的广谱性和高选择性,在临床前研究中显示出广泛而持久的抗肿瘤活性,且安全性良好。➣NO.15:Y-3开发公司为南京宁丹新药技术有限公司,为抗缺血性脑卒中新药。Y-3是目前全球唯一在研的全新结构小分子PSD-95/nNOS解偶联剂,药效明确,安全性良好,药代性质稳定,能够透过血脑屏障,无被纤溶酶降解的风险。➣NO.16:LNK01004开发公司为凌科药业(杭州)有限公司,临床拟用于银屑病的治疗。据悉该品种可以同时抑制多个与银屑病相关的炎症细胞因子和疾病诱导信号通道,具有较好的功效潜力。➣NO.17:HSK36212开发公司为海思科医药集团股份有限公司,是自主研发的一种核因子相关因子通路小分子激动剂,临床拟用于治疗慢性肾脏病及急性肾损伤引起的肾脏疾病。➣NO.18:RGT-419B开发公司为上海齐鲁锐格医药研发有限公司,临床有望改善目前已上市的CDK4/6抑制剂的安全性,并克服耐药性。该品种的单药活性,与abemaciclib和palbociclib相比,对ER+肿瘤细胞生长的抑制作用更大。➣NO.19:QHL-236开发公司为上海亲合力生物医药科技股份有限公司,是一种结构新颖的紫杉类新药,可在肿瘤部位聚集和释放药效,从而显著降低化疗毒副作用和提升疗效。临床拟用于实体瘤的治疗。➣NO.20:BEBT-305开发公司为广州必贝特医药股份有限公司,是全球首个口服治疗银屑病和其他自身免疫性疾病的二代HSP90抑制剂,通过下调或降解参与自身免疫和炎症相关的多种细胞因子,抑制T细胞参与的自身免疫和炎症反应。➣NO.21:SYHX2005开发公司为石药集团欧意药业有限公司,是一种高选择性FGFR4抑制剂,具有优异的体内外活性和良好的安全性,临床拟用于晚期实体瘤的治疗。➣NO.22:XTR006开发公司为北京先通国际医药科技股份有限公司,是一种Tau蛋白神经纤维缠结(NFT)脑部正电子发射断层扫描成像的放射性诊断显像剂。➣NO.23:EVER001开发公司为云顶新耀医药科技有限公司,是新一代共价可逆布鲁顿酪氨酸激酶(BTK)抑制剂,临床拟用于治疗肾小球疾病。➣NO.24:QR060127开发公司为武汉朗来科技发展有限公司,是一种TRPC5抑制剂,通过阻断FSGS等肾脏疾病足细胞RAC1过度激活引起的肌动蛋白重构,阻碍足细胞从基底膜脱落,维持肾小球屏障系统的完整性,临床拟用于炎症性疼痛和局灶性阶段性肾小球硬化症等疾病的治疗。➣NO.25:XZB-0004开发公司为轩竹生物科技股份有限公司,是一款高活性和高选择性的AXL靶向抑制剂,临床拟用于晚期实体瘤、血液系统恶性肿瘤的治疗。➣NO.26:ASK0912开发公司为江苏奥赛康药业有限公司,是一种抗菌药物,对临床严重耐药的革兰氏阴性菌(G-)具有广谱活性,多项体内外药效研究显示抗菌活性强于多黏菌素B和E,并且毒性降低。➣NO.27:TRN-157开发公司为山东鲁抗医药股份有限公司,为一种雾化吸入剂,临床拟用于治疗慢性阻塞性肺疾病,包括慢性支气管炎和肺气肿、伴随性呼吸困难的维持治疗及急性发作的预防。该项目已至少累计投入1491.45万元人民币。➣NO.28:INS018_055开发公司为英矽智能科技(上海)有限公司,是该公司依托AI药物发现平台生成的首个抗纤维化小分子抑制剂,用于治疗特发性肺纤维化。另,英矽智能宣布已完成INS018_055在澳大利亚的I期临床试验的多名受试者的给药。➣NO.29:RP903开发公司为君实润佳(上海)医药科技有限公司,是一种PI3K-α抑制剂,该品种具备抑制PI3K通路的潜力,并具有抑制细胞增殖作用。➣NO.30:JDB383开发公司为上海嘉葆药银医药科技有限公司,是经首创人源化PDX模型验证的集落刺激因子(CSF1R)抑制剂,可有效调节巨噬细胞的存活、增殖和分化。临床前药代显示JDB383吸收较快,生物利用度较好。➣NO.31:JS116开发公司为上海君实生物医药科技股份有限公司,是一种具有全新结构的KRASG12C小分子不可逆共价抑制剂,用于治疗KRASG12C突变的非小细胞肺癌患者。临床前研究表明,JS116具有较宽的安全窗,良好的有效性和安全性。➣NO.32:ceralasertib开发公司为阿斯利康全球研发(中国)有限公司,为一款ATR抑制剂,该品种全球最高阶段已进入临床II~III期,临床使用该药单药或联合疗法针对多种肿瘤的临床试验。➣NO.33:WJ13404开发公司为苏州君境生物医药科技有限公司,为一款四代EGFR抑制剂,拟用于EGFR突变非小细胞肺癌和其他实体瘤的治疗。➣NO.34:ZKLJ02开发公司为云南中科龙津生物科技有限公司,是一款抗凝药,作用机制为抑制接触激肽系统关键靶标FXII和KLK、阻断凝血瀑布反应和炎症级联信号通路,临床拟用于急性缺血性脑卒中以改善神经功能缺损。该品种来源于森林山蛭,后经人工合成,是一种多肽类候选药物。➣NO.35:CGT-1881开发公司为盛世泰科生物医药技术(苏州)有限公司,口服给药,临床适用于非霍奇金淋巴瘤或多发性骨髓瘤的治疗。➣NO.36:CGT-9475开发公司为盛世泰科生物医药技术(苏州)有限公司,是一款间变性淋巴瘤激酶抑制剂,临床拟解决耐药性和中枢神经系统转移,癌种仍指向非小细胞肺癌及其脑转移。➣NO.37:HH3806开发公司为上海海和药物研究开发股份有限公司,是一种BD2选择性BET抑制剂,对BD2结构域的抑制活性是BD1的200多倍。在临床前研究的动物实验中,相比非选择性的BET抑制剂,HH3806保留了对部分实体瘤和血液瘤的良好药效,但对正常细胞的杀伤大幅减少,消化道和血液学毒性显著降低。➣NO.38:NRT6003开发公司为成都纽瑞特医疗科技股份有限公司,是一款选择性内照射治疗(SIRT)用放射性微球,即通过以炭微球为载体负载高活度的放射性钇[90Y]而得,临床拟开发治疗转移性肝癌。➣NO.39:RFUS-144开发公司为宜昌人福药业有限责任公司,是一种选择性阿片受体激动剂,临床用于治疗瘙痒症。非临床研究数据证实其具有高亲和性和高选择性,镇痛效果确切,兼具良好的安全性和耐受性,无成瘾、心脏、呼吸抑制等不良反应。➣NO.40:CIGB-814开发公司为山东鲁抗医药股份有限公司,是一种HSP60的CD4+T细胞表位的修饰肽配体,临床用于治疗类风湿性关节炎。➣NO.41:BGM0504开发公司为博瑞生物医药(苏州)股份有限公司,是一款GLP-1和GIP受体双重激动剂,以产生控制血糖、减重和治疗NASH等生物学效应,展现多种代谢疾病治疗潜力。➣NO.42:RJ4287开发公司为南京奥利墨斯医药科技有限公司,是一款新型的THRβ选择性激动剂,以通过促进肝脏脂代谢和降低脂毒性来改善NASH。PS:该品种同步计划美国FDA的注册申报。➣NO.43:ICP-490开发公司为北京诺诚健华医药科技有限公司,是一款通过该公司的分子胶平台开发的新型靶向蛋白降解剂,即通过与CRL4 CRBN-E3泛素连接酶复合物的底物受体CRBN特异性结合,可诱导淋巴转录因子Ikaros和Aiolos的泛素化和降解,从而诱导细胞凋亡,临床拟用于治疗多发性骨髓瘤、非霍奇金淋巴瘤等血液肿瘤。➣NO.44:WS015开发公司为中美华世通生物医药科技(武汉)股份有限公司,是一种口服不吸收的高分子聚合物创新药。PS:该品种的获批,进一步证明中美华世通在高分子聚合物药物领域的创新研发能力。➣NO.45:HS248开发公司为瀚晖制药有限公司,是一种高选择性的PI3Kγ抑制剂,可通过促进巨噬细胞向抗肿瘤的表型极化,增强肿瘤微环境中CD8+T细胞的活化来抑制肿瘤生长和转移,临床拟与PD-1等免疫检查点抑制剂进行联用,有望为PD-1抑制剂耐药性患者带来更多获益。➣NO.46:HRS-8427开发公司为江苏恒瑞医药股份有限公司,是一款抗菌药物,通过抑制细胞壁的生物合成发挥抑菌杀菌作用,临床前显示其在多个标准菌株和临床分离菌株构建的小鼠感染模型中发挥抗菌药效,安全性良好。PS:该品种已至少投入研发费用约3307万元。➣NO.47:HRS-1167开发公司为江苏恒瑞医药股份有限公司,该品种是通过抑制肿瘤细胞增殖,发挥抗肿瘤作用,临床拟进行晚期实体肿瘤的治疗。PS:该品种已至少投入研发费用约1,879万元。➣NO.48:SPN0103-009开发公司为杭州澳赛诺生物科技有限公司,是一种新型、长效的GLP-1肽类似物,临床拟用于治疗2型糖尿病和肥胖症,并期望最终拓展到非酒精性脂肪肝和阿尔茨海默症。➣NO.49:APS03118开发公司为北京志健金瑞生物医药科技有限公司,是一种高选择性第二代RET抑制剂,临床拟用于针对RET基因改变导致的非小细胞肺癌、甲状腺癌、胰腺癌、乳腺癌、卵巢癌、结直肠癌及其他晚期实体瘤的治疗,以及对第一代选择性RET抑制剂产生的耐药性的患者。➣NO.50:WJ-39开发公司为宁夏康亚药业股份有限公司,是一种基于糖尿病并发症关键靶点醛糖还原酶结构设计的喹啉酮乙酸类化合物,临床拟用于糖尿病肾病的治疗,以及肾功能的改善。➣NO.51:HRS-4642开发公司为江苏恒瑞医药股份有限公司,是一款KRAS G12D抑制剂,可靶向KRAS G12D突变,抑制肿瘤细胞增殖,是国内首个获批临床的KRAS G12D抑制剂。➣NO.52:HRS-5965开发公司为成都盛迪医药有限公司,可改善免疫复合物沉积导致的肾小球炎症,临床前显示其在大鼠肾炎模型中起到了显著的治疗性作用,安全性良好。PS:该品种已至少投入研发费用约2720万元。➣NO.53:氟[18F]思睿肽注射液开发公司为上海蓝纳成生物技术有限公司,是一种靶向PSMA的放射性体内诊断药物,与PSMA蛋白具有较高的特异性和亲和力,临床拟用于前列腺癌患者前列腺特异性膜抗原阳性病灶的正电子发射断层扫描成像。➣NO.54:BB102开发公司为北京伯汇生物技术有限公司,是一款新型小分子激酶抑制剂,具有高选择性、作用机制新颖、对基因突变型肿瘤同样有效、安全性好等特点,临床拟用于治疗异常基因驱动的晚期实体肿瘤。➣NO.55:MT1011开发公司为陕西麦科奥特科技有限公司,是一种小分子广谱抗凝拮抗剂,拟开发用于接受抗凝剂治疗(如凝血因子Xa抑制剂)的患者因危及生命或无法控制的出血而需要逆转抗凝治疗时的使用。➣NO.56:CG001419开发公司为上海睿跃生物科技有限公司,是一款高选择性强效口服TRK蛋白降解剂,临床拟用于NTRK基因融合、NTRK基因点突变和NTRK基因扩增或过表达晚期或转移性成人实体瘤。➣NO.57:Exd391209开发公司为成都奥达生物科技有限公司,是一款长效降糖新药,拟用于2型糖尿病的治疗。该品种是通过氨基酸长效化修饰技术,对原有的多肽药物GLP-1受体激动剂进行“升级”处理,通过突变肽链关键位点,降低多肽酶解率、延长药物血浆半衰期,满足周给药甚至双周给药。➣NO.58:SAL0112开发公司为深圳信立泰药业股份有限公司,是一款胰高血糖素样肽-1受体(GLP-1R)的口服小分子激动剂,临床拟用于2型糖尿病的治疗、及成人肥胖患者或超重患者的体重管理。➣NO.59:AC-003开发公司为爱科诺生物医药(苏州)有限公司,是一款靶向受体相互作用蛋白激酶1(RIPK1)的新型口服小分子抑制剂,能调节全身组织中的炎症和细胞死亡,临床拟用于特发性肺纤维化的治疗。➣NO.60:SR750开发公司为上海赛默罗德生物科技有限公司,是一款自主研发的治疗周围神经病理性疼痛候选药物,临床前研究结果显示,SR750具有较好的安全性和药代动力学特性。➣NO.61:VCT220开发公司为苏州闻泰医药科技有限公司,是一种新型非肽类口服小分GLP-1激动剂,能部分恢复胰岛β细胞功能,降低体重,改善血脂谱及降低血压,并且低血糖风险较小。临床拟用于2型糖尿病的治疗。➣NO.62:HRS-9821开发公司为广东恒瑞医药有限公司,是一款抑制呼吸道炎症、扩张支气管药物,临床拟用于慢性阻塞性肺疾病的维持治疗。PS:该品种已至少投入研发费用约2325万元。➣NO.63:SYHX2009开发公司为石药集团中奇制药技术(石家庄)有限公司,是一种选择性的NTRK和ROS1双靶点抑制剂,临床拟用于NTRK或ROS1基因重排/融合及其耐药突变阳性的实体瘤。➣NO.64:HRS-6209开发公司为江苏恒瑞医药股份有限公司,是一种选择性细胞周期阻断剂,可诱导肿瘤细胞发生G0/G1期阻滞,进而发挥抗肿瘤作用,临床拟用于晚期恶性肿瘤治疗。PS:该品种已至少投入研发费用约3014万元。➣NO.65:D3S-001开发公司为德昇济医药(无锡)有限公司,是一款高活性、高选择性、差异化的KRAS G12C抑制剂,具有成药性高,对靶点的抑制性强、抑制速度快、抑制完全,以及安全性好等潜在优势,临床拟开发用于治疗携带KRAS G12C突变的晚期实体瘤。➣NO.66:QLH11811开发公司为齐鲁制药有限公司,是一款四代EGFR抑制剂,可逆转C797S突变,同时也可抑制常见的ex19del、L858R以及T790M。另,该药还对多个肿瘤异种模型表现出优异的抑制活性。➣NO.67:EVT-401开发公司为浙江金华康恩贝生物制药有限公司,是一种非选择性阳离子通道P2X7抑制剂,临床拟用于类风湿性关节炎的治疗。PS:该品种已至少投入研发费用约2280万元。➣NO.68:WXSH0208开发公司为辰欣药业股份有限公司,是一种流感病毒RNA聚合酶抑制剂,可阻断病毒RNA的转录和复制,抑制流感病毒的增殖,临床拟用于甲型和乙型流感的治疗。PS:该品种已至少投入研发费用约4944.52万元。➣NO.69:RBD7022开发公司为苏州瑞博生物技术股份有限公司,是一款自主研发的针对ASGPR和PCSK9的siRNA疗法,临床拟用于治疗以低密度脂蛋白胆固醇升高为特征的原发性(家族性和非家族性)高胆固醇血症或混合型高脂血症。➣NO.70:Tinlarebant开发公司为倍亮生技医药(上海)有限公司,是一种口服的非维甲酸类RBP4小分子拮抗剂,可以减少和维持维生素A向眼睛的输送,以减少有毒维生素A副产物在眼组织中的积累,临床用于治疗青少年遗传性黄斑变性疾病。➣NO.71:GW201开发公司为北京广为医药科技有限公司,是一种高选择性、高亲和力的NMDA受体部分激动剂,临床拟开发用于治疗抑郁症。➣NO.72:BGB-15025开发公司为百济神州(苏州)生物科技有限公司,是一款造血干细胞激酶1(HPK1)抑制剂,在临床前研究中,抑制HPK1可有效促进T细胞激活,从而加强临床部分PD-1抑制剂的抗肿瘤活性。➣NO.73:HE009开发公司为南昌弘益药业有限公司,是一款S1P1小分子抑制剂,拟用于系统性红斑狼疮(SLE)的治疗。➣NO.74:YZJ-4729开发公司为上海海雁医药科技有限公司,是一种靶向μ-阿片受体(MOR)的小分子药物,可激活MOR受体。体外试验显示,YZJ-4729较TRV130有更高的选择性。体内在不同动物疼痛模型中均表现出剂量依赖性的强效镇痛作用,关键的呼吸抑制和便秘副反应都远远弱于吗啡,且明显好于TRV130。➣NO.75:ICP-248开发公司为北京诺诚健华医药科技有限公司,是一种新型的高选择性BCL2抑制剂,拟用于单药或与BTK抑制剂等其他药物联合治疗非霍奇金淋巴瘤、急性淋巴细胞白血病等恶性血液系统肿瘤。➣NO.76:BGC1201开发公司为赣江新区博瑞创新医药有限公司,是一款RTK-RAS-MAPK信号通路靶向药物,拟用于晚期实体瘤的治疗。➣NO.77:BT-114143开发公司为赛诺哈勃药业(成都)有限公司,是一款全新小分子纤维蛋白溶解酶/酶原抑制剂,拟用于治疗和预防纤维蛋白溶解亢进引起的各种出血和疾病。➣NO.78:RG002开发公司为上海凌济生物科技有限公司,是一种不可逆pan-FGFR抑制剂,适应症为晚期恶性肿瘤。➣NO.79:GH55开发公司为勤浩医药(苏州)有限公司,是一款双机制ERK1/2抑制剂,它在抑制ERK1/2激酶活性的同时,抑制MEK对于ERK1/2的激活,临床拟开发用于MAPK信号通路突变的晚期实体瘤。➣NO.80:HT-101开发公司为苏州星曜坤泽生物制药有限公司,为一款GalNAc偶联的siRNA创新药物,临床用于乙肝相关治疗。➣NO.81:LF0001开发公司为杭州瓴方生物医药科技有限公司,是一款KRAS G12C抑制剂,临床拟开展用于KRAS G12C突变的肺癌、结直肠癌、胰腺癌及其他实体瘤的治疗。➣NO.82:XH-5102开发公司为上海勋和医药科技有限公司,是一种高选择性JAK2抑制剂,可作为自身免疫系统疾病的治疗药物,而本次获批是拟开发治疗骨髓增殖性肿瘤。➣NO.83:GFH312开发公司为浙江劲方药业有限公司,是一款RIPK1抑制剂,临床用于外周动脉疾病伴间歇性跛行。该品种已获得美国FDA批准临床,且完成了澳大利亚地区的I期临床。➣NO.84:TUL01101开发公司为珠海联邦制药股份有限公司,是一种JAK抑制剂外用制剂,临床用于轻中度特应性皮炎的治疗。➣NO.85:RAB001开发公司为中山莱博瑞辰生物医药有限公司,是一款针对非创伤性骨坏死的小分子多肽偶联双重靶向创新药,通过增进内源性干细胞靶向到骨头,改善血液循环,修复骨坏死,刺激新骨形成。➣NO.86:HBW-3210开发公司为成都海博为药业有限公司,是一款三代BTK抑制剂,来自于该公司的透脑创新药物开发平台,临床拟用于B细胞非霍奇金淋巴瘤,主要开发适应症为原发性/继发性中枢神经系统淋巴瘤或可能累及中枢神经系统的弥漫大B细胞淋巴瘤。➣NO.87:BEBT-503开发公司为广州必贝特医药股份有限公司,是一种高活性泛PPAR激动剂,拟用于治疗糖尿病合并非酒精性脂肪性肝炎。➣NO.88:HRS-1780开发公司为山东盛迪医药有限公司,是一种临床拟用于治疗慢性肾脏疾病的口服小分子药物。PS:该品种已至少投入研发费用约1417万元。➣NO.89:TB-D004C开发公司为深圳市图微安创科技开发有限公司,是一款超长效内源性胃泌酸调节素类似物,能够同时作用于人胰高血糖素样肽-1受体和胰高血糖素受体的双重激动剂,临床拟用于2型糖尿病的治疗。➣NO.90:ATG-037开发公司为德丽(浙江)医药有限公司,是一款口服CD73小分子抑制剂,临床用于局部晚期及转移性实体瘤的治疗。➣NO.91:HRS-1358开发公司为山东盛迪医药有限公司,可抑制肿瘤细胞的增殖,与传统的小分子药物相比,可克服靶蛋白突变耐药以及对靶蛋白具有更高的选择性。PS:该品种已至少投入研发费用约2973万元。➣NO.92:RGT-264开发公司为上海齐鲁锐格医药研发有限公司,是一种高选择性HPK1(也称MAP4K1)抑制剂,拟用于晚期实体瘤的治疗。➣NO.93:KMHH-03开发公司为北京康明海慧生物科技有限公司,是一种多肽药物,该品种通过与肿瘤细胞膜表面的gp96相结合,抑制蛋白HER2受体的二聚化,并下调ER-α36受体水平,进而抑制肿瘤细胞增殖,同时可降低uPAR的稳定性,抑制肿瘤细胞的侵袭与转移,临床拟用于乳腺癌的治疗。➣NO.94:TR128开发公司为安徽中科拓苒药物科学研究有限公司,是新一代pan-RAF激酶抑制剂,体内外实验显示TR128对具有RAS及RAF突变的结直肠癌、胰腺癌、非小细胞肺癌及黑色素瘤等细胞表现出强烈的抑制细胞增殖、诱导细胞凋亡等活性。➣NO.95:ASC61开发公司为歌礼生物科技(杭州)有限公司,是一款口服PD-L1抑制剂,其活性代谢物是强效、高选择性的抑制剂,通过诱导PD-L1二聚体的形成和内吞,从而阻断PD-1/PD-L1的相互作用。➣NO.96:IMG-004开发公司为英脉生物医药(杭州)有限公司,是一种非共价、可逆的第三代BTK抑制剂,具有强效性、高选择性和脑渗透性,临床拟用于免疫性疾病的治疗。➣NO.97:AB-218开发公司为葆元生物医药科技(杭州)有限公司,是一种口服型脑渗透突变型IDH1选择性抑制剂,耐受性良好,脑分布良好,临床拟用于治疗具有IDH1突变的多种实体瘤。➣NO.98:BEBT-607开发公司为广州必贝特医药股份有限公司,是一种高活性KRAS G12C抑制剂,临床拟开发单药和联合用药用于治疗KRAS G12C突变的非小细胞肺癌、结直肠癌、胰腺癌等实体瘤。➣NO.99:GMDTC开发公司为健尔圣(珠海)医药科技有限公司,是一种重金属中毒解毒剂,临床用于驱除人体内镉、铅、铂等有害重金属,可用于治疗镉中毒,也可用于治疗铅中毒。➣NO.100:CGT-1967开发公司为盛世泰科生物医药技术(苏州)有限公司,是一种CDK4/6抑制剂,拟用于治疗血液肿瘤。➣NO.101:HJM-353开发公司为和径医药科技(上海)有限公司,是一种强效、选择性和口服生物可利用的EED抑制剂,拟开发治疗血液系统恶性肿瘤和实体瘤。➣NO.102:THDBH151开发公司为东宝紫星(杭州)生物医药有限公司,是一款痛风双靶点抑制剂,既能抑制黄嘌呤氧化酶,也可抑制肾小管URAT1转运体对尿酸重吸收,临床拟用于痛风的治疗。➣NO.103:ZX-4081开发公司为南京征祥医药有限公司,是一款高选择性的PI3Kγ抑制剂,临床与PD-1/L1、CTLA4等免疫检查点抑制剂进行联用,可用于PD1和CTLA4类抑制剂的耐药。➣NO.104:NH130开发公司为江苏恩华药业股份有限公司,是一种强效的5-HT2A受体反向激动剂,临床前试验结果表明,NH130枸橼酸盐对帕金森精神病动物模型有效,且不影响运动功能。PS:该项目已至少投入研发费用1300万元。➣NO.105:TL118开发公司为苏州韬略生物科技股份有限公司,是一款针对NTRK基因融合突变的抗肿瘤新药,临床拟用于晚期NTRK融合实体肿瘤的治疗。该品种较拉罗替尼和恩曲替尼结构有优势,能够作用于脑部。➣NO.106:NHL35700开发公司为江苏恩华药业股份有限公司,一种小分子磷酸二酯酶10A酶抑制剂,可靶向多巴胺受体、血清素受体和肾上腺素受体。该品种对多巴胺D1受体的亲和力高于D2受体,有望减少锥体外系反应、高泌乳素血症等副作用的发生率。➣NO.107:[177Lu]Lu-XT033开发公司为北京先通国际医药科技股份有限公司,是一种拟用于治疗前列腺特异性膜抗原阳性的转移性前列腺癌成人患者的放射性配体疗法药物。➣NO.108:OAB-14开发公司为山东新华制药股份有限公司,是一种贝沙罗汀衍生物,通过增加APP/PS1小鼠的β-淀粉样蛋白清除率,改善阿尔茨海默病相关的病理学和认知障碍。➣NO.109:BPI-460372开发公司为贝达药业股份有限公司,是一种靶向Hippo信号通路1的新分子实体化合物,属于新型强效转录增强因子TEAD小分子抑制剂,拟用于晚期实体瘤患者的治疗。➣NO.110:UA021开发公司为祐森健恒生物医药(上海)有限公司,是一种高效、高选择性及高口服生物利用度的TYK2变构抑制剂,拟开发用于治疗炎症性肠病、银屑病等自身免疫性疾病。.➣NO.111:AK0706开发公司为厦门特宝生物工程股份有限公司,是一种全新结构的PAPD5/7小分子抑制剂,能够抑制乙肝HBeAg的活性,降低乙肝表面抗原的表达水平,临床拟用于治疗慢性乙型肝炎。➣NO.112:ECC4703开发公司为上海诚益生物科技有限公司,是一种β-选择性、肝靶向性的THR完全激动剂;临床前研究已证明相较部分激动剂MGL-3196的高效,并且在NASH和血脂异常的动物模型中显示出优异的疗效。➣NO.113:BPI-452080开发公司为贝达药业股份有限公司,是一种创新、口服的小分子HIF-2α抑制剂,临床拟用于晚期实体瘤患者的治疗。➣NO.114:APG-5918开发公司为苏州亚盛药业有限公司,是一种口服的、新型强效、选择性小分子EED抑制剂;作为一种变构抑制剂,APG-5918能选择性结合EED蛋白,通过调节肿瘤表观遗传学及肿瘤微环境,有望克服肿瘤耐药,实现完全和持久的肿瘤消退。➣NO.115:SAL0119开发公司为深圳信立泰药业股份有限公司,是一款口服小分子免疫抑制剂,具有独特的、不同于JAK类的作用机制和广谱的细胞因子抑制作用,拟开发临床适应症包括活动性强直性脊柱炎及中重度活动性类风湿关节炎。➣NO.116:ABSK121-NX开发公司为无锡和誉生物医药科技有限公司,是新一代口服抗FGFR耐药突变抑制剂,临床拟用于治疗晚期实体瘤。2022全年首次申报-受理的IND品种♡左下角分享,右下角赞、在看,为赛柏蓝充电
临床申请申请上市一致性评价
2022-12-28
·药智网
过去3年,我国创新药的发展迎来了一次阶段性的高潮。在首次全年IND新增品种超过100个后,短短2年又内迅速突破了200个,国内创新药市场很快出现了“卷”的现象。随着近年来疫情所致的大环境变化,2022全年1类新药新增IND品种数量虽依旧很多,但走势已趋于平稳,新药开发和资本市场在逐渐冷静的同时也更好的反映了现阶段国内新药开发的现状。012022年,国内化药1类新药新增IND品种227个国内1类新药新增品种数量,是衡量2022年全年我国创新药研发进展的重要数据之一。在2019年化药1类新药注册新增品种首次超过100个以后,2020、2021两年内几乎是以近50%的速度快速增长,2021年全年的化药1类IND新增品种数量为243个。在新药开发迎来井喷式势头之后,开发的节奏正在逐渐减缓,并趋向平稳。截止2022年12月26日(全文以此时间统计),通过对国内新药注册申报1类品种(化药)进行统计并对数据进行逐一确定,2022年全年国内化药1类品种新增数量应为227个。PS:药智网公众号(ID:yaozh008)后台回复【首次IND】获取本文数据统计表格 图1 2019-2022全年中国化药1类IND首次申报-受理品种统计数据来源:药智数据022022年,恒瑞领跑,一骑绝尘申办方维度,仅从注册的申报企业来看(不关联子母公司),2022年国内注册申报IND新增品种数量最多的企业为山东盛迪,共7个品种。紧随其后的申报企业依次为齐鲁制药、江苏恒瑞、东阳光药业、中美华世通生物、盛世泰科生物、广州必贝特医药、江苏恩华等等。而进一步关联,恒瑞医药成绩突出,本年度恒瑞(包括广东恒瑞、江苏恒瑞、山东盛迪、成都盛迪)大约有14个品种首次申报IND,应为本年度化药IND新增品种数量最多的企业。图2 2022年国产1类化药新药IND申请数量较多的企业数据来源:药智数据032022全年首次申报-受理的IND品种新药IND阶段品种,基于申办方的开发策略不同,对外披露信息的程度也不同。通过查询,将部分新增品种的重点信息进一步摘录如下(以时间排序)。➣NO.1:GNP开发公司为广州雷恩康亚生物医药科技有限公司,临床适应症应为肺动脉高压以及心衰合并肺动脉高压。GNP是由17个氨基酸组成,并通过半胱氨酸二硫键相连的环状结构,来自于东非绿曼巴蛇的毒腺组织。➣NO.2:HSK36273开发公司为海思科医药集团股份有限公司,静脉给药,临床拟用于血液透析及术中患者的全身抗凝。作为一种小分子高选择XIa因子抑制剂,HSK36273具有高效、起效快、解离快等特点。已有研究表明,其疗效与肝素相当,同时安全性更好。➣NO.3:SCR-6920开发公司为江苏先声药业有限公司,是一款口服蛋白精氨酸甲基转移酶5(PRMT5)抑制剂,为合成致死领域抗肿瘤药物,临床适应症为晚期恶性肿瘤。该品种具有PRMT5高抑制活性和高选择性,药代证实其易分布于肿瘤内,肿瘤内药物浓度与血浆药物浓度比值是其他在研PRMT5抑制剂的10倍左右,有望降低靶点相关的血液毒性。➣NO.4:AC682开发公司为冰洲石生物科技(上海)有限公司,作用靶点为ER,是一款PROTAC产品。该品种已获得美国FDA的临床批准,适应症为ER+/HER2-局部晚期/转移性乳腺癌。➣NO.5:FHND5071开发公司为江苏正大丰海制药有限公司,为一种RET选择性抑制剂,具更优的体内药效特点、更高的肿瘤组织分布以及更低的有效剂量,同时还可以透过血脑屏障,对于原发或转移至中枢神经系统的肿瘤具有潜在的疗效。➣NO.6:DAJH-1050766开发公司为成都地奥九泓制药厂,是一款四代EGFR抑制剂。结构上同二代ALK抑制剂布加替尼和四代EGFR抑制剂BPI-361175的结构具有一定的相似性。➣NO.7:SMP-100开发公司为科岭源生物科技(深圳)有限公司,是一种选择性5-羟色胺3(5-HT3)受体部分激动剂。该品种可与5-HT3受体有高亲和性和高选择性,口服药代动力学特性较好,与其他药物相互作用低。➣NO.8:QR056251开发公司为武汉朗来科技发展有限公司,该品种为ROCK抑制剂,临床拟用于特发性肺纤维化(IPF)的治疗。➣NO.9:ABSK043开发公司为上海和誉生物医药科技有限公司,为一种PD-L1抑制剂,具有选择性高、生物利用度较好的特点,临床前数据证实了该品种的强效抑制效果,以及在多个临床前模型中的抗肿瘤效果。➣NO.10:DC05F01开发公司为北京双鹤润创科技有限公司,是一种Fascin蛋白抑制剂,为抗肿瘤口服品种。同时该品种是华润双鹤通过创新事业部从美国NOVITA引进的跨境创新药合作项目。据报道该品种的相关研发项目累计已至少投入研发费用1.49亿元。➣NO.11:ASC60开发公司为歌礼生物科技(杭州)有限公司,是一款强效、高选择性、安全的口服小分子脂肪酸合成酶抑制剂,拟用于治疗晚期实体瘤。➣NO.12:HHT120开发公司为上海华汇拓医药科技有限公司,是一款靶向凝血酶抑制剂,拟口服用于预防骨科大手术术后的静脉血栓栓塞症。目前,公司在该项目上已合计至少投入研发费用约人民币2898万元。➣NO.13:QY101开发公司为启元生物(杭州)有限公司,是一款磷酸二酯酶4(PDE4)抑制剂,以软膏剂临床拟用于特应性皮炎的治疗。临床前试验已初步显示了良好的PK特性,较好的药效和安全性。➣NO.14:H002开发公司为南京红云生物科技有限公司,是一款四代EGRF抑制剂,具有针对多种EGFR突变的广谱性和高选择性,在临床前研究中显示出广泛而持久的抗肿瘤活性,且安全性良好。➣NO.15:Y-3开发公司为南京宁丹新药技术有限公司,为抗缺血性脑卒中新药。Y-3是目前全球唯一在研的全新结构小分子PSD-95/nNOS解偶联剂,药效明确,安全性良好,药代性质稳定,能够透过血脑屏障,无被纤溶酶降解的风险。➣NO.16:LNK01004开发公司为凌科药业(杭州)有限公司,临床拟用于银屑病的治疗。据悉该品种可以同时抑制多个与银屑病相关的炎症细胞因子和疾病诱导信号通道,具有较好的功效潜力。➣NO.17:HSK36212开发公司为海思科医药集团股份有限公司,是自主研发的一种核因子相关因子通路小分子激动剂,临床拟用于治疗慢性肾脏病及急性肾损伤引起的肾脏疾病。➣NO.18:RGT-419B开发公司为上海齐鲁锐格医药研发有限公司,临床有望改善目前已上市的CDK4/6抑制剂的安全性,并克服耐药性。该品种的单药活性,与abemaciclib和palbociclib相比,对ER+肿瘤细胞生长的抑制作用更大。➣NO.19:QHL-236开发公司为上海亲合力生物医药科技股份有限公司,是一种结构新颖的紫杉类新药,可在肿瘤部位聚集和释放药效,从而显著降低化疗毒副作用和提升疗效。临床拟用于实体瘤的治疗。➣NO.20:BEBT-305开发公司为广州必贝特医药股份有限公司,是全球首个口服治疗银屑病和其他自身免疫性疾病的二代HSP90抑制剂,通过下调或降解参与自身免疫和炎症相关的多种细胞因子,抑制T细胞参与的自身免疫和炎症反应。➣NO.21:SYHX2005开发公司为石药集团欧意药业有限公司,是一种高选择性FGFR4抑制剂,具有优异的体内外活性和良好的安全性,临床拟用于晚期实体瘤的治疗。➣NO.22:XTR006开发公司为北京先通国际医药科技股份有限公司,是一种Tau蛋白神经纤维缠结(NFT)脑部正电子发射断层扫描成像的放射性诊断显像剂。➣NO.23:EVER001开发公司为云顶新耀医药科技有限公司,是新一代共价可逆布鲁顿酪氨酸激酶(BTK)抑制剂,临床拟用于治疗肾小球疾病。➣NO.24:QR060127开发公司为武汉朗来科技发展有限公司,是一种TRPC5抑制剂,通过阻断FSGS等肾脏疾病足细胞RAC1过度激活引起的肌动蛋白重构,阻碍足细胞从基底膜脱落,维持肾小球屏障系统的完整性,临床拟用于炎症性疼痛和局灶性阶段性肾小球硬化症等疾病的治疗。➣NO.25:XZB-0004开发公司为轩竹生物科技股份有限公司,是一款高活性和高选择性的AXL靶向抑制剂,临床拟用于晚期实体瘤、血液系统恶性肿瘤的治疗。➣NO.26:ASK0912开发公司为江苏奥赛康药业有限公司,是一种抗菌药物,对临床严重耐药的革兰氏阴性菌(G-)具有广谱活性,多项体内外药效研究显示抗菌活性强于多黏菌素B和E,并且毒性降低。➣NO.27:TRN-157开发公司为山东鲁抗医药股份有限公司,为一种雾化吸入剂,临床拟用于治疗慢性阻塞性肺疾病,包括慢性支气管炎和肺气肿、伴随性呼吸困难的维持治疗及急性发作的预防。该项目已至少累计投入1491.45万元人民币。➣NO.28:INS018_055开发公司为英矽智能科技(上海)有限公司,是该公司依托AI药物发现平台生成的首个抗纤维化小分子抑制剂,用于治疗特发性肺纤维化。另,英矽智能宣布已完成INS018_055在澳大利亚的I期临床试验的多名受试者的给药。➣NO.29:RP903开发公司为君实润佳(上海)医药科技有限公司,是一种PI3K-α抑制剂,该品种具备抑制PI3K通路的潜力,并具有抑制细胞增殖作用。➣NO.30:JDB383开发公司为上海嘉葆药银医药科技有限公司,是经首创人源化PDX模型验证的集落刺激因子(CSF1R)抑制剂,可有效调节巨噬细胞的存活、增殖和分化。临床前药代显示JDB383吸收较快,生物利用度较好。➣NO.31:JS116开发公司为上海君实生物医药科技股份有限公司,是一种具有全新结构的KRASG12C小分子不可逆共价抑制剂,用于治疗KRASG12C突变的非小细胞肺癌患者。临床前研究表明,JS116具有较宽的安全窗,良好的有效性和安全性。➣NO.30:ceralasertib开发公司为阿斯利康全球研发(中国)有限公司,为一款ATR抑制剂,该品种全球最高阶段已进入临床II~III期,临床使用该药单药或联合疗法针对多种肿瘤的临床试验。➣NO.33:WJ13404开发公司为苏州君境生物医药科技有限公司,为一款四代EGFR抑制剂,拟用于EGFR突变非小细胞肺癌和其他实体瘤的治疗。➣NO.34:ZKLJ02开发公司为云南中科龙津生物科技有限公司,是一款抗凝药,作用机制为抑制接触激肽系统关键靶标FXII和KLK、阻断凝血瀑布反应和炎症级联信号通路,临床拟用于急性缺血性脑卒中以改善神经功能缺损。该品种来源于森林山蛭,后经人工合成,是一种多肽类候选药物。➣NO.35:CGT-1881开发公司为盛世泰科生物医药技术(苏州)有限公司,口服给药,临床适用于非霍奇金淋巴瘤或多发性骨髓瘤的治疗。➣NO.36:CGT-9475开发公司为盛世泰科生物医药技术(苏州)有限公司,是一款间变性淋巴瘤激酶抑制剂,临床拟解决耐药性和中枢神经系统转移,癌种仍指向非小细胞肺癌及其脑转移。➣NO.37:HH3806开发公司为上海海和药物研究开发股份有限公司,是一种BD2选择性BET抑制剂,对BD2结构域的抑制活性是BD1的200多倍。在临床前研究的动物实验中,相比非选择性的BET抑制剂,HH3806保留了对部分实体瘤和血液瘤的良好药效,但对正常细胞的杀伤大幅减少,消化道和血液学毒性显著降低。➣NO.38:NRT6003开发公司为成都纽瑞特医疗科技股份有限公司,是一款选择性内照射治疗(SIRT)用放射性微球,即通过以炭微球为载体负载高活度的放射性钇[90Y]而得,临床拟开发治疗转移性肝癌。➣NO.39:RFUS-144开发公司为宜昌人福药业有限责任公司,是一种选择性阿片受体激动剂,临床用于治疗瘙痒症。非临床研究数据证实其具有高亲和性和高选择性,镇痛效果确切,兼具良好的安全性和耐受性,无成瘾、心脏、呼吸抑制等不良反应。➣NO.40:CIGB-814开发公司为山东鲁抗医药股份有限公司,是一种HSP60的CD4+T细胞表位的修饰肽配体,临床用于治疗类风湿性关节炎。➣NO.41:BGM0504开发公司为博瑞生物医药(苏州)股份有限公司,是一款GLP-1和GIP受体双重激动剂,以产生控制血糖、减重和治疗NASH等生物学效应,展现多种代谢疾病治疗潜力。➣NO.42:RJ4287开发公司为南京奥利墨斯医药科技有限公司,是一款新型的THRβ选择性激动剂,以通过促进肝脏脂代谢和降低脂毒性来改善NASH。PS:该品种同步计划美国FDA的注册申报。➣NO.43:ICP-490开发公司为北京诺诚健华医药科技有限公司,是一款通过该公司的分子胶平台开发的新型靶向蛋白降解剂,即通过与CRL4 CRBN-E3泛素连接酶复合物的底物受体CRBN特异性结合,可诱导淋巴转录因子Ikaros和Aiolos的泛素化和降解,从而诱导细胞凋亡,临床拟用于治疗多发性骨髓瘤、非霍奇金淋巴瘤等血液肿瘤。➣NO.44:WS015开发公司为中美华世通生物医药科技(武汉)股份有限公司,是一种口服不吸收的高分子聚合物创新药。PS:该品种的获批,进一步证明中美华世通在高分子聚合物药物领域的创新研发能力。➣NO.45:HS248开发公司为瀚晖制药有限公司,是一种高选择性的PI3Kγ抑制剂,可通过促进巨噬细胞向抗肿瘤的表型极化,增强肿瘤微环境中CD8+T细胞的活化来抑制肿瘤生长和转移,临床拟与PD-1等免疫检查点抑制剂进行联用,有望为PD-1抑制剂耐药性患者带来更多获益。➣NO.46:HRS-8427开发公司为江苏恒瑞医药股份有限公司,是一款抗菌药物,通过抑制细胞壁的生物合成发挥抑菌杀菌作用,临床前显示其在多个标准菌株和临床分离菌株构建的小鼠感染模型中发挥抗菌药效,安全性良好。PS:该品种已至少投入研发费用约3307万元。➣NO.47:HRS-1167开发公司为江苏恒瑞医药股份有限公司,该品种是通过抑制肿瘤细胞增殖,发挥抗肿瘤作用,临床拟进行晚期实体肿瘤的治疗。PS:该品种已至少投入研发费用约1,879万元。➣NO.48:SPN0103-009开发公司为杭州澳赛诺生物科技有限公司,是一种新型、长效的GLP-1肽类似物,临床拟用于治疗2型糖尿病和肥胖症,并期望最终拓展到非酒精性脂肪肝和阿尔茨海默症。➣NO.49:APS03118开发公司为北京志健金瑞生物医药科技有限公司,是一种高选择性第二代RET抑制剂,临床拟用于针对RET基因改变导致的非小细胞肺癌、甲状腺癌、胰腺癌、乳腺癌、卵巢癌、结直肠癌及其他晚期实体瘤的治疗,以及对第一代选择性RET抑制剂产生的耐药性的患者。➣NO.50:WJ-39开发公司为宁夏康亚药业股份有限公司,是一种基于糖尿病并发症关键靶点醛糖还原酶结构设计的喹啉酮乙酸类化合物,临床拟用于糖尿病肾病的治疗,以及肾功能的改善。➣NO.51:HRS-4642开发公司为江苏恒瑞医药股份有限公司,是一款KRAS G12D抑制剂,可靶向KRAS G12D突变,抑制肿瘤细胞增殖,是国内首个获批临床的KRAS G12D抑制剂。➣NO.52:HRS-5965开发公司为成都盛迪医药有限公司,可改善免疫复合物沉积导致的肾小球炎症,临床前显示其在大鼠肾炎模型中起到了显著的治疗性作用,安全性良好。PS:该品种已至少投入研发费用约2720万元。➣NO.53:氟[18F]思睿肽注射液开发公司为上海蓝纳成生物技术有限公司,是一种靶向PSMA的放射性体内诊断药物,与PSMA蛋白具有较高的特异性和亲和力,临床拟用于前列腺癌患者前列腺特异性膜抗原阳性病灶的正电子发射断层扫描成像。➣NO.54:BB102开发公司为北京伯汇生物技术有限公司,是一款新型小分子激酶抑制剂,具有高选择性、作用机制新颖、对基因突变型肿瘤同样有效、安全性好等特点,临床拟用于治疗异常基因驱动的晚期实体肿瘤。➣NO.55:MT1011开发公司为陕西麦科奥特科技有限公司,是一种小分子广谱抗凝拮抗剂,拟开发用于接受抗凝剂治疗(如凝血因子Xa抑制剂)的患者因危及生命或无法控制的出血而需要逆转抗凝治疗时的使用。➣NO.56:CG001419开发公司为上海睿跃生物科技有限公司,是一款高选择性强效口服TRK蛋白降解剂,临床拟用于NTRK基因融合、NTRK基因点突变和NTRK基因扩增或过表达晚期或转移性成人实体瘤。➣NO.57:Exd391209开发公司为成都奥达生物科技有限公司,是一款长效降糖新药,拟用于2型糖尿病的治疗。该品种是通过氨基酸长效化修饰技术,对原有的多肽药物GLP-1受体激动剂进行“升级”处理,通过突变肽链关键位点,降低多肽酶解率、延长药物血浆半衰期,满足周给药甚至双周给药。➣NO.58:SAL0112开发公司为深圳信立泰药业股份有限公司,是一款胰高血糖素样肽-1受体(GLP-1R)的口服小分子激动剂,临床拟用于2型糖尿病的治疗、及成人肥胖患者或超重患者的体重管理。➣NO.59:AC-003开发公司为爱科诺生物医药(苏州)有限公司,是一款靶向受体相互作用蛋白激酶1(RIPK1)的新型口服小分子抑制剂,能调节全身组织中的炎症和细胞死亡,临床拟用于特发性肺纤维化的治疗。➣NO.60:SR750开发公司为上海赛默罗德生物科技有限公司,是一款自主研发的治疗周围神经病理性疼痛候选药物,临床前研究结果显示,SR750具有较好的安全性和药代动力学特性。➣NO.61:VCT220开发公司为苏州闻泰医药科技有限公司,是一种新型非肽类口服小分GLP-1激动剂,能部分恢复胰岛β细胞功能,降低体重,改善血脂谱及降低血压,并且低血糖风险较小。临床拟用于2型糖尿病的治疗。➣NO.62:HRS-9821开发公司为广东恒瑞医药有限公司,是一款抑制呼吸道炎症、扩张支气管药物,临床拟用于慢性阻塞性肺疾病的维持治疗。PS:该品种已至少投入研发费用约2325万元。➣NO.63:SYHX2009开发公司为石药集团中奇制药技术(石家庄)有限公司,是一种选择性的NTRK和ROS1双靶点抑制剂,临床拟用于NTRK或ROS1基因重排/融合及其耐药突变阳性的实体瘤。➣NO.64:HRS-6209开发公司为江苏恒瑞医药股份有限公司,是一种选择性细胞周期阻断剂,可诱导肿瘤细胞发生G0/G1期阻滞,进而发挥抗肿瘤作用,临床拟用于晚期恶性肿瘤治疗。PS:该品种已至少投入研发费用约3014万元。➣NO.65:D3S-001开发公司为德昇济医药(无锡)有限公司,是一款高活性、高选择性、差异化的KRAS G12C抑制剂,具有成药性高,对靶点的抑制性强、抑制速度快、抑制完全,以及安全性好等潜在优势,临床拟开发用于治疗携带KRAS G12C突变的晚期实体瘤。➣NO.66:QLH11811开发公司为齐鲁制药有限公司,是一款四代EGFR抑制剂,可逆转C797S突变,同时也可抑制常见的ex19del、L858R以及T790M。另,该药还对多个肿瘤异种模型表现出优异的抑制活性。➣NO.67:EVT-401开发公司为浙江金华康恩贝生物制药有限公司,是一种非选择性阳离子通道P2X7抑制剂,临床拟用于类风湿性关节炎的治疗。PS:该品种已至少投入研发费用约2280万元。➣NO.68:WXSH0208开发公司为辰欣药业股份有限公司,是一种流感病毒RNA聚合酶抑制剂,可阻断病毒RNA的转录和复制,抑制流感病毒的增殖,临床拟用于甲型和乙型流感的治疗。PS:该品种已至少投入研发费用约4944.52万元。➣NO.69:RBD7022开发公司为苏州瑞博生物技术股份有限公司,是一款自主研发的针对ASGPR和PCSK9的siRNA疗法,临床拟用于治疗以低密度脂蛋白胆固醇升高为特征的原发性(家族性和非家族性)高胆固醇血症或混合型高脂血症。➣NO.70:Tinlarebant开发公司为倍亮生技医药(上海)有限公司,是一种口服的非维甲酸类RBP4小分子拮抗剂,可以减少和维持维生素A向眼睛的输送,以减少有毒维生素A副产物在眼组织中的积累,临床用于治疗青少年遗传性黄斑变性疾病。➣NO.71:GW201开发公司为北京广为医药科技有限公司,是一种高选择性、高亲和力的NMDA受体部分激动剂,临床拟开发用于治疗抑郁症。➣NO.72:BGB-15025开发公司为百济神州(苏州)生物科技有限公司,是一款造血干细胞激酶1(HPK1)抑制剂,在临床前研究中,抑制HPK1可有效促进T细胞激活,从而加强临床部分PD-1抑制剂的抗肿瘤活性。➣NO.73:HE009开发公司为南昌弘益药业有限公司,是一款S1P1小分子抑制剂,拟用于系统性红斑狼疮(SLE)的治疗。➣NO.74:YZJ-4729开发公司为上海海雁医药科技有限公司,是一种靶向μ-阿片受体(MOR)的小分子药物,可激活MOR受体。体外试验显示,YZJ-4729较TRV130有更高的选择性。体内在不同动物疼痛模型中均表现出剂量依赖性的强效镇痛作用,关键的呼吸抑制和便秘副反应都远远弱于吗啡,且明显好于TRV130。➣NO.75:ICP-248开发公司为北京诺诚健华医药科技有限公司,是一种新型的高选择性BCL2抑制剂,拟用于单药或与BTK抑制剂等其他药物联合治疗非霍奇金淋巴瘤、急性淋巴细胞白血病等恶性血液系统肿瘤。➣NO.76:BGC1201开发公司为赣江新区博瑞创新医药有限公司,是一款RTK-RAS-MAPK信号通路靶向药物,拟用于晚期实体瘤的治疗。➣NO.77:BT-114143开发公司为赛诺哈勃药业(成都)有限公司,是一款全新小分子纤维蛋白溶解酶/酶原抑制剂,拟用于治疗和预防纤维蛋白溶解亢进引起的各种出血和疾病。➣NO.78:RG002开发公司为上海凌济生物科技有限公司,是一种不可逆pan-FGFR抑制剂,适应症为晚期恶性肿瘤。➣NO.79:GH55开发公司为勤浩医药(苏州)有限公司,是一款双机制ERK1/2抑制剂,它在抑制ERK1/2激酶活性的同时,抑制MEK对于ERK1/2的激活,临床拟开发用于MAPK信号通路突变的晚期实体瘤。➣NO.80:HT-101开发公司为苏州星曜坤泽生物制药有限公司,为一款GalNAc偶联的siRNA创新药物,临床用于乙肝相关治疗。➣NO.81:LF0001开发公司为杭州瓴方生物医药科技有限公司,是一款KRAS G12C抑制剂,临床拟开展用于KRAS G12C突变的肺癌、结直肠癌、胰腺癌及其他实体瘤的治疗。➣NO.82:XH-5102开发公司为上海勋和医药科技有限公司,是一种高选择性JAK2抑制剂,可作为自身免疫系统疾病的治疗药物,而本次获批是拟开发治疗骨髓增殖性肿瘤。➣NO.83:GFH312开发公司为浙江劲方药业有限公司,是一款RIPK1抑制剂,临床用于外周动脉疾病伴间歇性跛行。该品种已获得美国FDA批准临床,且完成了澳大利亚地区的I期临床。➣NO.84:TUL01101开发公司为珠海联邦制药股份有限公司,是一种JAK抑制剂外用制剂,临床用于轻中度特应性皮炎的治疗。➣NO.85:RAB001开发公司为中山莱博瑞辰生物医药有限公司,是一款针对非创伤性骨坏死的小分子多肽偶联双重靶向创新药,通过增进内源性干细胞靶向到骨头,改善血液循环,修复骨坏死,刺激新骨形成。➣NO.86:HBW-3210开发公司为成都海博为药业有限公司,是一款三代BTK抑制剂,来自于该公司的透脑创新药物开发平台,临床拟用于B细胞非霍奇金淋巴瘤,主要开发适应症为原发性/继发性中枢神经系统淋巴瘤或可能累及中枢神经系统的弥漫大B细胞淋巴瘤。➣NO.87:BEBT-503开发公司为广州必贝特医药股份有限公司,是一种高活性泛PPAR激动剂,拟用于治疗糖尿病合并非酒精性脂肪性肝炎。➣NO.88:HRS-1780开发公司为山东盛迪医药有限公司,是一种临床拟用于治疗慢性肾脏疾病的口服小分子药物。PS:该品种已至少投入研发费用约1417万元。➣NO.89:TB-D004C开发公司为深圳市图微安创科技开发有限公司,是一款超长效内源性胃泌酸调节素类似物,能够同时作用于人胰高血糖素样肽-1受体和胰高血糖素受体的双重激动剂,临床拟用于2型糖尿病的治疗。➣NO.90:ATG-037开发公司为德丽(浙江)医药有限公司,是一款口服CD73小分子抑制剂,临床用于局部晚期及转移性实体瘤的治疗。➣NO.91:HRS-1358开发公司为山东盛迪医药有限公司,可抑制肿瘤细胞的增殖,与传统的小分子药物相比,可克服靶蛋白突变耐药以及对靶蛋白具有更高的选择性。PS:该品种已至少投入研发费用约2973万元。➣NO.92:RGT-264开发公司为上海齐鲁锐格医药研发有限公司,是一种高选择性HPK1(也称MAP4K1)抑制剂,拟用于晚期实体瘤的治疗。➣NO.93:KMHH-03开发公司为北京康明海慧生物科技有限公司,是一种多肽药物,该品种通过与肿瘤细胞膜表面的gp96相结合,抑制蛋白HER2受体的二聚化,并下调ER-α36受体水平,进而抑制肿瘤细胞增殖,同时可降低uPAR的稳定性,抑制肿瘤细胞的侵袭与转移,临床拟用于乳腺癌的治疗。➣NO.94:TR128开发公司为安徽中科拓苒药物科学研究有限公司,是新一代pan-RAF激酶抑制剂,体内外实验显示TR128对具有RAS及RAF突变的结直肠癌、胰腺癌、非小细胞肺癌及黑色素瘤等细胞表现出强烈的抑制细胞增殖、诱导细胞凋亡等活性。➣NO.95:ASC61开发公司为歌礼生物科技(杭州)有限公司,是一款口服PD-L1抑制剂,其活性代谢物是强效、高选择性的抑制剂,通过诱导PD-L1二聚体的形成和内吞,从而阻断PD-1/PD-L1的相互作用。➣NO.96:IMG-004开发公司为英脉生物医药(杭州)有限公司,是一种非共价、可逆的第三代BTK抑制剂,具有强效性、高选择性和脑渗透性,临床拟用于免疫性疾病的治疗。➣NO.97:AB-218开发公司为葆元生物医药科技(杭州)有限公司,是一种口服型脑渗透突变型IDH1选择性抑制剂,耐受性良好,脑分布良好,临床拟用于治疗具有IDH1突变的多种实体瘤。➣NO.98:BEBT-607开发公司为广州必贝特医药股份有限公司,是一种高活性KRAS G12C抑制剂,临床拟开发单药和联合用药用于治疗KRAS G12C突变的非小细胞肺癌、结直肠癌、胰腺癌等实体瘤。➣NO.99:GMDTC开发公司为健尔圣(珠海)医药科技有限公司,是一种重金属中毒解毒剂,临床用于驱除人体内镉、铅、铂等有害重金属,可用于治疗镉中毒,也可用于治疗铅中毒。➣NO.100:CGT-1967开发公司为盛世泰科生物医药技术(苏州)有限公司,是一种CDK4/6抑制剂,拟用于治疗血液肿瘤。➣NO.101:HJM-353开发公司为和径医药科技(上海)有限公司,是一种强效、选择性和口服生物可利用的EED抑制剂,拟开发治疗血液系统恶性肿瘤和实体瘤。➣NO.102:THDBH151开发公司为东宝紫星(杭州)生物医药有限公司,是一款痛风双靶点抑制剂,既能抑制黄嘌呤氧化酶,也可抑制肾小管URAT1转运体对尿酸重吸收,临床拟用于痛风的治疗。➣NO.103:ZX-4081开发公司为南京征祥医药有限公司,是一款高选择性的PI3Kγ抑制剂,临床与PD-1/L1、CTLA4等免疫检查点抑制剂进行联用,可用于PD1和CTLA4类抑制剂的耐药。➣NO.104:NH130开发公司为江苏恩华药业股份有限公司,是一种强效的5-HT2A受体反向激动剂,临床前试验结果表明,NH130枸橼酸盐对帕金森精神病动物模型有效,且不影响运动功能。PS:该项目已至少投入研发费用1300万元。➣NO.105:TL118开发公司为苏州韬略生物科技股份有限公司,是一款针对NTRK基因融合突变的抗肿瘤新药,临床拟用于晚期NTRK融合实体肿瘤的治疗。该品种较拉罗替尼和恩曲替尼结构有优势,能够作用于脑部。➣NO.106:NHL35700开发公司为江苏恩华药业股份有限公司,一种小分子磷酸二酯酶10A酶抑制剂,可靶向多巴胺受体、血清素受体和肾上腺素受体。该品种对多巴胺D1受体的亲和力高于D2受体,有望减少锥体外系反应、高泌乳素血症等副作用的发生率。➣NO.107:[177Lu]Lu-XT033开发公司为北京先通国际医药科技股份有限公司,是一种拟用于治疗前列腺特异性膜抗原阳性的转移性前列腺癌成人患者的放射性配体疗法药物。➣NO.108:OAB-14开发公司为山东新华制药股份有限公司,是一种贝沙罗汀衍生物,通过增加APP/PS1小鼠的β-淀粉样蛋白清除率,改善阿尔茨海默病相关的病理学和认知障碍。➣NO.109:BPI-460372开发公司为贝达药业股份有限公司,是一种靶向Hippo信号通路1的新分子实体化合物,属于新型强效转录增强因子TEAD小分子抑制剂,拟用于晚期实体瘤患者的治疗。➣NO.110:UA021开发公司为祐森健恒生物医药(上海)有限公司,是一种高效、高选择性及高口服生物利用度的TYK2变构抑制剂,拟开发用于治疗炎症性肠病、银屑病等自身免疫性疾病。.➣NO.111:AK0706开发公司为厦门特宝生物工程股份有限公司,是一种全新结构的PAPD5/7小分子抑制剂,能够抑制乙肝HBeAg的活性,降低乙肝表面抗原的表达水平,临床拟用于治疗慢性乙型肝炎。➣NO.112:ECC4703开发公司为上海诚益生物科技有限公司,是一种β-选择性、肝靶向性的THR完全激动剂;临床前研究已证明相较部分激动剂MGL-3196的高效,并且在NASH和血脂异常的动物模型中显示出优异的疗效。➣NO.113:BPI-452080开发公司为贝达药业股份有限公司,是一种创新、口服的小分子HIF-2α抑制剂,临床拟用于晚期实体瘤患者的治疗。➣NO.114:APG-5918开发公司为苏州亚盛药业有限公司,是一种口服的、新型强效、选择性小分子EED抑制剂;作为一种变构抑制剂,APG-5918能选择性结合EED蛋白,通过调节肿瘤表观遗传学及肿瘤微环境,有望克服肿瘤耐药,实现完全和持久的肿瘤消退。➣NO.115:SAL0119开发公司为深圳信立泰药业股份有限公司,是一款口服小分子免疫抑制剂,具有独特的、不同于JAK类的作用机制和广谱的细胞因子抑制作用,拟开发临床适应症包括活动性强直性脊柱炎及中重度活动性类风湿关节炎。➣NO.116:ABSK121-NX开发公司为无锡和誉生物医药科技有限公司,是新一代口服抗FGFR耐药突变抑制剂,临床拟用于治疗晚期实体瘤。数据来源:药智数据声明:本内容为作者独立观点,不代表药智网立场。如需转载,请务必注明文章作者和来源。如对本文有异议或投诉,请联系18323856316(同微信)。责任编辑 | 提特转载开白 | 马老师 18323856316(同微信)— Tips —如果您有医药行业相关的线索或对医药政策、研发创新、资本市场、行业发展有深度观察欢迎投稿给我们马老师 18323856316(同微信)邮箱:maxuelian@yaozh.com 阅读原文,是昨天最受欢迎的文章哦
临床申请申请上市一致性评价
100 项与 SLC-391 (SignalChem) 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 转移性非小细胞肺癌 | 临床2期 | 美国 | 2023-05-31 | |
| 转移性非小细胞肺癌 | 临床2期 | 加拿大 | 2023-05-31 | |
| 黑色素瘤 | 临床1期 | 中国 | 2023-03-24 | |
| 急性早幼粒细胞白血病 | 临床1期 | 中国 | 2023-02-01 | |
| 骨髓增生异常综合征 | 临床1期 | 中国 | 2023-02-01 | |
| 难治性急性髓细胞白血病 | 临床1期 | 中国 | 2023-02-01 | |
| 难治性骨髓增生异常综合征 | 临床1期 | 中国 | 2023-02-01 | |
| 复发性急性髓细胞白血病 | 临床1期 | 中国 | 2023-02-01 | |
| 晚期恶性实体瘤 | 临床1期 | 加拿大 | 2019-09-17 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
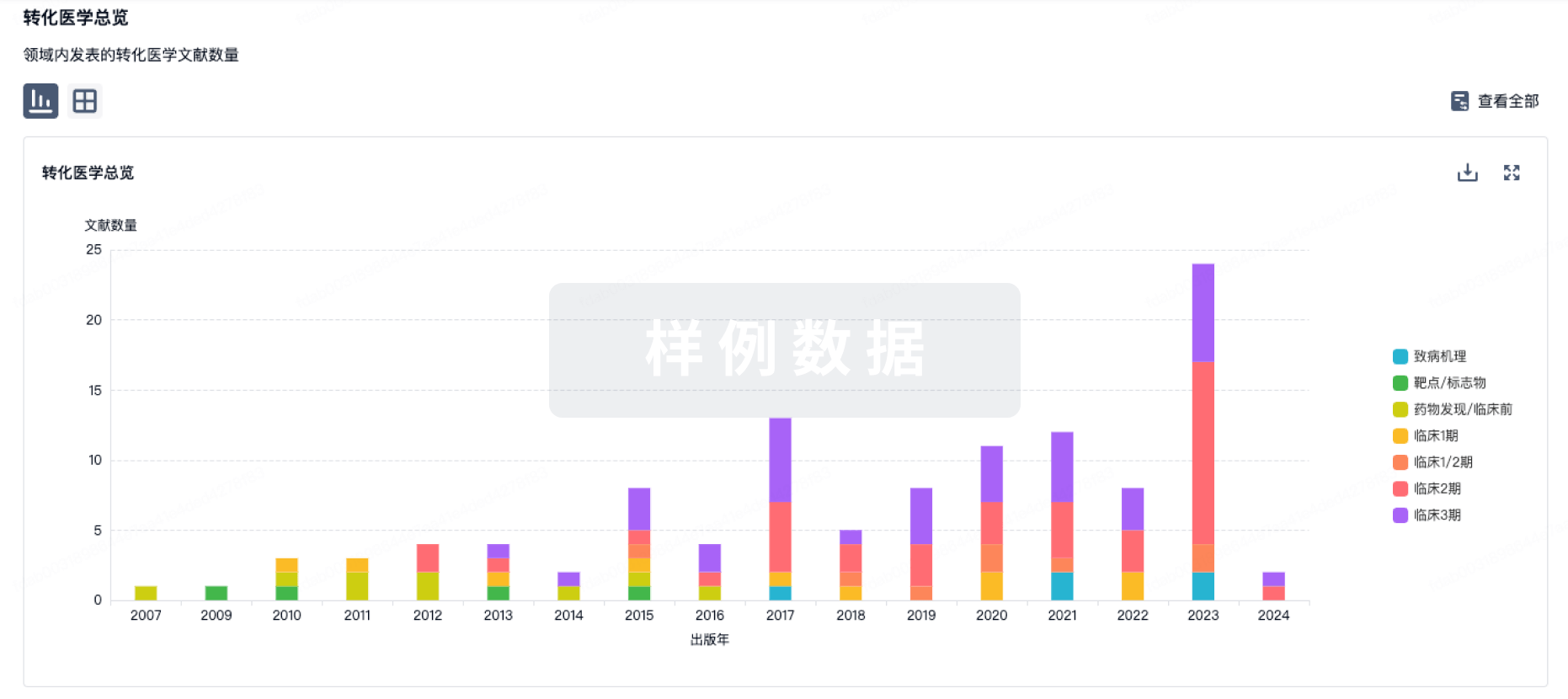
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
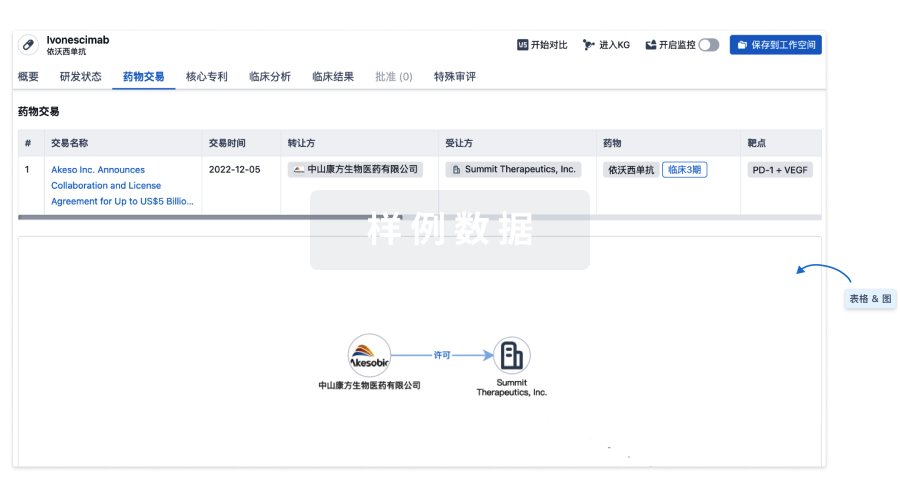
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
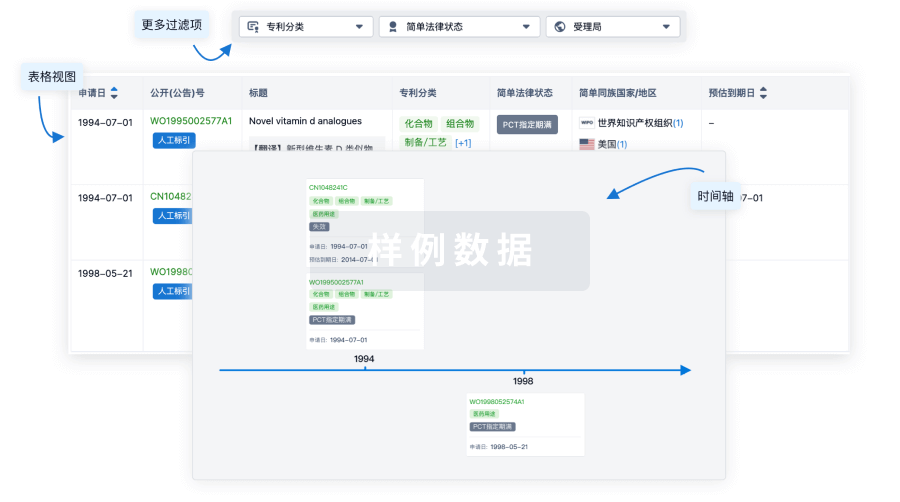
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
临床分析
紧跟全球注册中心的最新临床试验。
登录
或

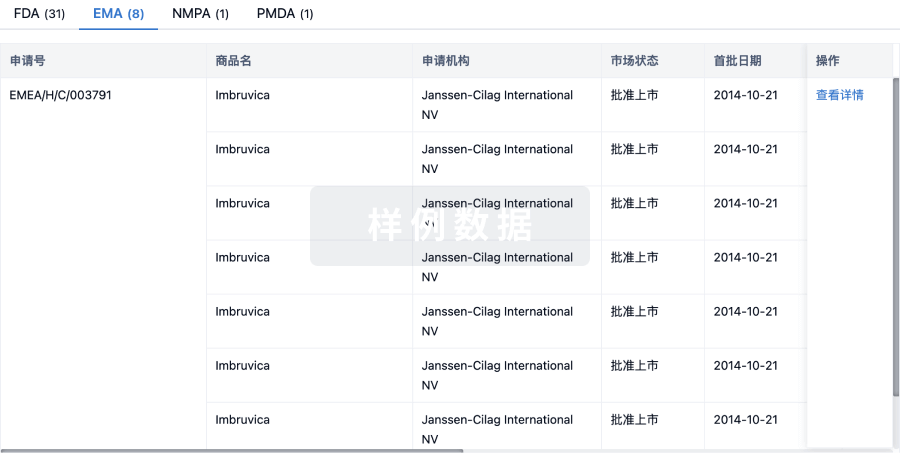
批准
利用最新的监管批准信息加速您的研究。
登录
或
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
Eureka LS:
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用

