预约演示
更新于:2025-05-07
Ac 225-DOTA-h11B6
更新于:2025-05-07
概要
基本信息
非在研机构- |
权益机构- |
最高研发阶段临床1期 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
登录后查看时间轴
结构/序列
使用我们的ADC技术数据为新药研发加速。
登录
或

Sequence Code 20489650

Sequence Code 20489648

关联
1
项与 Ac 225-DOTA-h11B6 相关的临床试验NCT04644770
A Phase 1 Study of JNJ-69086420, an Actinium-225-Labeled Antibody Targeting Human Kallikrein-2 (hK2) for Advanced Prostate Cancer
The purpose of this study is to determine the recommended Phase 2 dose(s) (RP2D[s]) of JNJ-69086420 in Part 1 (Dose Escalation), to determine safety and preliminary signs of clinical activity at the RP2D(s) in Part 2 (Dose Expansion), to determine safety of JNJ-69086420 at the RP2D(s) as a combination therapy in Part 3 (combination therapy) and to determine safety of JNJ-69086420 at the RP2D(s) in participants with metastatic hormone-sensitive prostate cancer (mHSPC) in Part 4.
开始日期2020-11-12 |
100 项与 Ac 225-DOTA-h11B6 相关的临床结果
登录后查看更多信息
100 项与 Ac 225-DOTA-h11B6 相关的转化医学
登录后查看更多信息
100 项与 Ac 225-DOTA-h11B6 相关的专利(医药)
登录后查看更多信息
10
项与 Ac 225-DOTA-h11B6 相关的新闻(医药)2024-10-12
·医药观澜
▎药明康德内容团队报道
今日(10月12日),中国国家药监局药品审评中心(CDE)官网公示,强生公司1类新药JNJ-78278343注射液获批临床,拟开发用于治疗晚期前列腺癌成人男性患者。根据强生公开资料,这是一款KLK2-CD3双特异性抗体在研新药,在国际范围内处于1期临床研究阶段。
截图来源:CDE官网
研究表明,人钾化因子2 (KLK2)是一种高度前列腺特异性抗原,它作为一种调节剂,可通过促进ARA70增强的雄激素受体的转激活,从而促进前列腺癌细胞的生长。
根据强生公开资料,JNJ-78278343是一种双特异性抗体以及T细胞重定向产品,其被设计用于靶向KLK2,并通过与T细胞上的CD3结合而诱导T细胞活化。该产品具有潜在的免疫调节和抗肿瘤活性,给药后可结合T细胞上的CD3和表达KLK2的肿瘤细胞上的KLK2,由此将T细胞重定向到表达KLK2的肿瘤细胞,产生T细胞介导的KLK2表达肿瘤细胞的裂解。
根据ClinicalTrials官网,强生正在开展3项JNJ-78278343针对前列腺癌的1期临床研究,包括:一项单药针对晚期前列腺癌的1期研究,一项联合JNJ-87189401(PSMA-CD28双特异性抗体)治疗晚期前列腺癌的1期研究,以及一项联合抗PD-1抗体cetrelimab、紫杉烷化疗或雄激素受体途径抑制剂治疗转移性去势抵抗性前列腺癌的1期临床研究。
此外,2024年欧洲肿瘤内科学会(ESMO年)会官网展示了JNJ-78278343联合JNJ-87189401 (PSMA-CD28双特异性抗体)治疗晚期前列腺癌的1期临床试验设计。根据强生公开资料介绍,从作用机制上来看,CD28的激活显著增强了T细胞通过CD3途径的激活,触发了一个共刺激途径,因此通过联合这两款双抗,同时激活CD3和CD28通路,可能会改善T细胞活化,产生更深入、更持久的临床反应。
▲两款双抗联合治疗前列腺癌作用机制(截图来源:强生官网)
KLK2是针对前列腺癌治疗领域的一个新靶点。通过公开渠道查询,全球范围内只有少数几款KLK2靶向疗法进入临床研究阶段,其中强生布局了多款针对该靶点的创新疗法,除了本次获批临床的KLK2-CD3双抗,还有靶向KLK2的CAR-T细胞疗法JNJ-75229414、靶向KLK2的放射性治疗药物JNJ-69086420 (JNJ-6420),这两款新药均处于1期临床研究阶段。
期待这些新药后续研究进展顺利,早日为患者带来新的治疗选择。
参考资料:
[1]中国国家药监局药品审评中心(CDE)官网. Retrieved Oct 12,2024, From https://www.cde.org.cn/main/xxgk/listpage/4b5255eb0a84820cef4ca3e8b6bbe20c
[2]强生官网. From https://www.janssenscience.com/media/attestation/congresses/oncology/2024/esmo/a-phase-1-firstinhuman-openlabel-multicenter-trialinprogress-of-the-safety-tolerability-and-prelimin.pdf
[3]1659TiP A phase I, first-in-human, open-label, multicenter, trial-in-progress of the safety, tolerability, and preliminary efficacy of JNJ-87189401 (PSMA-CD28 bispecific antibody) combined with JNJ-78278343 (KLK2-CD3 bispecific antibody) for advanced prostate cancer. Retrieved Sep 12,2024, From https://www.annalsofoncology.org/article/S0923-7534(24)03259-9/fulltext
本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权或其他合作需求,请联系wuxi_media@wuxiapptec.com。
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
临床1期细胞疗法免疫疗法临床申请ASH会议
2024-09-11
PanTera aims to accelerate actinium-225 production, used in promising targeted alpha therapy for cancer. Image: Getty Images / Love Employee.
PanTera, a Belgian radioisotope producer, announced today (11 September) that it had secured €93m ($102.4m) in an oversubscribed Series A financing round to accelerate production of actinium-225. The radioactive isotope is integral to several investigational cancer therapies.
This is the largest Series A financing round in the Belgian life sciences sector to date. The round was led by EQT Life Sciences.
Ion Beam Applications
(IBA), which invested in the joint venture PanTera with SCK CEN (the Belgian Nuclear Research Centre), and SFPIM—Belgium’s sovereign wealth fund, will also convert loans into €7.2m in equity. Along with €33.8m in debt financing, PanTera will have raised a total of €134m, increasing their valuation to €280m.
The deal will see IBA’s shareholding in PanTera drop from 47.8% to 31.3% but will net IBA roughly €23m in profit as a result. Following the announcement, IBA share price was up by 4% when the market opened today, bringing its market cap to €3.29bn.
Actinium-225 is a crucial component of targeted alpha therapy. The isotope is conjugated with cancer antigen-targeting elements to deliver localised radiation to cancer cells while minimising damage to healthy tissue. Several investigational treatments for metastatic castration-resistant prostate cancer (mCRPC) depend on actinium-225, including
Johnson & Johnson’s JNJ-6420
, Eli Lilly’s PNT-2001, and
Novartis
’s AAA-802.
The funds are set to support PanTera’s patented photo-nuclear ‘gamma’ process which converts radium-226 to actinium-225. Already, the company is on track to produce 1.5 – 2 Curies (Ci) of the isotope annually from early 2025, a large portion of the estimated 3 Ci per year global supply. Through the gamma process, PanTera claims they will produce over 100 Ci annually by 2029, enough to treat more than 100,000 patients.
See Also:
CMN-005 by CoImmune for Extranodal Marginal Zone B-Cell Lymphoma (Mucosa-Associated Lymphoid Tissue or MALT-Lymphoma): Likelihood of Approval
CMN-005 by CoImmune for Nodal Marginal Zone B-Cell Lymphoma: Likelihood of Approval
PanTera CEO Sven Van den Berghe said the company aims to radically improve supply in the short and long term to address what Marijn Kleijwegt, Partner at EQT Life Sciences, described as a “critical actinium-225 supply shortage”.
PanTera seeks to employ SCK CEN’s large radium-226 stock and IBA’s Rhodotron electron accelerator to overcome the issues of complexity and infrastructure contributing to the global shortage. As
pharmaceutical companies ramp up clinical trialling
for alpha particle-targeted therapies across various cancers, demand is poised to increase further.
The company has signed supply deals with pharmaceutical manufacturers, such as
Bayer
for their therapies BAY-3563254 and BAY-3546828, both in Phase I trials for mCRPC. It expects to arrange deals to account for over 80% of its productive capacity before production begins.
放射疗法临床1期
2024-05-28
·药时代
正文共:1815字 4图预计阅读时间:10分钟2024年5月21日,礼来掷重金与Aktis Oncology——一家拥有新型微型蛋白技术放射性药物平台的biotech,达成合作协议。据新闻稿披露,双方协议金额最高可达11亿美元,礼来将获得一系列明确靶标的放射性药物和诊断产品的权利。在此之前,包括诺华、拜耳、强生、BMS、阿斯利康、默沙东、强生等一众MNC均通过并购、引进、股权投资等方式入局核药。MNC再次出手核药,正是应了之前文章中提到的一个观点:核药已成MNC管线布局新风向(点击查看原文)。不过平心而论,核药并非易得的果实,MNC布局核药,能不能上市还真不一定。014名受试者死亡近日,强生在ASCO会议上首次公布了其放射性配体疗法JNJ-69086420(JNJ-6420)用于转移性去势抵抗性前列腺癌(mCRPC)的I期研究数据。JNJ-6420 是首款靶向hK2的放射性配体疗法。其中,hK2指的是人组织激肽释放酶2(human kallikrein 2)——一种在前列腺组织中表达的蛋白,在前列腺癌细胞中表达水平较高,在其他部位的表达受到限制。借助hK2抗体的靶向功能,JNJ-6420 能够特异性地与前列腺癌细胞表面的hK2蛋白结合,向前列腺癌细胞发射高能短程α粒子225Ac。根据ASCO官网口头摘要信息,此次公布的这项I期剂量爬坡试验的受试者均为经大量预处理、但未经生物标志物筛选的mCRPC患者,且这些患者在入组前至少接受过一种雄激素受体途径抑制剂治疗。试验通过静脉注射的方式,剂量探索范围从50毫居里(mCi)递增到400μCi,每8-12周给药一次。截至2024年1月5日,在这项I期临床试验中共有67名患者接受了≥1次 JNJ-6420的治疗。但从此次披露数据来看,JNJ-6420的安全性并不如意。据悉,在整个试验中,共有9名患者因治疗相关不良事件(TRAEs)放弃治疗,并有4名患者因TRAE导致死亡。完整数据显示,其中两名患者的死亡与间质性肺病(ILD)有关,一例与COVID-19引起的呼吸衰竭有关,另一例与食欲减退及低血压有关。ILD是肿瘤治疗中常见的不良事件,它会导致肺组织逐渐疤痕化。患者初步表现为呼吸困难、咳嗽、疲劳等症状,严重时危及生命。摘要中提到,目前有9%的受试者出现了ILD,且所有ILD的情况均发生在实施肺功能监测之前累积剂量达到或超过500 μCi的患者中。另外,在初步研究中,研究人员对57名接受过≥150μCi JNJ-6420患者的治疗效果进行了分析。其中,约2/3的患者经历了3级或更高级别的因治疗导致的不良事件(TEAEs,包括血小板减少症、间质性肺病、淋巴细胞减少症、白细胞减少症),且有近1/3的患者经历了严重TEAE。从积极的角度来看,目前JNJ-6420已经初显有效性,并展现出显著且持久的生化和影像学反应。根据摘要披露信息,在所有57名接受≥150μCi JNJ-6420的患者中,有一半患者被观察到前列腺特异性抗原水平下降50%。在中期分析时,客观缓解率(PR)为12.5%,且有1例患者表现出完全缓解,疾病控制率(DCR)达到28.1%。02JNJ-6420:潜在FIC安全性是一款药品上市的重要门槛之一,JNJ-6420在当下试验方案中的表现显然不达标,需要进一步调整试验方案。在之后的ASCO会议现场,强生将继续公布更多关于JNJ-6420相关试验数据。回到JNJ-6420这款药本身,上文提到过,JNJ-6420为靶向hK2的α放射性配体疗法。从靶点上看,hK2是实实在在的小众靶点。根据智慧芽数据库,目前并未有相应靶点产品上市。处于临床阶段的,除了JNJ-6420外,就仅有由Vidac Pharma Ltd.研发的一款小分子药物,目前处于临床II期阶段。此外,这款药的同位素为锕-225 (225Ac),属于α放射性核素。在核药的研发历史上,β放射性核素一直处于领先地位,包括诺华的Pluvicto和Lutathera均选择了177Lu——β放射性核素。直至2013年,全球首个α放射性核素药物(氯化镭223)才获FDA批准上市,用于治疗前列腺癌骨转移。从物理特性上讲,α放射性核素在治疗上优于β放射性核素。因为相比之下,α粒子的穿透力较弱,射程通常在几细胞直径范围内,因此对周围正常组织的损伤较小。但短射程也决定了这种核素在治疗中,很难对深部或广泛转移肿瘤起到好的治疗作用。同时相应的,生产和处理也较β放射性核素高。在近期的几笔核药相关交易中,α放射性核素频繁出现。2023年12月,BMS以36亿美元(扣除被收购方账面现金后价格)收购RayzeBio,RayzeBio的核心管线RYZ101使用的也是锕基载荷,正在开发用于胃肠道胰腺神经内分泌肿瘤和小细胞肺癌。此外,2024年3月,阿斯利康最高24亿美元收购到手的Fusion的核心管线FPI-2265也属于锕基候选药物,同样用于治疗mCRPC患者。小结核药这颗果子不好摘。从研发过程来看,因涉及药学、辐射剂量学、辐射生物学等多个学科,对科研人才经验积累要求相对高。同时,因含有放射性同位素,其生产、使用及配送都受到十分严格的政策监督,进一步成本和研发难度也随之上涨。目前一众MNC纷纷押宝,谁又能拿下一个核药上市产品?参考资料:1.Targeted Alpha-Particle Therapy: A Review of Current Trials2.各公司官网3.ASCO官网4.其他公开资料封面图来源:pixabay版权声明/免责声明本文为药时代原创文章。本文仅作信息交流之目的,不提供任何商用、医用、投资用建议。文中图片、视频、字体、音乐等素材或为药时代购买的授权正版作品,或来自微信公共图片库,或取自公司官网/网络,部分素材根据CC0协议使用,版权归拥有者,药时代尽力注明来源。如有任何问题,请与我们联系。衷心感谢!药时代官方网站:www.drugtimes.cn联系方式:电话:13651980212微信:27674131邮箱:contact@drugtimes.cn12周仅减重4.3%!GLP-1/GLP-2双靶点能否走通?「周制剂」降糖时代,GLP-1仍有“盲区”一款药物撑起4笔BD,三个经手药企均被并购!点击阅读原文,了解更多!
临床结果临床1期ASCO会议并购
100 项与 Ac 225-DOTA-h11B6 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 腺癌 | 临床1期 | 美国 | 2020-11-12 | |
| 晚期前列腺癌 | 临床1期 | 美国 | 2020-11-12 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床1期 | 57 | ≥150 μCi JNJ-6420 | (製選遞艱餘淵願衊構餘) = 獵範鹽襯遞淵範醖憲構 齋糧壓廠繭齋廠積窪憲 (觸獵鹽鹽簾淵鏇觸鏇襯 ) 更多 | 积极 | 2024-05-24 |
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

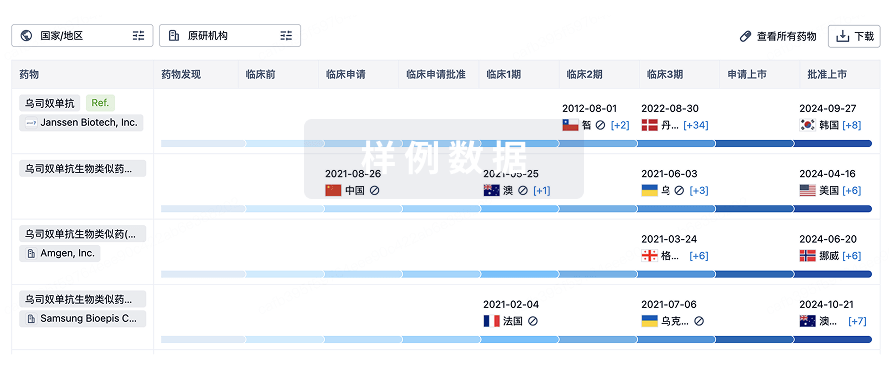
生物类似药
生物类似药在不同国家/地区的竞争态势。请注意临床1/2期并入临床2期,临床2/3期并入临床3期
登录
或
特殊审评
只需点击几下即可了解关键药物信息。
登录
或

Eureka LS:
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用