更新于:2024-09-28
SYH-2055
更新于:2024-09-28
概要
基本信息
关联
100 项与 SYH-2055 相关的临床结果
登录后查看更多信息
100 项与 SYH-2055 相关的转化医学
登录后查看更多信息
100 项与 SYH-2055 相关的专利(医药)
登录后查看更多信息
8
项与 SYH-2055 相关的新闻(医药)2024-07-23
·药通社
仿制药要如何突破内卷重围?改良型新药要如何抓住风口时机?立项是企业统领全局的关键步骤,是企业打造竞争力的第一步。清晰科学的立项战略不仅能让企业在市场拼杀中发挥最强战斗力,而且能帮企业节约成本与资源。基于此,2024年8月15-16日,2024 CMC博览会同期举办仿制药和改良新药立项“稳准狠”论坛,邀请行业专家,凝聚智慧、出谋划策,一同规划仿制药和改良新药未来!
一键报名 · 见证合作!
距离2022年底的新冠疫情全国大爆发已经过去一年半,此时政府在为经济复苏绞尽脑汁,老百姓在为生活忙碌奔波时,身边虽偶有亲朋好友“羊”了,但症状较之前轻了许多,慢慢的大家已忽视新冠病毒的存在。
从中国疾控预防控制中心2024年7月10日发布的最新全国新型冠状病毒感染疫情情况看,其实新型冠状病毒SARS-CoV-2从未离开过我们。
这一年多来,流感和新冠此起彼伏,老百姓纷纷囤积奥司他韦和玛巴洛沙韦于家中常备,而屯新冠药的却在少数。
目前国内已批准的小分子新冠药物主要是“2+5”,即辉瑞进口的奈玛特韦片/利托那韦片组合包装和默沙东进口的莫诺拉韦胶囊,国产新势力有河南真实生物科技有限公司阿兹夫定片、先声药业的先诺特韦片/利托那韦片组合包装、君实生物的氢溴酸氘瑞米德韦片、广东众生睿创的来瑞特韦片和广生堂的阿泰特韦片/利托那韦片组合包装。除了先声药业已转常规批准,其他均是附条件批准。此次不讨论那些治疗新冠中国特色的中药注射剂和中药汤剂。
辉瑞和默沙东早已赚的盆满钵满,辉瑞2023年报披露Paxlovid全球销售 12.79 亿美元,默沙东2023年报披露莫诺拉韦胶囊全球销售 14.28 亿美元,国内四小强也是勉强抓住了新冠大爆发的尾巴完成了三期临床试验,真正商业化时,新冠流行病显著下降,可谓时运不济,先声研发不低于5亿,广东众生研发不低于6亿元,君实研发不低于8.8亿,广生堂研发不低于3.5亿,数亿的投入相信离回本还要看天吃饭。目前的销量先声>君实>众生>广生堂,阿兹夫定主要是在2022年上述药物均未获批时踩上了红利。
也因为新冠疫情已趋于局部流感化,多数企业纷纷终止了新冠药物的研发,包括疫苗、抗体和小分子药物,但仍有一批企业仍默默前行,实属不易!
其实在新冠疫情的那些年,很多企业都立项或者引进过新冠项目,比如石药的SYH2055、翰森的HS-10517、中国生物制药的TDI01、歌礼的ASC10、前沿生物的FB2001、英矽智能的ISM3312、远大医药的GS221和STC3141,远大医药甚至还披露:在持续研发第二代小分子3CLpro抑制剂,在研产品有望实现对 COVID-19 患者的轻、中、重症治疗的全覆盖。
笔者研究了远大医药披露信息的措辞后发现,GS221和STC3141对新冠有疗效的趋势;不出意外,远大医药已在去年的年报里找不到新冠项目的身影。但笔者却在CDE登记平台发现一个陌生的名字:富马酸恩昔特韦片正在做生物等效性试验,原来是远大医药改变策略,与其投入数亿元去研发新药,不如直接做个BE来的快,但比较的激进的是选择了日本上市的盐野义品种。
富马酸恩昔特韦片目前未纳入参比制剂目录,无中国患者数据,甚至当年CDE都未批准盐野义附条件进口,这样的情况下去仿制是不是太冒险?BE总结报告版本日期是2024-06-18,理论上近期应该会申报,敬请期待!
其实仿制进口新冠药的不仅仅是远大,早在2022年,当时原研默沙东的莫诺拉韦胶囊还没有批准附条件进口,安徽贝克已经于2022年8月完成莫诺拉韦胶囊生物等效性试验,按照化药3类申请注册了,2023年中披露的信息显示:“目前该项目处于国家药审中心审评阶段,具体为“特别审批”窗口待受理状态”,2023年底终止IPO至今再无该项目的信息,笔者分析:首先原研仅为附条件批准进口,尚未转为常规批准,附条件批准上市的药品尚未满足常规注册要求,安全性和有效性数据尚不充分。
2023年底广生堂的阿泰特韦片/利托那韦片组合包装都是附条件批准,那时的新冠阳性率还不及现在,笔者猜测CDE目前仍认为新冠药是公共卫生事件急需用药,及时是仿制药也会优先批准,所以认为安徽贝克莫诺拉韦仿制药批准的可能性已不大。
当下立项难困扰很多企业,各自都在寻求差异化,有转型改良新药,有转型高端制剂,有转型上下游一体化,有转型细分(儿童、透皮、眼科)领域,有转型非药品(医美兽药)赛道,有坚定走集采的,有转型出海的,大家各显神通,都能杀出一条血路。
而以上莫诺拉韦和恩昔特韦两个品种无中国人群数据,专利情况尚不明朗,加上新冠病毒亚型仍在不断变异,即使可能亚洲人和白人没有明显的种族差异,冒然做BE,还是值得商榷的!
仿制药立项思路和产品布局如今有何变化?仿制药要如何突破内卷重围?改良型新药要如何抓住风口时机?
2024年8月15-16日,2024 CMC博览会同期举办仿制药和改良新药立项“稳准狠”论坛,邀请行业专家,凝聚智慧、出谋划策,一同规划仿制药和改良新药未来!
一键报名 · 见证合作!
08/15 AM
入门篇—B证企业法规政策
▷9:30-10:10
从仿制走向改良:在细分领域挖掘机会王立峰慧药咨询创始人
▷10:10-10:50
缓释制剂的改良立项及临床开发策略夏燕
百花村医药集团轮值总经理,礼华生物董事长
▷10:50-11:30
基于临床需求的改良型新药立项策略与实施案例吴涛
北京汇诚瑞祥医药生物科技有限公司 首席科学家
▷11:30-12:10
成功上市的505(b)(2)案例对改良新药立项启示陈洪 外专局特聘专家
08/15 PM
▷14:00-14:40
以透皮给药技术平台为导向的产品立项及案例分享孙亚洲长沙晶易医药科技股份有限公司联合创始人、董事、高级工程师、NMPA高级研修学院特聘讲师
▷14:40-15:20
以渗透泵技术平台为导向的产品立项及案例分享石劲敏汉都医药副总经理
▷15:20-16:00
以眼部给药技术平台为导向的产品立项及案例分享
▷16:00-16:40
以儿科药物掩味技术平台为导向的产品立项及案例分享
08/16 AM
▷9:30-10:20
独一无二——以特色、差异化布局选品思路
郭新峰
南京循证生物科技有限公司创始人
▷10:20-11:30
成本优势——以集采品种选品思路张廷杰
风云药谈 创始人
▷11:30-12:10
技术领先—高技术壁垒改良型新药立项及成功案例分享
魏世峰
北京罗诺强施医药技术研发中心有限公司董事长兼CEO
08/16 PM
▷13:30-14:30
产品为王—高度内卷之下,仿制药的立项思路与产品布局
魏利军
北京药眼信息咨询有限公司创始人兼CEO
▷14:30-15:00
顺势而为——以市场消费趋势为导向选品
立即扫码报名
推荐阅读
临床3期疫苗
2023-02-15
在开年来的第一个月内,已经有5款新药在国内成功获批,分别是武田制药的琥珀酸莫博赛替尼胶囊(安卫力®)、诺华制药的琥珀酸瑞波西利片(凯丽隆®)、旺实生物的氢溴酸氘瑞米德韦片(民得维®)、先声药业的先诺特韦片/利托那韦片组合包装(先诺欣®)和百时美施贵宝的盐酸奥扎莫德胶囊(热珀西亚®)。注:由于艾迪药业的艾诺米替片批文发证日期为2022年12月30日,故不纳入统计。来源:药渡数据库国内首款肺癌EGFR 20ins靶向药 琥珀酸莫博赛替尼胶囊 2023年1月11日,NMPA官网最新公告显示,武田(Takeda)申报的1类新药琥珀酸莫博赛替尼胶囊(Mobocertinib)已通过NMPA的优先审评程序附条件获批上市,用于含铂化疗期间或之后进展且携带表皮生长因子受体(EGFR)20号外显子插入突变的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。这是国内首款用于EGFR Exon20插入突变NSCLC的新药,对国内肺癌患者具有重大的意义。莫博赛替尼是一种Ariad和武田合作开发的新一代强效口服小分子酪氨酸激酶(TKIs)抑制剂,被专门设计用于选择性靶向EGFR外显子20插入突变。2021年9月15日,Mobocertinib获FDA加速批准上市,商品名EXKIVITY®,用于治疗含铂化疗期间或之后疾病进展的伴表皮生长因子受体(EGFR)外显子20插入突变的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者,这也是全球首个也是唯一获批的针对EGFR外显子20插入突变的药物。莫博赛替尼的获批主要基于1/2期研究(NCT02716116)结果,临床数据显示,莫博赛替尼160mg QD治疗114例铂类化疗经治患者(PPP队列,包括6例剂量递增队列+22例剂量扩展队列1+86例EXCLAIM队列患者),独立审查委员会(IRC)确认的ORR为28%,研究者确认的ORR为35%。并且,无论插入突变发生在近环(near-loop)或远环(far-loop),ORR都相似,分别为29%和25%。莫博赛替尼起效迅速且疗效持久,中位起效时间为1.9个月,中位缓解持续时间(DoR)为17.5个月。中位OS为24个月,中位无进展生存期(PFS)为7.3个月。来源:药渡数据库目前全球有多家企业布局EGFR 20号外显子插入突变抑制剂,国内布局EGFR 20号外显子插入突变抑制剂的企业也有多家。其中,进展最快的是迪哲医药的舒沃替尼(DZD9008),迪哲医药已经向CDE提交NDA并已于2023年1月10日获CDE正式受理,根据公布的临床试验数据,可看出该药具有非常优秀的市场潜力(数据来自中国注册临床研究:WU-KONG6);其次进展较快的是大鹏/再鼎医药的CLN-081、君境生物的AP-L1898,目前最高研发状态为临床2期;福沃药业的FWD1509和壹典医药的HTMC-0503处于1期临床阶段。来源:药渡数据库国内首个晚期一线绝经前乳腺癌疗法 琥珀酸瑞波西利片 2023年1月19日,诺华发布消息,其乳腺癌治疗产品凯丽隆® (琥珀酸瑞波西利片)获中国国家药品监督管理局批准,与芳香化酶抑制剂联合用药,作为激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性局部晚期或转移性乳腺癌绝经前或围绝经期女性患者的初始内分泌治疗,使用内分泌疗法治疗时应联用黄体生成素释放激素(LHRH)激动剂。信息显示,这是目前国内唯一获批晚期一线绝经前适应症的CDK4/6抑制剂。据世界卫生组织国际癌症研究机构发布的2020年全球最新癌症数据,全球乳腺癌新发病例高达226万例,已取代肺癌成为全球第一大癌种。在中国,乳腺癌是女性常见的恶性肿瘤之一,发病率位居女性恶性肿瘤之首。而这个群体中,有约70%的患者为激素受体阳性(HR+)、人表皮生长因子受体2阴性(HER2-)乳腺癌。疾病的复杂性给这类晚期乳腺癌治疗带来了巨大挑战,亟需创新的治疗方式。内分泌治疗是HR+/HER2-晚期乳腺癌经典的系统性治疗手段,然而,仍然有患者难免会出现原发或继发耐药,使得内分泌治疗疗效大打折扣。随着内分泌治疗联合分子靶向治疗的开展,CDK4/6抑制剂越来越成为其中的“重头戏”。瑞波西利分子结构式瑞波西利是拥有非常大规模临床试验证据的CDK4/6抑制剂。MONALEESA全球研究包括诺华申报的三项试验,其中MONALEESA-7研究结果提示,与内分泌治疗相比,瑞波西利内分泌治疗作为绝经前HR+/HER2-晚期乳腺癌(ABC)患者的初始治疗,无进展生存期(PFS)和总生存期(OS)具有统计学的显著获益。尽管MONALEESA-7研究显示亚洲患者OS获益(HR 0.609)ITT人群一致,但仍缺乏针对中国绝经前HR+/HER2- ABC患者的循证医学证据。为此,该药在中国大陆开展了一项瑞波西利的多中心2期桥接研究。在这项桥接研究中,有156例初始治疗的绝经前HR+/HER2- ABC患者被纳入绝经前队列,随机(1:1)接受瑞波西利或安慰剂+NSAI+OFS(戈舍瑞林),研究结果显示达到了主要终点:瑞波西利组的PFS相较于安慰剂组延长了12.9个月(27.6 vs 14.7个月),疾病进展或死亡风险降低32.8%(HR 0.672,95%CI:0.448~1.009)。在次要终点方面,瑞波西利组的ORR相较于安慰剂组提高了15.1%(53.6% vs 38.5%),OS尚未成熟。在安全性方面,该桥接研究中瑞波西利的总体安全性与已知的安全性特征大致相似,并与全球研究(MONALEESA-7)基本一致,没有发生新的不良事件。截止目前,国内已上市5款CDK4/6抑制剂新药,除去诺华的瑞波西利,其他4款分别为2018年7月批准的辉瑞“哌柏西利”,2020年12月批准的礼来“阿贝西利”,2021年12月批准的恒瑞医药“达尔西利”和2022年7月批准的先声药业从G1 Therapeutics引进的“曲拉西利”。国内还有数十款CDK4/6抑制剂在临床研究阶段,除了创新药间的竞争外,仿制药的入局或将给CDK4/6赛道带来巨大的变数。哌柏西利的专利将于2023年到期,齐鲁制药的哌柏西利首仿已于2020年12月获批上市,目前已有13个哌柏西利仿制批文获批。CDK4/6抑制剂赛道的仿制药VS创新药,创新药VS创新药的混战已经来袭。来源:NMPA官网头对头PAXLOVID,效果不输 氢溴酸氘瑞米德韦片 2023年1月28日,旺实生物(君实生物和旺山旺水的合资子公司)口服核苷类抗新冠病毒药物氢溴酸氘瑞米德韦片(商品名:民得维®,VV116)获得国家药品监督管理局(NMPA)批准上市,用于治疗轻中度新型冠状病毒感染的成年患者。瑞米德韦(VV116)是一款我国自主研发的口服核苷类抗病毒药物,可抑制SARS-CoV-2复制,原理是通过靶向RNA依赖的RNA聚合酶(RdRp)抑制病毒RNA合成,与瑞德西韦、阿兹夫定、莫诺拉韦同一靶点。VV116在研发过程中采用了氘代策略,设计灵感来自于瑞德西韦,VV116从瑞德西韦优化而来,保留了瑞德西韦的抗病毒活性,并能够口服给药。临床前的药代动力学等研究结果显示,VV116具有很高的口服生物利用度,口服吸收后水解为母体核苷(氘GS-441524)。VV116体内代谢为活性化合物的过程2022年12月29日,国际顶级医学期刊《新英格兰医学杂志》(The New England Journal of Medicine,NEJM,影响因子:176.079)在线发表了一项中国非劣效性3期随机对照临床试验(NCT05341609),其结果表明,对于有高危因素的轻中度Covid-19成人患者,在至持续临床康复时间方面,口服核苷类抗新冠病毒药物VV116非劣于奈玛特韦片/利托那韦片组合药物Paxlovid(4天 vs. 5天;风险比:1.17;95%置信区间:1.02~1.36),且不良事件更少。2023年2月3日,四川省医疗保障局正式公示上海旺实生物医药科技有限公司自主申报的氢溴酸氘瑞米德韦片(商品名:民得维®)首发报价,每疗程795元的新款国产新冠治疗药品有望快速进入中国市场。截止目前国内一共有5款新冠小分子口服药上市,分别是Paxlovid(奈玛特韦片/利托那韦片组合包装),阿兹夫定片,莫诺拉韦胶囊(商品名:利卓瑞®/LAGEVRIO®),氢溴酸氘瑞米德韦片(商品名:民得维®)和先诺特韦片/利托那韦片组合包装(商品名:先诺欣®)。国产新冠口服药物定价均大幅低于进口新冠口服药,同时疗效方面也有非常确切的证据,为我国抗击疫情提供了坚实后盾。首个国产3CL靶点新冠口服药 先诺特韦片/利托那韦片组合包装 2023年1月28日,由中国科学院上海药物研究所、中国科学院武汉病毒研究所联合先声药业合作研发的抗新冠病毒创新药先诺欣®获国家药品监督管理局通过特别审批程序,进行应急审评审批,附条件批准上市,用于治疗轻中度新型冠状病毒感染(COVID-19)成年患者。这是我国首款自主研发的靶向3CL蛋白酶的抗新冠病毒口服药物。先诺欣®是一款口服小分子抗新冠病毒创新药,是先诺特韦片与利托那韦片的组合包装药物,其中先诺特韦针对SARS-CoV-2病毒复制必须的3CL蛋白酶(和辉瑞Paxlovid同个靶点),与低剂量利托那韦联用有助于减缓先诺特韦在体内的代谢或分解,提高抗病毒效果。已完成的临床前研究显示,先诺欣®具有高活性、低毒性、依从性高等特性。 先诺欣®的获批主要基于注册性3期临床试验(NCT05506176),这是一项评估先诺欣®治疗轻中度COVID-19成年感染者的有效性和安全性多中心、随机、双盲、安慰剂对照的注册性临床研究,本项研究计划共招募1208名患者,2022年12月16日已完成全部患者入组。来源:药渡数据库研究结果证实,先诺欣®对中国轻至中度COVID-19成年患者安全有效,有显著的临床疗效。加快症状恢复,缩短病程:在1208例有症状的轻中度COVID-19成年患者中,相较安慰剂,先诺欣®显著缩短11种目标COVID-19症状首次达到持续恢复时间约1.5天,其中重症高风险亚组人群显著缩短约2.4天,同时临床数据提示尽早使用先诺欣®疗效更优。目前先诺欣的最新定价为750元/盒,价格远低于辉瑞的Paxlovid,非常具有性价比。当然先诺欣也具有与Paxlovid同样的局限性,多种药物相互作用造成使用受限的情况依然存在,需要非常注意合理用药。聚焦国产企业,3CL靶点赛道“人才济济”。首先,进展最快的莫过于先声药业的先诺欣®(SIM0417),目前最高研发状态为批准上市;其次前沿生物的FB-2001、众生生物的RAY-1216、广生堂药业的GST-HG171,均处于临床III期研究阶段;歌礼制药的ASC11、西湖大学的Mprosevir、石药集团的SYH-2055均处于I期临床研究阶段;此外,信立泰的SAL-0133已于去年12月提交IND。预计在2023年一年中,将会有至少3款国产3CL靶点药物获批,花落谁家,大家拭目以待。针对多发性硬化症的S1P受体调节剂 盐酸奥扎莫德胶囊 在2023年02月02日NMPA发布药品批准证明文件送达信息中,百时美施贵宝(BMS)的新药盐酸奥扎莫德胶囊(Ozanimod)在2023年1月31日获得中国国家药品监督管理局(NMPA)批准,用于治疗成人复发型多发性硬化,包括临床孤立综合征、复发-缓解型多发性硬化和活动性继发进展型多发性硬化。奥扎莫德是百时美施贵宝在中国自身免疫疾病领域首个获批的创新疗法。奥扎莫德是一款口服选择性S1P受体调节剂,最初由Receptos公司开发,后被BMS子公司新基以73亿美元收购引入。其通过选择性结合S1PR1和S1PR5,降低血液和淋巴循环中的淋巴细胞数目,减少中枢神经系统的炎症反应。2020年3月,奥扎莫德首次获批上市,商品名为Zeposia®,适应症为成人复发型多发性硬化症(RMS)。2021年5月27日,其获FDA批准用于治疗成人中重度溃疡性结肠炎。此次获批基于SUNBEAM(12个月)和RADIANCE(B部分,24个月)这两项大型阳性药物对照III期研究结果。研究共计纳入了2600多名患者,旨在评估奥扎莫德胶囊(口服,每日一次)对比Avonex®(重组人干扰素β-1a,肌肉注射,每周一次,下简称“干扰素β-1a”)在治疗成人复发型多发性硬化患者中的有效性和安全性。研究结果显示,与干扰素β-1a相比,奥扎莫德可带来显著临床获益。①年复发率(ARR)降低:与干扰素β-1a相比,持续接受奥扎莫德治疗12个月的患者,其ARR可降低48%;持续治疗24个月,ARR降低38%;②MRI病灶数减少:与干扰素β-1a相比,持续接受奥扎莫德治疗12个月的患者,其T1加权钆增强(GdE)病灶数减少63%,新发/扩大T2病灶数减少48%;持续治疗24个月,其T1加权钆增强(GdE)病灶数减少53%,新发/扩大T2病灶数减少42%;③脑容量丢失减少:与干扰素β-1a相比,接受奥扎莫德治疗12个月的患者,其全脑容量丢失减少31%,皮层灰质容量丢失减少84%,丘脑容量丢失减少32%;持续治疗24个月,其全脑容量丢失减少26%,皮层灰质容量丢失减少60%,丘脑容量丢失减少27%;④认知功能保护:在SUNBEAM研究中,接受奥扎莫德治疗12个月,35.6%患者的符号数字模式测试(SDMT)出现具有临床意义的改善(SDMT评分增加≥4分),高于干扰素β-1a治疗组患者(27.9%);在这两项研究中,奥扎莫德整体安全性和耐受性良好,最常见的不良事件(发生率≥4%)为上呼吸道感染、肝转氨酶升高、直立性低血压、尿路感染、背痛和高血压。目前全球获批上市的S1P受体调节剂共4款,除去BMS奥扎莫德,其余3款分别是罗氏/强生Ponesimod、诺华西尼莫德和芬戈莫德。国内仅辉瑞/云顶新耀Etrasimod进展较快,已进入3期临床,适应症为中重度活动性溃疡性结肠炎(UC)。Etrasimod由Arena Pharmaceuticals公司开发,辉瑞于今年早前完成了对Arena Pharmaceuticals的收购,而云顶新耀于2017年从Arena获得了在大中华区和韩国开发、生产和商业化Etrasimod的独家权利。Etrasimod已经在2022年12月提交了有关治疗中重度活动性溃疡性结肠炎的FDA上市申请,预计在今年大概率获批。往期推荐2023年,中国创新药将上演“狂飙”END👇关注药渡数据媒体矩阵
优先审批上市批准申请上市加速审批
2023-01-17
2023年1月16日,先声药业宣布,与中国科学院上海药物研究所、武汉病毒研究所联合开发的抗SARS-CoV-2候选药物先诺欣®(先诺特韦片/利托那韦片组合包装)NDA获NMPA以药品特别审批程序正式受理,拟用于治疗轻至中度新型冠状病毒感染(COVID-19)成年患者。来源:先声药业公告 关于先诺欣®先诺欣®是一款口服小分子抗新冠病毒创新药,是先诺特韦片与利托那韦片的组合包装药物,其中先诺特韦针对SARS-CoV-2病毒复制必须的3CL蛋白酶,与低剂量利托那韦联用有助于减缓先诺特韦在体内的代谢或分解,提高抗病毒效果。已完成的临床前研究显示,先诺欣®具有高活性、低毒性、依从性高等特性。 2022年3月28日先诺欣®获NMPA批准临床,这是先诺欣®获得的第一项药物临床试验批准通知书,用于轻至中度且伴有进展为重症(包括住院或死亡)高风险因素的新型冠状病毒肺炎患者。2022年5月13日先诺欣®获NMPA批准临床,拟用于曾暴露于新冠检测阳性感染者的密接人群的暴露后预防治疗。2022年7月23日先诺欣®用于COVID-19成年感染者的Ib期临床试验在深圳市第三人民医院完成全部受试者给药及观察。初步数据显示,先诺欣®展现出对病毒载量、转阴时间和新冠相关症状消失均有积极作用。2023年1月16日先诺欣®(先诺特韦片/利托那韦片组合包装)NDA获NMPA以药品特别审批程序正式受理,拟用于治疗轻至中度新型冠状病毒感染(COVID-19)成年患者。2021年11月17日先声药业与中国科学院上海药物研究所、武汉病毒研究所订立技术转让合同,根据协议内容,先声药业获得先诺特韦在全球开发、生产及商业化的独家权利。2022年4月10日先诺欣®在健康成年受试者中单词/多次给药后的安全性、耐受性及药代动力学I期临床试验在山东省千佛山亿元达成FPI;2022年6月1日,该研究完成全部受试者入组及院内观察。2022年6月13日先诺欣®治疗COVID-19的II期临床试验在上海复旦大学附属中山医院达成FPI。2022年12月19日先诺欣®注册性III期临床试验完成全部患者入组。研发进展临床前动物试验在临床前动物试验中,先诺欣®显示出良好的安全性、体内药代动力学特性和高效、广谱的抗新冠病毒活性,未发现遗传学毒性。安全药理、14天重复给药毒性(GLP)毒理和遗传毒性均未发现任何药物毒性反应。肺组织暴露高,具有更低的人血浆蛋白结合率。对多种新冠病毒变异株,包括野生型、德尔塔、奥密克戎均表现出良好的抗病毒活性,能抑制肺部、脑组织中病毒复制,保护由病毒感染引起的组织损伤。根据药渡数据调研,目前先诺欣®正在国内进行注册性III期临床研究。来源:药渡数据库注册性III期临床试验(NCT05506176)这是一项评估先诺欣®治疗轻中度COVID-19成年感染者的有效性和安全性多中心、随机、双盲、安慰剂对照的注册性临床研究,本项研究计划共招募1208名患者,2022年12月16日已完成全部患者入组。来源:药渡数据库此项临床研究由中国医学科学院、国家呼吸医学中心王辰院士、中日友好医院曹彬教授牵头,复旦大学附属中山医院樊嘉院士、复旦大学附属中山医院感染病科主任胡必杰教授共同指导完成,是第一个针对中国人群感染奥密克戎毒株的大样本临床试验,也是国内外第一个针对奥密克戎毒株感染者达成“以咳嗽、鼻塞流涕、咽痛、发热、头痛、肌肉或全身痛等11个症状持续恢复”为主要终点的III期注册临床研究。本项注册临床研究共纳入全国20个省市自治区43家临床参研中心,在深圳第三人民医院院长卢洪洲教授、武汉金银潭医院院长黄朝林教授等多位临床专家的大力支持下,快速而高质量完成了全部1208例患者临床试验。先声药业表示,关于本项注册临床研究有效性、安全性的详细数据将在产品批准上市后公布或公开发表。3CLpro靶点药物研究进展3CL蛋白酶负责新冠病毒在宿主细胞繁殖过程中“拆装重组”多聚蛋白(对病毒生产、繁殖非常重要的结构蛋白),因此,3CL蛋白酶又被称为主蛋白酶。3CL蛋白酶抑制剂可以抑制3CL蛋白酶的活性,从而干扰病毒复制过程,达到抗病毒的效果。3CLpro作为“病毒生命咽喉”,成为新冠防治多种环节中重要的一环。根据药渡数据调研,目前国内外约有45家企业在3CLpro赛道布局。其中,辉瑞的Paxlovid、盐野义的Ensitrelvir已经分别于2021、2022年获批上市。另外,国外企业仍有多款3CLpro抑制剂处于临床或临床前研究阶段。来源:药渡数据库聚焦国内,3CLpro抑制剂赛道“人才济济”。首先,进展最快的莫过于先声药业的先诺欣®(SIM0417),目前最高研发状态为申请上市;其次前沿生物的FB-2001、众生生物的RAY-1216、广生堂药业的GST-HG171,均处于临床III期研究阶段;歌礼制药的ASC11、西湖大学的Mprosevir、石药集团的SYH-2055均处于I期临床研究阶段;此外,信立泰的SAL-0133已于去年12月提交IND。FB-2001前沿生物的福布特韦(FB2001)是前沿生物与中国科学院上海药物研究所、中国科学院武汉病毒研究所合作开发的一款抗新冠病毒小分子3CL蛋白酶抑制剂。它有两种剂型,分别为注射用和雾化吸入用,前者拟治疗新冠病毒感染住院患者,后者则针对轻型、普通型新冠病毒感染患者,当前均已在开展II/III期临床试验。RAY-1216众生药业的RAY1216是众生药业自主开发的一款口服3CL蛋白酶抑制剂。RAY1216在野生株、阿尔法、贝塔、德尔塔、奥密克戎等多种新冠病毒感染的细胞模型中,均可有效抑制新冠病毒复制,展现了广谱抗新冠病毒的能力。1月2日,众生药业宣布RAY1216用于新冠感染者轻型和普通型的III期临床研究已经按临床方案要求完成全部病例数入组。GST-HG171广生堂的新冠口服小分子创新药GST-HG171(泰阿特韦,泰中定),是由广生堂和药明康德合作开发的,属于高活性、高选择性的口服3CL蛋白酶抑制剂。1月9日,广生堂发布了泰阿特韦完成并获得研究者发起的临床研究(IIT)总结报告。结果显示新冠患者核酸转阴时间明显优于阳性对照Paxlovid及安慰剂对照,同时安全性和耐受性良好。ASC11ASC11是歌礼利用包括分子模拟对接在内的多种专有技术自主研发的口服小分子候选药物,作用靶点为蛋白酶(3CLpro)。与同靶点的口服蛋白酶抑制剂Nirmatrelvir相比,ASC11有新的和差异化的化学结构。在新冠病毒感染的抗病毒细胞实验中,与奈玛特韦、S-217622、PBI-0451和EDP-235等其它3CLpro抑制剂相比,ASC11显示出更高的抗新冠病毒活性。ASC11对多种广泛传播的奥密克戎变异株如BA.1和BA.5均保持强效抗病毒活性。在新冠病毒感染动物模型中,ASC11同样表现出强效抗病毒活性。MprosevirMprosevir是西湖大学团队研发的SARS-CoV-2 3CLpro小分子非共价抑制剂。与辉瑞Nirmatrelvir的作用机理不同,艾普司韦与盐野义的Ensitrelvir(S-217622)作用机理相同,都是通过与3CLpro的活性口袋进行非共价结合继而抑制3CLpro活性。不同于以往的3CLpro抑制剂,艾普司韦具有全新的骨架结构。 SYH-2055SYH2055是石药集团开发的一款拥有全球自主知识产权的口服小分子抗新冠病毒3CL蛋白酶抑制剂。SYH2055通过作用于新冠病毒主蛋白酶(Mpro/3CLpro)抑制病毒前体蛋白的切割,进而阻断病毒复制并发挥抗新冠病毒的作用。临床前研究表明,SYH2055对包含Omicron BA.4、BA.5变异株在内的当前主流突变毒株均具有强效和广谱的抗病毒活性,在新冠真病毒感染的动物模型体内显著降低肺部病毒载量并明显改善肺部炎症,优于同剂量奈玛特韦。药代动力学性质上,SYH2055在大鼠和食蟹猴上较奈玛特韦的体内药代动力学性质明显改善,有望克服奈玛特韦必须与利托那韦联用的缺陷,将药物的适用人群扩展至因与利托那韦联用而无法覆盖的患者群体。基于3CL蛋白酶在不同属冠状病毒间高度保守,在人体内没有同源蛋白的特性,临床前安全性评价数据也充分证明了SYH2055的安全性。 从去年12月国家防疫政策调整至今,第一轮感染高峰已过,但考虑到不断变异的新冠毒株,重复感染将是必然。除了疫苗预防、药物防重症,药物减轻或缓解感染症状,在反复感染的背景下,也是重中之重。期待更多的新冠口服药物早日获批上市,为消除全球此起彼伏的疫情带来新的希望。参考来源先声药业官网、公告各公司官网「 往期文章 」P药无缘医保,M药上市开售,国内新冠口服药的博弈,才刚刚开始……A股疫苗板块年度盘点:仅1家逆势上涨,智飞生物跌掉半个“万泰生物”后疫情时代,仿转创“模范生”先声药业即将全面起势👇关注药渡数据媒体矩阵
申请上市临床3期
100 项与 SYH-2055 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 新型冠状病毒感染 | 临床3期 | 中国 | 2023-06-14 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
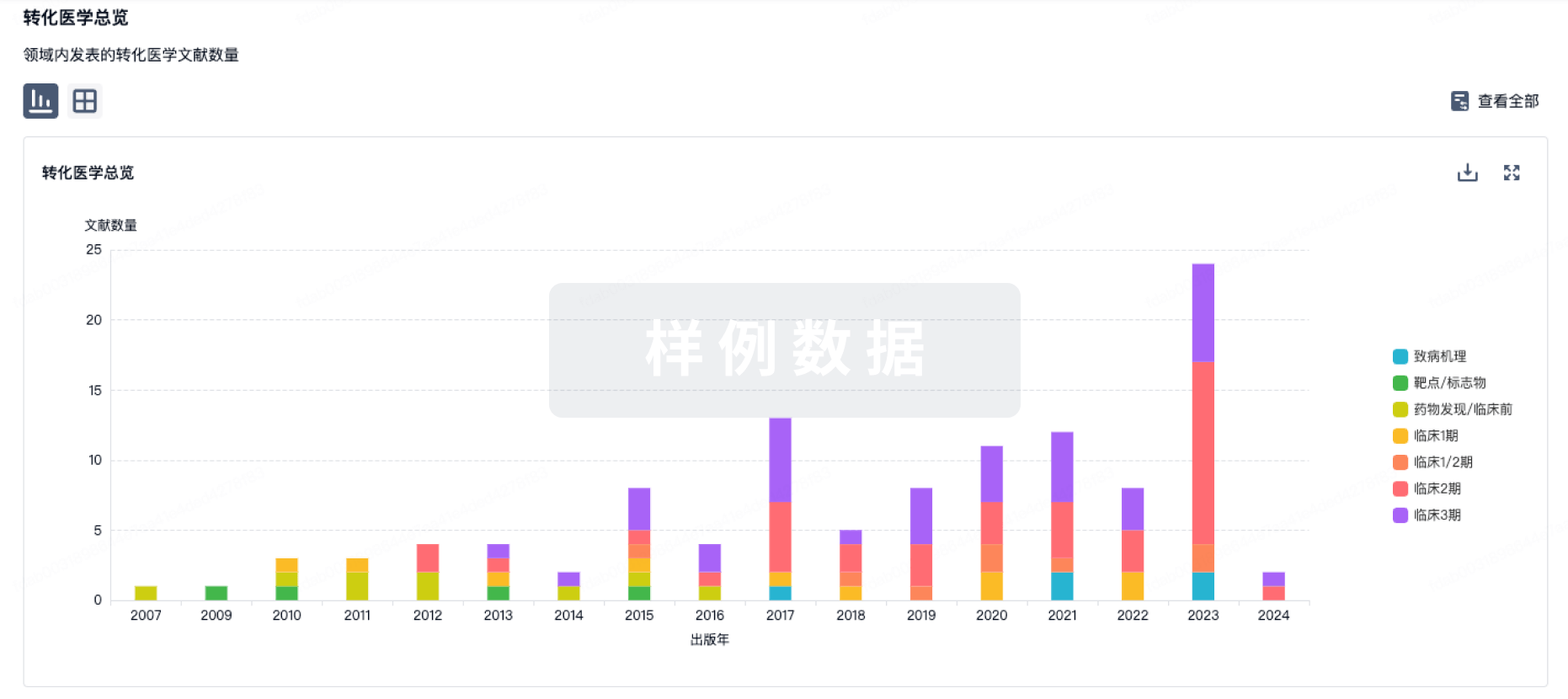
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
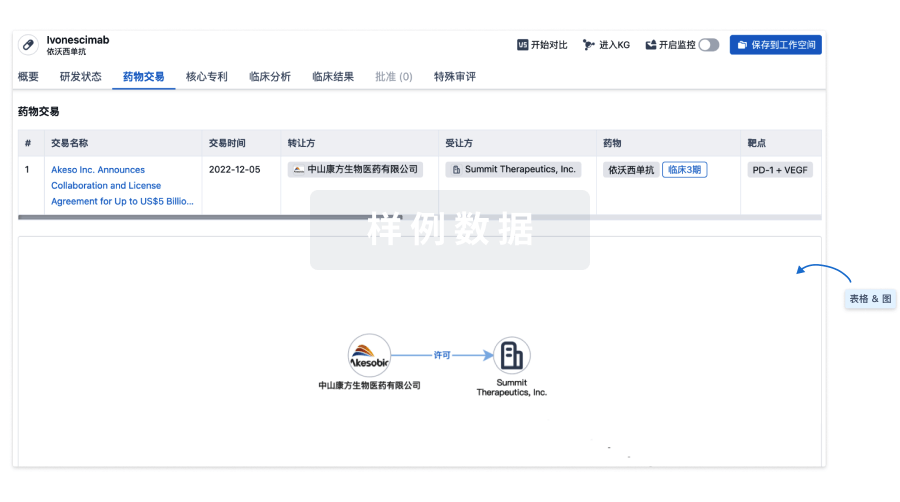
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
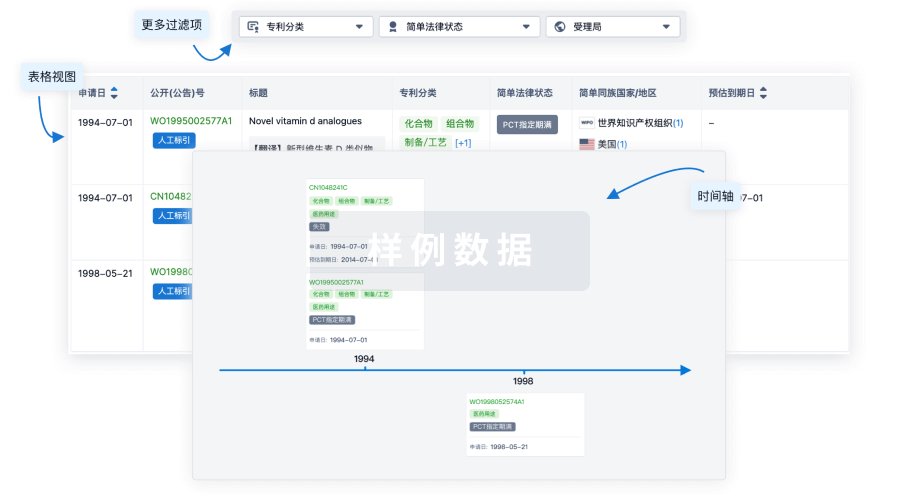
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
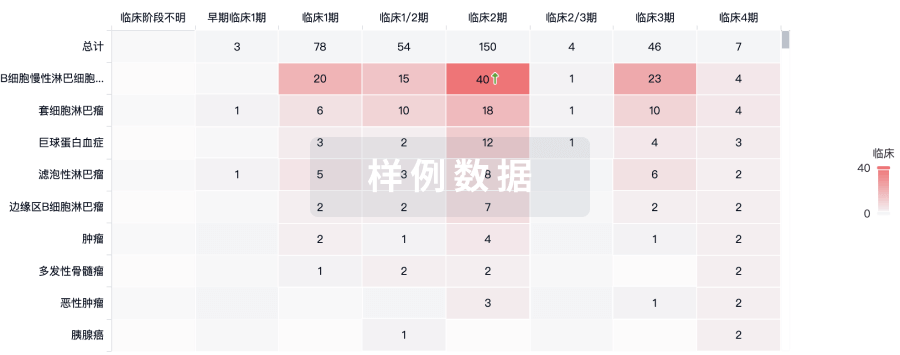
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
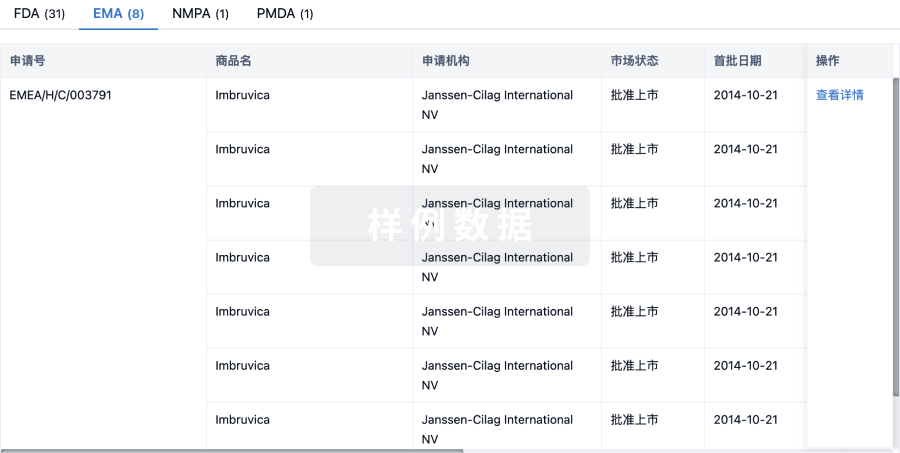
批准
利用最新的监管批准信息加速您的研究。
登录
或
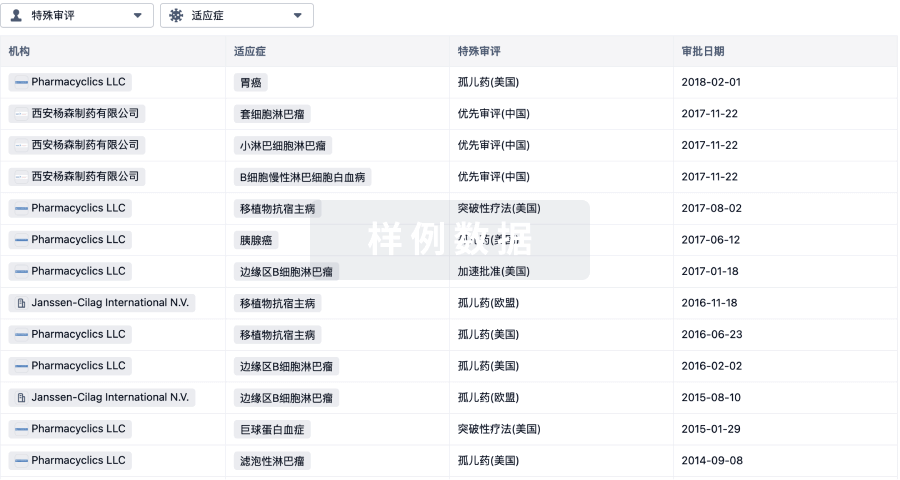
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用

