预约演示
更新于:2025-07-02
JNJ-80948543
更新于:2025-07-02
概要
基本信息
药物类型 三特异性T细胞接合器 |
别名 JNJ 80948543、JNJ 8543、JNJ-8543 + [2] |
作用方式 抑制剂、刺激剂 |
作用机制 CD20抑制剂(B淋巴细胞抗原CD20抑制剂)、CD3刺激剂(T细胞表面糖蛋白CD3复合体刺激剂)、CD79B抑制剂(B细胞抗原受体复合物相关蛋白β链抑制剂) |
在研适应症 |
非在研适应症- |
非在研机构- |
权益机构- |
最高研发阶段临床1期 |
首次获批日期- |
最高研发阶段(中国)临床1期 |
特殊审评- |
登录后查看时间轴
关联
4
项与 JNJ-80948543 相关的临床试验CTIS2024-514176-41-00
- 80948543LYM1002
开始日期2024-12-16 |
申办/合作机构- |
NCT06660563
A Phase 1b Study of JNJ-80948543 in Combination With Other CD3 T-Cell Engagers (TCEs) in Participants With Relapsed/Refractory B-Cell Non-Hodgkin Lymphoid (R/R B-Cell NHL) Malignancies
The purpose of this study is to determine the recommended phase 2 regimen (RP2R) for JNJ-80948543 in combination with JNJ-75348780 (Part 1: Dose Escalation) and to further assess the safety of JNJ-80948543 at the RP2R in combination with JNJ-75348780 (Part 2: Dose Expansion).
开始日期2024-10-22 |
NCT06139406
A Phase 1, First-in-human Study of JNJ-87801493 in Combination With CD3 T-Cell Engagers in Participants With Relapsed/Refractory B-cell Non-Hodgkin Lymphoid Malignancies (NHLs)
The purpose of this study is to characterize safety and to determine the recommended phase 2 regimen (RP2R) for JNJ-87801493 in combination with T-cell engagers (TCEs) [Part A: Dose Escalation] and to further assess the safety of JNJ-87801493 at the RP2R in combination with TCEs [Part B: Dose Expansion].
开始日期2023-12-06 |
100 项与 JNJ-80948543 相关的临床结果
登录后查看更多信息
100 项与 JNJ-80948543 相关的转化医学
登录后查看更多信息
100 项与 JNJ-80948543 相关的专利(医药)
登录后查看更多信息
15
项与 JNJ-80948543 相关的新闻(医药)2025-01-15
·抗体圈
1月13日,先声药业发布与艾伯维的BD交易公告,就其三抗资产SIM0500(早期代号:SCR-8572)达成deal,BD金额的首付款未披露,里程碑付款达到了10.55亿美元,业内人士预估,该交易的首付款的规模可能与恒瑞、信达DLL3 ADC相近,是一笔非常典型的早期交易。
该三抗靶向BCMA/GPRC5D/CD3三个靶点,CD3是用来链接T细胞的靶点,不必多说,BCMA和GPRC5D都是血液瘤疾病的经典靶点。目前三个靶点都相同的药物有强生的JNJ-79635322和信达的IBI-3003。
站在今天的视角来看,作为MNC的艾伯维,选择在先声双抗处于如今没有临床数据读出的阶段进行BD,是非常早期的超前布局,也体现了MNC在药物密集的大赛道领域技术更新迭代的日渐频繁。
站在今天的视角去看,三抗相对于双抗的优势有哪些,本次BD,又该如何看待SIM0500的初步数据?
01
从双抗到三抗
从双抗到三抗,首先进行的是结构上的改良。先从双抗开始说起,经典的双抗结构如图所示,中间的横线即为二硫键,两个臂其中一个是抗CD3臂,募集T细胞,另一个臂链接靶细胞,例如teclistamab,其另一个臂链接的就是抗BCMA臂。
从双抗到三抗,首先进行的是结构上的改良。先从双抗开始说起,经典的双抗结构如图所示,中间的横线即为二硫键,两个臂其中一个是抗CD3臂,募集T细胞,另一个臂链接靶细胞,例如teclistamab,其另一个臂链接的就是抗BCMA臂。
(图片来源:Bi- and trispecifc immune cell engagers for immunotherapy of hematological malignancies)
在经典双抗结构的基础上,一种前沿的改良探索是在抗体臂上进行改良,例如如图所示的EMB-06(与teclistamab同靶点),它的抗体臂是2+2的形式,一个抗体理论上可以结合两个T细胞和两个靶细胞,以此来加强抗体对两种抗原的的亲和力。
此外,还有下图的ABBV-383,它的差异化在于采用2+1的形式,抗CD3臂低亲和力,抗BCMA臂高亲和力,根据其结构的改良来看,如果将低亲和力的CD3替换成了高亲和力的抗CD3臂,一方面会降低双抗对靶细胞的杀伤能力,另一方面由于与T细胞的亲和力增强,导致其过度激活,引起炎症的比例将显著提高。此外,二价抗BCMA减少了可溶性BCMA的负面影响,从而减少了炎性细胞因子的产生,这也提高了其安全性。
(图片来源:https://doi-org.libproxy1.nus.edu.sg/10.1182/blood-2023-179039)
以上为同靶点双抗的几种经典形式,那么更进一步的三抗呢?三抗在双抗的基础上再增加了一个结合位点,那么这个位点有两条路可以选择:进一步链接T细胞,或者进一步链接靶细胞。前一种道路,比较典型的是CD28或4-1BB,当然,也可以链接抗PD-1臂增强免疫效应,典型的如下图所示的SAR442257,除了靶向CD3外,还多了个共刺激因子CD28的靶点。
后一种道路就是不同靶细胞靶点的自由组合了,主要是通过增强亲和力达到力大砖飞增强对靶细胞亲和力来清除靶细胞,并且有着削弱抗原逃逸的效用,以此来降低耐药性。如文首所述,光是BCMA×GPRC5D就有先声,强生和信达和天广实四家在做。如下图为强生JNJ-79635322的机制图解。
(图片来源:https://doi-org.libproxy1.nus.edu.sg/10.1182/blood-2023-174941)
先声的SIM-0500结构如下图所示,三个靶点各一个臂。从Kd值来看,与GPRC5D的亲和力大约为BCMA的将近两倍。
(图片来源:A novel T cell engager targeting BCMA and GPRC5D showed promising preclinical activity with low toxic risk for multiple myeloma treatment)
强生方面,从机制图解的图像披露看,其抗体结构类似于下图中强生的三抗JNJ-80948543,二硫键链接两个臂分别为抗CD3臂和抗BCMA臂,下方Fc链连接一个抗GPRC5D臂。
信达方面,目前没有看到对IBI3003具体结构的披露,从其专利书的披露来看,其设计的三抗结构与先声的SIM0500是大致类似的,也是不对称的抗体结构,CD3放在其中一条臂的中间位置。
(图片来源:专利书WO2022174813)
02
三抗疗效初窥
当然,目前与先声药业同靶点的三抗中,唯一披露数据的是天广实生物的MBS314。这里我们对比数据的话,先间接去对比:先声目前披露了临床前试验中SIM0500和强生的两款双抗:JNJ-7957和JNJ-7564的数据对比:JNJ7957(Teclistamab)靶向BCMA×CD3,JNJ7564靶向GPRC5DxCD3,目的也是为了在临床前试验中头对头比较三抗之于双抗是否有明显的迭代效应。
如图所示,对于经典的MM适应症细胞系:NCI-H929,RPMI8226和MOLP-8而言,SIM0500(图中红色曲线)都显示出了相较另外两条曲线更强的结合效应。
在NCIH929-hPBMC人源化异种移植小鼠模型的药效试验如图所示,图B进行的是剂量依赖性疗效评价:G5(红色曲线)即为SIM0500中等剂量的曲线,表现出了最强的抗肿瘤活性,达到近似疗效的是JNJ7564的高剂量组,但是肿瘤前期一直效果不如SIM0500明显。简而言之,SIM0500可以用更低的剂量达到与JNJ7564相等或者更好的效果。
图C更为直观,是在0.1mg/kg剂量下抗肿瘤的效果,同样直接观察红色曲线SIM0500,对肿瘤的抑制效应是最明显的。
之后再看强生这两款双抗的临床数据。
靶向BCMA×CD3的Teclistamab目前正在进行全球三期临床,已经获得FDA加速批准。其治疗复发或难治性MM的临床试验数据详见文献《Teclistamab in Relapsed or Refractory Multiple Myeloma》,临床人数为165人,样本不算小。baseline方面,此前患者的中位治疗线数为5,疗效方面,ORR达到了63.0%(104/165),CR达到了39.4%,
PFS和OS曲线如图所示,mPFS达到了11.3个月,mOS达到了18.3个月。
(图片来源:Teclistamab in Relapsed or Refractory Multiple Myeloma)
安全性方面,正如上文所述的对TCE双抗结构方面的叙述,Teclistamab属于最经典的双抗结构,对其CD3臂未做非常明显的改造或者遮蔽,所以不良反应看起来较高:三级或四级不良反应发生率达到了94.5%,最常发生的就是中性粒细胞减少(64.2%),其次是贫血(37%),未来先声的SIM0500针对Teclistamab安全性方面的迭代也是非常值得关注的方面。
然后再看天广实生物披露的MBS314数据:但数据非常早,样本不算大:4名患者接受治疗,中位治疗线数为3,第1和第2个剂量水平(0.03 mg和 0.09 mg)的两名患者分别达到病情稳定和部分缓解(PR)状态。未达到最大耐受剂量。
03
艾伯维的血液瘤布局
艾伯维在血液瘤方面并不缺少布局。
其近年来较为著名的BD是与Genmab关于Epcoritamab(CD20×CD3,主要适应症为弥漫性大B细胞瘤)的巨额BD:2020年的deal,BD总额达到了39亿美元(预付款便达到了7.5亿美元)。如图所示,其去年已经被FDA批准上市。其2024年上半年销售额已经达到了6300万美元,年峰值销售额为12亿美元,进入了重磅炸弹的门槛。
(图片来源:insight数据库)
当然,正如第一部分的图所示,Epcoritamab是最经典的双抗结构,两个对称的臂,这样设计或许会导致较为明显的安全性问题,这个在上文Teclistamab中已经有过叙述。从Epcoritamab的临床试验EPCORE NHL-6来看,CRS发生率达到了49.7%,当然,大多是1级和二级,三级发生率为2.5%,是可以接受的。
Epcoritamab之后便是ABBV-383,二者的靶点不同,适应症也并不同,ABBV-383的靶点是BCMA×CD3,主要攻克的适应症是MM(多发性骨髓瘤),如前文所述,ABBV-383在经典双抗的结构上进行较大改造,CD3臂的亲和力较低,以此来提高安全性。
ABBV-383的临床数据参见文献《A Phase I First-in-Human Study of ABBV-383, a B-Cell Maturation Antigen×CD3 Bispecific T-Cell Redirecting Antibody, in Patients With Relapsed/Refractory Multiple Myeloma》,与强生的同靶点药物Teclistamab对比来看,安全性确实不错:所有等级的中性粒细胞减少症发生率为37%,所有等级的贫血发生率为29%。
此外,ORR方面也非常不错:剂量≥40mg时ORR为达到了68%。
当然,由于这是临床I期数据,存在多剂量组以及样本不足的情况,还需要后续临床试验的数据来验证。目前该管线的临床三期试验已经完成了首例患者给药。
在上述的双抗基础上,艾伯维再次出手,去选择双抗之后有足够实力迭代的药物,从而选择了先声药业的SIM0500,该次BD便是在此背景下发生的。
04
国内格局
如上文所述,目前国内与先声同靶点的三抗为信达的IBI3003和天广实生物的MBS314。
信达的IBI3003于2023年10月在clinicaltrial.gov上登记了一项临床I/II期试验,开始时间为2024年2月,结束时间为今年2月,也就是说,该三抗马上将要读出初步的I期数据。
其招募患者52人,临床试验地点为澳洲,从临床试验计划来看,该药的研发基本可以确定是奔着出海去的,至于是BD还是自主出海,目前来看BD的概率较大,并且如果BD的话,大概率将发生在临床I期数据读出,在疗效和安全性预期兑现的前提下。
天广实生物的MBS314的临床数据已经在上文叙述,它的亮点在于与辉瑞的合作:去年11月6日,天广实与辉瑞就MBS314达成战略合作,具体金额未见披露。其剂量扩展(Ib/II期)完成要等到2026年2月份,但目前已经有了稳定的合作方,至少研发现金流的紧迫问题已经不是问题了。
结语:正如前文所述,目前该三抗还处于早期的阶段,仅天广实读出了早期的小样本数据。但其为了提高疗效,解决耐药性和提升安全性是的初衷是毋庸置疑的,未来能否达到理想的效果,就需要之后样本更大临床数据的验证了。
过去的我们总认为三抗,四抗遥不可及,但从去年开始接二连三的BD使我们将目光转向这些早期的三抗,四抗分子,多抗的新一代迭代的理想正在慢慢照进现实。
识别微信二维码,添加抗体圈小编,符合条件者即可加入抗体圈微信群!
请注明:姓名+研究方向!
本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观点,不代表本站立场。
抗体药物偶联物引进/卖出
2025-01-09
·医药速览
三特异性抗体之所以备受瞩目,是因为它相较于单抗和双抗,在肿瘤免疫治疗中展现出了独特的优势。三抗能够同时激活多个信号通路,增强免疫细胞对肿瘤细胞的识别和杀伤能力,从而提高治疗效果。此外,三抗还可以通过结合不同的抗原表位,实现对肿瘤微环境的精准调控,减少副作用。
目前,全球有136款在研的三特异性抗体,其中进入临床研究的有41款。这些药物的开发主要集中在多发性骨髓瘤(MM)、非小细胞肺癌(NSCLC)等癌症的治疗上。例如,JNJ-79635322和HPN217等药物已经在临床试验中显示出积极的结果。目前,国内多家药企已布局三抗药物的研发,并在一些关键靶点上取得了突破性进展(下文不完全统计)。
国内药企动态
维立志博
2024年11月7日,维立志博宣布与Aditum Bio成立研发公司Oblenio Bio,并将CD3/CD19/BCMA三抗授权给Olenio Bio,后者支付3500万美元预付款和近期里程碑金额,5.79亿美元的开发、监管、销售里程碑金额。Aditum Bio为Oblenio Bio提供研发资金,维立志博还将获得Oblenio Bio的股权。
恩沐生物
2024年10月29日,葛兰素史克(GSK)宣布和恩沐生物达成合作,将以3亿美元的首付款从恩沐生物收购CMG1A46,后者将有资格获得总计5.5亿美元的开发和商业化里程碑付款。CMG1A46是一种靶向CD19、CD20和CD3的三特异性抗体,从机制上来说属于T细胞衔接器(TCE),该抗体对B细胞表面的CD19和CD20具有高亲和力,对T细胞表面的CD3具有低亲和力,可以降低与TCE相关的毒性。该药是首个进入临床研究阶段的CD19/CD20/CD3三特异性抗体。
百济神州
2024年9月18日,百济神州注射用BG-T187的临床试验申请获得国家药品监督管理局受理。BG-T187 是一款靶向 EGFR (epidermal growth factor receptor) 和细胞间质上皮转换因子 (c-Mesenchymal-epithelial transition factor, c-MET) 的三特异性抗体,应用于肺癌领域。
泽璟制药
2024年9月8日,泽璟制药宣布三特异性抗体注射用ZG006(CD3 × DLL3 × DLL3),在治疗晚期小细胞肺癌或神经内分泌癌患者的1/2期临床研究中表现出良好的耐受性、安全性及优异的抗肿瘤疗效,特别是晚期小细胞肺癌患者接受ZG006 10 mg及以上剂量治疗后的疗效显著,客观缓解率(ORR)达到66.7%,疾病控制率(DCR)达到88.9%。目前已经同时获得美国FDA和中国NMPA临床试验许可,已被美国FDA授予孤儿药资格。
惠和生物
2024年8月初,惠和生物开发的1类新药CC312冻干粉针剂已获得临床试验批准,用于治疗系统性红斑狼疮。CC312是一款创新的靶向CD19、CD3和CD28的三特异性抗体,此前已在美国和中国获得针对血液肿瘤的临床试验许可。
信达生物
2024年7月23日 ,中国国家药监局药品审评中心(CDE)官网最新公示,信达生物1类新药IBI3003获批临床,拟开发治疗复发或难治性多发性骨髓瘤患者。根据信达生物公开资料,这是一款GPRC5D/BCMA/CD3三抗产品。
先声再明
2024年3月12日,先声药业集团旗下抗肿瘤创新药公司先声再明宣布,其自主研发的人源化GPRC5D-BCMA-CD3三特异性抗体SIM0500的新药临床试验申请(IND)于本周内接连获得美国食品药品管理局(FDA),以及中国药品监督管理局(NMPA)批准,将开展用于复发或难治性多发性骨髓瘤患者的临床研究。SIM0500是一种人源化GPRC5D-BCMA-CD3三特异性抗体,在中美两国同步开发。
强生
2024年3月初,中国国家药监局药品审评中心(CDE)官网公示,强生(Johnson & Johnson)旗下强生创新制药(Johnson & Johnson Innovative Medicine)1类新药JNJ-80948543注射液获批临床,拟开发治疗淋巴细胞恶性肿瘤。公开资料显示,这是一款新型CD79b x CD20 x CD3三特异性T细胞重定向抗体。
博锐生物
2024年1月18日,博锐生物的BR115注射液获NMPA临床批准,用于治疗晚期恶性实体肿瘤。BR115是一款T细胞介导三特异性抗体,可同时靶向T细胞表面受体CD3和肿瘤相关抗原(TAA)的不同表位,具有更好的肿瘤特异性,同时可以选择性地针对TAA高表达肿瘤,有明显优于MNC同类在研产品的显著杀伤作用,而对TAA正常水平表达组织作用大幅减弱。
天广实
2023年12月28日,中国国家药监局药品审评中心(CDE)官网公示,天广实1类新药MBS314注射液获批临床,拟开发治疗复发/难治性多发性骨髓瘤(r/r MM)。公开资料显示,MBS314注射液是一款CD3/BCMA/GPRC5D三特异性抗体。
嘉和生物
嘉和生物旗下GB263T (EFGR/cMET/cMET,三特异性抗体) (以下称GB263T)也在2024ESMO年会上公布了最新临床有效性和安全性数据。GB263T是全球首个EGFR/cMET/cMET三特异性抗体,作为一种针对EGFR和两个不同cMet表位的三特异性抗体,GB263T拥有两个Fab结合EGFR。其Fc片段发生了突变,增强了Fc功能。因此,GB263T具有高度差异化的设计,表现出多种作用机制,可同时抑制原发性及继发性EGFR突变及cMet信号通路。
往期链接
“小小疫苗”养成记 | 医药公司管线盘点
人人学懂免疫学 | 人人学懂免疫学(语音版)
综述文章解读 | 文献略读 | 医学科普 | 医药前沿笔记
PROTAC技术 | 抗体药物 | 抗体药物偶联-ADC
核酸疫苗 | CAR技术 | 化学生物学
温馨提示
医药速览公众号目前已经有近12个交流群(好学,有趣且奔波于医药圈人才聚集于此)。进群加作者微信(yiyaoxueshu666)或者扫描公众号二维码添加作者,备注“姓名/昵称-企业/高校-具体研究领域/专业”,此群仅为科研交流群,非诚勿扰。
简单操作即可星标⭐️医药速览,第一时间收到我们的推送
①点击标题下方“医药速览”
②至右上角“...” ③点击“设为星标
并购孤儿药免疫疗法临床申请引进/卖出
2024-11-22
DUBLIN--(
BUSINESS WIRE
)--The
"B-cell Lymphoma - Pipeline Insight, 2024"
clinical trials has been added to
ResearchAndMarkets.com's
offering.
This "B-cell Lymphoma- Pipeline Insight, 2024" report provides comprehensive insights about 295+ companies and 300+ pipeline drugs in B-cell Lymphoma pipeline landscape. It covers the pipeline drug profiles, including clinical and nonclinical stage products. It also covers the therapeutics assessment by product type, stage, route of administration, and molecule type. It further highlights the inactive pipeline products in this space.
Report Highlights
The companies and academics are working to assess challenges and seek opportunities that could influence B-cell Lymphoma R&D. The therapies under development are focused on novel approaches to treat/improve B-cell Lymphoma.
B-cell Lymphoma Emerging Drugs Chapters
This segment of the B-cell Lymphoma report encloses its detailed analysis of various drugs in different stages of clinical development, including phase III, II, II/III I, preclinical and Discovery. It also helps to understand clinical trial details, expressive pharmacological action, agreements and collaborations, and the latest news and press releases.
B-cell Lymphoma: Therapeutic Assessment
This segment of the report provides insights about the different B-cell Lymphoma drugs segregated based on following parameters that define the scope of the report, such as:
Major Players in B-cell Lymphoma
There are approx. 295+ key companies which are developing the therapies for B-cell Lymphoma. The companies which have their B-cell Lymphoma drug candidates in the most advanced stage, i.e. Phase III include, Denovo BioPharma.
The report covers 300+ products under different phases of clinical development like:
Late stage products (Phase III)
Mid-stage products (Phase II)
Early-stage product (Phase I) along with the details of
Pre-clinical and Discovery stage candidates
Discontinued & Inactive candidates
Route of Administration
B-cell Lymphoma pipeline report provides the therapeutic assessment of the pipeline drugs by the Route of Administration. Products have been categorized under various ROAs such as
Intravenous
Subcutaneous
Oral
Intramuscular
Molecule Type
Products have been categorized under various Molecule types such as
Monoclonal antibody
Small molecule
Peptide
Product Type
Drugs have been categorized under various product types like Mono, Combination and Mono/Combination.
B-cell Lymphoma: Pipeline Development Activities
The report provides insights into different therapeutic candidates in phase II, I, preclinical and discovery stage. It also analyses B-cell Lymphoma therapeutic drugs key players involved in developing key drugs.
Pipeline Development Activities
The report covers the detailed information of collaborations, acquisition and merger, licensing along with a thorough therapeutic assessment of emerging B-cell Lymphoma drugs.
B-cell Lymphoma Report Insights
B-cell Lymphoma Pipeline Analysis
Therapeutic Assessment
Unmet Needs
Impact of Drugs
B-cell Lymphoma Report Assessment
Pipeline Product Profiles
Therapeutic Assessment
Pipeline Assessment
Inactive drugs assessment
Unmet Needs
Key Questions
Current Treatment Scenario and Emerging Therapies:
How many companies are developing B-cell Lymphoma drugs?
How many B-cell Lymphoma drugs are developed by each company?
How many emerging drugs are in mid-stage, and late-stage of development for the treatment of B-cell Lymphoma?
What are the key collaborations (Industry-Industry, Industry-Academia), Mergers and acquisitions, licensing activities related to the B-cell Lymphoma therapeutics?
What are the recent trends, drug types and novel technologies developed to overcome the limitation of existing therapies?
What are the clinical studies going on for B-cell Lymphoma and their status?
What are the key designations that have been granted to the emerging drugs?
Key Players
Lisocabtagene maraleucel
Hoffmann-La Roche
Nektar Therapeutics
Miltenyi Biomedicine
AVM Biotechnology
Lin BioScience
Incyte Corporation
ADC Therapeutics
Genor Biopharma
Beijing InnoCare Pharma Tech Co., Ltd.
CARGO Therapeutics
Chia Tai Tianqing Pharmaceutical Group Co., Ltd.
SystImmune
LIBO PHARMA
Abclon
BeiGene
Cellectis
Iovance Biotherapeutics, Inc.
Guangzhou Excelmab
Y-mAbs Therapeutics
TG Therapeutics
Sutro Biopharma
AbbVie
Aleta Biotherapeutics
Janssen Research & Development
Lantern Pharma
Beijing Immunochina Medical Science and Technology
Bantam Pharmaceutical
Lin Bioscience
SFA Therapeutics
neoX Biotech
March Biosciences
HUTCHMED
Key Products
Bristol Myers Squibb
Glofitamab
NKTR-255
Zamtocabtagene autoleucel
MB-CART20.1
AVM0703
LBS-007
Parsaclisib
Loncastuximab tesirine
GB-241
ICP-248
CRG-022
TQB3702
GNC-038
NM-IL-12
AT101
BGB-16673
UCART20x22
IOV-2001
EX103
CD38-SADA
TG-1801
STRO-001
ABBV-319
ALETA-001
JNJ-80948543
LP-284
INS19 CAR-T Cells
BTM 3566
LBS-007
SFA-001
NXD07
MB-105
HMPL A067
For more information about this clinical trials report visit
https://www.researchandmarkets.com/r/qxd94m
About ResearchAndMarkets.com
ResearchAndMarkets.com is the world's leading source for international market research reports and market data. We provide you with the latest data on international and regional markets, key industries, the top companies, new products and the latest trends.
临床2期ASCO会议细胞疗法临床1期
100 项与 JNJ-80948543 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| B细胞淋巴瘤 | 临床1期 | 美国 | 2022-08-18 | |
| B细胞淋巴瘤 | 临床1期 | 日本 | 2022-08-18 | |
| B细胞淋巴瘤 | 临床1期 | 澳大利亚 | 2022-08-18 | |
| B细胞淋巴瘤 | 临床1期 | 丹麦 | 2022-08-18 | |
| B细胞淋巴瘤 | 临床1期 | 法国 | 2022-08-18 | |
| B细胞淋巴瘤 | 临床1期 | 以色列 | 2022-08-18 | |
| B细胞淋巴瘤 | 临床1期 | 波兰 | 2022-08-18 | |
| 慢性淋巴细胞白血病 | 临床1期 | 美国 | 2022-08-18 | |
| 慢性淋巴细胞白血病 | 临床1期 | 美国 | 2022-08-18 | |
| 慢性淋巴细胞白血病 | 临床1期 | 中国 | 2022-08-18 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

生物类似药
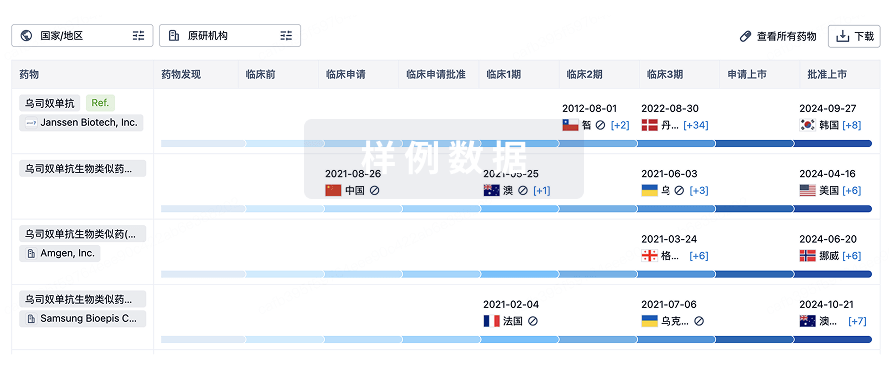
生物类似药在不同国家/地区的竞争态势。请注意临床1/2期并入临床2期,临床2/3期并入临床3期
登录
或
特殊审评
只需点击几下即可了解关键药物信息。
登录
或

Eureka LS:
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
