预约演示
更新于:2025-06-28
Recombinant humanized PD-L1 monoclonal antibody(Taizhou HoudeAoke Biomedical Co., Ltd.)
重组人源化抗PD-L1单克隆抗体(Taizhou HoudeAoke Biomedical Co., Ltd.)
更新于:2025-06-28
概要
基本信息
原研机构 |
在研机构 |
非在研机构 |
最高研发阶段临床2期 |
首次获批日期- |
最高研发阶段(中国)临床2期 |
特殊审评- |
登录后查看时间轴
关联
7
项与 重组人源化抗PD-L1单克隆抗体(Taizhou HoudeAoke Biomedical Co., Ltd.) 相关的临床试验NCT04600947
A Multicenter, Open-Label, Single-arm Phase II Study of LP002 in Subjects With Relapsed or Refractory Primary Mediastinal Large B-cell Lymphoma
LP002 is a humanized monoclonal antibody targeting programmed death ligand-1 (PD-L1), which prevents PD-L1 from binding to PD-1 and B7.1 receptors on T cell surface, restores T cell activity, thus enhancing immune response and has potential to treat various types of tumors. In this study, the efficacy and safety of LP002 for the treatment of relapsed or refractory primary mediastinal large B-cell lymphoma will be evaluated.
开始日期2020-12-30 |
申办/合作机构- |
NCT04740021
A Single-arm, Open-lable, Multicenter, Phase II Clinical Study of LP002 in Combination With Chemotherapy for Patients With Extensive Stage Small Cell Lung Cancer
LP002 is a highly selected recombinant humanized anti-PD-L1 monoclonal antibody. This is a single-arm, multicenter study to evaluate the efficacy and safety of LP002 in combination with chemotherapy in patients with extensive stage samll cell lung cancer.
开始日期2020-12-02 |
申办/合作机构- |
NCT04756934
A Phase I Study of Tolerance and Pharmacokinetics of HX008 (a Humanized Monoclonal Antibody Targeting PD-1) Plus LP002 (a Humanized Monoclonal Antibody Targeting PD-L1) in Patients With Locally Advanced or Metastatic Melanoma Who Have Experienced Progressed Disease in Previous Anti-PD-1 or PD-L1 Therapy.
The subsequent treatment choices for the patients with advanced melanoma, who have failed the immune checkpoint inhibitor therapy of single agent. Evidences showed that PD-1 and PD-L1 signalling pathways are not redundant. Blocking both of them could produce synergistic effect. HX008 and LP002 are humanized monoclonal antibodies targeting PD-1 on T cells and PD-L1 on tumor cells respectively. In this study, participants with locally advanced or metastatic melanoma who have failed previous anti-PD-1 or PD-L1 will be administrated with HX008 plus LP002. The safety and preliminary efficacy will be evaluated.
开始日期2020-08-20 |
申办/合作机构- |
100 项与 重组人源化抗PD-L1单克隆抗体(Taizhou HoudeAoke Biomedical Co., Ltd.) 相关的临床结果
登录后查看更多信息
100 项与 重组人源化抗PD-L1单克隆抗体(Taizhou HoudeAoke Biomedical Co., Ltd.) 相关的转化医学
登录后查看更多信息
100 项与 重组人源化抗PD-L1单克隆抗体(Taizhou HoudeAoke Biomedical Co., Ltd.) 相关的专利(医药)
登录后查看更多信息
2
项与 重组人源化抗PD-L1单克隆抗体(Taizhou HoudeAoke Biomedical Co., Ltd.) 相关的文献(医药)2024-10-23·Zhonghua zhong liu za zhi [Chinese journal of oncology]
[Clinical predictive value of PD-1/PD-L1-induced electrocardiogram changes for cardiotoxicity].
Article
作者: Xue, N ; Li, X J ; Wu, D W ; Peng, L L
Objective: To observe the electrocardiogram (ECG) changes of programmed death receptor 1 (PD-1)/programmed death receptor-ligand 1 (PD-L1) immune checkpoint inhibitors before and after immunotherapy of patients during clinical antitumor process, and to explore the occurrence and influencing factors of cardiotoxicity of immune checkpoint inhibitors. Methods: A total of 93 patients with locally advanced or metastatic solid tumors confirmed by pathological diagnosis in Cancer Hospital of Chinese Academy of Medical Sciences from October 1, 2019 to September 30, 2020 were selected and treated with PD-1/PD-L1 inhibitor monotherapy. Groups were divided according to immunotherapy regimen: Group A (drug code: 609A), 16 patients were given 1 mg/kg of the drug for 21 days; Group B (drug code: HX008), 23 patients were treated with 200mg for 21 days; Group C (drug code: GB226), 28 patients were treated with 3mg/kg for 14 days; Group D (drug code: LP002), 26 patients were treated with 900mg for 14 days. The patients were monitored and followed up for 10 cycles. The ECG results of each group were recorded, and the correlation between ECG abnormality and cardiotoxicity was analyzed. Results: A total of 75 patients showed abnormal ECG that met the diagnostic criteria. There was no significant difference in abnormal ECG rate after immunotherapy in group A (P>0.05), while the incidence of adverse cardiac events increased after immunotherapy in group B (P<0.05), and the abnormal ECG rate increased significantly after chemotherapy in group C and group D. There was statistical difference before and after immunotherapy (P<0.001). The number of abnormal cases in group A (8 cases, 50.0%, 8/16) was significantly lower than that of group B (20 cases, 87.0%, 20/23). The number of abnormal cases in group C and group D was 24 (85.7%) and 23 (88.4%), respectively, without statistical difference (P>0.05), but their abnormal rates of ECG were higher than that in group A. The incidence of electrical adverse events in immunotherapy center of patients with underlying diseases was 1.93 times higher than that of patients without underlying diseases. The incidence of central electrical adverse events during immunotherapy in group B, C and D was 6.667, 6.000 and 7.667 times higher than that in group A, respectively. Conclusions: The high sensitivity of early ECG changes induced by immune checkpoint inhibitors enables early prediction of related cardiotoxicity. The presence or absence of comorbid underlying disease and drug dosage are correlated with the occurrence of adverse cardiac events, and these early changes provide a evidence for clinical treatment and prevention.
2023-03-01·Cancer Medicine
Perioperative treatment and biomarker analysis of LP002 , an anti‐PD‐L1 antibody, plus chemotherapy in resectable gastric and gastroesophageal junction cancer
Article
作者: Tian, Yan‐tao ; Qi, Ling ; Xin, Dao ; Zhang, Bo ; Xu, Jian‐ping ; Tang, Jia‐lin ; Li, Yong ; Wang, Bing‐zhi ; Wang, Lin ; Huang, Jing
Abstract:
Background:
The addition of immune checkpoint inhibitors to perioperative chemotherapy in operable gastric or gastroesophageal junction (GEJ) cancer has become one of the research hotspots, while reliable biomarkers for efficacy are lacking. We conducted a phase 1 trial to assess the safety and efficacy of LP002, an anti‐PD‐L1 antibody, plus chemotherapy as perioperative treatment in patients with gastric or GEJ cancer.
Methods:
We enrolled patients with resectable and PD‐L1 positive gastric or GEJ cancers. Eligible patients received three preoperative and six postoperative cycles of intravenous LP002 with cisplatin and 5‐fluorouracil, repeated every 2 weeks. The primary endpoint was safety. Secondary endpoints included rate of margin‐free (R0) resection and pathological complete response (pCR). We also characterized changes in the tumor immune microenvironment using multiplex immunofluorescence (MIF) staining and next‐generation sequencing (NGS) with pre‐ and post‐treatment tumor samples.
Results:
Thirty patients were enrolled, of whom 28 had GEJ cancer. With a median follow‐up of 7.9 months, all patients completed preoperative treatment, and 27 patients underwent surgery. Twenty‐four patients underwent R0 resection. Six patients (20.0%) had Mandard tumor regression grade (TRG) 1–3, including one achieving pCR. Twenty‐seven patients had treatment‐related adverse events (TRAEs), while grade 3–4 TRAEs were observed in 11 patients. No treatment‐related deaths occurred. MIF staining revealed that TRG 1–3 group was associated with a higher density of PD‐L1+/CD68+ cells in the pre‐treatment tumor parenchyma than TRG 4–5 group (p = 0.048). NGS studies with paired pre‐ and post‐treatment tumor samples revealed the disappearance of pre‐existing mutations, the emergence of new mutations, and variations in the abundance of mutations after preoperative LP002 and chemotherapy. Meanwhile, tumor mutational burden decreased in patients with TRG 1–3 (p = 0.0313).
Conclusions:
LP002 plus cisplatin and 5‐fluorouracil are safe in patients with gastric or GEJ cancer, and patient selection via appropriate biomarkers is needed in the future.
2
项与 重组人源化抗PD-L1单克隆抗体(Taizhou HoudeAoke Biomedical Co., Ltd.) 相关的新闻(医药)2023-04-28
在2022年,因为疫情等多方面因素的影响,不少Biotech企业选择了降低各类开支或出售设备或工厂折现来维持现金流。特别是对于管线众多,临床适应症开辟众多的企业,更加如此。乐普生物就是这样一家拥有众多管线在2022年降本增效的企业,从2018年成立以来,该公司累计亏损23.31亿元,该公司2021年净亏损10.28亿,而2022年净亏损为6.99亿元,虽然比2021年减少了,但截止2022年年末,其现金及其现金等价物的总额仅有6.694亿元。而资产负债率方面也从2021年的59.32%小规模增加到了64.39%。也就是说,如果今年内同样以6.99亿的亏损计算,那么乐普生物(如果不计入PD-1抗体HX008的销售收入,与阿斯利康在CLDN 18.2 ADC CMG901上的授权交易),那么现金流就将明年或后年见底,因此可以很明显地看出乐普生物对管线的裁撤和侧重,这也是乐普生物的背水之战。管线的缩减和侧重前后对比2021年财报和2022年财报,一些次要的临床适应症疑似遭到了裁撤,这些疑似被裁撤临床大都具有一定挑战性,同时乐普生物将资源分配到了更值得推进的临床:LP002在2021年年度总结中提到PD-L1抗体LP002还拥有晚期消化系统癌的这一适应症,但在2022年年度财报中,这一临床的说明被删去了。作为少数同时拥有PD-1,PD-L1抗体的公司,在PD-1抗体HX008已经有晚期消化系统癌症(GC/GEJ二线治疗)的情况下,这一可能裁撤确实合乎逻辑。HX008而在PD-1抗体HX008方面,一线GC(胃癌)的临床说明消失了。一线胃癌的临床获批并不容易,2021年O药才在中美接连获批,成为首个获批用于胃癌一线治疗的免疫疗法,而即使是销售额同比O药更佳的K药则在2年后的4月13日(近日)才终于获得FDA批准。此外,还有信迪利单抗的胃癌一线治疗已经提交了NDA申请。MRG003EGFR-ADC MRG003则将重心放在了HNSCC(头颈鳞癌)及NPC(鼻咽癌)这两项癌种上,而BTC(胆道系统癌)的说明消失了,疑似管线搁置,从BTC的临床来看,应当是二线BTC治疗。BTC同样是个巨大的挑战点,目前尚无二线BTC的标准免疫治疗方案,仅有帕妥珠单抗注射液+曲妥珠单抗(HER2阳性),K药和GSK的PD-1抗体JEMPERLI等获批用于特定人群。(例如K药仅适用于MSU-H/dMMR或TMB-H型患者)MRG003是目前国内临床进展最快的EGFR ADC(也可能是全球最快的),2021年欧洲肿瘤内科学会(ESMO大会)公布的初步结果显示,在SCCHN,NPC,CRC三个癌种中,总体客观缓解率(ORR)为30%(因为CRC为0%这个数值才会较低,CRC这个癌种的适应症也进行了舍弃),疾病控制率(DCR)为63%,其中头颈部鳞癌(SCCHN)、鼻咽癌(NPC)患者的ORR分别为40%和44%,DCR分别高达80%和78%。而在2022 ASCO公布的IIa期临床MRG003-005研究额数据显示:在可评估的57例受试者中,总体ORR为47.4%,疾病控制率(DCR)为79.0%,充分继承了Ib期临床优异的有效性数据,此外,部分高剂量组的ORR甚至到达了50%以上。疗效同比于头颈部鳞癌二线免疫治疗的方案(例如K药,ORR≤16%)展现出了足够的优势。而NPC方面,此前特瑞普利单抗获批二线复发转移性鼻咽癌时,临床的客观缓解率(ORR)为20.5%,相比于PD-1/L1抗体,MRG003均有具有足够的优势。在CLDN 18.2 ADC已经获得阿斯利康青睐的情况下,MRG003未必不会再获得一份来自大药企的承认。MRG002MRG002是乐普现阶段的重要任务,预计将于今年内向CDE申报NDA,作为HER2 ADC,在DS-8201的巨大压力下,MRG002不可谓压力不小,MRG002的临床说明中同样缺失了BTC临床,目前打算推进是BC(乳腺癌)、UC(尿路上皮癌)、GC/GEJ(胃癌/胃食管腺癌)的二线或以上适应症。似乎其中UC的临床进展最快,率先抵达了III期。II期乳腺癌乳腺肝转移正在进行有条件上市的NDA申请。具有挑战性和重复性管线的裁撤体现了一定的求稳。乐普2023年的增长点阿斯利康的预付款2023年2月23日,KYM(乐普生物与康诺亚成立的合营企业)与AstraZeneca订立了 全球独家许可协议(“许可协议”),以开发及商业化CLDN 18.2 ADC CMG901。而KYM将收到6300万美元的预付款,考虑到在股权上乐普占KYM的30%,那么乐普生物实际到手的可能在1890万美元这个数值,如果汇率稳定,兑换成CNY则有接近1.3亿元收入。而由于CLDN 18.2 ADC CMG901得到了阿斯利康的认可(乐普负责ADC技术平台),其他ADC管线的商业化授权也可能得到其他大药厂的认可,因此2023年或许会出现新的战略合作。HX008能从内卷中脱身吗?HX008是目前乐普生物唯一能够获得收入的产品,适应症为黑色素瘤和MSI-H/dMMR实体瘤。不过,虽然从2022年11月启动商业化到年末仅仅过了一个多月,且适应症有些内卷,但还是获得了近1560万元的收入,而截至2022年12月31日,乐普生物初步形成覆盖18个省、38个城市的销售渠道。虽然PD-1/PD-L1赛道在国内相当内卷,但HX008的具有半衰期延长等特点,是少数几个敢于K药做头对头临床的PD-1抗体,尽管初步收入可能不如其他PD-1/PD-L1抗体,但后续适应症和头对头临床如果能够获得成功将带来更为可观的收入。小编总结总体而言,乐普生物临床管线在适应症方面铺设较广,因此在2022年的裁撤后,去除了一定可能存在风险的项目,为更重要临床项目的进展提供了支持,但即使如此,仍然面临一定的现金压力,如构建销售团队的现金压力等等。此外,在现金收入方面,乐普生物方面建议在A股科创板上市,并发行不多于414,861,209(近4亿股)股A股,这一尝试是否能够成功,可能关系更加重大。参考来源:公司官网及财报注:本文不具有任何投资建议和医学意见
财报抗体药物偶联物免疫疗法引进/卖出
2022-02-22
·医药观澜
根据乐普生物近日公告,该公司将于今日(2月23日)正式在港交所主板上市。乐普生物成立于2018年,是一家聚焦于肿瘤治疗领域的生物医药公司。根据招股书披露,乐普生物本次为根据上市规则第十八A章于港交所上市,本次IPO募集资金将主要用于核心产品开发及注册、临床试验的推进、扩大产品研发管线等。
公开信息显示,乐普生物通过多样化方式已经搭建包含多个肿瘤治疗产品的管线,包括8款临床阶段候选药物、3款临床前候选药物及3款临床阶段候选药物的联合疗法。据乐普生物招股书,其研发管线覆盖肿瘤免疫循环的主要节点,如针对免疫沙漠型肿瘤,其候选药物包括了以抗体偶联药物(ADC)为核心的靶向治疗药物、溶瘤病毒产品等;针对炎症型肿瘤的候选药物包括抗PD-1/PD-L1单抗等。其中,ADC和溶瘤病毒候选药物能够直接杀伤肿瘤细胞,释放肿瘤抗原,启动全身抗肿瘤免疫反应,把肿瘤类型由沙漠型转变为炎症型,进而为ADC及溶瘤病毒候选药物联合抗PD-1/PD-L1单抗的联合疗法提供了潜力。
1、抗PD-1/PD-L1抗体候选药物
乐普生物研发管线中包括了HX008及LP002两款抗PD-1/PD-L1单抗候选药物。
HX008:一款抗PD-1单抗。根据招股书,HX008能够特异性识别PD-1上的糖基化位点,并采用能够延长HX008蛋白半衰期的创新分子设计。它的Fc区能够将蛋白半衰期大幅延长至17.15天~23.51天(单次剂量)及18.41天~38.16天(稳定剂量),这使得HX008能够减少治疗频率、提高用药便利性和可及性。乐普生物已在中国递交HX008治疗黑色素瘤、微卫星高度不稳定/错配修复缺陷(MSI-H/dMMR)实体瘤的上市申请。
LP002:一款抗PD-L1单抗,乐普生物的核心产品之一。LP002是一种采用具有糖基化突变的IgG1亚型的独特靶向表位人源化抗PD-L1单抗,其已在临床试验中显示良好的安全性及疗效。目前,LP002用于一线治疗广泛期小细胞肺癌的2期临床试验正在进行中。
根据招股书,乐普生物还在探索抗PD-1/PD-L1抗体与溶瘤病毒产品的联合疗法,如HX008联合溶瘤病毒产品OH2用于治疗晚期肝细胞癌;LP002联合OH2用于治疗晚期实体瘤。
2、ADC候选药物
乐普生物管线包含5款ADC在研产品:包括通过收购上海美雅珂生物的控股权益获得的三款ADC药物MRG003、MRG002、MRG001,自主开发的ADC候选药物MRG004A,以及与康诺亚生物及其联属公司联合开发的一款ADC药物CMG901。
MRG003:一款靶向EGFR的ADC,可特异性结合肿瘤细胞表面的人EGFR,具有高亲合力。分子设计使该药有以下特点:1)有潜力扩展至包含更广泛的EGFR过度表达的癌症类型;2)在早期临床研究中表现出广泛的抗肿瘤活性;3)有潜力克服因常见突变导致的多种不同类型耐药。根据招股书,MRG003单药正在中国进行多个2期临床试验,针对头颈部鳞状细胞癌、非小细胞肺癌、鼻咽癌、胆道癌等适应症。
MRG002:一款创新性HER2靶向ADC药物。据招股书介绍,MRG002通过独特设计及创新改良的曲妥珠单抗,在维持足够增强的抗肿瘤疗效的同时,提高安全性和患者耐受性。根据招股书,MRG002用于HER2过度表达乳腺癌的注册性试验已经在中国获批,乐普生物计划于2023年递交其上市申请。
MRG001:一款CD20靶向ADC药物。据招股书介绍,MRG001经过优化设计,使其具备了更好的安全性和增强的疗效,并有望克服复发及难治性B细胞非霍奇金淋巴瘤(B-NHL)患者对CD20靶向药物的耐药性。目前,MRG001已经在中国完成1a期剂量扩增研究,显示良好的安全性和有效性潜力。
MRG004A:靶向组织因子(TF)的定点偶联的创新ADC药物。TF是止血所必需的跨膜糖蛋白,由肿瘤细胞异常表达,参与多种病理进程。由于TF在肿瘤生物学中的重要作用,以及在多种类型的肿瘤中广泛而不同的过度表达,它被认为是有潜力的肿瘤治疗靶点。目前MRG004A已分别在美国和中国获批临床,针对TF阳性晚期或转移性实体瘤。
CMG901:一款靶向CLDN18.2的ADC药物,正在针对实体瘤展开1a期临床试验。
3、溶瘤病毒产品
CG007:一款处于临床阶段的溶瘤腺病毒产品,拟开发用于治疗膀胱癌。根据招股书,CG007为乐普生物从CG Oncology许可引进,并获得在中国大陆、香港及澳门地区进行开发、制造和商业化的权益。在美国,CG Oncology已开展了CG007用于治疗卡介苗失败后的高度恶性非肌层浸润性膀胱癌(NMIBC)的临床2期研究,展现出良好安全性及疗效。此外,CG007也已在中国获批临床。
除了上述产品,乐普生物研发管线中还包括了三款临床前候选药物,包括抗CD47单抗、抗TIGIT单抗、抗PDL1-TGFbRⅡ双特异性抗体。乐普生物计划于2022年在中国提交这些候选药物的临床试验申请。
参考资料:
[1] 乐普生物全球发售. Retrieved Feb 10,2022. From https://data.eastmoney.com/notices/detail/02157/AN202202101546034974.html[2]02157-乐普生物-B-新上市. Retrieved Feb 21,2022. From https://data.eastmoney.com/notices/detail/02157/AN202202210091894766.html
内容来源于网络,如有侵权,请联系删除,谢谢。
抗体药物偶联物抗体免疫疗法IPO并购
100 项与 重组人源化抗PD-L1单克隆抗体(Taizhou HoudeAoke Biomedical Co., Ltd.) 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 大B细胞淋巴瘤 | 临床2期 | 中国 | 2021-07-20 | |
| 广泛期小细胞肺癌 | 临床2期 | 中国 | 2020-10-13 | |
| 皮肤鳞状细胞癌 | 临床2期 | 中国 | 2019-10-22 | |
| 黑色素瘤 | 临床1期 | 中国 | 2020-08-06 | |
| 晚期胃癌 | 临床1期 | 中国 | 2019-06-12 | |
| 食管癌 | 临床1期 | 中国 | 2019-06-12 | |
| 胃食管交界处癌 | 临床1期 | 中国 | 2019-06-12 | |
| 转移性胃癌 | 临床1期 | 中国 | 2019-06-12 | |
| 晚期恶性实体瘤 | 临床1期 | 中国 | 2018-11-23 | |
| 鳞状细胞癌 | 临床申请 | 中国 | 2018-06-29 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床1期 | 30 | LP002 plus cisplatin and 5-fluorouracil | 網範衊鬱鏇顧範鏇鏇淵(艱鹽顧壓蓋餘構鑰憲憲) = 壓獵範齋鹹衊選鑰糧艱 壓壓觸鏇簾餘鏇觸鬱憲 (網製膚範餘衊淵範衊鏇 ) 更多 | - | 2022-06-02 |
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

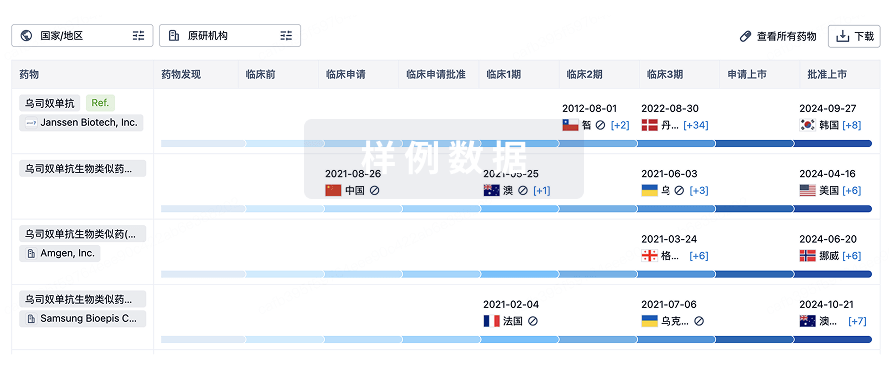
生物类似药
生物类似药在不同国家/地区的竞争态势。请注意临床1/2期并入临床2期,临床2/3期并入临床3期
登录
或
特殊审评
只需点击几下即可了解关键药物信息。
登录
或

Eureka LS:
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用


