更新于:2024-06-19
Linclatamig
更新于:2024-06-19
概要
基本信息
药物类型 双特异性T细胞结合器 |
别名 BLYG-8824A、RG 6286 |
作用机制 CD3ε抑制剂(CD3e molecule inhibitors)、LY6G6D抑制剂(lymphocyte antigen 6 family member G6D inhibitors) |
在研适应症- |
原研机构 |
在研机构- |
非在研机构 |
最高研发阶段终止临床1期 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
关联
1
项与 Linclatamig 相关的临床试验A Phase I, Open-Label, Dose-Escalation Study Of The Safety And Pharmacokinetics Of BLYG8824A Administered Intravenously In Patients With Locally Advanced Or Metastatic Colorectal Cancer
This study will evaluate the safety, tolerability, and pharmacokinetics of BLYG8824A and will make a preliminary assessment of the anti-tumor activity of BLYG8824A in patients with locally advanced or metastatic colorectal cancer.
开始日期2020-08-31 |
申办/合作机构 |
100 项与 Linclatamig 相关的临床结果
登录后查看更多信息
100 项与 Linclatamig 相关的转化医学
登录后查看更多信息
100 项与 Linclatamig 相关的专利(医药)
登录后查看更多信息
12
项与 Linclatamig 相关的新闻(医药)2024-06-08
转自:蒲公英Ouryao 综合:无忧
5月1日,上海医药发布公告,决定终止三个临床试验及后续开发。三个抗癌药研发项目累计投入超3亿元。
近40天后,6月8日,上海医药又宣布终止四个研发项目的临床试验及后续开发,四个项目总计研发投入约为1.15亿元。
据统计,2023年,有3895款候选药物退出在研管线。
又终止四个研发项目
上海医药6月8日发布公告,为合理配置研发资源、聚焦优势研发项目,公司基于对研发项目未来市场价值、业务协同以及后续开发投入等因素的综合评估,决定终止B001、B001-A、I022以及I022-K四个研发项目的临床试验及后续开发。
B001是新型人用重组单克隆抗体制品,拟用于CD20阳性的B细胞非霍奇金淋巴瘤的治疗。2016年8月,该项目获国家药品监督管理局批准开展临床试验,目前处于I期临床试验结束阶段,截至目前该项目累计研发投入共计约人民币6,466.68万元,
本次拟终止针对B细胞非霍奇金淋巴瘤(B-NHL)治疗的临床开发。
B001-A项目是与B001完全相同的新型人用重组单克隆抗体制品,拟用于多发性硬化症(MS)的治疗,2021年6月获得国家药品监督管理局批准开展该适应症临床试验,之后未开展临床,本次拟终止针对MS的临床研发。截至目前该项目累计研发投入共计约人民币593.46万元。
另外两个终止的管线I022和I022-K,都是化药1类小分子创新药。
I022是化药1类小分子创新药,拟用于晚期乳腺癌/脂肪肉瘤等的治疗;与来曲唑联用,拟用于乳腺癌一线的治疗;与内分泌药物联用,拟用于乳腺癌后线、乳腺癌脑转移的治疗;与开坦尼®联合用药,拟用于脂肪肉瘤的治疗。
2020年5月,该项目获国家药品监督管理局批准开展临床试验,目前处于II期临床试验结束阶段,截至目前针对本次终止所涉适应症累计研发投入共计约人民币699.37万元。针对上述其他适应症的临床试验及后续开发仍正常进行中。
I022-K是化药1类小分子创新药,拟用于晚期实体瘤的治疗。2021年8月,该项目获国家药品监督管理局批准开展临床试验,目前处于I期临床试验结束阶段,本次拟终止该药物的后续研发。截至目前该项目累计研发投入共计约人民币3,699.90万元。
5月份已终止3个研发项目
5月1日,上海医药发布公告称,为合理配置研发资源、聚焦优势研发项目,公司基于对研发项目未来市场价值、业务协同以及后续开发投入等因素的综合评估,决定终止I010项目、B002项目以及B003项目三个研发项目的临床试验及后续开发;三个项目累计研发投入共计约3.22亿元。 详见<<多家药企密集终止研发管线>>
两次终止的7个新药研发项目涉及研发投入达4.37亿元,7个项目中有4个是单抗项目,涉及研发投入达3.45亿元,占比达79%。
2023年,3895款候选药物退出在研管线
据Citeline近期发布的《2024医药研发趋势年度回顾白皮书》(简称白皮书)显示:2023年,全球研发管线新增5428款药物,与此同时,有3895款候选药物退出在研管线。
而进入2024年以来,基于成本控制、战略调整以及提升研发效率的需求,仍有不少药企宣布公司候选药物终止开发。
普洛药业,终止1项目III期临床试验:今年1月,普洛药业股份有限公司全资子公司浙江普洛家园药业有限公司发布公告,基于目前临床研究进展及后续研发投入等因素的综合评估,公司决定终止创新药注射用索法地尔治疗急性缺血性脑卒中的III期临床试验。
天坛生物,终止一项III期临床试验:1月31日,天坛生物发布公告称,决定终止控股子公司蓉生药业的“静注巨细胞病毒人免疫球蛋白(pH4)”III期临床试验研究及后续研发。公司在该药物研发上已投入7069.09万元人民币。
拜耳终止1项II期临床:5月14日,拜耳在公布2024年Q1业绩时透露,已终止Zaberdosertib(BAY1834845)治疗特应性皮炎的II期临床。
Zaberdosertib是一款靶向白细胞介素-1受体相关激酶4(IRAK4)的小分子抑制剂,于2017年2月首次启动I期临床试验。
BMS,削减12条管线:今年4月,BMS关闭了其位于加利福尼亚州红木城的癌症免疫学和细胞治疗主题研究中心。BMS目前大约有12个项目已经停止或指定委外开发,包括其免疫疗法Yervoy的后续版本、SIRPα和BET靶向药物,并将在今年剩余时间内继续审查其产品线。
罗氏,削减6项临床项目:4月24日,罗氏在2024年第一季度财报中披露:削减6项临床项目,分别为用于实体肿瘤的camonsertib和belvarafenib;用于结直肠癌的双特异性抗体RG6286;用于精神疾病的RG6163以及用于尿路感染的LepB抑制剂RG6319。大部分处于1期开发阶段。
武田制药,精简三个管线:5月9日,武田制药在2023财年业绩报告中提到,精简其药物管线,明确放弃TAK573、TAK981以及CAR-NK疗法TAK007的血液肿瘤适应。
参考:企业公告 制药网
欢迎留言,更多观点。
推荐阅读:
蒲公英Ouryao视频号
投稿、广告、商务合作:
Qinrenlvcha
临床1期
2024-05-12
·药事纵横
声明:因水平有限,错误不可避免,或有些信息非最及时,欢迎留言指出。本文仅作医疗健康相关药物介绍,非治疗方案推荐(若涉及);本文不构成任何投资建议。面对新药研发困难、销售业绩下滑等压力冲击,药企巨头也不得不做出管线调整、裁员的决定。跨国大药企的斧头快速抡起,消减研发管线,聚焦更有前景的资产,为的是保持竞争优势。让我们一起来看看2024年第一季度都有哪些跨国药企削减了管线项目。一、罗氏:砍掉6条管线4月24日,罗氏在2024年第一季度财报中披露:削减6项临床项目,分别为用于实体肿瘤的camonsertib和belvarafenib;用于结直肠癌的双特异性抗体RG6286;用于精神疾病的RG6163以及用于尿路感染的LepB抑制剂RG6319。大部分处于1期开发阶段。camonsertib是一款潜在的BIC口服ATR抑制剂,用于治疗具有特定合成致死基因组改变的肿瘤,包括ATM基因改变。今年1月份,II期 TAPISTRY研究中第1名患者接受了Camonsertib治疗,由此触发了一个4000万美元的里程碑付款。但情况突然急转而下,半个月后罗氏突然宣布将终止协议,罗氏给出的理由是:出于对罗氏的管线和不断变化的外部因素进行审查后的结果。belvarafenib是一款选择性泛RAF激酶抑制剂,目前处于2项临床,但已停止患者招募,即使已从管线移除此项目,但公司将继续提供研究治疗并监测已入组患者。2016年,Genentech从韩国公司Hanmi Pharmaceutical中引入该药物,获得该药物在除韩国之外的全球权益。Hanmi因此获得8000万美元预付款,以及高达8.3亿美元的开发、监管和商业化里程碑费用等。在交易时,Belvarafenib开发正处于I期阶段。双特异性抗体RG6286可与T细胞上的结直肠癌抗原LY6G6D和CD3结合。I期临床试验预计将于2026年初完成。基因泰克于2020年开始在结直肠癌患者中测试该候选药物(也称为 BLYG8824A)。此外,放弃了用于精神疾病的RG6163以及用于尿路感染的LepB抑制剂RG6319,而转向推进一种名为RG6436的替代性LepB抑制剂。在此过程中,罗氏产品线的平衡从神经科学和肿瘤学(较小程度)转向了免疫学、心血管和代谢疾病领域。神经科学项目的数量从18个降至12个,尽管其中一个项目被转移到了研发管线的另一部分。自2023年第3季度以来,罗氏为重点关注影响力大的项目,已终止了20%的管线。首席执行官Thomas Schinecker表示:“罗氏的目标是使其产品线中80%为最佳管线或一流资产。确定优先次序和不断重新分配是正常业务的一部分,确保其拥有的资金其用于患者和公司的最佳用途。”二、BMS:砍掉12条管线4月25日,百时美施贵宝(BMS)在2024年第一季度财报中披露:BMS正在施行一项全面成本削减计划,到2025年底,该计划将节省约15亿美元的成本,大部分将用于再投资以资助创新和推动增长。作为计划的一部分将从其产品线中削减大约12个项目,还包括裁员约2200人,约占其全球员工总数的6%。BMS在决定停止药物开发时考虑的因素包括公司是否认为某个项目的数据可以击败现有药物或其他在研药物,某个项目是否会成为潜在的增长动力,以及是否可以成为 "同类第一"或 "同类最佳"。涉及的一些实验性药物包括抗CTLA-4项目、抗SIRPα抗体和BET抑制剂。抗CTLA-4和抗SIRPα的研究可能无法击败Yervoy。BET抑制剂(BMS-986158)被取消的原因是,虽然该药显示了良好的数据,但没有达到成为增长动力的门槛。在周四早盘交易中,该公司股价$BMY下跌超过8%。根据Endpoints News对其2023年第四季度和2024年第一季度报告的审查,百时美施贵宝总体上从1期开发中撤消了8个项目,从2期开发中撤消了6个项目。该公司还增加了五个进入1期的项目,同时将一种药物从1期推进到2期,将两种药物从1期推进到3期。最近收购的Karuna和RayzeBio公司的两个项目也进入了 3 期开发阶段。三、吉利德:砍掉10条管线4月22日,吉利德在2024年第一季度财报中披露:共砍掉10条管线。其中,吉利德终止2个细胞疗法项目:分别为自体抗CD19 CAR-T细胞疗法Brexucabtagene autoleucel (ZUMA-25)治疗罕见B细胞恶性肿瘤的2期试验和CLL-1 (KITE-222)治疗复发难治性急性髓系白血病的1期试验。剔除了CD47单抗magrolimab联合疗法治疗头颈部鳞状细胞癌、三阴性乳腺癌、结直肠癌等实体瘤的6项研究。2月7日,吉利德宣布,终止magrolimab所有血液瘤项目开发,而此次6项试验从管线中移除意味着吉利德彻底放弃该款药物的开发。此外,吉利德还停止与Arcus合作的PD-1单抗zimberelimab联合抗TIGIT抗体domvanalimab±化疗用于一线非小细胞肺癌的2个项目。在研产品管线方面,吉利德在肿瘤、抗病毒、免疫疾病领域将继续打造丰富的产品储备。目前,吉利德已有54款项目进入临床研究阶段,同时还有10款可供临床阶段选择的资产。四、赛诺菲:砍掉3条管线4月25日,赛诺菲在2024年第一季度财报中披露:放弃了部分免疫学及神经学管线适应症项目,包括自免赛道的CD40L抗体Frexalimab在干燥综合征上的2期研究、RIPK1抑制剂Oditrasertib治疗肌萎缩性侧索硬化症(ALS)的2期研究、一项用于治疗罕见遗传性疾病GM2神经节脂质沉积症的分子Venglustat的2期研究。Frexalimab:由于2期研究数据未达到“必要的疗效结果”,赛诺菲暂停开发治疗Sjögren综合征的CD40L抗体药物Frexalimab。不过,Frexalimab其他适应症不会受影响,公司继续进行多发性硬化症和继发性进展性多发性硬化症(SPMS)的3期试验,以及1型糖尿病和系统性红斑狼疮的2期试验。Oditrasertib:赛诺菲停止了RIPK1抑制剂Oditrasertib治疗肌萎缩性侧索硬化症(ALS)的2期研究,因其未能达到基于ALS功能评定量表修订的主要改善终点。赛诺菲将在即将召开的医学会议上分享完整的安全性和有效性数据,并继续在多发性硬化症患者中进行Oditrasertib的2期研究。Venglustat:用于治疗罕见遗传性疾病GM2神经节脂质沉积症的分子Venglustat的2期研究因试验的临床终点“缺乏积极趋势”而被终止。五、阿斯利康:砍掉7条管线4月25日,阿斯利康在2024年第一季度财报中披露:将放弃4款早期药物涉及7条管线:口服Porcupine抑制剂AZD5055,该药物用于特发性肺纤维化,由AZ于2020年8月以1700万美元首付、3.6亿美元的潜在里程碑从Redx Pharma引进,目前阿斯利康由于战略投资组合优先顺序而终止其在健康志愿者中的两项I期试验;反义寡核苷酸药物AZD7503:由于战略投资组合优先顺序而终止该药物用于治疗非酒精性脂肪性肝炎的两项1期试验和健康志愿者中测试安全性和耐受性的一项1期试验;LOX-1靶向单克隆抗体MEDI6570:该药物旨在阻断LOX-1受体的多种配体。由于战略投资组合优先顺序,阿斯利康终止了其正在进行的一项名为GOLDILOX的2b期临床试验;口服D因子抑制剂Vemircopan(维米克泮):终止其用于治疗全身性重症肌无力的一项2期研究,其用于治疗狼疮性肾炎的2期试验和治疗肝功能受损的1期试验还在进行中;六、诺华:砍掉2条管线与上一季度对比来看,诺华砍掉了一项早期资产CD73拮抗剂NZV930和一项2期临床资产CSF-1R抑制剂BLZ945。诺华此前在开展NZV930单独使用以及与PDR001和/或 NIR178联合使用对晚期癌症患者的安全性、耐受性和初步抗肿瘤活性的I/Ib期、开放标签、多中心研究(NCT03549000)。对于BLZ945,此前在一项开展ALS患者在多次服用 BLZ945 后的安全性、耐受性和脑小胶质细胞反应的II期试验(NCT04066244),和一项口服BLZ945单药或与PDR001静脉注射联合用于晚期实体瘤成年患者中的安全性、耐受性、药代动力学(PK)、药效学和抗肿瘤活性的I/II 期研究(NCT02829723)。七、辉瑞:砍掉4条管线5月1日,辉瑞发布了2024 Q1业绩报告。在管线方面,公司停止了VTX-801的开发,VTX-801是一款重组AAV基因疗法,用于治疗罕见遗传性疾病威尔逊氏症,该疗法是辉瑞与Vivet Therapeutics共同开发的。辉瑞于2019年3月收购了Vivet的少数股权,并正在为1/2期研究生产该疗法的载体。此外,辉瑞还取消了其溃疡性结肠炎药物Velsipity(etrasimod)在特应性皮炎和斑秃中的两个潜在新适应症,以及口服Zavzpret(zavegepant)的偏头痛预防项目。这三项研究均已进入第二阶段。总体而言,辉瑞的研发管线在过去三个月中净增加了一个项目,从112个增加到113个。除了削减的4个项目外,辉瑞还增加或推进了10个项目,并在美国和欧盟获得了5项批准。八、强生:砍掉2条管线与2023年12月的管线对比发现,强生2024Q1砍掉了两个肿瘤的I期项目,一个是JNJ-8114 (PSMA/CD3),一个是JNJ-4916溶瘤病毒。强生的创新药业务主要聚焦于免疫调节、抗感染、神经系统、肿瘤、肺动脉高压和心血管六大管线。目前强生管线中共有95个项目,包括23个1期项目,20个2期项目,39个3期项目和13个项目处于上市申报阶段。总结仅在2024年Q1就有8家药企巨头就已砍了40多条管线,终止原因多因疗效数据不及预期临床失败,或因市场变化进行战略调整。对于跨国药企来说,加速从不具优势的领域抽身,从原计划试验中节约的资金将用于加速推进其全球首创或同类最佳候选药物,是公司研发战略调整的重要部分。不过,管线项目的消失仍浪费了大量资源和精力,因此这提醒了药企应该更加注重风险管理和决策的科学性,以减少砍掉管线造成的损失。参考资料:各公司官网
引进/卖出财报临床1期ASH会议临床2期
2024-05-06
转自:蒲公英Ouryao 整理:无忧5月1日,上海医药发布公告,决定终止I010项目、B002项目以及B003项目的临床试验及后续开发。三个抗癌药研发项目累计投入超3亿元。2024年以来,多个药企包括跨国公司,终止冗余药品研发项目,引起业内的关注。 上海医药,终止三个研发项目5月1日,上海医药发布公告,决定终止I010项目、B002项目以及B003项目的临床试验及后续开发。其中,I010项目及B002项目处于Ⅰ期临床试验阶段,B003项目处于Ⅱ期临床试验阶段。 上海医药表示,为合理配置研发资源、聚焦优势研发项目,基于对上述研发项目未来市场价值、业务协同以及后续开发投入等因素的综合评估,决定终止上述研发项目。 I010是表皮生长因子受体酪氨酸激酶抑制剂,拟用于非小细胞肺癌(NSCLC)等恶性肿瘤的治疗。2016年11月,该项目获国家药品监督管理局批准开展临床试验,如今处于Ⅰ期临床试验结束阶段。截至目前,该项目累计研发投入共计约人民币4759.90万元。 B002是新型人用重组单克隆抗体制品,拟用于HER2阳性的转移性乳腺癌以及新辅助治疗HER2阳性乳腺癌的治疗。2017年9月,该项目获国家药品监督管理局批准开展临床试验,如今处于Ⅰ期临床试验收尾阶段。截至目前,该项目累计研发投入共计约人民币1.33亿元。 B003是人用重组单克隆抗体与小分子药物偶联制品,拟用于HER2阳性的局部晚期或转移性乳腺癌的治疗。2018年1月,该项目获国家药品监督管理局批准开展临床试验,如今处于Ⅱ期临床试验入组阶段。截至目前,该项目累计研发投入共计约人民币1.41亿元。舒泰神,终止4个新冠临床3月25日,舒泰神发布公告,称基于当前新冠疫情形势,结合年度审计工作开展,对在研项目进行了梳理,经审慎判断,决定终止BDB-001注射液、STSA-1002注射液、STSA-1005注射液、STSA-1002和STSA-1005联合用药项目在COVID-19适应证方向的研究工作。 根据被终止临床试验的药物基本信息,四款新冠项目累计研发总投入为3.83亿元。最早获批临床的产品为BDB-001注射液,时间为2020年2月。BDB-001注射液在国内完成I期临床后,还在印度、印尼、西班牙、孟加拉展开了国际多中心II/III期临床。 此外,有三大新冠项目在2021年进入临床,还有一个在2022年8月才获批临床试验,几大研发项目的进度都较靠后,尚未进入临床后期。 舒泰神表示,以上项目在COVID-19适应证方向的研究工作终止后,不会影响在其它适应证上继续研究,而已开展的临床研究工作将为相关项目后续拓展适应证建立良好基础。 天坛生物,终止一项III期临床试验1月31日,天坛生物发布公告称,决定终止控股子公司蓉生药业的“静注巨细胞病毒人免疫球蛋白(pH4)”III期临床试验研究及后续研发。原因是:根据中国异基因造血干细胞移植后巨细胞病毒感染的预防和治疗现状,基于市场情况全面、谨慎分析,并结合天坛生物战略规划,决定终止该药物III期临床试验研究及后续研发。 公告显示,静注巨细胞病毒人免疫球蛋白(pH4)项目于2016年取得药物临床试验批件,主要用于造血干细胞移植等免疫缺陷患者巨细胞病毒(CMV)血症及相关疾病的治疗。公司在该药物研发上已投入7069.09万元人民币。 视线转向跨国药企。2024年多家跨国药企通过砍掉冗余管线并集中资源,聚焦更有前景的业务资产,推动企业的重组转型。 BMS,削减12条管线 BMS首席执行官Christopher Boerner在一份重组声明中表示:公司将削减12条研发管线。节省下来的资金将用于投资潜在重磅产品,例如细胞疗法Breyanzi。 据公司首席医疗官SamitHirawat透露,目前为止BMS已经停止或指定委外开发12个项目,包括其免疫疗法Yervoy的后续版本、SIRPα-和BET靶向药物,并将在今年剩余时间内继续审查其产品线。 吉利德,砍了10个项目 今年第一季度,吉利德终止了2个细胞疗法项目,分别为自体抗CD19CAR-T细胞疗法Brexucabtageneautoleucel(ZUMA-25)治疗罕见B细胞恶性肿瘤的2期试验和CLL-1(KITE-222)治疗复发难治性急性髓系白血病的1期试验。 此外,吉利德还将关于CD47单抗magrolimab的6项试验从管线中剔除,包括magrolimab联合疗法治疗头颈部鳞状细胞癌、三阴性乳腺癌、结直肠癌等多项实体瘤研究。Magrolimab是一种潜在的first-in-class抗CD47免疫疗法,由吉利德49亿美元收购FortySeven公司获得,但在进入后续临床开发后,却遭遇接连挫折。罗氏,砍掉6条管线 4月24日,据第一季报显示,罗氏在今年第一季度削减了六个项目,包括用于实体肿瘤的camonsertib和belvarafenib、用于结直肠癌的双特异性抗体RG6286、用于精神疾病的RG6163以及用于尿路感染的LepB抑制剂RG6319、camonsertib和治疗重症肌无力的Enspryng。 首席执行官Thomas Schinecker在与媒体进行的第一季度财报电话会议上表示,确定优先次序和不断重新分配是正常业务的一部分,确保公司拥有的资金其用于患者和公司的最佳用途,罗氏的目标是使其产品线中80%为最佳管线或一流资产。 辉瑞,放弃4个项目5月1日,辉瑞公布了2024年Q1财报,财报显示,在推进潜力产品的同时,辉瑞在第一季度适时放弃了4个项目:终止开发基因疗法VTX-810用于治疗Wilson病,目前处于I期阶段;终止开发CGRP受体拮抗剂zavegepant用于预防偏头痛发作,目前处于II期阶段; 终止开发S1P受体etrasimod用于治疗特应性皮炎和斑秃II期研究。诺华,移除了2个项目 4月23日,诺华发布2024Q1业绩;在研发管线上,通过对比诺华2024Q1与2023Q4财报中披露的管线发现,其进行了管线调整,移除了2个项目,包括CD73单抗NZV930项目和CSF-1R抑制剂sotuletinib。其中,NZV930是诺华从SurfaceOncology引进,此前已经有多个临床被终止。 赛诺菲,放弃部分适应症项目4月25日,赛诺菲发布2024Q1业绩;财报显示,赛诺菲在免疫学及神经学管线放弃了部分适应症项目,包括自免赛道的CD40L抗体Frexalimab在干燥综合征上的2期研究、RIPK1抑制剂Oditrasertib治疗肌萎缩性侧索硬化症(ALS)的2期研究、一项用于治疗罕见遗传性疾病GM2神经节脂质沉积症的分子Venglustat的2期研究。 阿斯利康,放弃几款早期药物 4月25日,据第一季报显示,阿斯利康将放弃几款早期药物,包括MEDI6570、AZD7503(ION455)、AZD5055。 MEDI6570是一款LOX-1靶向单克隆抗体,用于阻断LOX-1受体的多种配体。该资产正在进行一项名为GOLDILOX的2期临床试验,用于治疗心肌梗死后,但由于“战略投资组合优先”而停止。 AZD7503,该管线是阿斯利康从Ionis那里获得的配体偶联反义寡核苷酸(LICA)药物,旨在抑制17β-羟基类固醇脱氢酶13(HSD17B13)蛋白的产生,适应症选择的是非酒精性脂肪性肝炎。 AZD5055是一款口服Porcupine抑制剂,在进行特发性肺纤维化(IPF)和其他进行性纤维化的间质性肺疾病(ILDs)的1期试验。参考:企业公告 医药之梯推荐阅读:蒲公英Ouryao视频号投稿、广告、商务合作: Qinrenlvcha
临床1期临床2期
100 项与 Linclatamig 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 结直肠癌 | 临床1期 | 美国 | 2020-08-31 | |
| 结直肠癌 | 临床1期 | 澳大利亚 | 2020-08-31 | |
| 结直肠癌 | 临床1期 | 加拿大 | 2020-08-31 | |
| 结直肠癌 | 临床1期 | 西班牙 | 2020-08-31 | |
| 转移性结直肠癌 | 临床1期 | 美国 | 2020-08-31 | |
| 转移性结直肠癌 | 临床1期 | 澳大利亚 | 2020-08-31 | |
| 转移性结直肠癌 | 临床1期 | 加拿大 | 2020-08-31 | |
| 转移性结直肠癌 | 临床1期 | 西班牙 | 2020-08-31 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
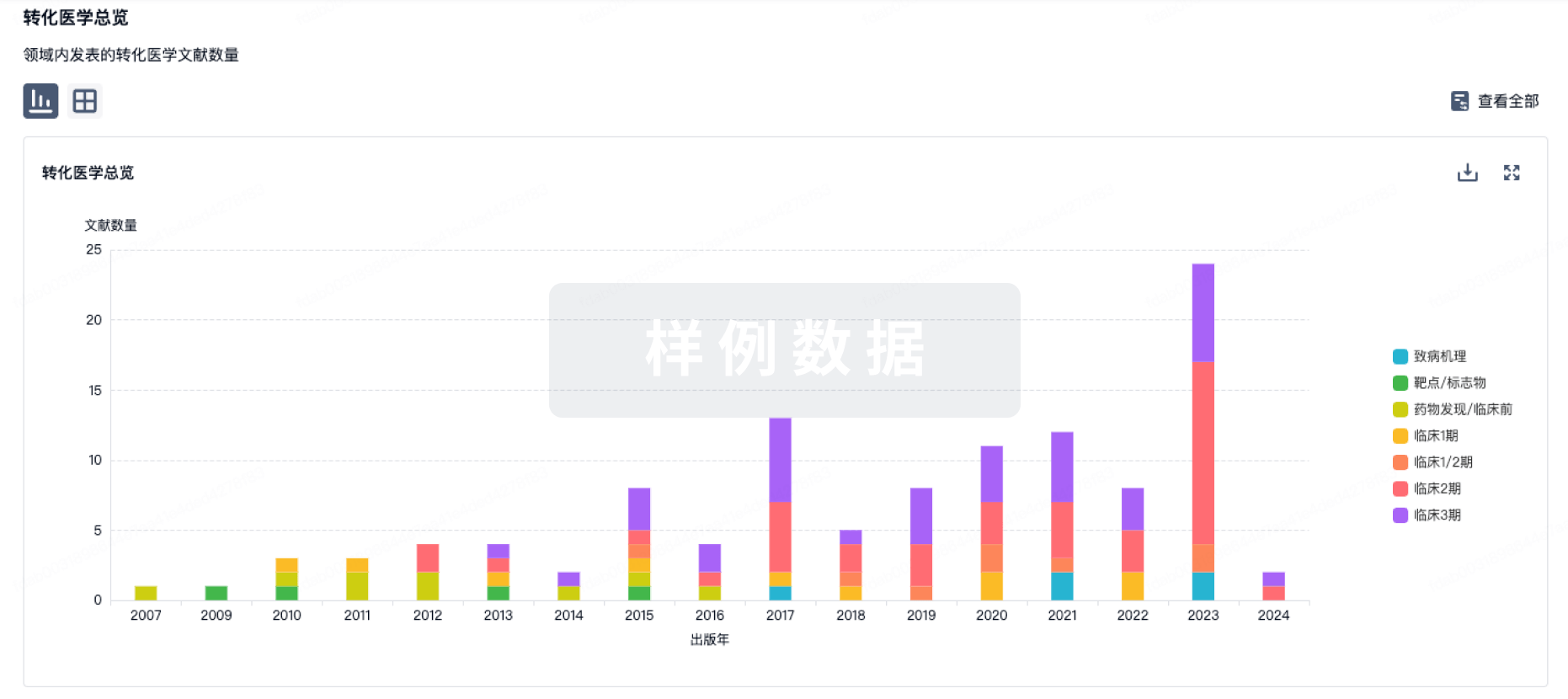
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
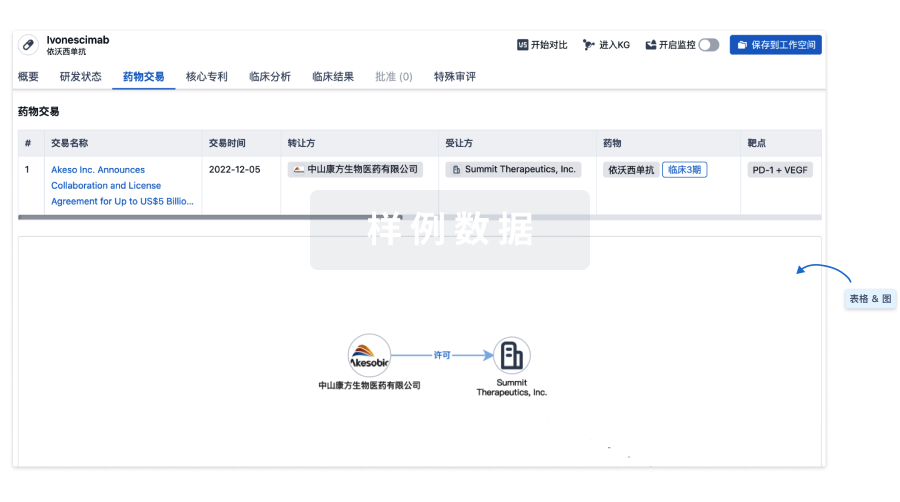
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
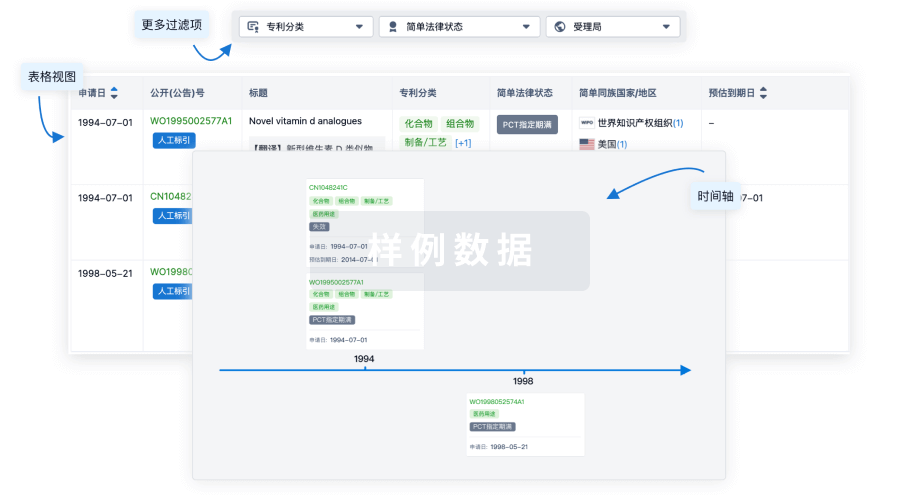
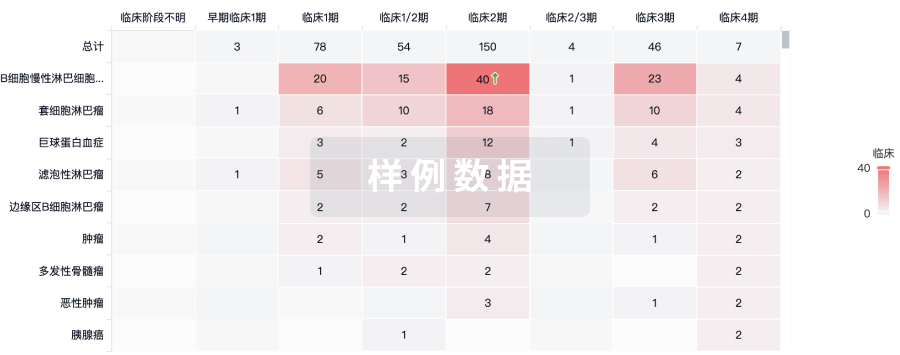
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
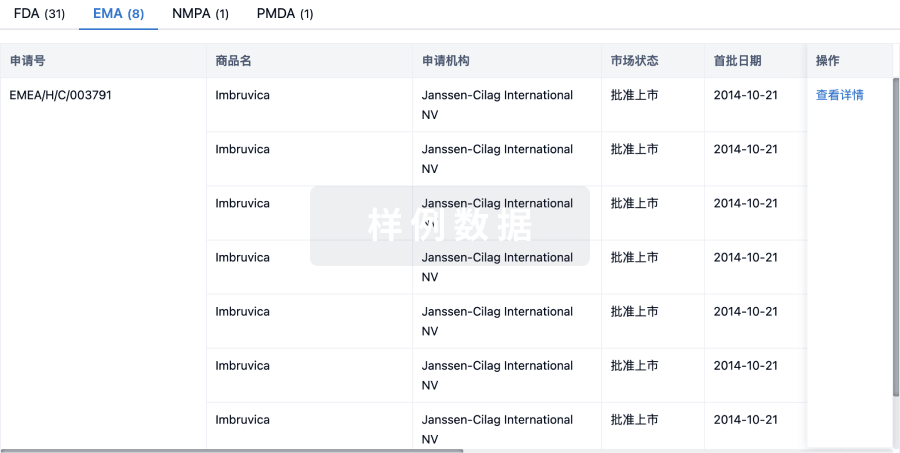
批准
利用最新的监管批准信息加速您的研究。
登录
或
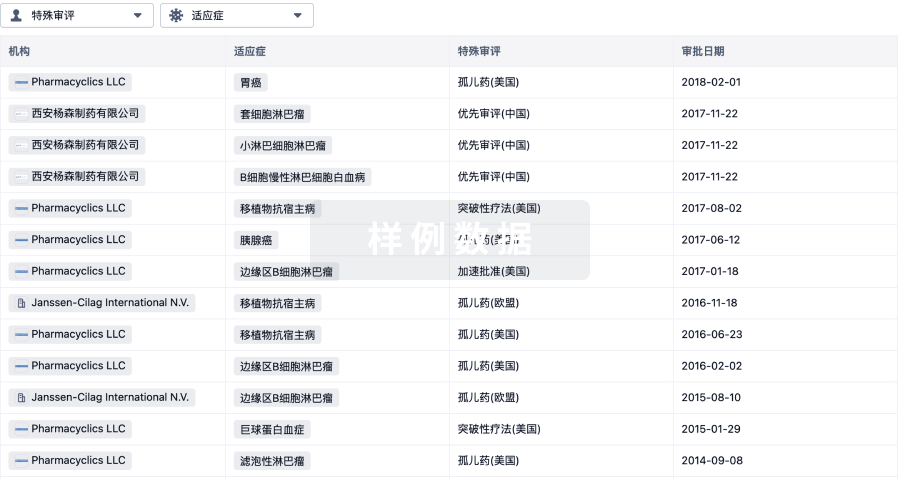
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用