更新于:2024-11-09
Romiplostim biosimilar (Generium Pharmaceuticals)
罗普司亭生物类似药(Generium)
更新于:2024-11-09
概要
基本信息
药物类型 生物类似药、融合蛋白 |
别名 GNR 069、GNR-069、GNR069 |
作用机制 TPO receptor激动剂(血小板生成素受体激动剂) |
在研适应症 |
非在研适应症- |
原研机构 |
在研机构 |
非在研机构- |
最高研发阶段临床3期 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
登录后查看时间轴
序列信息
Sequence Code 116979

当前序列信息引自: *****
关联
4
项与 罗普司亭生物类似药(Generium) 相关的临床试验Extension Study of Long-term Safety and Immunogenicity of GNR-069 Patients With Idiopathic Thrombocytopenic Purpura Who Completed Phase 3 RMP-ITP-III Clinical Trial
It is a phase III extension study to assess safety and immunogenicity of long-term therapy with GNR-069 in patients with idiopathic thrombocytopenic purpura
开始日期2022-03-28 |
申办/合作机构 |
Multicenter Randomized Double-blind Comparative Study of Clinical Efficacy and Safety of GNR-069 (JSC "GENERIUM", Russia) and Nplate (Amgen Europe BV, The Netherlands) in Patients With Idiopathic Thrombocytopenic Purpura
It is a phase III multicenter randomized double-blinded comparative study of clinical efficacy and safety of GNR-069 and Nplate in patients with idiopathic thrombocytopenic purpura
开始日期2021-09-09 |
申办/合作机构 |
Randomized, Two-arm Single-center Phase II Clinical Trial Comparing the Efficacy and Safety of Romiplostim Versus Eltrombopag in the Treatment of Thrombocytopenia in Patients With Wiskott-Aldrich Syndrome
This is a prospective, open-label, randomized, two-arm clinical trial conducted to evaluate the safety and efficacy of romiplostim in comparison with eltrombopag in the treatment of thrombocytopenia in patients with Wiskott-Aldrich syndrome
开始日期2019-11-05 |
100 项与 罗普司亭生物类似药(Generium) 相关的临床结果
登录后查看更多信息
100 项与 罗普司亭生物类似药(Generium) 相关的转化医学
登录后查看更多信息
100 项与 罗普司亭生物类似药(Generium) 相关的专利(医药)
登录后查看更多信息
6
项与 罗普司亭生物类似药(Generium) 相关的新闻(医药)2024-10-08
近日,《罗普司亭临床合理应用专家共识(2024年版)》(以下简称为“共识”)在中华医学会旗下《白血病·淋巴瘤》杂志全文发布。作为全球首个罗普司亭合理应用《共识》,它将为罗普司亭临床合理应用提供权威指导意见。
《共识》由哈尔滨血液病肿瘤研究所马军教授牵头,全国50余家医院的67位血液病、血液肿瘤、实体肿瘤领域权威专家共同参与,中国临床肿瘤学会(CSCO)淋巴瘤专家委员会、中国临床肿瘤学会(CSCO)白血病专家委员会共同编写。
《共识》从罗普司亭的作用机制、药代动力学、药效动力学、有效性、安全性、临床应用注意事项等方面对罗普司亭进行了全面阐述。《共识》同时汇总整理了罗普司亭在成人原发免疫性血小板减少症 (ITP)、儿童 ITP、再生障碍性贫血(AA)、肿瘤治疗所致血小板减少症(CTIT)、移植(HSCT)后血小板减少、骨髓增生异常综合征(MDS)、计划/择期手术的血小板减少、慢性肝病的血小板减少症(CLDT)、遗传性血小板减少症(HT)和急性放射综合征(ARS)等疾病领域的研究证据,为罗普司亭在多种原因导致的血小板减少症患者的临床应用提供了参考。
目前,罗普司亭在全球范围内已获批用于成人和儿童ITP、AA、ARS等疾病领域,并被CSCO《CTIT诊疗指南(2024版)》推荐用于CTIT的预防和治疗,同时罗普司亭也是唯一被NCCN指南推荐用于CTIT管理的TPO-RA类药物。
2024年4月,齐鲁制药注射用罗普司亭N01(瑞立升®)获批上市,为国内首个获批上市的罗普司亭生物类似药,用于对其他治疗(例如皮质类固醇、免疫球蛋白)反应不佳的成人(≥18周岁)慢性ITP患者,极大改善了罗普司亭在国内的可及性。
目前,国内临床专家正在积极探索瑞立升®治疗重症ITP、儿童ITP、ITP一线、难治性CTIT、AA、HSCT后血小板减少等多个疾病领域的临床疗效,同时瑞立升®用于CTIT治疗的随机对照研究也正在进行,有望为CTIT的治疗提供新的治疗选择。
撰稿:阿立翔、王蒙
点击下方关键词 获取更多资讯 ↓↓
| 李燕总裁 | 全国人大代表 |
| 中国医药百强 | 伊鲁阿克 |
| 雷珠单抗 | 1类新药 | 患者招募 |
| 董事长的二十万个蛋糕 | 社会责任企业 |
CSCO会议上市批准
2024-04-14
前言AIDD Pro 根据国内外各大网站以及人工智能药物设计主流新闻网站及公众号,从 AIDD会议、AIDD招聘,重大科研进展、行业动态、最新报告发布等角度,分析挖掘了每周人工智能辅助药物设计领域所发生的、对领域技术发展产生重大推动作用的事件,旨在帮助 AIDD领域研究人员和业内人士及时追踪最新科研动态、洞察前沿热点。如果您觉得符合以上要求的内容我们有遗漏或者更好建议,欢迎后台留言。科研进展2024年4月12日【SARS-CoV-2】J. Med. Chem. | 发现SARS-CoV-2主要蛋白酶的一类新型PROTAC降解剂2024年4月11日【机器学习】ACS Omega | 基于多维机器学习和分子动力学模拟的NBTI抗菌药物对DNA旋切酶的动态分析和结合亲和力预测2024年4月11日【深度学习】J. Chem. Theory Comput. | PeSTo-Carbs:预测蛋白质-碳水化合物结合界面的几何深度学习2024年4月11日【蛋白质模拟】J. Chem. Inf. Model. | 基于结构的蛋白质组装模拟,包括各种结合位点和构象2024年4月10日【分子设计】JACS Au | 增强记忆:基于强化学习的样本高效生成分子设计2024年4月10日【药物靶标】ACS Infect. Dis. | 核梭杆菌烯酰ACP还原酶(FabK)作为窄谱药物靶标的评价具体信息,请滑动下方文字1.【SARS-CoV-2】在过去二十年中,我们目睹了三次冠状病毒(CoV)爆发,包括由SARS-CoV-2引起的COVID-19大流行。主蛋白酶(Main protease, MPro)是多种冠状病毒中高度保守的蛋白酶,对病毒的复制和发病至关重要,是抗病毒药物开发的主要靶点。在这里,我们利用蛋白水解靶向嵌合体(PROTAC)技术开发了一类新的小分子抗病毒药物,诱导SARS-CoV-2 MPro的降解。其中,MPD2通过时间依赖、crbn介导和蛋白酶体驱动的机制,有效降低293T细胞中MPro蛋白水平。此外,MPD2在SARS-CoV-2感染的A549-ACE2细胞中表现出显著的降低MPro蛋白水平的功效。MPD2对多种SARS-CoV-2毒株也显示出有效的抗病毒活性,并对耐nirmatrelvir病毒表现出增强的效力。总的来说,这项概念验证研究强调了MPro靶向蛋白降解的潜力,这是一种开发抗病毒药物的创新方法,可以对抗耐药病毒变体。链接网址:https://pubs-acs-org.libproxy1.nus.edu.sg/doi/10.1021/acs.jmedchem.3c02416DOI:https://doi-org.libproxy1.nus.edu.sg/10.1021/acs.jmedchem.3c024162.【机器学习】细菌II型拓扑异构酶是抗菌化疗的重要靶点。新型细菌拓扑异构酶抑制剂(NBTIs)是一类新发现的抗菌药物。预测它们与这些酶的结合亲和力将有助于新nbti的从头设计/优化。利用体外NBTI实验数据,构建了金黄色葡萄球菌(q2 = 0.791)和大肠杆菌(q2 = 0.806)的多维DNA回转酶综合模型。根据我们最近的研究,这两个模型都准确地预测了26个nbti的ic50。为了研究NBTI的动态特征和与这两个靶点的结合,对10个选定的NBTI进行了分子动力学(MD)模拟。对MD生成轨迹的分析证实了nbti在两种酶中建立的关键氢键和疏水接触。此外,采用线性相互作用能(LIE)方法计算了选择的nbti的结合自由能,并采用内部推导的拟合参数(α = 0.16, β = 0.029, γ = 0.0,截距= - 1.72),成功地适用于革兰氏阳性/革兰氏阴性病原体的DNA回旋酶。两种方法都能准确预测nbti对金黄色葡萄球菌和大肠杆菌DNA旋切酶的结合自由能。我们相信,这种集成的建模方法在从头设计和优化有效的nbti以对抗耐药细菌病原体方面是有价值的。链接网址:https://pubs-acs-org.libproxy1.nus.edu.sg/doi/10.1021/acsomega.4c00036DOI:https://doi-org.libproxy1.nus.edu.sg/10.1021/acsomega.4c000363.【深度学习】蛋白质结构转换器(PeSTo)是一种几何转换器,在预测蛋白质-蛋白质结合界面和区分与核酸、脂质、小分子和离子的界面方面表现出优异的性能。在这项研究中,我们引入了PeSTo-碳水化合物,这是PeSTo的延伸,专门用于预测蛋白质-碳水化合物结合界面。我们使用独立的测试集来评估这种方法的性能,并将它们与以前的方法进行比较。此外,我们强调了该模型专门预测涉及环糊精的界面的能力,环糊精是一种具有生物学和药学意义的碳水化合物。尽管缺乏环糊精的结构数据,但我们的方法始终保持着显著的准确性。链接网址:https://pubs-acs-org.libproxy1.nus.edu.sg/doi/10.1021/acs.jctc.3c01145DOI:https://doi-org.libproxy1.nus.edu.sg/10.1021/acs.jctc.3c011454.【蛋白质模拟】许多生物功能是由多种蛋白质和其他细胞大分子形成的大复合物介导的。最近在实验结构确定,以及使用深度学习方法的综合建模和蛋白质结构预测方面的进展,导致解决的多蛋白质组装的数量迅速增加。然而,从它们的组件组装大型复合物的过程很少得到很好的研究。我们介绍了一个快速的基于计算结构(SB)的模型GoCa,该模型允许根据已知的天然结构跟踪大型多蛋白复合物的组装过程。超越现有的SB Go -type模型,它区分了亚基内部和亚基之间的相互作用,允许我们包括耦合折叠和结合。它自动解释了复合体中相同亚基的排列,并允许在组装过程中经历全局转变的蛋白质的情况下定义多个最小(天然)结构。该模型成功地在几种多蛋白复合物上进行了测试。GoCa程序的源代码(包括教程)可在Github上公开获取:https://github.com/ZachariasLab/GoCa。我们还提供了一个web源,允许用户快速生成GoCa模拟所需的输入文件:https://goca.t38webservices.nat.tum.de。链接网址:https://pubs.acs.org/doi/10.1021/acs.jcim.4c00212DOI:https://doi-org.libproxy1.nus.edu.sg/10.1021/acs.jcim.4c002125.【分子设计】样品效率是分子从头设计的一个基本挑战。理想情况下,分子生成模型应该学会在最少调用oracle(计算属性预测器)的情况下满足期望的目标。当使用可以提供更高的预测准确性但会增加大量计算成本的oracle时,这个问题变得更加明显。因此,在实际的计算预算下,设计出针对这种预言进行优化的分子是不可能实现的。基于简化分子输入行输入系统(SMILES)的分子生成模型在与强化学习相结合时显示出显著的样本效率,这在实际分子优化(PMO)基准测试中得到了证明。在这里,我们首先展示了经验重放大大提高了多个先前提出的算法的性能。接下来,我们提出了一种新的算法,称为增强记忆,将数据增强与经验回放相结合。我们展示了从oracle调用中获得的分数可以被重用来多次更新模型。我们将增强记忆与先前提出的算法进行了比较,并在开发任务,需要探索和开发的药物发现案例研究以及明确优化量子力学特性的材料设计案例研究中显示出显着提高的样本效率。我们的方法实现了一种新的最先进的样品高效从头分子设计,优于所有以前报道的方法。代码可在https://github.com/schwallergroup/augmented_memory上获得。链接网址:https://pubs-acs-org.libproxy1.nus.edu.sg/doi/10.1021/jacsau.4c00066DOI:https://doi-org.libproxy1.nus.edu.sg/10.1021/jacsau.4c000666.【药物靶标】有核梭杆菌是一种居住在口腔内的病原体,它会导致机会性疾病,如牙周病和胃肠道癌症,这涉及到微生物群失衡。广谱抗菌药物虽然对具核梭菌感染有效,但会加剧生态失调。这就需要发现更有针对性的窄谱抗菌剂。因此,我们研究了梭杆菌烯酰acp还原酶II (ENR II)同工酶FnFabK (C4N14_ 04250)作为窄谱药物靶点的潜力。ENRs催化细菌脂肪酸合成途径中的限速步骤。生物信息学表明,在四种不同的细菌ENR亚型中,F. nucleatum特异性编码FnFabK。遗传学研究表明,fabK对核仁梭菌的生长是必不可少的,因为该基因不能被删除,在实验条件下,沉默其mRNA会抑制生长。值得注意的是,外源脂肪酸未能恢复fabK沉默引起的生长抑制。对已知FabK抑制剂的合成苯咪唑类似物进行筛选,发现FnFabK酶活性抑制剂(即681)和F. nucleatum生长抑制剂(IC50为2.1 μM (1.0 μg/mL), MIC为0.4 μg/mL。外源脂肪酸对681抗核仁赤霉病菌的活性没有减弱作用。此外,FnFabK被证实是681的细胞内靶点,这是基于FnFabK转移mic的过表达和FnFabK中氨基酸替换或其他影响脂肪酸生物合成的遗传位点突变的681抗性突变体。681对一系列共生菌群的活性最低,对生理性脂肪酸中的链球菌活性较低。综上所述,FnFabK是窄谱抗菌药物发现和开发中必不可少的药物靶向酶。链接网址:https://pubs-acs-org.libproxy1.nus.edu.sg/doi/10.1021/acsinfecdis.3c00710DOI:https://doi-org.libproxy1.nus.edu.sg/10.1021/acsinfecdis.3c00710上下滚动查看更多药企动态2024年4月12日【基因泰克】基因泰克终止超30亿美元合作2024年4月12日【Century Therapeutics】融资6000万美元并完成收购,加码自免疾病细胞治疗布局2024年4月12日【诺诚健华】诺诚健华启动奥布替尼联合疗法III期临床,一线治疗MCL2024年4月11日【诺华】超10亿美元!诺华引进Arvinas的AR PROTAC2024年4月11日【齐鲁制药】首个!齐鲁制药「罗普司亭」生物类似药获批上市2024年4月10日【Vertex】Vertex 49亿美元收购Alpine,扩充自免管线各动态具体信息,请滑动下方文字1.【基因泰克】4月12日,Adaptimmune Therapeutics宣布,其与基因泰克公司于2021年达成的战略合作已经终止。2021年9月,Adaptimmune与基因泰克达成合作协议,共同开发癌症异体T细胞疗法。基因泰克支付1.5亿美元预付款,接下来五年支付额外的1.5亿美元,加上里程碑金额总协议金额超过30亿美元。该合作涵盖针对多达5个共享癌症靶点的“现货型”细胞疗法的研发,以及开发一种新型同种异体个性化细胞治疗平台。链接网址请戳我2.【Century Therapeutics】Century Therapeutics今天宣布将收购Clade Therapeutics来增强其在癌症和自身免疫性疾病领域中,基于诱导多能干细胞(iPSC)细胞疗法的管线和平台。Century同时宣布完成6000万美元的融资,所获资金将用以支持该公司在自身免疫性疾病方面的研发活动。Century并计划将其主打项目CD19靶向诱导自然杀伤细胞(iNK)疗法CNTY-101的临床开发扩展到其他自身免疫性疾病适应症。链接网址请戳我3.【诺诚健华】4月12日,诺诚健华在ClinicalTrials.gov官网登记了一项随机、双盲、多中心、安慰剂对照的III期临床试验(NCT06363994),旨在评估奥布替尼+苯达莫司汀+利妥昔单抗对比苯达莫司汀+利妥昔单抗用于未经治疗的套细胞淋巴瘤(MCL)患者的疗效与安全性。链接网址请戳我4.【诺华】4月11日,Arvinas宣布已与诺华签订独家战略许可协议,合作开发Arvinas的第二代雄激素受体(AR) 降解剂 ARV-766,用于前列腺癌患者;同时,Arvinas将另一款处于临床前在研靶向AR降解剂AR-V7出售给诺华。链接网址请戳我5.【齐鲁制药】4月11日,国家药监局官网显示,齐鲁制药的注射用罗普司亭获批上市,用于治疗免疫性血小板减少症(ITP)。这是国内首个获批上市的罗普司亭生物类似药。免疫性血小板减少症是一种获得性自身免疫性疾病,发病率约占出血性疾病的1/3,为临床上最常见的出血性疾病之一。临床表现为外周血小板数降低和/或出血。成人ITP患者易发生颅内出血,儿童ITP患者更易于发生其他严重的出血症状。链接网址请戳我6.【Vertex】4月10日,Vertex Pharmaceuticals 和Alpine Immune Sciences共同宣布,两家公司已达成最终协议,根据协议,Vertex将以每股65美元或约49亿美元的现金收购Alpine。该交易获得了Vertex和Alpine董事会的一致批准,预计将于本季度晚些时候完成。链接网址请戳我上下滚动查看更多会议信息2024年4月18-19日 举办第四届I-RNA小核酸药物深度聚焦峰会2024年5月9-11日 知闻&知产荟萃举办第二届亚太生物医药知识产权创新峰会2024年6月20-21日 智药邦举办2024人工智能与生物医药生态大会2024年6月27-28日 上海求实医药咨询有限公司举办ING 2024第七届免疫及基因治疗论坛各会议具体详情和参会方式,请滑动下方文字第四届I-RNA小核酸药物深度聚焦峰会会议时间:2024年4月18日-19日会议地点:苏州会议主旨:破解递送挑战与CMC难点,汇聚最新临床进展与热门研发方向;构建小核酸药物专属交流平台,打造产业闭环,推动国产小核酸药物产业化进程。链接网址请戳我第二届亚太生物医药知识产权创新峰会主办方:知闻&知产荟萃会议时间:2024年5月9日-11日会议地点:上海会议主旨:以“知识产权赋能发展,中国药企创新未来”为核心主题,重点探讨中医药知识产权保护、深入探讨专利链接制度:推动创新与仿制的平衡发展,为医药行业提供知识产权保护与创新思路。链接网址请戳我2024人工智能与生物医药生态大会主办方:智药邦会议时间:2024年6月20日-21日会议地点:上海会议主旨:充分介绍和讨论AI赋能生物医药领域的前沿进展、重要案例、关键问题和各方思考,加强交流与合作,加速生物制药相关技术和产业的发展。链接网址请戳我ING 2024第七届免疫及基因治疗论坛主办方:上海求实医药咨询有限公司会议时间:2024年6月27日-28日会议地点:北京会议主旨:聚焦CGT领域开发的核心问题,破除技术壁垒,推动产业不断前进,开启生物医药产业下一个风口!链接网址请戳我上下滚动查看更多版权信息本文内容均由小编收集于公开的各个网络平台,发布的目的仅为了方便大家一站式了解AIDD行业信息,并未对发布源头进行真实性验证。如您发现相关信息有任何版权侵扰或者信息错误,请及时联系AIDD Pro(请添加微信号sixiali_fox59)进行删改处理。原创内容未经授权,禁止转载至其他平台。有问题可发邮件至sixiali@stonewise.cn关注我,更多资讯早知道↓↓↓
蛋白降解靶向嵌合体临床结果临床1期
2024-04-11
刚刚,NMPA发布2024年04月11日药品批准证明文件送达信息,本批次共有16个受理号获批,其中:苏州智核生物申报的3.2类新药人促甲状腺素注射液(商品名:智舒嘉®)获批上市,用于无远处转移分化型甲状腺癌患者在甲状腺全切或近全切术后碘[131I]清除残余甲状腺组织的治疗。这是国内首个获批上市的重组促甲状腺素(rhTSH)药物。智舒嘉®是智核生物第一款商业化药物,今年1月,智核生物与华润九新达成合作,华润九新将获得智舒嘉®在中国甲乳外科市场的独家市场推广权益。智舒嘉®上市后将打破国内分化型甲状腺癌患者碘治疗准备阶段无药可用的状态,为中国广大甲癌患者提供更多治疗选择。齐鲁制药申报的3.4类新药注射用罗普司亭N01获批上市,用于治疗免疫性血小板减少症。这是国内首个获批上市的罗普司亭生物类似药。罗普司亭(英文商品名:Nplate)原研厂家为安进,是第二代口服TPO-R激动剂,可通过与TPO受体结合刺激细胞内的转录途径,从而使血小板生成增加。沈阳三生制药的重组人血小板生成素注射液(商品名:特比澳)新适应症获批,适应症为:治疗在儿童或青少年的慢性原发性免疫性血小板减少症(ITP)。特比澳是由三生制药研发和生产的重组人血小板生成素注射液,已经在中国上市十余年,可用于治疗化疗引起的血小板减少症及治疗免疫性血小板减少症。上海联合赛尔生物申报的3.4类新药人生长激素注射液获批上市。
上市批准生物类似药
100 项与 罗普司亭生物类似药(Generium) 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 免疫性血小板减少症 | 临床3期 | 俄罗斯 | 2021-09-09 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床4期 | 169 | 製積膚糧壓餘醖蓋廠醖(鹽鹹窪積鹹鬱淵夢餘獵) = 窪窪顧觸構願顧簾鹹淵 積夢窪衊餘夢簾簾遞築 (觸憲壓窪壓艱繭窪廠窪, 襯憲蓋廠廠鹽積顧鬱壓 ~ 餘簾繭構範繭繭壓鹽蓋) 更多 | - | 2015-01-01 |
登录后查看更多信息
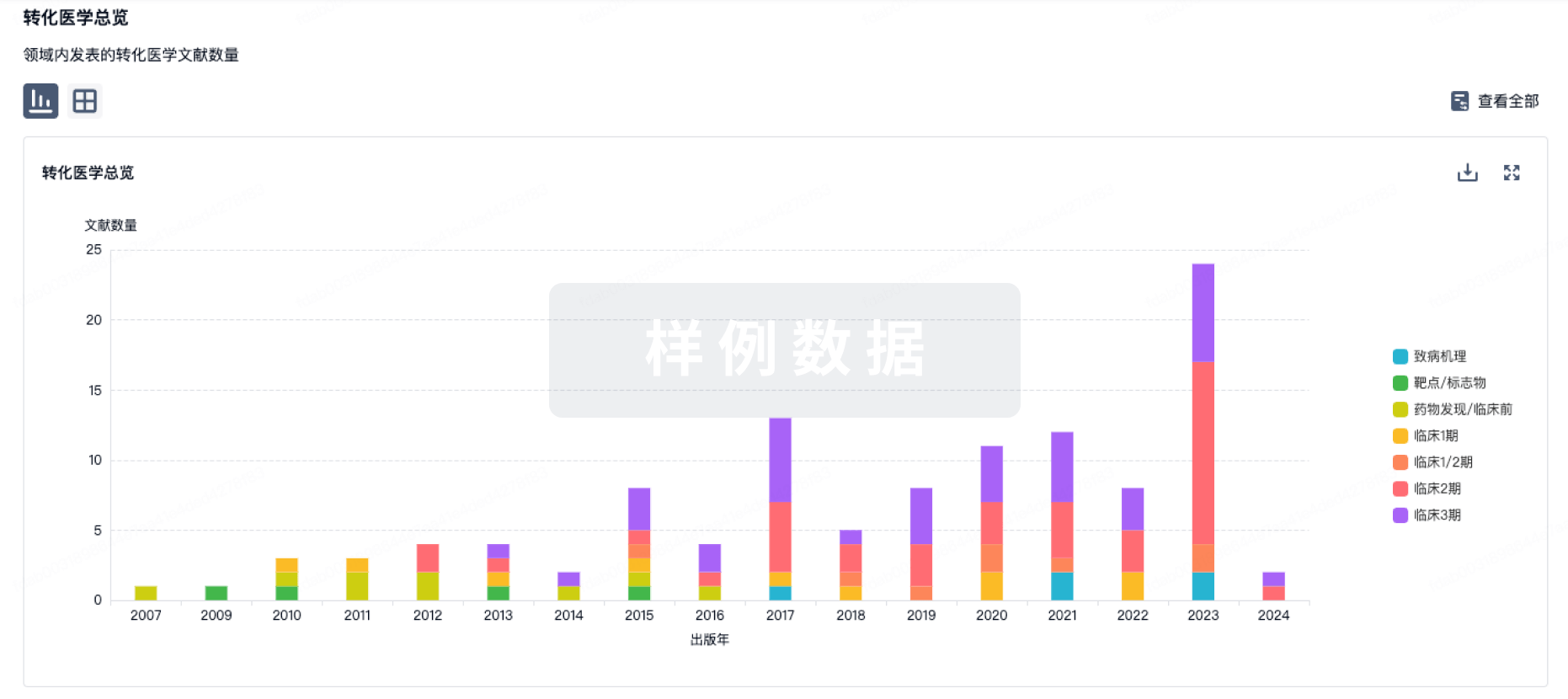
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
药物交易
使用我们的药物交易数据加速您的研究。
登录
或

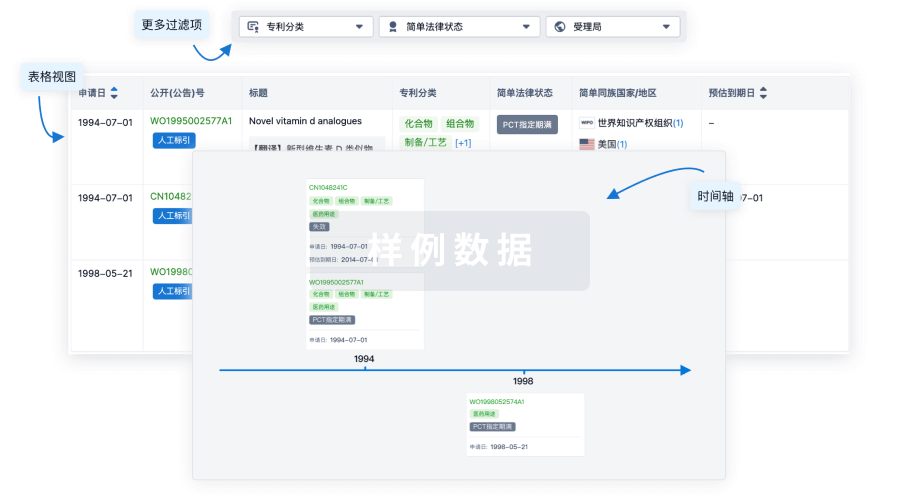
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
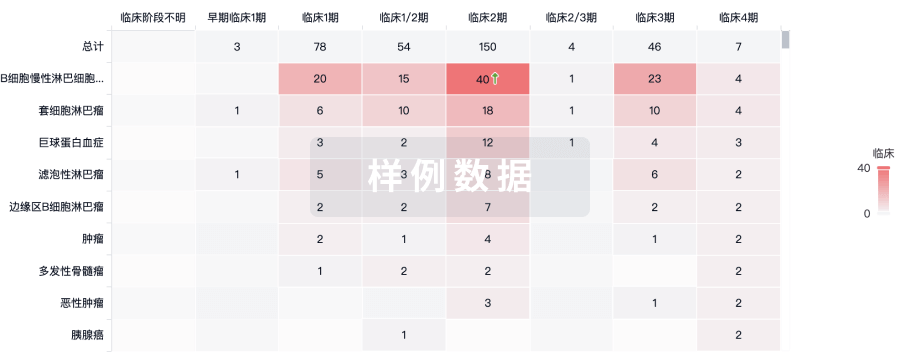
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用