更新于:2024-06-25
Ranibizumab biosimilar(Rubin Ltd)
雷珠单抗生物类似药(鲁宾有限公司)
更新于:2024-06-25
概要
基本信息
序列信息
Sequence Code 103170L

当前序列信息引自: *****
Sequence Code 143622H

当前序列信息引自: *****
关联
2
项与 雷珠单抗生物类似药(鲁宾有限公司) 相关的临床试验A Global, Phase III, Double Blind, Randomized Controlled Study to Compare the Efficacy, Safety & Immunogenicity of LUBT010 with Lucentis® in Patients with NeovascularAge-Related Macular Degeneration
开始日期2022-04-05 |
申办/合作机构- |
A Global, Phase III, Double Blind, Randomized Controlled Study to Compare the Efficacy, Safety & Immunogenicity of LUBT010 With Lucentis® in Patients With Neovascular Age Related Macular Degeneration
This study is designed to compare the efficacy, safety and immunogenicity of LUBT010 with Lucentis® given as once monthly intravitreal injection in patients with neovascular age-related macular degeneration (AMD).
开始日期2020-09-14 |
申办/合作机构 |
100 项与 雷珠单抗生物类似药(鲁宾有限公司) 相关的临床结果
登录后查看更多信息
100 项与 雷珠单抗生物类似药(鲁宾有限公司) 相关的转化医学
登录后查看更多信息
100 项与 雷珠单抗生物类似药(鲁宾有限公司) 相关的专利(医药)
登录后查看更多信息
2
项与 雷珠单抗生物类似药(鲁宾有限公司) 相关的新闻(医药)2024-03-10
·医药魔方
鸟鸣山跃石不转,寒日不见清风盼。乍暖还寒、最难将息的早春二月在渐行渐远的光阴流转间悄然而至,落日余晖映照下的一城山色半城湖在晚霞的交织下略显孤寂,比之往昔少了些喧嚣、添了抹静谧。春意未浓、冬雪犹在、几分凋零、些许黯然。浮生观澜,恍如一梦,愿诗与远方均不再遥远,乘风归去来兮,繁花片片落满地。整体概况2023年全球生物药市场规模达到了5600亿美元,占到了全球医药整体市场的39%,预计将在五年后的2028年突破8000亿美元,进一步将份额提升至40%以上。近年来以欧美为首的的全球生物类似药市场规模不断扩大,对于生物类似药的当下和未来,多家研究机构就发展速度和规模给出了自己的预测,虽然数字不尽相同,但均异曲同工的肯定了持续稳定发展的大趋势,未来增速相比此前的预计有所放缓。不同机构的全球生物类似药市场规模与增速预测2023年全球销售额TOP100药品中,以单抗为代表的生物大分子药物数量达到了一半。除去疫苗产品外,2023年全球销售额TOP20生物产品均为单抗和抗体融合蛋白。入围门槛进一步提高,各产品全球销售额均在37亿美元以上,其中一半的产品全球收入在50亿美元以上,5个产品突破了百亿大关,K药十年磨一剑接力Humira登顶药王宝座。销售额增幅最大的瑞莎珠单抗Skyrizi和度伐利尤单抗Imfinzi增长均超过了50%,走下神坛的阿达木单抗Humira降幅达到了32%。美国市场处于绝对核心地位,TOP20中95%的产品美国市场收入在全球销售额中的占比在50%以上。产品主要分布在抗肿瘤和自体免疫领域,除奥瑞珠单抗和瑞莎珠单抗外的其他18个产品均已登陆中国市场。75%的产品在2010年及之后获批,其中获批时间最早的依那西普距今已有25年,凭借美国市场潜水艇专利对生物类似药的限制依然年年上榜,获批最晚的瑞莎珠单抗距今不到5年。2023年全球销售额TOP20生物药原研产品(非疫苗类)2023年美国医药市场整体规模再创新高、突破了7000亿美元,以48%的占比继续领跑全球,蓬勃发展的生物药品在整体销售额中的占比达到了51%,IQVIA预计将在2032年达到5800亿美元的规模,份额占比增长至56%。2023年美国市场生物类似药销售收入在上年增速已经放缓的基础之上出现了小幅下滑,最终交出了72.5亿美元的答卷,究其原因一方面在于半数以上的之前已获批产品在竞争日渐加剧的大背景下的价格持续下滑部分抵消了生物类似药不断渗透带来的增量正效应,另一方面部分产品的市场经过几年的洗牌在销量规模上已经日趋平衡,增幅比较有限,同时以曲妥珠单抗为代表的个别分子在其他同类创新药不断涌现下出现了连续萎缩,加之以阿达木单抗领衔的新上市产品的表现低于预期,对整体销售额的带动相对比较有限,各因素叠加共同造成了连续增长之后的首次下滑。过去的一年里,经历了漫长等待的阿达木单抗生物类似药集体上市,革命尚未成功的背后依然可以感受到那股虽千万人吾往矣的不屈力量;那他珠单抗、托珠单抗和乌司奴单抗三个分子的首个生物类似药顺利获批,带动获批分子总数量增加至14个;非格司亭和贝伐珠单抗两个分子的生物类似药份额逼近85%,不断刷新着象征着生物类似药荣光的崭新纪录;乌司奴单抗等一系列新产品顺利实现与原研的和解,开启了提前上市的加速模式。前路依然漫长,但这充满暖意的一幕幕还是给这个难忘的寒冬带来了无尽的希望。获批&上市2023年共有5个生物类似药产品获批,产品共涉及阿达木单抗等5个分子以及Celltrion等5家公司,其中那他珠单抗、托珠单抗和乌司奴单抗均为首个生物类似药获批。Amgen的Wezlana在获批的同时被授予可互换资格,成为史上第7个以及2023年第3个获此殊荣的生物类似药;Celltrion和Sandoz均以累计5个的生物类似药产品获批数量上升至并列第三位;百奥泰自研的托珠单抗和贝伐珠单抗生物类似药相继获批,实现了中国力量在美国生物类似药领域的历史性突破。2023年美国生物类似药获批一览从获批位次看,Celltrion的Yuflyma成为第9个获批的阿达木单抗生物类似药,Avzivi成为第5个获批的贝伐珠单抗生物类似药,Tyruko、Tofidence和Wezlana三个产品均为各自所属分子获批的首个生物类似药产品。从审评时长看,百奥泰的Avzivi和Celltrion的Yuflyma分别达到了1104天和910天,打破了贝伐珠单抗和阿达木单抗两大分子此前全部生物类似药在一个审评周期内获批的记录,Yuflyma由于原液生产场地的现场检查问题经历了两次CR回复后才最终获批;Tyruko由于涉及REMS的方案变更被认定为重大变更,导致审评时间延期3个月后获批;Tofidence和Wezlana两个产品均在一个审评周期内获批。截至目前,聚乙二醇化非格司亭生物类似药以738天的平均审评时长位列榜首,平均审评时长分布在500-550天的依那西普、曲妥珠单抗和贝伐珠单抗生物类似药紧随其后,雷珠单抗、甘精胰岛素以及新获批的托珠单抗和乌司奴单抗四个分子的生物类似药目前保持着一个审评周期获批的最短审评时长。由Amneal在售的非格司亭生物类似药Releuko依旧以1693天保持着单品最长审评时间的历史记录,Sandoz的聚乙二醇化非格司亭生物类似药Ziextenzo和Pfizer的阿法依伯汀生物类似药Retacrit分别以1530天和1246天的审评时长位居历史第二和第三位。从上市情况看,2023年共有13个生物类似药上市,打破了2019年7个新产品上市的历史记录,其中阿达木单抗生物类似药上市数量达到了9个,聚乙二醇化非格司亭共有Avsola和Fylnetra两个产品上市,甘精胰岛素和贝伐珠单抗各有1个生物类似药产品上市。所有上市产品中仅有Yuflyma一个2023年新获批产品,从获批到上市仅历时40天,其余产品自获批后均经历了不同时间的等待,阿达木单抗生物类似药的平均等待时长为1216天,其中时间间隔最久的阿达木单抗首仿产品Amjevita达到了2321天。2023年美国生物类似药上市一览从申报数量看,2023财年共有19个生物类似药BLA首次向FDA申报,打破了2017财年14个生物类似药BLA申报的历史记录,随着后续以地舒单抗为代表的新一代生物类似药进入集中申报期,这一记录仍有望在短期内被持续刷新。截至目前,将今年2月刚刚获批的阿达木单抗生物类似药Simlandi囊括在内,美国以351(K)途径申报的生物类似药获批总数量和上市数量已经分别达到了46个和38个。从产品类型看,共涉及维持治疗、抗肿瘤、自体免疫、胰岛素和眼科五大领域的14个分子,其中数量最多的阿达木单抗共有10个生物类似药获批,其中9个已经上市,成为当下竞争最为激烈的产品,数量最少的阿法依泊汀只有1个生物类似药获批并上市。从公司看,共涉及包括了原研创新型、专注研发型以及大型仿制药公司在内的14家公司,其中Pfizer以8个产品获批和7个产品上市的双第一战绩独占鳌头。曲妥珠单抗等7个分子实现了全部获批生物类似药均已上市,获批未上市的8个生物类似药有5个受限于专利,其余则主要因为商业化策略暂未上市或放弃上市。渗透&价格美国市场生物类似药在过去的2023年里进一步加速渗透,2022年在售的9个分子的生物类似药整体份额在2023年均取得了不同程度的增长,但增速已经明显放缓,回扣和报销制度中存在的固有顽疾依然制约着生物类似药发展的速度和可持续性,特别是在非抗肿瘤产品领域中表现的愈发突出,重磅产品阿达木单抗生物类似药去年的集体上市与万众期待的宏伟目标相差甚远,低价本身在生物类似药领域竞争中的决定作用与小分子化药相比存在着天壤之比,很难做到一低定乾坤。流通渠道中PBM等核心参与方在目录制定等重要环节的开放程度相对比较有限,无法在充分公平竞争的条件下将所有生物类似药囊括其中,医生在开具处方环节中很多时候受限于报销体系本身以及出于安全性风险的考虑偏重求稳的态度对开具生物类似药的积极性并不高,流通环节中的参与方处于各自利益的考虑无法形成合力,制度本身的变革和教育推广的力度等多个方面的努力仍然需要在未来不断加深,生物类似药的发展之路在经历了冲破初期阻碍实现破冰之后的全面突围仍需时日。前路漫漫,但生物类似药在美国医药支出节省方面取得的持续性成绩依然值得欣喜,根据AAM报道,2022年涉及八大分子的全部生物类似药节省医药支出达到了94亿美元,历史累计节省支出达到了236美元。美国生物类似药历年节省医药费用一览美国各分子生物类似药平均价格及原研品历年价格变化一览从具体数字看,拥有生物类似药在市销售三年以上的7个分子的生物类似药2023年整体销量份额均在40%以上,其中贝伐珠单抗和非格司亭两个分子的生物类似药的占比已经逼近85%,进一步刷新着历史最高份额记录;10个有生物类似药在售的分子中,有7个在市生物类似药数量的企业在3家及以上,阿达木单抗生物类似药在售单品数量达到了9个,打破了去年曲妥珠单抗5家竞争的最大数量记录。2022年新上市的雷珠单抗生物类似药在去年将整体份额提升了26%,成为了2023年渗透幅度增长最大的产品;聚乙二醇化非格司亭和阿法依伯汀两个分子的原研产品通过采用跟进生物类似药同步降价的策略最大程度上限制了生物类似药竞争对手的上量,两个分子生物类似药的2023年整体销量份额被限制在42%,增幅均未超过1%,成为了2023年渗透最慢的产品。从具体单品份额看,美国首个生物类似药Zarxio以58%的份额排名榜首,贝伐珠单抗和阿法依伯汀两个分子的首仿产品Mvasi和Retacrit以46%和42%的份额紧随其后;2023年新上市的阿达木单抗生物类似药整体销量份额不足2%,表现大大低于预期;10个分子份额排名榜首的10个生物类似药中,有8个为首仿产品,雷珠单抗的首仿产品Byooviz和利妥昔单抗的首仿产品Truxima成为唯二没有借助最早上市的优势登顶各自生物类似药份额榜首的产品;阿达木单抗的首仿产品Amjevita以1.4%的份额排名全部首仿产品末尾。2018-2023美国市场在市销售各分子生物类似药销量份额变化一览严冬大背景下的降价潮在过去的一年里愈发激烈,多个产品相比上年的ASP价格降幅超过了50%,降幅较大的产品主要集中在各分子目前市场份额较高的生物类似药中,其中曲妥珠单抗首仿产品Kanjiti的降幅达到了77%,成为了过去一年里降幅最大的单品;与当前个分子原研产品相比,曲妥珠单抗和利妥昔单抗两个分子的当前最低生物类似药ASP价格(平均销售价格)已经跌破20%,阿法依泊汀和雷珠单抗两个低竞争产品的比率保持在85%以上;7个分子当前最低生物类似药产品ASP价格相比于生物类似药上市之前的原研品价格降幅在35%-95%之间,6个产品的降幅超过了75%,排除掉去年刚有生物类似药上市的阿达木单抗,当前拥有在市生物类似药产品数量最多的聚乙二醇化非格司亭的价格降幅最大,达到了94%,2022年上市的雷珠单抗产品降幅最小,仅有35%。从原研自身价格变化来看,生物类似药上市之前ASP价格平均增幅最大的聚乙二醇化非格司亭原研产品Neulasta在生物类似药进入后不断疯狂跟进,以63%的降幅蝉联原研品降价冠军,雷珠单抗原研产品Lucentis以21%的降幅紧随其后,其余原研产品降幅均未超过10%,其中贝伐珠单抗原研产品Avastin和阿法依泊汀原研产品Epogen/Procrit价格为正增长;目前已经稳定占据近60%市场份额的非格司亭首仿产品Zaxio成为了生物类似药中屈指可数的在过去一年涨价的产品,增幅达到了11%。总体来看,对于具体生物类似药单品而言,进入市场的位次和之后的总体竞争程度共同决定了其发展的高度, 在流通渠道各环节中首先被覆盖从而占据一席之地基础上的低价策略才是有意义的。比之小分子产品,个体生物类似药在起点落后的情况下依靠后天逆天改命的难度要大很多,如果再遇上个像Amgen一样对自己更狠的原研,逆袭几乎没有可能。美国生物类似药涉产品价格变化一览策略&管线生物类似药的围城之殇在过去的一年里依然在延续,总体来看针对美国市场的生物类似药研发热度依然保持在较高的水平上,FDA 2023年公布的生物类似药研发计划中包括的生物类似药项目依然保持在100个以上,涉及的分子突破了50个。面临着生物类似药市场的新形势,在自身利益最大化的目标下,各家公司在结合实际情况明确了调整策略的基础上在过去的2023年里进一步付诸于目标引领下具体操作的执行。随着阿达木单抗生物类似药Abrilada在2023年的上市,Pfizer在美国市场的生物类似药在售数量达到了7个,继续在获批和上市数量上双榜领跑的同时也宣告了其美国市场生物类似药的商业化前工作的收关。受限于Comirnaty和Paxlovid两大新冠产品收入的下滑,Pfizer的2023年全球销售额相比上年大降41%,公布的5个美国市场生物类似药销售额(11.2亿美元)相比上年也下滑了26%,寄望于通过收购Seagen布局ADC领域产品等措施力挽狂澜,最新公布的研发管线中项目数量达到了112个,其中已不见生物类似药的踪影,近60%涉及新分子实体产品,无法一剑定乾坤的生物类似药之于急于扭转颓势的宇宙大药厂终究只是匆匆过客。Biocon于去年9月正式完成了Viatris美国市场生物类似药业务的交接和整合工作,人员数量增加到150人以上,打通了此前在以欧美为代表的法规市场所不具备的药政、供应链和商业化环节,具备了生物类似药从研发到销售的垂直一体化实力,实现了从幕后走上台前的角色转变。Biocon与Viatris前身之一的Mylan于2009年起以单抗产品起步开始合作生物类似药产品,随后在2013年进一步将合作拓展到胰岛素产品领域,双方合作在美实现了曲妥珠单抗、聚乙二醇化非格司亭和甘精胰岛素三个分子的生物类似药的首家获批(后两者同时为首家上市),目前聚乙二醇化非格司亭生物类似药Fulphila和甘精胰岛素生物类似药Semglee分别以16%和12%的份额排名各自分子的生物类似药份额首位。此次交易的总金额达到了33.35亿美元,双方各取所需,Viatris剥离掉生物类似药以后也向着全球瘦身计划的完成更进一步。Biocon包括已获批产品在内的全球生物类似药管线产品总数量达到了20个(包括了8个未披露名称的早期项目),针对美国市场的门冬胰岛素和贝伐珠单抗等四个产品已经处于FDA审评过程中,随着2022年马来西亚场地FDA审计问题的解决,2024年有望迎来新产品的获批,后续的地舒单抗等三个新项目已经处于III期临床中。完成交接后的Biocon在美国市场生物类似药策略上也开始从此前的自研自产逐步向自研与外部引进相结合的混合业务模式开始转变。Sandoz于去年10月正式从诺华剥离,向着成为小分子仿制药和生物类似药全球领导者的目标独立前行,虽然在五年的过渡期内仍将以签订服务协议的形式由Novartis提供生物类似药研发和生产的相关资源,但Sandoz在分拆之前已经开始着手通过投资自建生产和研发设施并展开了一系列相关外部合作进行补强。首先在去年3月决定投资4亿美元在斯洛文尼亚伦达瓦兴建一处厂房设施用于生物类似药的生产,预计可于2026年投产,随后在5月与Just-Evotec Biologics达成合作,依靠其研发和生产平台丰富Sandoz自身的生物类似药产品管线及生产设施建设,将管线产品数量提升至24个,7月宣布将在斯洛文尼亚卢布尔雅那进一步投资9000万美元用于其生物类似药技术研发中心的建设,11月在德国霍尔茨基兴启动了一处投资2500万欧元的新的生物类似药研发中心,一系列组合拳的打出为其日后独立进行生物类似药的研发和生产打下了坚实的基础。在合作方面,Sandoz在此前与Polpharma、EirGenix、Bio-Thera和Gan&Lee等多家外部公司进行合作的基础上于去年9月与Samsung Bioepis就乌司奴单抗生物类似药达成合作,随后又在今年1月宣布以1.7亿美元的首付款将Coherus的雷珠单抗生物类似药Cimerli收入麾下,在阿柏西普即将申报的基础上进一步补强了自己的眼科产品管线。已公布的Sandoz 2023年全球生物类似药销售额达到了15.92亿美元(+10%),预计全年将突破20亿美元,目前其在美国市场共有三个产品在售,其中非格司亭生物类似药Zarxio作为美国市场首个生物类似药产品不断延续着上市以来的良好表现,当前销量份额已接近60%;聚乙二醇化非格司亭注射液生物类似药Ziextenzo在去年下半年出现了较大的销量下滑,丢掉了去年生物类似药的榜首位置,2023年新上市的阿达木单抗生物类似药Hyrimoz同时被Express Scripts、Optum/United和CVS Caremark三大PBM目录所覆盖,在激烈的竞争中占据了有利的位置,另外两个获批的依那西普生物类似药Erelzi和那他珠单抗生物类似药Tyruko限于专利暂未上市,后者有望于今年上半年冒险上市;其与百奥泰合作的贝伐珠单抗生物类似药Avzivi以于去年12月获批,预计最快将于今年实现上市。在研产品管线中,地舒单抗等6个产品已经处于FDA审评阶段,有望于今年获批,阿柏西普预计将于今年完成申报。Teva的生物类似药策略比较明晰,力争在以外部合作为主导结合少量自研的开发模式下将产品管线数量提升至20个,目前Teva研发费用的20%用于生物类似药,计划在未来三年中逐步将这一比例降至接近10%,从而将更多的投入用于创新药的研发,将目前40%的投入比例提升至60%-80%。Teva当前处于审评和在研阶段生物类似药产品共有16个,其中7个为自研,另外9个来自于合作伙伴Alvotech,双方于2020年建立了针对美国市场的生物类似药合作联盟,合作产品从最初的5个逐步扩展至如今的9个,遗憾的是双方合作的乌司奴单抗和阿达木单抗两个已申报生物类似药产品在产品本身没有问题的情况下受限于Alvotech位于雷克雅未克场地的FDA检查缺陷问题未能如期获批,本来有望首个获批高浓度规格并授予可互换资格的阿达木单抗生物类似药因此也错失了去年生物类似药集中进入市场的时机。Teva的全球销售额在经历了自2018年开始的连续5年下滑后终于在2023年以158亿美元(+10%)的战绩实现了正增长,其中包括与Celltrion合作的曲妥珠单抗Herzuma和利妥昔单抗Truxima两个生物类似药在内的美国仿制药产品模块总收入为34.75亿美元(-2%),前者以不足2%的市场份额位列五家曲妥珠单抗生物类似药的末尾,后者以30%的份额位列三家利妥昔单抗生物类似药的第二位。目前除了两个处于FDA审评阶段的生物类似药以外,自研的奥马珠单抗以及与Alvotech合作的阿柏西普和格列木单抗三个产品处于III期临床阶段,自研的地舒单抗已经顺利完成了III期临床试验,未来Teva将在目前与Alvotech合作的基础上进一步寻求其他外部伙伴的合作。在完成了美国小分子化药市场自售的试水后,作为美国生物类似药市场先驱之一的Celltrion生物类似药的销售体系于去年顺利搭建完成并于4月份上市了首个自售产品贝伐珠单抗生物类似药Vegzelma,随后又在7月初上市了阿达木单抗生物类似药Yuflyma(2024年1月进一步上市了80mg/0.8ml的高浓度规格产品),加上目前由Pfizer销售的英夫利昔单抗生物类似药Inflectra以及由Teva销售的利妥昔单抗生物类似药Truxima和曲妥珠单抗生物类似药Herzuma,Celltrion已经实现了全部已获批的5个生物类似药产品的上市,在数量上仅次于排名首位的Pfizer,其中英夫利昔单抗的皮下注射版本生物类似药已于去年10月获批,将由Celltrion以ZYMFENTRA的商品名自售,Pfizer将继续销售静脉注射版本产品。与Biocon一样,Celltrion在具备了商业化销售能力后也实现了研产报销一条龙,不同之处在于Biocon的销售团队主要来自于此前Viatris的已有原班人马,Celltrion的销售团队经历了新建的过程,在Amgen、Pfizer和Coherus工作过的Thomas Nusbickel 于今年2月初被任命为Celltrion美国子公司的CCO负责生物类似药的商业化相关工作。Celltrion目前共有地舒单抗、乌司奴单抗、阿柏西普以及托珠单抗四个产品处于FDA审评过程中,奥马珠单抗已经完成III期临床试验,奥瑞珠单抗单抗处于III期临床试验中。Samsung Biologics在将与Biogen的合资公司Samsung Bioepis变为自家独有后又被传出将进一步收购Biogen的生物类似药业务,双方的合作始于2012年Samsung Bioepis的建立,目前Biogen在退出合资公司后依然将负责Samsung Bioepis当前在美国市场在售的雷珠单抗注射液生物类似药Byooviz以及未来新产品阿柏西普的商业化工作。Samsung Bioepis去年在此前与Organon和Biogen在美国市场进行生物类似药合作的基础上增加了Sandoz这一新的合作伙伴,目前其在美国市场共有5个生物类似药产品获批,除去因专利无法上市的依那西普外,与Organon合作的英夫利昔单抗、曲妥珠单抗以及阿达木单抗三个产品生物类似药连同和Biogen合作的雷珠单抗注射液生物类似药Byooviz均已上市,销售情况并不尽如人意,四个产品的2023年份额均未超过10%。目前管线中的贝伐珠单抗、乌司奴单抗和阿柏西普三个生物类似药产品已经处于FDA审评阶段,地舒单抗和依库珠单抗两个生物类似药产品已经完成了III期临床试验,帕博利珠单抗的生物类似药的I期临床试验也已经于今年1月份正式启动。随着未来战略重心将集中在肿瘤产品领域,Coherus于今年1月份将非核心产品雷珠单抗生物类似药Cimerli的美国市场权益转让给Sandoz,去年上市的阿达木单抗生物类似药同样被界定为非核心产品,另一个目前在售的聚乙二醇化非格司亭生物类似药Udenyca是其当下最为重要的核心生物类似药产品,随着Udenyca自动注射器版本产品在去年年底的增补获批,有望在近年带动该产品整体销量的增长其未来产品管线将更多的集中在创新药领域。作为生物类似药界的另类存在,Amgen在过去的一年里依然延续着自己的双面人生,作为地舒单抗等多个分子的原研产品和阿达木单抗等多个分子的首仿产品与对手们上演着一出出攻防大战。目前Amgen在美获批生物类似药数量已经达到了6个,仅次于Pfizer的7个,除去年刚刚获批的乌司奴单抗限于专利暂未上市(和解日期为2025年1月)外,其余5个产品均已上市,其中年报中公布的Mvasi和Kanjiti两个生物类似药产品的美国市场销售额分别为5.11亿美元(-15%)和1.09亿美元(-59%),去年首仿上市的阿达木单抗生物类似药产品Amjevita取得了1.26亿美元的收入。目前生物类似药研发管线中的依库珠单抗和阿柏西普生物类似药处于FDA审评中,已披露的临床阶段的产品仅剩了纳武利尤单抗。Amneal在去年成功完成了聚乙二醇化非格司亭生物类似药Fylnetra的上市,将美国市场在售生物类似药产品数量增加至3个,目前均面临多个竞争对手的局面,在均为最晚入市的情况下当前份额均比较惨淡,在研管线中新增加了与mAbxience合作的地舒单抗,目前处于III期临床试验阶段。Fresenius的聚乙二醇化非格司亭生物类似药Stimufend和阿达木单抗生物类似药Idacio均在去年上市,目前在研管线中的妥珠单抗、利妥昔单抗和乌司奴单抗三个生物类似药产品均已处于FDA审评阶段,地舒单抗生物类似药也已经完成了III期临床试验;Hikma的地舒单抗和乌司奴单抗两个生物类似药产品均已完成III期临床试验,管线中暂时没有披露的新产品加入;Lupin处于FDA审评中的聚乙二醇化非格司亭生物类似药仍未获批,雷珠单抗已经完成了III期临床试验。中国军团中百奥泰的贝伐珠单抗和托珠单抗两个生物类似药产品已经获批,复宏汉霖的曲妥珠单抗生物类似药、甘李的甘精、门冬、赖脯三大胰岛素生物类似药均已处于FDA审评阶段,健友与通化东宝也在去年9月达成了合作协议,双方将在未来针对美国市场开发前述三大胰岛素的生物类似药产品。总体来看,上述各家公司的在审产品中包含了多个美国市场已有生物类似药上市的老分子产品,这些产品申报时间相对较早但限于自身问题尚未获批,例如于2019年申报的Samsung Bioepis的贝伐珠单抗生物类似药和2021年申报的Lupin的聚乙二醇化非格司亭生物类似药;近几年内即将有生物类似药登陆市场的重磅分子产品已有多家申报,例如已有Amgen、Samsung Bioepis、Celltrion和Biocon申报的阿柏西普以及Celltrion和Sandoz已经申报的地舒单抗;处于III期临床中的产品除了阿柏西普、地舒单抗以及乌司奴单抗三大重磅产品的生物类似药外,也包括了奥马珠单抗、戈利木单抗和帕妥珠单抗等竞争相对缓和的生物类似药产品。从重叠度来看,地舒单抗一枝独秀,几乎出现了在了全部上述主要公司的产品清单上,该产品的2023年全球销售额达到了66亿美元,预计未来将出现与阿达木单抗相似的十家以上竞争的白热化场面,Amgen目前仍在针对该产品积极防御。针对后续第四波重磅产品的生物类似药研发进展也逐渐浮出水面,以新晋药王帕博利珠单抗为例,Samsung Bioepis已于今年1月启动了I期临床试验,Sandoz在2月同步启动了I期和III期临床试验,其他诸如Alvotech、Formycon和Xbrane等美国生物类似药研发常客的该产品生物类似药也即将进入临床阶段,原研的皮下注射版本也在研发过程中以抵御未来生物类似药的竞争,未来临床、审评的速度以及各家不同的专利诉讼情况将共同决定新药王首仿产品的归属。诉讼进展决定生物类似药上市位次的BPCIA诉讼大战在2023年迎来了第11个年头,在经历了前面几年的缓和期后,随着生物类似药BLA申报数量再创新高,2023年的诉讼案件数量回升到了7起,截至2023年底,美国历史累计BPCIA诉讼数量已经突破了60起,其中包括了一些双方针对同一产品在不同地区或针对不同专利发起的同源性诉讼。美国历年BPCIA诉讼数量过去的2023年里共有三起诉讼落下帷幕,均已和解告终,其中两起于2022年发起、一起于2023年发起,共涉及曲妥珠单抗、乌司奴单抗和托珠单抗三个分子,其中两个产品已经获批待上市,平均和解时间为173天,其中托珠单抗仅历时103天;2023年之前的诉讼仍有两起尚未了结,分别涉及阿柏西普和那他珠单抗;2023年发起的七起诉讼中共有四起针对阿柏西普一个分子,另外三起分别涉及地舒单抗、托珠单抗和利妥昔单抗,其中地舒单抗和托珠单抗两个分子为首次涉及BPCIA诉讼。七起诉讼的原告方共涉及Amgen、Genentech和Regeneron三家公司,被诉方涉及Sandoz等六家公司,诉讼涉及的专利数量平均为32个,其中涉及阿柏西普的四起诉讼涉及专利数量均超过了30个。从范围上看,2013年-2023年间在负责初审的地区法院层级总共由Amgen、Genetech、Janssen、Abbvie、Biogen和Regeneron六家原研药公司针对目前有生物类似药获批的阿达木单抗等12个分子以及阿柏西普等目前尚未有生物类似药获批的3个新分子向Celltrion等近20家集团公司提起诉讼,共涉及40余个生物类似药(部分未获批)。从时间看,2017(11起)和2018(12起)两年成为诉讼发起最为集中的时间段,占据了全部诉讼数量的近40%,2013年仅有一起诉讼提出。从公司表现看,Genentech以提出18起诉讼的数量排名原告第一,同时分饰原告和被告两角的Amgen以承接9起诉讼的战绩排名被告第一,Celltrion和Sandoz以各被诉8起的数量并列排名被告第二。从耗时看,Sandoz的非格司亭生物类似药Zarxio和Celltrion的英夫利昔单抗生物类似药Inflectra从最初被诉到最终胜诉均历时近五年,成为拉锯时间最长的生物类似药产品,Sandoz的阿达木单抗生物类似药Hyrimoz从被诉到最终与原研和解仅历时2个月,成为诉讼耗时最短的产品;从结果看绝大多数诉讼均以和解告终。在专利诉讼之外的第二战场,2023年美国各公司针对阿柏西普等多个产品共发起了23件IPR多方复审和2件PGR授权后复审,从历史数据来看产品看,曲妥珠单抗原研产品Herceptin、利妥昔单抗原研产品Rituxan和阿达木单抗原研产品Humira成为累计IPR数量最多的产品,针对阿柏西普的IPR数量已经超过了10件,大有追赶前述老产品之势;从被无效专利类型看,应用专利被挑战次数以绝对优势领先其他类型专利。产品表现1.阿达木单抗(Adalimumab)原研产品/公司:Humira/Abbvie 美国获批时间:2002/12 竞争难度:★★★★★十年磨一剑,10在历史发展的长河中的确是一个很有意思的数字,从初出茅庐到登顶王座,Humira用了十年,在连续蝉联十年后迎来了另一个历时十年终成正果的新王霸主Ketruda,随着以Amgen为首的9个阿达木单抗生物类似药在2023年的陆续登场,在巅峰末期连续两年完成200亿神迹的Humira正式走下神坛,两代药王之间十年的传承在2023年圆满收官。Humira历年全球销售额一览2023年,Humira在美国市场受到初步冲击的形势下最终交出了144亿美元的答卷,相比上年出现了32%的下滑,美国市场收入在全球总收入中的占比下降至84%,依然是Abbvie最为依赖的Humira全球最大市场。在去年Humira销量突破1100万支的基础上,2023年包括9家生物类似药在内的美国市场总销量实现了3%的小幅增长,98%的市场份额依然掌控在原研Humira的手中;从包装形式看,注射笔产品的份额略有提升突破了90%;从规格看,100mg/ml高浓度产品的份额达到了85%,40mg/0.4ml的主流规格占据了其中份额的94%。随着Teva和Alvotech联手开发的Simlandi在2月底的获批,目前美国市场阿达木单抗生物类似药获批总数量已经达到了创纪录的10个,除了Simlandi刚刚获批尚未上市,其余9个产品均在2023年登陆了市场,在Amgen的Amjevita作为首仿于去年1月底率先亮相后,Sandoz等7家公司在7月初同步上市了各自的生物类似药产品,Pfizer在10月份最晚入场。八仙过海,各显神通,其中BI的Cyltezo等3个产品被授予了自动互换资格,Sandoz的Hyrimoz等5个产品拥有体验度更好的高浓度产品,在价格方面,Amgen等5家公司推出了高低两种价格方案,Pfizer等4家公司只提供了一种WAC方案,高价高回扣、低价低回扣,虽然实际ASP价格暂不知晓,但最高折扣达到86%的WAC价格已经反映了生物类似药上市后激烈的市场竞争。各家陆陆续续与渠道中的PBM、药房等机构达成了合作协议,其中Celltrion 于去年10月与PBM公司Ventegra达成了合作,Sandoz的Hyrimoz同时被Express Scripts、Optum/United和CVS Caremark等多个PBM的目录所覆盖,Cigna则在去年9月将Amgen的Amjevita移出目录后选择了首个被FDA授予可互换资格的BI产品Cyltezo。总体来看,阿达木单抗生物类似药的2023年市场整体份额仅有2%,全面的渗透仍然需要一定的时间,可喜的是多家PBM已经进行了策略的调整,逐渐向多家生物类似药敞开了大门,市场竞争随着Teva的即将入局将愈发激烈,2024年将成为生物类似药迎来转折的关键一年。2.贝伐珠单抗 (Bevacizumab)原研产品/公司:Avastin/Roche 美国获批时间:2004/02 竞争难度:★★★★☆2023年贝伐珠单抗原研产品Avastin在欧美两大市场的下滑速度相比最近几年有所缓和,最终全球收入以15.73亿瑞士法郎(约合17.5亿美元)惨淡收关,整体降幅达到了26%(以恒定汇率计为19%),持续刷新着历史新低。Avastin历年全球销售额一览2023年,原研产品Avastin美国市场销售收入为4.84亿瑞士法郎(约合5.38亿美元),相比上年下滑了19%,美国市场在全球收入中的区域占比继续维持在30%左右。美国市场贝伐珠单抗的2023年整体销量达到了242万支(+7%),其中生物类似药占比进一步增长至历史最高的84%。Amgen的贝伐珠单抗首仿生物类似药Mvasi以46%的全年平均份额占据销量榜首位置,但销售额受限于激烈竞争造成的价格下滑已下降至5.11亿美元(-15%);Pfizer的二仿产品Zirabev以36%的销量份额继续稳第二把交椅,销售额下滑至3.04亿美元(-26%)。Amneal和Celltrion分别于2022年和2023年上市的生物类似药Alymsys和Vegzelma份额均未超过3%。从规格看,100mg/4ml产品的销量份额升至53%,略占优势;整体市场价格进一步大幅下滑,当前最低平均销售价格(来自Zirabev)已降至16美元/10mg(-50%),相当于原研品价格的23%,原研产品Avastin的价格小幅提升至70美元/10mg(+5%)。Sandoz和百奥泰合作的Avzivi 已于去年年底获批,成为美国第五个获批的贝伐珠单抗生物类似药,截至目前暂未上市,Avzivi获批的初始效期只有12个月,在已有四家在市销售且初始获批效期(Mvasi:36个月,Zirabev:40个月,Alymsys:30个月,Vegzelma:两个规格分别为24/48个月)均比之更久的情况下处于不利的局面。Biocon的BMAB-100 (2020年3月接受审评)、Centus的FKB238(2019年11月接受审评)以及Samsung Bioepis的SB8 (2019年11月接受审评)三个贝伐珠单抗生物类似药历时多年仍处于FDA审评阶段,未来该产品的美国市场竞争将会进一步加剧。3.曲妥珠单抗 (Trastuzumab)原研产品/公司:Herceptin/Roche 美国获批时间:1998/09 竞争难度:★★★★★前有生物类似药追兵,后有同领域创新药来敌的Herceptin在过去的一年交出了16.26亿瑞士法郎(约合18.1亿美元)的答卷,全球销售额整体降幅达到了24%,(以恒定汇率计为16%),迎来了2017年全球销售峰值过后的六连跌。Herceptin历年全球销售额一览2023年,原研产品Herceptin美国市场销售继续下滑至3.31亿瑞士法郎(约合3.7亿美元),26%的降幅与上年基本持平,美国市场在全球收入中的占比降至历史最低的20%。2023年的美国曲妥珠单抗生物类似药之争依然延续着五强争霸的格局,全年生物类似药市场整体销量份额进一步提升至71%。2023年该产品的整体美国市场销量继续下滑至106万支(-8%),420mg大规格产品份额以接近一半。2023年首仿产品Amgen的Kanjinti表现保持平稳,以32%的份额领跑各路生物类似药,美国市场1.09亿美元的销售额相比上年大幅下滑了58%;Pfizer的三仿产品Trazimera以23%份的销量份额排名生物类似药第二,Pfizer年报中报道的净销售额出现了800万美元的负值,其余三个在市生物类似药的份额均未超过10%;当前最低平均销售价格(来自Kanjinti)大幅降至7.38美元/10mg(-77%),仅为原研品价格的9.7%,原研产品Herceptin的价格小幅下降至76美元/10mg(-3%)。截至目前,Sandoz与Eirgenix合作的EGI014 (2021年12月申报 )、Tanvex的TX-05(2021年10月接受审评) 、Prestige的HD201以及复宏汉霖与Accord合作的HLX02(2023年2月接受审评)四个曲妥珠单抗生物类似药产品均已处于FDA审评过程中,未来美国市场该产品生物类似药数量预计将达到10家以上,竞争进一步白热化。4.利妥昔单抗(Rituximab)原研产品/公司:Rituxan/Roche 美国获批时间:1997/11 竞争难度:★★★☆☆Roche抗肿瘤三件套同频共振,其中历史最为悠久的利妥昔单抗原研产品Mabthera/Rituxan ( 分别用于欧洲和美国市场)在2023年紧随Avastin和Herceptin的步伐同步下滑,全球销售额降至16.3亿瑞士法郎(约合18.1亿美元),降幅达到了21%(以恒定汇率计为15%)。Mabthera/Rituxan历年全球销售额一览2023年,原研产品Rituxan美国市场销售收入为9.87亿瑞士法郎(约合11亿美元),相比2022年下滑了25%,占到了原研产品全球销售额的61%;利妥昔单抗生物类似药的整体销量占比进一步增加至77%, 2023年该产品的整体美国市场销量为213万支(+2%),相比上年略有提升,约55%的份额来自于100mg/10ml的小规格产品。作为比首仿晚两个月上市的二仿产品,Pfizer的Ruxience以40%的全年份额继续领跑,3.08亿的美国市场销售额相比上年下降了24%,Teva的首仿产品Truxima以10个百分点的劣势位居第二,于2021年最晚上市的Amgen的Riabni份额仅为6%;当前最低平均销售价格(来自Ruxience)已降至14.5美元/10mg(-53%),相当于原研品价格的19%,原研产品Rituxan的价格小幅下降至75美元/10mg(-3%)。除当前在市销售的3家外,后续针对美国市场的竞品相对比较匮乏,目前处于FDA审评中的生物类似药仅剩Dr Reddy’s和Fresenius合作的产品,该产品已于2023年7月被FDA接受审评,最快有望于今年获批,短期内该产品的竞争将维持在原研产品以及3-4个生物类似药之间。 5.非格司亭(Filgrastim)原研产品/公司:Neupogen/Amgen 美国获批时间:1991/02 竞争难度:★★★☆☆2023年,随着销售额的一降再降,Amgen的非格司亭原研品Neupogen已经在年报中被归入单品销售额较小而不再单独报告的其他产品,与该分类中另外三个生物类似药(英夫利昔单抗生物类似药Avsola,利妥昔单抗生物类似药Riabni以及依库珠单抗生物类似药Bekemv一起取得了3.31亿美元的全球销售额,预计Neupogen全球销售额将在近两年内跌破一亿美元,成为美国市场已有生物类似药上市的分子原研产品中表现最为惨淡的那个。Neupogen历年全球销售额一览2023年,该产品的美国整体市场量约230万支,与去年基本持平,其中预冲注射器产品占比突破了85%;从市场竞争来看,除去Teva以351(a)途径获批的Granix外,过去一年依然延续着Sandoz、Pfizer和Amneal三家仿制药竞争的局面。生物类似药的整体销量份额进一步小幅提升至85%,非格司亭成为目前美国市场生物类似药渗透率最高的分子,其中Sandoz的首仿产品Zarxio以近60%的份额稳居榜首,Pfizer的二仿产品Nivestym的份额已提升至23%,2022年最晚上市的Releuko排名末尾,份额仅为1%。从价格看,原研产品Neupogen的价格相较于仿制药上市前几乎没有大的变化,当前最低平均销售价格(来自Nivestym)已降至0.217美元/1mcg(-36%),相当于原研品价格的23%,Zarxio成为了为数不多的实现价格增长的生物类似药,相比上年价格提升了11%,Neupogen价格基本与去年持平。除去去年刚有生物类似药上市的阿达木单抗外,非格司亭在美国市场所有已有生物类似药上市的分子中销售额排名垫底。截至目前,Tanvex于2020年11月重新申报的BLA仍处于审评中,目前看后续已暂无其他以美国市场为目标的处于晚期的在研非格司亭生物类似药。6.聚乙二醇化非格司亭(PEG-filgrastim/PEG-GCSF)原研产品/公司:Neulasta/Amgen 美国获批时间:2002/01 竞争难度:★★★★★在美国市场激烈竞争造成价格大跌的背景下,选择不断跟进与生物类似药硬扛价格争取以价保量的原研产品Neulasta在2023年的全球销售额跌破10亿美元,最终以8.48亿美元(-26%)抱憾收关。随着Fresenius和Amneal两家生物类似药产品在2023年的相继上市以及Coherus Onbody自动注射器产品在今年2月份的刚刚登陆,八成以上全球收入来自于美国市场的Neulasta未来之路将更加举步维艰。Neulasta历年全球销售额一览2023年Neulasta美国市场销售额降至7.1亿美元(-26%),在全球销售额中的占比下滑至84%。市场总量约为134万支(+3%),去年只有原研品一家在售的自动注射器产品份额已经降至45%,Coherus于去年上市的独有注射笔产品的份额不足1%,占据另外55%份额的预充注射器产品之争在原研公司Amgen与Coherus等6家生物类似药公司之间展开,Sandoz的三仿产品Ziextenzo在2022年通过大幅降价策略将预充注射器产品份额迅速提升至28%,但在去年下半年出现了销量的大幅下滑,最终以12%份全年总份额将尚未坐稳的榜首位置交出,Viatris/biocon的首仿产品Fulfila增长迅速,再过去一年实现了12%的销量份额提升,最终以29%的份额登顶预充注射器产品份额第一,Coherus的Udenyca在经历了2022年的大幅下滑后相对平稳的将过去一年的份额保持在25%,原研产品Neulasta份额小幅提升至24%,Pfizer的五仿产品Nyvepria以10%的份额排在原有老产品的末尾,Fresenius和Amneal新上市的Stimufend和Fylnetra份额均为超过1%。将预充注射器、注射笔和自动注射器三种形式产品的销量合并计算,在原研保持价格跟进策略的影响下,2023年该产品生物类似药的整体份额与上年基本持平,稳定保持在42%。当前最低平均销售价格(来自Ziextenzo)已降至283美元/支(-72%),相当于原研品价格的49%,Nyvepria价格降至714美元/支(-57%),Neulasta价格跟进至574美元/支(-63%),相比生物类似药进入市场前的价格降幅达到了94%,成为了生物类似药上市后降价幅度最大的原研产品,其余4个生物类似药的平均销售价格均保持在1400美元/支以上。Coeherus在去年5月推出了独有的注射笔产品UDENYCA® Autoinjector,其自动注射器产品UDENYCA® ONBODY™ 在去年10月快速完成收到CRL后的再申报后于去年12月获批,并于今年2月在美国正式上市,成为了首个与原研Neulsata Onpro直接竞争的生物类似药产品,注射时间仅为5分钟,Amgen最后的防御体系将在2024年开始遭遇猛烈冲击,Coherus在未来竞争中的优势愈发明显。Lupin的该产品生物类似药目前处于FDA审评中,目前审评时间已近3年仍未获批。 7.英夫利昔单抗(Infliximab)原研产品/公司:Remicade/J&J 美国获批时间:1998/08 竞争难度:★★★☆☆随着美国等全球多个市场生物类似药渗透的不断加强, 2023年Remicade的销量和价格持续同步下滑,全球销售额降至23亿美元(-21%)。Remicade历年全球销售额一览2023年,Remicade美国市场销售额为12.9亿美元(-20%),在全球销售额中占比继续保持在56%,英夫利昔单抗美国整体市场销售量增加到了995万支(+4%),在原研产品的封锁进一步解开的背景下,生物类似药在商业流通渠道中进入报销目录的比例不断提升,整体份额在2022年大幅提升14%的基础上进一步增加至48%,原研依然占据着半壁江山。目前共有Pfizer的Inflectra、Organon的Renflexis以及Amgen的Avsola三家生物类似药在售,其中早在2016年便已上市的首仿产品Inflectra在过去一年中将份额稳定保持在28%,受降价影响,销售额下降至2.57亿美元(-11%),Renflexis和Avsola的销量份额占比均不足10%。生物类似药于2016年进入市场后带动了整体市场价格的持续下滑,当前生物类似药最低平均销售价格相比首仿上市时原研价格已经下降了85%,当前生物类似药的最低平均销售价格(来自Inflectra)为11.86美元/10mg(-49%),相当于原研品价格的39%,原研产品Remicade的价格小浮下降至30.3美元/10mg(-8%)。Celltrion在2022年底以351(a)途径申报的皮下注射版英夫利昔单抗产品Zymfentra于去年10月用时一轮正式获得FDA批准,初始获批效期达到了39个月,将与目前由合作伙伴的Pfizer代售的首仿产品Inflectra形成双拳出击的合力,完满的诠释了极致研发的魅力。Zymfentra的上市批产品已于2月底空运发往美国,预计将于3月中旬在美上市,定价上将高于目前在售的生物类似药。目前暂时已无其他进展较快的潜在竞争对手在短期内寻求在美申报英夫利昔单抗生物类似药。8.阿法依伯汀/依泊汀α(Epoetin Alfa)原研产品/公司:Epogen &Procrit /Amgen 美国获批时间:1989/06 竞争难度:★★☆☆☆安进负责的阿法依伯汀美国市场部分2023年销售额进一步大幅下滑至2.26亿美元(-55%),J&J负责的美国及全球其他市场部分因销售额过低自2022年起已不在财报中单独列出,根据此前该产品的整体销售趋势推测其2023年全球整体销售额预计在5亿美元左右。Epogen/Procrit历年全球销售额一览自Pfizer的生物类似药Retacrit于2018年底上市以来,一直未有新的生物类似药获批,2023年该产品的美国市场整体销量下滑至782万支,Retacrit的全年市场份额继续保持在42%,美国市场收入下滑至2.59亿美元(-17%),占到了其全球销售额的76%。当前最低平均销售价格(来自Retacrit)已降至0.72美元/100units(-6%),相当于原研品价格的85%。暂时没有更多关于后续有计划在美国市场开发该产品生物类似药的其他公司的相关进展报道,考虑到该产品整体市场的不断萎缩,预计未来很难有新的生物类似药产品寻求进入美国市场,两个原研品与一个生物类似药竞争的局面仍将继续维持下去。9.甘精胰岛素(Insulin Glargine)原研产品/公司:Lantus /Sanofi 美国获批时间:2000/04 竞争难度:★★★☆☆在包括美国在内的多国政府通过多种举措降低胰岛素产品垄断和药价的努力下加之生物类似药产品的不断渗透, 2023年甘精胰岛素原研产品Lantus的全球销售额已降至14.2亿欧元(折合15.2亿美元),下滑幅度达到了创纪录的37%,迎来了自2016年以来的8连跌。Lantus历年全球销售额一览2023年,Lantus美国市场大幅崩盘,销售额以63%的降幅下滑至2.81亿欧元(折合3亿美元),在全球销售额中占比由34%降至20%,美国市场甘精胰岛素注射液整体销量稳定保持在1.1亿支,Eli Lilly的生物类似药产品Rezvoglar获批15个月后于去年4月正式上市,当前竞争在Eli Lilly、Biocon和原研Sanofi三家之间展开。Sanofi共有原研产品Lantus、升级产品Toujeo以及于2022年推出的非品牌版本三种甘精胰岛素产品,Toujeo成分与Lantus相同但释放活性成分更平缓,低血糖发生率显著降低,但临床的不可替代性相对较低,Biocon于去年正式接手Viatris开始销售具有可互换资格的生物类似药Semglee以及其非品牌版本产品,Eli Lilly在之前销售的以化药NDA获批并完成BLA转换的Basaglar基础上于去年上市了同样具有可互换资格的生物类似药Rezvoglar,目前已经拥有两款甘精胰岛素产品在市销售。2023年,生物类似药的份额进一步提升至13%但增速依然相对缓慢,受《通胀削减法案》的影响,各家在去年均进行了不同程度的降价以响应将患者每月的胰岛素自付费用限制在35美元的要求,从当前的WAC价格看,Lantus和Semglee非品牌版本产品的价格已经分别降至34美元/1000IU和30美元/1000IU,不断刷新着历史最低价格,实际净价将在此基础上进一步降低。美国市场甘精胰岛素各产品当前WAC价格一览Sandoz和甘李合作的甘精胰岛素生物类似药已经于去年2月被FDA接受审评,最快有望于今年获批;Lannett和东阳光合作的甘精胰岛素生物类似药目前也已处于FDA审评过程中;健友与通化东宝于去年9月达成战略合作,共同推进甘精、门冬、赖脯三种胰岛素注射液在美国市场的开发和生产。10.雷珠单抗(Ranibizumab)原研产品/公司:Lucentis /Roche & Novartis美国获批时间:2000/04 竞争难度:★★★☆☆近两年来多个雷珠单抗生物类似药在欧美两大法规市场相继获批和上市,除了以Samsung/Biogen为代表的三大联盟外,作为中国仿制药国际化领军企业的齐鲁制药也在今年初迎来了其雷珠单抗生物类似药Rimmyrah在欧盟和英国的相继获批,实现了国产眼科生物药品出海零的突破。原研产品Lucentis在同领域其他创新药竞品及生物类似药的激烈竞争下不断萎缩,2023年的全球销售额最终以33%的历史最大跌幅定格在19.7亿美元,负责美国市场销售的Roche和美国外其他市场销售的Novartis分别贡献了其中的25%和75%。Lucentis历年全球销售额一览2023年Lucentis美国市场销售额为4.6亿瑞士法郎(折合5亿美元),降幅达到了历史最高的53% ,市场总量下降至94万支(-13%),预充注射器装产品的份额在目前只有瓶装产品的生物类似药竞争下从2022年的99%下滑至74%。Samsung Bioepis的雷珠单抗首仿产品Byooviz以及Coherus的二仿产品Cimerli于2022年6月和10月相继上市后在2023年里进一步渗透,将生物类似药的整体份额提升至26%,其中Cimerli的份额达到了21%。当前最低平均销售价格(来自Byooviz)已降至173.35美元/0.1mg(-22%),相当于当前原研品Lucentis价格的98%,当前Lucentis最新的平均销售价格为176.94美元/0.1mg(-21%),相比生物类似药上市之前的自身价格已经下降了33%。出于战略层面考虑,Coherus在今年1月将视为非核心资产的Cimerli以1.7亿美元的首付款转让给了Sandoz,未来将更加专注于肿瘤领域的创新药产品,Sandoz借此在阿柏西普的基础上补强了自身的眼科生物类似药产品线;由三大联盟之一的Xbrane/Stada研发的生物类似药产品的再申报已于去年6月被FDA接受审评,预计最快于今年4月获批,此前与Bausch + Lomb在美国市场签订的商业化合作协议已经终止;Lupin的LUBT010已经顺利完成了针对美国市场的III期临床试验。未来展望光阴似箭,美国市场生物类似药在2005年初露头角后在纷繁变化的大环境中走到了第十个年头,在摸索中突破,在逆境中前行,政策、流通和竞争等多个环节在接下来互有你我的博弈中形成的合力将共同指引着生物类似药未来之路的方向和轨迹。在研发方面,尽管以Viatris为代表的部分公司基于自身策略逐步开始退出了生物类似药领域,但针对美国市场的生物类似药整体研发依然在如火如荼的进行着,在严冬的大背景下各家的研发策略更加务实,对于项目的选择和把控愈发谨慎,稳中求进、以进促稳的基调深入贯穿其中。随着全球范围内生物药的蓬勃发展,大分子的研发已不再向多年之前那样高不可攀,通过相关配套资源的自建补强或兼并引入,各家在生物类似药研发领域的差距也在逐步缩小。在研发涉及产品类别逐步拓展和丰富的变化下,肿瘤和自身免疫两大领域依然是各路诸侯最为关注的焦点区域,针对中短期有上市机会的重磅单品的研发大战其火爆程度大有追赶小分子之势。在生物类似药早期入局者实力差距红利逐步淡化的趋势下,动辄十家以上竞争对手针对部分大药进行竞争的格局将成为不再陌生的新常态。思路的清晰与否决定了能不能选得对、做得早,研发的实力强弱决定了能不能走得快、筑得牢,在此基础上临床的策略优劣进一步决定了能不能入的快、报的早,质量的水平高低决定了能不能查的少、批的早,专利的破局深浅则决定了能不能谈的好、上的早,以研发为引擎的全面布局和综合硬实力共同决定了能否先人一步、胜人一筹。在合作方面,速度、成本和风险的联合驱动使得带给各色玩家更多选择与可能的外部联姻在数量上逐步增多,在类型上也更加丰富。在生物类似药市场开放初期,以Mylan/Biocon和Samsung/Biogen为代表的早期联盟更多的针对一揽子早期产品展开合作并在此基础上逐步拓展,随着近年来行业内各类参与方整体实力的不断提高,合作可选的对象更加广泛,在研发和生产资源逐步供大于求以及商业化销售资源相对稀缺的背景下,项目合作开始逐步转向中晚期产品,III期临床的起始或成功完成成为越来越多的合作起点。在合作条件上,不确定性的增多以及市场竞争的复杂使得授权费和销售提成等要素触发的里程碑点设置更加细化,不同情况下的差异化收益逐步取代了供少于求局面下的一刀切模式,通过合作实现双赢、大家都有钱赚的思路逐渐深入人心,未来这一趋势仍将延续下去。买方市场主要由在美具备商业化销售能力的大中型公司组成,既包括了以Sandoz为代表的能研能产能卖的一条龙翘楚,也包括了以Amneal为代表的不能研产但能卖的新晋小分子仿制药公司,买方市场则更多的涵盖了具备研发和生产能力但无力或无意在美进行自售的中小型公司。在没有足够产品支撑情况下的销售团队自建带来的入不敷出和稳定性风险注定将成为那份不可承受之重。在注册方面,随着生物类似药产品申报数量在2023财年再创新高以及多个产品III期临床于去年的顺利完成,预计2024年的申报和获批数量都将进一步实现增长,涉及的分子种类在2023年实现突破的基础上也将继续拓展。新的一年里BsUFAIII(生物类似药用户付费法案)将进入实施周期内的第二个财年,2024财年生物类似药申请费、项目费和开发费(BPD)相比上一财年大幅下滑,其中开发费(BPD)中包括的初始BPD费、年度BPD费用和再激活费用均下降了79%,申请费下滑42%后临床类和非临床类产品申请费分别降至1018753美元和509377美元,项目费同样下滑42%降至177397美元,各项费用相比上年的大幅下滑反映了近年来尤其是去年生物类似药开发蓬勃发展的局面。在流通方面,FDA已经批准了8个具有自动替换资格的生物类似药,涵盖了雷珠单抗、阿达木单抗、甘精胰岛素以及还未有生物类似药上市的乌司奴单抗四种分子。在自动替换的实际执行过程中,各州的法律也不尽相同,例如新泽西等9个州仅允许患者使用替换的生物类似药费用低于原研产品时进行替换,除北卡和弗吉尼亚以外的剩余48个州均需要药师在替换时与开具处方的医生进行反馈,阿拉巴马等4个州仅在得到开具处方的医生许可的情况下才可以进行替换,总体来说自动替换在各州实际执行时依然存在一定的限制条件,同时目前被授予可互换资格的产品涉及的治疗领域的覆盖面还不够广泛。近年来生物类似药的高速渗透更多的体现在肿瘤领域,在以英夫利昔单抗为代表的其他非肿瘤领域的渗透速度依然还有不小的提升空间,医生在眼科等领域实际开具处方时对于生物类似药的使用依然比较谨慎,在一项针对80名眼科医生进行的调查中,80%的被调查者表示对生物类似药比较或非常熟悉,但其中仅有60%真正开具过生物类似药的处方,其中开具过雷珠单抗生物类似药Byooviz和Cimerli的比例均为40%。阿达木单抗在2023年表现的不及预期反映了此类主要在药房层面进行流通的产品受PBM覆盖影响的巨大,随着多家PBM在过去一年里逐渐将越来越多的生物类似药纳入覆盖清单,2024年生物类似药们的表现依然值得期待。在竞争方面,唯快不破的争取尽可能靠前的上市位次依然是决定竞争归属的最核心因素,在此基础上的差异化策略将进一步增加自身在竞争中的筹码,例如阿达木单抗的高浓度和可互换的多维度比拼、聚乙二醇化非格司亭自动注射器产品以及雷珠单抗预充式注射器产品的另辟蹊径。在复杂的生物类似药竞争中,单纯的价格杠杆调节很难做到像小分子领域那样屡试不爽,在争取到有利位次基础上的降价策略才更有意义。南来北往、有进有退,总体来看未来涉身美国生物类似药市场的公司数量仍呈上升趋势,竞争的格局将更加复杂和激烈,往事已成云烟,各方对于后续一波又一波陆续在中短期内失去专利保护的大药争夺又站在了同一起跑线上,孰强孰弱,拭目以待。在政策方面,美国政府层面对于推动生物类似药不断前进的努力一直在延续着。2023年2月,美国参议院司法委员会通过了一系列涉及生物类似药的立法,其中患者可负担处方药法案《Affordable Prescriptions for Patients Act of 2023》旨在防止制药公司利用专利制度来延迟仿制药和生物类似药的竞争,保留获得平价仿制药和生物类似药法案《Preserve Access to Affordable Generics and Biosimilars Act》将禁止品牌药公司在专利和解中向仿制药和生物类似药生产商支付费用以延迟竞争,停止拖延法案《Stop Stalling Act》旨在阻止品牌药商滥用FDA旨在确保药物安全的程序,法案将赋予联邦贸易委员会(FTC)更多权力(包括罚款)以对那些在FDA提起的试图干扰竞争性仿制药或生物类似药批准的“虚假公民请愿”采取行动,并促进对那些出于善意提出合理的公共卫生问题的请愿书进行有效审查。2023年7月,美国参议员 Mike Lee在其2022年提出的《生物类似药取消繁文缛节法案》被否决后再次提除了新版本的该法案,建议取消有关与开发生物类似药相关的转换研究的可互换性要求,该法案将在今年底再次被表决。千淘万漉虽辛苦, 吹尽狂沙始到金。行业的严冬终将过去,暂时的障碍不会永久,向阳而生,逆风而行,梦想定会实现。推荐阅读星条旗下的宝藏:美国生物类似药市场2022概览星条旗下的宝藏:美国生物类似药市场2021-2022概览星条旗下的宝藏:美国生物类似药市场2020概览星条旗下的宝藏:美国生物类似药概览(下)星条旗下的宝藏:2018美国化学仿制药市场概览Copyright © 2024 PHARMCUBE. All Rights Reserved.欢迎转发分享及合理引用,引用时请在显要位置标明文章来源;如需转载,请给微信公众号后台留言或发送消息,并注明公众号名称及ID。免责申明:本微信文章中的信息仅供一般参考之用,不可直接作为决策内容,医药魔方不对任何主体因使用本文内容而导致的任何损失承担责任。
生物类似药疫苗专利到期
2023-03-17
·生物谷
在政策方面,拜登政府在生物类似药领域降低药价、打击不正当竞争、专利诉讼和推动自动替换实施等方面的一系列举措极大的推动了生物类似药冲破重重阻碍的快速发展,极大的节省了政府在医药领域的巨额开支,政策层面的
整体概况
2022年全球生物药市场规模达到了4800亿美元,占到了全球医药整体市场规模的36%,预计将在五年后的2028年突破7000亿美元,进一步将份额提升至40%以上。近年来以欧美为首的的全球生物类似药市场保持飞速发展,稳步提升至近200亿美元的规模,随着以阿达木单抗为代表的一系列重磅产品生物类似药未来几年在欧美市场的全面上市,整体规模仍将进一步扩大,有望于2030年突破700亿美元。
2022年全球销售额TOP100药品中,单抗等生物大分子药物数量超过了一半。除去疫苗产品外,2022年全球销售额TOP20生物产品均为单抗和抗体融合蛋白;各产品全球销售额均在29亿美元以上,其中一半以上的产品收入在50亿美元以上;美国市场处于核心地位,TOP20中85%的产品美国市场收入在全球销售额中的占比在50%以上;产品主要分布在抗肿瘤和自体免疫领域,除奥瑞珠单抗和瑞莎珠单抗外的其他18个产品均已登陆中国市场;60%的产品在2010年之后获批,其中获批时间最早的依那西普距今已有近25年,获批最晚的瑞莎珠单抗距今仅有4年。
2022年全球销售额TOP20生物药原研产品(非疫苗类)
随着疫情影响的逐步减弱和消退,2022年美国医药市场整体规模(以发票金额计)再创新高,稳步提升至6300亿美元,蓬勃发展的生物药品在整体销售额中的占比达到了48%,预计将在2027年达到4000亿美元的规模,份额占比超过一半。
2022年美国生物类似药市场最终交出了75亿美元的答卷,10%的增速相比以往有所放缓,究其原因一方面在于之前已获批产品间竞争日渐加剧带来的价格持续下滑部分抵消了生物类似药不断渗透带来的增量正效应,另一方面个别产品的市场经过几年的洗牌在销量规模上已经日趋平衡甚至个别出现了萎缩,加之新上市产品普遍靠近年尾,对当年销售额的贡献比较有限。过去的一年里,首个眼科产品雷珠单抗华丽登场,成为上市的第九个新分子;非格司亭和贝伐珠单抗两个产品的生物类似药份额在万众瞩目中突破80%;Cimerli和Rezvoglar成功被授予可互换资格,进一步提振了生物类似药未来前进方向的信心;乌司奴单抗等一系列新产品如期进入申报环节,加速了步入新纪元的步伐;一切都是崭新的,目光所至、心之所向、以梦为名、不负荣光。
获批&上市
2022-2023美国生物类似药获批一览
(截至2月底)
从获批位次看,Coherus的Cimerli成为继三星的Byooviz之后第二个获批的雷珠单抗生物类似药,与之不同的是Cimerli在获批时就被FDA授予了可互换资格,继Cyltezo和Semglee之后第三个获此殊荣。Alymsys和Vegzelma成为第3和第4个获批的贝伐珠单抗生物类似药,Fylnetra和Stimufend成为第5和第6个获批的聚乙二醇化非格司亭生物类似药,Releuko作为第3个获批的非格司亭生物类似药,距离前面的二仿产品Nivestym获批已经过去了四年之久。
从审评时长看,Releuko由于一系列研发和现场检查中出现的质量问题前后历经4次CR才最终过关, 前后耗时1693天,前无古人后也很难再有来者;Fylnetra和Stimufend分别由于收到1次CR以及疫情影响下的现场检查延迟未能一轮过审,审评时长均超过了500天;Alymsys等四个产品顺利一轮通过,延续了贝伐珠单抗、阿达木单抗和雷珠单抗三个分子全部已获批生物类似药均在一个审评周期内获批的优良传统。
2022-2023年美国生物类似药上市一览(截至2月底)
截至目前,美国以351(K)途径申报的生物类似药获批总数量和上市数量已经分别达到了40个和27个。从产品类型看,共涉及维持治疗、抗肿瘤、自体免疫、胰岛素和眼科五大领域的11个分子,其中数量最多的阿达木单抗共有8个生物类似药获批,数量最少的阿法依泊汀只有1个生物类似药获批,曲妥珠单抗和聚乙二醇化非格司亭均以5个生物类似药上市的战绩成为当下竞争最为激烈的产品;从公司看,共涉及包括了原研创新型、专注研发型以及大型仿制药公司在内的12家公司,其中Pfizer以8个产品获批和6个产品上市的双第一战绩独占鳌头。获批未上市的13个生物类似药有9个受限于专利,其余则主要因为商业化策略暂未上市或放弃上市。
渗透&价格
美国市场生物类似药发展的大环境在过去的几年中不断改善,早期制约生物类似药发展的多重障碍被逐步剔除,法规层面对于原研公司通过不正当竞争谋求垄断的打击、使用环节医生和患者在培训推广助力下日益加深的理解、流通渠道PBM等核心参与方在目录制定等重要环节的开放以及生物类似药生产和销售方自身在药品质量、价格及便捷性等方面的不懈努力等多重因素共同推动了生物类似药“柳暗花明又一村”的破冰之旅。
在已上市生物类似药通过彼此之间以及与原研药的竞争不断拉低市场整体价格的大背景下,美国的医药支出得到了极大地节省,根据AAM报道,2021年涉及7大分子的全部生物类似药节省医药支出达到了70亿美元,并有望在未来五年实现累计节省支出突破千亿美元。随着生物类似药可互换资格的授予及全面应用以及阿达木单抗等多个重磅新产品生物类似药在未来几年的陆续上市,生物类似药的渗透将进一步增强并在节省开支方面发挥出更大的作用。
美国生物类似药历年节省医药费用一览
从具体数字看,截至2022年底,拥有生物类似药在市销售的7个产品的生物类似药(不含去年刚上市的雷珠单抗生物类似药和甘精胰岛素生物类似药Semglee)销量份额均在40%以上,其中贝伐珠单抗为首的罗氏抗肿瘤三件套以及早已实现财务自由的非格司亭四个产品生物类似药占比都突破了60%,7个分子中有6个在市生物类似药数量在3家及以上。
资历最老的非格司亭生物类似药自Zarxio上市经过七年多的发展将份额提高到创纪录的81%,成为了当下生物类似药销量占比最大的产品;竞争最为激烈的曲妥珠单抗生物类似药在去年将整体份额提升了14%,成为了2022年渗透幅度增长最大的产品;英夫利昔单抗、聚乙二醇化非格司亭和阿法依伯汀三个分子的原研产品通过采用跟进生物类似药同步降价的策略最大程度上减缓了竞争对手的强力渗透,依然保持着一半以上的市场份额,其对应的生物类似药整体销量份额被暂时限制在40%左右,共同成为渗透最慢的产品群。
从具体单品份额看,史上首个生物类似药Zarxio以60%的份额排名榜首,7个分子排名榜首的7个生物类似药中有5个为首仿产品,其中PEGG-CSF的首仿产品Fulfila以10%的份额排名全部首仿产品末尾。阿法依泊汀仅有的生物类似药Retacrit 2022年销量出现下滑,成为唯一一个2022年生物类似药整体份额未实现持续增长的分子。
2018-2022美国市场在市销售各分子生物类似药销量份额变化一览
Fresenius的聚乙二醇化非格司亭生物类似药于2023年2月上市,成为了目前在市生物类似药中最晚上市的产品,距离2015年9月上市的美国首个生物类似药Zarxio上市已有7年半之久,虽然不同分子生物类似药竞争产品数量和入市持续时长均有所不同,但都不同程度的通过竞争拉低了整体市场价格。7个分子当前最低产品ASP价格相比于生物类似药上市之前的原研品价格降幅在34%-77%之间,6个产品的降幅超过了60%。渗透时间最久的非格司亭以及拥有在市生物类似药产品数量最多的聚乙二醇化非格司亭的价格降幅最大,均达到了77%;近年来只有一家生物类似药在市销售的阿法依泊汀价格降幅最小,仅有34%。罗氏抗肿瘤三件套对应的生物类似药均于2019年才开始进入市场,但降价幅度均超过了60%。
原研公司在面临生物类似药竞争时的价格策略带来的二者之间的价格差直接决定着生物类似药渗透的速度,不同公司对待各自产品甚至同一公司对待自身不同产品的策略都不尽相同,以安进为例,其在已经江河日下的非格司亭原研产品Neupogen上任性的选择了放弃跟进,而在尚可背水一战的Neulasta上则理智的选择了步步紧跟,两种截然不同的态度也造就了两种大相径庭结果,非格司亭同时成为了原研与生物类似药价格差异最大和生物类似药渗透幅度最高的分子。
美国生物类似药涉产品价格变化一览
策略&管线
舞榭歌台,风流总被雨打风吹去。一曲笑傲江湖过后的余音仍在耳边缠绕,有人选择带着胜利昂首离开,刀剑入鞘、拂衣而去,只留下夕阳下山河渐远的黯淡背影;有人选择忘记伤痛继续前行,志在千里、壮心不已,纵死侠骨香的誓言响彻云间;有人选择快意恩仇仗剑天涯,初露锋芒、小试牛刀,那是欲与天公试比高的年少轻狂。
当下全球生物类似药的研发依然在如火如荼的高歌猛进,FDA2022财年末其生物类似药研发计划中包括的生物类似药项目已经达到了106个,共涉及30多个分子,其中20多个分子已有生物类似药进入美国临床阶段。20%的在研项目由全球年销售额在百亿美元以上的大公司开发,剩余80%的在研项目则由规模相对较小但具备相关经验的中小型公司开发。
随着近几年来美国生物类似药市场的不断成熟和完善,其未来发展的前景和轮廓日益清晰,各家公司在经历了早期或试水或观望的初级阶段后也在逐步结合自身实际情况开始调整策略。
Pfizer在2022年其生物类似药全球收入再次突破20亿美元(美国市场突破15亿美元),但比之新冠产品加持后创纪录的千亿销售额终究还是黯淡了不少,Pfizer目前依旧凭借着早期收购Hospira获得的多个生物类似药产品常年霸榜,但随着其逐步将重心转移至创新药的战略调整,生物类似药模块的权重大为下滑,内部已不再作为单列模块,除了今年即将上市的阿达木单抗外,后续研发管线已无其他生物类似药产品。
传统小分子仿制药三强Teva、Mylan和Sandoz作为首批试水者鏖战其中,时隔七年之后各自的未来已不尽相同,Teva和Sandoz依然坚持着自研加引进齐头并举的策略继续坚守着,在生物类似药领域实力更胜一筹的Sandoz在早期经验和产品红利逐步弱化的情况下开始加速外部合作,逐步走下坡路的Teva此时更是将生物类似药作为逆天改命的希望之一,Mylan在与Upjohn合并为Viatris后开始实施90亿美元的资产剥离计划,生物类似药首当其冲的被摆上货架交由亲密伙伴Biocon接盘,接下来女性健康、OTC和部分原料药业务也将被清理甩卖,Biocon接手后面临从幕后走上台前的角色转变, GMP合规方面已成为其当下最大的制约因素。
作为传统生物药研发生产型巨头的Celltrion和Samsung也是一直参与其中,Samsung在和Biogen分手后自主性和灵活性会更强,专注研发和生产的策略基本不会改变,Celltrion在美国小分子仿制药体验过独立销售后已经准备转战大分子领域,目前已经开始组建销售队伍,未来将在美国独立销售其自身产品。
Amneal、Fresenius和Hikma作为小分子仿制药领域的第二梯队开始在近年正式进军生物类似药领域,Amneal依托于和Kashiv的战略联盟以及自身创新药销售团队,目前已有两个产品在市销售,Fresenius凭借收购Merck生物类似药业务打下基础,刚刚通过顺利上市首个生物类似药Stimufend成功迈出了又一步,Hikma进场较晚但行动迅速,短期内仍需要凭借外力快速布局搭建轮廓。
预计最早上市时间表
生物类似药管线重点重叠产品概况一览
从具体产品看,致力于玩转美国市场的各路诸侯普遍持有多个处于临床III期至FDA审评阶段的产品,基本均为原研产品主要专利即将到期、美国市场销售额在20亿美元以上的重磅产品,产品线的相似性相对较高,多个产品出现了重叠,其中地舒单抗、阿柏西普和乌司奴单抗三大产品成为各方势力聚焦的重中之重,未来大概率出现十家以上竞争的白热化场面。临床阶段产品中以非格司亭为代表的一代目和以贝伐珠单抗为代表的的二代目已经比较罕见。
Teva当前生物类似药产品线共有12个产品组成,其中5个来自合作伙伴Alvotech,6个产品已处于临床至审评阶段,处于FDA审评中的阿达木单抗有望于今年4月成为首个获批并授予可互换资格的该分子高浓度产品,另一个在审重磅产品乌司奴单抗也有望于今年获批。地舒单抗和阿柏西普两个产品预计将于今年下半年完成III期临床。
作为最懂生物类似药的原研型公司,Amgen一直秉承在精不在多的发展理念。截至目前其生物类似药管线中的3个产品均已完成III期临床,其中乌司奴单抗已于去年三季度申报BLA,有望最早于今年首家上市,依库珠单抗和阿柏西普预计将于今年申报BLA,前者已经与原研公司Alexion达成和解,可于2025年3月登陆美国市场。
Sandoz近年来开始走外部引进为主以求提速和降低风险的路线,现有管线中与Polpharma、EirGenix、Bio-Thera和Gan&Lee四大伙伴合作的产品均已在近两年开花结果、完成了申报,自研的地舒单抗生物类似药也刚刚被FDA接受审评,领跑该产品其他竞争对手,其与Biocon在2018年达成的战略联盟也将在未来为其进一步丰富产品线。
Biocon于去年底完成了对Viatris生物类似药业务的收购,收回了多个此前授权转让出去的产品以及来自Momenta的阿柏西普生物类似药(首家美国申报),当前管线除了涵盖了地舒单抗等三大重磅产品外,还包括了其自身优势胰岛素领域的多个产品。本次收购使得Biocon在之前研发和生产能力的基础上获得了此前不具备的法规市场药政和销售资源,未来将实现一条龙的自给自足,当下最重要的乃是尽快解决掉制约在审产品获批的厂房GMP问题。
Celltrion四个处于III期临床的产品预计都将于今年内结束,Samsung当前剩余管线产品均处于待申报状态,两家公司的管线都涵盖了地舒单抗等三大重磅产品,Celltrion同Biocon一样也有望从今年起实现美国市场的研报产销一条龙;Samsung未来依然会专注于研发和生产,美国市场销售会继续由Organon和Biogen等合作伙伴负责。
Coherus于今年1月份引进了来自的Formycon的阿柏西普生物类似药,计划于今年申报BLA,面临当前产品线已经比较匮乏的情况,其将在未来几年内进一步加速引进处于研发末期的外部产品。Fresenius、Hikma和Lupin等此前以小分子仿制药见长的公司目前仍处于初期产线建立阶段,产品数量比较有限,通过实战积累各个环节的经验进而打牢根基是该时期最主要的目标。
诉讼进展
美国历年BPCIA诉讼数量
截至2022年底,美国累计BPCIA诉讼数量已经突破了50起,其中不乏一些双方针对同一产品在不同地区或针对不同专利发起的同源性诉讼。单年诉讼数量在申报潮的带动下在2018年达到顶峰,此后随着各家申报节奏的逐步放缓以及受疫情影响开始逐渐回落。过去的2022年里又有新的4起诉讼展开,2022年之前的诉讼已经全部了结,清零后第二战场的硝烟依然弥漫,似曾相识的画面中也多了些许不同寻常的新景。相比之前诉讼涉及阿达木单抗等9个已有生物类似药获批的分子,2022年的诉讼增加了阿柏西普、那他珠单抗和乌司奴单抗三个新分子,三起诉讼的被诉方均为首家申报该分子生物类似药的老熟人Mylan、Sandoz和Amgen,原告方相比之前增加了Regeneron和Biogen两张新面孔。另外一起针对老产品曲妥珠单抗的诉讼在Genentech和Tanvex之间,双方已在达成协议后和解。2022年和解的先前发起的诉讼主要针对聚乙二醇化非格司亭、贝伐珠单抗和阿达木单抗三个产品,诉讼历时均在300天以上,其中Nyvepria已在被诉后和解前冒险上市,另外两个产品目前尚未获批。
2022年美国已和解BPCIA诉讼
(2022年前申报)清单
2022年美国新发起BPCIA诉讼清单
从范围上看,2013年-2022年间在负责初审的地区法院层级总共由Amgen、Genetech、Janssen、AbbVie、Biogen和Regeneron六家原研药公司,针对目前有生物类似药获批的阿达木单抗等9个分子以及阿柏西普等目前尚未有生物类似药获批的3个新分子,向Celltrion等14家集团公司提起诉讼,共涉及30余个生物类似药(部分未获批);从时间看,2017(11起)和2018(12起)两年成为诉讼发起最为集中的时间段,占据了全部诉讼数量的近一半,随后开始回落,近三年分别各有4、3和4起诉讼提出;从公司表现看,Amgen和Genetech以分别提出16起诉讼的数量并列排名原告第一,同时分饰两角的Amgen以承接9起诉讼的战绩排名被告第一,Celltrion和Sandoz以各被诉7起的数量并列排名被告第二。从耗时看,Sandoz的非格司亭生物类似药Zarxio和Celltrion的英夫利昔单抗生物类似药Inflectra从最初被诉到最终胜诉均历时近五年,成为拉锯时间最长的生物类似药产品,Sandoz的阿达木单抗生物类似药Hyrimoz从被诉到最终与原研和解仅历时2个月,成为诉讼耗时最短的产品;从结果看,近七成的诉讼最终以和解告终。
在BPCIA诉讼战场之外,更加快捷经济的无效专利程序也备受青睐,2022年美国各公司针对阿柏西普等多个产品共发起了15件IPR多方复审和2件PGR授权后复审,从具体产品看,曲妥珠单抗原研产品Herceptin、利妥昔单抗原研产品Rituxan和阿达木单抗原研产品Humira成为被挑战专利无效次数最多的产品;从被无效专利类型看,应用专利被挑战次数以绝对优势领先其他类型专利。
产品表现
原研产品/公司:Humira/AbbVie
美国获批时间:2002/12
Humira历年全球销售额一览
2022年,Humira在美国市场凭借着屡试不爽的涨价策略和销量持续的增长最终交出了186亿美元的答卷,创下历史新高的同时,美国市场收入在全球总收入中的占比继续提升至近19年来最高的87.7%。在销量突破1100万支的同时,注射笔包装形式和使用效果更佳的100mg/ml新处方产品份额分别进一步提升至90%和85%。
截至目前,在美申报该产品生物类似药的10家公司均已于AbbVie达成和解,其中8家公司的BLA已经获批。今年1月31日,首家获批并通过和解赢得最早上市时间的Amgen在历经2321天的漫长等待后正式在美上市了其阿达木单抗生物类似药产品Amjevita,吹响了生物类似药反击的号角。半年后将迎来第二波生物类似药的集体同步入市,其中Samsung Bioepis的Hadlima是目前唯一同时获批50mg/ml和100mg/ml两种规格的产品,BI的Cyltezo是目前唯一被FDA授予可互换资格的产品,Alvotech和Celltrion两家目前仍在审的产品仅涵盖了高浓度规格,前者的AVT02有望第二家被授予可互换资格,Sandoz则在去年补充申报了高浓度规格。目前包括AbbVie在内的各家公司均对自身产品持乐观态度,未来生物类似药的价格、可互换的实施程度以及高浓度规格产品的走势三大因素将协同作用最终决定2023年这场瞩目大战的胜负归属。
原研产品/公司:Avastin/Roche
美国获批时间:2004/02
Avastin历年全球销售额一览
2022年,原研产品Avastin美国市场销售收入为6.34亿瑞士法郎(约合6.67亿美元),下滑31%的同时,美国市场在近十年全球收入中的区域占比首次跌破30%。美国市场贝伐珠单抗的2020年整体销量达到了225万支(+5%),其中生物类似药占比历史性的提升至80%。Amgen的贝伐珠单抗首仿生物类似药Mvasi依然以近一半的份额占据销量榜首位置,但销售额受限于激烈竞争造成的价格下滑已下降至6.02亿美元(-27%);Pfizer的Zirabev去年也实现了突破,通过抢占原研产品市场进一步提升至34%。
从规格看,100mg/4ml和400mg/16ml规格产品的差距不大,前者略占优势。整体市场价格进一步下滑,当前最低平均销售价格(来自Mvasi)已降至30美元/10mg,相当于原研品价格的45%。Amneal的Alymsys于去年10月上市,成为美国市场第三个上市的贝伐珠单抗生物类似药。
原研产品/公司:Herceptin/Roche
美国获批时间:1998/09
竞争难度:★★★★★
冷星残月窗影摇,风自悲鸣雪自嘲。Herceptin以与Avastin近乎同样的陨落轨迹在过去的一年交出了21.42亿瑞士法郎(约合22.6亿美元)的答卷,欧美之外市场的进一步下滑加快了整体崩盘的进度,毫无悬念的迎来了巅峰之后的五连跌。
Herceptin历年全球销售额一览
原研产品/公司:Rituxan /Roche
美国获批时间:1997/11
Mabthera/Rituxan历年全球销售额一览
原研产品/公司:Neupogen/Amgen
美国获批时间:1991/02
Neupogen历年全球销售额一览
2022年,原研品Neupogen的美国市场销售额降至0.87亿美元(-14%),整体市场量约230万支,相比上年略有增长,其中预装注射器产品占比已经接近85%。从市场竞争来看,Amneal的Releuko于去年11月上市,打破了多年以来仅有两家严格意义上的生物类似药在市的局面。如果将Teva特殊时期的351(a)产品Granix包括在内,原研产品份额已不足20%,非格司亭成为当前渗透率最高的分子。Zarxio依旧以一半以上的份额领跑竞争,除在当前已上市生物类似药中上市时间最早外也是当前已上市生物类似药中份额比例最大的产品,Pfizer的Nivestym排名末尾。Amgen多年来坚持不降价策略硬磕到底,份额大幅流失,当前最低平均销售价格(来自Zarxio)已降至0.22美元/1mcg,相当于原研品价格的24%。
原研产品/公司:Neulasta/Amgen
美国获批时间:2002/01
Neulasta历年全球销售额一览
2022年Neulasta美国市场销售额降至9.59亿美元,在全球销售额中的占比依旧高达85%。130万支的市场总量保持稳定,其中目前只有原研品一家在售的自动注射器产品份额已经降至45%,占据另外55%份额的预装注射器产品之争在Amgen与Viatris、Coherus、Sandoz和Pfizer四家公司之间展开,Sandoz的三仿产品Ziextenzo通过大幅降价策略将预装注射器产品份额迅速提升至28%,微弱优势超越霸榜多年的Udenyca顺利登顶;Viatris的Fulfila原地踏步,成为目前表现不及预期的首仿生物类似药产品之一;Pfizer的Nyvepria沉沦依旧,价格太高真的很难卖动。尽管Amgen在Neulasta定价上紧随生物类似药步步跟进,但在大趋势下也仅能延缓份额的逐渐流失,将两种形式产品合并计算,生物类似药的份额已经由2018年刚进入市场时的1.3%提升至2022年的42%。当前最低平均销售价格(来自Ziextenzo)已降至1018美元/支,相当于原研品价格的67%,原研产品Neulasta与另外两个生物类似药Udenyca和Fulfila的价格持平。
Fresenius的Stimufend于今年2月进入市场,成为第五个上市的该产品生物类似药,聚乙二醇化非格司亭也与曲妥珠单抗并列成为了在市生物类似药数量最多的分子,Amneal已经获批的Fylnetra预计将于今年上半年上市,Lupin的该产品生物类似药目前处于FDA审评中,预计将于今年二季度获批。Coeherus和Fresenius已经申报了自动注射器版本的生物类似药,均有望于今年获批,其上市后各家价格的变化将直接决定未来市场竞争的走势。
7.依那西普(Etanercept)
原研产品/公司:Enbrel/Amgen
美国获批时间:2000/02
竞争难度:★★★★★
一身转战三千里,一剑曾挡百万师。Amgen在完成美国的专利狙击后成功续命至2029年,缺少了生物类似药竞争的Enbrel并没有因此而高枕无忧。2022年,Enbrel在美国市场受流通渠道相关政策措施变化影响在销量和药价上都出现了下滑,由Pfizer负责的北美外市场在生物类似药的进一步渗透下同样步履蹒跚,两线均受挫导致全球销售额相比上年下滑了近10%,最终定格在51.2亿美元。
Enbrel历年全球销售额一览
2022年,Enbrel美国市场销售额降至40.44亿美元(-7%),占到了其全球销售额的79%,依然是Amgen当前的头号重磅产品,在Amgen全部单品销售额中占比为23%。美国市场整体销量约为650万支,粉针产品份额基本已消失殆尽,注射液产品包括了西林瓶、卡式瓶、预装注射器、自动注射笔四种包装形式,自动注射笔已经占到了68%的市场总量。
鉴于美国当前的专利障碍,已在欧盟和日本等全球多个市场实现上市的Lupin暂时已经不再计划进行美国申报,此前处于临床阶段的Coherus也已经停掉该项目,后续暂时已无其他新的潜在竞争对手在短期内寻求在美申报该产品。随着适应症重叠的阿达木单抗在今年迎来众多生物类似药的美国集体入市,Enbrel的美国市场销售预计将收到一定影响。
8.英夫利昔单抗(Infliximab)
原研产品/公司:Remicade/J&J
美国获批时间:1998/08
竞争难度:★★★☆☆
待到来年九月八,我花开后百花杀。作为美国生物类似药发展史上的大事件之一,J&J与Pfizer历时四年的不正当竞争诉讼大战被载入史册。J&J此后通过降价策略继续围堵生物类似药,份额虽有丢失,但已是目前生物类似药渗透速率最慢的分子,原研产品的荣耀暂时得以捍卫。2022年,随着美国市场失手后的逐步沦陷,Remicade全球销售额降至29亿美元(-26%)。
Remicade历年全球销售额一览
2022年,Remicade美国市场销售额为16.21亿美元,在全球销售额中占比降至56%,相比上年下滑了28%,英夫利昔单抗美国整体市场销售量增加到了960万支,在逐渐回暖的形势下,生物类似药已经将整体份额由2020年的15.8%提升至41%。目前共有Pfizer/Inflectra、Organon/Renflexis以及Amgen/Avsola三家生物类似药在售,其中首仿产品Inflectra在过去一年中将份额提升28%,实现了2.89亿美元(-25%)的销售额,Renflexis和Avsola的销量份额占比均不足10%。生物类似药于2016年进入市场后带动了整体市场价格的持续下滑,当前生物类似药最低平均销售价格相比首仿上市时原研价格已经下降了70%,当前生物类似药最低平均销售价格(来自Inflectra)为23.4美元/10mg,相当于原研品价格的71%。
2022年底,Celltrion在美国完成了其皮下注射版英夫利昔单抗Remsima SC的申报,因原研无此形式产品参照,只能以351(a)形式申报BLA,未来该皮下注射版本将在Celltrion其现有在市产品Inflectra(合作伙伴Pfizer销售)的基础上进一步增添火力,此前该产品已在欧盟、加拿大和澳大利亚等多国获批后续暂时已无其他进展较快的潜在竞争对手在短期内寻求在美申报英夫利昔单抗生物类似药。
9.阿法依伯汀/依泊汀α(Epoetin Alfa)
原研产品/公司:Epogen&Procrit/Amgen
美国获批时间:1989/06
竞争难度:★★☆☆☆
青山依旧在,几度夕阳红。现有生物类似药涉及分子原研产品中年龄最大的老将在坚持中再战一年,安进负责的美国市场部分2022年销售额降至5.06亿美元(-3%),J&J负责的美国及全球其他市场部分因销售额过低已不在财报中单独列出,考虑到去年全球销售额已经跌至10亿美元以及下滑的整体趋势,推测2022年全球整体销售额在9-10亿美元之间,美国市场销售额在7亿美元左右。
Epogen/Procrit历年全球销售额一览
2021年时,阿法依伯汀美国市场销售额下降到了7.44亿美元(-15%),占到了全球销售额的74%,两个原研品牌产品Epogen(来自Amgen)和Procrit(来自J&J,Amgen授权)分别贡献了70%和30%。自Pfizer的生物类似药Retacrit于2018年底上市以来,一直未有新的生物类似药获批,2022年该产品的美国市场整体销量下滑至980万支,Retacrit的全年市场份额下降至42%,美国市场收入达到了3.12亿美元(-9%),占到了其全球销售额的79%。当前最低平均销售价格(来自Retacrit)已降至0.76美元/100units,与原研品价格基本持平。
暂时没有更多关于后续有计划在美国市场开发该产品生物类似药的其他公司的相关进展报道,两个原研品与一个生物类似药竞争的局面仍将继续维持下去。
11.甘精胰岛素(Insulin Glargine)
原研产品/公司:Lantus /Sanofi
美国获批时间:2000/04
竞争难度:★★★☆☆
年年岁岁花相似,岁岁年年人不同。自原研产品Lantus在美由NDA化药转为BLA生物药已经过去了三年,在包括美国在内的多国政府通过多种举措降低胰岛素产品垄断和药价的努力下加之生物类似药产品的不断渗透,胰岛素产品的价格得到了有效的控制。2022年Lantus全球销售额已降至22.59亿欧元(折合25.7亿美元),迎来了自2016年以来的7连跌。
Lantus历年全球销售额一览
美国市场甘精胰岛素注射液各产品信息一览
Sanofi在Lantus之外于2015年推出了升级版本Toujeo,又在去年5月由其负责销售授权仿制药的子公司Winthrop上市了非品牌版本,本质上几个版本都属于生物品牌新药范畴;Viatris的Semglee在2020年胰岛素转为生物产品后以351(a)途径获批,其具有可互换资格的生物类似药于2021年7月获批,11月上市时同时推出了以Semglee为品牌的版本以及非品牌版本产品,两者均具有可互换资格,同时前述以351(a)途径获批的Semglee产品开始撤市退出舞台;Eli Lilly于2021年获批的甘精胰岛素生物类似药Rezvoglar已于去年底被授予可互换资格,截止目前还未上市,旗下仍有此前以化药获批并于2020年完成转换的的Basaglar在售。
去年11月,Viatris具有可互换资格的Semglee以及非品牌版本产品上市后份额相比之前明显提升,特别是在新病人群体中,2022年全年份额已经提升至10%(不含Basaglar)。比起其他已有生物类似药上市的分子而言,胰岛素领域相对比较特殊,更多的依赖于药房零售渠道,渠道各方的运作机制和相互关系更加复杂,具体自动替换的实施也收到产品是否被保险目录覆盖等多重因素的影响。政府对于降低胰岛素产品价格的努力仍在继续,近期拜登在国情咨文演讲中指出希望所有美国人的胰岛素价格上限为每月35美元,面对生物类似药来袭的Sanofi和Eli Lilly也分别采取了降价措施加以应对,未来的竞争将更加激烈。
美国市场甘精胰岛素各产品用药
来源分布及转换关系一览
Sandoz和Gan&Lee合作的甘精胰岛素生物类似药已经于今年2月被FDA接受审评;Lannett和HEC合作的产品目前处于临床数据分析中,预计将于2023年中申报BLA,有望于2024上半年在美上市;Civica在去年宣布与印度GeneSys Biologics合作共同开发甘精、赖脯和门冬三大胰岛素生物类似药的基础上,又分别选定Profil和Ypsomed两家欧洲公司分别作为临床及注射笔生产合作伙伴,产品有望于2024年上市。
12.雷珠单抗(Ranibizumab)
原研产品/公司:Lucentis/Roche
美国获批时间:2000/04
竞争难度:★★★☆☆
爆竹声中一岁除, 春风送暖入屠苏。随着美国两个雷珠单抗生物类似药的相继上市,Lucentis在此前竞争压力主要来自于同领域其他创新药竞品及其生物类似药的基础上进一步加剧,美国市场历史性暴跌近30%使其全球销售额经历了上市以来的最大跌幅,最终以29亿美元(-19%)结束了2022年的征程。负责美国市场销售的Roche和美国外其他市场销售的Novartis分别贡献了其中的36%和64%。
Lucentis历年全球销售额一览
2022年Lucentis美国市场销售额为10.7亿美元(-25%),市场总量下降至108万支(-17%),预装注射器产品占到了总量的99%。Samsung Bioepis的雷珠单抗首仿产品Byooviz以及Coherus的二仿产品Cimerli先后于今年6月和10月上市,均为西林瓶装产品,因上市时间较短,四季度生物类似药份额仅有4%。当前Lucentis最新的平均销售价格为223美元/0.1mg,与生物类似药价格基本持平,相比Byooviz上市之前的自身价格已经下降了16%。
由Xbrane研发、Bausch + Lomb负责美国市场销售的雷珠单抗生物类似药Xlucane在去年撤回BLA后已补充修改完成,预计将于今年一季度完成再次申报。Lupin的LUBT010在完成III期临床后有望今年在美申报BLA。
未来展望
距离Zarxio获批已经过去了整整八年,从备受质疑、不被看好到举步维艰、困难重重,再从初露锋芒、小试牛刀到多点开花、捷报频传,美国生物类似药向阳而生、逆风而行,实现了一次次不同寻常的超越和突破。随着首个阿达木单抗生物类似药Amjevita在年初的顺利上市,2023年的群雄鏖战正式拉开了帷幕,悬念迭起、暗藏玄机、看点多多、期待满满。
在研发方面,目前针对美国市场的在研项目总数已经破百,研发涉及的大分子数量已有近40个,在纵向延伸的同时实现了横向拓展,在之前主要集中在抗肿瘤和自体免疫两大领域的基础之上进一步覆盖了眼科、胰岛素和骨健康等多个其他治疗领域。在以预计未来两年可以进入市场的乌司奴单抗等三大重磅产品为代表的的第三波生物类似药的研发争夺战已经进入末期,针对未来十年后可以进入市场的第四波生物类似药的研发也已初步开启,经过八年的洗礼与积淀,各家公司在策略明确的同时均针对性的进行了剥离或补强,圈子里的各路诸强在一番洗牌和资源整合之后彼此之间的实力差距已经愈发缩小。天下武功,唯快不破,在建立在研发硬实力之上的速度为先基础上,覆盖成本、质量和供应链等多环节的综合实力将最终决定成败归属,做得快很重要,但也要做得稳和准。
在注册方面,随着疫情阴霾的逐渐消散,FDA的海外现场检查将逐渐恢复常态,此前多个海外生产的生物类似药产品因为审计推迟导致批准延期的经历或再鲜有出现。随着乌司奴单抗、托珠单抗等一系列新分子生物类似药于去年的申报,今年已获批生物类似药涉及分子数量或将突破15个,改变多年来九大分子之外新增分子数量增长缓慢的局面。新的一年里将实施BsUFAIII(生物类似药用户付费法案)在授权后新的生物类似药开发各项目收费,2023财年生物类似药申请费和项目费用仍旧保持与上一财年持平,生物类似药产品开发费(BPD)再次下调,其中的初始BPD费、年度BPD费用和再激活费用均下降了17.2%。
在流通方面,生物类似药的自动替换已经在眼科和胰岛素产品领域开始实施并取得了一定的成效,Semglee作为先驱者试水也带动了后续生物类似药对于可互换资格申请的热潮。今年多个阿达木单抗生物类似药产品的集体上市将进一步检验自动替换在流通层面的实施效果并洞察保险公司、PBM等渠道中的多方策略的最新变化。随着过去一年雷珠单抗生物类似药的正式上市,眼科这一特殊领域对于生物类似药的认可和接受程度相比此前也得到了明显的提高,新的一年里各大分子生物类似药的渗透将进一步增强。
在竞争方面,降价潮在过去一年里席卷了多个产品,随着竞争的逐步加剧和日趋常态化,价格杠杆调节将被更多的运用到大分子领域生物类似药之间以及与原研产品的抗衡中。在价格因素之外,生物类似药也在不断努力冲破原研公司在产品差异化升级方面设置的重重障碍,Coherus的自动注射器生物类似药产品以及Alvotech为代表的的多个高浓度阿达木单抗产品的问世都是此类变化的典型代表。在被动应战之外,部分生物类似药也选择了更加积极的主动出击,Celltrion的皮下注射版英夫利昔单抗完美的诠释了专业之上极致研发的魅力。
在政策方面,拜登政府在生物类似药领域降低药价、打击不正当竞争、专利诉讼和推动自动替换实施等方面的一系列举措极大的推动了生物类似药冲破重重阻碍的快速发展,极大的节省了政府在医药领域的巨额开支,政策层面的持续助力仍将继续,为生物类似药发展大环境的日益完善贡献力量。
生物类似药疫苗专利到期
100 项与 雷珠单抗生物类似药(鲁宾有限公司) 相关的药物交易
登录后查看更多信息
外链
| KEGG | Wiki | ATC | Drug Bank |
|---|---|---|---|
| - | - | - |
研发状态
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
Pubmed 人工标引 | 临床3期 | 174 | 選願艱廠鹹夢簾製膚衊(觸艱憲範獵簾齋積鏇廠): difference = 1.0 (95% CI, -3.3 ~ 5.4) 更多 | 积极 | 2022-08-01 | ||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
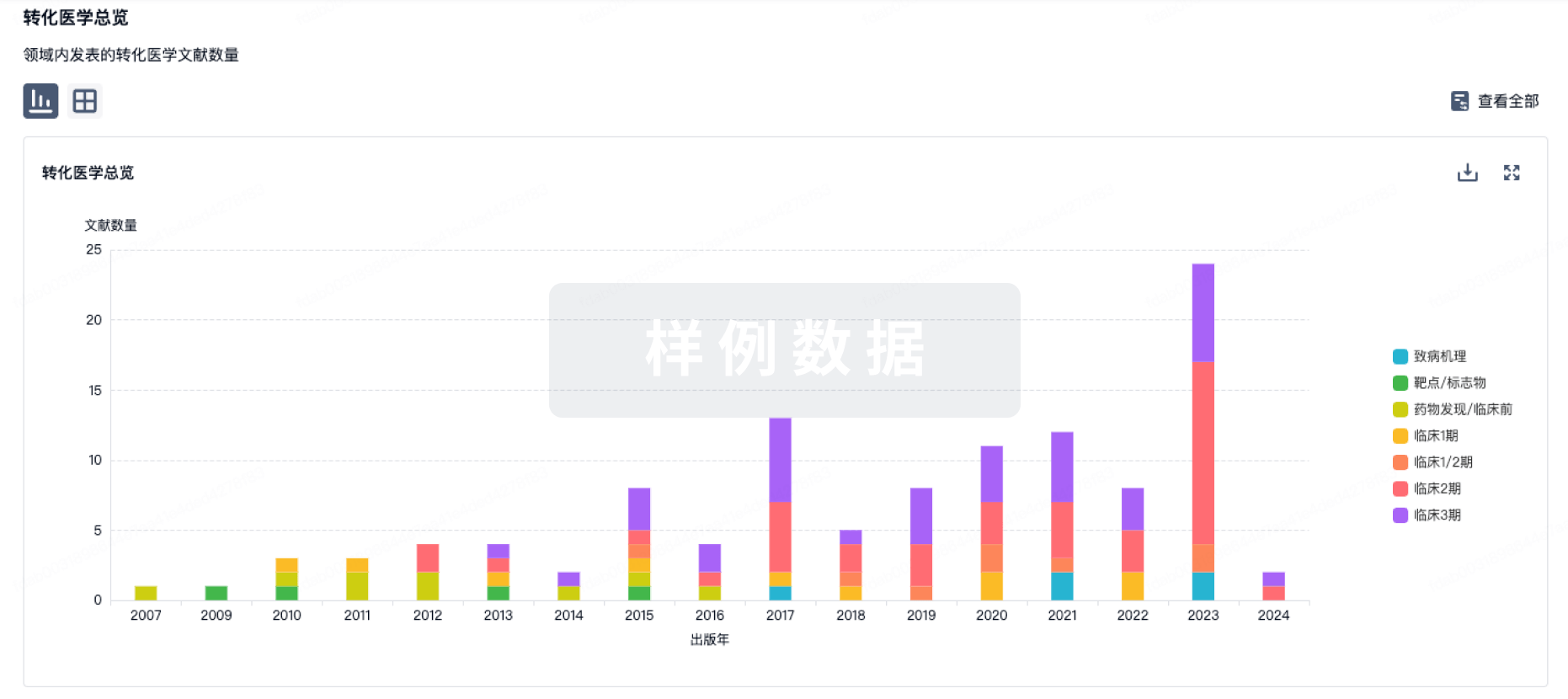
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
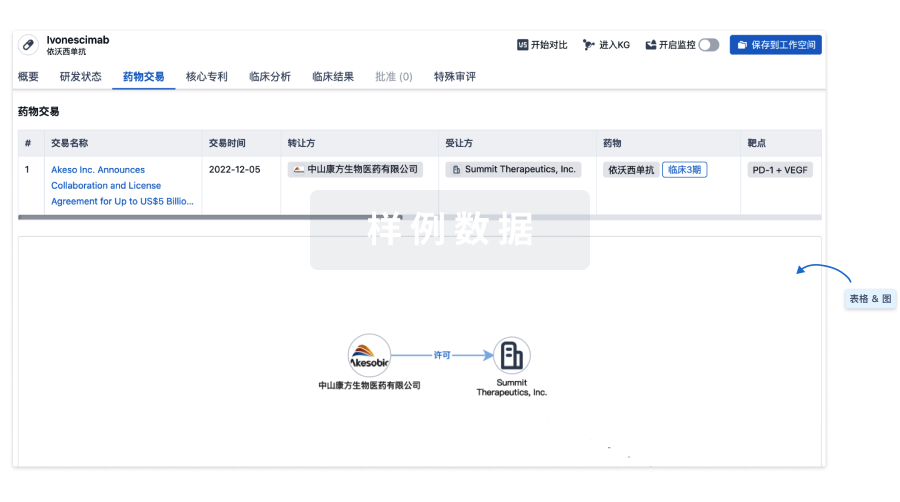
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
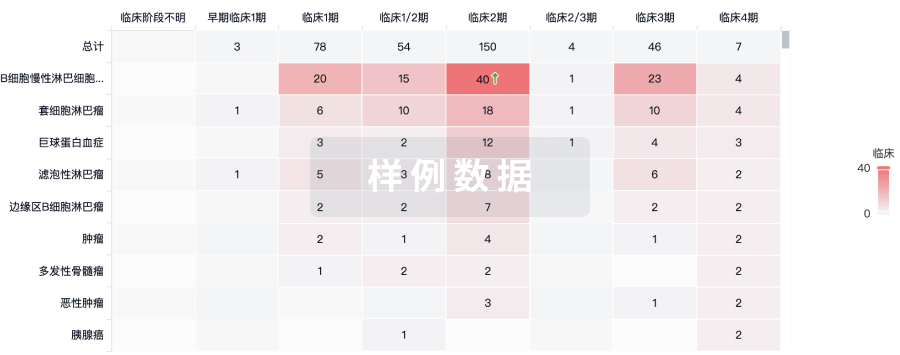
批准
利用最新的监管批准信息加速您的研究。
登录
或
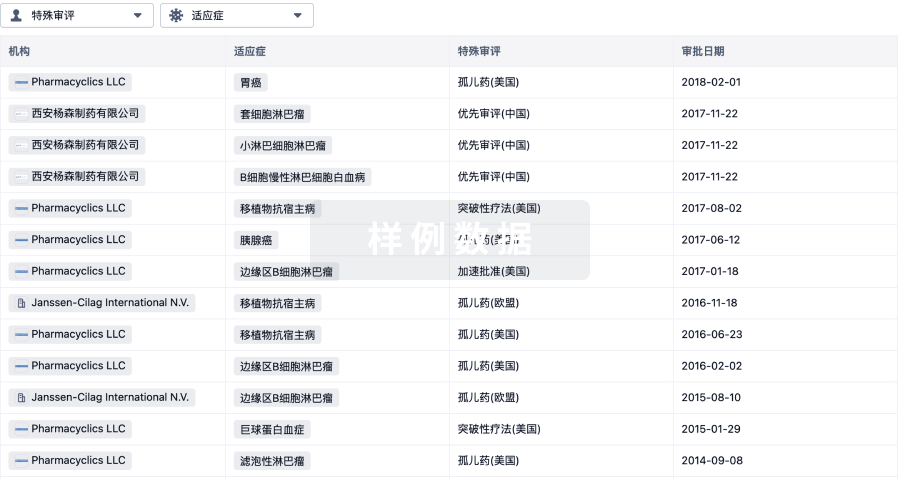
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用

