更新于:2024-11-01

Beijing Jiannenglong Biomedical Technology Co., Ltd.
私营公司|
2012|
中国北京市
私营公司|
2012|
中国北京市
更新于:2024-11-01
概览
关联
100 项与 Beijing Jiannenglong Biomedical Technology Co., Ltd. 相关的临床结果
登录后查看更多信息
0 项与 Beijing Jiannenglong Biomedical Technology Co., Ltd. 相关的专利(医药)
登录后查看更多信息
3
项与 Beijing Jiannenglong Biomedical Technology Co., Ltd. 相关的新闻(医药)2024-09-22
流通、原料药、仿制药、生物药……亿帆医药“大而全”的业务下并未诞生太多的“拳头产品”,虽创新药中美欧上市,但亿立舒所处升白针早已是群雄割据的赛道,创新转型并不算早的亿帆医药,市场给它打几分?
资深分析师:长路
编审:苏叶
业绩触底反弹、创新药出海屡传捷报的亿帆医药,股价却仍在一路滑坡,怎么都刹不住!是投资人想得太多?还是业绩含金量不够?
2023年5月-2024年9月亿帆医药股价走势图
来源丨百度股市通
半年营收增长35%,扣非净利大涨90%在医药股里是个什么水平?
不妨把这个数据放到整个A股来看,据东吴证券统计,今年上半年,405家医药类上市公司的总收入仅实现了0.18%的同比微增,而扣非归母净利润总额则是同比4%的增长。
可以说,在如今这个年月,营收净利均实现双位数大增可以算的上是交出了一份不错的答卷了。
今天故事的主人公亿帆医药,更是凭借着一份四年来交出的最佳半年报,宣告着自己回归增长态势。自2023年大幅亏损以来,亿帆医药如今又“活了”。2024年上半年实现收入26.3亿元,同比增长35.4%;扣非净利润1.8亿元,同比增长90.5%。扭亏为盈的原因,亿帆医药解释的相对直观:国内医药自有产品营业收入大幅增长88.29%是业绩回暖的基础。
从流通商到原料药与仿制药企,再到成为创新药MAH出海第一人,亿帆虽然是行业里少有覆盖化药、中成药、原料药、生物药的全能选手,5年并购十余起,虽成就了“大而全”,但却未诞生太多的“拳头产品”。
加上创新转型的脚步在国内一众传统药企中并不算早,虽有亿立舒加持,但该产品早已是群雄割据的赛道,亿帆医药能从中分几杯羹?此外,自2023年11月实现在FDA上市后,亿立舒的海外供应要到今年9月才能开始,上市后能在海外市场放量吗?CM10医药研究中心将从行业稀缺值、财务健康度、业务健康度、综合建议,来一一回答。
年均5起BD,狂人没有“拳头”
提起产业中的“BD狂人”往往会想起华东医药,2020年阿卡波糖集采失利后华东开启了大手笔的BD交易连续剧。而亿帆医药以BD推动转型的动作,其实要比华东更早上数年。
亿帆医药能成为主营业务板块中同时涵盖化药、中成药、原料药、生物药的全能选手,离不开数年来的收购战略。
亿帆医药的前身,是成立于2003年的“合肥亿帆医药经营”有限公司,这是一家主要从事药品的配送、代理和销售的药品流通公司,并不具有什么创新药基因。
创始人程先锋十多年来一直在医药行业深耕,直到2014年,经过重大资产重组,程先锋将亿帆生物和亿帆药业分别作价14.8亿和2.7亿注入鑫富药业构成借壳上市。
被亿帆“借壳”的鑫富药业,成立于2000年,以精细化工产品、食品和饲料添加剂,泛酸钙等原料药为主营业务。和许多借壳上市的案例不同的是,亿帆医药没有把鑫富药业本来的业务“甩掉”,许多业务至今仍在运行。据亿帆医药年报披露,公司原料药维生素B5及原B5产品全球市场占有率40%~45%,居龙头地位。
借壳上市成功后,恰逢泛酸钙价格上行周期,业绩飘红,钱袋子鼓起来的亿帆医药,自此开启了扩张模式。
2015年,与国药一心签订协议,以2.35亿元自有资金受让国药一心制药的7个血液肿瘤药品种和1个皮肤科肿瘤药品种。
年内亿帆再以自有资金2.4亿元收购收购安徽天康(现名天长亿帆)100%股权,获得治疗白血病、妇科病及品牌OTC等药品批准文号62个,其中独家品种、独家剂型与规格产品10个,中药三类新药产品7个。最具亮点的独家品种为复方黄黛片,主要用于治疗白血病。
同年年底,亿帆又以自有资金3.03亿受让四川天联药业有限公司100%的股权;以自有资金7142万元受让沈阳澳华制药有限公司100%的股权。前者拥有除湿止痒软膏、银杏叶丸等产品;后者的独家产品皮敏消胶囊较为知名。
如今回看亿帆医药在2015年的一系列收购,虽然占用的资金不算大,涉及的赛道很多,包括了肿瘤药、皮肤病药、降血脂中成药,但是却找不出一个重点方向,更像是“有枣没枣先先打一杆子”。
亿帆医药一系列收购的动作被资本市场广泛关注到要从2016年说起。当年,亿帆医药斥资10亿元收购了创新药公司健能隆(后更名为“亿一生物”)53.8%股权,正式进入生物创新药领域,获得双分子技术平台(Di-KineTM)和免疫抗体技术平台(ITabTM),以及在研创新药F-627、F-652。F-627也就是如今的亿立舒。
同年,公司中文证券简称由“亿帆鑫富”变更为“亿帆医药”,证券代码不变。
拿下健能隆后,亿帆医药展现出了国际化的野心。
2017年,亿帆再以1.36亿元收购了进口药品代理商业公司NovoTek的100%股权,为后续公司引进进口产品打开通道,并为公司国际化战略奠定基础。
自2018年起,亿帆医药的关注重心基本就移到了胰岛素上。先以2.5亿人民币从Summit Bioteck收购了胰岛素类似物产品(Insulin Analogues)平台技术;然后要约收购了赛臻公司(SciGenLtd),后者的业务同样也是胰岛素;与佰通公司(Bioton S.A.)签订了《全球产品代理协议》,成为其重组人胰岛素国际销售的唯一代理商。
次年,亿帆医药又拿下了佰通公司31.65%股权,成为其第一大股东。而佰通此前正是赛臻的母公司。
此外值得一提的是,2018年底,亿帆医药以3000万美元收购了注册于意大利的非索医药和特克医药,从而拥有了具有美国FDA与欧盟GMP等审计认证的小分子注射剂药品的生产能力和质控水平,以及意大利、德国、加拿大、克罗地亚、荷兰、英国、以色列等10余个国家或地区的药品销售与市场资源。
据不完全统计,自2014年至2019年的数年,由亿帆医药发起的并购不低于15起,涉及金额高达30亿元左右。
经过一系列收购布局,亿帆医药的主营业务从原料药、医药商业跨越到医药生产、研发领域,形成了大分子、小分子、特色中药、原料药四大核心板块,并成功实现海外布局,为后续拓展海外市场奠定了基础。
持续的并购也让亿帆医药的业绩得到迅速提升,2014年-2020年,亿帆医药的营业收入从16.85亿元增长至54亿元,净利润也从2.38亿元增长至最高13.05亿元。
亿帆医药营收及增速
来源丨同花顺
杀入卷王赛道,差点运气
然而,亿帆业绩增长的势头,因突如其来的新冠疫情而戛然而止。
在转型路上雄心壮志的亿帆,受疫情等因素的影响,亿帆医药2018年启动的第三代胰岛素项目的研发遇阻。
屋漏偏逢连夜雨,国家第六批集中带量采购导致胰岛素市场大幅“缩水”,国内胰岛素龙头甘李药业、通化东宝等都出现了业绩承压,亿帆医药代理的波兰佰通第二代胰岛素A类虽然中标,销量增长了42.83%,但销售收入却下降了18.63%。可以说,胰岛素发展战略受挫,元气大伤。
此时就不得不提亿帆生物业绩的另一个“寄托”——亿一生物的艾贝格司亭α注射液(F-627,亿立舒)。
2023年5月,艾贝格司亭α注射液(亿立舒)在国内获批上市。亿立舒正是亿帆医药旗下首款获批上市的大分子创新药,亿立舒的获批上市让亿帆医药开启了从中药、仿制药向创新药转型的序幕。
虽然如今肿瘤新疗法此起彼伏,但许多患者依然需要接受化疗,并承受其副作用,对升白药(G-CSF)的需求一直在增长。据弗若斯特沙利文预测,中国长效G-CSF类药物在2025年预计达到102.70亿元的销售规模,在2030年将达到135.37亿元。
作为与安进的原研Neulasta头对头达到非劣效果的自主研发创新型1类生物药,全球首个双分子G-CSF Fc融合蛋白,亿帆医药对亿立舒寄予了厚望。
然而现实残酷,升白药赛道太卷了。前有安进的原研药,后有百克生物的津优力(培非格司亭,2011年获批上市)、齐鲁的新瑞白(培非格司亭,2015年获批上市)、恒瑞的艾多(硫培非格司亭,2018年获批上市)、鲁南的申力达(培非格司亭,2021年获批上市)。
国内长效G-CSF的市场格局基本已经“定型”了。据药渡数据,在2022年,国内长效G-CSF呈现三足鼎立的局面,其中石药百克销售额25.99亿元,市占率40.12%;齐鲁制药销售额22.78亿元,市占率35.16%;恒瑞医药销售额15.53亿元,市占率23.96%。获批时间较晚的产品已经很难撼动巨头的地位,如新时代药业的产品市占率仅0.76%。2023年才姗姗来迟的亿立舒入场时间显然已经有点晚了。
可想而知,同样获批上市的时间较晚的亿立舒想从中切下一块蛋糕,并非易事。亿帆也了解,早在2021年就与正大天晴签署了合作协议推进亿立舒的商业化,抱大腿,分散风险。根据正大天晴对亿立舒的预测,预计该产品2023年至2025年国内销售额分别为8.52亿元、23.9亿元、30.24亿元,期间CAGR将达到88.36%。
但理想很丰满,现实很骨感。亿立舒上市后销售不及预期,亿帆医药只能在财报中进行大额减值。
今年1月底,亿帆医药发布公告,宣布对控股子公司亿一生物自主研发的无形资产F-627进行减值计提,该资产原值为16.84亿元,拟计提减值准备8亿-8.8亿元,预计减少归属于上市公司股东净利润4.86亿-5.47亿元。
关于该项操作的原因,亿帆医药认为:虽然艾贝格司亭α注射液于2023年先后在中国、美国成功获批,但全球市场竞争格局与竞争态势发生重大变化,竞品数量增加及竞品价格下降,对公司的产品呈现不利影响,预计未来可收回金额不及预期,因此导致减值。
相比于其他药企在研发失败之后进行计提减值,这是极其罕见的在药物刚刚上市,相关公司就进行资产减值。
到了今年4月20日,亿帆医药发布公告称,本次计提资产减值准备合计约9.52亿元,其中对亿立舒的无形资产计提就高达8.48亿元。直接导致的结果是,2023年,亿帆医药的利润为负值,亏掉5.5亿元,同比下降388%。
随着2023年12月亿立舒成功纳入国家医保目录,并在2024年上半年加速放量,有分析师认为,亿立舒在国内的销售峰值有望达到20亿元。
只不过,亿立舒所要攻克的是“前有来者后有追兵”的战局。在亿帆之后,国内市场又陆续有特宝生物的拓培非格司亭、双鹭药业的聚乙二醇化人粒细胞刺激因子注射液的同类药物获批,20亿元的销售峰值能否兑现,还要先画个问号。
MAH出海第一人,想象力多少?
但不要忘了,亿立舒是国内唯一一个海外市场获批的产品,所以市场还有额外的期待:亿立舒能否在海外市场放量。
作为肿瘤化疗后防治中性粒细胞减少症的第三代长效G-CSF,艾贝格司亭α注射液是目前全球G-CSF治疗药品中既与长效原研产品,也与短效原研产品进行头对头对比临床研究并达到预设目标、并实现中国、美国、欧洲同步申报上市的在研产品。
据亿帆医药此前介绍,在中国、欧洲及美国分别开展的三项III期临床试验结果显示,在一些具有临床意义的指标上,亿立舒的临床疗效优于临床上原研短效升白药(非格司亭)和长效升白药(培非格司亭)。
2023年11月,亿立舒的在美上市申请(商品名:Ryzneuta)获FDA通过。亿帆医药便成为了国内首家以药品上市持有人(MAH)身份在美国FDA获得批准的创新生物药企业。
今年3月,该药品又获准在欧盟上市。
至此,艾贝格司亭α注射液在一年不到的时间内,成功实现在中国、美国、欧盟等全球主要市场的上市。这种速度,在众多的出海的国产药物中,也能称得上是佼佼者。
在研管线
来源丨亿一生物官网
海外市场上,目前亿立舒已在美国、欧盟、冰岛、挪威等多个国家获批上市,但尚未贡献收入。亿帆医药已计划今年9月底开始向境外市场发货,今年下半年,亿立舒的海外市场或迎来“0”的突破。至于销售情况如何,需要等到年报见分晓。
在大分子领域,除了亿立舒,亿帆医药还有另一款重磅在研产品F-652,一款重组人白介素22-Fc融合蛋白,用于治疗慢加急性肝衰竭、重度酒精性肝炎等治疗领域的中美双报产品,同时也是全球首创IL-22抗体的药物。
2023年底,慢加急性肝衰竭(ACLF)中国II期临床试验结果显示,F-652在乙肝并发ACLF的病人中安全性和PK/PD特征良好,同时也显示了F-652能产生比现有治疗手段更显著临床疗效的趋势。目前,亿帆医药已与国内监管机构就ACLF 适应证IIb临床试验达成了共识,同时治疗重度酒精性肝炎(AH)适应证的II期临床试验获得美国 FDA默示许可。有机构预测,这一产品的全球峰值销量将超过10亿美元。
在整体研发上来看,亿帆医药已经在旧金山、上海、北京、杭州、合肥搭建了五大自主科研中心,持续加码。2018-2023年,亿帆医药的研发投入基本保持在5亿元左右,近6年研发总投入超32亿元。在研管线50条,覆盖创新药、生仿药、仿制药、中成药、合成生物等,聚焦血液肿瘤、机体炎症、内分泌/代谢、皮肤科、妇儿科等疾病领域。
曾有亿一生物的内部人士向外界透露,随着亿立舒完成中、欧、美三地上市也就意味着这套兼顾三地上市的策略将得到充分验证,新药研发能力获得了国际认可。在此基础上,后续管线,如F-652也将跑得更快。
市场正在拭目以待,亿帆医药的“出海”能否成为其业绩的下一个增长点,不过已经可以预见的是,亿立舒的海外获批,正在加速亿帆医药的全球商业化收获期。
“ 任何伟大的变革都是痛苦的。我们已经见证了,诸多仿制药企走向创新药企历经的黑暗与迷茫岁月。我们已经看见了,一些蜕变,和新价值的诞生。E药经理人旗下CM10医药研究中心致力于上市公司的价值发现、挖掘与诊断。”
免责声明:本文章是基于上市公司的公众公司属性、以上市公司公开披露的信息(包括但不限于临时公告、定期报告和官方互动平台等)为核心依据的独立第三方研究;CM10医药研究中心力求报告(文章)所载内容及观点客观公正,但不保证其准确性、完整性、及时性等:本报告(文章)中的信息或所表述的意见不构成任何投资建议,CM10医药研究中心不对因使用本报告(文章)所采取的任何行动承担任何责任。
一审| 黄佳
二审| 李芳晨
三审| 李静芝
精彩推荐
CM10 | 集采 | 国谈 | 医保动态 | 药审 | 人才 | 薪资 | 榜单 | CAR-T | PD-1 | mRNA | 单抗 | 商业化 | 国际化 | 猎药人系列专题 | 出海
启思会 | 声音·责任 | 创百汇 | E药经理人理事会 | 微解药直播 | 大国新药 | 营销硬观点 | 投资人去哪儿 | 分析师看赛道 | 药事每周谈 | 医药界·E药经理人 | 中国医药手册
创新100强榜单 | 恒瑞 | 中国生物制药 | 百济 | 石药 | 信达 | 君实 | 复宏汉霖 |翰森 | 康方生物 | 上海医药 | 和黄医药 | 东阳光药 | 荣昌 | 亚盛医药 | 齐鲁制药 | 康宁杰瑞 | 贝达药业 | 微芯生物 | 复星医药 |再鼎医药|亚虹医药
跨国药企50强榜单 | 辉瑞 | 艾伯维 | 诺华 | 强生 | 罗氏 | BMS | 默克 | 赛诺菲 | AZ | GSK | 武田 | 吉利德科学 | 礼来 | 安进 | 诺和诺德 | 拜耳 | 莫德纳 | BI | 晖致 | 再生元
并购
2024-08-21
近日,亿帆医药发布2024年半年度报告。2024年上半年实现收入26.3亿元,同比增长35.4%;归母净利润2.5亿元,同比增长133%;扣非净利润1.8亿元,同比增长90.5%。
这是亿帆医药自2023年大幅亏损以来实现的扭亏为盈,也是其近4年来最佳半年报业绩。支撑其业绩快速扭亏为盈的主要因素是国内医药自有产品营业收入大幅增长,达到16.5亿元,同比增长88.29%,为营收结构持续优化和利润率提高奠定了基础。
同时,首款创新生物药亿立舒纳入医保目录后迎来加速放量,标志着亿帆医药开启了从中药、仿制药向创新药转型的序幕。
老牌收购之王
亿帆医药成立于2003年,创立之初主要专注于药品流通环节,从事药品的配送、代理和销售。2009年,亿帆医药基本完成了安徽省内的销售渠道建设,并在全国范围内进行业务布局。
2014年,亿帆医药借壳以泛酸钙等原料药作为主营业务的鑫富药业登陆A股市场。
借壳上市后的亿帆医药,恰逢泛酸钙价格走出历史罕见的牛市,公司业绩一路高歌猛进,手里现金充裕后就开启了一系列的收购。
2015年,亿帆医药以2.4亿元收购收购安徽天康 100%股权,获得 62 个治疗白血病、妇科病及品牌 OTC 等药品批准文号,其中独家品种、独家剂型与规格产品10个,中药三类新药产品7个;
同年年底,以3.03亿元、7142万元收购沈阳澳华、四川天联 100%股权,获得除湿止痒软膏、银杏叶丸、皮敏消胶囊等皮肤科、心脑血管等领域产品;
2016 年,耗资10亿元收购创新药公司健能隆(后更名为“亿一生物”)53.8%股权,正式进入生物创新药领域,获得双分子技术平台(Di-KineTM)和免疫抗体技术平台(ITabTM),以及在研创新药 F-627、F-652;
2017 年,以1.36亿元收购了进口药品代理商业公司NovoTek的100%股权,为后续公司引进进口产品打开通道,并为公司国际化战略奠定基础;
2018年,以2800万美元收购赛臻公司不低于 90%股份,拓展亚太地区销售推广渠道;
2019年,花费7.1亿元拿下了佰通公司31.65%股权,成为其第一大股东,将业务拓展至胰岛素领域。
据统计,2014年-2019年,亿帆医药发起的并购案不低于15宗,涉及金额高达30亿元左右。
经过一系列收购,亿帆医药的主营业务从原料药、医药商业跨越到医药生产、研发领域,形成了大分子、小分子、特色中药、原料药四大核心板块,并成功实现海外布局,为后续拓展海外市场奠定了基础。
并购项目也让亿帆医药的业绩得到迅速提升,2014年-2010年,亿帆医药的营业收入从16.85亿元增长至54亿元,净利润也从2.38亿元增长至最高13.05亿元。
亿帆医药营收变化情况
图片来源:同花顺财经
然而,2021年受新冠疫情以及药品集采政策推进的影响,亿帆医药的业绩出现下滑,2021年及2022年连续两年营收下降,净利润也大幅萎缩。
但随着疫情影响逐渐消退,前期的创新及国际化布局逐渐兑现价值,产品结构持续优化,业绩将重回增长轨道。
四大核心板块
半年报显示,推动亿帆医药业绩增长的核心驱动力是医药板块中医药自有产品(含进口)取得突破,实现营收18.56亿元,同比增长76.58%。其中境内部分,自有生物药产品(含进口)收入0.88亿元,同比增长154.11%;化药自有(含进口)产品收入9.4亿元,同比增长130.64%;中药自有产品收入6.14亿元,同比增长51.72%。
2020-2024年上半年同期国内自产(含进口)销售变动额
图片来源:亿帆医药
在大分子领域,自研的三代长效G-CSF亿立舒于2023年上市,同年进入国家医保,并同时在中美欧三地获批,是首个以药品上市持有人(MAH)身份在美国FDA获得批准的创新生物药,还是目前全球G-CSF治疗药品中既与长效原研产品,也与短效原研产品进行了头对头临床对比研究而且达到临床预设目标的产品。
目前,亿立舒已在31个国家/区域获准上市销售,2024年迎来首个完整销售年度,2024年上半年境内累计发货超过11万支,并计划9月底陆续向境外部分市场发货,届时终端市场将有望实现加速放量。
在小分子领域,以特色原料+高端辅料为基础,围绕“小、尖、特”及“可快速实现销售”的布局初步实现差异化产品组合,拥有高端化药研发生产制造平台和与国际接轨的高标准生产质量管理体系。是国内为数不多同时拥有境内外成熟的化药直营和分销体系,以及药品研产销境外一体化产业布局的中国医药企业之一。
在中成药领域,拥有108个中药品种,包括柏雪康(复方黄黛片)、小儿青翘颗粒、除湿止痒软膏等独家中药医保产品14个,国家基药目录产品6个,国家中药二级保护品种1个,世界卫生组织基本药物标准清单1个,是拥有独家产品,尤其是独家医保或基药产品数量较多的国内医药企业之一。此外,亿帆医药还拥有三个成功实现海外注册的中药产品,复方银花解毒颗粒、麻芩消咳颗粒以及银杏叶丸。
在原料药领域,面临竞争加剧、下游需求持续偏弱等情况,亿帆医药通过降本增效与强化管理,产品销售价格大幅下降,但主要产品销量获得大幅提升,维生素B5在全球市场的占有率达到40%-45%,继续保持在细分领域的市场龙头地位。
然而,虽然亿帆医药通过前期的大量收购,实现了在四大领域的全面布局,但始终缺乏一款或者多款重磅品种,作为拳头产品。
因此,近年来亿帆医药也在积极培育重点品种。2024年上半年,国内药品业务中有22个自有(含进口)产品实现销售收入过千万元,合计15亿元,同比增长102.6%,其中过亿元产品5个、过五千万元产品3个,形成了“大品种群、多品种群”稳步发展的态势。
将收购的资源整合在一起发挥协同效应,只是亿帆医药发展战略的第一步。在保持原有业务,尤其是优质业务的基础上,不断创新,进行转型升级,才是接下来亿帆医药发展的重中之重。
研发创新之路
在研发方面,亿帆医药围绕四大核心业务,在旧金山、上海、北京、杭州、合肥搭建了五大自主科研中心,持续加码创新研发。2018年-2023年,研发投入6.2亿元、4.98亿元、5.99亿元,5.23亿元,5.2亿元、5.2亿元,近6年研发投入超32亿元。
目前已初步形成了差异化、多元化、有竞争力的产品研发管线,拥有近50个在研产品,覆盖创新药、生仿药、仿制药、中成药、合成生物等,聚焦血液肿瘤、机体炎症、内分泌/代谢、皮肤科、妇儿科等疾病领域。
在大分子领域,除了亿立舒已获得NMPA和FDA批准上市外,亿帆医药还有另一款重磅在研产品F-652,一款重组人白介素22-Fc融合蛋白,用于治疗慢加急性肝衰竭、重度酒精性肝炎等治疗领域的中美双报产品,同时也是全球首创IL-22抗体的药物。
2023年底,慢加急性肝衰竭(ACLF)中国II期临床试验结果显示,F-652在乙肝并发ACLF的病人中安全性和PK/PD特征良好,同时也显示了F-652能产生比现有治疗手段更显著或者更重要临床疗效的趋势。目前,亿帆医药已与中国监管机构就ACLF 适应症IIb临床试验达成了共识,同时治疗重度酒精性肝炎(AH)适应症的II期临床试验获得美国 FDA默示许可。值得期待的是,该药市场潜力巨大,部分机构预测全球峰值销量将超过10亿美金,预计最快明年申报上市。
大分子研发管线
图片来源:亿帆医药
在小分子化药研发方面,近年来将战略定位由单一仿制向改良型和有一定技术壁垒的创新药正式过渡。2024年上半年,获得了二氮嗪口服混悬溶液等5个产品注册证书,并提交了维生素K1注射液等5个制剂产品注册申报或再注册。
在中药研发领域,坚持经典发现与经典创新并举,对可能性方案展开科学验证,不断发掘具有临床价值的有效产品。一方面,继续推动产品上市后研究和开发;另一方面,继续推进中药1.1类新药断金戒毒胶囊Ib期患者临床研究、4个经典名方中药制剂和改良型新药研究工作。
在原料药领域,明确将合成生物学做为未来发展的方向,首个运用合成生物学技术研发的维生素产品已基本完成第四个里程碑的研究内容,目前处于验收阶段。杭州合成生物产业园土建工程建设和生产线设备招标采购工作正在进行中,以确保新技术研发的维生素产品及营养品顺利投产。
与国内部分医药企业不同,亿帆医药深入布局国际市场,在医药研发上能实现国际国内协同,对国际国内的审批政策和前沿研究有信息交流和共享的渠道,可以最大程度兑现创新价值,是为数不多真正可以走出去的中国药企。
结语
从医药销售到医药生产,再到创新药研发,亿帆医药一路走来,四面出击,斩获颇丰。如今在生物创新药方面取得重大突破,后续研发管线梯队合理,有望形成良性循环,值得持续关注。
参考资料
1.亿帆医药年报、公告
2.《亿帆医药:业绩拐点到来,迈入“创新国际化”成长新阶段》,华福医药,2024年07月21日
3. 《亿帆医药F-652治疗慢加急性肝衰竭II期研究成功》,医药魔方,2023年12月22日
并购财报
2024-06-05
·药时代
错过了「星起点」宣讲会?问答实录拿走不谢~
正文共: 3391字 7图
预计阅读时间: 9分钟
2024年6月3日
医麦客新闻 eMedClub News
备受全球瞩目的 2024 年美国临床肿瘤学会(ASCO)年会将于美国东部时间 5 月 31 日至 6 月 4 日在芝加哥盛大召开。本届 ASCO 年会的主题为癌症治疗的艺术与科学:从舒适医疗到疾病治愈。ASCO一直是抗肿瘤药物的盛宴,可以看作是各家药企肿瘤药物的“秀场”让大家能够欣赏其亮眼的临床数据。
其中抗体药物方兴未艾,一直以来都具有很高的热度。在近几年的抗体药研发中,双抗一直备受关注。双特异性抗体是指可以同时结合两个不同抗原或一个抗原不同表位的抗体,可通过其特有的作用方式,如衔接T细胞和肿瘤细胞、协同抑制信号通路、形成蛋白复合物等,发挥单抗无法实现的生物学功能。简单来讲,双抗药物是两个不同的单抗结构融合而形成,一直具有很高的热度,有望成为未来临床的重要选择。下表不完全总结了在2024 ASCO年会中国上展示的双抗。
CD3位居双抗靶点热度榜首
eMedClub
从表格中,可以看出,双抗中有PD1靶点的有康方生物,健信生物,荣昌生物等。PDL1靶点的有天境生物,原启生物,齐鲁制药等,4-1BB的有天境生物,齐鲁制药,维立志博等,这些靶点也都具有很高的热度。其中,可以看到CD3在多个四分之一的双抗中都有出现,数量居高,可以说是位居榜首,备受人们关注。
CD3蛋白是免疫系统中关键的分子之一,参与激活细胞毒性T细胞(CD8+初始T细胞)和T辅助细胞(CD4+初始T细胞),负责监测和抵御体内的感染和异常细胞。CD3靶向药研究最多的就是双抗,CD3双抗能够使CD3+ T细胞重定向靶向杀伤癌细胞。目前,海内外布局CD3靶点相关生物药研究管线的公司和机构很多。在国内市场,CD3同样是药物研发的热门靶点。
2024ASCO大会上CD3双抗关键管线盘点
eMedClub
BI 764532
eMedClub
2023年7月24日,勃林格殷格翰靶向DLL3/CD3双抗BI 764532用于治疗复发性/难治性广泛期小细胞肺癌(ES-SCLC)和其他复发性/难治性神经内分泌癌患者的II期临床试验获得中国国家药品监督管理局(NMPA)药品审评中心批准。
DLL3是Notch信号通路的配体,能够选择性地在小细胞肺癌和肺外神经内分泌肿瘤细胞中表达。BI 764532 (NCT04429087) 在预处理的 DLL3 阳性肿瘤患者中的 I 期试验显示,总体缓解率为 28%,疾病控制率为54%,安全性可控。
据公开信息显示,截止2023年7月7日,全球共有 5 款(Tarlatamab,B1 764532,89ZrZr-B1 764532,PT217,QLS31904)靶向 DLL3 的双特异性抗体进入临床阶段,包括 4 款 DLL3/CD3 双抗。其中进展最快的当属 Tarlatamab,其余均处于早期临床阶段。
CN201
eMedClub
CN201是同润生物医药有限公司的一款CD19/CD3双抗。同润生物医药是一家肿瘤免疫治疗药物研发商,致力于研发下一代肿瘤免疫治疗药物,其研发管线中拥有数个具有竞争力的全新肿瘤免疫治疗分子。
2018年7月27日,同润生物医药有限责任公司宣布完成1.5亿美元A轮融资,本次融资由通和毓承、博裕资本以及淡马锡共同投资。同润生物致力于研发下一代肿瘤免疫治疗药物,应用独特生物技术及多种协同组合联合疗法,研发针对恶性肿瘤的下一代创新疗法,使癌症成为可控的慢性疾病。现已布局并构建丰富且极具竞争力的产品管线,拥有数个具有创新性的新一代肿瘤免疫治疗分子,其研发管线中拥有数个具有竞争力的全新肿瘤免疫治疗分子。
CN201在针对复发或难治性急性淋巴细胞白血病患者中的Ⅰ期临床实验显示,完全缓解率(CR)为30%,37位受试者中,有1例有完全缓解和不完全血液恢复 (CRi),75% 的应答者有 MRD 阴性。
针对CD3×CD19靶点,国内多家企业也在加速创制,包括绿竹生物、健能隆、爱思迈、同润生物等公司(据不完全统计):
IBI389
eMedClub
2022年3月30日,信达生物制药集团宣布其自主研发的重组靶向紧密蛋白连接蛋白18.2(Claudin18.2,CLDN18.2)和分化抗原簇3(CD3)的双特异性抗体IBI389在治疗晚期恶性肿瘤的I期临床试验中完成首例患者给药。IBI389通过连接T细胞受体复合物中的CD3分子和肿瘤细胞膜上的CLDN18.2抗原,诱导免疫突触的形成。
截至 2024 年 1 月 31 日,IBI389的ORR为30.4%(95%CI:13.2-52.9),DCR为69.6%(95%CI:47.1-86.8)。有关安全性和有效性的更多最新数据将在会议上公布。
当前全球共有 13 个 CD3/CLDN18.2 双特异性抗体和 1 个抗体类融合蛋白在研,其中最快的 4 个项目处于 I 期临床阶段,分别来自安斯泰来(ASP2138)、信达生物(IBI389)、齐鲁制药(QLS31905)和安进/百济神州(AMG910);AZD5863 / HBM7022 如今也已申报临床。可以看出,在第一梯队里中国企业身影频现。
M701
eMedClub
2024年3月4日,国家药品监督管理局药品审评中心(CDE)官网显示,由武汉友芝友生物制药有限公司研发的注射用重组抗EpCAM和CD3人鼠嵌合双特异性抗体(M701)已经开始Ⅲ期的临床研究,正在招募晚期上皮性恶性实体瘤(包括卵巢癌、胃癌、结直肠癌)伴恶性腹水患者入组。
武汉友芝友生物制药股份有限公司是一家致力于开发用于治疗癌症相关并发症、癌症及老年性眼科疾病的基于双特异性抗体(BsAb)疗法的生物技术公司,以解决肿瘤学及老年眼科病领域的医疗需求。
M701是友芝友生物通过自主专利非对称双特异性抗体YBODY®平台开发的同时靶向EpCAM和CD3的生物一类新药,已于2016年获批开展治疗恶性腹水的临床研究,是中国第2个由国内企业研制并获批进入临床的双特异性抗体。M701双抗一端靶向EpCAM抗原,同时通过另一端CD3抗体可以桥接T细胞并激活T细胞杀伤EpCAM阳性肿瘤细胞。目前,M701正在开展联合全身治疗对恶性腹水的II期安全性和疗效研究,与腹腔化疗组相比已初步显示出更好的腹水控制效果。
基于全身肿瘤治疗的 M701 IP 输注耐受性良好,不会造成更高的风险。接受 M701 治疗的 MA 上皮癌患者具有更长的 PuFS (无穿刺生存期)和 OS(总生存期)。这些结果是有希望的,并支持M701作为MA新疗法的关键试验。
在同靶点的研究中,2023年3月24日,据CDE官网显示,天劢源和生物医药有限公司提交的“重组抗EpCAM-CD3抗体注射液”新药研究性申请获得受理。
epcoritamab-bysp
eMedClub
艾可瑞妥单抗,是由Genmab 和艾伯维共同开发的一种皮下注射的 CD20×CD3 T 细胞接合双特异性抗体,通过与T细胞表面的CD3及B细胞表面的CD20相结合,激活T细胞表面的CD3及B细胞表面的CD20,发挥免疫抑制作用。用于治疗成熟 B 细胞非霍奇金淋巴瘤亚型(B- NHL),包括弥漫性大 B 细胞淋巴瘤 (DLBCL)。
试验结果证明,艾可瑞妥单抗(Epkinly)的客观缓解率(ORR)为63.1%,完全缓解率(CR)在38.9%。安全性良好。
CD20/CD3双抗已有同类药物上市,罗氏开发的Mosunetuzumab,靶向CD20/CD3,利用Knob-In-Hole技术防止抗体重链错配,该抗体的Fc同样进行了突变沉默ADCC等效应。目前该抗体已经被FDA授予突破性药物资格。
结语
eMedClub
相信随着更多靶点的发现和更多样化设计的分子形式的涌现,双抗在实体瘤领域也必将迎来重大的突破。当然,药物开发要平衡有效性和安全性,CD3多特异性细胞连接器普遍出现发生率比较高的CRS(细胞因子释放综合征),毒性问题是一个挑战,很多公司也想出来了很多应对方法。CD3靶点一直热度颇高,这么多款CD3靶点的双特异性抗体真的很值得期待。
参考资料:
[1]https://www.asco.org/
声明:本文旨在于传递行业发展信息、探究生物医药前沿进展。文章内容仅代表作者观点,并不代表医麦客立场,亦不构成任何价值判断、投资建议或医疗指导,如有需求请咨询专业人士投资或前往正规医院就诊。
封面图来源:123rf
版权声明/免责声明
本文为授权转载文章。
本文仅作信息交流之目的,不提供任何商用、医用、投资用建议。
文中图片、视频、字体、音乐等素材或为药时代购买的授权正版作品,或来自微信公共图片库,或取自公司官网/网络,部分素材根据CC0协议使用,版权归拥有者,药时代尽力注明来源。
如有任何问题,请与我们联系。
衷心感谢!
药时代官方网站:www.drugtimes.cn
联系方式:
电话:13651980212
微信:27674131
邮箱:contact@drugtimes.cn
股价一度跌近10%,市值蒸发80亿美元!GSK或将面临巨额索赔
ASCO速递:从“低表达”到“更低表达”,最畅销 ADC进入next level!
全球首款mRNA RSV疫苗获批,但公司股价却大跌,为何?
从1000亿到1580亿,全球「减重药」市场又增重了!
点击阅读原文,把握BD机会!
ASCO会议临床1期临床结果免疫疗法
100 项与 Beijing Jiannenglong Biomedical Technology Co., Ltd. 相关的药物交易
登录后查看更多信息
100 项与 Beijing Jiannenglong Biomedical Technology Co., Ltd. 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2024年11月20日管线快照
无数据报导
登录后保持更新
药物交易
使用我们的药物交易数据加速您的研究。
登录
或

转化医学
使用我们的转化医学数据加速您的研究。
登录
或
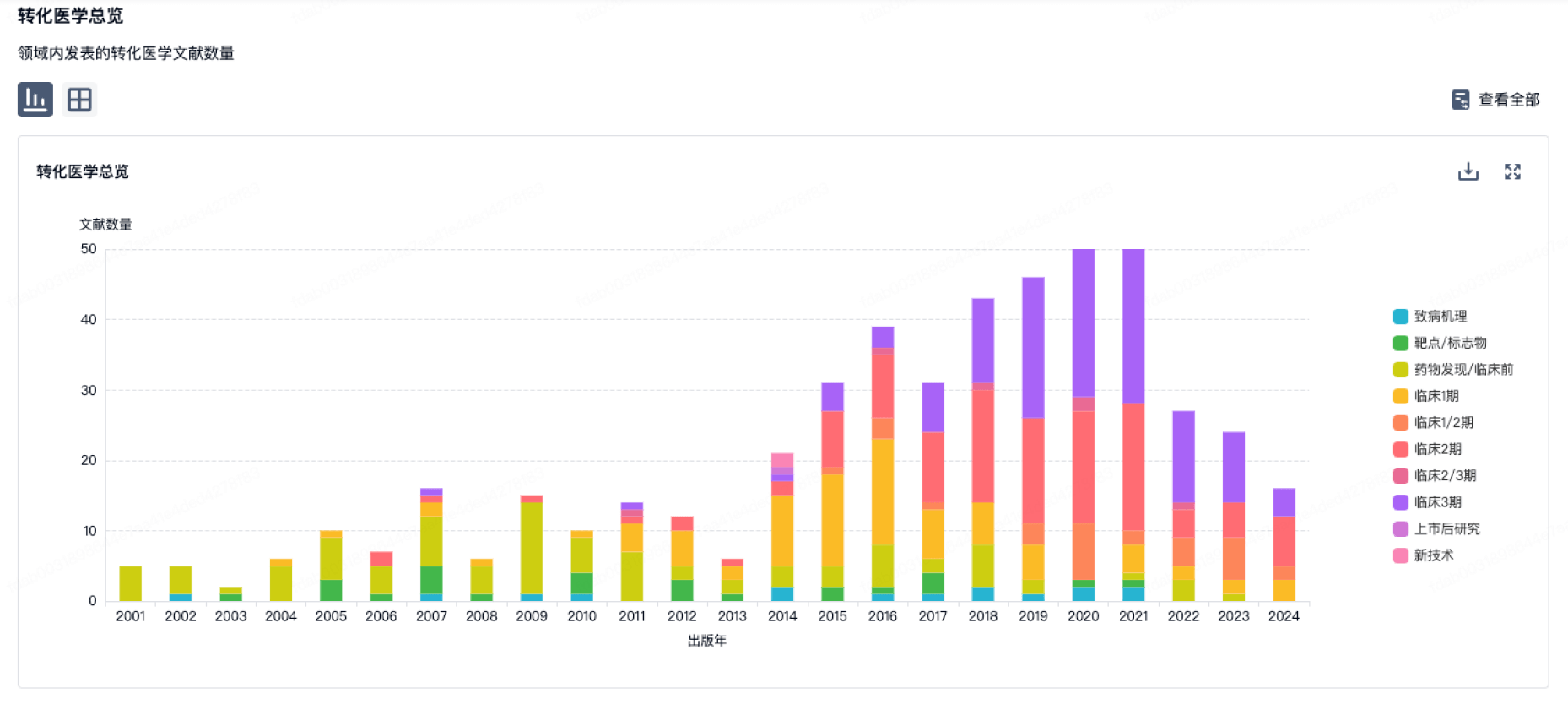
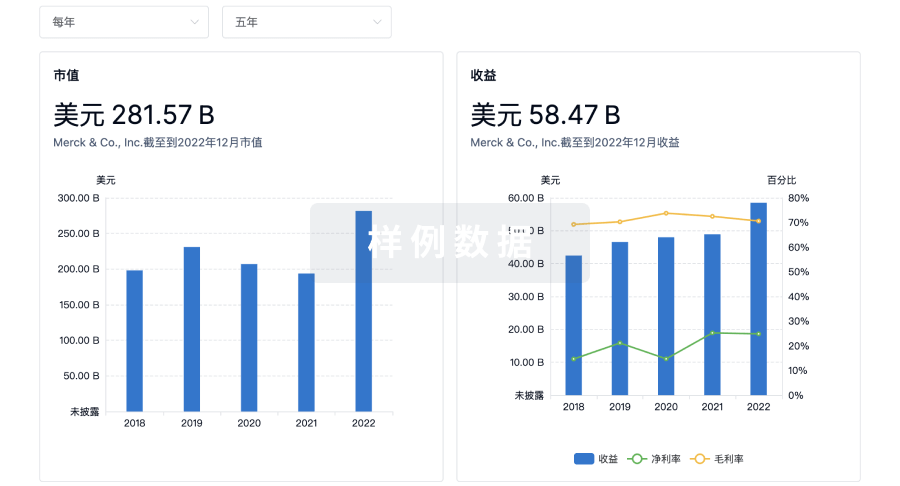
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或

投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或

融资
发掘融资趋势以验证和推进您的投资机会。
登录
或

标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用