更新于:2024-09-19

Marijuana Company of America, Inc.
更新于:2024-09-19
概览
关联
100 项与 Marijuana Company of America, Inc. 相关的临床结果
登录后查看更多信息
0 项与 Marijuana Company of America, Inc. 相关的专利(医药)
登录后查看更多信息
16
项与 Marijuana Company of America, Inc. 相关的新闻(医药)2022-12-28
·药明康德
▎药明康德内容团队编辑本期看点[1] 继AlphaFold之后,AI在蛋白药物设计和创新疗法开发上取得新突破。[2] 基因疗法设计。多款AI设计药物进入临床试验。在传统小分子药物之外,AI也被用于细胞疗法、基因疗法、以及蛋白降解疗法的设计。[3] 基于AI,研究人员可分析患者临床与基因组学数据,进行病患分层,识别应答群体,进行更精准的治疗。[4] 2022年AI领域投融资活跃,共有90起投融资事件(涉及84家新锐公司),融资金额达41.2亿美元,与细胞和基因疗法领域投融资总金额接近。扫描文中二维码或点击文末“阅读原文/Read more”,即可访问下载页面,获取这些新锐的详细列表。随着全球医药产业逐渐朝着数字化、智能化、自动化的方向升级,人工智能在近年来也成为产业热衷的话题。基础研究中,AlphaFold的横空出世降低了蛋白结构预测的门槛;而在新药研发里,也有越来越多的医药公司使用人工智能来寻找候选新药、优化分子结构、完善患者分层、或是预测临床结果。这些进展,无不揭示着人工智能有望在未来新药研发中扮演着日趋关键的角色。在今日的这篇年度盘点中,药明康德内容团队将总结2022年人工智能在新药研发方面的最新进展,并基于投融资趋势,试着从中探索未来的发展方向。▲长按扫描二维码或点击文末“阅读原文/Read more”,即可下载今年在人工智能领域获得早期融资的新锐公司列表(下载有效期至2023年1月8日)。分析的详细方法请参见文末。AlphaFold带来的新浪潮这两年,AI在预测蛋白结构上取得的突破为产业所瞩目。今年,AI在这一领域取得了更多进展,也让产业对其未来的应用充满期待。继通过序列预测蛋白结构后,今年3月,华盛顿大学David Baker教授团队在《自然》杂志上发表一篇论文,带来了新的应用前景。这篇论文指出只需要知道靶点蛋白的结构信息,就能够发现与它们以高亲和力结合的迷你蛋白(miniproteins)。值得一提的是,这些蛋白均小于65个氨基酸,非常稳定,经过实验优化后可以与靶点以nM或pM亲和力结合,具有一定的成药潜力。Baker教授表示,这一发现有望带来药物发现和分子生物学的范式的改变。而《科学》杂志对这项研究的评论也指出,这一策略可能带来新的药物类型。9月,该团队又在《科学》杂志连发两篇论文,利用全新的深度学习工具,从头设计出具有全新功能性的蛋白分子。而且,这一蛋白设计的时间从“月”缩短至“秒”。12月,科学家们再进一步。Baker教授与初创公司Generate Biomedicines同日发布了各自的最新研究成果,基于扩散模型(diffusion models)算法,他们开发的AI平台可以按照研究人员的要求,精准生成自然界中没有的全新蛋白结构!Baker教授的团队指出,与此前的蛋白设计程序相比,这种模型在解决不同设计挑战方面的表现都更为优越。它能够设计更为大型和复杂的蛋白,以及可以相互结合形成多聚体的蛋白单体。图片来源:123RF在蛋白设计上的应用外,AI科技也被应用于非蛋白类药物的设计与开发。今年8月,Baker教授团队于《细胞》杂志上发表论文,利用AI技术平台精准地从头设计出能够穿过细胞膜的大环多肽分子。这些大分子与小分子药物相比,具有更大的表面积与靶点蛋白结合,从而能够靶向很多小分子不能影响的蛋白相互作用。而与抗体相比,它们的分子量又更小,可能可以穿过细胞膜来靶向细胞内靶点,并且具有可以口服,并且穿越血脑屏障的潜力,这项突破开辟了设计全新口服药物的新途径。Baker教授团队成员联合创建的初创公司Vilya也将利用这一技术开发新一代精准靶向疾病生物学的口服疗法,有望跳过高通量筛选直接合成候选药物!AI药物最新临床进展自产业界看到人工智能在新药研发中的巨大潜能后,就期望由AI设计的药物有朝一日能在临床中取得出色的效果。这不仅将是这一技术的重要验证,也有望提升产业的研发产率,带来更多造福病患的药物。在推进至临床试验上,AI在2022年取得了一定的进展。比如Oncocross所开发的在研疗法OC514在今年2月启动全球性1期临床试验,用于治疗包括肌肉减少症(sarcopenia)在内的肌肉疾病。这款疗法诞生于其公司的RAPTOR AI平台——该平台利可用基于转录组数据,发现创新疗法,或是为已有药物寻找新适应症。根据公司新闻稿,这是治疗肌肉减少症的在研疗法中,首批由AI协助开发,并进入临床试验的疗法之一。Schrödinger公司亦于今年6月宣布,基于其物理计算平台发现的MALT1抑制剂SGR-1505获准开启1期临床试验,治疗复发/难治性B细胞淋巴瘤。根据Schrödinger公司的介绍,该计算平台能在一周内评估数十亿种化合物,并在不断的迭代过程中,对化合物进行全面评估和优化选择。图片来源:123RF此外,维智基因的在研疗法VRG50635于今年10月完成1期临床试验首例受试者给药。VRG50635是一款小分子抑制剂,针对的是PIKfyve——一款治疗肌萎缩侧索硬化(ALS)的创新靶点。这款在研疗法由该公司基于人体组织和人类数据,AI赋能的技术平台CONVERGE发现。更好地理解靶点在新药开发上,靶点具有举足轻重的地位。许多创新公司正使用海量的数据和计算算法,来迅速克服靶点相关的各种挑战,找到潜在的药物结合位点。例如,Nimbus Therapeutics和合作伙伴Schrödinger使用AI发现靶点蛋白上的别构位点,加快候选化合物的设计和优化。Nimbus的两款小分子候选药物已进入2期临床试验,用于治疗癌症和自身免疫性疾病。最近,武田也以40亿美元预付款囊获其一款TYK2抑制剂。Nested Therapeutics则致力于结合基因组学、计算生物物理学、化学生物学和AI平台,获取与肿瘤生物学相关的分子机制洞见,解决靶点复杂性的挑战。该公司利用其平台加快发现蛋白突变,这些突变可能在蛋白复合体中产生全新结合“口袋”,或者导致与疾病相关的蛋白构象变化。这些洞见被用于驱动抗癌创新药物的开发。CHARM Therapeutics则挑战解决靶点药理学的复杂性。该公司名为“Dragonfold”的AI平台可以基于蛋白靶点的氨基酸序列,和配体的化学结构,预测蛋白/配体复合体的晶体结构。寻找潜在新疗法在寻找潜在新药上,产业同样对AI寄予厚望。同样,今年有不少新锐公司取得积极进展,而它们关注的对象则超越了传统的小分子药物。在今年获得2.2亿美元B轮融资的ArsenalBio利用其AI平台来打造新型细胞疗法。根据其公司官网介绍,该公司利用实验数据来筛选上千种嵌合抗原受体(CAR)设计,并且构建预测性模型,更好地理解不同基因修改的效果。同样是在今年,ArsenalBio先后与百时美施贵宝(BMS)以及基因泰克(Genentech)两家大型药企达成合作,也从侧面支持了其平台技术的潜力。图片来源:123RF今年4月,TRIANA Biomedicines完成1.1亿美元A轮融资,正式亮相。该公司旨在开发利用E3泛素连接酶,促进蛋白靶向降解的分子胶。E3连接酶家族具有超过600个成员,而与其进行结合的潜在靶点数更多。为了加快靶点与连接酶之间的匹配速度,该公司启用了其深度学习平台,在包容不同结合机制多样性的同时,支持对该公司的分子胶候选化合物库的筛选。AI工具同样可以用于协助基因疗法的开发。在种子轮中斩获5500万美元融资的Replay公司的技术平台包括一系列用于基因组书写(genome-writing)的科技。这些工具有望理解蛋白序列空间的复杂性,从而指导编码蛋白的基因组书写,优化蛋白产物的功能。更精准的疗法除了以上这些进展,AI平台也被用来更好地开发“精准疗法”,发现最可能对靶向疗法产生应答的患者群体。Alto Neuroscience在今年获得了3500万美元的B轮融资,该公司将临床检测数据(比如脑电图),可佩戴器械获得的数据和基因组学数据整合在一起,指导选择针对特定患者亚群的合适药物。目前Alto正在2b期临床试验中检验一款治疗抑郁症的药物。OncXerna Therapeutics的一款在研单克隆抗体在2期临床试验中与免疫检查点抑制剂联用,治疗胃癌。该公司的专有AI平台利用基于RNA的基因表达数据,对癌症患者基于他们肿瘤的主要生物学特征进行分类。另外,Celsius Therapeutics专有的AI平台可对精选的组织样本集进行单细胞基因组学分析,从而发现特定患者群体中存在的特异性靶点,让基于靶点的精准治疗成为可能。该公司预计在2023年启动其抗TREM单克隆抗体的1期临床试验,用于治疗炎症性肠病。今年,Celsius获得了8300万美元的融资。它也已与强生(Johnson & Johnson)旗下的杨森(Janssen)达成生物标志物合作,并与施维雅(Servier)达成靶点发现合作。▲长按扫描二维码或点击文末“阅读原文/Read more”,即可下载今年在人工智能领域获得早期融资的新锐公司列表(下载有效期至2023年1月8日)。分析的详细方法请参见文末。结语从上述进展可以看到,AI在生物医药产业的各个环节都有潜在的应用机会。除了在蛋白质设计上的突破外,AI也被用于靶点的探索,潜在疗法的发现与优化,以及患者的精准分层选择。尽管目前由AI带来的药物尚未在临床中证实自身的潜力,但这不影响产业对AI在医药研发中的期待。今年,84家公司完成了90起融资事件,金额达41.2亿美元。而Nimbus公司与武田就TYK2抑制剂达成的合作,也可被视为是一个积极的信号。我们期待这一领域未来能迎来更多成功,让更多好药新药加速问世,造福全球病患!分析方法论:本次统计包括2022年1月1日~12月19日发布投融资新闻的人工智能新锐公司(定义为使用人工智能/机器学习技术,辅助其创新疗法的研发。范围涵盖靶点分析、分子筛选、分子优化、患者分层等领域。疾病诊断、医疗器械、疾病数字化管理等非新药研发类的公司未统计在内),仅统计融资轮次在B轮及之前,且融资金额大于1000万美元的融资事件。如果融资事件的货币单位不是美元,则依据当时汇率进行换算。考虑到汇率会随时间发生变化,融资总数仅做参考,详细融资情况还请见附件。未符合以上条件的公司(如获得融资,但未公布金额)未被纳入列表。需注意目前人工智能为产业热词,以上统计在列表中的新锐公司,可能仅将人工智能技术用于其研发过程的少数环节,本文不对其进行额外区分。免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。版权说明:本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「药明康德」微信公众号回复“转载”,获取转载须知。分享,点赞,在看,聚焦全球生物医药健康创新
基因疗法细胞疗法临床研究
2022-12-08
·创鉴汇
▎药明康德内容团队编辑11月,AI应用于小分子药物研发领域热度不减。明星AI公司英矽智能(Insilico Medicine)与知名药企赛诺菲(Sanofi)达成12亿美元新合作,利用前者的AI药物发现平台,针对多达6个新靶点开发候选药物。此外,今年年初与赛诺菲达成52亿美元合作的AI生物技术公司Exscientia,也在本月与知名癌症研究机构MD安德森癌症中心敲定新战略合作,运用前者的AI平台加速开发新型小分子肿瘤疗法。值得一提的是,Exscientia开发的端到端AI驱动精准医药平台,在近期获得了有“医药界诺贝尔奖”之称的盖伦奖。本文从交易、融资、研发三个方面整理了本月该领域值得一看的行业资讯。01# 交易概览 # 最高达12亿美元,英矽智能与赛诺菲达成合作,推进多个创新靶点的候选药物研发11月8日,由人工智能(AI)驱动的临床阶段药物发现公司英矽智能宣布,与赛诺菲达成一项将持续多年、针对多个靶点的战略研究合作。根据协议条款,该合作将利用英矽智能人工智能驱动的Pharma.AI药物发现平台,推进基于不超过6个创新靶点的候选药物研发。根据协议条款,赛诺菲将支付英矽智能总额不超过2150万美元的预付款和靶点提名费用,获得英矽智能的端到端人工智能药物发现平台Pharma.AI和跨学科药物研发科学家团队的支持,用于识别、合成和推进高质量先导化合物的研究,使其达到临床开发候选阶段。如果该合作达到关键的研发和商业里程碑,英矽智能还将获得额外的里程碑付款,总额预计最高可达12亿美元。了解更多英矽智能信息,请点击>>Exscientia和MD Anderson启动战略合作,利用AI加速新型抗癌疗法研发11月14日,Exscientia和德克萨斯大学MD安德森癌症中心宣布了一项战略合作,将把Exscientia以患者为中心的AI能力与MD安德森癌症中心在药物发现和开发方面的专业知识相结合,推进新型小分子肿瘤疗法的开发。该合作将利用Exscientia的精准医疗平台,针对双方共同确定的治疗靶点,开发新的细胞固有的抗肿瘤小分子化合物。Exscientia利用AI,使用患者数据来优化和筛选更有可能在临床中产生积极影响的分子。该公司开发的功能性精准肿瘤学平台,在前瞻性干预性临床研究中成功指导了治疗选择和改善患者预后,新型化合物通过AI系统可自动设计并优先合成,并迅速将化合物发展成符合临床开发所需候选标准的药物。该平台利用表型组学、新型生物物理学和深度学习生物数据来评估药物靶点和机制,然后通过数千个模型驱动的AI算法,将该信息转化为精准药物的设计。AI基因网络开发公司Unravel Biosciences敲定新合作,发现罕见癌症的新型治疗靶标11月8日,Unravel Biosciences宣布与Spanios建立合作伙伴关系。此次合作将Unravel Biosciences专有的人类健康和药物反应的基因调控网络,以及药物-基因相互作用网络模型,与Spanios的患者来源的类肿瘤(PDTs)相结合,以期发现罕见癌症的新型治疗靶标。Unravel将应用其基于AI基因网络的计算模型,根据转录组学信息预测治疗化合物和潜在的新靶点。该公司专有的BioNAV平台结合靶标和药物发现、临床前筛查和患者分层技术,发现了RVL001(一种靶向Rett综合征的专利制剂,将于2022年末进入临床)和RVL002(一种新的小分子,应用于中枢神经系统和代谢性疾病)。02# 融资动态 # Sensorium Therapeutics完成3000万美元的A轮融资,推进AI平台建设和精神类药物研发11月8日,Sensorium Therapeutics完成3000万美元的A轮融资,本轮融资由Santé Ventures领投,融资资金将用于精神类药物研发和其生物动力学发现平台(BDP)开发。Sensorium Therapeutics是一家通过药物化学、神经科学和机器学习(ML)开发精神疾病药物的生物技术公司。该公司旗下的BDP是一种药物发现引擎,可快速识别、合成和增强靶向分子作为新疗法。BDP将其天然产品库和高通量表征的数据输出至其专有的机器学习算法。在该平台的助力下,Sensorium可以更快地开发药物,提高药物疗效和耐受性,减少副作用,并降低患者对药物依赖的可能性。图片来源:123RF同诺康完成天使轮融资,推进小分子创新药研发管线并助力人工智能平台建设近日,同诺康完成天使轮融资,本轮融资由动平衡资本领投。本轮融资资金将用于研发管线推进、人工智能(AI)平台的升级以及团队建设。同诺康以“未被满足的临床需求”为导向,关注基因组脆弱性靶点(如合成致死,染体质不稳定和全基因组倍增等),将原创的AI和生物数据挖掘技术以及高通量筛选技术贯穿于新药靶点发现、药物分子设计、临床试验设计和病人入组等新药研发各环节,同时结合对疾病生物学的深刻理解和高效药物化学经验,开发具有价值的小分子创新药。了解更多同诺康信息,请点击>>03# 研发进展 # 渐冻症创新疗法!维智基因AI平台驱动针对新靶点的药物开发近日,维智基因(Verge Genomics)宣布VRG50635的1期临床试验已对首例受试者给药。VRG50635是针对靶点PIKfyve的一种小分子抑制剂,PIKfyve是由维智基因AI技术平台ConVERGE发现的肌萎缩侧索硬化症(ALS)的新型治疗靶点。ConVERGE平台作为一个端到端的系统,整合从发现到转化的技术创新,以简化药物开发流程。通过使用AI“无偏倚”(unbiased)的算法,可以发现复杂疾病的治疗靶标。该平台是一个闭环学习系统,将行业领先的人类基因组学与先进的计算工具相结合,以更高的临床成功率预测新药。了解更多全球AI制药领域新动态请点击下图访问我们的小程序免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。版权说明:本文由药明康德内容团队根据公开资料整理编辑,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转发/复制至其他平台。转发授权请在「创鉴汇」微信公众号留言联系我们。读者们请星标⭐创鉴汇,第一时间收到我们的推送新型疗法专题PROTAC疗法 | 细胞疗法 | 基因疗法 | 溶瘤病毒 | mRNA | 反义寡核苷酸 | RNAi | 寡核苷酸疗法 | | 人工智能Medtech专题生物材料 | 液体活检 | 二尖瓣技术 | 手术机器人 | 神经介入 | POCT | 脑机接口 | 人工心脏 |投资机构专题高瓴创投 | 礼来亚洲基金 | 红杉中国 | 诺华 | RA Capital Management | 启明创投 | 奥博资本 | Alexandria Venture Investments | Flagship pioneering | 腾讯 国家园区专题以色列 | 日本 | 英国 | 张江 点击“在看”,分享创鉴汇健康新动态
引进/卖出
2022-11-06
·药明康德
▎药明康德内容团队编辑本期看点1. 治疗乙肝病毒感染的RNAi疗法AB-729公布早期临床数据,停药44周仍未发现临床复发迹象。2. 靶向CD20的自体CAR-T细胞疗法MB-106,在针对各种血液系统恶性肿瘤的1/2期临床试验中,观察到总缓解率(ORR)高达96%,完全缓解率(CR)高达75%。3. 潜在“best-in-class”ROS1选择性抑制剂NVL-520的1/2期临床试验结果公布,近半数ROS1阳性非小细胞肺癌耐药患者获得缓解。4. 针对肝细胞癌,靶向MYC的创新mRNA疗法OTX-2002完成首例患者给药。药明康德内容团队整理AB-729:公布1/2a期临床试验数据Arbutus Biopharma公司公布了其RNAi疗法AB-729在1/2a期临床试验中的数据。AB-729是一种靶向肝细胞的RNAi药物,它采用了Arbutus公司开发的新型共价偶联N-乙酰半乳糖胺(GalNAc)递送技术,能够皮下注射。在临床前模型中,AB-729可以抑制HBV病毒复制,减少所有病毒RNA转录副本,并降低所有HBV抗原,包括乙型肝炎表面抗原(HBsAg),在所有HBV基因型中显示出泛基因型活性。此次公布的1期试验结果显示,停止AB-729和核苷(酸)类似物(NA)治疗后长达44周内患者,没有临床复发的迹象,HBsAg和HBV的DNA依旧保持着低水平。联合给药的2a期试验中,与仅使用AB-729+NA治疗相比,再多添加第一代HBV核心抑制剂vebicorvir(VBR)不会对HBV感染标志物有更大的治疗改善,但也不会对HBsAg的减少产生负面影响。在该2a期试验中,所有方案总体上都是安全且耐受性良好的。MB-106:公布1/2期临床试验的中期数据Mustang Bio公司公布了其靶向CD20的自体CAR-T细胞疗法MB-106在1/2期临床试验中,华氏巨球蛋白血症(WM)队列中的中期数据。WM也称为淋巴浆细胞性淋巴瘤,是一种罕见的非霍奇金淋巴瘤(NHL)。CD20是一种在B细胞分化为浆细胞中起调节作用的跨膜蛋白。此次公布的数据显示,在包括滤泡性淋巴瘤、慢性淋巴细胞白血病、弥漫性大B细胞淋巴瘤在内的各种血液系统恶性肿瘤患者中,观察到的ORR为96%,CR为75%。其中,两名WM患者均获得了CR。获得CR的患者中,维持时间最长的为33个月。此外,所有既往接受过靶向CD-19的CAR-T细胞治疗的患者均对MB-106有反应。MB-106作为门诊治疗的安全性良好,没有出现3级以上的细胞因子释放综合征(CRS)或免疫效应细胞相关神经毒性综合症(ICANS)。NVL-520:公布1/2期临床试验的初步数据Nuvalent公司公布了其在研ROS1抑制剂NVL-520于临床1/2期试验中剂量爬坡部分的初期结果。NVL-520是一种创新、选择性、具脑渗透性的ROS1抑制剂,设计用以治疗那些对现有ROS1抑制剂具抗性的癌症,例如那些带有G2032R、S1986Y/F、L2026M或D2033N突变的肿瘤。由于NVL-520具脑渗透性,因此具潜力改善那些肿瘤转移至脑部患者的治疗。这次所公布的ARROS-1临床1/2期试验是NVL-520的“first-in-human”研究,招募带有ROS1阳性的NSCLC与其他实体瘤患者入组,这些患者之前曾接受过前期治疗。在所有可检视疗效的病患中,有48%(10/21)达成部分缓解(PR),有76%(16/21)仍于试验中持续接受治疗。100%(3/3)具有可测量(>10mm)中枢神经系统转移的病患达成颅内部分缓解。此外,在所有35位入组的病患中,NVL-520展现出良好的安全性。OTX-2002:1期临床试验完成首例患者给药OTX-2002是一款在研、潜在“first-in-class”用于治疗肝细胞癌的表观基因组学调节物。据估计,在多达70%的肝细胞癌患者中,MYC的过度表达与肝细胞癌的侵袭性有关。此药物能够通过脂质纳米颗粒(LNP)递送mRNA疗法,可在MYC基因转录以前,通过调节表观基因组来降低MYC的表达。Omega此前公布的临床前数据,支持了OTX-2002在多种体外和体内模型中的作用机制和抗肿瘤活性。多项体外研究表明,OTX-2002具有调节MYC表观基因组学谱并控制其转录前表达的能力。而OTX-2002单药或与标准疗法组合,在多种体内HCC模型中均能诱导强大的抗肿瘤活性。此外,使用OTX-2002治疗非人灵长类动物时,成功诱导了其肝细胞MYC转录前的下调。这些积累的临床前数据支持了OTX-2002为肝癌患者提供新的治疗策略的临床潜力。HMI-103:介绍1期临床试验设计HMI-103是一种一次性体内基因编辑候选药物,用于治疗苯丙酮尿症(PKU)。PKU是一种由PAH基因突变引起的罕见先天性代谢错误疾病,若不及时治疗,苯丙氨酸在血液中的积聚将会导致进行性和严重的神经损伤。目前,尚无针对该疾病潜在遗传原因的治疗选择。HMI-103旨在利用人体同源重组的自然DNA修复过程,把具功能的PAH基因和肝脏特异性启动子整合到基因组,以最大限度地提高该基因的长期表达。TIDAL-01:IND申请获得FDA许可TIDAL-01是一种下一代肿瘤浸润淋巴细胞(TIL)疗法,通过鉴定、选择和扩增患者特异性肿瘤反应性T细胞的最有效亚群,TIDAL-01旨在改善和扩大TIL的临床疗效,并克服当前基于TIL的疗法的局限性。目前,TIDAL-01正在两项1期临床试验中进行评估,一项针对乳腺癌和结直肠癌,另一项针对皮肤和非皮肤黑色素瘤。ORM-5029:1期临床试验完成首例患者给药ORM-5029是一种潜在“first-in-class”抗体偶联药物(ADC)候选药物,旨在通过抗体选择性地将催化GSPT1蛋白降解剂递送给表达HER2的肿瘤细胞,使癌细胞死亡。临床前研究显示,与小分子GSPT1降解剂或标准护理的ADC相比,ORM-5029在低HER2环境中仍具有强大的体外和体内效力,并且作用具有剂量依赖性。VGL101:公布1期临床试验的中期数据Vigil Neuroscience公布了靶向髓样细胞触发受体2(TREM2)的激活性全人源单克隆抗体VGL101,在健康受试者中的1期临床试验的积极中期数据。TREM2是小胶质细胞表达的一种重要受体,在小胶质细胞对中枢神经系统(CNS)的损伤应答中发挥作用,是治疗神经退行性疾病的一个具有潜力的分子靶点。VGL101的首个适应症将是伴有轴突球体和色素性胶质细胞的成人发作性白质脑病(ALSP)。这是一种罕见的遗传性神经退行性疾病,由CSF1R基因突变引起。小胶质细胞功能障碍被认为是ALSP发病机制的核心,Vigil公司认为激活TREM2可以恢复小胶质细胞功能,从而为该疾病患者提供治疗益处。研究结果显示,VGL101具有良好的安全性、耐受性、药代动力学(PK)特征和脑渗透性。VGL101重复给药能使脑脊液中的sTREM2水平呈剂量依赖性的持续降低,sCSF1R水平持续升高,在给药三次或末次给药28天后仍能观察到sTREM2水平的降低。Vigil有望在本季度启动针对ALSP患者的2期试验。TAK-594/DNL593:公布1/2期临床试验的中期数据Denali Therapeutics公司公布了其前颗粒蛋白(PGRN)替代疗法TAK-594/DNL593在1/2期临床试验A部分的中期结果。TAK-594/DNL593一种研究性静脉注射、脑渗透疗法,采用Denali的蛋白质运输载体(PTV)技术,用于治疗额颞叶痴呆(FTD)和颗粒蛋白(GRN)基因突变患者。FTD是60岁以下人群中最常见的痴呆形式。编码PGRN蛋白的GRN基因突变通常会导致PGRN水平降低,并且是FTD最常见的遗传原因之一。目前尚无获批的药物来阻止或减缓FTD或FTD-GRN的进展。此次公布的数据显示,与基线时和安慰剂相比,接受TAK-594/DNL593治疗的患者脑脊液中测量的PGRN水平呈剂量依赖性地增加,且超过了临床前模型中认为治疗PGRN缺乏相关的缺陷所必需的水平,表明该疗法实现了有效的大脑递送。此外,单剂量DNL593通常耐受性良好。这些数据为研究的B部分中对FTD-GRN突变患者进行治疗提供了参考依据。SON-1010:公布1期临床试验的中期数据Sonnet BioTherapeutics公司公布了其免疫治疗候选药物SON-1010在两项1期临床试验的中期数据。SON-1010是一种使用Sonnet的全人源白蛋白结合平台开发的专有人类白细胞介素-12(IL-12),有潜力在节省剂量的同时,提高IL-12的安全性和有效性。此次公布针对健康受试者和晚期实体瘤成年患者的试验结果表明,SON-1010的安全性和耐受性良好,尚未发生剂量限制性毒性。细胞因子数据显示,SON-1010具有延长的半衰期,且IFNγ诱导在控制范围内,未出现CRS的迹象。AU-007:IND申请获得FDA许可AU-007是通过计算设计的人IgG1单克隆抗体,对IL-2的CD25结合部分具有高度选择性,用于治疗实体肿瘤。AU-007的作用机制不同于任何其他正在开发中的IL-2治疗,它能够在防止IL-2(无论是外源性的还是由T效应细胞分泌的)与调节性T细胞上的三聚体受体结合的同时,仍允许IL-2与T效应细胞和NK细胞结合并使之扩增,从而增强了IL-2的抗肿瘤免疫作用。这种机制防止了其他基于IL-2的治疗引起的负反馈环路,并使免疫系统偏向于激活而不是抑制。AU-007还能够防止IL-2与血管和肺内皮上的三聚体受体结合,有望显著降低与高剂量IL-2治疗相关的血管泄漏综合征和肺水肿。GB1211:公布1b/2a期临床试验数据Galecto公司公布了其口服、高亲和力的小分子碳水化合物基半乳糖凝集素-3(Gal-3)抑制剂GB1211,在治疗严重肝脏疾病的1b/2a期临床试验中的积极数据。Gal-3是一种促纤维化β-半乳糖苷结合蛋白,在纤维化的肝脏中高表达,与严重的肝脏疾病相关。GB1211在多个临床前模型中表现出抗纤维化活性和抗癌作用。在此前的针对健康受试者的1期试验中,GB1211具有良好的耐受性,并表现出剂量依赖性的PK。此次公布的研究结果显示,在失代偿期肝硬化患者中,GB1211的耐受性良好,PK可预测,并显示出令人鼓舞的临床疗效迹象——肝脏酶水平和肝脏脂肪水平降低。数据表明,GB1211对严重肝硬化有积极的治疗效果,为GB1211在严重肝脏疾病中的进一步开发提供了有力支持。SBT-272:公布1期临床试验的新数据Stealth BioTherapeutics公司公布了其候选药物SBT-272令人鼓舞的1期临床试验数据。SBT-272是一种靶向富含心磷脂的线粒体内膜的新型小分子药物,该膜对正常的线粒体结构和功能至关重要。临床前研究显示,SBT-272在ALS、FTD、α-突触核蛋白病模型中具有线粒体保护和神经保护作用。此次公布的1期数据显示,该临床试验中所选的剂量,有望在大脑中达到有效治疗浓度。虽然最终的安全性分析正在进行中,但目前临床评估确定的剂量水平,显示可能是安全的,且耐受性良好。近期,SBT-272还获得了FDA授予的孤儿药资格,用于治疗ALS患者。VRG50635:1期临床试验完成首例患者给药VRG50635是一款潜在“best-in-class”的PIKfyve小分子抑制剂,用于治疗肌萎缩侧索硬化(ALS)。ALS是一种进行性神经退行性疾病,影响大脑和脊髓中的神经细胞,目前尚不清楚其确切的发病机制。该公司基于人体组织和人类数据,通过AI赋能的技术平台CONVERGE发现内体/溶酶体功能的丢失是ALS的新致病机制,并发现PIKfyve是具有潜力的新治疗靶点。VRG50635是一款强力PIKfyve抑制剂,能够恢复ALS患者神经元的内体/溶酶体功能。临床前研究显示,VRG50635在ALS相关运动神经元退化模型中显示出效力。BMF-219:两项早期临床试验完成首例患者给药BMF-219是一种特异性抑制menin的小分子抑制剂。目前正在一项针对2型糖尿病的1/2期临床试验以及1项针对慢性淋巴细胞白血病(CLL)的1期临床试验中进行评估。β细胞丢失是1型和2型糖尿病的关键病因。BMF-219旨在通过恢复患者的胰岛β细胞库来为糖尿病患者提供长期的血糖控制能力。Menin被认为是胰腺中β细胞恢复的刹车,抑制menin有可能使正常、健康的β细胞再生。临床前研究表明,BMF-219具有恢复功能性β细胞的潜力。此外,临床前数据还显示,在临床可达到的浓度下,BMF-219能够对多种不同遗传风险和Rai分期的CLL模型中超过98%的细胞具有杀伤力。药明康德为全球生物医药行业提供一体化、端到端的新药研发和生产服务,服务范围涵盖化学药研发和生产、生物学研究、临床前测试和临床试验研发、细胞及基因疗法研发、测试和生产等领域。如您有相关业务需求,欢迎点击下方图片填写具体信息。▲如您有任何业务需求,请长按扫描上方二维码,或点击文末“阅读原文/Read more”,即可访问业务对接平台,填写业务需求信息▲欲了解更多前沿技术在生物医药产业中的应用,请长按扫描上方二维码,即可访问“药明直播间”,观看相关话题的直播讨论与精彩回放参考资料(可上下滑动查看)[1] OMEGA THERAPEUTICS ANNOUNCES FIRST PATIENT DOSED IN LANDMARK MYCHELANGELO™ I TRIAL OF OTX-2002 IN HEPATOCELLULAR CARCINOMA AND OTHER SOLID TUMOR TYPES ASSOCIATED WITH THE MYC ONCOGENE. Retrieved October 27, 2022, from https://ir.omegatherapeutics.com/news-releases/news-release-details/omega-therapeutics-announces-first-patient-dosed-landmark[2] Mustang Bio Announces Phase 1/2 Clinical Trial Data of MB-106, a First-in-Class CD20-targeted, Autologous CAR T Cell Therapy, to be Presented at 11th International Workshop for Waldenstrom's Macroglobulinemia. Retrieved October 27, 2022, from https://ir.mustangbio.com/news-events/press-releases/detail/150/mustang-bio-announces-phase-12-clinical-trial-data-of[3] Biomea Fusion Announces First Patient Dosed with Chronic Lymphocytic Leukemia (CLL) in COVALENT-101 Trial. Retrieved October 27, 2022, from https://investors.biomeafusion.com/news-releases/news-release-details/biomea-fusion-announces-first-patient-dosed-chronic-lymphocytic[4] Biomea Fusion Announces Dosing of First Patient with Type 2 Diabetes and Completion of Phase I Healthy Volunteer Portion of Phase I/II (COVALENT-111) Study of BMF-219. Retrieved October 31, 2022, from https://investors.biomeafusion.com/news-releases/news-release-details/biomea-fusion-announces-dosing-first-patient-type-2-diabetes-and[5] Homology Medicines Presents on Design of pheEDIT Trial Evaluating One-Time Nuclease-Free Gene Editing Candidate HMI-103 for PKU at American Society of Human Genetics Meeting. Retrieved October 27, 2022, from https://www.homologymedicines.com/news-story/homology-medicines-presents-on-design-of-pheedit-trial-evaluating-one-time-nuclease-free-gene-editing-candidate-hmi-103-for-pku-at-american-society-of-human-genetics-meeting[6] Nuvalent Reports Preliminary Phase 1 Clinical Data from ARROS-1 Trial that Support Best-In-Class Potential of NVL-520 for Patients with ROS1-Positive NSCLC. Retrieved October 28, 2022 from https://investors.nuvalent.com/2022-10-28-Nuvalent-Reports-Preliminary-Phase-1-Clinical-Data-from-ARROS-1-Trial-that-Support-Best-In-Class-Potential-of-NVL-520-for-Patients-withROS1-Positive-NSCLC[7] Aulos Bioscience Announces FDA Clearance of IND Application for AU-007, a Novel Immunotherapy for the Treatment of Solid Tumors. Retrieved October 31, 2022 from https://aulosbio.com/aulos-bioscience-announces-fda-clearance-of-ind-application-for-au-007-a-novel-immunotherapy-for-the-treatment-of-solid-tumors/[8] Turnstone Biologics Announces FDA Clearance of IND for TIDAL-01, a Next-Generation TIL Therapy for Solid Tumors. Retrieved October 31, 2022 from https://www.businesswire.com/news/home/20221031005275/en/Turnstone-Biologics-Announces-FDA-Clearance-of-IND-for-TIDAL-01-a-Next-Generation-TIL-Therapy-for-Solid-Tumors[9] ORUM THERAPEUTICS ANNOUNCES FIRST PATIENT DOSED IN PHASE 1 CLINICAL TRIAL OF ORM-5029 IN DEVELOPMENT TO TREAT HER2-EXPRESSING ADVANCED SOLID TUMORS. Retrieved October 31, 2022 from https://www.orumrx.com/news/2022/11/1/orum-therapeutics-announces-first-patient-dosed-in-phase-1-clinical-trial-of-orm-5029-in-development-to-treat-her2-expressing-advanced-solid-tumors-1[10] Verge Genomics Initiates First-In-Human Dosing in Phase 1 Trial of VRG50635, a Novel Therapeutic for Amyotrophic Lateral Sclerosis. Retrieved October 31, 2022, from https://www.businesswire.com/news/home/20221031005225/en[11] Galecto to Present Topline Data from GULLIVER-2 Clinical Trial Showing GB1211 Reduced Signs of Liver Impairment at AASLD’s The Liver Meeting® 2022. Retrieved October 31, 2022, from https://ir.galecto.com/news-releases/news-release-details/galecto-present-topline-data-gulliver-2-clinical-trial-showing[12] Denali Therapeutics Announces Phase 1/2 Study Single Dose Healthy Volunteer Data with TAK-594/DNL593 (PTV:PGRN) and Progression to Enrolling Participants with FTD-GRN. Retrieved November 1, 2022, from https://www.denalitherapeutics.com/investors/press-release?id=9051&type=api[13] Teon Therapeutics Announces First Patient Treated in Phase 1/2 Clinical Trial of TT-816, a Novel Oral Immune Checkpoint Inhibitor, in Patients with Advanced Solid Tumors. Retrieved November 1, 2022, from https://teontherapeutics.com/teon-therapeutics-announces-first-patient-treated-in-phase-1-2-clinical-trial-of-tt-816/[14] Arbutus Presents AB-729 Clinical Data and AB-101 Preclinical Data at AASLD - The Liver Meeting®. Retrieved November 1, 2022, from https://investor.arbutusbio.com/news-releases/news-release-details/arbutus-presents-ab-729-clinical-data-and-ab-101-preclinical[15] Monte Rosa Therapeutics Announces First Patient Dosed in Phase 1/2 Clinical Trial Evaluating MRT-2359, a GSPT1-directed Molecular Glue Degrader, for Treatment of MYC-driven Tumors. Retrieved November 1, 2022, from https://ir.monterosatx.com/news-releases/news-release-details/monte-rosa-therapeutics-announces-first-patient-dosed-phase-12[16] Stealth BioTherapeutics Announces SBT-272 Data Updates and Orphan Drug Designation for the Treatment of Amyotrophic Lateral Sclerosis (ALS). Retrieved November 1, 2022, from https://investor.stealthbt.com/websites/stealthbio/English/5200/us-press-release.html?airportNewsID=e03054fa-3903-43d3-8495-7b12df26c5d1[17] VIGIL NEUROSCIENCE ANNOUNCES INTERIM TOPLINE RESULTS FROM ITS ONGOING PHASE 1 CLINICAL TRIAL EVALUATING VGL101 IN HEALTHY VOLUNTEERS SUPPORTING PHASE 2 INITIATION IN ALSP. Retrieved November 2, 2022, from https://investors.vigilneuro.com/news-releases/news-release-details/vigil-neuroscience-announces-interim-topline-results-its-ongoing[18] Equillium Announces Initiation of Phase 1 study of EQ102, A First-in-Class Multi-Cytokine Inhibitor of IL-15 and IL-21 Targeting Celiac Disease. Retrieved November 2, 2022, from https://www.equilliumbio.com/investors/press-releases/news-details/2022/Equillium-Announces-Initiation-of-Phase-1-study-of-EQ102-A-First-in-Class-Multi-Cytokine-Inhibitor-of-IL-15-and-IL-21-Targeting-Celiac-Disease/default.aspx[19] Sonnet BioTherapeutics Announces Interim Data in Two Phase 1 Dose-Escalation Trials of SON-1010. Retrieved November 2, 2022, from https://www.sonnetbio.com/news-media/press-releases/detail/55/sonnet-biotherapeutics-announces-interim-data-in-two-phase[20] 브렉소젠, '엑소좀 후보물질' 아토피 "美 1상 승인". Retrieved October 31, 2022 from http://brexogen.com/?page_id=194[21] Regulus Therapeutics Announces First Patient Dosed in Phase 1b Multiple-Ascending Dose (MAD) Clinical Trial of RGLS8429 for the Treatment of Autosomal Dominant Polycystic Kidney Disease (ADPKD). Retrieved November 2, 2022, from https://ir.regulusrx.com/2022-11-02-Regulus-Therapeutics-Announces-First-Patient-Dosed-in-Phase-1b-Multiple-Ascending-Dose-MAD-Clinical-Trial-of-RGLS8429-for-the-Treatment-of-Autosomal-Dominant-Polycystic-Kidney-Disease-ADPKD免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。版权说明:本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「药明康德」微信公众号回复“转载”,获取转载须知。分享,点赞,在看,聚焦全球生物医药健康创新
免疫疗法细胞疗法基因疗法小分子药物First in Class
100 项与 Marijuana Company of America, Inc. 相关的药物交易
登录后查看更多信息
100 项与 Marijuana Company of America, Inc. 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2024年10月13日管线快照
无数据报导
登录后保持更新
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
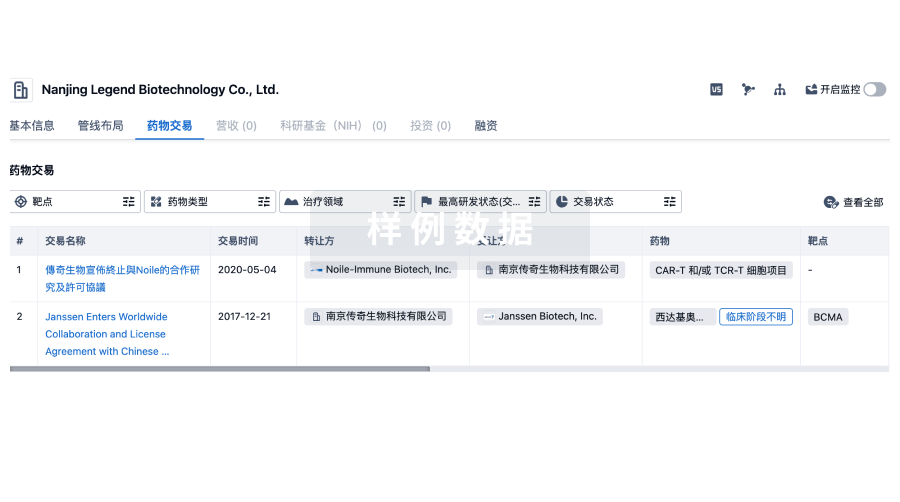
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
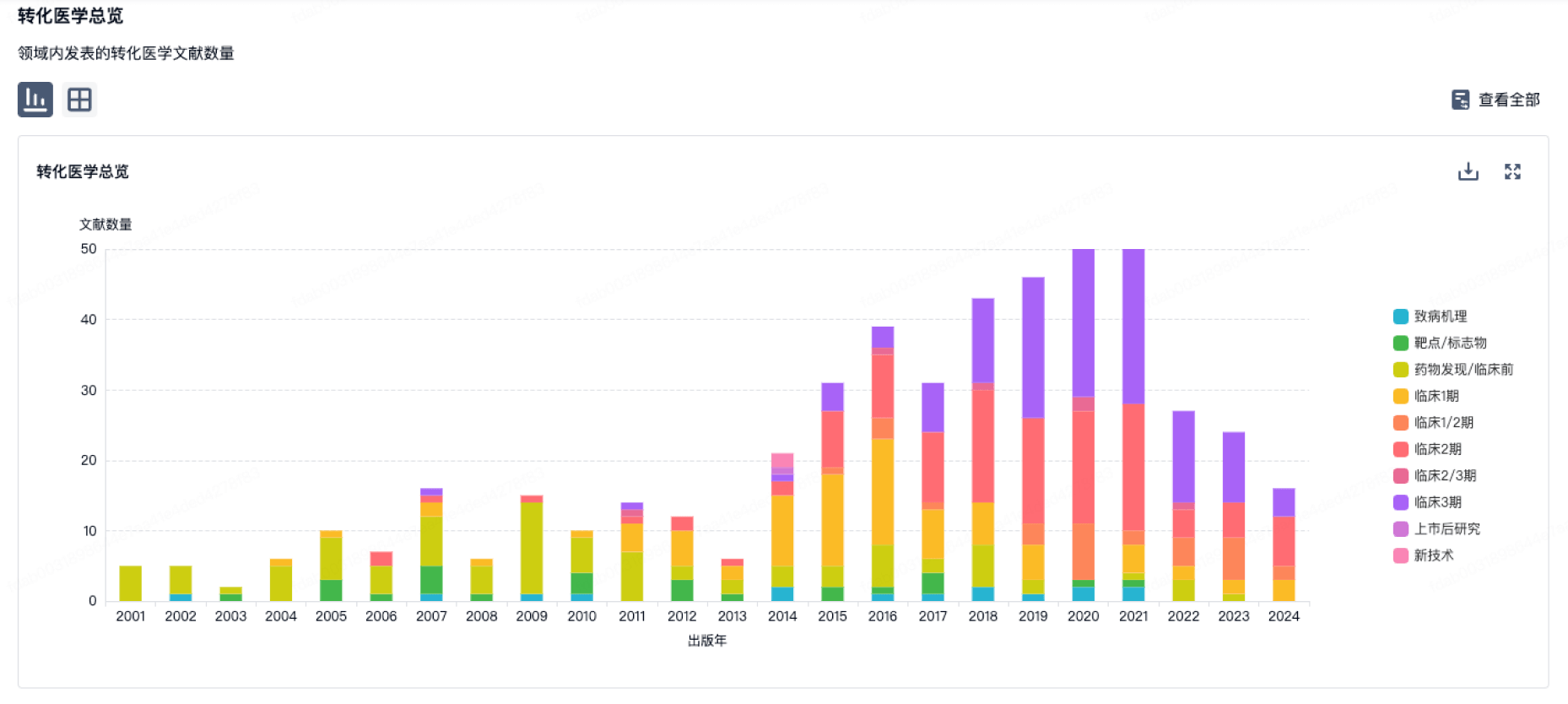
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
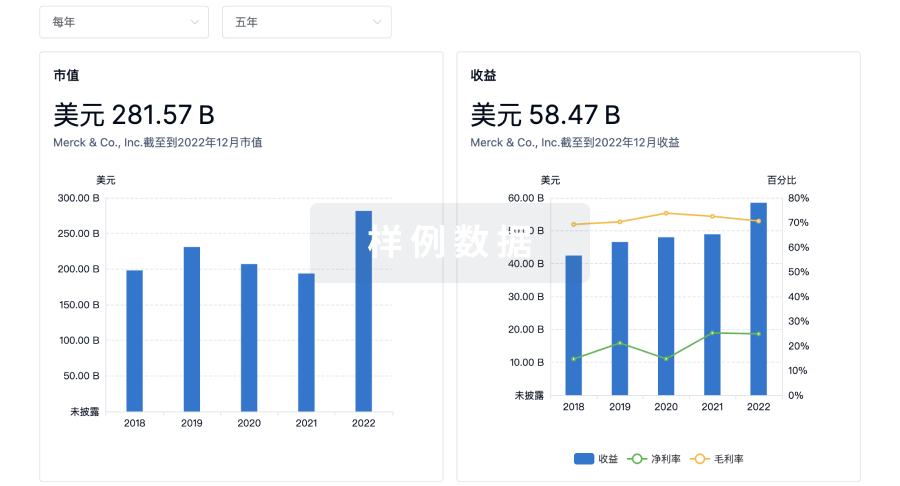
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
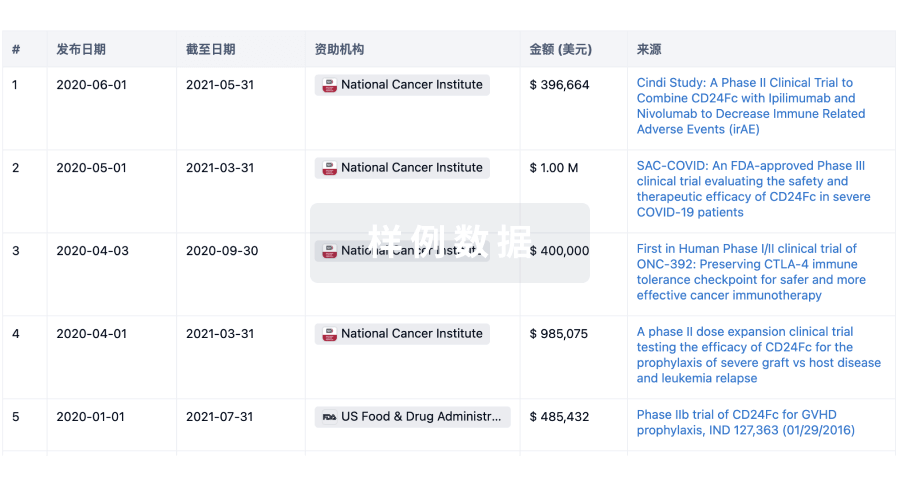
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用