预约演示
更新于:2025-03-07

Clade Therapeutics, Inc.
更新于:2025-03-07
概览
关联
2
项与 Clade Therapeutics, Inc. 相关的药物1
项与 Clade Therapeutics, Inc. 相关的临床试验NCT04688853
A Phase I Study to Investigate the Safety, Tolerability and Preliminary Efficacy of TEG002 Infusion in Relapsed/Refractory Multiple Myeloma Patients
This is a single arm, open-label, multicenter phase I study to assess the safety, tolerability and preliminary efficacy of autologous T cells transduced with a specific γδTCR, i.e. TEG002, in a dose escalation and expansion study in relapsed/refractory Multiple Myeloma patients.
The study will comprise of a Dose Escalation Segment and an Expansion Segment. The study consists of a screening period, leukapheresis of mononuclear cells, and conditioning chemotherapy, followed by TEG002. All subjects continue to be followed regularly for safety and efficacy assessments until 1 year after TEG002 administration.
The study will comprise of a Dose Escalation Segment and an Expansion Segment. The study consists of a screening period, leukapheresis of mononuclear cells, and conditioning chemotherapy, followed by TEG002. All subjects continue to be followed regularly for safety and efficacy assessments until 1 year after TEG002 administration.
开始日期2021-05-13 |
申办/合作机构  Gadeta BV初创企业 Gadeta BV初创企业 |
100 项与 Clade Therapeutics, Inc. 相关的临床结果
登录后查看更多信息
0 项与 Clade Therapeutics, Inc. 相关的专利(医药)
登录后查看更多信息
1
项与 Clade Therapeutics, Inc. 相关的文献(医药)2025-01-28·Blood Advances
Universal protection of allogeneic T-cell therapies from natural killer cells via CD300a agonism
Article
作者: Fang, Justin ; Austgen, Kathryn ; Thomas, Faith ; Cowan, Chad ; Welstead, G. Grant ; Zhang, Shu-Qi
Abstract:
Immunogenicity limits the persistence of off-the-shelf allogeneic cell therapies and transplants. Although ablation of HLA removes most T cell and humoral alloreactivity, no solution has enabled universal protection against the resulting natural killer (NK) cell response. Here, we engineered trans-antigen signaling receptors (TASRs) as a new class of NK inhibitory ligands and discovered CD300a, a previously inaccessible receptor, as a functional target. CD300a TASR outperformed leading alternative strategies in focused screens, including CD47 and HLA-E, and was solely capable of universally protecting allogeneic T cells against a large human cohort (45/45 donors), spanning diverse demographics and NK cell phenotypes. A model allogeneic T-cell therapy coexpressing an anti-CD19 chimeric antigen receptor and CD300a TASR, produced using multiplexed nonviral integration, exhibited enhanced B-cell killing potency under allogeneic immune pressure. CD300 TASR represents a universal solution to NK alloreactivity, broadening the population that could be effectively treated by next-generation allogeneic cell therapies.
21
项与 Clade Therapeutics, Inc. 相关的新闻(医药)2024-10-02
REDDING, Calif., Oct. 2, 2024 /PRNewswire/ -- According to a new market research report titled, '
Regenerative Medicine Market
Size, Share, Forecast, & Trends Analysis by Product (Gene Therapy, Stem Cell, Tissue Engineering), Application (Musculoskeletal, Cancer, Cardiovascular, Immunology, Dermatology, Ophthalmology), End User—Global Forecast to 2031.
The regenerative medicine market is projected to reach $37.27 billion by 2031, at a CAGR of 21.5% from 2024 to 2031.
Download FREE PDF Brochure Of Regenerative Medicine Market Size, Share, Forecast, & Trends Analysis -
The growth of the regenerative medicine market is driven by the growing number of new regenerative medicine approvals, consistent advancements in the regenerative medicine space, the rising incidence of chronic diseases, the availability of funding for regenerative medicine development, and the increasing utilization of regenerative medicines in diverse therapeutic areas. However, high treatment costs and ethical issues related to stem cells restrain the growth of this market.
Furthermore, the rising demand for personalized medicines, increasing organ transplant procedures, and the strong product pipeline for regenerative medicines are expected to generate market growth opportunities. However, unfavorable reimbursement policies, complexities in the manufacture of regenerative medicines, and the lack of standardized frameworks for the safety & efficacy of regenerative medicines are major challenges in the regenerative medicine market.
Increasing Funding for Regenerative Medicine Development Expected to Drive Market Growth During the Forecast Period
The field of regenerative medicine has gained traction in recent years owing to increasing applications in oncology, cardiology, orthopedics, and other medical domains. The key players operating in this market are raising funds for regenerative therapy development. Additionally, governments around the globe are offering grants and funding to advance regenerative medicine research.
Some of the recent developments in this space are as follows:
In April 2024, Century Therapeutics, Inc. (U.S.) acquired Clade Therapeutics (U.S.) and raised $60 million for the testing of natural killer cell therapy in certain blood cancers. Bain Capital Life Sciences (U.S.) provided the funding. With this acquisition, the company is likely to benefit from three preclinical programs and technology, allowing it to better engineer stem cell-derived medicines.
In March 2024, Pandorum Technologies Pvt. Ltd. (India), a tissue engineering and regenerative medicine company, raised $11 million in a pre-Series B funding round. The funding was raised for the clinical phase study of 'Liquid Cornea,' a treatment for corneal blindness and advancing the company's Tunable technology platform.
In November 2023, Siren Biotechnology (U.S.) received a $4 million grant from the California Institute for Regenerative Medicine (CIRM). The grant was awarded to aid the development of novel AAV immunogene therapies for cancer.
Regenerative Medicine Market Analysis: Key Findings
By Product: In 2024, the cell therapy segment is anticipated to dominate the regenerative medicine market with a share of
51.2%. The increasing public and private funding for stem cell therapy development, government efforts to streamline approval procedures, and collaborations among key players to advance stem cell therapy are factors contributing to the segment's dominant position in the regenerative medicine market.
By Application: The oncology segment is slated to register the highest CAGR of
26.5% during the forecast period. The high global burden of cancer, increasing research on regenerative medicine for cancer treatment, increasing approvals for regenerative medicine products for oncology applications, the growing number of oncology clinical trials, and increasing public & private funding dedicated to advancing oncology treatments are factors expected to support the segment's high growth. In March 2023, researchers at the University of California received a grant of $5.7 million from the California Institute of Regenerative Medicine to support advancements in stem cell therapy for cancer treatment.
By End user: In 2024, the hospitals & clinics segment is expected to account for the larger share of the regenerative medicine market. The segment is also slated to register the higher CAGR of 22% during the forecast period.
Explore the Key Market Segments Driving Growth (Download Free Sample) -
Geographic Analysis:
Based on geography, the regenerative medicine market is segmented into North America, Europe, Asia-Pacific, Latin America, and the Middle East & Africa. In 2024, North America is expected to account for the largest share of
41.8% of the regenerative medicine market. This market is projected to reach
$14.35 billion by 2031.
North America's dominant position in the regenerative medicine market is attributed to the rising prevalence of chronic conditions such as cancer and cardiovascular diseases, increasing funding for the development of regenerative medicine, the presence of key market players in the region, and the rising number of clinical trials in the region.
In 2024, the U.S. is expected to account for the major share of
89.0% of the regenerative medicine market in North America. The country's large market share is mainly attributed to the presence of key players involved in the development of regenerative medicine and rising investments from public and private players in the development of novel therapies. The number of clinical trials for regenerative medicine is also increasing in the country, further driving market growth. The number of key players involved in the development of regenerative medicine is also gradually increasing in the U.S. For instance, the number of developers reached 625 in 2022, a 2% increase over 2021 (source: Alliance for Regenerative Medicine).
Asia-Pacific: The Fastest-growing Regional Market
Asia-Pacific is projected to register the highest CAGR of
25.0% during the forecast period. In 2024, Japan is expected to account for the largest share of the regenerative medicine market in Asia-Pacific. The Asia-Pacific region is becoming an attractive market for healthcare product manufacturers due to ongoing improvements in healthcare infrastructure, the increasing number of hospitals, and growing government investments in the healthcare sector. Rapid economic growth in many countries within the Asia-Pacific region has increased government focus on healthcare, with rising investments aimed at enhancing access to healthcare facilities and building better healthcare infrastructure.
The Asia-Pacific region is one of the fastest-growing markets for regenerative medicine, driven by rising healthcare expenditures, a growing geriatric population, and an increasing burden of target diseases. Additionally, conferences promoting the use of regenerative medicine and active research initiatives are expected to further boost awareness and adoption of these therapies in the region.
Have specific research needs? Request a customized research report -
Germany Continues to Dominate the Regenerative Medicine Market in Europe
In 2024, Germany is expected to account for the largest share of
26.6% of the regenerative medicine market in Europe. Germany is the largest healthcare market in Europe by market volume, healthcare providers, number of patients, and medical technology manufacturers (source: Germany Trade & Invest). In 2022, the gross value added to the healthcare industry was $463.2 billion (€439.6 billion) (source: International Trade Administration). The high number of fatalities in Germany is marked by the rising incidence of chronic diseases such as ischemic heart disease, stroke, Chronic Obstructive Pulmonary Disease (COPD), and cancer. Cardiovascular diseases account for 37% of all deaths in Germany. According to Eurostat, ischemic heart disease is responsible for over one in ten deaths in the country. Furthermore, lung cancer is the most common cancer, accounting for 20% of all cancer-related deaths. Thus, the rising prevalence of chronic diseases, high healthcare expenditure, and well-developed healthcare infrastructure are the factors supporting Germany's large market share.
Regenerative Medicine Market: Competition Analysis
This report offers a competitive analysis based on an extensive assessment of the leading players' product portfolios, geographic presence, and key growth strategies adopted over the past 3–4 years. Major companies in the regenerative medicine market have implemented various strategies to expand their product offerings and global footprints and augment their market shares. The key strategies followed by leading companies in the regenerative medicine market include product launches, expansions, mergers & acquisitions, agreements, collaborations, and partnerships. The key players operating in the regenerative medicine market include
Novartis AG (Switzerland), Biogen Inc. (U.S.), Kite Pharma, Inc. (U.S.), Spark Therapeutics, Inc. (U.S.), Integra LifeSciences Corporation (U.S.), Sarepta Therapeutics, Inc. (U.S.), Takeda Pharmaceutical Company Limited (Japan), Amgen Inc. (U.S.), CORESTEMCHEMON Inc. (South Korea), Smith & Nephew plc (England), Vertex Pharmaceuticals Incorporated (U.S.), CSL Behring, LLC (U.S.), Janssen Global Services, LLC (U.S.), Medtronic plc (Ireland), AbbVie Inc. (U.S.), Bristol-Myers Squibb Company (U.S.), Ferring Pharmaceuticals A/S (Sweden), Pfizer Inc. (U.S.), bluebird bio Inc. (U.S.), and Vericel Corporation (U.S.).
Regenerative Medicine Industry Overview: Latest Developments from Key Industry Players
In January 2024, Smith & Nephew plc (U.K.) acquired CartiHeal Ltd. (Israel), a developer of Agili-C, an innovative sports medicine technology designed for cartilage regeneration in the knee.
In May 2024, Amgen Inc. (U.S.) received U.S. Food and Drug Administration (FDA) approval for IMDELLTRA, a T-cell engager therapy for the treatment of extensive-stage small-cell lung cancer.
In August 2024, Vericel Corporation (U.S.) received FDA approval for MACI Arthro, a device designed for arthroscopic administration to repair knee cartilage defects. This approval enhanced the company's product portfolio in the MACI segment.
In April 2023, Biogen Inc. (U.S.) received the U.S. Food and Drug Administration (FDA) approval for QALSODY (tofersen), a gene therapy used for treating amyotrophic lateral sclerosis (ALS) in people with a mutation in the superoxide dismutase 1 (SOD1) gene.
The report provides a competitive dashboard summarizing the market positioning of the 25 profiled market players in four quadrants, namely Industry Leaders, Differentiators, Emerging Companies, and Vanguards. These companies are positioned based on various parameters, including revenue, depth of offerings, brand equity, geographic presence, innovation, and organic & inorganic growth strategies. Novartis AG (Switzerland), Kite Pharma, Inc. (U.S.), Bristol-Myers Squibb Company (U.S.), Janssen Global Services, LLC (U.S.), and Biogen, Inc. (U.S.) are positioned in the Industry Leaders quadrant.
IMMEDIATE DELIVERY AVAILABLE | BUY THIS RESEARCH REPORT (Insights, Charts, Tables, Figures and More)-
Scope
of the Report:
Regenerative Medicine Market Assessment—by Product
Gene Therapy
Cell Therapy
Stem Cell Therapy
Autologous Therapy
Allogenic Therapy
Platelet-rich Plasma Therapy
Cell-based Immunotherapy
Tissue Engineering
Regenerative Medicine Market Assessment—by Application
Cardiology
Ophthalmology
Oncology
Neurology
Immunology & Inflammation
Musculoskeletal
Dermatology
Other Applications
Note: Other applications include wound care, orthopedics, and blood disorders.
Regenerative Medicine Market Assessment—by End User
Hospitals & Clinics
Ambulatory Surgical Centers
Regenerative Medicine Market Assessment—by Geography
North America
U.S.
Canada
Europe
Germany
France
U.K
Italy
Spain
Switzerland
Netherlands
Sweden
Rest of Europe (RoE)
Asia-Pacific (APAC)
China
Japan
India
South Korea
Australia
Rest of Asia-Pacific (RoAPAC)
Latin America
Brazil
Mexico
Rest of Latin America
Middle East & Africa
Browse Related Reports:
Sports Medicine Market
- Sports Medicine Market is set to hit $10.59 billion by 2031, growing at an 8.2% CAGR from 2024. Discover trends and market dynamics driving this growth.
Collagen and Gelatin Market
- The collagen and gelatin market for regenerative medicine is expected to reach USD 709.9 million by 2022, at a CAGR of 8.5% during the forecast period of 2017 to 2022.
Radiation Dose Management Market
- Radiation Dose Management Market is projected to reach $749.1 million by 2029, at a CAGR of 13.3%.
Molecular cytogenetics market -
Molecular cytogenetics market is expected to reach USD 2,266.4 million by 2022, at a CAGR of 11% during the forecast period of 2017 to 2022.
Next Generation Sequencing (NGS) Informatics Market
- Next Generation Sequencing (NGS) Informatics Market is projected to reach $4.3 billion by 2030, at a CAGR of 15.4% from 2023 to 2030.
Regenerative Medicine Market Research Summary:
Contact:
Mr. Khushal Bombe
Meticulous Market Research Pvt. Ltd.
1267 Willis St, Ste 200 Redding,
California, 96001, U.S.
USA: +1-646-781-8004
Europe: +44-203-868-8738
APAC: +91 744-7780008
Email- [email protected]
Visit Our Website:
Connect with us on LinkedIn-
Content Source:
Logo:
SOURCE Meticulous Market Research Pvt. Ltd.
WANT YOUR COMPANY'S NEWS FEATURED ON PRNEWSWIRE.COM?
440k+
Newsrooms &
Influencers
9k+
Digital Media
Outlets
270k+
Journalists
Opted In
GET STARTED

免疫疗法上市批准细胞疗法
2024-08-08
– Initiation of Phase 1 CALiPSO-1 Trial of CNTY-101 in Systemic Lupus Erythematosus, marking strategic expansion into autoimmune disease; protocol amended to include additional cohort of Lupus Nephritis patients – – Presented interim results from Phase 1 ELiPSE-1 trial of CNTY-101 demonstrating encouraging preliminary efficacy and tolerability data in heavily pretreated relapsed/refractory – – Completed dose escalation for ELiPSE-1 and advancing into dose expansion in 2H 2024 – – Ended second quarter 2024 with cash, cash equivalents, and investments of $269.6 million; Cash runway expected into 2026 – PHILADELPHIA, Aug. 08, 2024 (GLOBE NEWSWIRE) -- Century Therapeutics, Inc. (NASDAQ: IPSC), an innovative biotechnology company developing induced pluripotent stem cell (iPSC)-derived cell therapies in immuno-oncology and autoimmune disease, today reported financial results and business highlights for the second quarter ended June 30, 2024. “Our strategic autoimmune expansion, as highlighted by the recent initiation of the CALiPSO-1 trial in Systemic Lupus Erythematosus and addition of a Lupus Nephritis-specific cohort, positions Century as a potential leader in allogeneic cell therapies for autoimmune diseases. 2024 remains a time of focused execution as we work to advance our next-generation allogeneic iPSC-derived cell therapy platform and pipeline, equipped with our proprietary Allo-Evasion™ technology, capturing a diversified opportunity to address a broad range of indications with high unmet need. I am proud of the significant progress we have achieved in such a short period of time, particularly underscored by the evolution of our platform and capabilities, which we anticipate will enable our iPSC candidates to have a more controlled, durable, and tolerable profile,” said Brent Pfeiffenberger, Pharm.D., Chief Executive Officer of Century Therapeutics. “We remain focused on progressing CNTY-101 in both of our clinical-stage programs, including advancement into dose expansion in the ELiPSE-1 trial in patients with r/r B-cell lymphomas and acceleration of patient enrollment following the recent initiation of the CALiPSO-1 trial. We’ve made strides in our initial execution of autoimmune expansion as evidenced by our CALiPSO-1 trial updates, while simultaneously pursuing additional regulatory filings for CNTY-101 in other autoimmune disease indications in the second half of the year. We look forward to continued execution and the opportunity to deliver on our next set of potential catalysts, including the expectation of initial clinical data from CALiPSO-1 by year-end.” Research & Development Highlights Consistent with Century’s autoimmune disease expansion efforts announced in April 2024, the Company recently initiated the Phase 1 CALiPSO-1 trial of CNTY-101 (NCT06255028) in Systemic Lupus Erythematosus (SLE). The first clinical trial site has been activated, with additional sites continuing to open across the United States. The Company expects initial clinical data from CALiPSO-1 by year-end 2024. Furthermore, Century recently amended the protocol to include a new indication-specific cohort of Lupus Nephritis (LN) patients. CALiPSO-1 is an open-label multi-center clinical trial to evaluate the safety, tolerability, pharmacokinetics, and clinical response of CNTY-101 in patients with moderate to severe SLE and LN who have failed at least two standard immunosuppressive therapies. The inclusion of LN patients highlights Century’s execution in pursuing additional regulatory filings as a way of accelerating and broadening its research and development initiatives in autoimmune diseases. The Company intends to submit additional regulatory filings for CNTY-101 in autoimmune disease indications with limited current treatment options and high unmet need in the second half of 2024.In May 2024, Century presented two posters at the American Society of Gene and Cell Therapy (ASGCT) Annual Meeting showcasing the potential ability of its lead program, CNTY-101, a CD19 targeting allogeneic iNK cell therapy with 6 precision gene edits powered by Century’s Allo-Evasion™ technology, to treat B-Cell driven autoimmune diseases including SLE, and new preclinical data demonstrating the potential utility of using a novel synthetic ligand targeting CD300a as a universal strategy for preventing natural killer (NK) cell mediated rejection in allogeneic cell therapies. The Company believes that these capabilities demonstrate the potential protection of allogeneic cell therapies with the possibility for improved outcomes, while delivering a broadly beneficial treatment option across a range of indications.In June 2024, the Company presented encouraging interim efficacy and safety data from the ongoing Phase 1 ELiPSE-1, multicenter, open-label clinical trial of CNTY-101 (NCT05336409) in heavily pre-treated patients with R/R CD19-positive B-cell lymphomas at the American Society of Clinical Oncology (ASCO) Annual Meeting. Evaluable preliminary safety (n=12) and efficacy (n=10) as of the data cutoff date of March 27, 2024, from the ongoing dose escalation portion of the trial, demonstrated a manageable tolerability profile with no observed dose limiting toxicities (DLT) or graft-versus-host disease (GvHD). After rapidly trafficking out of circulation, pharmacokinetics (PK), evaluated by a novel cell-free DNA method, showed that CNTY-101 persistence outside the bloodstream trended with increases in dose. Data also showed additional responses across escalating doses and different types of B-cell malignancies in heavily pretreated patients with predominantly aggressive or high-risk histologies.The Company recently completed dose escalation of schedule A (single dose per cycle) and schedule B (3 doses per cycle) in the ELiPSE-1 trial and is currently enrolling patients in the dose confirmation portion. Progression into dose expansion is expected in the second half of 2024. Corporate Highlights In April 2024, the Company completed a private placement of common stock with gross proceeds of $60 million with new and existing investors. Also in April 2024, the Company closed the acquisition of Clade Therapeutics, bringing enhancement of its Allo-Evasion™ platform and adding three preclinical stage αβ iT programs spanning across cancer and autoimmune diseases to its pipeline. Second Quarter 2024 Financial Results Cash Position: Cash, cash equivalents, and marketable securities were $269.6 million as of June 30, 2024, as compared to $261.8 million as of December 31, 2023. Net cash used in operations was $57.6 million for the six months ended June 30, 2024, compared to net cash used in operations of $48.5 million for the six months ended June 30, 2023.Collaboration Revenue: Collaboration revenue generated through the Company’s collaboration, option, and license agreement with Bristol-Myers Squibb was $0.8 million for the three months ended June 30, 2024, compared to $0.1 million for the same period in 2023.Research and Development (R&D) expenses: R&D expenses were $27.2 million for the three months ended June 30, 2024, compared to $22.7 million for the same period in 2023. The increase in R&D expenses was primarily due to increased manufacturing activity for CNTY-101 and the acquisition of Clade Therapeutics.General and Administrative (G&A) expenses: G&A expenses were $8.3 million for the three months ended June 30, 2024, compared to $8.2 million for the same period in 2023.Net loss: Net loss was $31.2 million for the three months ended June 30, 2024, compared to $33.3 million for the three months ended June 30, 2023. Financial Guidance The Company expects full year generally accepted accounting principles (GAAP) operating expenses to be between $150 million and $160 million.The Company estimates its cash, cash equivalents, and investments will support operations into 2026. About Century Therapeutics Century Therapeutics (NASDAQ: IPSC) is harnessing the power of adult stem cells to develop curative cell therapy products for cancer and autoimmune diseases that we believe will allow us to overcome the limitations of first-generation cell therapies. Our genetically engineered, iPSC-derived cell product candidates are designed to specifically target hematologic and solid tumor cancers, with a broadening application to autoimmune diseases. We are leveraging our expertise in cellular reprogramming, genetic engineering, and manufacturing to develop therapies with the potential to overcome many of the challenges inherent to cell therapy and provide a significant advantage over existing cell therapy technologies. We believe our commitment to developing off-the-shelf cell therapies will expand patient access and provide an unparalleled opportunity to advance the course of cancer and autoimmune disease care. For more information on Century Therapeutics please visit www.centurytx.com. Century Therapeutics Forward-Looking Statement This press release contains forward-looking statements within the meaning of, and made pursuant to the safe harbor provisions of, The Private Securities Litigation Reform Act of 1995. All statements contained in this press release, other than statements of historical facts or statements that relate to present facts or current conditions, including but not limited to, statements regarding our clinical development plans and timelines and the initial safety and efficacy profiles of CNTY-101 are forward-looking statements. These statements involve known and unknown risks, uncertainties and other important factors that may cause our actual results, performance, or achievements to be materially different from any future results, performance or achievements expressed or implied by the forward-looking statements. In some cases, you can identify forward-looking statements by terms such as “may,” “might,” “will,” “should,” “expect,” “plan,” “aim,” “seek,” “anticipate,” “could,” “intend,” “target,” “project,” “contemplate,” “believe,” “estimate,” “predict,” “forecast,” “potential” or “continue” or the negative of these terms or other similar expressions. The forward-looking statements in this press release are only predictions. We have based these forward-looking statements largely on our current expectations and projections about future events and financial trends that we believe may affect our business, financial condition, and results of operations. These forward-looking statements speak only as of the date of this press release and are subject to a number of risks, uncertainties and assumptions, some of which cannot be predicted or quantified and some of which are beyond our control, including, among others: our ability to successfully advance our current and future product candidates through development activities, preclinical studies, and clinical trials; our dependence on the success of our lead product candidate, CNTY-101; the ability of CNTY-101 to be administered as part of a multi-dose strategy and to enable responses without lymphodepletion; uncertainties inherent in the results of preliminary data, pre-clinical studies and earlier-stage clinical trials, which may not be predictive of final results or the results of later-stage clinical trials; the timing of and our ability to successfully enroll the Phase 1 SLE and LN trial; the timing of and our ability to enter dose expansion of the Phase 1 R/R CD19-positive B-cell lymphomas trial; our ability to obtain FDA clearance of our future IND submissions and commence and complete clinical trials on expected timelines, or at all; our reliance on the maintenance of certain key collaborative relationships for the manufacturing and development of our product candidates; the timing, scope and likelihood of regulatory filings and approvals, including final regulatory approval of our product candidates; the impact of geopolitical issues, banking instability and inflation on our business and operations, supply chain and labor force; the performance of third parties in connection with the development of our product candidates, including third parties conducting our clinical trials as well as third-party suppliers and manufacturers; our ability to successfully commercialize our product candidates and develop sales and marketing capabilities, if our product candidates are approved; our ability to recruit and maintain key members of management and our ability to maintain and successfully enforce adequate intellectual property protection. These and other risks and uncertainties are described more fully in the “Risk Factors” section of our most recent filings with the Securities and Exchange Commission and available at www.sec.gov. You should not rely on these forward-looking statements as predictions of future events. The events and circumstances reflected in our forward-looking statements may not be achieved or occur, and actual results could differ materially from those projected in the forward-looking statements. Moreover, we operate in a dynamic industry and economy. New risk factors and uncertainties may emerge from time to time, and it is not possible for management to predict all risk factors and uncertainties that we may face. Except as required by applicable law, we do not plan to publicly update or revise any forward-looking statements contained herein, whether as a result of any new information, future events, changed circumstances or otherwise. For More Information: Investor Relations & Media Contacts Century Therapeutics Katja Buhrer SVP, Head of Corporate Affairs and Strategy katja.buhrer@centurytx.com 917-969-3438 Argot Partners Julie Seidel/Noor Pahlavi century@argotpartners.com 212-600-1902 Century Therapeutics, IncCondensed Balance Sheets(unaudited, in thousands)
June 30, December 31,Assets 2024 2023Current Assets: $ $ Cash and cash equivalents 41,457 47,324 Short-term investments 154,945 125,414 Prepaid expenses and other current assets 7,076 4,256 Total current assets 203,478 176,994 Property and equipment, net 69,405 71,705 Operating lease right-of-use assets, net 28,570 20,376 Long-term investments 73,226 89,096 Goodwill 5,091 - Intangible assets 33,300 - Other long-term assets 3,376 2,520 Total assets $416,446 $360,691
Liabilities, convertible preferred stock, and stockholders' equity
Current liabilities:
Accounts payable $3,358 $2,741 Accrued expenses and other liabilities 11,445 10,733 Long-term debt, current - - Deferred revenue, current 4,360 4,372 Total current liabilities 19,163 17,846 Operating lease liability, noncurrent 52,713 46,658 Other long-term liabilities 3,386 56 Deferred revenue 109,768 111,381 Contingent consideration liability 9,312 - Total liabilities 194,342 175,941 Stockholders' equity
Common stock 8 6 Additional paid-in capital 937,445 840,407 Accumulated deficit (715,040) (655,771)Accumulated other comprehensive loss (309) 108 Total stockholders' equity 222,104 184,750 Total liabilities and stockholders' equity $416,446 $360,691 Century Therapeutics, IncCondensed consolidated statements of operations(unaudited, in thousands, except share and per share amounts)
Three Months Ended Three Months Ended Six Months Ended Six Months Ended June 30, 2024 June 30, 2023 June 30, 2024 June 30, 2023Collaboration Revenue$771 $99 $1,625 $1,819
Operating Expenses
Research and development 27,220 22,727 50,641 47,626 General and administrative 8,306 8,229 17,052 17,131 Impairment on long-lived assets - 4,220 - 4,220 Total operating expenses 35,526 35,176 67,693 68,977
Loss from operations (34,755) (35,077) (66,068) (67,158)
Interest expense - (136) - (540)Interest income 3,582 3,058 6,820 5,681 Other income, net (12) (186) 1 (380)Loss before provision for income taxes (31,185) (32,341) (59,247) (62,397)Provision for income taxes (22) (950) (22) (2,158)Net Loss$(31,207) $(33,291) $(59,269) $(64,555)
Unrealized (loss) gain on investments (102) 59 (453) 1,255 Foreign currency translation adjustment gain (loss) 35 9 36 - Comprehensive loss$(31,274) $(33,223) $(59,686) $(63,300)
Net loss per common share - Basic and Diluted (0.38) (0.56) 0.82 (1.10)
Weighted average common shares outstanding 82,092,167 59,251,363 72,194,402 58,904,726
临床1期细胞疗法财报并购ASCO会议
2024-05-09
- Announced plans to pursue additional autoimmune disease regulatory filings for its iPSC derived NK cell therapy, CNTY-101, beyond systemic lupus erythematosus (SLE)
- Closed $60 million private placement led by Bain Capital Life Sciences supporting accelerated expansion in autoimmune disease
- Acquired Clade Therapeutics bringing enhancement of Allo-Evasion™ platform and three preclinical stage αβ iT programs spanning across cancer and autoimmune diseases
- Additional clinical data from Phase 1 ELiPSE-1 trial in relapsed/refractory (R/R) B-cell lymphoma to be presented at American Society for Clinical Oncology (ASCO) Annual Meeting
- Ended 1Q24 with cash, cash equivalents, and investments of $249.9 million; Cash runway into 2026
PHILADELPHIA, May 09, 2024 (GLOBE NEWSWIRE) -- Century Therapeutics, Inc. (NASDAQ: IPSC), an innovative biotechnology company developing induced pluripotent stem cell (iPSC)-derived cell therapies in immuno-oncology and autoimmune diseases, today reported financial results and business highlights for the first quarter ended March 31, 2024.
"We have made significant clinical, operational and research-oriented progress so far this year, and I am incredibly excited by the momentum we’ve been able to achieve in such a short period of time,” said Brent Pfeiffenberger, Pharm.D., Chief Executive Officer of Century Therapeutics. “Looking ahead, we will be sharing additional clinical data from the ELiPSE-1 trial of CNTY-101 in R/R NHL at the upcoming ASCO Annual Meeting in June. In addition, we are on track to initiate the Phase 1 CALiPSO-1 trial of CNTY-101 in SLE in the first half of 2024, while also continuing to progress the multiple planned regulatory filings for CNTY-101 in additional autoimmune disease indications later this year. We believe Century’s position as a leader in allogeneic, iPSC-derived cell therapy is fortified by the recent expansion of our pipeline and platform capabilities through the acquisition of Clade Therapeutics, and we are looking forward to continued execution across our robust portfolio of novel assets providing us with multiple near- and long-term potential value drivers.”
Research and Development Highlights and Upcoming Milestones
CNTY-101
CNTY-101 is a CD19 targeting allogeneic iNK cell therapy with 6 precision gene edits powered by Century’s Allo-Evasion™ technology, which enables repeat dosing without the need for continued lymphodepletion. Century’s core Allo-Evasion™ edits are designed to overcome the three major pathways of host versus graft rejection: CD8+ T cells, CD4+ T cells and NK cells.
In April 2024, the Company announced plans to expand clinical development of CNTY-101 into additional autoimmune disease indications beyond SLE. In the second half of 2024, Century intends to submit additional regulatory filings for CNTY-101 in autoimmune disease indications with limited current treatment options and high unmet need. Additionally, the Company is planning to evaluate CNTY-101 for SLE in the Phase 1 CALiPSO-1 trial, which is on track to be initiated in the first half of 2024 with preliminary data expected by the end of 2024.
Century plans to share additional data from its Phase 1 ELiPSE-1 trial in R/R non-Hodgkin lymphoma (NHL) at the upcoming ASCO Annual Meeting, being held May 31-June 4, 2024, in Chicago, IL. As previously announced, in this heavily pretreated and refractory patient population, CNTY-101 has demonstrated a favorable safety pro the initial seven patients treated with Dose Level 1 (100 million cells) and Dose Level 2 (300 million cells) on a once monthly schedule. In these low dose levels, CNTY-101 demonstrated encouraging early response signals, including two complete responses (CRs) and one partial response (PR). Initial translational data supports the potential for Allo-Evasion™ to enable a multidose regimen without the need for continued lymphodepletion.
Platform Technology and Additional Pipeline Programs
In April 2024, Century shared six poster presentations at the 2024 American Association for Cancer Research (AACR) Annual Meeting showcasing new preclinical data on additional Allo-Evasion™ edits in addition to the Company’s end-to-end cell therapy capabilities including expertise across iPSC reprogramming, gene editing, protein engineering, Allo-Evasion™ technology and computational biology. Key abstracts highlighted Century’s novel, dual-targeting CAR for B-cell mediated malignancies demonstrating in vitro and in vivo cytotoxicity and antigen loss resistance; and new data on the Allo-Evasion™ platform showcasing its potential to evade identification by the host immune system, which would allow for repeat dosing without rejection, enabling increased persistence of the cells during the treatment period and potentially leading to deeper and more durable responses. Across all six posters, the findings highlight Century’s unique gene editing, protein engineering, and manufacturing capabilities that are the foundations of its allogeneic cell therapy pipeline and platform. The presented posters are available at the Scientific Resources page of the Company’s website.
In April 2024, the Company announced the acquisition of Clade Therapeutics, a privately held biotech company focused on discovering and delivering engineerable, off-the-shelf, scalable, and consistent stem cell-based medicines, with a focus on iPSC-derived αβ T cells. This acquisition brings complementary technology to enhance Century’s Allo-Evasion™ platform and additional next-generation iT programs spanning targets in cancer, and autoimmune diseases. These programs include CLDE-308, an αβ iT cell program targeting CD19 in autoimmune disease and B-cell malignancies, CLDE-361, an αβ iT cell program targeting BCMA in myasthenia gravis, and an undisclosed iT cell focused research program in solid tumors.
Business Highlights
In April 2024, the Company entered into a securities purchase agreement with a select group of institutional investors for an approximately $60 million private placement of its common stock. The private placement closed on April 15, 2024, and was led by new investors Bain Capital Life Sciences, Adage Capital Partners LP, Octagon Capital, and Superstring Capital, and existing investors including Casdin Capital, Boxer Capital, Venrock Healthcare Capital Partners and DAFNA Capital Management, LLC.
First Quarter 2024 Financial Results
Cash Position: Cash, cash equivalents, and marketable securities were $249.9 million as of March 31, 2024, as compared to $261.8 million as of December 31, 2023. Net cash used in operations was $30.2 million for the three months ended March 31, 2024, compared to net cash used in operations of $29.2 million for the three months ended March 31, 2023.
Collaboration Revenue: Collaboration revenue generated through the Company’s collaboration, option and license agreement with Bristol-Myers Squibb (BMS) was $0.9 million for the three months ended March 31, 2024, compared to $1.7 million for the same period in 2023.
Research and Development (R&D) expenses: R&D expenses were $23.4 million for the three months ended March 31, 2024, compared to $24.9 million for the same period in 2023. The decrease in R&D expenses was primarily due to the reduction in force that occurred in January of 2023.
General and Administrative (G&A) expenses: G&A expenses were $8.7 million for the three months ended March 31, 2024, compared to $8.9 million for the same period in 2023.
Net loss: Net loss was $28.1 million for the three months ended March 31, 2024, compared to $31.3 million for the three months ended March 31, 2023.
Financial Guidance
The Company expects full year generally accepted accounting principles (GAAP) operating expenses to be between $150 million and $160 million as compared to the previous guidance range of $135 million to $145 million. The increase is driven by additional operating expenses related to the integration of Clade Therapeutics, as well as the Company’s planned expanded clinical development of CNTY-101 into additional autoimmune disease indications. The Company is currently in the process of completing its accounting analysis of the acquisition of Clade. The revised guidance does not include any potential non-cash charges related to the acquisition.
The Company estimates its cash, cash equivalents, and investments will support operations into 2026.
About Century Therapeutics
Century Therapeutics (NASDAQ: IPSC) is harnessing the power of adult stem cells to develop curative cell therapy products for cancer and autoimmune and inflammatory diseases that we believe will allow us to overcome the limitations of first-generation cell therapies. Our genetically engineered, iPSC-derived cell product candidates are designed to specifically target hematologic and solid tumor cancers, with a broadening application to autoimmune and inflammatory diseases. We are leveraging our expertise in cellular reprogramming, genetic engineering, and manufacturing to develop therapies with the potential to overcome many of the challenges inherent to cell therapy and provide a significant advantage over existing cell therapy technologies. We believe our commitment to developing off-the-shelf cell therapies will expand patient access and provide an unparalleled opportunity to advance the course of cancer and autoimmune and inflammatory disease care. For more information on Century Therapeutics please visit .
Forward-Looking Statements
This press release contains forward-looking statements within the meaning of, and made pursuant to the safe harbor provisions of, The Private Securities Litigation Reform Act of 1995. All statements contained in this press release, other than statements of historical facts or statements that relate to present facts or current conditions, including but not limited to, statements regarding our clinical development plans and timelines, and our financial guidance are forward-looking statements. These statements involve known and unknown risks, uncertainties and other important factors that may cause our actual results, performance, or achievements to be materially different from any future results, performance or achievements expressed or implied by the forward-looking statements. In some cases, you can identify forward-looking statements by terms such as “may,” “might,” “will,” “should,” “expect,” “plan,” “aim,” “seek,” “anticipate,” “could,” “intend,” “target,” “project,” “contemplate,” “believe,” “estimate,” “predict,” “forecast,” “potential” or “continue” or the negative of these terms or other similar expressions. The forward-looking statements in this press release are only predictions. We have based these forward-looking statements largely on our current expectations and projections about future events and financial trends that we believe may affect our business, financial condition, and results of operations. These forward-looking statements speak only as of the date of this press release and are subject to a number of risks, uncertainties and assumptions, some of which cannot be predicted or quantified and some of which are beyond our control, including, among others: our ability to successfully advance our current and future product candidates through development activities, preclinical studies, and clinical trials; our dependence on the success of our lead product candidate, CNTY-101; the ability of CNTY-101 to be administered as part of a multi-dose strategy and to enable responses without lymphodepletion; uncertainties inherent in the results of preliminary data, preclinical studies and earlier-stage clinical trials, which may not be predictive of final results or the results of later-stage clinical trials; the timing of and our ability to initiate and successfully enroll the Phase 1 SLE trial; our ability to successfully integrate operations with Clade Therapeutics; our ability to obtain FDA clearance of our future IND submissions and commence and complete clinical trials on expected timelines, or at all; our reliance on the maintenance of certain key collaborative relationships for the manufacturing and development of our product candidates; the timing, scope and likelihood of regulatory filings and approvals, including final regulatory approval of our product candidates; the impact of geopolitical issues, banking instability and inflation on our business and operations, supply chain and labor force; the performance of third parties in connection with the development of our product candidates, including third parties conducting our clinical trials as well as third-party suppliers and manufacturers; our ability to successfully commercialize our product candidates and develop sales and marketing capabilities, if our product candidates are approved; our ability to recruit and maintain key members of management and our ability to maintain and successfully enforce adequate intellectual property protection. These and other risks and uncertainties are described more fully in the “Risk Factors” section of our most recent filings with the Securities and Exchange Commission and available at You should not rely on these forward-looking statements as predictions of future events. The events and circumstances reflected in our forward-looking statements may not be achieved or occur, and actual results could differ materially from those projected in the forward-looking statements. Moreover, we operate in a dynamic industry and economy. New risk factors and uncertainties may emerge from time to time, and it is not possible for management to predict all risk factors and uncertainties that we may face. Except as required by applicable law, we do not plan to publicly update or revise any forward-looking statements contained herein, whether as a result of any new information, future events, changed circumstances or otherwise.
For More Information:
Investors and media: Julie Seidel/ Noor Pahlavi – century@argotpartners.com
Century Therapeutics, Inc
Condensed Balance Sheets
(unaudited, in thousands)
March 31,
December 31,
Assets
2024
2023
Current Assets:
$
$
Cash and cash equivalents
46,812
47,324
Short-term investments
145,204
125,414
Prepaid expenses and other current assets
7,797
4,256
Total current assets
199,813
176,994
Property and equipment, net
69,005
71,705
Operating lease right-of-use assets, net
19,314
20,376
Long-term investments
57,852
89,096
Other long-term assets
2,522
2,520
Total assets
$
348,507
$
360,691
Liabilities, convertible preferred stock, and stockholders' equity
Current liabilities:
Accounts payable
$
3,432
$
2,741
Accrued expenses and other liabilities
8,023
10,733
Long-term debt, current
-
-
Deferred revenue, current
4,610
4,372
Total current liabilities
16,065
17,846
Operating lease liability, noncurrent
44,251
46,658
Other long-term liabilities
20
56
Deferred revenue
110,288
111,381
Total liabilities
170,624
175,941
Stockholders' equity
Common stock
6
6
Additional paid-in capital
861,952
840,407
Accumulated deficit
(683,833
)
(655,771
)
Accumulated other comprehensive loss
(241
)
108
Total stockholders' equity
177,883
184,750
Total liabilities and stockholders' equity
$
348,507
$
360,691
Century Therapeutics, Inc
Condensed consolidated statements of operations
(unaudited, in thousands, except share and per share amounts)
March 31,
March 31,
2024
2023
Collaboration Revenue
$
855
$
1,720
Operating Expenses
Research and development
23,421
24,899
General and administrative
8,743
8,902
Total operating expenses
32,164
33,801
Loss from operations
(31,309
)
(32,081
)
Interest expense
-
(404
)
Interest income
3,237
2,623
Other income, net
11
(194
)
Loss before provision for income taxes
(28,061
)
(30,056
)
Provision for income taxes
(1
)
(1,208
)
Net Loss
$
(28,062
)
$
(31,264
)
Unrealized gain (loss) on investments
(351
)
1,196
Foreign currency translation adjustment gain (loss)
2
(9
)
Comprehensive loss
$
(28,411
)
$
(30,077
)
Net loss per common share - Basic and Diluted
(0.45
)
(0.53
)
Weighted average common shares outstanding
62,296,637
58,610,375
细胞疗法临床1期并购AACR会议财报
100 项与 Clade Therapeutics, Inc. 相关的药物交易
登录后查看更多信息
100 项与 Clade Therapeutics, Inc. 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2025年03月31日管线快照
管线布局中药物为当前组织机构及其子机构作为药物机构进行统计,早期临床1期并入临床1期,临床1/2期并入临床2期,临床2/3期并入临床3期
药物发现
1
1
临床前
其他
2
登录后查看更多信息
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
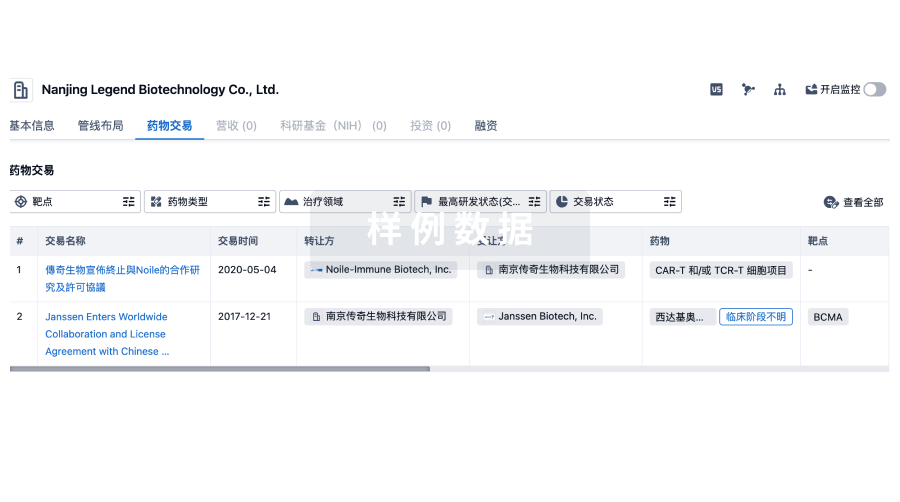
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
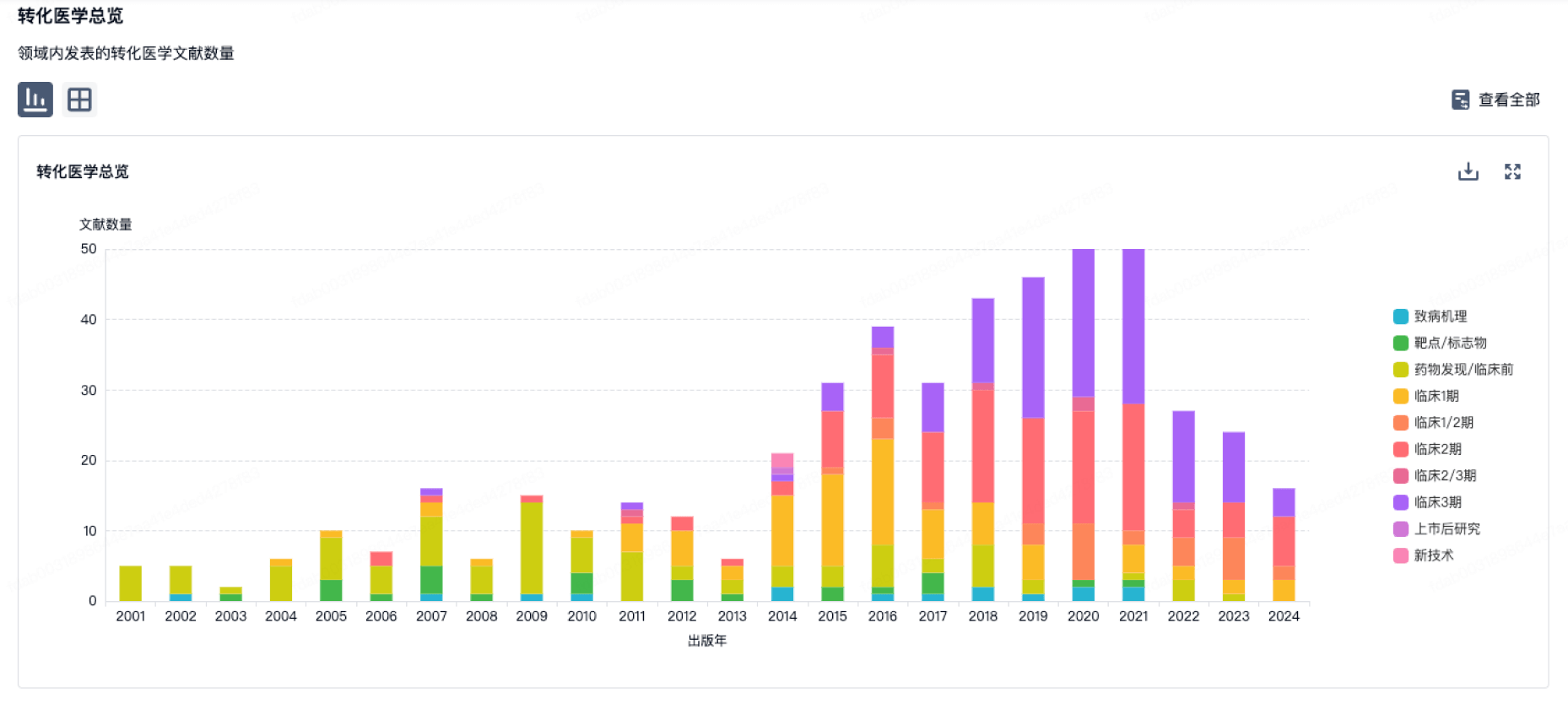
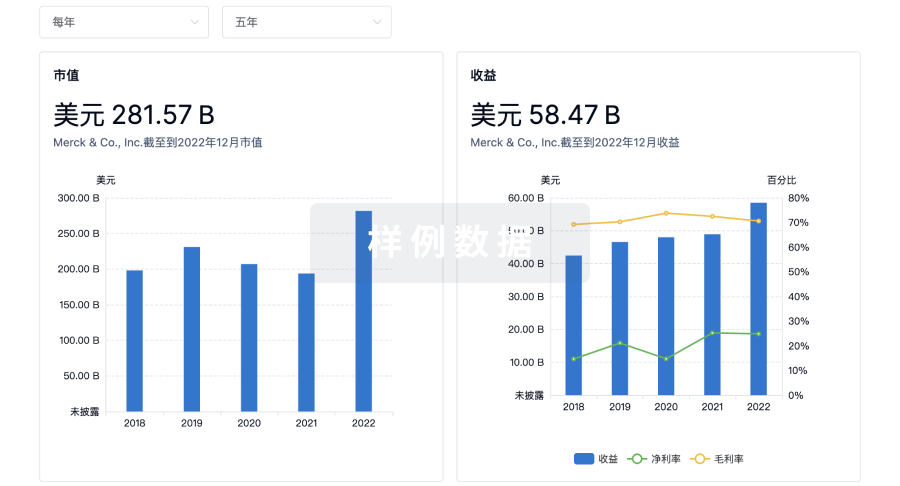
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
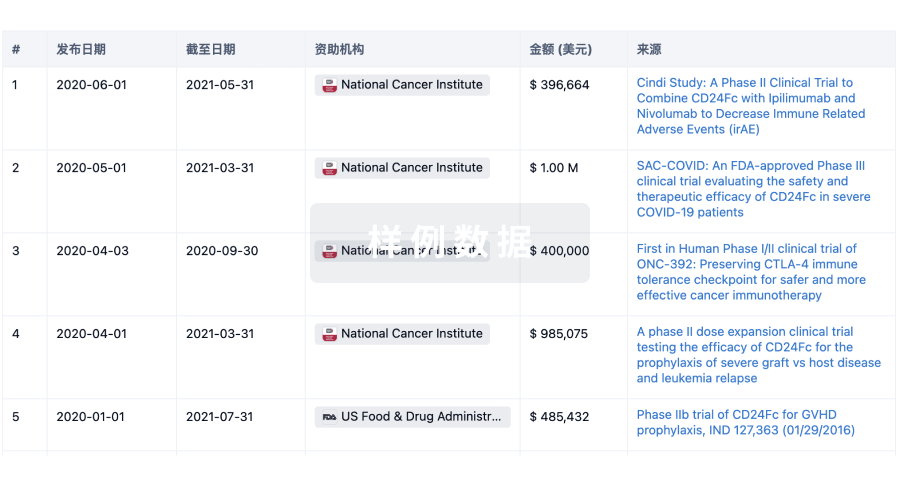
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
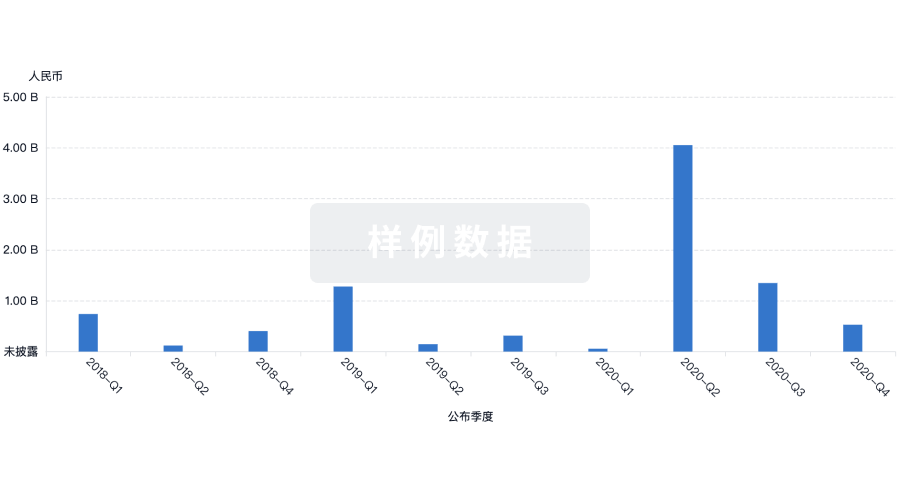
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
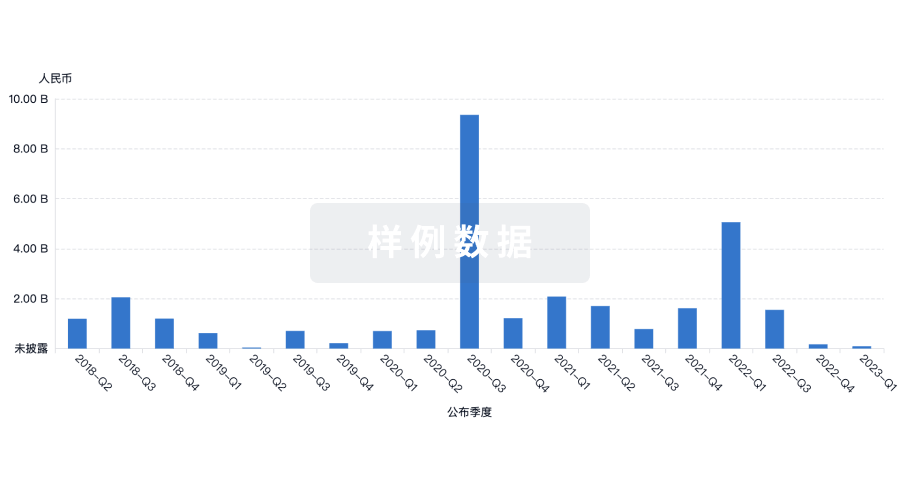
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用