更新于:2024-11-04
Chongqing Xiwei Medical Technology Co., Ltd.
重庆希韦医药科技有限公司|
私营公司 | 子公司|
2021|
中国重庆市
重庆希韦医药科技有限公司|
私营公司 | 子公司|
2021|
中国重庆市
更新于:2024-11-04
概览
关联
3
项与 重庆希韦医药科技有限公司 相关的临床试验硫酸艾沙康唑胶囊在空腹及餐后条件下的人体生物等效性试验
考察空腹及餐后条件下,健康受试者单次口服由重庆希韦医药科技有限公司提供的硫酸艾沙康唑胶囊【受试制剂T,规格:100mg(按C22H17F2N5OS计)】与相同条件下单次口服由Basilea Pharmaceutica Deutschland GmbH持证的硫酸艾沙康唑胶囊【参比制剂R,商品名:康新博®/CRESEMBA®,规格:100mg(按C22H17F2N5OS计)】的药动学特征,评价两制剂的生物等效性及安全性,为该受试制剂注册申请提供依据。
开始日期2024-06-12 |
申办/合作机构 |
来特莫韦片(240mg)在中国健康受试者中空腹和餐后给药条件下随机、开放、单剂量、两序列、两周期、双交叉生物等效性试验
主要研究目的:按有关生物等效性试验的规定,选择Merck Sharp & Dohme B.V.为持证商的来特莫韦片(商品名:Prevymis(普瑞明),规格:240mg)为参比制剂,对重庆博腾药业有限公司生产,重庆希韦医药科技有限公司提供的受试制剂来特莫韦片(规格:240mg)进行空腹和餐后给药人体生物等效性试验,比较受试制剂中药物的吸收速度和吸收程度与参比制剂的差异是否在可接受的范围内,评价两种制剂在空腹和餐后给药条件下的生物等效性。
次要研究目的:观察健康受试者口服受试制剂来特莫韦片(规格:240mg)和参比制剂来特莫韦片(商品名:Prevymis(普瑞明),规格:240mg)的安全性。
开始日期2023-11-26 |
申办/合作机构 |
二甲双胍恩格列净片在中国健康受试者空腹和餐后状态下的单中心、随机、开放、两制剂、两周期、两序列、单次给药、双交叉生物等效性研究
主要目的:以二甲双胍恩格列净的主要药代动力学参数(AUC和Cmax)为生物等效性的评价指标,在中国健康受试者空腹和餐后状态下评估受试制剂(重庆华森制药股份有限公司生产的二甲双胍恩格列净片,规格:每片含盐酸二甲双胍1000mg与恩格列净12.5mg)和参比制剂(Boehringer Ingelheim Promeco S.A. de C.V.生产的二甲双胍恩格列净片,规格:每片含盐酸二甲双胍1000mg与恩格列净12.5mg,商品名:Synjardy ®)的生物等效性。
次要目的:观察空腹和餐后状态下口服受试制剂和参比制剂的安全性。
开始日期2023-04-14 |
申办/合作机构 |
100 项与 重庆希韦医药科技有限公司 相关的临床结果
登录后查看更多信息
0 项与 重庆希韦医药科技有限公司 相关的专利(医药)
登录后查看更多信息
3
项与 重庆希韦医药科技有限公司 相关的新闻(医药)2024-10-15
·米内网
精彩内容
近日,国家药监局官网显示,南京正大天晴制药的4类仿制药来特莫韦注射液获批生产并视同过评,此前该产品仅原研厂家默沙东在售。米内网数据显示,2024上半年中国公立医疗机构终端来特莫韦注射液的销售额增速超过732%。
来特莫韦是一种新型巨细胞病毒末端酶抑制剂,与传统的DNA聚合酶抑制剂相比,来特莫韦对巨细胞病毒的选择性更高,作用强度也有显著提高。近年来,默沙东的来特莫韦在全球的销售额保持快速增长态势,2023年超过了6亿美元。
2021及2022年,默沙东的来特莫韦片及来特莫韦注射液先后获批进入国内市场,目前均已通过谈判纳入全国医保乙类目录;2024年4月及10月,南京正大天晴制药的来特莫韦片及来特莫韦注射液获批上市,均为国内首仿(含剂型首仿)。此外,齐鲁制药、重庆希韦医药的来特莫韦片,以及齐鲁制药、山东诚创蓝海医药、重庆希韦医药的来特莫韦注射液报产在审。
来特莫韦片及来特莫韦注射液新分类报产情况
来源:米内网一致性评价进度数据库
米内网数据显示,2024上半年在中国城市公立医院、县级公立医院、城市社区中心以及乡镇卫生院(简称中国公立医疗机构)终端来特莫韦片的销售额超过1亿元,同比增长约159%,而来特莫韦注射液的销售额增速则超过732%。
今年以来,南京正大天晴制药已有来特莫韦注射液、达比加群酯胶囊、氯苯唑酸葡胺软胶囊、沙库巴曲缬沙坦钠片、舒更葡糖钠注射液、来特莫韦片6个品种获批上市并视同过评,其中来特莫韦片、来特莫韦注射液为首仿(含剂型首仿)+首家过评,氯苯唑酸葡胺软胶囊国产第2家获批。
在产品申报方面,今年以来南京正大天晴制药有8个品种以新注册分类提交上市/临床申请,其中氘丁苯那嗪片、琥珀酰明胶电解质醋酸钠注射液、奥贝胆酸片、苯磺酸美洛加巴林片、瑞舒伐他汀依折麦布片(Ⅰ)等均暂无首仿获批(不含原研地产化)。
2024年以来南京正大天晴制药新分类申报的品种
来源:米内网中国申报进度(MED)数据库注:米内网《中国公立医疗机构药品终端竞争格局》,统计范围是:中国城市公立医院、县级公立医院、城市社区中心以及乡镇卫生院,不含民营医院、私人诊所、村卫生室;上述销售额以产品在终端的平均零售价计算。数据统计截至10月15日,如有疏漏,欢迎指正!
本文为原创稿件,转载请注明来源和作者,否则将追究侵权责任。投稿及报料请发邮件到872470254@qq.com稿件要求详询米内微信首页菜单栏商务及内容合作可联系QQ:412539092
【分享、点赞、在看】点一点不失联哦
上市批准一致性评价
2024-04-15
刚刚,NMPA发布2024年04月15日药品批准证明文件送达信息,本批次共有65个受理号获批,其中5个为一致性评价受理号,过评品种为:南京正科医药股份有限公司,2品规盐酸左氧氟沙星片四川制药制剂有限公司,3品规注射用氨苄西林钠本次另有43个上市申请受理号获批,涉及近30个品种,如:成都倍特药业、浙江华海药、国药集团容生制药的恩格列净片同日获批;康缘华威医药的泊沙康唑肠溶片;杭州民生药业的利格列汀片;浙江恒研医药的阿司匹林肠溶片;南京恒道医药的盐酸奥洛他定滴眼液;扬子江药业集团江苏紫龙药业的磷酸特地唑胺片等。其中,南京正大天晴制药的来特莫韦片获批上市,拿下国内首仿!来特莫韦最早由德国AiCurisanti-infectivecures GmbH开发,后公司被默沙东收购。来特莫韦是新型非核苷类巨细胞病毒(CMV)抑制剂,用于接受异基因造血干细胞移植(HSCT)的巨细胞病毒(CMV)血清学阳性的成人受者[R+]预防巨细胞病毒感染和巨细胞病毒病。来特莫韦片剂和注射剂最早于2017年获美国FDA批准上市,商品名为Prevymis。2022年1月,默沙东的来特莫韦片(商品名:普瑞明)获NMPA批准上市,同年5月,来特莫韦注射液(商品名:普瑞明)获批。图源:药融云数据库据药融云数据库显示,南京正大天晴制药的来特莫韦注射液还处于审批状态。除此之外,CDE还受理了重庆希韦医药与重庆博腾制药联合申报的来特莫韦片剂和注射剂的上市申请。图源:药融云数据库据悉,默沙东的来特莫韦片未在国内获批之前,来特莫韦片(规格:240mg*28片/盒)代购价格为35840元/盒。2023年,来特莫韦片/注射液被纳入《国家基本医疗保险、工伤保险和生育保险药品目录(2022年)》,目前药品销售平台显示,来特莫韦片单盒价格(规格:240mg*28片/盒)仍超过4000元。
上市批准一致性评价并购
2024-02-20
·赛柏蓝
编者按:本文来自新康界,作者豫笠;赛柏蓝授权转载,编辑陈芋近日,国家药品监督管理局药品审评中心官网显示,山西德元堂药业按仿制4类提交的注射用硫酸艾沙康唑上市申请获受理。作为一款广谱的新型三唑类抗真菌药物,艾沙康唑主要用于18周岁及以上患者侵袭性曲霉菌病和侵袭性毛霉菌病的治疗。有研究显示,硫酸艾沙康唑疗效不亚于目前抗真菌药物的“头牌”伏立康唑,且不良反应较伏立康唑更低。01注射用硫酸艾沙康唑,同比增长8190%6家药企争国产首仿据悉,硫酸艾沙康唑胶囊在2021年12月国内获批上市;2022年6月注射用剂型紧接着在国内获批上市,并被纳入2022年医保乙类品种目录,随后迎来医院市场快速放量。中康开思系统数据显示,注射用硫酸艾沙康唑在2023年1-3季度全国等级医院销售达1.43亿元,3季度同比增长8190%,增长势头明显。注射用硫酸艾沙康唑全国等级医院销售情况此外,硫酸艾沙康唑胶囊在全国等级医院2023年1-3季度销售额在1730万元左右,同比增长194%。由于其研发成本较高,国内售价每盒上千元,这也在一定程度上限制了硫酸艾沙康唑胶囊快速放量。硫酸艾沙康唑胶囊全国等级医院销售情况截至目前,注射用硫酸艾沙康唑已有奥赛康药业、齐鲁制药、山东齐都药业、华北制药、重庆希韦医药、山西德元堂药业6家企业报产抢首仿。02我国抗真菌药市场有望达551亿元“TOP1”年销超30亿元目前抗真菌药物在临床上应用广泛,据预测,我国抗真菌药物市场在2025年有望达到551亿元。来源:共研网目前国内抗真菌药物市场以伏立康唑、泊沙康唑、氟康唑、伊曲康唑等三唑类抗真菌药物为主。其中伏立康唑是毫无疑问的“领跑选手”。数据显示,伏立康唑在2022年全国等级医院销售规模达31.88亿元,同比下滑8.4%;但2023年伏立康唑的销售有所复苏,前三季度全国等级医院销售规模已达27亿,同比增长超12%。伏立康唑全国等级医院销售情况此外,伏立康唑注射剂(注射用粉针剂)、口服常释剂型、口服液体剂均被纳入国家医保乙类目录;伏立康唑干混悬剂暂未进医保;伏立康唑片和注射用伏立康唑分别被列入第四批和第八批国家集采目录。END内容沟通:13810174402医药代表交流群扫描下方二维码加入银发经济市场机遇交流群扫描下方二维码加入左下角「关注账号」,右下角「在看」,防止失联
上市批准
100 项与 重庆希韦医药科技有限公司 相关的药物交易
登录后查看更多信息
100 项与 重庆希韦医药科技有限公司 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2024年11月19日管线快照
无数据报导
登录后保持更新
药物交易
使用我们的药物交易数据加速您的研究。
登录
或

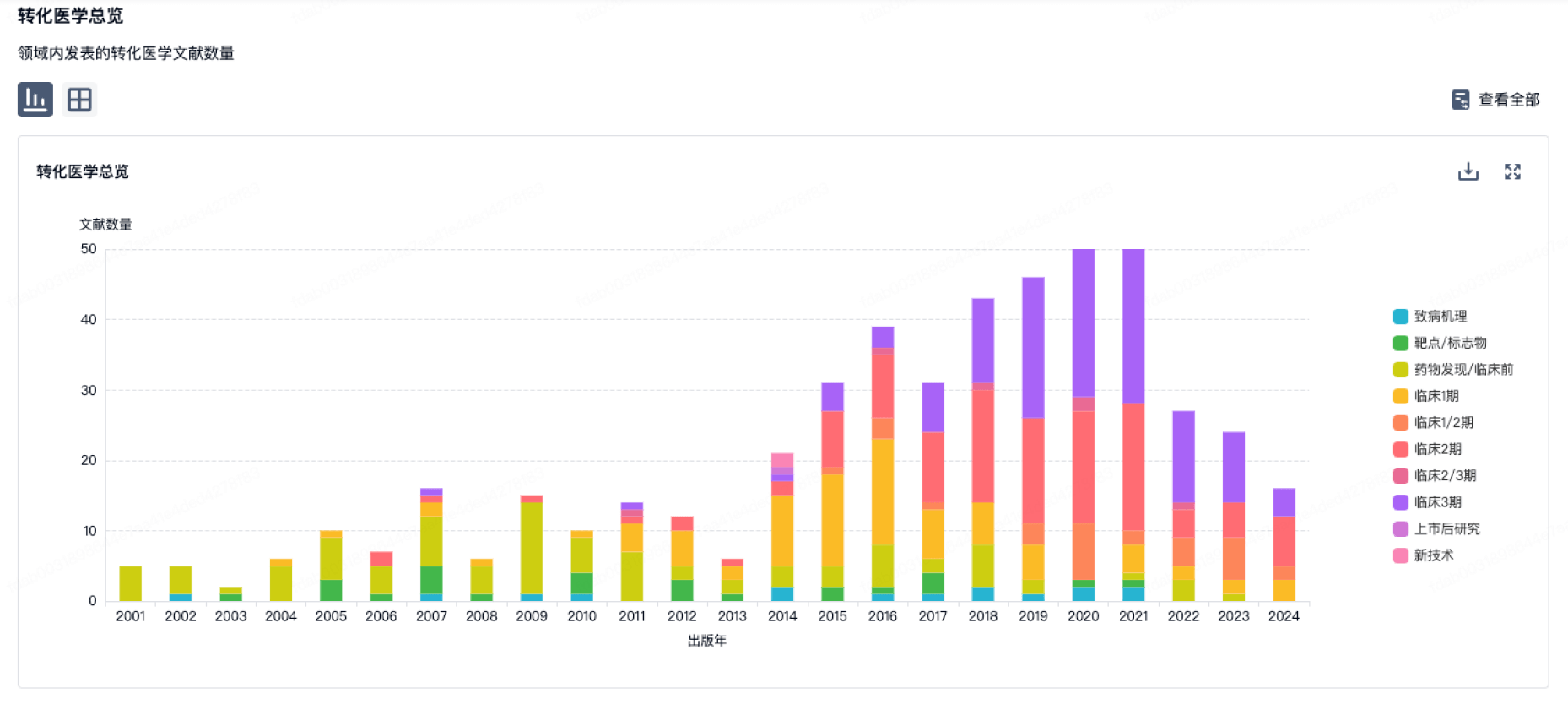
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
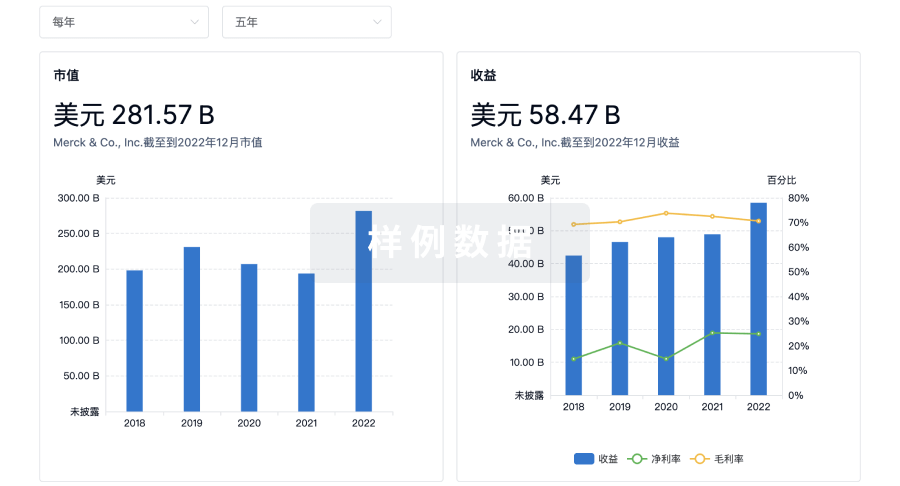
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或

投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或

融资
发掘融资趋势以验证和推进您的投资机会。
登录
或

标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用