100 项与 Harbin Kaiteng Biotechnology Co., Ltd. 相关的临床结果
0 项与 Harbin Kaiteng Biotechnology Co., Ltd. 相关的专利(医药)
声明:因水平有限,错误不可避免,或有些信息非最及时,欢迎留言指出。本文仅作医疗健康相关药物介绍,非治疗方案推荐(若涉及);本文不构成任何投资建议。
2024年10月18日,吉利德在与FDA协商后,宣布将自愿撤回Trodelvy用于治疗先前已接受过含铂化疗以及PD-1/PD-L1抗体治疗的局部晚期或转移性尿路上皮癌成年患者在美国的加速批准。
吉利德表示,该药物在乳腺癌方面的其他美国上市适应症仍然有效。
这一撤回并不令人意外。早在5月,吉利德就表示,TROPiCS-04研究作为膀胱癌条件性批准的确认性试验未能达到预期目标。这种TROP2靶向的抗体药物偶联物未能在延长接受过PD-1/L1治疗和化疗的膀胱癌患者的生命方面超过化疗。关于这一失败的详细数据尚未披露。
Trodelvy于2021年获得膀胱癌适应症的批准,基于II期单臂研究的数据,该药物在27.7%的患者中产生了肿瘤反应,其中5.4%的患者达到了完全反应。应答的中位持续时间为7.2个月。
膀胱癌是Trodelvy的一个相对较小的适应症,占该药销售额的不到10%,吉利德的首席财务官安德鲁·迪金森在公司八月举行的第二季度财报电话会议上表示。2023年Trodelvy(戈沙妥珠单抗,10.63亿美元,同比增长56%。然而,膀胱癌的失败是在另一个更重要的试验失败之后发生的,在与化疗对比的二线非小细胞肺癌(NSCLC)试验中,Trodelvy未能有所作为。在被称为EVOKE-01的试验中出现挫折后,吉利德确认了24亿美元的资产减值损失。Trodelvy曾是吉利德在2020年收购Immunomedics时的璀璨明珠,收购价高达210亿美元。
这两个试验的失败给Trodelvy蒙上了阴影,而它曾被视为吉利德实体肿瘤业务的基石。同时,这也削弱了Trodelvy的市场首发优势,因为两个竞争对手的合作正在推进各自的TROP2抗体药物结合体,分别是阿斯利康与第一三共的合作,以及默克与凯腾生物的合作,他们都在进行大规模的三期临床试验。
Trodelvy接下来的重要数据公布是EVOKE-03,该试验正在测试吉利德的药物与默克的PD-1抑制剂Keytruda在PD-L1高表达的非小细胞肺癌中的联用效果。该试验于2023年2月开始,目前预计的主要完成日期为2027年1月。
国内布局Trop2 ADC的企业主要有科伦博泰、君实生物、多禧生物、映恩生物、迈威生物、百利天恒和恒瑞医药等。
数据来源:
https://www.fiercepharma.com/pharma/gilead-withdraws-trodelvy-bladder-cancer-after-trial-flop
100 项与 Harbin Kaiteng Biotechnology Co., Ltd. 相关的药物交易
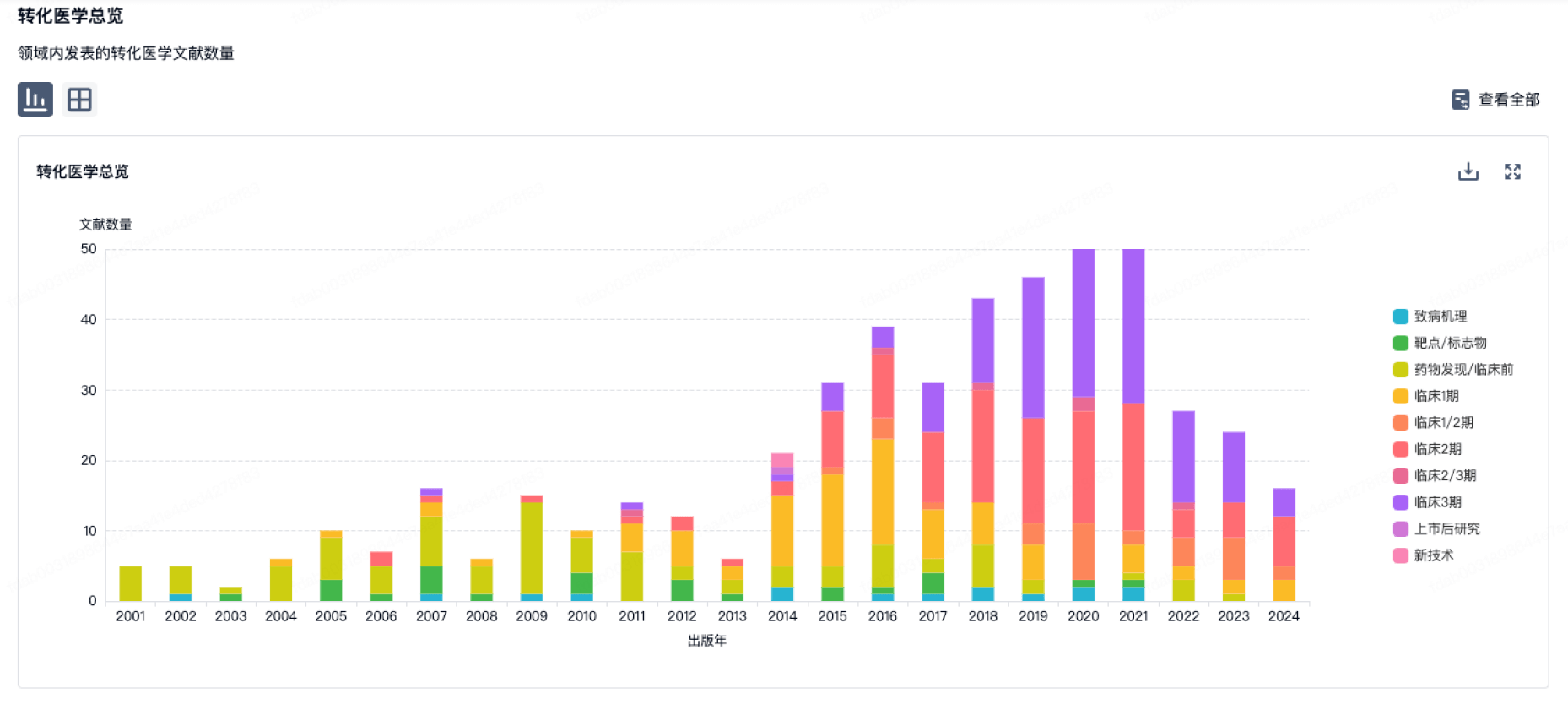
100 项与 Harbin Kaiteng Biotechnology Co., Ltd. 相关的转化医学