更新于:2024-11-01

RiboX Therapeutics, Inc.
私营公司|
2021|
中国上海市
私营公司|
2021|
中国上海市
更新于:2024-11-01
概览
关联
100 项与 RiboX Therapeutics, Inc. 相关的临床结果
登录后查看更多信息
0 项与 RiboX Therapeutics, Inc. 相关的专利(医药)
登录后查看更多信息
6
项与 RiboX Therapeutics, Inc. 相关的新闻(医药)2024-10-28
药械追踪
No.1 / RiboX环形RNA药物RXRG001在美获批临床,治疗放射性口干症
2024年10月26日,转录本(上海)生物科技有限公司(RiboX Therapeutics,简称“RiboX”)宣布, RXRG001治疗放射性口干症的新药临床试验申请(IND)已获得美国食品药品监督管理局(FDA)批准,即将在美国开展I/IIa期临床试验SPRINX-1。
此次IND获批后,RXRG001成为全球首个获FDA许可进入临床试验的circRNA疗法,同时也是目前全球唯一获批用于放射性口干症临床研究的circRNA药物。
->点击文末阅读原文,解锁完整双语新闻
No.2/ 阿斯利康诺雷得10.8mg剂型乳腺癌适应证在华获批
2024年10月25日,阿斯利康宣布,旗下肿瘤药物诺雷得(英文商品名:Zoladex,通用名:醋酸戈舍瑞林缓释植入剂)10.8mg剂型获中国国家药品监督管理局(NMPA)批准,适用于可用激素治疗的绝经前期及围绝经期妇女的乳腺癌。
醋酸戈舍瑞林是一种合成的促性腺激素释放激素类似物(GnRHa),长期使用可抑制脑垂体促性腺激素的分泌,从而降低女性血清中的雌二醇(E2)水平和抑制雌激素敏感的肿瘤生长。
本次10.8mg剂型在中国获批乳腺癌适应证,有望为可用激素治疗的绝经前期及围绝经期乳腺癌患者带来更好的生存获益。
->点击文末阅读原文,解锁完整双语新闻
No.3 / 百济神州PD-1单抗百泽安在美国正式上市
2024年10月28日,百济神州宣布,自研PD-1单抗替雷利珠单抗(英文商品名:TEVIMBRA,中文商品名:百泽安)在美国开出了首张处方,正式进入美国市场。
替雷利珠单抗于2024年3月获得美国食品药品监督管理局(FDA)批准,用于治疗既往接受过系统化疗(不含PD-1/L1抑制剂)后不可切除或转移性食管鳞状细胞癌(ESCC)的成人患者。
此次正式上市,替雷利珠单抗以低于获批用于该适应证的其他PD-1疗法10%的定价惠及这一患者群体。
->点击文末阅读原文,解锁完整双语新闻
No.4/ 全球首创!万泰生物/厦门大学EB病毒BNLF2b抗体检测试剂盒在华获批
2024年10月28日,万泰生物宣布,其与厦门大学联合研制的EB病毒BNLF2b抗体(简称P85-Ab)检测试剂盒(磁微粒化学发光法)获得国家药品监督管理局批准上市(国械注准20243402134)。
此前,厦门大学夏宁邵团队全球首次发现了全新的鼻咽癌血清学标志物——针对BNLF2b基因编码的假定蛋白的总抗体(P85-Ab)。
作为鼻咽癌筛查的新型生物标志物,P85-Ab拥有更高的灵敏度、特异性以及阳性预测值,且与现有方案存在良好互补性,有助于提高鼻咽癌筛查的效能。
->点击文末阅读原文,解锁完整双语新闻
企业动态
No.1 / GSK在美最大单笔投资,注资宾夕法尼亚工厂8亿美元
2024年10月24日,葛兰素史克(GSK)向美国宾夕法尼亚玛丽埃塔工厂投资8亿美元,用于配备用于药物和疫苗生产的最先进的设施,并创造200多个新工作岗位。
新的多功能设施将满足不断增长的无菌疫苗和药物需求,此外,GSK 将在该工厂建立一个新的疫苗原料药设施,专门用于生产基于公司新型多抗原平台系统(MAPS)技术产品,用于后续提交上市审批。新设施的建设预计将于今年年底开始。
原料药设施预计将于2027年底投入运营,药品设施将于2028年底投入运营。从2017年起,GSK已陆续在美国工厂投资13亿美元。
->点击文末阅读原文,解锁完整双语新闻
No.2 / BMS退还礼新医药CLDN18.2 ADC权益
近日,根据礼新医药官网公开信息,BMS已将靶向CLDN18.2的抗体偶联药物(ADC)LM-302相关权益退还礼新医药,礼新医药现重新拥有LM-302的全球权益。
礼新医药曾于2022年5月与美国肿瘤精准疗法公司Turning Point达成授权合作,将LM-302在全球除大中华区与韩国以外国家及地区的独家开发和商业化权益授予Turning Point;交易对价包括2500万美元首付款和最高达10亿美元的里程碑付款。BMS通过收购Turning Point获得LM-302相关权益。
->点击文末阅读原文,解锁完整双语新闻
全球医疗情报领导者
解锁隐藏在数据中的商业潜力
关于 G B I
”
自从2002年成立以来,GBI始终以技术为驱动,为药企、器械及行业相关服务商提供贯穿生命周期的全球药品市场竞争数据、全球行业资讯、HCPs洞察、全国医疗器械数据等商业信息与洞察,助力企业在进行战略布局和决策时,脱颖而出。历经20余年的深耕细作GBI已成为95%以上跨国药企、国内头部药企、咨询与投资机构等医疗圈灯塔用户值得信赖的长期合作伙伴。
联系我们
投稿 | 发稿 | 媒体合作
▶ zhangxinyue13@baidu.com
数据库 | 咨询服务 | 资讯追踪
▶ 点击左下“阅读原文”完成表单填写
点击阅读原文,解锁完整双语新闻
上市批准临床申请诊断试剂
2024-10-27
·研发客
上海、美国新泽西州普林斯顿,2024年10月26日——转录本(上海)生物科技有限公司(RiboX Therapeutics,简称“RiboX”),一家专注于发现和开发完全工程化的环形 RNA疗法的生物技术公司,近日宣布其自主研发的针对放射性口干症的RXRG001获得美国食品药品监督管理局 (FDA)的新药临床试验申请(IND)批准,即将在美国开展I/IIa期临床试验SPRINX-1。
RXRG001不仅是全球首个获FDA许可进入临床试验的环形RNA疗法,同时也是全球唯一获批用于放射性口干症临床研究的环形RNA药物。这一重大进展标志着环形RNA 药物正式进入临床开发阶段。
头颈部肿瘤发病率持续上升,现已成为全球第六大常见恶性肿瘤。放射治疗是头颈部肿瘤的主要治疗方法,但其通常会导致患者唾液腺受损,唾液分泌显著减少,进而导致口干、咀嚼和吞咽困难以及口腔健康受损,严重影响患者长期的生活质量。目前临床上缺乏有效的治疗方法,在过去20年尚无新药获批用于治疗放射性口干症,仍存在巨大的未被满足的医疗需求。
作为新一代RNA疗法,环形RNA展现出高蛋白表达效率、低免疫原性以及良好的生产和工艺稳定性等多个方面的显著优势。RXRG001是RiboX自主研发的由脂质纳米颗粒(LNP)包裹的环形RNA药物,通过LNP递送环形RNA在唾液腺中表达水通道蛋白AQP1增强透水性,从而提高进入口腔中的唾液流量及流速,改善患者口干症状。非临床研究表明,RXRG001 展现了持久疗效同时具备良好的耐受性和安全性。单次给药后可显著增加唾液流量,并且效果可持续长达四周。
RiboX首席医学官徐一甄博士表示,“放射性口干症是头颈癌患者终身面临的健康问题。尽管目前放射治疗可以提高患者的生存率,但其对唾液腺的损害导致许多癌症患者的生活质量明显下降。RXRG001 有望为放射性口干症患者提供一种有效且持久的治疗选择。我们对即将开展的临床试验充满信心,期待进一步评估其临床疗效和安全性。”
RiboX联合创始人兼首席执行官张巍怡博士表示,“RXRG001获得美国FDA临床试验许可,是对RiboX在环形RNA领域的创新能力、技术水平和全球竞争力的高度认可。RiboX将持续发挥环形RNA在治疗应用方面的独特优势,有力推进RXRG001的临床开发,早日为全球患者带来更多创新的治疗方案。”
关于RiboX Therapeutics
RiboX Therapeutics于2021年9月由陈玲玲博士、Dan Peer博士和张巍怡博士联合创立,致力于发现和开发完全工程化的环形RNA 疗法。公司总部及全球研发中心位于中国上海,并在美国新泽西州普林斯顿和以色列雷霍沃特设有分支机构。环形RNA作为新一代RNA疗法,是一种共价闭合的单链 RNA 结构。与线性mRNA 相比,环形RNA具有更好的稳定性和更低的免疫原性,可精准调节蛋白表达,能够克服现有mRNA 疗法的局限性,充分发挥 RNA 药物的治疗潜力。
RiboX以创新为驱动,在环形RNA分子设计及优化、LNP递送载体以及工艺放大生产等关键领域实现了全面突破,为环形RNA药物的临床开发提供了有力支持。产品管线涵盖多个治疗领域,包括放射性口干症、单基因遗传病,自身免疫病以及疫苗等。RiboX致力于开拓及引领新一代核酸药物的创新研究,为全球患者带来生命曙光。
更多信息,请访问网站:www.riboxtx.com
商务合作,请联系 bd@ribox-tx.com
临床申请放射疗法
2024-10-27
·医药观澜
▎药明康德内容团队编辑
转录本(上海)生物科技有限公司(RiboX Therapeutics,简称RiboX)近日宣布其针对放射性口干症的在研疗法RXRG001的IND申请获得美国FDA的许可,即将在美国开展1/2a期临床试验SPRINX-1。新闻稿指出,RXRG001是全球首个获FDA许可进入临床试验的环形RNA疗法,同时也是全球首个获批用于放射性口干症临床研究的环形RNA药物。这一重大进展标志着环形RNA药物正式进入临床开发阶段。
头颈部肿瘤发病率持续上升,现已成为全球第六大常见恶性肿瘤。放射治疗是头颈部肿瘤的主要治疗方法,但其通常会导致患者唾液腺受损,唾液分泌显著减少,进而导致口干、咀嚼和吞咽困难以及口腔健康受损,严重影响患者长期的生活质量。目前临床上缺乏有效的治疗方法,在过去20年尚无新药获批用于治疗放射性口干症,仍存在巨大的未被满足的医疗需求。
作为新一代RNA疗法,环形RNA展现出高蛋白表达效率、低免疫原性以及良好的生产和工艺稳定性等多个方面的显著优势。RXRG001是RiboX自主研发的由脂质纳米颗粒(LNP)包裹的环形RNA药物,通过LNP递送环形RNA在唾液腺中表达水通道蛋白AQP1增强透水性,从而提高进入口腔中的唾液流量及流速,改善患者口干症状。临床前研究显示,RXRG001展现了持久疗效同时具备良好的耐受性和安全性。单次给药后可显著增加唾液流量,并且效果可持续长达四周。
RiboX首席医学官徐一甄博士表示:"放射性口干症是头颈癌患者终身面临的健康问题。尽管目前放射治疗可以提高患者的生存率,但其对唾液腺的损害导致许多癌症患者的生活质量明显下降。RXRG001有望为放射性口干症患者提供一种有效且持久的治疗选择。我们对即将开展的临床试验充满信心,期待进一步评估其临床疗效和安全性。"
参考资料:
[1]RiboX Therapeutics首款环形RNA药物RXRG001临床IND获美国FDA批准. Retrieved Oct 26, 2024, from https://www.prnasia.com/story/archive/4540322_ZH40322_1?utm_source=cleartime-customer&utm_medium=email
本文由药明康德内容团队根据公开资料整理编辑,欢迎个人转发至朋友圈。转发授权及其他合作需求,请联系wuxi_media@wuxiapptec.com。
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
临床申请放射疗法
100 项与 RiboX Therapeutics, Inc. 相关的药物交易
登录后查看更多信息
100 项与 RiboX Therapeutics, Inc. 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2024年11月18日管线快照
无数据报导
登录后保持更新
药物交易
使用我们的药物交易数据加速您的研究。
登录
或

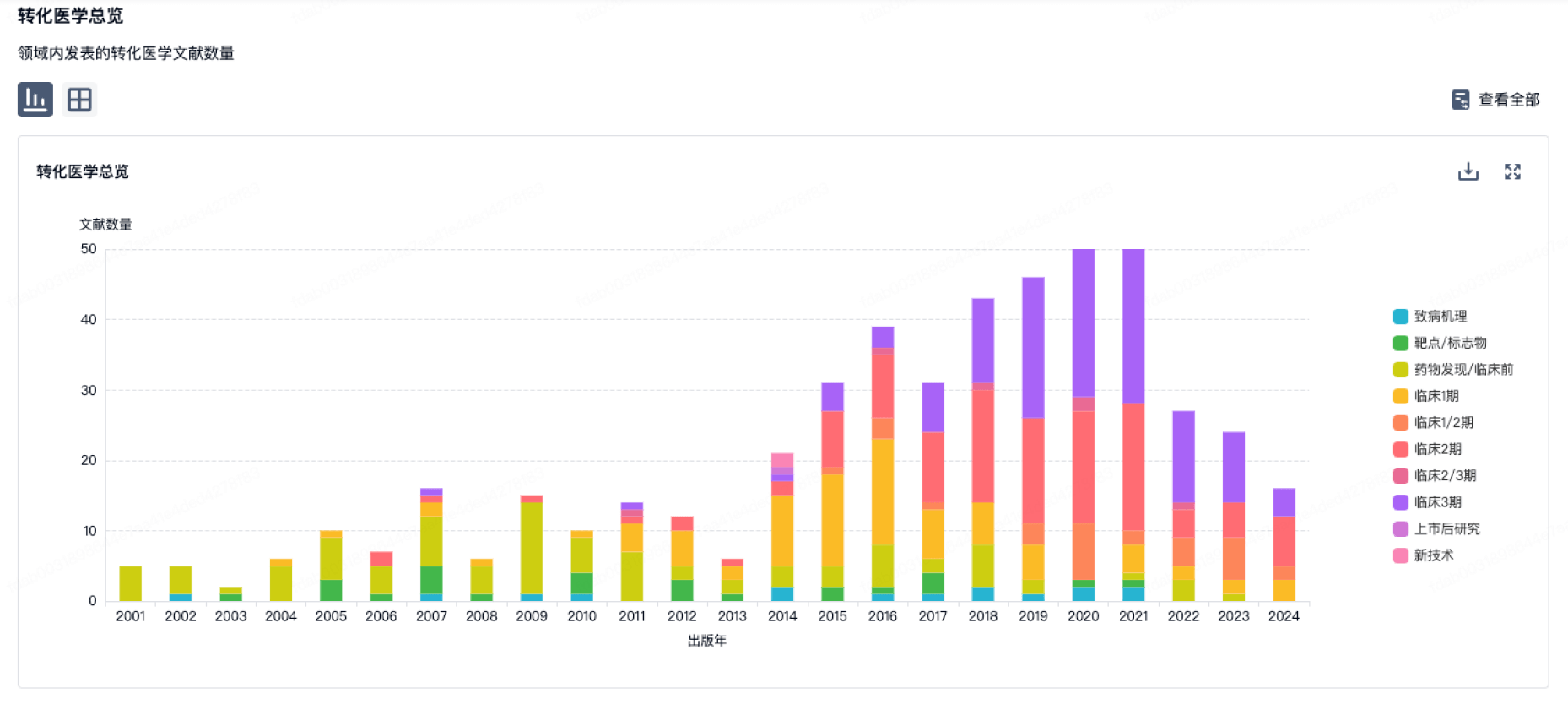
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
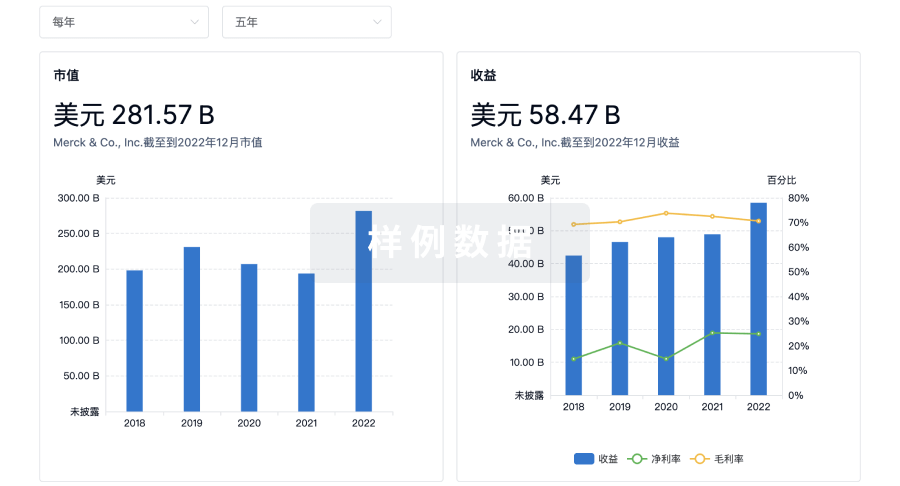
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或

投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或

融资
发掘融资趋势以验证和推进您的投资机会。
登录
或

标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用