预约演示
更新于:2025-08-20
BioTroy Therapeutics
更新于:2025-08-20
概览
标签
肿瘤
呼吸系统疾病
血液及淋巴系统疾病
单克隆抗体
抗体
疾病领域得分
一眼洞穿机构专注的疾病领域
暂无数据
技术平台
公司药物应用最多的技术
暂无数据
靶点
公司最常开发的靶点
暂无数据
| 排名前五的药物类型 | 数量 |
|---|---|
| 单克隆抗体 | 3 |
| 未知 | 1 |
| 抗体 | 1 |
关联
5
项与 上海柏全生物科技有限公司 相关的药物靶点 |
作用机制 ITPRIPL1 抑制剂 |
在研机构 |
原研机构 |
非在研适应症- |
最高研发阶段临床1/2期 |
首次获批国家/地区- |
首次获批日期- |
靶点 |
作用机制 SEMG2拮抗剂 |
在研机构 |
原研机构 |
在研适应症 |
非在研适应症- |
最高研发阶段临床前 |
首次获批国家/地区- |
首次获批日期- |
CN116688125
专利挖掘靶点 |
作用机制- |
在研机构 |
原研机构 |
在研适应症 |
非在研适应症- |
最高研发阶段药物发现 |
首次获批国家/地区- |
首次获批日期- |
5
项与 上海柏全生物科技有限公司 相关的临床试验NCT07107178
A Phase Ib Study of the Safety, Tolerability and Efficacy of BT02 for the Treatment of Patients With Advanced Malignant Melanoma
The goal of this clinical trial is to learn about the safety, tolerability and preliminary effectiveness of a treatment for patients with advanced melanoma,regardless of gender, aged between 18 and 75 years (inclusive).
Participants will receive the investigational product intravenously every two or three weeks. The treatment will continue for a maximum of two years for those who do not show signs of disease progression or experience intolerable side effects.
Participants will receive the investigational product intravenously every two or three weeks. The treatment will continue for a maximum of two years for those who do not show signs of disease progression or experience intolerable side effects.
开始日期2025-08-08 |
申办/合作机构 |
NCT07110363
An Open-label Phase Ib Study on the Safety, Tolerability, and Efficacy of BT02 in Treating Patients With Advanced Lung Cancer
The goal of this clinical trial is to assess whether an investigational treatment is safe and tolerable for patients with advanced lung cancer, and to get a preliminary idea of its effectiveness. Participants of all genders, aged between 18 and 75(inclusive), are eligible to join. These patients will receive the investigational drug intravenously every two weeks. If their condition doesn't worsen and they don't experience unbearable side effects, they can continue the treatment for up to two years.
开始日期2025-08-01 |
申办/合作机构 |
NCT07107204
A Multicenter, Open-label, Single-arm Phase Ib/IIa Clinical Study to Evaluate the Safety and Efficacy of BT02 in Patients With Relapsed or Refractory Hematologic Malignancies
The goal of this clinical trial is to learn about the safety, tolerability and preliminary effectiveness of a treatment for patients with relapsed or refractory hematologic malignancies, regardless of gender, aged between 18(inclusive) and 70 years .
Participants will receive the investigational product intravenously every two or three weeks. The treatment will continue for a maximum of two years for those who do not show signs of disease progression or experience intolerable side effects.
Participants will receive the investigational product intravenously every two or three weeks. The treatment will continue for a maximum of two years for those who do not show signs of disease progression or experience intolerable side effects.
开始日期2025-08-01 |
申办/合作机构 |
100 项与 上海柏全生物科技有限公司 相关的临床结果
登录后查看更多信息
0 项与 上海柏全生物科技有限公司 相关的专利(医药)
登录后查看更多信息
57
项与 上海柏全生物科技有限公司 相关的新闻(医药)2025-07-24
·药时代
全文共2874字,共0图预计阅读时间:8分钟继科济药业公布其在研的Claudin18.2自体CAR-T疗法——舒瑞基奥仑赛的新药上市申请已获NMPA正式受理的喜讯后,实体瘤CAR-T再度引发市场关注。当地时间2025年7月23日,一家初创的实体瘤CAR-T公司——Dispatch Bio(Dispatch)宣布获得2.16亿美元A轮融资。从融资规模来看,2.16亿美元的A轮融资在如今的大环境下是鲜少的。就国内最近情况来看,A轮融资金额数值普遍在数千万元。比较高的,比如柏全生物、凯米生物也只到2亿元左右。再从Biospace提到的国外初创公司(比如Draig Therapeutics和Granite Bio)情况来看,A轮融资金额也普遍徘徊在1亿美元左右。放在CGT领域,这2.16亿美元更是难得。以同类的实体瘤CAR-T海外公司的融资情况进行类比。2024年9月,实体瘤CAR-T明星企业——Arsenal Biosciences的C轮融资也不过3.25 亿美元。此前,Arsenal的A轮融资仅8500万美元。值得探讨的是,在资本寒冬背景下,此次大额融资叠加全球首款实体瘤CAR-T疗法即将上市的预期,是否预示着该赛道拐点已经到来?关于Dispatch Bio分析认为,投资人看上Dispatch主要有两大原因:1)创始团队“咖位”大;2)技术平台有优势。Dispatch于2022年由美国知名VC Arch Venture Partners和帕克癌症免疫治疗研究所(PICI)合作成立。此本轮融资的投资者除Arch和PICI外,还有BMS、宾夕法尼亚大学、斯坦福大学和亚历山大风险投资公司。Dispatch的核心技术平台——Flare技术源自“CAR-T之父”Carl June、斯坦福大学Chris Garcia教授、加州大学旧金山分校的Kole Roybal教授,以及斯隆-凯特琳癌症中心免疫肿瘤学新任主席Andy Minn实验室的突破性技术的融合而建立。基于Flare技术的CAR-T疗法与我们所熟知的CAR-T疗法的主要区别在于:不依赖肿瘤天然表达的有限抗原。传统CAR-T疗法起作用的核心逻辑是,让经改造的T细胞去识别并清除带有特定靶标的肿瘤细胞。目前,全球共获批上市12款CAR-T疗法,其中8款靶向CD 19,另4款靶向BCMA。这两个靶点的共同特点是,均在特定的血液系统恶性肿瘤表面高表达,但在正常组织中几乎不表达。这反映了传统CAR-T设计理念的一个问题,即对靶点本身具有较高要求。这在很大程度上限制了CAR-T疗法在肿瘤领域的”开疆扩土”。相比之下,Flare技术则是先通过基因工程改造的病毒给肿瘤细胞安装上一个特定的“信号弹”——抗原Flare,之后让经改造的T细胞去识别带有“Flare”标识的肿瘤细胞,进而达到清除目的。此外,Dispatch信息显示,抗原Flare的载体病毒还能递送炎症细胞因子和趋化因子,这可以帮助摧毁肿瘤周围的环境防御。基于这种“没有靶标就创造靶标”,“靶标难识别、易脱靶就人工创造容易识别靶标”的思路,经Flare技术加持的下一代CAR-T疗法或许能使CAR-T赛道突破现有瓶颈。Flare:实体瘤治愈的利器?Dispatch成立的宗旨是希望有朝一日所有癌症患者都能得到治愈。这是一个宏伟的愿景。癌症,根据生物学特性和发生部位,可被笼统的分为实体瘤和血液肿瘤。最早出现的肿瘤治疗手段的是手术治疗,就是简单的肿块/瘤子切除。然后是放疗,即放射治疗,主要是通过大量辐射杀死癌细胞。全球首个抗肿瘤药物的上市要追溯到20世纪40年代。1949年,氮芥获FDA批准上市,成为历史上第一个有记载的抗肿瘤化疗药物。后随生物技术发展,包括阿霉素、顺铂、紫杉醇、吉西他滨等在内的化疗药物陆续获批上市。科研界在上世纪后半叶取得的一系列突破促生了肿瘤靶向治疗药物。后来CTLA-4、PD-1等免疫检查点的陆续发现又为肿瘤患者群体带来了突破性的免疫检查点抑制剂。现如今的肿瘤治疗方式呈现手术、放化疗、靶向治疗、免疫治疗、细胞基因疗法等多种治疗方式单药/联合治疗的多元格局。其中,CAR-T细胞疗法凭借其突破性疗效,已成为肿瘤免疫治疗领域最受瞩目的技术方向之一。在一些科普文章中,CAR-T疗法常与“肿瘤治愈”相关联。这倒不是什么夸张说法,因为目前确实有真实治愈案例——白血病患者艾米莉。艾米莉于7岁时接受CAR-T治疗,到2025年已经无癌生存13年。CAR-T疗法治愈肿瘤的核心在于其独特的“精准强化+免疫突破”双作用模式。通过人工嵌入特定”CAR"基因片段,改造后的T细胞一方面可直接识别肿瘤表面抗原(如CD19),另一方面体外扩增的CAR-T细胞回输后数量可达10^9级别,形成“免疫风暴”,并在患者体内长期存活。这种独特优势是ADC和免疫检查点抑制剂所不能的,是深层的机制差异。科济药业的舒瑞基奥仑赛目前显示出的疗效离治愈仍有差距。据舒瑞基奥仑赛II期确证性CT041-ST-01研究结果,相较标准治疗方案,舒瑞基奥仑赛可实现mPFS显著延长,至3.25个月。mOS也显示出获益趋势,至7.92个月。不过据科济早期报道,在一项研究中,接受局部治疗和另一款实体瘤CAR-T疗法联合治疗后,两名患者在长期随访(从2015年到2023年)中均保持了无瘤状态。从机制上讲,如果Flare技术平台能同时解决传统CAR-T抗原依赖及肿瘤微环境防御两大难题,的确让实体瘤的治愈愿景离实现又近了一步。参考资料:1.https://www.biopharmadive.com/news/disptach-bio-universal-cancer-immunotherapy-solid-tumors/753743/ 2.https://www.zhihu.com/tardis/zm/art/3362446693.人类肿瘤药物治疗史上的三次革命:从化疗药物到靶向药物、免疫治疗药物——中国医保肿瘤用药发展史-中国医疗保险杂志社4.https://www.hangyan.co/charts/35931998528146000855.各公司官网6.其他公开资料图片来源:即梦AI股价暴涨400%!IBD领域迎来新秀2025-07-23多款药物惨遭FDA拒批!居然因为...2025-07-23下一代靶向TMPRSS6的siRNA疗法寻找合作伙伴 | 药时代BD项目2025-07-22版权声明/免责声明本文为原创文章。本文仅作信息交流之目的,不提供任何商用、医用、投资用建议。文中图片、视频、字体、音乐等素材或为药时代购买的授权正版作品,或来自微信公共图片库,或取自公司官网/网络,部分素材根据CC0协议使用,版权归拥有者,药时代尽力注明来源。如有任何问题,请与我们联系。衷心感谢!药时代官方网站:www.drugtimes.cn联系方式:电话:13651980212微信:27674131邮箱:contact@drugtimes.cn点击这里,查看更多精彩!
2025-07-23
·创鉴汇
2025年第二季度,上海创新药领域展现出强劲活力。据公开披露数据,本季度上海至少有18家创新药公司完成融资,已披露融资总额超26亿元。上海凭借其成熟的生物医药产业集群、浦东张江等核心区域的研发高地优势,以及活跃的资本支持,持续引领技术创新与产业升级。本季度融资亮点显著:大额融资占比高,早期融资显著活跃:在披露金额的融资事件中,6起金额超亿元,占比60%。其中,潜在最高融资额来自映恩生物完成的2.1亿美元IPO。此外,超七成融资事件为B轮及以前的早期融资,显示上海创新药源头创新活力充沛,资本积极布局前沿技术。抗体药物受到关注:6家获融资公司布局抗体药物管线,包括成功IPO的映恩生物、获超2亿元融资柏全生物、天辰生物等。其中,以双特异性抗体、抗体偶联药物为最大热门。细胞与基因疗法(CGT)向通用型解决方案迭代:8家获融资公司推进CGT疗法创新,聚焦平台技术升级。如天泽云泰开发ViCas CRISPR平台拟治疗遗传性退行性疾病等;纽欧申医药设计开发新型腺相关病毒(AAV)衣壳突破血脑屏障;渤因生物剑指基因治疗不可重复给药痛点;智新浩正则开发通用型再生胰岛技术。各公司关注通过载体工程化改造提升治疗持久性,反映平台技术从单次治疗向可持续性方案演进。映恩生物:癌症抗体偶联药物研发公司4月15日,映恩生物宣布在香港联合交易所主板正式挂牌上市。映恩生物此次IPO招股引入15名基石投资者,包括BioNTech、LAV Star、Lake Bleu Prime、Lake Bleu Innovation、TruMed、富国香港、富国基金、易方达基金、易方达香港、汇添富基金、盘京基金、MY Asian、EMHCP、WWHCP、苏州苏创,共认购6500万美元(约5.05亿港元)。公司原有股东包括礼来亚洲基金、楹联健康产业基金、中金阿斯利康、华盖资本、松禾资本、天士力国际资本、汉康资本等。映恩生物成立于2019年,致力于为癌症和自身免疫性疾病等患者研发创新ADC疗法。据招股书介绍,该公司已建立由12款自主研发的ADC候选药物组成的管线,其中包括两款在研核心产品,即HER2靶向ADC及B7-H3靶向ADC。此外其还有5款其他临床阶段ADC产品,多款其他临床前ADC,以及2款双特异性ADC(BsADC)产品。柏全生物:肿瘤免疫药物研发公司6月17日,柏全生物(BioTroy Therapeutics)宣布完成超两亿元人民币A轮融资。本轮融资由龙磐投资领投,上海科创基金、浦东创投跟投,原有股东上实资本、凯风创投继续追加投资。新闻稿表示,此次融资将重点用于加速柏全生物核心产品——CD3L1靶点抗肿瘤药物的注册临床试验进程,同步推进多个全新靶点肿瘤治疗管线的研发布局,进一步夯实柏全生物在肿瘤免疫治疗领域的源头创新能力。目前,该公司前已有3个具潜力的新靶点进入临床前研究。柏全生物是一家处于临床阶段的创新驱动型药物研发企业。该公司专注于突破PD-1/L1耐药、冷肿瘤免疫微环境重塑等全球性临床治疗难题。凭借优秀的源头创新能力,该公司研发的CD3L1免疫治疗靶点相关研究成果荣登国际期刊CELL,基于该靶点开发的抗肿瘤药物已同步获得美国FDA和中国NMPA的临床试验许可,目前正在开展针对多种实体瘤与血液肿瘤的1期多中心临床研究。天辰生物:自身免疫性疾病抗体研发公司6月3日,天辰生物宣布完成超2亿元C轮融资。本轮融资由弘晖基金、原有股东方启明创投共同领投,临创蓝湾基金、贝达基金、真脉基金跟投,原有股东方三奕资本、山证创新等持续加码。本轮融资资金将重点用于核心管线——新一代抗IgE抗体LP-003的3期临床和后续的商业化准备,以及补体双功能抗体LP-005的多个适应症的2期临床开发,进一步巩固天辰生物在过敏与补体疾病领域的创新优势。LP-003作为在研抗IgE抗体,已进入过敏性鼻炎的3期临床,预计2026年初提交产品上市申请;第二个适应症慢性荨麻疹的3期临床也将于2026年启动;除此之外过敏性哮喘、食物过敏等适应症的2期临床也在推进中。LP-005为潜在“first-in-class”、可同时抑制补体三条通路的双功能抗体融合蛋白,在阵发性睡眠性血红蛋白尿症(PNH)的2期临床中已展现显著疗效。2025年将启动针对补体介导肾病(IgA, C3G等肾病)以及其他疾病的临床研究。思璞锐:小分子抗肿瘤药物研发公司6月5日,思璞锐(SciBrunch Therapeutics)宣布完成超2亿元人民币天使轮融资。本轮融资由博远资本和汉康资本联合领投,骊宸投资和LongRiver江远投资参与跟投。所募资金将主要用于公司现有管线的临床前和早期临床开发。思璞锐是一家专注于小分子抗肿瘤药物迭代创新的研发型生物技术公司,由资深连续创业者胡滔博士携手药物化学专家张杨博士共同创立。该公司旨在以新视角挖掘临床验证靶点,前瞻性地进行差异化的产品性能设计,打造具有潜力的产品管线。纽欧申医药:精神和神经系统疾病药物研发公司4月18日,纽欧申医药宣布完成数千万美元的A轮融资。本轮融资由上实资本旗下的上海生物医药基金领投,现有股东龙磐投资继续支持,谢诺投资等多家机构共同参与。本轮融资将用于推进纽欧申医药核心研发项目的临床开发,包括已完成1期临床试验的针对癫痫、情感障碍和疼痛等多个适应症的NS-041(选择性KCNQ2/3通道激动剂)项目和针对精神分裂症以及阿尔茨海默病等老年痴呆伴随的激越症状的NS-136(M4毒蕈碱型乙酰胆碱受体正向变构调节剂)项目,以及推进针对难治性抑郁症、阿尔茨海默病和帕金森病等多个项目的IND开发。纽欧申医药是一家临床阶段的生物技术公司,专注于开发针对神经和精神类疾病的创新疗法。该公司创新药物管线已经迎来多项进展,核心产品NS-041在近期完成1期临床试验,已推进至局灶性癫痫的2期概念验证研究 (Proof-of-Concept) 阶段,并同步启动适应症拓展,针对情感障碍和神经病理性疼痛等重大未满足临床需求领域。读者们请星标⭐创鉴汇,第一时间收到推送免责声明:本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。版权说明:欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转发/复制至其他平台。转发授权请在「创鉴汇」微信公众号留言联系我们。更多数据内容推荐点击“在看”,分享创鉴汇健康新动态
IPO抗体药物偶联物基因疗法申请上市
2025-07-10
·药研发
2025年1-6月,中国医药行业共完成134起融资事件,涉及131家企业,披露金额的融资总额达41亿美元(约294亿元人民币)。其中:69%事件披露金额,平均单笔融资超3000万美元;IPO及后续融资贡献近六成资金,恒瑞医药、映恩生物等7家上市企业募资总额超20亿美元;战略投资占比显著提升,36%的融资发生在IPO前阶段,产业资本加速布局早期项目。一、融资轮次分布 上市后融资:巨头持续加码共16起,以增发为主,头部企业吸金能力突出:君实生物(103.9亿港元)、荣昌生物(7.96亿港元)通过增发扩充研发管线;科伦博泰(2.5亿美元)、和铂医药(1.053亿美元)获跨国药企战略投资。 IPO市场:港股主导,回暖信号明显恒瑞医药(97.47亿港元)成为年内最大规模IPO;映恩生物(2.11亿美元)、维昇药业(6.723亿港元)展现ADC与罕见病赛道热度。 早期融资:技术驱动型项目受青睐战略投资占比最高(48起),如呈元科技(7500万美元)、迈科康生物(2亿元);A轮以前项目融资额攀升,柏全生物(超2亿元)、泽安生物医药(4000万美元)等10家企业单笔融资破亿。二、细分赛道与投资机构动态 技术领域分布小分子药物(53家)、单抗(27家)、ADC(14家)为最活跃领域;基因治疗(愈方生物、予路乾行)、多肽药物(星联肽生物)等新兴技术增速显著。 机构投资图谱元生创投最活跃(投资5家),覆盖小分子、基因编辑等领域;博远资本、启明创投各投资4家,聚焦肿瘤免疫和代谢疾病;产业资本深度参与:阿斯利康、复星医药等通过战略投资绑定创新管线。三、典型案例分析 高额融资项目柏全生物(A轮超2亿元):全球首个CD3L1靶点研发企业;泽安生物医药(A+轮4000万美元):新一代免疫疗法开拓者;阳光安津(Pre-A轮超亿元):疼痛治疗领域钠离子通道靶点先锋。 IPO标杆企业恒瑞医药:港股上市募资近百亿港元,加速国际化布局;映恩生物:获BioNTech基石投资,ADC技术平台受全球认可。四、趋势与展望IPO通道逐步放开:6月单月11家药企递交港交所申请,科创板第五套标准重启;License-out持续活跃:上半年跨境授权合作达75项,ADC、双抗成主力;早期投资专业化:机构更关注“First-in-Class”技术,如基因编辑、RNA疗法等。尽管全球生物医药融资环境承压,中国创新药企通过技术突破与资本协作展现韧性。随着政策利好与国际化合作深化,下半年市场有望进一步复苏。- The End -
抗体药物偶联物IPO免疫疗法引进/卖出
100 项与 上海柏全生物科技有限公司 相关的药物交易
登录后查看更多信息
100 项与 上海柏全生物科技有限公司 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2025年08月25日管线快照
管线布局中药物为当前组织机构及其子机构作为药物机构进行统计,早期临床1期并入临床1期,临床1/2期并入临床2期,临床2/3期并入临床3期
药物发现
3
1
临床前
临床2期
1
登录后查看更多信息
当前项目
| 药物(靶点) | 适应症 | 全球最高研发状态 |
|---|---|---|
BT02 ( ITPRIPL1 ) | 晚期恶性实体瘤 更多 | 临床1/2期 |
BT01 ( SEMG2 ) | 实体瘤 更多 | 临床前 |
BT04 | 肿瘤 更多 | 药物发现 |
BT03 | 肿瘤 更多 | 药物发现 |
CN116688125 ( SEMA3G )专利挖掘 | 肿瘤 更多 | 药物发现 |
登录后查看更多信息
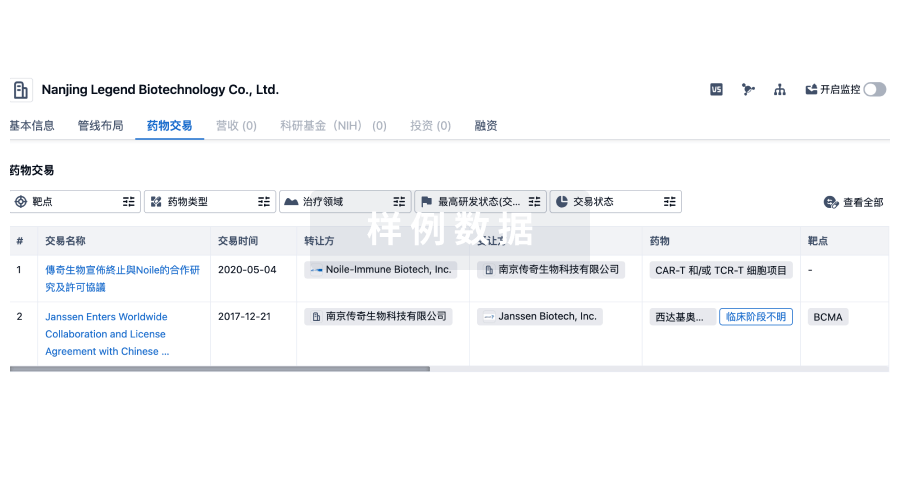
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
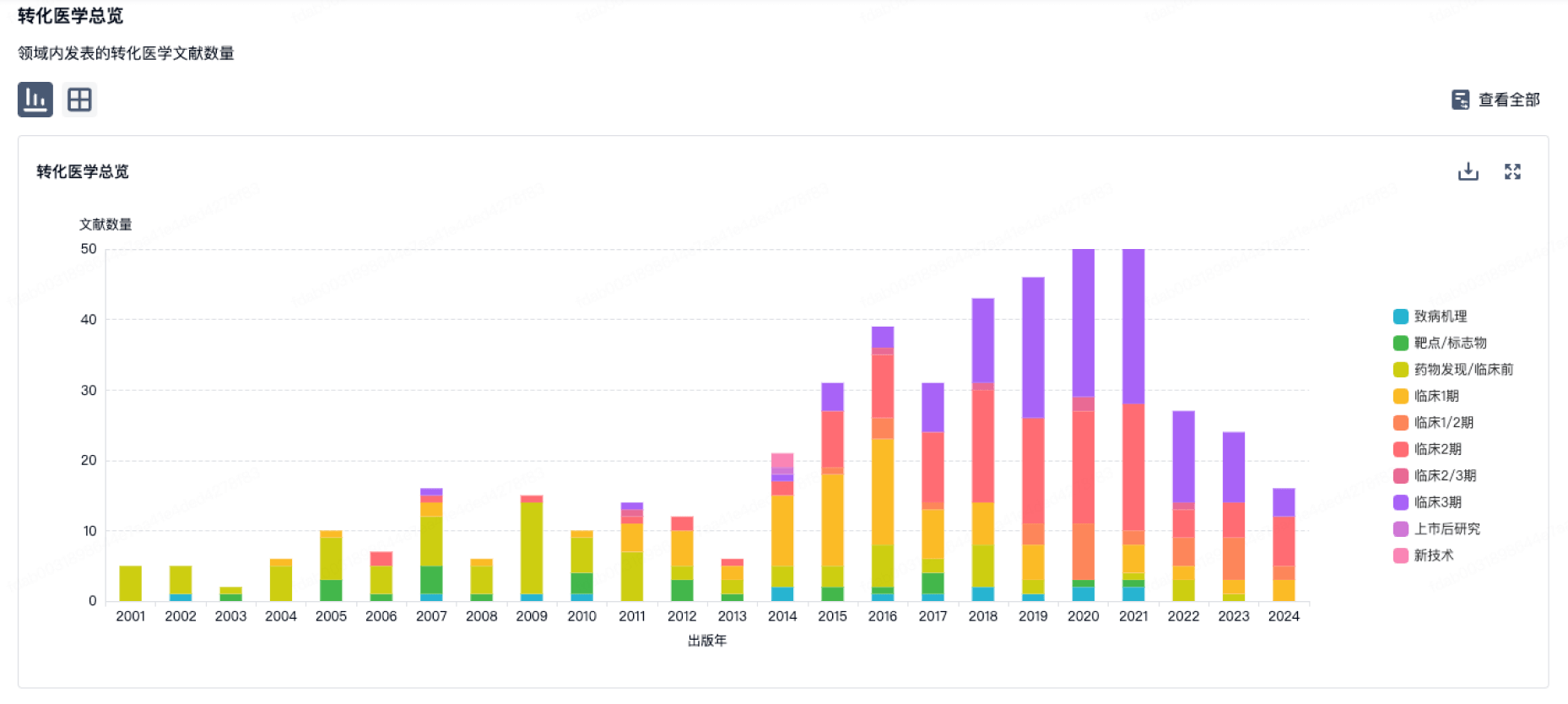
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
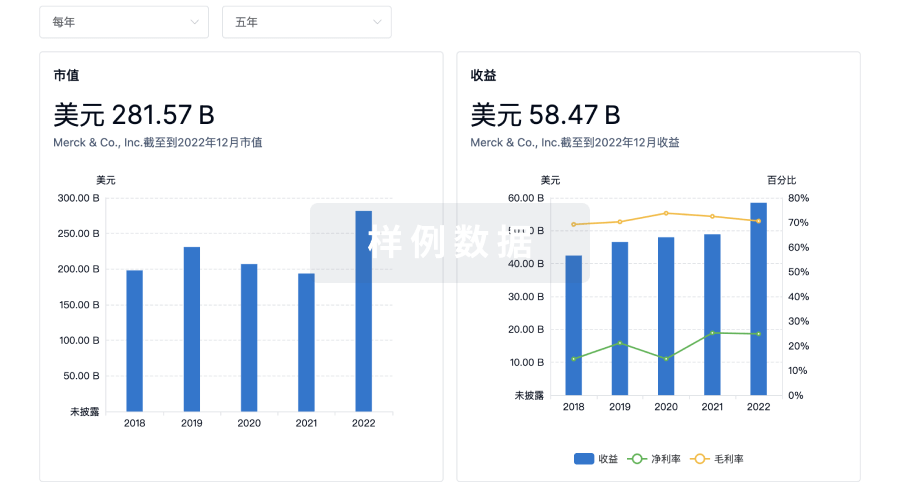
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
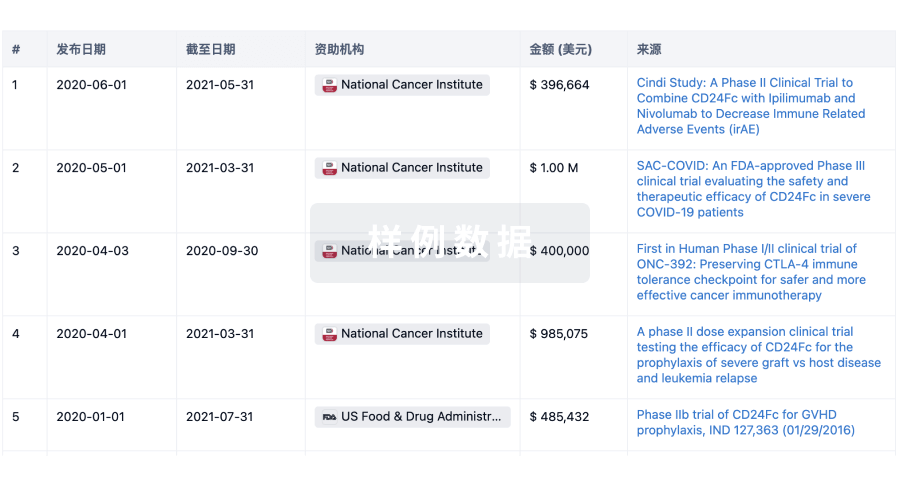
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
Eureka LS:
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用