预约演示
更新于:2025-10-27
Tonlamarsen
更新于:2025-10-27
概要
基本信息
在研机构 |
权益机构- |
最高研发阶段临床2期 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
登录后查看时间轴
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
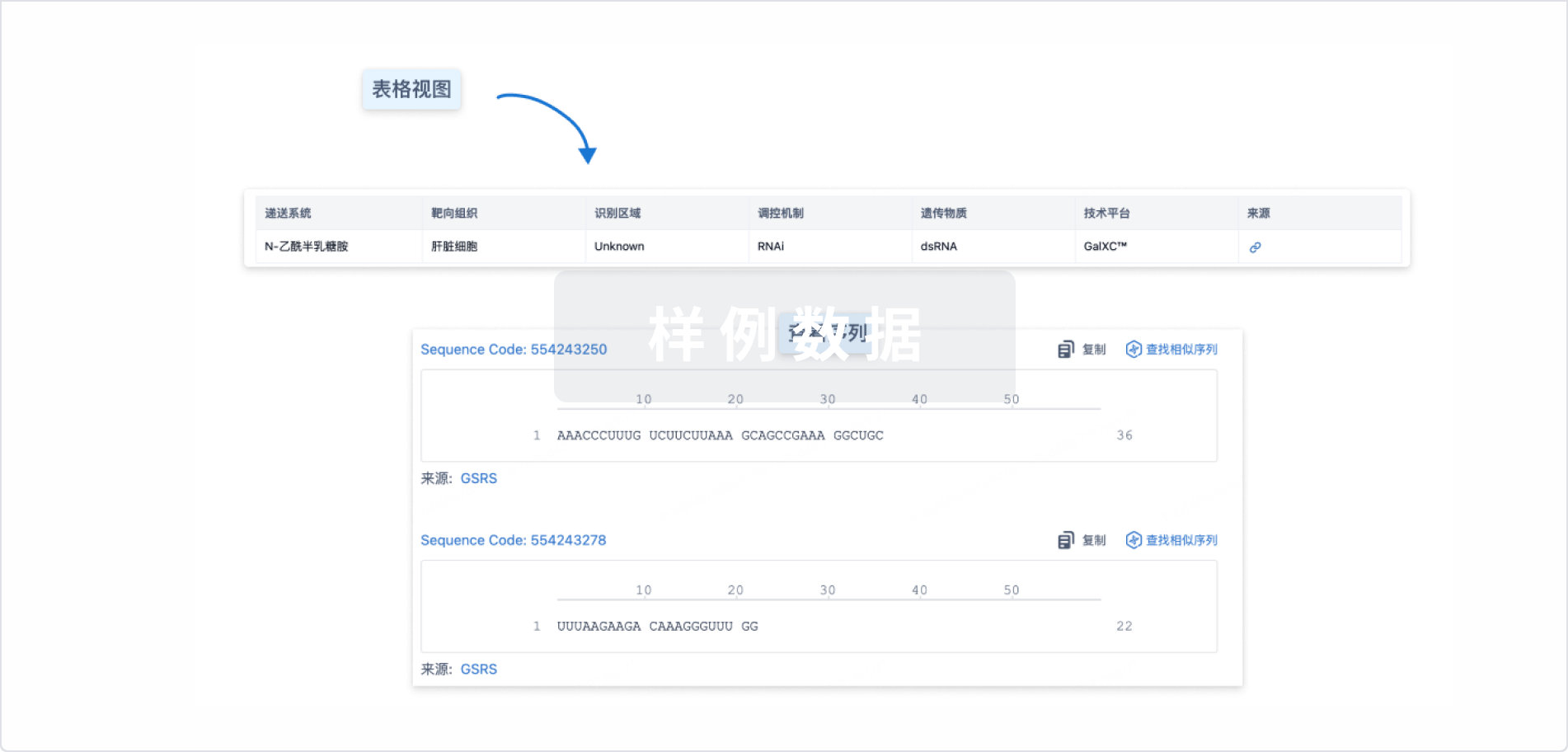
Sequence Code 317493258

来源: *****
关联
3
项与 Tonlamarsen 相关的临床试验NCT06864104
A Randomized, Double-Blind, Placebo-Controlled Study to Assess the Efficacy and Safety of Monthly Subcutaneous Administration of Tonlamarsen in Participants With Uncontrolled Hypertension (KARDINAL)
The purpose of this study is to evaluate the blood pressure-lowering effect of tonlamarsen in adult participants who, despite taking 2 or more antihypertensive medications, have not achieved their target blood pressure (BP).
开始日期2025-04-10 |
申办/合作机构 |
NCT05314439
A Double-Blind, Placebo-Controlled, Phase 2 Study to Assess the Safety, Tolerability and Efficacy of Monthly Subcutaneous Administration of ION904 in Patients With Uncontrolled Hypertension
The purpose of this study is to evaluate the effect of ION904 on plasma angiotensinogen (AGT) in participants with uncontrolled hypertension.
开始日期2022-04-29 |
申办/合作机构 |
NCT04731623
A Phase 1, Randomized, Double-Blind, Placebo-Controlled, Single Ascending, Dose-Escalation, Study to Assess the Safety, Tolerability, Pharmacokinetics and Pharmacodynamics of ION904 Administered Subcutaneously to Healthy Participants
The purpose of this study is to assess the safety and tolerability of ION904.
开始日期2021-02-26 |
申办/合作机构 |
100 项与 Tonlamarsen 相关的临床结果
登录后查看更多信息
100 项与 Tonlamarsen 相关的转化医学
登录后查看更多信息
100 项与 Tonlamarsen 相关的专利(医药)
登录后查看更多信息
18
项与 Tonlamarsen 相关的新闻(医药)2025-10-21
·创鉴汇
据创鉴汇不完全统计,上周(10月13日至10月19日)全球大健康领域共披露融资事件41起,总额超28亿美元。较前几周,融资数量和金额都有较大提升。
创新药融资较活跃,其中超亿美元的大额融资共6起。
代谢类疾病一直是关注的焦点。Kailera Therapeutics已完成上周潜在最高的6亿美元B轮融资,累计融资额达10亿美元,将研发差异化肥胖治疗管线。其中,核心管线KAI-9531是一款注射用GLP-1/GIP双靶点激动剂,有望在年底启动3期临床试验,目标覆盖BMI≥35的肥胖人群及伴发2型糖尿病患者。公司还将同步推进口服小分子GLP-1激动剂KAI-7535的全球临床研究,以及三靶点激动剂KAI-4729、口服型KAI-9531等早期项目。
2家抗体偶联药物(ADC)公司获融资。10月15日,Tubulis完成3.61亿美元C轮融资,将主要推进TUB-040的1/2期临床试验,该药物靶向NaPi2b抗原,拟治疗铂耐药卵巢癌以及晚期非小细胞肺癌患者,公司将于10月ESMO大会公布第一批临床数据。Tubulis依托Tubutecan平台整合专有载荷与P5缀合技术,通过减少循环中有效载荷的提前释放与聚集,降低脱靶毒性。平台已获BMS、吉利德两大公司青睐,合作开发新型ADC。
次日,另一家ADC公司Adcytherix宣布完成1.05亿欧元A轮融资,将推进其主导候选药物ADCX-020推进至临床阶段,并计划于今年年底前提交IND申请。
针对心脑血管疾病,Kardigan宣布完成2.54亿美元B轮融资。公司正在同时推进3款药物:包括心肌肌球蛋白激动剂Danicamtiv,引进自BMS,靶向遗传性扩张型心肌病(DCM)的肌节变异;血管紧张素原靶向疗法tonlamarsen,引进自Ionis,阻断急性重度高血压(ASH)的危险循环;以及ataciguat,这是一款口服sGC激活剂,治疗钙化性主动脉瓣狭窄(CAVS)。
2家公司针对雄激素性脱发推进口服与外用疗法,同时获得超亿美元融资。其中,Veradermics完成1.5亿美元C轮融资,开发口服缓释米诺地尔VDPHL01,通过延长毛囊药物暴露时间提升疗效。2期数据显示,治疗4个月后95%患者满意度提升,且没有严重的副作用,3期临床试验进行中。
Pelage Pharmaceuticals完成1.2亿美元B轮融资,由ARCH、谷歌风投领投,推进外用小分子PP405研发。其独特机制在于激活休眠毛囊干细胞并恢复身体自然生长头发的能力。2a期试验显示,给药4周后,脱发程度较高的男性中有31%的头发密度增加了20%以上,而安慰剂组为0%,计划2026年启动3期临床试验。
上周,中国创新药研发主要集中在细胞疗法领域。沙砾生物完成超6亿元C轮融资,开发治疗泛实体瘤TIL药物和现货型细胞疗法。此外,CAR-T细胞疗法公司华道生物也完成亿元级D+2轮融资。
其余融资详见下表。
读者们请星标⭐创鉴汇,第一时间收到推送
免责声明:本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
版权说明:欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转发/复制至其他平台。转发授权请在「创鉴汇」微信公众号留言联系我们。
更多数据内容推荐
点击“在看”,分享创鉴汇健康新动态
抗体药物偶联物临床2期临床申请临床3期
2025-10-20
10月14日,Kardigan 宣布完成 2.54 亿美元 B 轮融资,推进三个处于后期临床阶段的心血管产品,针对特定类型的扩张型心肌病、急性重度高血压和钙化性主动脉瓣狭窄,目前尚无有效治疗方法。
聚焦心血管疾病的 Kardigan 完成 2.54 亿美元 B 轮融资
by
TiPLab 木桃
Kardigan 于2025年1月10日成立,将其领先的发现和转化研究平台与战略性许可和收购相结合。该公司的研发平台利用一套专有的心脏专用工具,能够深入了解其候选疗法的机制以及患者对治疗的个体化反应,以更好匹配疾病驱动因素与患者人群,从而优化临床研究设计并增强结果的可信度。
Kardigan 研发平台的核心部分来自于其收购的临床智能公司 Prolaio,其经 FDA 批准的软件整合了真实世界的心血管临床数据和专有算法。
Prolaio 的平台技术包括通过 FDA 批准的五种算法和超过四百万小时的患者数据,可以将数据转化为对疾病的洞察,目前已有 20 多项授权专利保护。
Kardigan 的部分创始团队成员之前领导 MyoKardia 发现和开发了第一个心脏肌球蛋白抑制剂 mavacamten,2020年 MyoKardia 被 BMS 以 130 亿美元收购。
Kardigan 的三个管线包括:danicamtiv、tonlamarsen和ataciguat。
来源:TiPLab
Danicamtiv是一种潜在首创选择性心肌肌球蛋白小分子激动剂,用于治疗由肌节突变驱动的遗传性扩张型心肌病(DCM),由 MyoKardia 发现并由 BMS 进一步开发,Kardigan 获得了 danicamtiv 的全球独家开发和商业化权利。DCM 相关的 MYH7 和 TTN 致病变异可损害心肌肌球蛋白的功能,目前尚无针对其根本病因的治疗方法。Danicamtiv可选择性增强心肌肌球蛋白的功能,2a 期临床试验数据显示,其可显著改善左心房功能指数和左心室射血分数,且具有统计学意义。
急性重度高血压(ASH)是指血压突然急剧升高,需要立即就诊以预防心脏病发作、中风或其他器官损害。虽然许多 ASH 患者都患有慢性高血压,但 ASH 很少作为一种疾病状态进行研究。目前尚无针对 ASH 的治疗方法。Tonlamarsen 作为一种血管紧张素原靶向桥接疗法,用于阻断 ASH 的危险循环,并有望降低血压并降低器官损害、心力衰竭和其他严重心血管事件的风险。由 Ionis 发现和开发,Kardigan 获得了全球独家开发和商业化权利。
主动脉瓣钙化是美国和欧盟成人主动脉瓣狭窄的主要原因。Ataciguat 是一种每日一次口服的可溶性鸟苷酸环化酶激活剂,有望成为 CAVS 的首创治疗方法,取代目前“密切观察”的瓣膜置换术,后者是目前的标准治疗方法。Ataciguat 由赛诺菲和梅奥诊所开发,Kardigan 获得了许可。
* 以上文字仅为促进讨论与交流,不构成法律意见或咨询建议。
© 作为一家专业服务公司,TiPLab坚持原创的系统的研究,注重系统性知识积累与专业影响力。欢迎读者个人分享转发,各专业平台媒体如需转载请联系TiPLab获得授权。
TiPLab提供基于研究的核心知识产权服务
FTO:技术商业化实施的侵权风险防范
TiPLab通过对细分技术领域内核心技术和重要专利的长期研究,结合自身在数据检索和分析方面的专长,致力于帮助客户深入了解、积极应对潜在的专利侵权风险。
Due Diligence:商业活动中的知识产权尽职调查
在企业许可交易、融资、并购、上市等过程中,TiPLab帮助企业和投资方了解目标技术/产品的专利保护强度及产品商业化过程中潜在的专利侵权风险,从而为商业谈判和决策提供支持依据。
Patenting:全球范围内高价值专利资产的创设
TiPLab熟知全球主要国家和地区的法律实践和细分领域内的前沿技术进展情况,通过前瞻性的专利布局策略,帮助客户通过创设有价值的专利资产而获取、保持和巩固独特的竞争优势。
并购
2025-10-20
·医药观澜
根据公开信息,上周(10月13日~10月19日),全球范围内有至少13家致力于创新药研发的新锐公司宣布完成新一轮融资。通过梳理,这些获得资本青睐的新锐公司正在开发的产品包括小分子、多肽、抗体偶联药物(ADC)、反义寡核苷酸(ASO)、细胞疗法等等。
BridGene Biosciences
融资轮次:B+轮
融资金额:2800万美元
10月16日,BridGene宣布已于近期完成2800万美元B+轮融资。本轮融资由康君资本领投,高特佳投资、比邻星创投以及现有投资方龙磐投资和磐谷创投共同参与。BridGene是一家处于临床阶段的小分子创新药生物科技公司,专注于开发针对传统“不可成药”靶点的新型疗法。该公司核心候选药物BGC-515是一款针对实体瘤的共价TEAD抑制剂,目前在1期临床,并计划于近期启动2期临床研究。此外,资金还将用于推动公司第二个管线项目于2027年进入临床阶段,并加速公司在肿瘤及自身免疫疾病领域的后续管线布局。
Veradermics
融资轮次:C轮
融资金额:1.5亿美元
10月16日,Veradermics宣布完成超额认购的1.5亿美元C轮融资。此次融资将用于推进其核心在研产品VDPHL01的注册性试验及预定的新药申请(NDA)提交。VDPHL01是一款专为男女脱发患者设计、潜在首款缓释口服minoxidil候选药物,目前正在进行3期试验。该公司同时公布了进行中2期临床研究的初步结果,该研究评估VDPHL01用于治疗男女模式性脱发(pattern hair loss)的疗效与安全性。主观评价方面,在4个月结束时,95%的受试者表示对头发覆盖度的满意度提高。
Peptilogics
融资轮次:7800万美元
融资金额:B2轮
10月16日,Peptilogics宣布完成一轮超额认购的7800万美元B2轮融资。Peptilogics是一家临床阶段生物技术公司,致力于开发变革性外科治疗药物,以有效治疗和预防严重的医疗器械感染。此笔资金将用于支持其研究性药物zaloganan (PLG0206) 治疗假体关节感染 (PJI) 的关键性2/3期试验。这是一款广谱、抗菌和抗生物膜肽治疗药物,通过独特的作用机制靶向并破坏细菌膜,可快速局部渗透生物膜并杀死隐藏的细菌。在1b期研究中,在清创、抗生素治疗和假体保留 (DAIR)手术期间使用zaloganan冲洗液,14 名患者中的13名 (93%) 在12个月时保持无感染状态。
Adcytherix
融资轮次:A轮
融资金额:1.05亿欧元
10月16日,Adcytherix宣布成功完成1.05亿欧元(约合1.22亿美元)A轮融资。该公司致力于设计和开发具有新型有效载荷的专有抗体偶联药物(ADC),本轮融资资金将用于将其主导候选药物ADCX-020推进至临床阶段,并计划于2025年底前提交IND申请。与此同时,Adcytherix将扩展其使用新型有效载荷的专有ADC管线。
Step Pharma
融资轮次:C轮
融资金额:3800万欧元
10月15日,Step Pharma宣布完成3800万欧元C轮融资。本轮融资将支持该公司就其主导资产 dencatistat在多个适应症中进行的持续临床开发。这是一种高选择性、具有口服生物利用度的CTPS1抑制剂,正在开发用于治疗癌症和血液疾病,目前已经启动了针对T或B细胞淋巴瘤、实体瘤、原发性血小板增多症等适应症的临床研究。研究表明,多种都高度依赖CTPS1(嘧啶合成途径的关键组成部分)进行DNA合成和细胞增殖。
Pelage Pharmaceuticals
融资轮次:B轮
融资金额:1.2亿美元
10月15日,Pelage Pharmaceuticals宣布完成1.2亿美元B轮融资。所获资金将用于推进公司核心项目PP405的持续开发。基于之前在雄激素性脱发研究中获得的2a期试验积极结果,公司计划于2026年推进PP405进入3期临床。PP405是一种新型的外用小分子,设计用于激活休眠毛囊干细胞,重启毛发生长。此前一项2期临床研究结果显示,接受PP405治疗且脱发程度更高的男性中,有31%达成发密度较基线提升超过20%的应答,而此数值在安慰剂组为0%。
Tubulis
融资轮次:C轮
融资金额:3.61亿美元
10月15日,Tubulis宣布成功完成一笔3.08亿欧元(约合3.61亿美元)的C轮融资。本轮融资所得将用于将Tubulis的主导ADC候选产品TUB-040的临床开发扩展到更早的治疗线和更多的肿瘤适应症。TUB-040靶向NaPi2b,这是一种在卵巢癌和肺腺癌中过度表达的抗原。TUB-040目前正在一项针对铂耐药卵巢癌以及复发或难治性非小细胞肺癌患者的1/2a期研究中进行评估,并于2024年6月获得美国FDA的快速通道资格。该笔资金还将推进Tubulis的其它管线,包括临床阶段靶向5T4的ADC候选药物TUB-030、多个临床前项目,并扩展其专有的ADC平台技术。
Omnix Medical
融资轮次:C轮
融资金额:2500万美元
10月15日,Omnix Medical宣布获得2500万美元C轮融资。Omnix是一家致力于开发用于治疗危及生命感染的下一代抗感染药物的生物医药公司,此次融资将使该公司能够完成其先导化合物OMN6的2期概念验证研究。这些研究将侧重于治疗由革兰氏阴性菌(特别是鲍曼不动杆菌)引起的危及生命的感染,包括对碳青霉烯类和粘菌素等最后防线治疗耐药的菌株。OMN6是一种潜在“first-in-class”抗菌肽,其设计旨在对细菌膜具有高选择性,其特异性地结合细菌膜独特的脂质成分,并迅速形成孔洞,破坏其稳定性并摧毁膜结构,导致细菌迅速死亡。该产品速的作用机制、工程化的稳定性以及避免酶降解的能力使得治疗周期更短,并最大限度地降低了耐药性发展的风险。
Mission Therapeutics
融资轮次:未披露
融资金额:1330万美元
10月15日,Mission Therapeutics宣布已筹集1330万美元,用于推进一项主导候选药物MTX325在帕金森病患者中进行的1b期机制验证研究。Mission是一家临床阶段生物技术公司,致力于开发通过增强线粒体自噬来促进细胞和器官健康的“first-in-class”疗法。MTX325是一种具有口服生物利用度和脑渗透性的USP30抑制剂,旨在改善线粒体质量,通过抑制USP30(一种线粒体去泛素化酶)发挥作用,从而增加线粒体泛素化并促进适当的线粒体自噬——这是细胞用来清除自身功能失调线粒体的基本过程。线粒体功能障碍是帕金森病病理生理学的一个主要假说。抑制USP30是一种经过充分验证的方法,可通过恢复线粒体自噬来实现帕金森病的神经保护。
Kardigan
融资轮次:B轮
融资金额:2.54亿美元
10月15日,Kardigan宣布完成2.54亿美元B轮融资。Kardigan致力于新型心血管药物的开发,以提供能使患者超越症状管理、实现功能性治愈的药物。本轮融资将用于持续推动针对特定类型扩张型心肌病、急性严重高血压和钙化性主动脉瓣狭窄的三个后期研发项目取得进展,包括:danicamtiv,一种针对由肌节变异驱动的遗传性扩张型心肌病的心脏肌球蛋白激活剂;tonlamarsen,一种血管紧张素原靶向反义寡核苷酸(ASO)疗法,拟用于中断急性严重高血压的危险循环;以及ataciguat,一种每日一次的口服可溶性鸟苷酸环化酶激活剂,拟开发作为钙化性主动脉瓣狭窄的潜在"积极监测"的替代方案。
Tr1X Bio
融资轮次:未披露
融资金额:5000万美元
10月14日,Tr1X Bio宣布美国FDA批准其治疗进展型多发性硬化的同种异体CAR-Tr1 Treg细胞疗法TRX319的IND申请,并获得额外5000万美元融资。Tr1X 是一家临床阶段生物医药公司,致力于开发具有治愈自身免疫和炎症性疾病潜力的同种异体工程化1型调节性T细胞(Tr1 Treg)和CAR-Tr1 Treg细胞疗法。TRX319旨在将靶向B细胞控制与主动抗炎信号传导和致病性T细胞调节相结合,并具有中枢神经系统渗透性。本轮融资还将助力Tr1X Bio另一款在研新药TRX103开展针对难治性克罗恩病患者的1/2a期临床试验。TRX103是一种在研同种异体即用型工程化T细胞产品,可以模拟1型调节性T细胞(Tr1)功能的细胞,称为TRX细胞。
Kailera Therapeutics
融资轮次:B轮
融资金额:6亿美元
10月14日,Kailera Therapeutics宣布完成6亿美元B轮融资。本轮融资由Bain Capital Private Equity领投,所获资金将用于推进其差异化的肥胖症治疗产品管线的开发。融资款项将主要用于支持其核心候选药物KAI-9531(一款注射用GLP-1/GIP双受体激动剂,具有潜在“best-in-category”的减重效果)在年底前启动全球3期临床试验。同时,资金也将用于推进其口服小分子GLP-1受体激动剂KAI-7535开展全球临床研究。该药在中国的2期临床试验中已表现出具有竞争力的减肥效果。该公司也将继续推进其早期项目,包括注射用GLP-1/GIP/胰高血糖素受体三激动剂KAI-4729,以及每日一次口服型KAI-9531。
Excellergy
融资轮次:A轮
融资金额:7000万美元
10月13日,Excellergy宣布正式启动并完成7000万美元的A轮融资,以推进其潜在“first-in-class”效应细胞反应抑制剂(ECRIs)产品组合。Excellergy是一家旨在开发新型过敏治疗药物的生物技术公司,其通过设计新型三功能ECRIs重新定义过敏治疗,旨在通过靶向效应细胞实现强效、快速缓解并完全控制过敏反应。这类新的ECRIs采用三功能作用机制:1)快速移除肥大细胞和嗜碱性粒细胞上结合FceRI的IgE,且不触发这些细胞的激活;2)提供强效、高亲和力的游离IgE中和作用;3)加速 FceRI表达的下调。这三个功能同步作用,与现有已批准疗法相比,有潜力在更广泛的患者群体中实现更快速的起效和更完全的过敏控制。该公司计划在2026年初将其主导资产推进至临床阶段。
期待在资本的助力下,更多前沿疗法和技术能够更快惠及患者。
参考资料:
[1]各公司官网及公开资料
版权说明:本文欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权或其他合作需求,请联系wuxi_media@wuxiapptec.com。
免责声明:本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
临床2期抗体药物偶联物临床1期临床申请细胞疗法
100 项与 Tonlamarsen 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 高血压 | 临床2期 | 美国 | 2022-04-29 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用

