更新于:2024-06-29
RG1-VLP
更新于:2024-06-29
概要
基本信息
在研机构  PathoVax LLC初创企业 PathoVax LLC初创企业 |
非在研机构- |
最高研发阶段临床申请 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
关联
100 项与 RG1-VLP 相关的临床结果
登录后查看更多信息
100 项与 RG1-VLP 相关的转化医学
登录后查看更多信息
100 项与 RG1-VLP 相关的专利(医药)
登录后查看更多信息
3
项与 RG1-VLP 相关的文献(医药)2019-06-01·Vaccine3区 · 医学
Incorporation of RG1 epitope into HPV16L1-VLP does not compromise L1-specific immunity
3区 · 医学
Article
作者: Skoll, M ; Schellenbacher, C ; Kirnbauer, R ; Huber, B ; Roden, R B S ; Shafti-Keramat, S
The candidate pan-Human Papillomavirus (HPV) vaccine RG1-VLP are HPV16 major capsid protein L1 virus-like-particles (VLP) comprising a type-common epitope of HPV16 minor capsid protein L2 (RG1; aa17-36). Vaccinations have previously demonstrated efficacy against genital high-risk (hr), low-risk (lr) and cutaneous HPV. To compare RG1-VLP to licensed vaccines, rabbits (n = 3) were immunized thrice with 1 µg, 5 µg, 25 µg, or 125 µg of RG1-VLP or a 1/4 dose of Cervarix®. 5 µg of RG1-VLP or 16L1-VLP (Cervarix) induced comparable HPV16 capsid-reactive and neutralizing antibodies titers (62,500/12,500-62,500 or 1000/10,000). 25 µg RG1-VLP induced robust cross-neutralization titers (50-1000) against hrHPV18/31/33/45/52/58/26/70. To mimic reduced immunization schedules in adolescents, mice (n = 10) were immunized twice with RG1-VLP (5 µg) plus 18L1-VLP (5 µg). HPV16 neutralization (titers of 10,000) similar to Cervarix and Gardasil and cross-protection against hrHPV58 vaginal challenge was observed. RG1-VLP vaccination induces hrHPV16 neutralization comparable to similar doses of licensed vaccines, plus cross-neutralization to heterologous hrHPV even when combined with HPV18L1-VLP.
2013-12-01·The Journal of investigative dermatology1区 · 医学
Efficacy of RG1-VLP Vaccination against Infections with Genital and Cutaneous Human Papillomaviruses
1区 · 医学
Article
作者: Shafti-Keramat, Saeed ; Kirnbauer, Reinhard ; Schellenbacher, Christina ; Fink, Dieter ; Jindra, Christoph ; Roden, Richard B S ; Dillner, Joakim ; Kwak, Kihyuck ; Faust, Helena ; Huber, Bettina
Licensed human papillomavirus (HPV) vaccines, based on virus-like particles (VLPs) self-assembled from major capsid protein L1, afford type-restricted protection against HPV types 16/18/6/11 (or 16/18 for the bivalent vaccine), which cause 70% of cervical cancers (CxCas) and 90% of genital warts. However, they do not protect against less prevalent high-risk (HR) types causing 30% of CxCa, or cutaneous HPV. In contrast, vaccination with the minor capsid protein L2 induces low-level immunity to type-common epitopes. Chimeric RG1-VLP presenting HPV16 L2 amino acids 17-36 (RG1 epitope) within the DE-surface loop of HPV16 L1 induced cross-neutralizing antisera. We hypothesized that RG1-VLP vaccination protects against a large spectrum of mucosal and cutaneous HPV infections in vivo. Immunization with RG1-VLP adjuvanted with human-applicable alum-MPL (aluminum hydroxide plus 3-O-desacyl-4'-monophosphoryl lipid A) induced robust L2 antibodies (ELISA titers 2,500-12,500), which (cross-)neutralized mucosal HR HPV16/18/45/37/33/52/58/35/39/51/59/68/73/26/69/34/70, low-risk HPV6/11/32/40, and cutaneous HPV2/27/3/76 (titers 25-1,000) using native virion- or pseudovirion (PsV)-based assays, and a vigorous cytotoxic T lymphocyte response by enzyme-linked immunospot. In vivo, mice were efficiently protected against experimental vaginal challenge with mucosal HR PsV types HPV16/18/45/31/33/52/58/35/39/51/59/68/56/73/26/53/66/34 and low-risk HPV6/43/44. Enduring protection was demonstrated 1 year after vaccination. RG1-VLP is a promising next-generation vaccine with broad efficacy against all relevant mucosal and also cutaneous HPV types.
Journal of clinical medicine3区 · 医学
RG1-VLP and Other L2-Based, Broad-Spectrum HPV Vaccine Candidates
3区 · 医学
ReviewOA
作者: Wang, Joshua Weiyuan ; Huber, Bettina ; Roden, Richard B S ; Kirnbauer, Reinhard
Licensed human papillomavirus (HPV) vaccines contain virus-like particles (VLPs) self-assembled from L1 major-capsid proteins that are remarkably effective prophylactic immunogens. However, the induced type-restricted immune response limits coverage to the included vaccine types, and costly multiplex formulations, restrictive storage and distribution conditions drive the need for next generation HPV vaccines. Vaccine candidates based upon the minor structural protein L2 are particularly promising because conserved N-terminal epitopes induce broadly cross-type neutralizing and protective antibodies. Several strategies to increase the immunological potency of such epitopes are being investigated, including concatemeric multimers, fusion to toll-like receptors ligands or T cell epitopes, as well as immunodominant presentation by different nanoparticle or VLP structures. Several promising L2-based vaccine candidates have reached or will soon enter first-in-man clinical studies. RG1-VLP present the HPV16L2 amino-acid 17–36 conserved neutralization epitope “RG1” repetitively and closely spaced on an immunodominant surface loop of HPV16 L1-VLP and small animal immunizations provide cross-protection against challenge with all medically-significant high-risk and several low-risk HPV types. With a successful current good manufacturing practice (cGMP) campaign and this promising breadth of activity, even encompassing cross-neutralization of several cutaneous HPV types, RG1-VLP are ready for a first-in-human clinical study. This review aims to provide a general overview of these candidates with a special focus on the RG1-VLP vaccine and its road to the clinic.
3
项与 RG1-VLP 相关的新闻(医药)2023-04-02
·药明康德
▎药明康德内容团队编辑本期看点1. Agenus公司公布新CTLA-4/PD-1免疫组合疗法治疗卵巢癌的积极早期结果,缓解率较既往其他同类免疫组合疗法在类似人群中的结果有大幅度提高。2. Viking Therapeutics公司GLP-1/GIP受体双重激动剂VK2735临床数据亮眼,给药不到一个月患者体重减轻7.8%(约16斤)。3. 治疗阿尔茨海默病的反义寡核苷酸疗法BIIB080展现积极早期临床结果,2期临床试验已经展开。药明康德内容团队整理Botensilimab:公布1b期临床试验数据Agenus公司公布了其在复发性铂类药物耐药/难治性卵巢癌患者中开展的1b期扩展研究的积极结果。该研究使用botensilimab(一种多功能CTLA-4抗体)联合巴替利单抗(balstilimab,一种PD-1抗体)的方案。Botensilimab是一种研究性的新型多功能CTLA-4抗体,旨在将临床获益扩展到既往对标准治疗或试验性疗法无反应的“冷”肿瘤。除与CTLA-4受体结合外,其Fc增强的结构能够诱导记忆免疫反应,下调调节性T细胞,并使T细胞更好地启动和活化,从而放大免疫反应。在一项超过300例患者的1b期临床研究中,botensilimab已经在9种实体肿瘤中证明了其临床应答,无论是单独使用还是与巴替利单抗联合使用。此次公布的研究结果显示,该免疫联合疗法在包含24名可评估的卵巢癌患者的队列中的总缓解率(ORR)为33%,包括1例完全缓解(CR)和7例部分缓解(PR)。而在既往其他试验中,其他PD-(L)1抗体联用CTLA-4抗体在类似可比较的患者人群中报告的缓解率仅为3-10%。该研究中,患者的疾病控制率(DCR)为67%,中位缓解持续时间尚未达到。此外,该免疫组合疗法具有可管理的耐受性特征。VK2735:公布1期临床试验数据Viking Therapeutics公司公布了其GLP-1/GIP受体双激动剂VK2735在单剂量递增(SAD)和多剂量递增(MAD)临床1期试验的积极结果。VK2735是一款基于多肽的在研胰高血糖素样肽1(GLP-1)和葡萄糖依赖性促胰岛素多肽(GIP)受体的新型双重激动剂,用于各种代谢紊乱的潜在治疗。GIP和GLP-1是调控血糖的天然肠促胰岛素激素。此次公布的数据显示,患者在使用皮下注射VK2735(最高使用剂量为10 mg)28天时,其体重与基线相较下降幅度达7.8%(平均体重下降约16斤)。接受VK2735治疗的队列也显示其平均体重较安慰剂组减轻,幅度最高达6.0%。在第43天随访时间点(VK2735末次给药后21天)时,VK2735组患者与安慰剂组患者相比,其体重下降程度得以维持或改善,且差异具统计学意义。基于此1期试验结果,公司计划于2023年中启动VK2735在肥胖患者中的2期研究。BIIB080(IONIS-MAPT):公布1b期临床试验数据渤健(Biogen)与Ionis Pharmaceuticals共同宣布其合作开发的在研反义寡核苷酸(ASO)疗法BIIB080(IONIS-MAPT)在治疗阿尔茨海默病的临床1b试验中展现出积极结果。阿尔茨海默病的主要神经病理学特征是存在细胞外的β-淀粉样蛋白(Aβ)和细胞内过度磷酸化的tau蛋白沉积。病理性tau蛋白的积累已被证明可造成神经元损伤和死亡。BIIB080是IONIS发现的一种在研ASO疗法,旨在靶向微管相关蛋白tau(MAPT)的mRNA以阻止tau蛋白的产生。此次公布的结果显示,BIIB080以剂量依赖和持续性的方式降低了脑脊液(CSF)中可溶性tau的生物标志物(t-tau和p-tau181),所有剂量组在长期扩展试验结束时显示其CSF中tau水平较基线降低约60%。通过正电子发射断层扫描(PET)测量发现,BIIB080在第25周时便对聚集的病理性tau蛋白产生影响,并一直持续至第100周长期扩展试验结束。当扩展试验结束时,在评估的所有脑复合终点中,BIIB080降低了所有剂量组的病理性tau蛋白水平。安全性方面,大多数不良事件的严重程度为轻度或中度,其中最常见的是头痛、背痛和腰椎穿刺后综合征(PLPS)。CBP-4888:IND申请获得FDA许可CBP-4888是Comanche Biopharma公司开发的用于治疗先兆子痫的新型siRNA疗法。先兆子痫是一种普遍存在的妊娠期高血压疾病,其主要病因是胎盘过量产生的可溶性fms样酪氨酸激酶-1(sFLT1)蛋白进入了孕妇的血液,目前尚无可以改变疾病进程的治疗方法。CBP-4888是一种皮下递送的siRNA疗法,可减少胎盘中sFLT1蛋白的产生。CBP-4888有望改善先兆子痫的症状,包括高血压和对肾脏和肝脏等器官的损害,并可能安全地延长妊娠期。BDC-1001:公布1期临床试验数据Bolt Biotherapeutics公司公布了其抗体-免疫刺激偶联物(ISAC)候选药物BDC-1001针对表达HER2的实体瘤开展的剂量递增研究的积极结果。Bolt公司的ISAC技术平台结合了抗体靶向的精确性,与激发先天性和适应性免疫系统反应的作用。ISAC由三个主要组成部分:靶向肿瘤抗体、稳定且不可降解的连接子(linker)、和用于激活患者先天免疫系统的专有免疫刺激剂。BDC-1001能够靶向HER2,其包含的免疫刺激剂旨在募集和激活骨髓细胞。激活的骨髓细胞将释放细胞因子和趋化因子,吸引其他免疫细胞并降低免疫反应激活阈值的化学信号,开始前馈循环。这将重新编程肿瘤微环境并引发针对肿瘤的适应性免疫反应,以达到为癌症患者提供持久反应的目的。此次公布的结果显示,BDC-1001无论是作为单一疗法还是与纳武利尤单抗联合使用均具有良好的耐受性。此外,BDC-1001作为单一疗法和与纳武利尤单抗联合治疗多种表达HER2的实体肿瘤实现了客观的临床缓解,包括多个达到PR的患者和达到长期疾病稳定(SD)状态的患者。Bolt公司计划将BDC-1001推进到乳腺癌、结直肠癌、子宫内膜癌和胃食管癌的2期研究。MDNA11:公布1/2期临床试验数据Medicenna Corp公司公布了其下一代长效IL-2超级激动剂MDNA11治疗晚期实体肿瘤的新临床结果。MDNA11具有优秀的CD122(IL-2受体β)结合作用,而没有CD25(IL-2受体α)亲和力,从而能优先刺激癌症杀伤效应T细胞和NK细胞。在该研究中,MDNA11第5个剂量递增队列的药代动力学数据与前4个队列的发现相一致,MDNA11继续表现出长期的、选择性的和剂量依赖性的抗肿瘤免疫作用。前4个队列中,14例可评估的患者中有5例实现了肿瘤控制。其中,1例转移性胰腺导管腺癌患者(4线)达到了PR,并获得了持续缓解,非靶转移病灶实现了完全消退,还有1例转移性黑色素瘤患者(3线)保持SD状态超过70周。迄今为止,没有观察到由于安全问题导致的剂量限制性毒性、剂量中断、剂量减少或治疗中断。该研究的第6个剂量递增队列目前正在进行给药。ZP8396:公布1期临床试验数据Zealand Pharma公司公布了其研究性的强效、长效胰淀素(amylin)类似物ZP8396的首次人体1期临床试验的积极结果。此前的研究显示,胰淀素类似物具有作为治疗肥胖的单一药物和联合疗法的潜力。ZP8936已在肥胖和糖尿病的临床前模型中证明其具有减轻体重和改善血糖的潜力。此次公布的结果显示,给予单剂量的ZP8396后,患者的体重较基线时有剂量依赖性的下降,平均降低4.2%(安慰剂校正后为4.8%)。ZP8396的血浆半衰期为230小时,适合每周给药一次。此外,ZP8396在该研究中的耐受性良好,没有严重的不良事件,也没有患者退出试验。最常见的不良事件是食欲下降、恶心和呕吐,大多数事件是轻微且短暂的。CLN-617:IND申请获得FDA许可CLN-617是Cullinan Oncology开发的细胞因子疗法,由单个分子中的两种有效的抗肿瘤细胞因子IL-2和IL-12组成。该候选疗法的给药方式为肿瘤内注射,并采用胶原结合和尺寸增强的结构域,旨在将其分子保留在肿瘤内,从而提高疗效并降低毒性。临床前研究表明,尽管CLN-617为局部给药,但它同样会引发广泛的免疫反应,这不仅有助于根除注射区域的肿瘤,还可以攻击远处的肿瘤。此外,当CLN-617与检查点抑制剂联合使用时,它具有增强疗效的潜力。Cullinan公司计划在针对晚期实体瘤患者开展的1期临床试验中评估CLN-617。VYN201:公布1a期临床试验的初步结果VYNE Therapeutics公司公布了其用于治疗非节段性白癜风的在研新型BET抑制剂VYN201的早期临床试验的积极结果。VYN201是一种泛溴结构域BET抑制剂,通过局部给药降低其全身暴露量,用于治疗涉及多种不同炎症细胞信号通路的疾病。在临床前模型中,VYN201已被证明具有局部活性,能够持续减少促炎和疾病相关生物标志物,并改善疾病的严重程度。此次公布的结果显示,在五个递增剂量组中,局部使用VYN201没有检测到高于测定的量化下限(0.25 ng/ml)的可量化的药物血浆浓度。此外,该实验中,包括血小板计数在内的所有血液学参数均在正常范围内,而血小板计数偏低是全身给药的泛溴结构域BET抑制剂常见的剂量限制性不良事件。该结果支持VYN201的局部给药方案。ALG-055009:公布1期临床试验的初步数据Aligos Therapeutics公司公布了其治疗非酒精性脂肪性肝炎(NASH)的候选药物甲状腺受体-β(THR-ß)激动剂ALG-055009的1期临床数据。结果显示,ALG-055009在健康受试者和高脂血症受试者中表现出良好的安全性和药代动力学特征。此外,研究人员在该研究中还观察到了预期的拟甲状腺素效应,包括致动脉粥样化脂质(atherogenic lipids)的剂量依赖性减少。VTP-300:公布1b/2a期临床试验的新数据Vaccitech Limited公司宣布其针对慢性乙型肝炎(HBV)感染者的候选疫苗VTP-300在1b/2a期临床试验中达到了主要和次要终点。VTP-300是一种与疫苗作用机制非常类似的免疫疗法。利用Vaccitech的黑猩猩腺病毒载体(ChAdOx1)和改良牛痘安卡拉病毒(MVA)载体表达乙肝病毒抗原,激发抗HBV的免疫应答,有望为慢性乙肝患者带来功能性治愈。此次公布的数据显示,VTP-300能够诱导慢性乙型肝炎患者的乙型肝炎表面抗原(HBsAg)持续减少,基线时HBsAg较低的患者的下降程度最为显著。此外,在该试验中,VTP-300的耐受性良好,给药后没有发生与VTP-300相关的3级不良事件或严重不良事件。HPV16 RG1-VLP:IND申请获得FDA许可HPV16 RG1-VLP是PathoVax公司基于RGVax技术开发的预防性通用HPV疫苗,该技术衍生自约翰霍普金斯大学和维也纳医科大学的疫苗研究。RGVax技术及其配方已被证明可针对至少18种高风险HPV类型提供全面的保护,并且在无需加强针的情况下,其免疫原性能够维持一年以上。PathoVax公司认为这种额外的保护最终有望为许多患者建立新的护理标准。 大家都在看药明康德为全球生物医药行业提供一体化、端到端的新药研发和生产服务,服务范围涵盖化学药研发和生产、生物学研究、临床前测试和临床试验研发、细胞及基因疗法研发、测试和生产等领域。如您有相关业务需求,欢迎点击下方图片填写具体信息。▲如您有任何业务需求,请长按扫描上方二维码,或点击文末“阅读原文/Read more”,即可访问业务对接平台,填写业务需求信息▲欲了解更多前沿技术在生物医药产业中的应用,请长按扫描上方二维码,即可访问“药明直播间”,观看相关话题的直播讨论与精彩回放参考资料(可上下滑动查看)[1] Cullinan Oncology Announces U.S. FDA Clearance of Investigational New Drug Application for CLN-617, a Novel Fusion Protein Harnessing IL-2 and IL-12 Cytokines. Retrieved April 1, 2023, from https://www.globenewswire.com/news-release/2023/03/27/2634613/0/en/Cullinan-Oncology-Announces-U-S-FDA-Clearance-of-Investigational-New-Drug-Application-for-CLN-617-a-Novel-Fusion-Protein-Harnessing-IL-2-and-IL-12-Cytokines.html[2] Ocugen Announces FDA Approval for Enrollment of Pediatric Patients in Ongoing OCU400 Phase 1/2 Clinical Trial for the Treatment of Retinitis Pigmentosa (RP) and Leber Congenital Amaurosis (LCA). Retrieved April 1, 2023, from https://www.globenewswire.com/news-release/2023/03/27/2634720/0/en/Ocugen-Announces-FDA-Approval-for-Enrollment-of-Pediatric-Patients-in-Ongoing-OCU400-Phase-1-2-Clinical-Trial-for-the-Treatment-of-Retinitis-Pigmentosa-RP-and-Leber-Congenital-Amau.html[3] MaaT Pharma Receives Two Clinical Trial Application Authorizations to Evaluate MaaT033 in Two Therapeutic Indications in Europe. Retrieved April 1, 2023, from https://www.businesswire.com/news/home/20230327005480/en[4] OliX Pharmaceuticals Doses First Patient in Clinical Trial for RNAi Therapeutic OLX10212 for Dry and Wet Age-related Macular Degeneration. Retrieved April 1, 2023, from https://www.businesswire.com/news/home/20230327005291/en/[5] Agenus’ Botensilimab in Combination with Balstilimab Shows 33% Durable Responses in Ovarian Cancer. Retrieved April 1, 2023, from https://www.businesswire.com/news/home/20230327005068/en/[6] Zealand Pharma Announces Positive Phase 1 Clinical Results with Amylin Analogue ZP8396. Retrieved April 1, 2023, from https://www.globenewswire.com/news-release/2023/03/28/2635429/0/en/Zealand-Pharma-Announces-Positive-Phase-1-Clinical-Results-with-Amylin-Analogue-ZP8396.html[7] Direct Biologics Announces First Patient Dosed with ExoFlo™ in a Phase 1 Clinical Trial for Medically Refractory Ulcerative Colitis. Retrieved April 1, 2023, from https://www.businesswire.com/news/home/20230328005543/en/[8] Grey Wolf Therapeutics Announces Dosing of First Patient in Phase 1/2 Clinical Study of GRWD5769 in Patients with Advanced Solid Tumours. Retrieved April 1, 2023, from https://greywolftherapeutics.com/grey-wolf-therapeutics-announces-dosing-of-first-patient-in-phase-1-2-clinical-study-of-grwd5769-in-patients-with-advanced-solid-tumours/[9] Eloxx Pharmaceuticals Announces Submission of Investigational New Drug (IND) Application for ZKN-013. Retrieved April 1, 2023, from https://investors.eloxxpharma.com/news-releases/news-release-details/eloxx-pharmaceuticals-announces-submission-investigational-new[10] Precigen Announces Further Advancement of UltraCAR-T® Platform with First Patient Dosed in Phase 1/1b Dose Escalation/Dose Expansion Study of PRGN-3007 in Advanced ROR1+ Hematological and Solid Tumors. Retrieved April 1, 2023, from https://www.prnewswire.com/news-releases/precigen-announces-further-advancement-of-ultracar-t-platform-with-first-patient-dosed-in-phase-11b-dose-escalationdose-expansion-study-of-prgn-3007-in-advanced-ror1-hematological-and-solid-tumors-301784205.html[11] Vaccitech Announces Positive Topline Final Data for HBV002 Study in People with Chronic Hepatitis B. Retrieved April 1, 2023, from https://investors.vaccitech.co.uk/news-and-events/news-releases/news-release-details/vaccitech-announces-positive-topline-final-data[12] PathoVax's Licensed HPV Vaccine Receives FDA Clearance of HPV16 RG1-VLP Investigational New Drug Application. Retrieved April 1, 2023, from https://www.prnewswire.com/news-releases/pathovaxs-licensed-hpv-vaccine-receives-fda-clearance-of-hpv16-rg1-vlp-investigational-new-drug-application-301783805.html[13] DxVx Co., Ltd.'s affiliated company, Oxford Vacmedix (OVM) successfully completed Phase 1a in clinical trial of novel cancer vaccine OVM-200. Retrieved April 1, 2023, from https://www.prnewswire.com/news-releases/dxvx-co-ltds-affiliated-company-oxford-vacmedix-ovm-successfully-completed-phase-1a-in-clinical-trial-of-novel-cancer-vaccine-ovm-200-301785682.html[14] AFFIMED ANNOUNCES FIRST PATIENT SUCCESSFULLY DOSED IN THE FIRST-IN-HUMAN STUDY OF AFM28 FOR THE TREATMENT OF PATIENTS WITH RELAPSED / REFRACTORY CD123-POSITIVE ACUTE MYELOID LEUKEMIA. Retrieved April 1, 2023, from https://www.affimed.com/affimed-announces-first-patient-successfully-dosed-in-the-first-in-human-study-of-afm28-for-the-treatment-of-patients-with-relapsed-refractory-cd123-positive-acute-myeloid-leukemia/[15] Athos Therapeutics Receives Regulatory Approval to Commence Phase I Clinical Trial of ATH-063. Retrieved April 1, 2023, from https://www.prnewswire.com/news-releases/athos-therapeutics-receives-regulatory-approval-to-commence-phase-i-clinical-trial-of-ath-063-301785047.html[16] Bolt Biotherapeutics Announces Positive Topline Data from BDC-1001 Phase 1 Dose-Escalation Trial in HER2-Expressing Tumors, Supporting Advancement to Phase 2 Clinical Studies. Retrieved April 1, 2023, from https://investors.boltbio.com/news-releases/news-release-details/bolt-biotherapeutics-announces-positive-topline-data-bdc-1001[17] New data presented at AD/PD™2023 show IONIS-MAPT Rx (BIIB080) substantially reduced tau protein in patients with early-stage Alzheimer's disease. Retrieved April 1, 2023, from https://ir.ionispharma.com/news-releases/news-release-details/new-data-presented-adpdtm2023-show-ionis-mapt-rx-biib080[18] Aligos Therapeutics Presents Clinical Data from NASH Program at the 2023 Paris Hepatology Conference. Retrieved April 1, 2023, from https://investor.aligos.com/news-releases/news-release-details/aligos-therapeutics-presents-clinical-data-nash-program-2023[19] Comanche Biopharma Announces FDA Clearance of Investigational New Drug (IND) Application for CBP-4888, an siRNA Investigational Therapy for the Treatment of Preeclampsia. Retrieved April 1, 2023, from https://www.prnewswire.com/news-releases/comanche-biopharma-announces-fda-clearance-of-investigational-new-drug-ind-application-for-cbp-4888-an-sirna-investigational-therapy-for-the-treatment-of-preeclampsia-301784873.html[20] VYNE Therapeutics Announces Positive First-In-Human Pharmacokinetic and Hematology Data from Phase 1a Single and Multiple Ascending Dose Trial for Novel Pan-Bromodomain BET Inhibitor VYN201. Retrieved April 1, 2023, from https://www.globenewswire.com/news-release/2023/03/30/2637550/0/en/VYNE-Therapeutics-Announces-Positive-First-In-Human-Pharmacokinetic-and-Hematology-Data-from-Phase-1a-Single-and-Multiple-Ascending-Dose-Trial-for-Novel-Pan-Bromodomain-BET-Inhibit.html[21] Medicenna Provides Clinical Update from Monotherapy Dose Escalation Portion of Phase 1/2 ABILITY Study. Retrieved April 1, 2023, from https://ir.medicenna.com/news-releases/news-release-details/medicenna-provides-clinical-update-monotherapy-dose-escalation免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。版权说明:本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「药明康德」微信公众号回复“转载”,获取转载须知。分享,点赞,在看,聚焦全球生物医药健康创新
临床结果临床2期免疫疗法寡核苷酸
2023-03-31
FDA approves RGVax's (HPV16 RG1-VLP) IND for Phase 1 clinical trials.
PathoVax LLC ("PathoVax"), a biotech company focused on developing a universally preventative Human Papillomavirus (HPV) vaccine - "RGVax", today announced that the U.S. Food and Drug Administration (FDA) has completed its review of the investigational new drug (IND) application for its licensed monovalent component- HPV16 RG1-VLP and concluded that a Phase 1 clinical trial in the United States and Austria is now given the go-ahead to proceed.
This Phase 1, first-in-human, global multicenter clinical study seeks to demonstrate the safety and immunogenicity responses to HPV16 RG1-VLP in healthy volunteers. The underlying RGVax foundational technology was licensed from Johns Hopkins University and the subsequent GMP as well as Phase 1 development of this vaccine was supported by the NCI PREVENT cancer program.
"The world needs more, and particularly broad-based, HPV vaccines. We are excited that our collaborators have been able to move forward with the clinical development of HPV16 RG1-VLP. This clinical proof of concept will demonstrate the potential it holds for positively impacting the lives of many individuals at risk of HPV infection and diseases. We look forward to globally supporting these efforts in parallel and beyond this Phase 1 especially in Asia-Pacific and other developing countries too where there is a high burden of HPV diseases," said Dr Kevin Koh, Chairman of PathoVax.
PathoVax was co-founded to licensed and developed a game changing preventative universal HPV vaccine. The foundational technology (RGVax technology) is based off vaccine scientific research at the Johns Hopkins University and Medical University Vienna. Unlike existing HPV vaccines that do not target all HPV types, the RGVax technology and formulation has been shown to provide comprehensive protection against at least 18 high risk HPV types with immunogenicity lasting over a year without additional boosts in head-to-head studies with existing approved HPV vaccines.
This leapfrogs current vaccines as multiple diseases are now linked to HPV infection. It is anticipated that such additional protection will eventually establish new standards of care for many patients.
Dr Joshua Wang, a co-founder of PathoVax LLC said the following "Securing FDA clearance to start clinical trials is a significant achievement. This could not have been possible without the ongoing academic-industry collaborations that have occurred since day one between PathoVax LLC, Johns Hopkins and the National Cancer Institute's PREVENT program."
About PathoVax LLC:
PathoVax LLC, is a start-up company that is based on foundational technology developed at Johns Hopkins University to advance RGVaxTM, the world's first comprehensive HPV vaccine that aims to target all clinically relevant HPV. It is expected that such additional protection will eventually establish new standards in the $2B HPV market. PathoVax's collaborative partnerships include well-known institutions such as the U.S. National Cancer Institute to push forward an academic phase 1 study. For more information, visit: www.pathovax.com
SOURCE PathoVax
疫苗临床申请
2023-03-29
FDA approves RGVax's (HPV16 RG1-VLP) IND for Phase 1 clinical trials.
BALTIMORE, March 29, 2023 /PRNewswire/ -- PathoVax LLC ("PathoVax"), a biotech company focused on developing a universally preventative Human Papillomavirus (HPV) vaccine - "RGVax", today announced that the U.S. Food and Drug Administration (FDA) has completed its review of the investigational new drug (IND) application for its licensed monovalent component- HPV16 RG1-VLP and concluded that a Phase 1 clinical trial in the United States and Austria is now given the go-ahead to proceed.
This Phase 1, first-in-human, global multicenter clinical study seeks to demonstrate the safety and immunogenicity responses to HPV16 RG1-VLP in healthy volunteers. The underlying RGVax foundational technology was licensed from Johns Hopkins University and the subsequent GMP as well as Phase 1 development of this vaccine was supported by the NCI PREVENT cancer program.
"The world needs more, and particularly broad-based, HPV vaccines. We are excited that our collaborators have been able to move forward with the clinical development of HPV16 RG1-VLP. This clinical proof of concept will demonstrate the potential it holds for positively impacting the lives of many individuals at risk of HPV infection and diseases. We look forward to globally supporting these efforts in parallel and beyond this Phase 1 especially in Asia-Pacific and other developing countries too where there is a high burden of HPV diseases," said Dr Kevin Koh, Chairman of PathoVax.
PathoVax was co-founded to licensed and developed a game changing preventative universal HPV vaccine. The foundational technology (RGVax technology) is based off vaccine scientific research at the Johns Hopkins University and Medical University Vienna. Unlike existing HPV vaccines that do not target all HPV types, the RGVax technology and formulation has been shown to provide comprehensive protection against at least 18 high risk HPV types with immunogenicity lasting over a year without additional boosts in head-to-head studies with existing approved HPV vaccines. This leapfrogs current vaccines as multiple diseases are now linked to HPV infection. It is anticipated that such additional protection will eventually establish new standards of care for many patients.
Dr Joshua Wang, a co-founder of PathoVax LLC said the following "Securing FDA clearance to start clinical trials is a significant achievement. This could not have been possible without the ongoing academic-industry collaborations that have occurred since day one between PathoVax LLC, Johns Hopkins and the National Cancer Institute's PREVENT program."
About PathoVax LLC:
PathoVax LLC, is a start-up company that is based on foundational technology developed at Johns Hopkins University to advance RGVaxTM, the world's first comprehensive HPV vaccine that aims to target all clinically relevant HPV. It is expected that such additional protection will eventually establish new standards in the $2B HPV market. PathoVax's collaborative partnerships include well-known institutions such as the U.S. National Cancer Institute to push forward an academic phase 1 study. For more information, visit:
Forward-Looking Statements
Any statements in this release that are not historical facts may be considered to be "forward-looking statements." Forward-looking statements are based on management's current expectations and are subject to risks and uncertainties which may cause results to differ materially and adversely from the statements contained herein. Such statements include, but are not limited to, statements regarding the market opportunity for PathoVax's product candidates; and the business strategies and development plans of PathoVax. Some of the potential risks and uncertainties that could cause actual results to differ from those expected include Pathovax's ability to: make commercially available its products and technologies in a timely manner or at all; enter into other strategic alliances, including arrangements for the development and distribution of its products; obtain intellectual property protection for its assets; accurately estimate its expenses and cash burn and raise additional funds when necessary. Undue reliance should not be placed on forward-looking statements, which speak only as of the date they are made. Except as required by law, Pathovax does not undertake any obligation to update any forward-looking statements to reflect new information, events or circumstances after the date they are made, or to reflect the occurrence of unanticipated events.
CONTACT: info@pathovax.com
疫苗临床1期临床申请
100 项与 RG1-VLP 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| HPV16感染 | 临床申请 | 美国 | PathoVax LLC初创企业 | 2023-03-29 |
| HPV16感染 | 临床申请 | 奥地利 | PathoVax LLC初创企业 | 2023-03-29 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
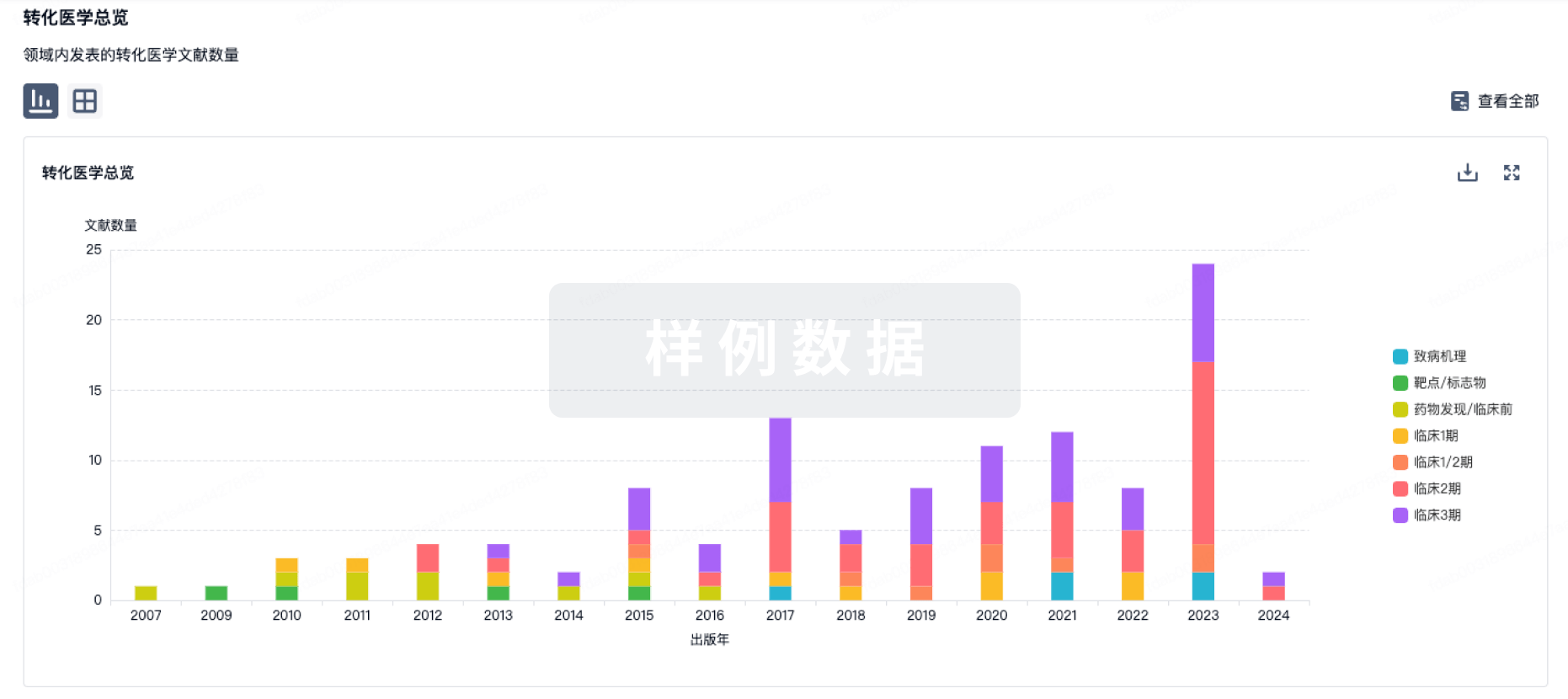
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
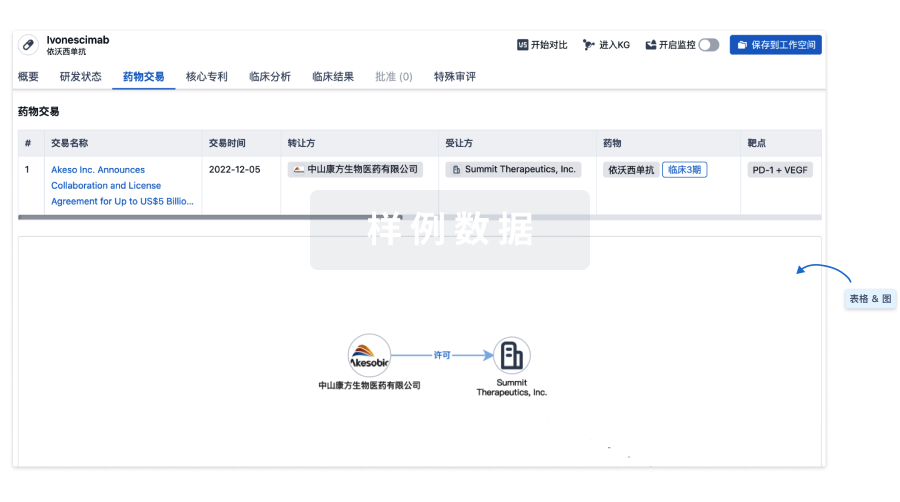
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
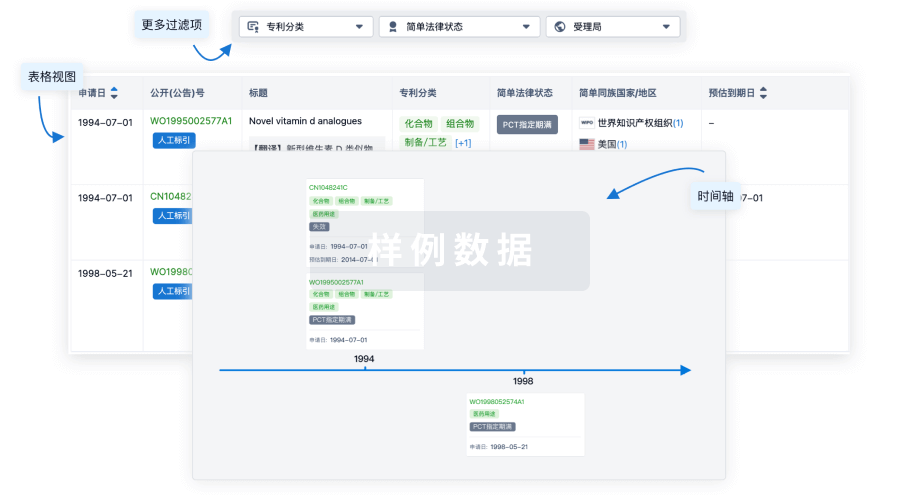
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
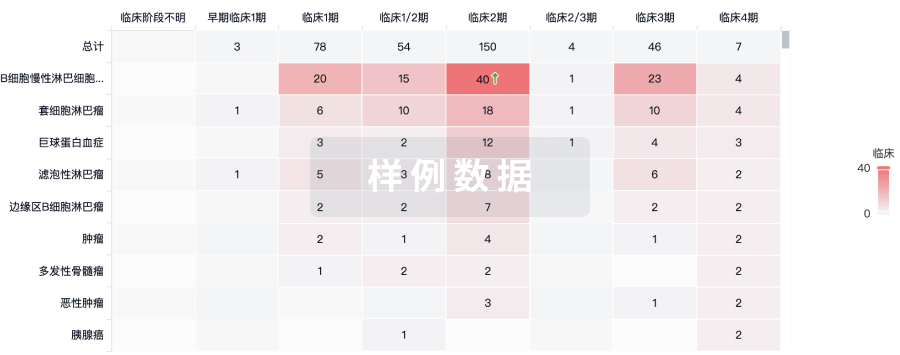
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
批准
利用最新的监管批准信息加速您的研究。
登录
或
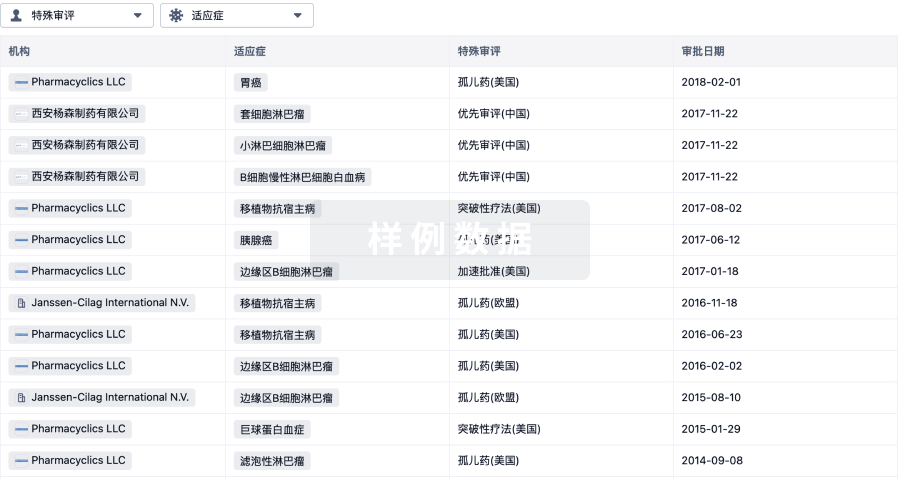
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
