预约演示
更新于:2025-06-12
BPR-30221616
更新于:2025-06-12
概要
基本信息
原研机构 |
在研机构 |
非在研机构- |
权益机构- |
最高研发阶段临床1期 |
首次获批日期- |
最高研发阶段(中国)临床1期 |
特殊审评孤儿药 (美国) |
登录后查看时间轴
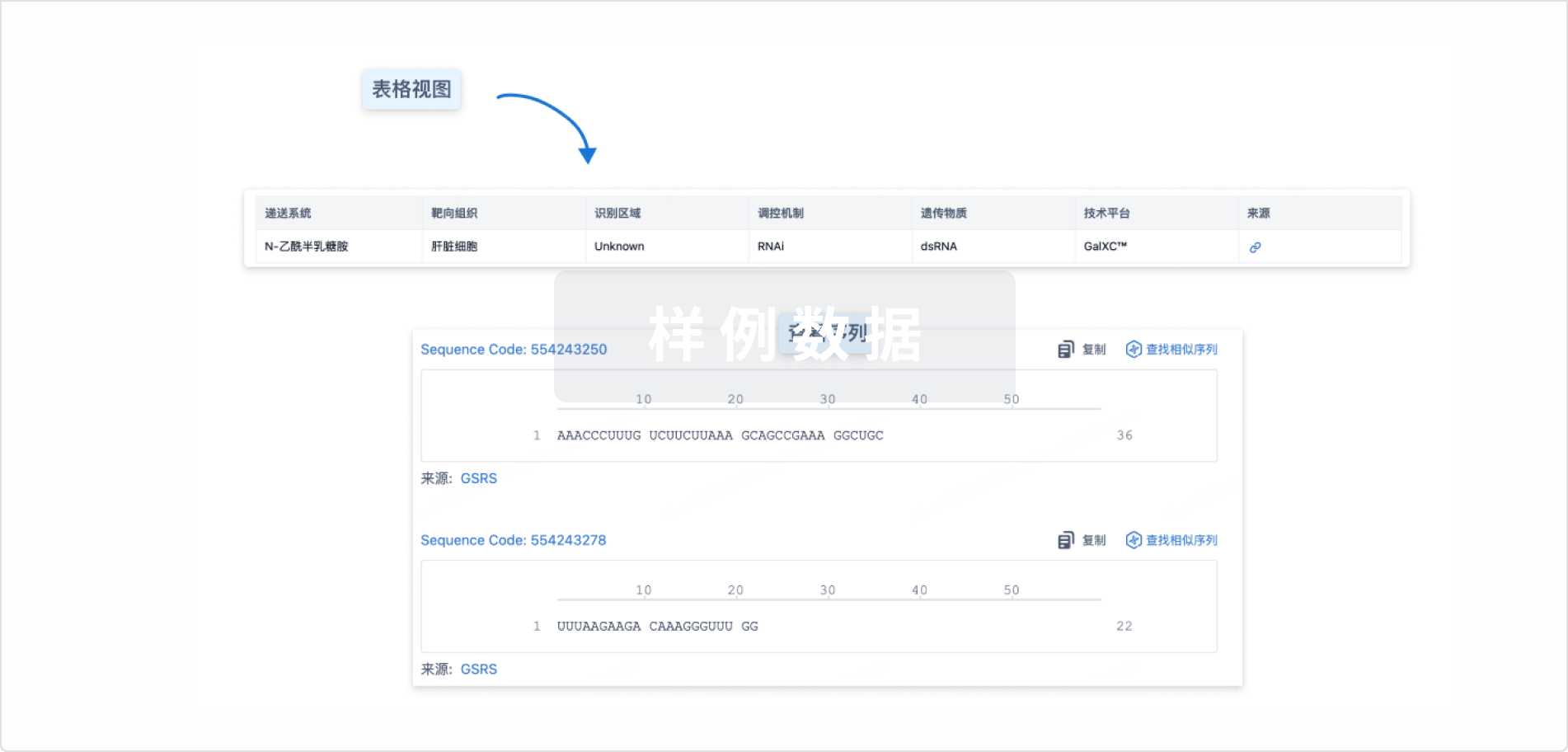
结构/序列
使用我们的RNA技术数据为新药研发加速。
登录
或
关联
1
项与 BPR-30221616 相关的临床试验NCT06760455
A Single-center, Double-blind, Placebo-controlled, Dose-escalation Phase I Clinical Study to Evaluate the Safety and Tolerability of BPR-30221616 Injection in Healthy Subjects
The purpose of this study is to determine the safety, tolerability, pharmacokinetics、 pharmacodynamics and immunogenicity of BPR-30221616 in healthy subjects.
开始日期2025-01-10 |
申办/合作机构 |
100 项与 BPR-30221616 相关的临床结果
登录后查看更多信息
100 项与 BPR-30221616 相关的转化医学
登录后查看更多信息
100 项与 BPR-30221616 相关的专利(医药)
登录后查看更多信息
10
项与 BPR-30221616 相关的新闻(医药)2025-06-05
·米内网
精彩内容6月4日,国家药监局官网显示,倍特药业拿下了伏立康唑干混悬剂和门冬氨酸钾注射液,今年以来公司已累计获批了14个新产品、4款1类新药获批临床,公司的创新转型之路越走越顺。2024年在中国三大终端六大市场,倍特药业首次登上全身用抗细菌化药国内龙头集团,18个产品大卖超过1亿元,成绩亮眼。目前,公司已过评产品超过150个,还有73个仿制药新品报产在审;1款改良新药已获批,20款新药在路上,未来可期。首夺千亿市场国内龙头,18个过亿产品超亮眼据米内网统计,截至目前倍特药业(含子公司)已拥有化学药和中成药合计超过350个产品(不含原料药),2024年在中国三大终端六大市场(统计范围见文末),公司的畅销产品分布在50多个亚类市场,并已成功挺进12个亚类市场TOP20集团(二级,下同)之列,优势明显。2024年全身用抗细菌化药的销售规模在1093亿元左右。倍特药业近几年不断加码抢攻这个千亿市场,从2019年的TOP44集团一路飞升,并在2024年成功登上TOP2集团之位,排在辉瑞之后,成为该市场的新国内龙头集团。倍特药业的注射用氨苄西林钠、注射用阿莫西林钠克拉维酸钾(5:1)、注射用哌拉西林钠、头孢克肟分散片2024年在中国三大终端六大市场的销售额均超过3亿元,此外还有7个产品达到了亿元级别。图1:倍特药业的全身用抗细菌化药销售额及市场份额(二级集团)情况(单位:万元)来源:米内网格局数据库2024年阻塞性气管疾病用药(化+生)的销售规模超过270亿元。倍特药业自2021年开始腾飞,连续增长了512%、118%、24%、23%,公司该类药物的销售额在2024年升至9.5亿元,并成功登上TOP7集团。公司在2021年获批的吸入用布地奈德混悬液,在2024年大卖超过6.5亿元。2024年其他妇科用药(化+生)的销售规模超过30亿元。倍特药业近几年持续正增长,2019-2021年稳坐TOP5集团,2022-2023年跃升至TOP2集团,2024年虽下滑了1位至TOP3集团,但市场份额却升至12.19%,为近六年新高。公司的马来酸麦角新碱注射液在2024年大卖近4亿元。2024年中成药糖尿病用药的销售规模超过20亿元。倍特药业2023-2024年的销售额保持在1亿元以上,集团排名稳定在TOP8。热销产品糖脉康颗粒、糖脉康片、糖脉康胶囊是公司的独家产品。2024年治疗用放射性药物(化+生)的销售规模在5.9亿元左右。倍特药业在2023年3月获批了氯化锶[89Sr]注射液(首家过评),该产品助力公司在2024年登上该类药物市场TOP8集团。此外,2024年倍特药业还是抗痛风制剂化药市场TOP12集团、皮肤病用抗生素和化疗药化药市场TOP14集团、造影剂(化+生)市场TOP14集团、治疗与胃酸分泌相关疾病的化药市场TOP15集团、全身用抗病毒药(化+生)市场TOP17集团、胃肠解痉药及抗胆碱药和胃动力药化药市场TOP17集团、全身用抗真菌化药市场TOP19集团。表1:2024年在中国三大终端六大市场倍特药业销售额过亿的产品情况来源:米内网格局数据库2024年在中国三大终端六大市场,倍特药业TOP20产品中有18个销售额超过1亿元,其中吸入用布地奈德混悬液已成为了公司最畅销的产品。公司的马来酸麦角新碱注射液、注射用氨苄西林钠、注射用哌拉西林钠、达比加群酯胶囊、注射用头孢美唑钠连续三年保持正增长态势,已成为了重要的潜力产品。改良新药先拔头筹,12款1类新药来势汹汹图2:2022年至今倍特药业申报上市的新药来源:米内网中国申报进度(MED)数据库2024年4月,化药2.2类新药盐酸右美托咪定鼻喷雾剂获批上市,为倍特药业的创新药研发揭开了新篇章。目前公司还有水合氯醛糖浆报产在审,该产品也是一款改良新药,预计将在今年迎来好消息。2025年至今1-5月,倍特药业有4款新药获批临床,其中化药1类新药PRT-064040鼻喷雾剂和生物药1类新药BPR-102胶囊为首次申报临床并获批,化药1类新药BPR-30221616注射液和生物药1类新药HC006注射液为新适应症获批临床。4月,公司提交了化药1类新药SNH-119014片的临床申请,目前正在审评审批中……近几年,倍特药业的1类新药矩阵不断壮大,已累计布局了12款1类新药(化+生)。表2:倍特药业部分在研的重磅新药来源:米内网综合数据库8款1类新药已进入临床阶段,其中生物药1类新药BPR-101胶囊在2024年9月启动了细菌性阴道病II期临床,是目前公司研发进度最快的1类新药;化药1类新药BPR-30221616注射液在2024年12月启动了转甲状腺素蛋白淀粉样变性心肌病(ATTR-CM)I期临床,并在2025年1月完成了第一例入组。公司继续加码改良新药,盐酸(R)-氯胺酮鼻喷雾剂在今年4月启动了伴有急性自杀意念或行为的抑郁症II期临床;卡托普利口服溶液在2023年9月完成了I期临床;吸入用PRT-068已获得临床批件,还有3款新药的临床申请正在审评审批中。倍特药业目前暂无生物药获批上市,司美格鲁肽注射液的两个适应症分别在2024年3月、9月进入III期临床,离报产仅一步之遥,该产品有望成为公司首款获批的生物药。73个高端仿制药在路上,153个产品已过评6月4日,国家药监局发布最新药品获批信息,倍特药业拿下伏立康唑干混悬剂和门冬氨酸钾注射液,今年以来公司已累计获批了14个新产品,其中巴氯芬口服溶液、沙美特罗替卡松吸入粉雾剂、卡络磺钠片均为国产第二家获批,公司的抢仿实力不容小觑。表3:倍特药业今年以来获批的新产品来源:米内网中国申报进度(MED)数据库开拓新市场方面,早前倍特药业暂无肌肉松弛药和其它所有治疗用药品获批,巴氯芬口服溶液和硫代硫酸钠注射液为公司打开了两个新市场大门,2024年在中国三大终端六大市场,肌肉松弛药(化+生)的销售规模超过了40亿元,其它所有治疗用药品(化+生)的销售规模达到了68亿元。2023年至今,倍特药业及子公司还有73个高端化学药报产在审。螺内酯口服混悬液目前暂未有进口或国产产品获批,佩玛贝特片和阿糖胞苷注射液仅有原研批文,复方氨基酸注射液(17AA-Ⅲ)目前有原研地产化产品获批,倍特药业将参与上述产品的国内首仿争夺。此外,公司或将再有5个亚类市场迎来新突破。阿帕他胺片和枸橼酸托瑞米芬片将为公司开拓内分泌治疗用药市场,碘[131I]化钠口服溶液或将成为公司首个诊断用放射性药物,注射用吲哚菁绿或将成为公司首个诊断用药,唑来膦酸注射液或将成为公司首个影响骨结构及其矿化的药物,黄体酮注射液或将成为公司首个性激素及生殖系统调节剂。图3:倍特药业集采中标产品情况来源:米内网中国上市药品(MID)数据库截至2025年6月4日,倍特药业及子公司已过评/视同过评的产品有153个(按产品名统计),公司积极参与国家集中带量采购,前十批(除了第六批胰岛素专项)均有产品中标,“集采中标大户”实至名归。表4:倍特药业备战第十一批集采的产品来源:米内网中国上市药品(MID)数据库目前,倍特药业已过评且竞争企业在7家或以上的产品有39个,其中口服占了18个、注射占了19个,吸入占了2个。2025上半年仅剩最后一个月,行业大事备受瞩目,“集采中标大户”能否再接再厉,我们将继续跟踪报道,敬请关注。资料来源:米内网数据库、国家药监局官网注:米内网《中国三大终端六大市场药品竞争格局》,统计范围是:城市公立医院和县级公立医院、城市社区中心和乡镇卫生院、城市实体药店和网上药店,不含民营医院、私人诊所、村卫生室,不含县乡村药店;上述销售额以产品在终端的平均零售价计算。数据统计截至6月4日,如有疏漏,欢迎指正!免责声明:本文仅作医药信息传播分享,并不构成投资或决策建议。本文为原创稿件,转载文章或引用数据请注明来源和作者,否则将追究侵权责任。投稿及报料请发邮件到872470254@qq.com稿件要求详询米内微信首页菜单栏商务及内容合作可联系QQ:412539092【分享、点赞、在看】点一点不失联哦
放射疗法上市批准
2025-05-23
近日,CDE官网显示,倍特药业(含子公司)申报的2款1类新药获得临床试验默示许可,分别为治疗绝经后萎缩性阴道炎的BPR-102胶囊,以及用于成人有或无先兆偏头痛急性治疗的PRT-064040鼻喷雾剂。米内网数据显示,按平均零售价计,2023年中国公立医疗机构终端(院内市场)创新药销售额约2000亿元,预计2029年院内市场创新药(专利期内)市场规模将超过4500亿元。
BPR-102胶囊是一款生物药1类新药,其临床申请于2025年3月获得CDE承办受理,并于近日获批临床,用于治疗绝经后萎缩性阴道炎。在妇科抗感染领域,倍特药业还有另一款1类新药正在开展II期临床,为BPR-101胶囊,这是一种针对细菌性阴道病(BV)的新型治疗药物,通过调节阴道微生态环境,抑制有害菌群的过度生长,从而恢复阴道的正常菌群平衡。
米内网数据显示,2024年中国三大终端六大市场(统计范围详见本文末)妇科抗感染药和抗菌剂(不含中成药)销售额超过38亿元,同比增长约3%。产品排名中,克霉唑阴道片以近7亿元排在首位,硝呋太尔制霉素阴道软胶囊以超3亿元紧接其后。
近年来中国三大终端六大市场妇科抗感染药和抗菌剂(不含中成药)销售情况(单位:万元)
来源:米内网格局数据库
PRT-064040鼻喷雾剂是一款化药1类新药,其临床申请于2025年3月获得CDE承办受理,并于近日获批临床,拟用于成人有或无先兆偏头痛的急性治疗。在神经系统领域,倍特药业开发的2类改良型新药水合氯醛糖浆(用于镇静催眠)已于2024年4月提交上市申请,目前还在审评审批中。
米内网数据显示,近年来中国三大终端六大市场(统计范围详见本文末)神经系统药物(不含中成药)销售额均超过1000亿元,其中止痛药、精神安定药近年来销售占比均超过17%、14%。
近年来中国三大终端六大市场妇神经系统药物(不含中成药)销售情况(单位:万元)
来源:米内网格局数据库
近年来,倍特药业以创新为发展的新引擎,加速布局新药开发,创新药、改良型新药、生物类似药齐头并进。今年以来,公司有4款1类新药获批临床,涉及神经系统药物、抗肿瘤和免疫调节剂等治疗领域。
2025年以来倍特药业获批临床的1类新药
来源:米内网中国申报进度(MED)数据库
值得一提的是,BPR-30221616注射液是中国首个且全球第二款针对转甲状腺素蛋白(ATTR)靶点的siRNA药物,同时也是倍特药业在小核酸药物研发领域的重大突破。其首个适应症于2024年底获批临床,用于治疗转甲状腺素蛋白淀粉样变性心肌病(ATTR-CM),目前已处于I期临床。(本文转自米内网)
siRNA临床申请临床1期
2025-05-20
·米内网
精彩内容近日,CDE官网显示,倍特药业(含子公司)申报的2款1类新药获得临床试验默示许可,分别为治疗绝经后萎缩性阴道炎的BPR-102胶囊,以及用于成人有或无先兆偏头痛急性治疗的PRT-064040鼻喷雾剂。米内网数据显示,按平均零售价计,2023年中国公立医疗机构终端(院内市场)创新药销售额约2000亿元,预计2029年院内市场创新药(专利期内)市场规模将超过4500亿元。BPR-102胶囊是一款生物药1类新药,其临床申请于2025年3月获得CDE承办受理,并于近日获批临床,用于治疗绝经后萎缩性阴道炎。在妇科抗感染领域,倍特药业还有另一款1类新药正在开展II期临床,为BPR-101胶囊,这是一种针对细菌性阴道病(BV)的新型治疗药物,通过调节阴道微生态环境,抑制有害菌群的过度生长,从而恢复阴道的正常菌群平衡。米内网数据显示,2024年中国三大终端六大市场(统计范围详见本文末)妇科抗感染药和抗菌剂(不含中成药)销售额超过38亿元,同比增长约3%。产品排名中,克霉唑阴道片以近7亿元排在首位,硝呋太尔制霉素阴道软胶囊以超3亿元紧接其后。近年来中国三大终端六大市场妇科抗感染药和抗菌剂(不含中成药)销售情况(单位:万元)来源:米内网格局数据库PRT-064040鼻喷雾剂是一款化药1类新药,其临床申请于2025年3月获得CDE承办受理,并于近日获批临床,拟用于成人有或无先兆偏头痛的急性治疗。在神经系统领域,倍特药业开发的2类改良型新药水合氯醛糖浆(用于镇静催眠)已于2024年4月提交上市申请,目前还在审评审批中。米内网数据显示,近年来中国三大终端六大市场(统计范围详见本文末)神经系统药物(不含中成药)销售额均超过1000亿元,其中止痛药、精神安定药近年来销售占比均超过17%、14%。近年来中国三大终端六大市场妇神经系统药物(不含中成药)销售情况(单位:万元)来源:米内网格局数据库近年来,倍特药业以创新为发展的新引擎,加速布局新药开发,创新药、改良型新药、生物类似药齐头并进。今年以来,公司有4款1类新药获批临床,涉及神经系统药物、抗肿瘤和免疫调节剂等治疗领域。2025年以来倍特药业获批临床的1类新药来源:米内网中国申报进度(MED)数据库值得一提的是,BPR-30221616注射液是中国首个且全球第二款针对转甲状腺素蛋白(ATTR)靶点的siRNA药物,同时也是倍特药业在小核酸药物研发领域的重大突破。其首个适应症于2024年底获批临床,用于治疗转甲状腺素蛋白淀粉样变性心肌病(ATTR-CM),目前已处于I期临床。资料来源:米内网数据库、CDE官网等注:米内网《中国三大终端六大市场药品竞争格局》,统计范围是:城市公立医院和县级公立医院、城市社区中心和乡镇卫生院、城市实体药店和网上药店,不含民营医院、私人诊所、村卫生室,不含县乡村药店;上述销售额以产品在终端的平均零售价计算。数据统计截至5月20日,如有疏漏,欢迎指正!免责声明:本文仅作医药信息传播分享,并不构成投资或决策建议。本文为原创稿件,转载文章或引用数据请注明来源和作者,否则将追究侵权责任。投稿及报料请发邮件到872470254@qq.com稿件要求详询米内微信首页菜单栏商务及内容合作可联系QQ:412539092【分享、点赞、在看】点一点不失联哦
siRNA临床申请临床1期
100 项与 BPR-30221616 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 转甲状腺素蛋白淀粉样变性心肌病 | 临床1期 | 中国 | 2025-01-10 | |
| 家族性淀粉样神经病 | 临床申请批准 | 中国 | 2024-12-31 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

特殊审评
只需点击几下即可了解关键药物信息。
登录
或

Eureka LS:
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
