预约演示
更新于:2025-06-21
CIM-053
更新于:2025-06-21
概要
基本信息
非在研机构- |
权益机构- |
最高研发阶段临床前 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
结构/序列
使用我们的ADC技术数据为新药研发加速。
登录
或

关联
100 项与 CIM-053 相关的临床结果
登录后查看更多信息
100 项与 CIM-053 相关的转化医学
登录后查看更多信息
100 项与 CIM-053 相关的专利(医药)
登录后查看更多信息
2
项与 CIM-053 相关的新闻(医药)2024-06-18
·生物探索
引言
造血干细胞移植(HSCT)是治疗多种血液系统恶性肿瘤的主要方法。然而,目前的治疗标准仍然依赖于非靶向化疗,使恶性细胞的清除变得困难【1】。最近,靶向性的药物模式如抗体-药物偶联物(ADC)或嵌合抗原受体(CAR)-T细胞的发展为这一问题带来了希望,因为它们可以特异性地消除造血干细胞(HSC)和肿瘤细胞【2】。但是,肿瘤细胞和健康细胞(如造血干细胞或T细胞)共有抗原的表达增加了治疗的毒性风险【3】,并使靶标选择变得更加复杂。
近日,来自瑞士巴塞尔大学生物医学部的Lukas T. Jeker团队在Nature期刊发表题为Selective haematological cancer eradication with preserved haematopoiesis(保留造血功能的选择性血液系统癌症的根除)的文章。研究表明,靶向CD45的ADC药物与工程化的造血干细胞移植(HSCT)技术相结合,能够选择性地清除全身造血系统中的白血病细胞,同时保留造血功能。这项研究为治疗血液系统恶性疾病提供了一种新的策略,具有广泛的应用潜力。
研究人员假设,一个理想的治疗靶点应该在所有造血细胞中广泛表达,包括造血干细胞和祖细胞(HSPCs)、白血病干细胞以及分化细胞。酪氨酸磷酸酶CD45只在造血细胞中表达,因此成为了全血液系统的一个标志物。通过工程化CD45,使其对靶向CD45的ADC产生抗性,同时保持HSCs功能的治疗策略,可为术后靶向治疗提供新途径。
CD45表位的工程化
首先,研究人员通过对CD45细胞外区域(ECD)的计算分析,确定了适合抗原表位工程化的区域,重点关注了非保守的D1和D2结构域,排除了可能发生翻译后修饰的残基,并评估了表面可及性、表位概率和残基进化保守性。最终他们确认了D1-1、D2-1和D2-2区域是可以耐受突变而不损害CD45结构或功能完整性的理想位点。随后,通过丙氨酸扫描,研究人员鉴定了影响三种单克隆抗体(BC8、HI30和MIRG451)结合的特定残基,并对候选残基的结构定位、空间接近度和溶剂暴露度进行分析。通过碱基编辑器(BEs)技术,研究人员评估了在D1-1、D2-1和D2-2中产生抗体可识别的氨基酸取代的可行性。最终,他们选择了CD45E259和CD45N286(都是BC8抗体)和CD45K352 (MIRG451抗体)进行后续实验。接下来,研究人员对CD45 屏蔽变体进行了研究,重点关注它们与 BC8 和 MIRG451 的结合能力以及生物物理性质的分析。通过流式细胞术和生物层析干涉术,他们发现 CD45H285R 和 CD45N286D 显著影响BC8 和 MIRG451 的结合,而CD45N286D 和 CD45K352E 显示出最好的生物物理特性。为了调查原代细胞中BE介导的细胞保护,研究人员利用电穿孔的人T细胞进行细胞保护研究,并通过调整编辑工具提高特定基因变体的编辑效率。研究发现,使用特定编辑组合成功保护了约50%的HSPC细胞,这些受保护的细胞在功能上与对照组相似,表明其功能完整。具体来说,通过使用ABE8e-SpRY mRNA和sgRNA-49.3的编辑组合,成功实现了对CD45K352E和CD45K352G的编辑,它们可以屏蔽靶向CD45的ADC药物的作用而不会被杀伤。研究人员将这些编辑后的HSPCs命名为sg49.3HSPCs,它们显示出与对照组(sgNTCHSPCs)相似的集落形成能力和细胞分化潜能。
靶向CD45的ADC药物开发
接下来,研究人员通过体内实验优化靶向人源化CD45的ADC药物细胞毒性。通过MIRG451 单克隆抗体的人源化和工程化,他们得到了CIM053,并将其与吡咯并苯二氮卓(PBD)二聚体载体SG3376共轭连接,形成ADC药物CIM053-SG3376。这种ADC药物能够选择性地杀死肿瘤细胞,而保留编辑的HSPCs。研究表明CD45是一个广泛适用的靶点,CIM053-SG3376能够有效清除表达CD45的细胞,在癌症治疗中具有潜在的临床意义。随后,研究人员利用NBSGW小鼠模型分析了移植HSPCs的分化潜能及其对ADC细胞毒性的屏蔽作用。他们将sgNTCHSPCs或sg49.3HSPCs注射到小鼠体内,并经CIM053-SG3376处理后发现,sg49.3HSPCs完全屏蔽了CIM053-SG3376的作用,成功保留了人源HSPCs。ADC处理后,sg49.3HSPCs组显示出多谱系分化潜能,而sgNTCHSPCs组中所有类型的细胞都被清除。连续移植实验结果表明,受保护的sg49.3HSPCs具有持久的重建潜能和和长期的ADC屏蔽效果。ADC处理消除了所有CD45WT细胞,但可以使编辑细胞完全富集。此外,研究人员还探索了潜在的脱靶编辑位点,结果显示,这些位点在所有样本中并不常见。这些结果表明sg49.3HSPCs允许正常HSC移植,并在不改变竞争适应性的情况下保持多谱系分化。脱靶分析表明采用高保真BEs、严格PAM或RNA-DNA混合向导RNA可以进一步改进靶向CD45的ADC治疗的安全性。ADC药物CIM053-SG3376可以有效清除体内造血细胞和肿瘤细胞,但sg49.3HSPCs及其后代成功地屏蔽了ADC的杀伤。
ADC药物用于血液肿瘤的治疗
研究人员对CIM053-SG3376在肿瘤治疗中的潜力进行了评估。通过小鼠模型,他们发现CIM053-SG3376能迅速消除多种肿瘤,包括AML和T细胞恶性肿瘤,并且在侵袭性AML模型中也表现出良好的效果。实验结果显示,在CIM053-SG3376处理后,肿瘤几乎完全消失,而且没有观察到明显的毒性反应。此外,ADC还能选择性地清除未受保护的非肿瘤人类细胞,但保留了受保护的造血系统细胞。这项研究揭示了CIM053-SG3376作为一种高效的靶向CD45 的ADC药物,将其与sg49.3HSPCs结合,在侵袭性AML模型中实现了肿瘤选择性免疫治疗,并保留了受保护造血系统的功能。这为免疫疗法,特别是是血液系统肿瘤的治疗,提供了新的可能性。最后,研究人员评估了AML样本中CD45的表达情况,并考察了CIM053-SG3376对患者来源的AML移植物的效力。结果显示,AML细胞中CD45表达丰富。将AML患者来源的异种移植物(PDX)移植到sgNTCHSPCs或sg49.3HSPCs小鼠中后,CIM053-SG3376治疗能够有效清除PDX细胞,同时保留受保护的造血细胞。这些结果证实了CIM053-SG3376治疗的选择性以及对AML细胞的清除效果。
综上所述,该研究开发了一种高效的靶向CD45的 ADC,并确定了一种碱基编辑器(BE)和向导RNA的组合,能够在体内为HSPC建立分子屏障,使其保持长期重建潜能。这项研究证明了ADC药物与HSCT技术相结合,可以有效清除血液系统中的癌细胞,而不影响编辑的HSCs的造血功能。
参考文献
1. Copelan, E. A. Hematopoietic stem-cell transplantation. N. Engl. J. Med. 354, 1813-1826 (2006).
2. Carter, P. J. & Rajpal, A. Designing antibodies as therapeutics. Cell 185, 2789-2805 (2022).
3. Perna, F. et al. Integrating proteomics and transcriptomics for systematic combinatorial chimeric antigen receptor therapy of AML. Cancer Cell 32, 506-519 (2017).
https://doi-org.libproxy1.nus.edu.sg/10.1038/s41586-024-07456-3
责编|探索君
排版|探索君
文章来源|“BioArt”
End
往期精选
围观
一文读透细胞死亡(Cell Death) | 24年Cell重磅综述(长文收藏版)
热文
Cell | 是什么决定了细胞的大小?
热文
Nature | 2024年值得关注的七项技术
热文
Nature | 自身免疫性疾病能被治愈吗?科学家们终于看到了希望
热文
CRISPR技术进化史 | 24年Cell综述
抗体药物偶联物细胞疗法免疫疗法
2023-12-12
Preclinical data for Cimeio’s CD45 universal heme ADC and shielded HSCs demonstrate effective depletion of an aggressive AML cell line in vivo
First data for Cimeio’s CD33 shielded HSCs show that cells are protected from antibody binding while maintaining CD33 receptor expression
BASEL, Switzerland & CAMBRIDGE, Mass.--(BUSINESS WIRE)-- Cimeio Therapeutics, the leading biotechnology company in the field of epitope shielding, presented data for its CD45 and CD33 programs during this weekend’s American Society of Hematology (ASH) meeting in San Diego. The two studies provide further evidence that epitope editing allows for the development of powerful immunotherapies that would not be safe to administer without first protecting healthy cells.
The first abstract, titled “Hematopoietic Stem Cells Expressing Engineered CD45 Enable a Near Universal Targeted Therapy for Hematologic Diseases,” demonstrated the efficacy of Cimeio’s proprietary CD45 targeting ADC (CIM053-ADC) at depleting an aggressive AML cancer cell line in vivo, while the CD45 engineered HSCs were fully protected, engrafted and reconstituted the hematopoietic system in humanized mice. After just two doses of CIM053-ADC, all mice were cancer-free while the healthy hematopoietic cells were unaffected. This study demonstrates the potential of CD45-targeted ADC therapy for patients with hematologic malignancies.
The second abstract, titled “Base Edited HSPCs Are Shielded From CD33 Therapy but Preserve CD33 Expression,” showed how Cimeio’s CD33 shielding variant effectively protected cells from a CD33 antibody, while maintaining CD33 expression. CD33 is a useful target for AML and other diseases of HSCs.
Collectively, these studies further underscore the potential for Cimeio’s therapies, when coupled with its shielding technology, to transform the treatment of hematologic malignancies, genetic, and autoimmune diseases.
“AML patients who have residual disease at the time of a bone marrow transplant have a high risk for relapse,” said Corey Cutler, M.D., M.P.H., Medical Director of the Stem Cell Transplantation Program at the Dana Farber Cancer Institute and Professor of Medicine at Harvard Medical School. “An effective therapy that could be given post-transplant to treat residual disease and prevent relapse, but would not affect the newly transplanted cells, would be a real advancement in the way we treat AML. Bone marrow transplant has the potential to cure patients of their leukemia, and improving upon this approach through epitope shielding and novel post-transplant therapies is an exciting possibility.”
About Cimeio
Cimeio is the leader of the field of epitope editing and is developing a portfolio of Shielded-Cell & Immunotherapy Pairs™ (SCIP), novel immunotherapies which have the potential to transform treatment of hematologic diseases. Cimeio develops state-of-the-art immunotherapies, along with paired, modified variants of naturally occurring cell surface proteins in HSCs. These novel epitope edited variants maintain their function but are resistant to depletion when targeted by the paired immunotherapy which has high affinity for the wild-type version of these proteins. These immunotherapies have significant therapeutic potential, which Cimeio is using to develop curative treatments for patients with hematologic malignancies, autoimmune disorders, and genetic diseases. Shielded Cell and Immunotherapy Pairs and SCIP are trademarks of Cimeio Therapeutics, Inc. For more information, please visit .
View source version on businesswire.com:
Contacts
Steve Edelson
sedelson@versantventures.com
415-801-8088
Source: Cimeio Therapeutics
View this news release online at:
免疫疗法ASH会议细胞疗法
100 项与 CIM-053 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 血液肿瘤 | 临床前 | 瑞士 | 2023-12-12 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或

药物交易
使用我们的药物交易数据加速您的研究。
登录
或

核心专利
使用我们的核心专利数据促进您的研究。
登录
或

临床分析
紧跟全球注册中心的最新临床试验。
登录
或

批准
利用最新的监管批准信息加速您的研究。
登录
或

生物类似药
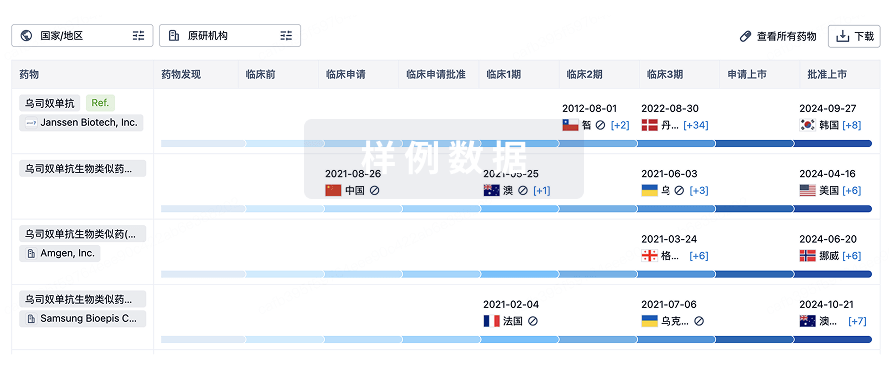
生物类似药在不同国家/地区的竞争态势。请注意临床1/2期并入临床2期,临床2/3期并入临床3期
登录
或
特殊审评
只需点击几下即可了解关键药物信息。
登录
或

Eureka LS:
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
