更新于:2024-09-19
Salmon calcitonin(Nektar Therapeutics)
鲑鱼降钙素(Nektar Therapeutics)
更新于:2024-09-19
概要
基本信息
在研机构- |
非在研机构 |
最高研发阶段无进展临床1期 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
关联
100 项与 鲑鱼降钙素(Nektar Therapeutics) 相关的临床结果
登录后查看更多信息
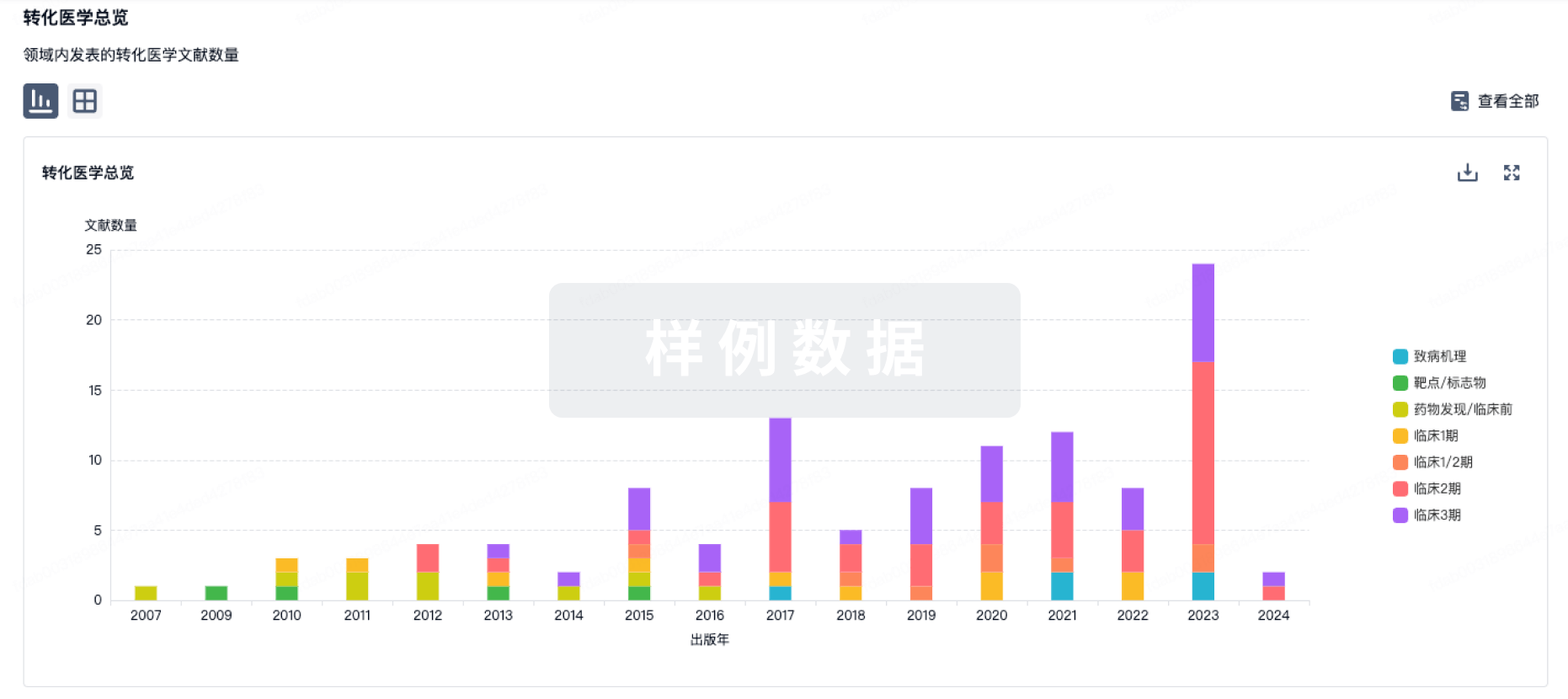
100 项与 鲑鱼降钙素(Nektar Therapeutics) 相关的转化医学
登录后查看更多信息
100 项与 鲑鱼降钙素(Nektar Therapeutics) 相关的专利(医药)
登录后查看更多信息
3
项与 鲑鱼降钙素(Nektar Therapeutics) 相关的新闻(医药)2024-02-23
过去一年,多肽类药物备受市场关注。一方面,GLP-1 多肽药物点燃肥胖和代谢性疾病治疗市场,另一方面,多家长期致力于开发多肽偶联核素的核药企业相继被国际制药巨头收购 (例如,礼来:布局新一代放射性配体疗法,收购POINT 生物制药公司)。核药赛道火爆,备受国内外药企追捧。本文解读一篇发表于2021年《自然综述-药物发现》杂志的综述文章,解读过去100年多肽类药物发展历史和趋势。自1922年胰岛素的首次医疗应用以来,肽类药物在治疗糖尿病、癌症、骨质疏松症、多发性硬化症、HIV感染和慢性疼痛等多种疾病中发挥了重要作用,目前全球市场上已有大约80种肽类药物,并且有超过150种正在临床开发阶段,另外还有400至600种正在进行临床前研究。本文不仅回顾了早期研究方法,例如通过对天然激素如胰岛素进行化学修饰以提高其稳定性和药效活性的方法,对于今天仍然具有重要意义的教训。同时,也探讨了正在崭露头角的新策略,比如毒液组学(venomics)和肽展示库技术,为肽类药物的发现开辟了全新的途径。此外,还分析了在当前制药环境中,肽类药物可能发挥独特价值的领域,特别是在传统小分子药物或生物制剂无法有效干预的治疗领域。然而,为了使肽类药物充分发挥其潜力,尚需解决一系列挑战,包括改善口服生物利用度、增加血浆稳定性、延长体内循环半衰期以及降低生产成本等关键问题。肽类药物疗法领域的发展简史肽类药物的起点可以追溯到肽激素时代,其中胰岛素作为首个来源于内源性激素的疗法,它最初是从牛和猪的胰腺中提取获得,也开启了肽类药物研发的大门。1954年,维克多·杜·维尼奥领导的研究团队完成了催产素和加压素的全合成工作,并因此获得了1955年的诺贝尔化学奖。这是肽类化合物化学合成的重大突破。在1950年代,人工合成的肽激素如催产素和加压素进入临床应用,瑞士Ciba和Sandoz等工业集团的参与进一步推动了肽类药物产业的兴趣与商业化进程。然而,早期的溶液相化学合成方法效率低下,直到1963年固相多肽合成技术的发明及其与高效液相色谱纯化方法的结合,才使得肽类药物的研发引起了制药行业的广泛关注。布鲁斯·默里菲尔德提出了在固相上组装氨基酸以自动化合成多肽的概念,从而发明了固相多肽合成技术,这项革命性的方法极大地提高了多肽合成的效率和精确度,并最终为他赢得了1984年的诺贝尔化学奖。随着对肽类生物介质关键作用的认识加深,人们认识到其卓越的活性、选择性和低毒性特征,但也注意到肽类药物的局限性,包括口服生物利用度低、血浆稳定性差和体内半衰期短等问题。尽管如此,在20世纪70-80年代小分子药物盛行的黄金时期,肽类药物的研究并未停滞不前,而是通过不断改进药物递送技术、制剂和合成工艺,克服了这些挑战。进入1980年代,随着重组技术的到来,科学家们能够更洁净地生产更大分子量的多肽。1980年代后期,伴随着风险投资和生物科技公司的支持,肽类药物发展迎来了第二波高潮,重组人胰岛素的成功商业化及促性腺激素释放激素类似物如亮丙瑞林和戈舍瑞林的批准上市,验证了肽类药物市场的可行性并激发了更多的投资和研究活动。90年代后期,研究者采取了一系列策略来增加肽的分子量,如将肽与脂质、较大蛋白质或聚乙二醇进行偶联,这些策略有效地解决了肽类药物快速肾清除的问题,延长了它们在血浆中的循环时间。此外,展示技术的进步也发挥了重要作用,比如噬菌体展示技术使得研究人员能够从大规模文库中定向发现具有更好药理特性和更高药物相似性的肽序列。随着时间推移,肽类药物市场不断壮大,批准上市的药物种类涵盖了糖尿病、癌症、骨质疏松症等多种疾病的治疗,并且通过持续的技术革新和生物学认识的深化,肽类药物的研发正继续朝着更加高效、安全和适应性更强的方向发展。从2000年至2010年间,进入临床试验的肽类药物数量几乎翻倍于上世纪90年代。多肽药物市场肽类药物市场占据了一个介于小分子药物和生物制剂之间的独特药理学领域。在全球医药市场中,肽类药物占比达到5%,2019年全球销售额超过500亿美元。在过去的六十年间,肽类药物的批准数量稳步增长,全球肽类治疗市场的平均增长率约为7.7%。在肽类药物的销售收入中,胰岛素及其类似物占据了大约一半的份额(约250亿美元),显示出其在该领域的主导地位。紧随其后的是一系列重要的肽类药物产品:例如用于糖尿病治疗的GLP-1受体激动剂杜拉鲁肽(商品名Trulicity),其2019年的销售额达到44亿美元;另一款GLP-1受体激动剂利拉鲁肽,分别以Victoza和Saxenda品牌应用于糖尿病和肥胖症治疗,销售额达41亿美元;合成促性腺激素释放激素类似物亮丙瑞林(商品名Lupron和Eligard),主要用于癌症治疗,销售额为20亿美元。根据目前获批的肽类药物,大部分属于激动剂类别,并且最常被针对的适应症与内分泌学、新陈代谢以及肿瘤学有关。2019年多肽类药物销量排行榜基于合成人体激素的多肽药物基于重组人体激素的多肽药物基于激素提取物的多肽药物多肽类诊断产品从动物、植物和细菌中提取的多肽药物基于偶然发现和合理设计的多肽药物基于可注射的聚乳酸-乙醇酸或聚乳酸的肽类药物缓释制剂类药物(这种技术利用了PLGA和PLA这类生物可降解聚合物,通过将肽类药物与这些聚合物结合,形成微粒或微球形式的长效给药载体。由于PLGA和PLA在体内可以逐步分解为无毒产物并被代谢排出体外,因此它们作为药物输送材料具有良好的生物相容性和安全性。)代表性的多肽药物降钙素 (Calcitonin) 和甲状旁腺激素 (PTH)降钙素是一种由32个氨基酸残基组成的肽类激素,1961年发现其能有效降低狗血液中的钙离子水平。随后的研究证明,降钙素能够强有力地抑制骨吸收过程。鲑鱼降钙素与人体降钙素相比,在序列上有16个氨基酸残基的不同,但效力却高出40至50倍。1978年,鲑鱼降钙素获得了用于治疗高钙血症和绝经后骨质疏松症的批准。起初,鲑鱼降钙素是从鲑鱼类似甲状腺的腺体中提取得到的天然物质,但在1978年合成版本被批准使用,并且在2005年进一步发展出了基于重组技术生产的鲑鱼降钙素。甲状旁腺激素(PTH)是一个含有84个氨基酸残基的激素,于1925年被发现。它的作用与降钙素的效果相反,主要通过激活 PTH1 受体和 PTH2受体,促进骨骼中钙库释放钙离子,从而显著提高血液中的钙含量。然而,长时间持续升高的 PTH 水平会导致骨骼中钙储备的耗竭,不利于维持骨骼健康。多款靶向 PTH1R 的药物获批上市2023-12-13 甲状旁腺功能减退症:靶向PTH1R 的小分子激动剂开发进展2023-08-08 Ascendis Pharma: 甲状旁腺功能减退症临床进展2023-11-29 由于PTH及其类似物的体内半衰期极短,不适用于临床治疗。随着化学修饰技术的发展,研究人员采用多种策略延长了PTH类似物的活性及稳定性,例如引入非天然氨基酸、N端或C端的延伸以及二硫键模拟物等方法。这些改进使得PTH类药物能够在人体内更有效地发挥生物学效应并降低清除率。首个基于PTH的疗法是 Teriparatide,这是一种重组的人PTH前34个氨基酸残基片段,即生物活性部分,于2002年获得批准,用于治疗骨质疏松症。Teriparatide 不仅抑制骨吸收,而且是首个能够促进新骨形成而非仅抑制旧骨流失的药物,从而显著提高了骨密度和骨折风险的管理效果。随后,在克服PTH不稳定性的基础上,研发出了全长度的PTH疗法,以控制低血钙症患者体内的血钙浓度,并在2015年获得了批准。此外,还出现了类似于PTH相关蛋白(PTHrP)的合成类似物 abaloparatide,该药物与PTH有41%的序列同源性,并在2017年获批用于骨质疏松症的治疗。生长抑素(Somatostatin)生长抑素是一种14个氨基酸残基组成的内源性激素,具有抑制多种内分泌腺分泌的作用,包括对生长激素、胰岛素、胃泌酸、胆囊收缩素等的抑制效应。由于其体内半衰期极短,不适合直接用于临床治疗,因此研究人员通过一系列化学修饰技术对其进行了改进。肢端肥大症:最新临床研究进展2023-11-14礼来:布局新一代放射性配体疗法,收购POINT 生物制药公司2023-10-21靶向 GPCR 药物开发的全球十大药企之诺华 (3)2023-10-06J.P. Morgan 2024 系列: 被受关注的GPCR靶点和管线(3)2024-01-17首先,通过对生长抑素进行截短、替换特定氨基酸残基以及N-到C-末端的环化改造,科学家们成功提高了该激素及其类似物的稳定性和生物活性。例如,采用d-氨基酸、非天然氨基酸替换,N端或C端保护以及二硫键模拟等方法,最终开发出了一系列在临床上广泛应用的药物,如奥曲肽,它能有效治疗肢端肥大症、某些类型的肿瘤以及其他相关疾病,并且拥有显著延长的体内作用时间。此外,针对生长抑素受体的研究发现,许多肿瘤细胞会过表达这些受体的不同亚型,这不仅推动了亚型选择性生长抑素类似物如 lanreotide、vapreotide 和 pasireotide 的研发,还催生了肽放射核素疗法这一新的治疗领域。通过将放射性同位素与生长抑素类似物结合,形成可用于诊断和治疗神经内分泌肿瘤等疾病的放射性药物,例如In 111 pentetreotide、Ga 68 DOTA-TATE等。胰岛素(insulin)胰岛素是首个用于治疗疾病的肽类药物,于1922年首次从动物(牛和猪)的胰腺中提取并应用于临床,成功地改变了1型糖尿病患者的治疗方式,并且至今仍然是商业上最成功的肽类药物之一,市场需求随着肥胖症发病率的上升而保持了每年约10%的复合增长率。针对胰岛素本身的局限性,例如其短的代谢半衰期,研究人员运用各种药物化学策略进行了优化,包括引入非天然氨基酸、进行N端或C端的保护与延伸、模拟二硫键结构等手段,以增强胰岛素的稳定性和生物活性。这些改良不仅提升了胰岛素类似物的效力和选择性,还改善了其药代动力学特性,从而发展出一系列疗效更好、使用更方便的胰岛素制剂,如长效胰岛素及其类似物。此外,随着基因重组技术在1980年代的发展,胰岛素生产进入了一个崭新的阶段,能够高效、清洁地制造更大规模的多肽,克服了早期提取法的不足。通过与脂质、大分子蛋白质及聚乙二醇等结合,进一步增加了胰岛素分子的分子量,有效解决了肾清除过快的问题,延长了药物在血浆中的循环时间,从而确保了药物具有更持久的降糖效果。催产素 (Oxytocin) 和血管加压素类似物 催产素是一个含有9个氨基酸残基的内源性激素,在1954年由 Vincent du Vigneaud 团队首次实现全合成,并因其在分娩、哺乳以及社交行为中的关键作用而闻名。早产:获批上市的临床治疗性药物催产素因其在体内的半衰期较短(仅几分钟),限制了其作为治疗药物的应用潜力。为克服这一局限,研究人员采用了一系列创新的药物化学方法对其进行结构改造。包括但不限于:使用d-氨基酸以增加稳定性;引入非天然氨基酸来改变药理特性;进行N-端或C-端的保护与延伸以延缓降解;以及探索二硫键模拟物以增强其构象稳定性和代谢稳定性。通过这些化学修饰手段,开发出了具有更长作用时间、更高活性及选择性的催产素类似物。例如,desmopressin是经过修饰的加压素类似物,在治疗尿崩症方面显示了优于天然激素的效果。此外,催产素类似物在临床上被用于诱导宫缩以促进分娩,并在减少产后出血、治疗某些妇科疾病等方面也发挥了重要作用。血管加压素和利普西秦(Lys8-vasopressin)曾被用于治疗中枢性尿崩症,但后来被去氨加压素(desmopressin)替代,后者具有更高的蛋白水解稳定性。去氨加压素是最早能够口服和鼻腔给药的肽类药物之一,其半衰期约为1.5至2.5小时。Gonadotropin 释放激素类似物Gonadotropin 释放激素(GnRH)类似物是通过改造自然存在的 GnRH 而合成的药物,该激素在调控性腺分泌性激素方面起着关键作用。GnRH 超级激动剂的制作过程中,在第6位点用不同的D-氨基酸替代了甘氨酸(Gly),这增强了与受体的结合亲和力,并赋予其对蛋白酶的抵抗能力。而在C端甘氨酰胺位置替换为乙胺或仿生的肼基甘氨酸衍生物,不仅像天然酰胺一样可以防止羧肽酶降解,还使得分子更具有疏水性,从而增加了药效强度和作用时间。早期尝试制备拮抗剂时,在第6位点引入了D-氨基酸;然而,由于在大鼠皮下注射后出现组胺性皮肤反应,阻碍了进一步的临床应用开发。为了避免水肿这一不良风险,研究人员将D-精氨酸替换为中性的D-脲基烷基氨基酸。相比于激动剂,拮抗剂使用了更多非天然氨基酸成分,除了4、7和9号位点之外,其他所有残基在至少一种拮抗剂中都被进行了修饰。Amylin 类似物Amylin是一种由37个氨基酸组成的内分泌激素,主要由胰岛β细胞分泌,在体内参与血糖调节,特别是在餐后抑制胰高血糖素释放和减慢胃排空速度方面起着关键作用。肥胖症治疗药物的最新临床研发进展2024-02-19 读懂百年诺和诺德之创新、增长与影响非凡的第100年2024-02-01 J.P. Morgan 2024 系列: 被受关注的GPCR靶点和管线(2)2024-01-13 劝君慎重:全球 GLP-1R 研发管线有多卷?2023-07-28Pramlintide 由31个氨基酸组成,是一种合成的人胰淀素类似物,这是一种在餐后与胰岛素共同从胰腺β细胞分泌的肽激素。Ⅰ型糖尿病患者体内的胰淀素水平异常低下,而在Ⅱ型糖尿病患者体内则高于正常水平。由于内源性人类胰淀素高度淀粉样变性,研究人员借鉴了高度同源但非淀粉样变性的大鼠胰淀素中的脯氨酸残基(已知能够干扰二级结构),将其植入到人胰淀素序列中,从而研制出了普兰林肽。GLP-1 多肽GLP-1是一种由31个氨基酸残基组成的内源性肠促胰岛素激素,具有显著的葡萄糖依赖性胰岛素分泌促进作用,并能够抑制餐后胰高血糖素释放、减慢胃排空速度以及影响食欲,因此在糖尿病治疗中扮演了重要角色。GLP-1R:肥胖及代谢疾病治疗靶点2024-02-13 安进减肥管线 AMG 133 进化史2024-02-09 GLP-1 小分子激动剂领域风起云涌!紧随辉瑞,硕迪 GSBR-1290 临床 2a 数据遇险2023-12-19 Novo Nordisk 的2023半年报:关于糖尿病和GLP-12023-08-15 节节败退!辉瑞终止 GLP-1R 小分子激动剂 Danuglipron 临床3期开发2023-12-03 礼来:替尔泊肽正式登陆减肥市场,“减肥药王”之争打响第一枪2023-11-29 GLP-1R 火爆全球,它的姐妹受体 GLP-2R呢?2023-11-21 辉瑞的一波三折: 三款 GLP-1R 小分子激动剂的不同命运2023-11-12 Tirzepatide 获批用于治疗肥胖后,礼来公司的 GLP-1R 小分子激动剂还有多久?2023-11-09早期的研究发现,静脉输注 GLP1(7–37) 对2型糖尿病患者的胰岛素分泌和血糖有显著影响之后,人们投入大量努力将其开发为药物。然而,GLP1(7–37) 会被二肽基肽酶4迅速分解,并在1至2分钟内通过肾脏清除。尽管用其他短侧链氨基酸替代位置2的丙氨酸可以保护该分子免受酶解降解,但快速的肾清除率仍使其不适合用于治疗。在20世纪90年代初,从吉拉怪兽毒液中分离出一种与 GLP1(7–37) 具有53%同源性的39个残基组成的肽,名为“exendin 4”。研究发现 exendin 4是GLP1受体的完全激动剂,它对DPP4降解稳定,在人体内的肾清除率较低(5至7小时),这个多肽后来被开发成为一种药物(商品名为exenatide,采用皮下注射,每日两次给药)以用于治疗2型糖尿病。自此以后,包括liraglutide, albiglutide, dulaglutide, lixisenatide 和 semaglutide 等多种其他 GLP1 受体激动剂,以及 exenatide 的一种长效制剂,相继被批准用于2型糖尿病或肥胖的治疗。本文中还提到肽类药物发现策略,包括毒液组学与展示技术,前者利用生物信息学分析毒蛇等有毒动物基因组及转录组数据结合蛋白质组学从粗毒样本中获得的数据,识别大量潜在的治疗用毒素肽;后者则通过构建大规模肽库并筛选针对特定靶标的高亲和力配体。例如,Ra Pharmaceuticals mRNA 展示平台衍生出的环状肽zilucoplan 已进入三期临床试验,用于治疗全身型重症肌无力。在药物化学策略方面,研究人员致力于改进肽类药物的代谢稳定性和血浆半衰期,采用诸如N端乙酰化、N-甲基化、使用d-氨基酸或非天然氨基酸以及酰胺键类似物(如硫代酰胺、肽类似物和β-氨基酸)等手段。此外,N到C末端的环化和二硫键模拟物(特别是硫醚键)越来越多地应用于肽类药物设计中,以调整它们的代谢稳定性和生物利用度。同时,一些高度稳定的环状构象骨架,比如环状缩氨酸和向日葵胰蛋白酶抑制剂,可作为载体将具有治疗意义的药效团嵌入其环内,进而研发出更稳定且具有靶向特异性的口服肽类药物,如已上市的 linaclotide 和 plecanatide 用于治疗便秘型肠易激综合征。未来展望未来展望部分,作者提到肽类药物的发展趋势预计会加速,因为生物制品的成功打破了必须口服给药的传统观念。肽类药物领域已经成熟,能够可靠快速地规模化生产结构复杂的多达约100个氨基酸的肽,并进行有效的构效关系(SAR)研究和先导化合物优化。新兴的肽类药物发现技术能在短时间内高效生成有潜力的高选择性和高活性候选化合物。随着新型递送技术和创新化学策略的整合,肽类药物领域将继续蓬勃发展。最后,作者提及,尤其是抗菌、抗病毒和抗衰老肽类药物在未来具有广阔的增长空间。肽类在化妆品行业也越来越受到关注,如市场上销售的六肽 Argireline 作为肉毒杆菌神经毒素类似物用于减少皱纹,五肽 Palmitoyl Pentapeptide-4(Matrixyl)通过刺激成纤维细胞中的细胞外基质更新而有助于减轻皱纹,铜肽 GHK-Cu 作为一种天然三肽,具有较高的铜离子亲和力,具备抗炎功能并能促进皮肤成纤维细胞中胶原蛋白和糖胺聚糖的合成。总体而言,过去60年间肽类药物的稳步批准见证了该领域的发展,随着新药发现和递送技术的进步,肽类药物有望继续占据药品市场的独特地位,成为介于小分子药物与大分子生物制剂之间的有力竞争者。以上文章来源于GPCR drug discovery,作者段思研本文仅作信息交流之目的,文中观点不代表相关疾病治疗立场,也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
放射疗法并购
2023-08-11
点击上方的 行舟Drug ▲ 添加关注作者|李斯文¹,杨 悦²(1. 沈阳药科大学;2.清华大学)美国现行的仿制药审评体系是自 1984 年颁布的《Hatch-Waxman 法案》确立的。该法案对仿制药的规定,主要针对结构相对简单的小分子药物,并没有将复杂仿制药考虑在内,全球也尚无一致的复杂仿制药监管和评价共识 [1]。美国 FDA 致力于此类仿制药的科学评价研究,倡导将“质量源于设计 (Quality by Design,QbD)”理念应用于复杂仿制药监管,监管路径已逐渐明晰。1复杂仿制药的定义及分类仿制药需要证明与参比制剂药学等效( pharmaceutical equivalence,PE)和生物等效(bioequivalence,BE) 才能获批上市,研发难度因参比制剂而异。复杂仿制药是复杂参比制剂的仿制版本。因复杂药物理化特性难以被完整表征,血浆药代动力学参数也难以确定药物吸收程度和速度,复杂仿制药的研发和技术审评给监管机构带来了新的挑战。复杂药物按活性成分来源分为生物制品和非生物制品 [2],监管机构对这两类药物的上市许可确立了各自独立的申请路径。本文只讨论通过简略新药申请 (abbreviated new drug application,ANDA) 途径提交的非生物复杂仿制药[药研公众号整理排版]。《仿制药使用者付费法案》(Generic Drug User Fee Act,GDUFA) 要求 FDA 和仿制药生产商遵守某些要求和承诺,详细内容记载在立法随附的《GDUFA 承诺书》中 [3]。FDA 在 2016 年 5 月 12日发布《GDUFA Ⅱ承诺书》,承诺在 GDUFA Ⅱ期间通过将复杂药物分类促进复杂仿制药监管。依据复杂药物的类别划分复杂仿制药的类别,包括 :①具有复杂活性成分的产品,如肽、高分子化合物、活性药物成分 (active pharmaceutical ingredient,API) 复杂混合物和天然来源成分 ;②具有复杂给药途径的产品,如乳膏或凝胶等局部作用药物 ;③具有复杂剂型 / 制剂的产品,如脂质体、胶体和混悬液 ;④复杂药械组合产品,如肾上腺素自动注射器和鼻用气雾剂 [ 4]。为保证复杂仿制药的安全性和有效性,制药企业和监管机构应当合作解决监管挑战,探索更合适的监管路径。2复杂仿制药监管的必要性1984 年颁布的《Hatch-Waxman 修正案》确立了仿制药的审评框架,但当时大多数药物都是结构相对简单的小分子药物,通常很容易通过传统方法(如 BE 研究等 ) 进行描述和评价。多数情况下,一种药物的活性与它进入血液的速度及其在血液中停留的时间直接相关,所以该药物可能会对其作用部位产生预期的效果。与之相比,复杂药物因其配方和活性成分复杂,通常不易配制和生产。而且,这类药物通常直接作用于局部组织,而非通过血液中的药物浓度发挥作用,包括直接作用于肺部的吸入药物,直接作用于皮肤的局部贴剂,或作用于眼部表面的滴眼液。这些不同剂型药物的治疗效果并不一定与其在血液中药物浓度有关,而且通过血液也难以检测出结果,因此传统上常用于评价仿制药并证明其与参比制剂等效的比较简单的度量指标难以适用于这类药物 [5]。自从《Hatch-Waxman 法案》颁布后,有关仿制药质量以及 BE 评价方面的法规至今基本没有重大变化 [6]。然而,用于治疗疾病的药物却越来越复杂,支撑普通仿制药安全性和有效性的研究已无法作为复杂仿制药与参比制剂治疗等效 (therapeutic equivalence,TE) 的证据,至少就公共领域中已经成熟的仿制药开发经验而言,开发和评估潜在的复杂仿制药具有挑战性 [7]。成功“仿制”一种复杂药物意味着高价值回报,但多数企业因成本和技术限制放弃仿制,FDA 通过发布技术指南尽可能地为复杂仿制药开发提供更加科学的指导和监管透明度以增加企业研发的信心和积极性。复杂仿制药将为患者提供重要的治疗方法,而且 FDA 认为它们对仿制药行业经济健康运行的影响也会越来越大,会不断推出其他新政策以加强复杂仿制药监管。3复杂仿制药监管进程吸入和鼻用药品是复杂药械组合产品,2003年 4 月,FDA 颁布了《鼻用气雾剂和鼻用喷雾剂的生物利用度和生物等效性研究行业指南》,为在 ANDA 下证明复杂药械组合产品 BE 提供了建议 [8]。此后有多项针对复杂药械组合产品的指南陆续颁布,如 2006 年的《新型组合产品的早期开发考虑》、2017 年的《ANDA 药械组合产品比较分析与相关的人为因素研究行业指南草案》和《评估 ANDA 透皮和局部给药系统的刺激性和致敏性行业指南草案》等。随着新型脂质表征和修饰技术的发展,各种脂质体被开发为药物递送系统,FDA在 2010 年 2 月发布了盐酸阿霉素脂质体注射液的BE 指南草案,这是促进脂质体仿制药研发的第一个 BE 指南。2015 年,FDA 又发布《脂质药品 :化学、生产和控制 ;人类药代动力学和生物利用度 ;标签文件》(Liposome Drug Products: Chemistry, Manufacturing, and Controls; Human Pharmacokinetics and Bioavailability; and Labeling Documentation)[9],进一步促进脂质体仿制药的开发。在 2012 年之前,FDA 对复杂 API 的研究比较有限,只集中在鲑鱼降钙素和依诺肝素等少数药品上。2012 年,美国的肽类药物市场不到 110 亿美元,到 2016 年已增长到 180 亿美元以上 [10]。FDA 对产品越了解越能更好地对其监管,《2013—2017 财年的监管科学报告 :复杂混合物和肽》(FYs 2013-2017 Regulatory Science Report: Complex Mixtures and Peptides) 总结了 FDA 的内部研究和外部合作研究活动,提高了FDA 对复杂 API 的理解 [11]。此外,FDA 前局长 Scott Gottlieb 在任期间高度关注仿制药监管,特别是高技术壁垒的复杂仿制药 [12]。为解决仿制药开发过程中遇到的相关问题,FDA 于 2015 年发布《与仿制药开发有关的书面咨询》,2017 年发布《FDA 与复杂产品 ANDA申请人之间的正式会议指南草案》,加强 FDA 与仿制药企业的沟通交流。2017 年,FDA 宣布了《药物竞争行动计划》(Drug Competition Action Plan,DCAP),最大限度地提高复杂仿制药的科学性和监管透明度,以促进复杂药物的仿制药竞争。为了促进仿制药的供应并协助仿制药行业确定最合适的药物开发方法和产生支持 ANDA 批准所需的证据,FDA 根据科学研究结果定期发布产品特定指南(Product-Specific Guidances,PSG)。2019 年,FDA发布了 269 份复杂仿制药产品特定指南,收到了105 份产品开发和 ANDA 提交前会议请求,举办了多次关于“复杂仿制药开发”的公共研讨会,以加速复杂仿制药的批准上市。在 FDA 和仿制药行业的共同努力下,FDA 在 2019 年批准了 110 个复杂仿制药,占仿制药批准总量的 11% [13]。4复杂仿制药监管增强路径FDA 将已成熟的书面咨询途径应用于复杂仿制药监管,加强企业与 FDA 关于仿制药开发问题的沟通交流。FDA 药品评价与研究中心 (Center for Drug Evaluation and Research,CDER) 下的仿制药办公室 (Office of Generic Drugs,OGD) 中的研究和标准办公室 (Office of Research and Standard) 将审评包含复杂药物或药械组合产品问题的书面咨询 [14]。当书面咨询无法解决申请人问题时,为帮助复杂仿制药申请人提交更完整的申请,促进更有效的 ANDA 审评流程,2018 年,GDUFA Ⅱ授权FDA 为复杂仿制药建立 ANDA 前 (pre-ANDA) 会议的新机制,作为复杂仿制药监管的增强路径 [15]。此外,2020 年 8 月 1 日,FDA 向马里兰大学和密歇根大学授予了为期 5 年 (2020 年 8 月 1 日至2025 年 7 月 31 日 ) 的赠款,以建立复杂仿制药研究中心 (Center for Research on Complex Generics,CRCG)。该中心旨在加强与仿制药行业的研究合作,以进一步实现 FDA 的使命,即增加获得安全有效的仿制药的机会。FDA、非仿制药行业和利益相关者之间将通过协作研究,培训和资源交换来实现这一目标。CRCG 致力于通过提供以下服务来支持仿制药和其他利益相关方 :合作研究和培训、网络研讨会、讲习班实验室项目、复杂仿制药学者计划,以及其他倡议。此类首创的前沿中心将激发创新对话,传播当前对复杂产品和规范的理解,并产生支持 FDA 通过增加获得安全有效的仿制药来促进和保护公共卫生使命的新知识 [16]。中心可以促进关于新的已被证明难以实施的复杂分析方法的培训,或者帮助发起人 (sponsor) 提高其建模和仿真技能。CRCG 可以连接多家企业的研究实验室进行方法测试或其他项目,这些都是 FDA 无法独自做到的。FDA 有一个或两个实验室,而每家企业都有自己的实验室。如果各方愿意协作,那么实验室的数量将十分充足。复杂仿制药学者计划将尝试让更多的药学专业的学生参与复杂仿制药研究。中心还计划举办年度活动,学生团体将为复杂产品科学问题提供解决方案。5QbD 理念促进复杂仿制药监管5.1 相关理念介绍5.1.1 QbD药品质量是最重要的因素,ICH 质量指导原 则 Q8 药物研发(ICH Quality Guidelines Q8 Pharmaceutical Development,ICH Q8) 由此纳入一个新的概念——QbD。QbD 是一种基于科学和质量风险管理,以预定目标为始并强调产品和工艺理解与工艺控制的系统开发方法,有助于将质量设计到产品中,而不仅仅是对最终产品进行测试,但前提是必须增加对产品和生产工艺的理解和控制 [17]。QbD 强调“以终为始”,应当首先界定目标产品质量概况 (quality target product profile,QTPP),再从 QTPP 中确定关键质量属性 (critical quality attributes,CQA),以此逐步实现预定目标。QTPP可以根据原研药说明书、质量标准和参考文献信息得以确定 [18]。从 QTPP 中选择 CQAs 的标准基于未满足该质量属性时对患者造成伤害 ( 安全性和有效性 ) 的严重程度 [19]。在药品开发过程中应当重点关注那些可能因为处方或制造工艺变化而受到影响的CQA[药研公众号整理排版]。实施 QbD 的目的不是避免生产过程中的偏差,而是建立一种可以在一定范围内调节偏差以保证产品质量稳定性的生产工艺。在 ICH 及 FDA 近年发布的相关技术要求和指南中多已贯彻 QbD 理念,如 2006 年的 ICH Q8,2009 年的 ICH Q8(R2),2011 年的《ANDA 的质量源于设计 :以改良释放剂型为例》以及 2016 年的《2016 财年监管科学报告 :局部作用的口服吸入和鼻用药品》。FDA 的OGD 在 2013 年初即要求申请人按照 QbD 要求提交 ANDA 申报资料,根据 QbD 理念准备的申请资料将包含更多的开发信息,使 FDA 对企业的产品申请更加了解。5.1.2逐步递进的比较研究策略复杂仿制药的等效性标准涉及三个方面 :一是PE,由于参比制剂的复杂性,其仿制药的 PE 既要考虑组成又要考虑结构 ;二是 BE,复杂仿制药的BE 具有多重标准;三是 TE,在 PE 和 BE 的前提下,根据标签规定条件给药,可以预期其与参比制剂具有相同的临床疗效和安全性,可临床替代参比制剂。根据国家药品监督管理局 2019 年 11 月 5 日颁布的《化学药品注射剂 ( 特殊注射剂 ) 仿制药质量和疗效一致性评价技术要求》( 征求意见稿 ) 所述,由于药物制剂组成和结构复杂,为降低等效的不确定性,应当基于产品特征,考虑采用从证明 PE、BE到临床 TE 的逐步递进的比较研究策略。所谓逐步递进策略是首先进行仿制药与参比制剂的药学和非临床的全面比较研究;然后进行人体 BE 比较研究;必要时再开展临床研究 [20]。如果药学研究和 / 或非临床研究结果高度一致,则 BE 试验一次性通过的概率很大。若结果显示仿制药与参比制剂不一致,建议重新比对仿制药与参比制剂的 API、辅料和剂型等药学参数的相同性,避免因后续 BE 偏差较大而浪费时间和资源。5.1.3逆向工程QbD 的前提是利用逆向工程对原研药进行充分表征,随后进行 PE 设计,开发有效的生产工艺,并开展关键批次 BE 研究。在 PE 方面,提升仿制药与参比制剂的处方相似程度,将增加开发出稳定性较好、与参比制剂生物等效的药物的机会。逆向工程有助于实现复杂仿制药与参比制剂处方定性和定量相同。在 QbD 理念下,参比制剂的定量信息有助于识别药物的 CQA,从而进行更有效的实验设计。但是,原研企业一般只公开其药品处方的辅料种类,并不提供辅料用量。仿制药研发企业可以运用逆向工程技术,结合元素分析法 ( 通过检测元素迅速确定关键辅料用量 ) 和重量法 ( 溶解制剂后过滤测定不溶性辅料的重量 ) 明确原研药的辅料用量 [21]。辅料组成和用量的明确将有助于仿制药与原研药药学等效和生物等效,从而提高仿制药的质量。5.2 QbD理念应用于各类复杂仿制药研发仿制药开发难度因参比制剂而异,应当对复杂仿制药分类审评。目前,GDUFA Ⅱ将复杂药物分为 4 类,即具有复杂活性成分、复杂给药途径、复杂剂型 / 制剂的产品以及复杂药械组合产品。应根据各类复杂制剂的 CQA 评估仿制药的生物等效性,例如,肽类混合物需额外考虑产品的生物学特性,计量气雾剂需额外研究产品的给药装置器械性能,贴剂需额外研究产品的粘附性和致敏性,乳膏需额外研究产品的黏度和延展性以及脂质体需额外研究考虑产品的释药机制等。5.2.1复杂活性成分复杂活性成分产品包括肽、高分子化合物、API 复杂混合物以及天然来源成分产品,覆盖多种治疗领域,开发此类药物及其仿制药已成为行业摆脱同质化竞争的重要策略。以仿制肽类产品为例,对于具有特定氨基酸序列的肽类产品,活性成分相同是仿制的关键,仿制的挑战性可能在于生产中无意引入杂质,影响拟用仿制药的安全性 [22]。不管肽类产品是通过重组还是合成方法生产,都可能含有来源于产品贮存过程中降解形成或生产方法引入的杂质。此外,氨基酸多为手性分子 ( 甘氨酸除外 ),在肽合成的过程中不可避免存在消旋化的可能 [23],因此应对多肽合成中的氨基酸消旋化以及非对映异构体杂质进行研究和控制。肽相关杂质通常具有与药物本身相似的序列,难以检测、分析和控制。FDA 建议申请人采用灵敏且高分辨率的分析程序来检测和鉴定拟议仿制合成肽中的有关杂质,例如液相色谱 - 质谱 (LC-MS) 联用仪 [24]。醋酸格拉替雷 (glatiramer acetate) 是包含 L- 谷氨酸、L- 赖氨酸、丙氨酸和 L- 酪氨酸的肽混合物,通过分析方法学对其复杂性进行精确表征是一项挑战 [25]。FDA 承认,虽然没有单一的理化或生物学表征技术可以对醋酸格拉替雷完全表征,但可以结合多角度光散射 (AFFFMALS)、核磁共振 (NMR) 和 LC-MS 等一系列科学方法,使仿制药与参比制剂制备方案、理化性质 ( 每种氨基酸的含量和光学纯度、分子量分布、光谱指纹等 )、聚合和解聚的结构特征 ( 肽混合物中的氨基酸以肽键相连,因此需将肽链解聚并将氨基酸纯化,才能得到氨基酸的结构和定量信息 ) 和生物测定结果一致。活性成分和结构的相同性是此类药物成功仿制的关键,这些方法的结合已成功应用于表征和评估各种仿制醋酸格拉替雷的申请。5.2.2复杂给药途径复杂给药途径产品指在局部作用 ( 如皮肤 ) 后发挥疗效的非口服产品,包括乳膏和凝胶等局部制剂。美国 FDA 对经皮给药的局部制剂仿制药的评价要求因具体品种而异,但一致的评价标准是证明仿制药与参比制剂 BE,通常用体外和体内 2 种方案来证明,满足下列条件时可采用体外研究替代局部给药制剂的体内研究。①仿制药与参比制剂的处方需满足定性 (Q1) 与定量 (Q2) 相同。为了证明PE,首先确保处方组成相同 [26],处方组成信息可从参比制剂说明书、专利及其他文献资料获得,Q1相同较易实现 ;然后通过逆向工程手段及专利信息确定辅料的用量范围,Q2 要求辅料的用量 ( 或浓度 ) 差异应在 ±5%以内 ;②与参比制剂的理化特性(physicochemical characterization) 具有可比性 ;③与参比制剂的体外释放速率具有可比性。局部制剂需在 Q1 和 Q2 的基础上满足 Q3 的要求,即仿制药与参比制剂在含有相同用量的相同组分的基础上具有相同微观结构。生产工艺可能对制剂的微观结构产生较大影响,因此,仿制药产品工艺开发的目标是实现与参比制剂相同的结构特征,从而确保与参比制剂相同的 CQA,包括外观性状、基质 (o/w 或 w/o)、多晶型、粒度、pH 值、乳滴大小与分布、物理稳定性、黏度、黏弹性、流变学特性等。通常黏度、黏弹性、铺展性等流变学性质对外用皮肤给药的疗效和顺应性有重要影响 ;乳滴大小和均匀性与乳膏物理稳定性直接相关 [27],这些关键指标均需采用适宜的方法进行考察。5.2.3复杂剂型 / 制剂复杂剂型 / 制剂包括脂质体、胶体和混悬液等非口服产品。以脂质体为例,随着新型脂质表征和修饰技术的发展,各种脂质体被开发为药物递送系统,其设计应当根据药物的预期用途进行调整 [28]。运用 QbD 理念将有助于理解脂质体开发过程中的变异性来源,从而制定可提高最终产品质量的有效方法 [29]。脂质体的制备工艺较复杂,一些 CQA 是脂质体质量审评中的常见痛点,包括粒径、脂质降解物和体外释放等。粒径 :脂质体的粒径和粒径分布影响药物的生物分布和药代动力学,通常是决定药物有效性的关键因素。此外,因仿制药和参比制剂的理化属性一致,其平均粒径和粒径分布通常处于相似的范围,但可能因所用技术和仪器不同而导致粒径参数差异。脂质降解物:脂质体产品的完整降解特征通常不能完全确定。体外释放 :脂质体产品的表征应当包括体外测试,使脂质体在合适的模拟生理介质中顺利释放药物。体外试验有助于理解产品的体内行为。关注脂质体产品成分、CQA 的识别和表征,以及在产品开发过程中采用适当的控制措施将会实现预期的产品质量和体内性能。以盐酸阿霉素脂质体注射液为例 [30],除了定性 (Q1)/ 定量 (Q2) 相同要求外,FDA 还建议证明脂质体 CQA 的等效性,例如表面修饰、表面电荷、载药量、药物释放机制、游离药物、脂质含量及脂质降解产物、脂质相变温度以及粒径分布等 [31]。脂质体性质的改变可通过影响脂质双层的稳定性、体内释放的位置和包封药物的释放速率来改变阿霉素脂质体的体内行为。5.2.4复杂药械组合复杂药械组合产品包括自动注射器和定量吸入器等,开发此类产品的仿制药可能比典型药品更具挑战性,不仅要理解活性成分与非活性成分之间的复杂相互作用,还要理解器械的设计和特征,体外表征是建立产品性能最敏感的方法,表征有助于更好地理解仿制药开发的关键特征。鼻用组合产品的性能取决于许多因素,例如制剂、给药装置设计特征和用户界面 ( 人 - 械交互,使用者能够方便有效率地操作产品 )[32]。制剂因素包括药物的理化性质以及辅料的组成和用量。此外,FDA 将考虑最终用户是否可以使用仿制药组合产品替代参比制剂,而无需医疗保健提供者的任何其他干预或在使用前无需任何额外的培训。以气雾剂为例,气雾剂通常由制剂、容器、阀门、传动装置 ( actuator)、防尘盖,相关附件和保护性包装组成,与药物共同构成药品。当试验制剂使用与参比制剂相同品牌和型号的器械 ( 特别是计量阀或泵以及传动装置 ) 时,基于体外试验的等效性概率最大。如果不可行,FDA 建议阀门、泵和传动装置在所有关键尺寸上尽可能接近参比制剂的尺寸 [33]。具体而言,6 项体外测试包括单喷含量、液滴粒径分布、小颗粒液滴中的药物、气雾模式、气雾几何形状和启动,这些测试表征了气雾剂的关键性能,被认为是证明等效性的必要条件 [34]。6应用 QbD 理念所涉及的研发和审评工具6.1 过程分析技术为了使 QbD 轻松应用于制药领域,需要使用各种工具,即试验设计 (design of experiment,DoE)、风险评估 (risk assessment) 和过程分析技术(process analytical technology,PAT) 等,这些工具主要应用于关键参数的识别和设计空间的定义 [35]。其中,DoE 是统计学工具,研究试验数据的获得以及科学分析和处理试验数据与结果的方法。PAT被定义为“一种通过及时检测 ( 即在生产过程中 )API 和中间体以及最终产品的关键质量和性能属性来设计、分析和控制生产过程的系统,目的是确保最终产品的质量”。通过在线获取技术和物料参数,PAT 可在不间断地实时监测制药过程中发挥作用 [36]。为了成功实施 PAT,药物制剂和生产过程的设计与优化分 3 个步骤 ( 即设计、分析和控制 )并运用 4 种工具 :①多变量数据采集和分析工具 ;②过程分析工具 ;③过程控制工具 ;④持续改进和信息管理工具。此外,PAT 还可以结合光谱、色谱和质谱等方法检测产品,以促进 QbD 理念的应用。6.2 生理药代动力学模型为了在药物开发中实施 QbD,研发人员需要能将药品特性与体内性能联系起来的工具,涉及体外释放机制和与药物吸收有关的生理学以及模拟体内释放特性的计算机模型已成为促进 QbD 实施的潜在工具 [37]。生理药代动力学 (physiologically based pharmacokinetics,PBPK) 模型由多个对应于机体不同组织器官的房室组成,药物以血液流动为转运动力,并遵循质量平衡原理进行药物在体内的代谢过程。FDA 大力提倡在仿制药研发和审评中应用PBPK 建模和模拟 [38]。FDA 科学家与外部专家合作开发、评估和改进了 PBPK 模型。2019 年 6 月 13 日,美国 Certara公司宣布,PBPK 模拟技术 Simcyp 被 FDA 用于证明复杂仿制药的 BE[39]。PBPK 模型有助于参比制剂表征,建立目标产品质量概况以及确定 CQA[40],以明确复杂仿制药与参比制剂在质量属性上的差异。此外,根据 PBPK 改进的皮肤吸收模型 MPML MechDermA 用于评估经皮肤吸收的药物的 BE,以应对局部作用仿制药研发的挑战 [41]。在 2019 财年,FDA 利用 PBPK 模型定量描述了透皮药物,促使仿制药Voltaren®(双氯芬酸钠 )1%局部用凝胶的批准,用于缓解与骨关节炎相关的疼痛。7启示美国关注复杂仿制药研发和审评,大力倡导应用 QbD 和逆向工程等理念,以提高仿制药研发质量和效率。复杂仿制药覆盖范围较广,其 PE 和 BE标准也较复杂,为促进研发和审评,应先将复杂仿制药分类,再根据类别特点和参比制剂 CQA 评估仿制药等效性。在 QbD 理念中,由于对产品和工艺的理解更加透彻,仿制药企业可大大减少批次失败的情况,药品监管机构也将对产品质量充满信心 [42]。同时,书面咨询、Pre-ANDA 会议以及复杂仿制药研究中心加强了 FDA 与仿制药企业之间的沟通交流和协作。FDA 可以在产品研发早期就介入,协助企业推进复杂仿制药研发和上市。复杂仿制药虽然组成和结构复杂,但有工艺路线可循就有仿制的方向,先透彻理解参比制剂的特性,再从源头处进行高质量仿制。QbD 理念将研发、审评、生产及监管等多个过程进行了整合,为从根本上提高药品质量奠定了科学基础,为药品监管提供了新的理念和手段。此外,逆向工程可以将潜在问题 ( 例如 CQA、稳定性和测试仿制产品的效率 ) 降至最低,进一步促进了复杂仿制药的研发。复杂仿制药有很大的临床价值和发展空间,监管机构应与行业合作以促进复杂仿制药的研发和批准,使患者及时获得高质量和可承担的药物[药研公众号整理排版]。文章信息源于公众号天咨医药,登载该文章目的为更广泛的传递行业信息,不代表赞同其观点或对其真实性负责。文章版权归原作者及原出处所有,文章内容仅供参考。本网拥有对此声明的最终解释权,若无意侵犯版权,请联系小编删除。学如逆水行舟,不进则退;心似平原走马,易放难收。行舟Drug每日更新 欢迎订阅+医药大数据|行业动态|政策解读
医药出海一致性评价
2023-07-20
·药融圈
2023年8月3日-4日第五届中国国际生物 & 化学制药博览会展位号:E-A05▼关于健元医药健元医药所在园区鸟瞰图-深圳市坪山区深圳市健元医药科技有限公司(以下简称健元医药)于2009年创建,致力于多肽及多肽相关产品的研发、生产、销售。健元医药有1个研发中心 + 3大生产基地(20条多肽API生产线,4条制剂生产线)。其拥有的逐级放大技术,能满足不同批量的需求,从mg级到50kg/批,并开设了多肽细胞毒专线(OEB4/OEB5)和多肽疫苗专线,是国内化学合成多肽原料药生产规模最大的企业之一。健元医药的核心研发团队已有20多年的多肽经验,曾两次通过FDA检查。健元医药完整高效的多肽产业化体系,为客户提供全方位的多肽产业化服务,包括药物肽、兽用肽、抗菌肽、美容肽的研发及生产,注册以及相关的法规支持。01 主营业务多肽及类肽CRO、CMO、OEMPDC药物(多肽-核素、多肽-小分子、多肽-蛋白、多肽-RNA)原料药国内外关联02 研发与生产优势研发基地坪山区生物医药创新产业园,约5000㎡的符合国家级工程技术中心要求的新药开发研究平台;▲健元医药-多肽与创新药物工程研究中心研发中心拥有完善的药品研发体系,配备先进的仪器设备,和一支在生物医药领域有高专业素质的科研队伍,同时与国内外知名院校与科研机构也建立长期合作关系。公司立足多肽原料、多肽CDMO、多肽制剂开发,每年有多个品种上报NMPA、FDA、EMA审批。3大生产基地广东深圳,拥有2条符合cGMP规范要求的制剂生产线,主要生产卡式瓶注射剂,小容量注射剂以及冻干粉针剂。江苏南京,拥有4条符合美国FDA要求的多肽原料药生产线;零缺陷通过US FDA与欧盟EDQM审计。湖北咸宁,计划建16条符合欧盟、FDA要求的多肽原料药生产线,是国内化学合成多肽原料药生产规模最大的企业之一,年产能1000Kg以上。湖北工厂(16条API产线目前已有8条投产)-鸟瞰图03 主要项目清单上下滑动查看更多*序号产品名01司美格鲁肽02利拉鲁肽03醋酸特利加压素04醋酸去氨加压素05缩宫素06卡贝缩宫素07替尔泊肽08比伐卢定09醋酸阿托西班10醋酸亮丙瑞林11醋酸戈舍瑞林12醋酸地加瑞克13醋酸特立帕肽14利那洛肽15奥曲肽16生长抑素17醋酸西曲瑞克18醋酸艾塞那肽19普卡那肽20辛卡利特21阿巴帕肽22艾替班特23依替巴肽24齐考诺肽25鲑鱼降钙素26普兰林肽27胸腺法新28后叶加压素29帕瑞肽30恩夫韦肽31精氨酸加压素32阿拉瑞林04 联系我们深圳市健元医药科技有限公司地址:深圳市坪山区坑梓街道金辉路14号深圳市生物医药创新产业园1号楼8楼9楼电话:0755-86350988 黄先生15818682250网址:http://www.jymedtech.com/欢迎您来咨询交流识别二维码添加微信好友8月03-04日 第五届中国国际生物&化学制药博览会限时免费报名中,点击图片了解会议详情↓↓
疫苗核酸药物
100 项与 鲑鱼降钙素(Nektar Therapeutics) 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 高钙血症 | 临床1期 | - | - | |
| 骨质疏松症 | 临床1期 | - | - |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
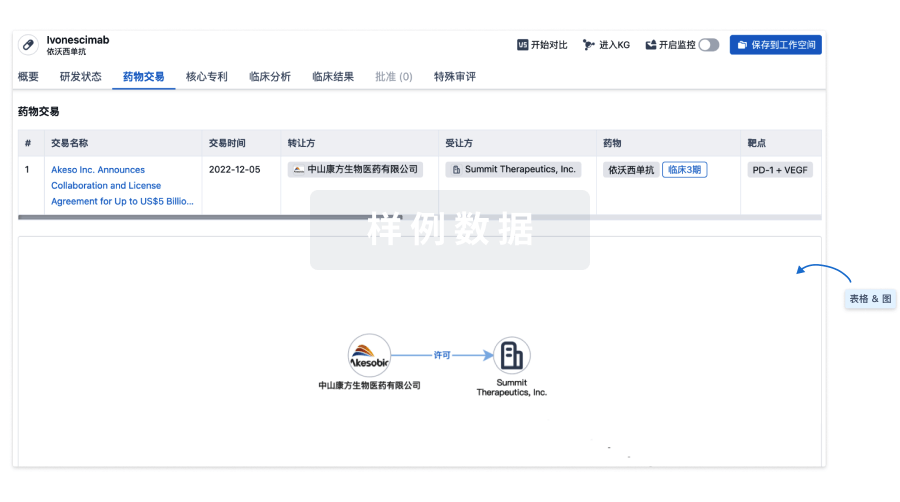
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
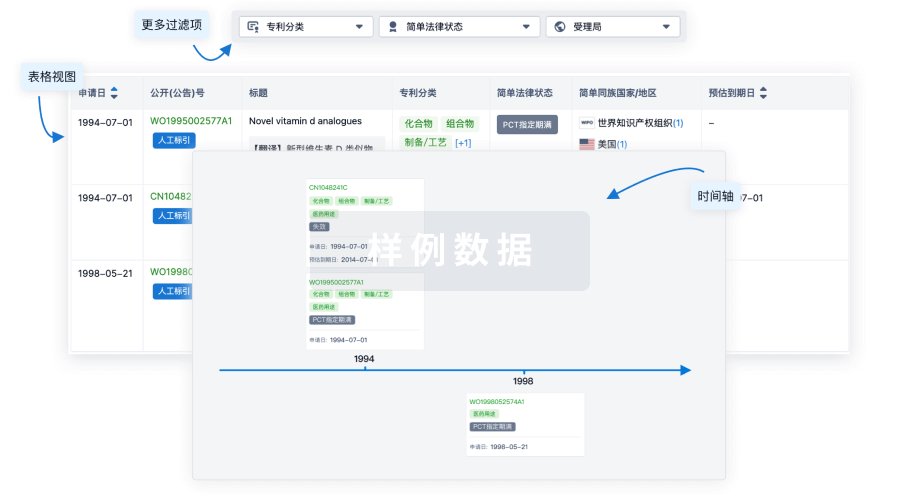
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
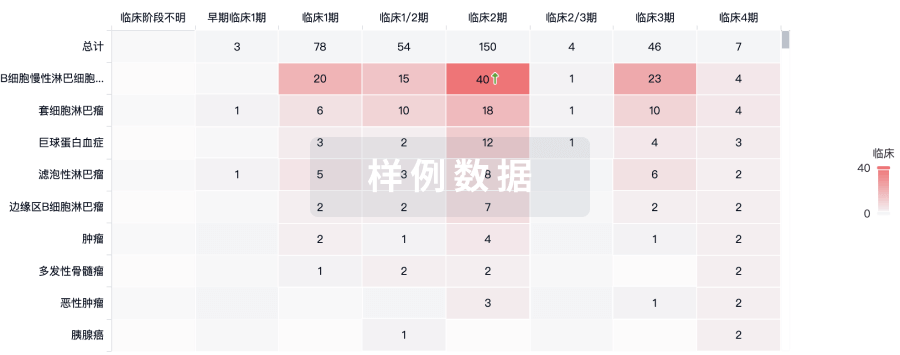
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
批准
利用最新的监管批准信息加速您的研究。
登录
或
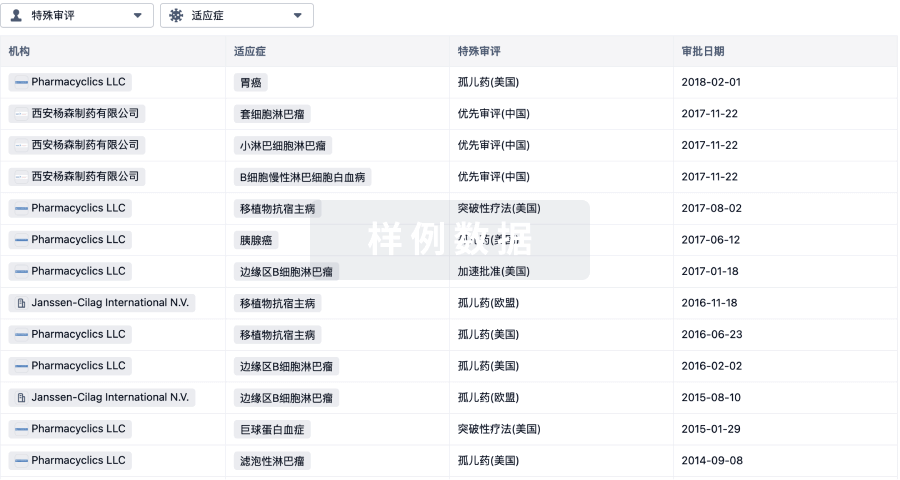
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
