更新于:2024-09-19
Era-379
更新于:2024-09-19
概要
基本信息
原研机构 |
在研机构 |
非在研机构- |
最高研发阶段临床前 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
关联
100 项与 Era-379 相关的临床结果
登录后查看更多信息
100 项与 Era-379 相关的转化医学
登录后查看更多信息
100 项与 Era-379 相关的专利(医药)
登录后查看更多信息
4
项与 Era-379 相关的新闻(医药)2024-07-12
深度聚焦多肽、多肽偶联药物研发、质控、工艺开发,展位咨询&免费入场券:联系电话181 1603 6798,扫码立即获取免费入场券:
1、诺和诺德Wegovy(司美格鲁肽)和礼来Mounjaro(替西帕肽)引爆降糖减肥市场
2021年中诺和诺德推出Wegovy(司美格鲁肽)后,引起了市场的剧烈轰动,公众和名人的竞相追求,导致药物供不应求和社交媒体风暴,一时“洛阳纸贵”。
图例:钢铁侠马斯克使用司美格鲁肽后减重效果明显
不过,后起之秀礼来的糖尿病药物Mounjaro(替西帕肽)有望在减肥领域超越司美格鲁肽,于4月发布的数据显示该药物的最新III期减重数据优异,。
图例:替西帕肽III期减重数据明显
据测算,司美格鲁肽和替西帕肽这两种药物将每年创造数十亿美元的销售额。虽然创新药的研发失败率远高于成功率,但巨大的市场想象空间仍使一众药企对该领域药物的开发充满热情。
司美格鲁泰和替西帕肽最初设计的适应症均是用于临床降糖药物,而减肥的适应症是“预料之外”的适应症拓展。司美格鲁泰是GLP-1类似物,可以和GLP-1受体结合,激活下游通路从而起到降糖减重的作用。
替西帕肽是GLP-1/GIP双通道激动剂,激活GLP-1受体和葡萄糖依赖性胰岛素促泌多肽(GIP)的肠道激素。通过同时作用于GLP-1和GIP这两个通道,替西帕肽可能比仅使用GLP-1激动剂的减重效果更优。
胰高血糖素样肽-1,英文全称Glucagon-like Peptide-1,简称:GLP-1。是一种由肠道内分泌L细胞和脑干孤束核内的某些神经元在进食后产生和分泌的活性肽类激素。其通过结合GLP-1受体(GLP-1R),激活受体的信号传导,起到增加胰岛素分泌、抑制胰高血糖素分泌、减缓胃肠道蠕动、抑制食欲等的生物学功能,从而可以降低体内血糖水平和食欲,有助于控制体重和血糖。在临床上,GLP-1类似药物已经被广泛地用于2型糖尿病和肥胖的治疗。
Uncle in town,公众号:胖猫的生命医学札记GLP-1药物延长半衰期技术(上)
图例:司美格鲁肽(上)和替西帕肽(下)
在替西帕肽为期72周的SURMOUNT-1肥胖试验中,接受最高剂量的替西帕肽患者平均减重比接受安慰剂的患者多出17.8%。对应的,在司美格鲁肽这边,与安慰剂相比,司美格鲁肽试验参与者的体重减轻了12.4%。
不过由于缺乏头对头临床试验,直接对两者的效果进行比较是不合理的。一些分析师预测,替西帕肽在肥胖症的销售巅峰时期将超过100亿美元,而司美格鲁肽约为80亿美元。
2、下一代的GLP-1在哪里?——改进和升级
然而,GLP-1激动剂并不是适合每一个肥胖症患者。哈佛医学院的肥胖医学专家Fatima Cody Stanford表示,尽管该类药物的长期安全性数据令人放心,但一些患者对这些药物没有反应。在Wegovy STEP试验中,有四分之一的参与者对药物有反应,但会出现恶心、腹泻或呕吐的轻微副作用。
图例:GLP-1药物的副作用
这两款药物均需要注射给药,给药方式的不便也是临床依从性的障碍。此外,司美格鲁肽每月的费用超过1300美元,并需长期使用以保持体重稳定。停药一年后,患者体重还会反弹(据报道会反弹三分之二)。这促使研究者们寻找下一代的降体重替代方案。
下一波减重药物的目标是对第一代药物进行改进和升级,使得药物的疗效、便利性或耐受性更优。诺和诺德正在进行口服塞格列肽的更高剂量的试验;IIIa期临床研究的初步结果显示,在68周的减重效果与注射剂版本相似。辉瑞和Sosei Heptares的口服GLP-1受体激动剂丹格列酮(Danuglipron)在一项二期研究中也显示除了显著的减重效果,不过该药物需要每天两次服用。
图例:丹格列酮(Danuglipron)临床效果
另外,其他公司也在追随礼来的双通路组合路线,将GLP-1激动剂与GIP调节效应相结合。GIP是小肠K细胞在食物刺激下分泌的激素,它可以增强胰岛β细胞的胰岛素反应。Viking Therapeutics是设置了GLP-1/GIP双重通路管线的公司之一,该公司于3月28日公布了其皮下给药的一期试验结果,并启动了一项口服每日一次制剂的一期试验。
图例:GIP和GLP-1药物的信号通路
然而,GLP-1和GIP并不仅仅是叠加的关系。这两个激素共同调节食欲、食物摄入和能量消耗,但它们需要被仔细平衡。
安进的双特异性抗体AMG 133结合了GLP-1激动和GIP拮抗作用。这种组合在开展的110名的肥胖患者的I期试验中,减重效果达到了14.5%。
图例:安进AMG 133的作用机制
柏林格格殷格翰/Zealand Pharma、礼来、阿斯利康和Altimmune等生物制药公司正在测试直接作用于胰高血糖素受体的化合物,结合GLP-1一起,进行降糖。临床前和早期人体研究还包括三重通路(GLP-1、GIP和胰高血糖素受体的单分子激动剂)等。
3、其他靶点
目前还有其他调节食欲和能量平衡的激素和信号分子正在进行研究。不废话直接上总结:
图注1:除了Wegovy之外非GLP-1机制的在研降糖减肥药物临床试验总结
(1)诺和诺德——双重机制疗法司美格鲁肽联合卡格列肽
2023年第83届美国糖尿病学会科学会议(ADA 2023)于当地时间6月23日在美国圣地亚哥举行。会议期间公布了一项研究,该研究评估了CagriSema(司美格鲁肽联合卡格列肽)应用于2型糖尿病患者的有效性和安全性。结果显示,在2型糖尿病患者中,与司美格鲁肽或卡格列肽单药治疗相比,CagriSema治疗改善了血糖控制,并显著减轻体重,且耐受性良好,无新的安全性信号。 根据ADA2023官方新闻稿描述,该研究是第一个评估CagriSema(联合给药)对比司美格鲁肽(单药)或卡格列肽(单药)在2型糖尿病患者中的有效性和安全性研究。
图注2:CagriSema组合疗法Phase II临床效果
(2)Scohia——GPR40激动剂
Scohia等公司正在寻求通过激活GPR40(也称为游离脂肪酸受体-1)来调节胰岛素和GLP-1的分泌;GPR40是一种由中长链脂肪酸的内源性配体激活的G蛋白偶联受体(GPCR)。GPR40在胰腺β细胞和肠内分泌细胞中表达,它在生理上调节胰岛素、胰高血糖素样肽-1(GLP-1)和葡萄糖依赖性胰岛素性多肽(GIP)的分泌。增加胰岛素分泌的策略以及GLP-1和GIP激动剂的活动将有效改善人类的糖尿病和肥胖。
图注3:GPR40激动剂作用机制示意图
(3)Shionogi——催化三酰甘油生成的酶
Shionogi的项目则抑制单酰甘油酰基转移酶,这是一种催化三酰甘油生成的酶,从而影响肠道激素的释放。
图注4:MGAT2抑制剂在代谢紊乱治疗中的作用机制:在小鼠肝脏中,抑制MGAT1已被证明可以改善胰岛素敏感性和肝脏脂肪变性。在人肝脏中,MGAT2/MGAT3的表达与进展相关在NAFLD中,在小肠中,MGAT2抑制导致TAG的吸收和合成以及肠促胰岛素分泌的变化。这些行动有助于减轻体重,改善胰岛素敏感性和高甘油三酯血症,并预防NAFLD进展。
(4)Aardvark Therapeutics——TAS2R激动剂
致力于唤醒在肥胖症中被破坏的自然肠道激素。这家生物技术公司使用具有极苦味的化合物,靶向口腔和肠道中的特定受体,触发抑制食欲的激素,如GLP-1、GIP、PYY和胆囊肽。Aardvark的味觉受体2(TAS2R)激动剂是口服的,但几乎只在肠道中起作用并停留。这种化合物名为ARD-101,是一种苦味化学物质丹尼酮的盐,丹尼酮被用于防止冷却液和其他产品的摄入。首席执行官Tien Lee表示:“我们让身体误以为自己受到了毒素的挑战。”Aardvark Therapeutics已经完成了肥胖症和胃肠手术后的2期试验。结果尚未公布,但CEO表示,即使低剂量也能引起积极的代谢变化,且没有严重的副作用。该化合物还能减少与肥胖相关的炎症,而GLP-1激动剂无法解决这个问题。Aardvark目前正在对普拉德-威利综合征进行2期试验,这是一种罕见的遗传病,特征是持续的饥饿、肥胖和糖尿病。
图注5:炎症和代谢疾病常常与肠脑循环有关系
(5)Aphaia Pharma——唤醒远端肠道对营养物质敏感的细胞
Aphaia Pharma追求的是一种不同的方法,即重新唤醒远端肠道中对营养物质敏感的细胞,这些细胞在肥胖时变得不那么敏感。这种损失可能是由于肠道蠕动的变化和上肠道中更多食物的吸收,这使得下肠道细胞无法接触到营养物质,并可能因炎症而加重。通过使用特制的胶囊直接将葡萄糖输送到这些细胞中,Aphaia旨在恢复正常的食物反应。“GLP-1激动剂并不针对神经末梢或其感知营养物质的能力,”首席科学官Steffen-Sebastian Bolz说,这暗指了控制食欲、饱腹感和能量利用的全方位信号,不仅包括内分泌,还包括神经内分泌和神经途径。Bolz表示,Aphaia的方法可能会辅助GLP-1激动剂,帮助维持体重减轻。人体早期试验也显示了独立的好处。20名肥胖患者的未公布的1期数据显示,治疗上具有相关性的GLP-1、PYY、oxyntomodulin(激活GLP-1和胰高血糖素)、glicentin和其他肠道激素释放。这种反应与胃旁路手术后的反应相当,后者是最有效的减重工具之一。一项招募了150名患者的APH-012候选药物2期试验正在进行中。
图注6:APH-012的作用机制以及优势展示
(6)Versanis Bio——关注肌肉质量,减少胰岛素抵抗和增强技术代谢
Versanis Bio的关注点是瘦肌肉质量。这种方法除了促进脂肪减少外,还具有减少胰岛素抵抗和增加基础代谢率等几个代谢优势。单克隆抗体bimagrumab最初是诺华制药公司为肌肉衰退症开发的,它靶向活化因子II受体。这种抗体阻断了肌肉降解的影响,减少了脂肪质量,尽管机制尚不清楚。它正在进行2b期试验,作为单药(静脉给药)和与semaglutide联合用于450名超重或肥胖患者。
图注7:Activin信号通过ActRII受体直接促进脂肪储存,成为内脏脂肪积累和肥胖的关键驱动因素。Bimagrumab是一种强效的首创单克隆抗体,可以阻断脂肪细胞中的ActRII信号传导,从而动员和代谢脂肪。
引起肌肉流失和体重减少,但它改善了整体瘦肉与脂肪的比例。Bimagrumab需要改进这一点;公司还希望它能避免与胰高血糖素治疗相关的体重反弹。其他人试图增加能量消耗、抑制脂肪吸收或利用有益的肠道细菌诱导减重。
图注8:通过ActRII受体的信号传导抑制肌肉生长并促进萎缩。阻断骨骼肌中的激活素信号可以抑制这种萎缩,并可以促进肌肉质量的增加,帮助肥胖患者改善身体成分和新陈代谢,同时减少脂肪。
(7)Rivus Pharmaceuticals利用线粒体解偶联
Rivus Pharmaceuticals利用线粒体解偶联,这是一种将脂肪和糖的氧化能量转化为热量而不是产生ATP的自然过程。Rivus的主要口服化合物HU6的未公开2期研究减少了肝脏、内脏和全身脂肪,并保留了肌肉质量,而没有改变饮食或运动。心血管和代谢健康指标也有所改善。
图注9:Rivus Pharmaceuticals利用线粒体解偶联平台
(7)EraCal Therapeutics——斑马鱼早期发现平台筛选抗肥胖化合物
EraCal Therapeutics使用基于斑马鱼的发现平台早期筛选潜在的抗肥胖化合物。这家位于瑞士斯利伦的公司的“整体器官”方法可以捕捉到比传统的还原主义筛选方法(使用细胞系或器官样本)更多的潜在药物的广泛生理和行为效应,该公司认为。该平台发现了利蒙巴替的缺乏行为选择性——它影响了食欲之外的其他行为,并产生了潜在更选择性和更强效的口服食欲抑制剂。临床前研究的ERA 379靶向一个未公开的肝脏蛋白质来改变外周营养感知。与胰高血糖素不同,ERA 379不依赖于连接肠道与大脑的迷走神经;因此,它可能与GLP-1激动剂协同作用。EraCal与诺和诺德达成了研究协议,寻找新的肥胖药物靶点,并与雀巢健康科学公司达成了另一个协议,寻找有益于新陈代谢的营养保健品。
图注10:EraCal开创了以斑马鱼为基础的药物发现技术,专注于代谢性疾病。通过斑马鱼为基础的表型筛选平台,EraCal已经开发出一系列候选药物,并且在临床前阶段展示了其疗效,其中包括其主力候选药物Era-379
总结:
在对抗肥胖这一复杂多样的疾病中,需要多种治疗和组合方法。科学家们才刚刚开始揭开肥胖的奥秘,肥胖最近才被认定为一种疾病,而不仅仅是不良生活方式的选择。纽约威尔康奈尔医学院代谢疾病专家路易斯·阿罗尼表示:“肥胖是新的高血压。”他继续说道,GLP-1激动剂的出现只是“刚刚开始”。其他方法也将出现,包括可以间断使用的药物。
参考文献:
1、After GLP-1, what’s next for weight loss?
2、Descamps-Solà M, Vilalta A, Jalsevac F, et al. Bitter taste receptors along the gastrointestinal tract: comparison between humans and rodents[J]. Frontiers in Nutrition, 2023, 10.
3、Senior M. After GLP-1, what’s next for weight loss?[J]. Nature Biotechnology, 2023.
4、Yabe D, Seino Y. Two incretin hormones GLP-1 and GIP: comparison of their actions in insulin secretion and β cell preservation[J]. Progress in biophysics and molecular biology, 2011, 107(2): 248-256.
5、Garvey W T, Frias J P, Jastreboff A M, et al. Tirzepatide once weekly for the treatment of obesity in people with type 2 diabetes (SURMOUNT-2): a double-blind, randomised, multicentre, placebo-controlled, phase 3 trial[J]. The Lancet, 2023.
6、https://www.amgen.com/stories/2022/12/targeting-obesity-using-biology-not-behavior
7、https://www.biochempeg.com/article/355.html
8、各公司官网等
END
免责声明:本文信息来源于网络,本文仅作知识交流与分享及科普目的,不涉及商业宣传,不作为相关医疗指导或用药建议。文章如有侵权请联系删除。
深度聚焦多肽、多肽偶联药物研发、质控、工艺开发,7月相约苏州,联系电话18116036798上下滑动查看议程
7月25日上午:主会场
多肽药物蓝海布局
9:00-9:30
李学臣,香港大学化学系理学院副院长
多肽药物和蛋白偶联的新策略
9:00-9:30
王珠银,深圳肽盛生物科技有限公司董事长
3D结构多肽库的构建和靶向穿膜肽筛选
9:30-10:00
马亚平,深创生物董事长
靶向核素药物研究与开发
10:30-10:50
茶歇&交流
10:50-11:20
徐寒梅,中国药科大学教授;南京安吉生物科技有限公司创始人
新靶点多肽药物发现及PDC药物研究进展
11:20-11:50
钱海,中国药科大学理学院院长兼药物科学研究院新药研究中心主任
话题确认中
11:50-12:20
圆桌讨论:多肽药物脱颖而出的关键、未来如何保持高热度、内卷何时到来?
刘东舟,华东医药首席科学官/创新药全球研发中心总经理
容明强,成都佩德生物医药有限公司董事长
马亚平,深创生物董事长
王珠银,深圳肽盛生物科技有限公司董事长
邵军,同宜医药(苏州)有限公司首席技术官
部分嘉宾确认中
12:20-14:00
午餐&休息
7月25日下午:论坛一
多肽药物研发进展
14:00-14:30
周建伟,南京医科大学教授/南京明人医药科技有限公司创始人
基于JWA基因的多肽创新药研究
14:30-15:00
容明强,成都佩德生物医药有限公司董事长
基于生存策略的动物毒素多肽新药开发
15:00-15:30
江苏万略医药科技有限公司
话题确认中
15:30-15:50
茶歇&交流
15:50-16:20
韩俊峰,上海贺普药业股份有限公司总裁
贺普拉肽研究进展
16:20-16:50
方小翠,国家纳米科学中心,高级工程师
肿瘤免疫治疗用靶向溶瘤多肽的药物转化
16:50-17:20
张晓君,石药集团北京研究院制剂四所所长
多肽药物长效递送研发进展
7月25日下午:论坛二
多肽药物质控与生产
14:00-14:30
邵军,同宜医药(苏州)有限公司首席技术官
多肽类药物工艺与质量控制要点
14:30-15:00
姜建军,江苏诺泰澳赛诺生物制药有限公司,多肽事业部总经理/集团副总经理/研究院副院长
多肽药物合成新工艺
15:00-15:30
大西 弘晃,三菱化学株式会社
Purification of Cyclic Peptide and Its Analogues with Polymeric Separation Media
15:30-15:50
茶歇&交流
15:50-16:20
李子刚,北京大学深圳研究生院,化学生物学与生物技术学院执行院长/深圳湾实验室,坪山生物医药研发转化中心主任
新颖稳定多肽方法学开发及其在多肽药物开发中的应用
16:20-16:50
苏贤斌,南京工业大学教授、博士生导师
连续流动绿色多肽合成(拟定)
16:50-17:20
刁星星,中国科学院上海药物研究所研究员,课题组长/苏州锐迪欧医药科技有限公司创始人
新类型药物PDC LN005体外、体内代谢研究策略
7月26日上午:论坛一
多肽药物研发进展
9:00-9:30
陈小新,广东众生睿创生物科技有限公司联合创始人、董事、总裁
基于GLP-1的单分子多重受体激动剂治疗肥胖和NASH的研究进展
9:30-10:00
谢天,甘李药业股份有限公司,医学事务部负责人
GLP-1研发的挑战与布局
10:00-10:30
温晓芳,浙江道尔生物科技有限公司副总裁
GLP-1/GCG/FGF-21三靶点激动剂在NASH中的临床前开发
10:30-10:50
茶歇&交流
10:50-11:20
景书谦,鸿运华宁(杭州)生物医药有限公司 创始人、董事长兼首席执行官
GLP药物研发进展及商业化前景
11:20-11:50
夏帅,复旦大学基础医学院青年研究员
广谱抗冠状病毒多肽类融合抑制剂的研究
11:50-14:00
午餐&休息
14:00-14:30
张传亮,青岛科技大学化工学院,副教授
长效降糖减重药物的差异化开发:基于BH3模拟肽的PTP1B/TC-PTP抑制剂/降解剂的设计与研发
14:30-15:00
韩智豪,中国药科大学特聘副研究员,硕士生导师
基于仿生多肽的放射性药物研究
15:00-15:30
杨浩哲,香港交易所,环球上市服务部助理副总裁
香港交易所助力医药企业融资上市
7月26日上午:论坛二
多肽药物质控与生产
9:00-9:30
丁伟,南京知和医药科技有限公司副总,多肽首席科学家
多肽药物质量研究中的常见问题与解决方案
9:30-10:00
刘磊,江苏大学材料科学与工程学院副院长
多肽基功能生物界面用于肿瘤细胞的捕获与分离
10:00-10:30
曹宇,重庆派金生物科技有限公司生产总监
长效胰岛素结构相关杂质控制和表征
10:30-10:50
茶歇&交流
10:50-11:20
赵军锋,广州医科大学教授
无保护氨基酸合成多肽
11:20-11:50
郭建,上海胜普泽泰医药科技有限公司副总裁
多肽偶联药物CMC要点分享
11:50-14:00
午餐&休息
7月26日下午:论坛二
PDC药物研发
14:00-14:30
张普文,浙江汉鼎医药有限公司总经理
多肽糖胺聚糖等新型PDC药物的研发
14:30-15:00
张富尧,上海弼领生物创始人、董事长&CEO
纳米PDC:用于药物高效递送的纳米列车
15:00-15:30
马步勇,上海交通大学药学院教授
蛋白质动态结构的AI预测与应用
15:30-16:00
朱勍,浙江工业大学,生物制药与生物材料研究所所长
C-C键环肽及其偶联药物新进展
戳“阅读原文”立即报名多肽药物论坛吧!
临床3期生物类似药
2024-05-12
·药渡
来源:药渡撰文:幻目 编辑:哦呼司美格鲁肽巨大的商业成功,卷起了减肥药物的研发热潮,诺和诺德为巩固其在肥胖症领龙头地位在近两年完成了多项并购及合作交易,从药物机制、优化药效等各个维度,布局自身的减肥药产品管线,本文对诺和诺德近两年针对肥胖适应症的多项交易进行总结。Metaphore Biotechnologies2024年5月,诺和诺德(Novo Nordisk)与签订研究协议达成一项总额高达6亿美元的合作,共同开发多达两种以上用于治疗肥胖症的下一代GLP-1受体激动剂。Metaphore是一家在2021年由Flagship创立并在2023年5月获得了5000万美元融资的生物技术公司,Metaphore专注仿生学,通过模拟自然界中发现的“生物活性”分子之间的相互作用来设计药物,开发治疗自身免疫疾病、代谢疾病以及癌症的药物。该公司的MIMIC平台是一种计算驱动的生物平台,将机器学习和分子模拟相结合以设计新型疗法,尤其专注于靶向之前难以攻克的药物靶点。MIMIC平台原理:首先确定要模拟的药效团,以高分辨率观察药效团,对模拟物进行改造,使其具有我们所靶向适应症的理想特性,例如功能、特异性、选择性和多靶点。通过精确调整模拟物以获得所需的特异性来最大限度地减少脱靶相互作用。根据 Metaphore 的说法,将通过创建 “药效团”或启动特定级联的分子基本特征的高分辨率图谱,来支持下一代GLP-1候选药物的开发。MIMIC设计的化合物可以对其靶标产生更好的特异性和选择性,或者会具备多种亲和力、更长半衰期和其他类似的功能。Novo利用Metaphore专有的MIMIC平台开发可以激活GLP-1受体并影响相关途径的多靶点研究疗法。这些候选药物将被设计为具有长效效果。EraCal Therapeutics2024年1月,诺和诺德签署价值2.56亿美元的合作协议,赋予Novo开发和商业化EraCal口服小分子减肥药项目的独家权利。瑞士初创公司EraCal Therapeutics是一家临床前阶段的公司,专注于开发代谢综合征(主要是肥胖症)的新疗法。EraCal的主要产品Era-379是一种口服活性小分子食欲抑制剂。每日一次口服Era-379单药治疗可在2周内将肥胖小鼠的体重减轻20%以上。Era-379的靶点是一种未公开的新型蛋白质,可驱动外周肝脑信号传导,并在体内与胰高血糖素样肽-1(GLP-1)靶向剂协同作用。Era-379预计将于明年进入非人类灵长类动物的概念验证研究。Omega Therapeutics2024年1月,诺和诺德与Flagship Pioneering旗下的Omega达成合作,将利用该公司平台开发表观基因组学调控物,并使其成为肥胖症管理新手段的组成部分。Omega Therapeutics是一家临床阶段生物技术公司,引领新型表观基因组学mRNA药物的开发。在世界知名的表观遗传学领域专家所开展的突破性研究基础上,Flagship Pioneering于2017年创立了Omega Therapeutics。Omega由一支经验丰富且成就卓越的领导团队引领,在创新和卓越的运营方面拥有出色的成就。基于OMEGA平台,公司拥有丰富的治疗候选药物管线,涵盖肿瘤学、再生医学、包括免疫学在内的多基因疾病领域以及选择性单基因疾病领域。OMEGA平台利用公司在基因调控、基因组结构和表观基因组学方面的深入见解,设计可控的表观基因组mRNA药物,通过对基因表达进行转录前修饰(Omega所采用的手段可对几乎所有人类基因进行可控的表观基因组学修饰,包括以前被认为无法通过药物和难以治疗的靶点,且无须改变其自身核酸序列),可精确地在转录前靶向和调控基因表达,将异常基因表达恢复到正常范围,纠正疾病的根本原因。OMEGA的专有平台利用人体固有机制对细胞成分和基因表达进行调控,有潜力创造出能够提高产热作用并进而提高代谢活动的表观基因组学调控物。从而控制体重。Inversago Pharma2023年8月,诺和诺德以11亿美元价格收购专注代谢紊乱疾病的药企Inversago Pharma,Inversago Pharma总部位于加拿大,是一家临床阶段公司,是开发下一代CB1受体(I型大麻素受体)阻滞剂疗法的领导者,旨在帮助患有代谢和纤维化疾病相关并发症的患者提供新的治疗方案,以改善受各种心脏代谢紊乱影响的患者的生活。CB1受体在大脑的特定区域(如下丘脑)中的活动与食欲和食物摄取有关。CB1受体的激活可以刺激食欲。诺和诺德对Inversago的收购包括该公司的主要开发药物INV-202,一种口服CB1阻断剂。INV-202旨在优先阻断脂肪组织、胃肠道、肾脏、肝脏、胰腺、肌肉和肺等外周组织中的受体蛋白CB1,从而治疗一系列心脏代谢疾病,包括糖尿病肾病。INV-202在1b期试验中显示出减肥潜力,在28天的治疗期内,INV-202在具有代谢综合征特征的受试者中具有良好的安全性、耐受性、药代动力学和药效学作用。接受INV-202治疗的受试者显示出临床上显著的、渐进的体重下降,平均下降3.5公斤,而服用安慰剂的受试者的体重平均增加了0.55公斤(P<0.01)。此外,接受INV-202治疗的受试者相较于接受安慰剂的受试者在血脂和血糖控制方面也展现出积极的趋势,包括糖化血红蛋白(HbA1c)、甘油三酯和低密度脂蛋白胆固醇的降低。该产品还在开发用于糖尿病肾病等代谢和纤维化疾病的其他管线。Embark Biotech2023年8月,诺和诺德公司以高达4.71亿欧元(5.12亿美元)的价格收购丹麦公司Embark Biotech,发现和开发治疗肥胖和相关合并症的新型药物。以期望在蓬勃发展的减肥领域保持优势。Embark Biotech是2017年从哥本哈根大学诺和诺德基础代谢研究基金会中心(CBMR)分出来的一家公司。目前,Embark正在开发一款EMB1的激动剂,这是一种全新的,从未被报道过的脂肪细胞G蛋白偶联受体,它是一种抑制食欲、增加能量消耗和提高胰岛素敏感性的新靶点。可以通过加速葡萄糖摄取和增加能量消耗来促进减肥。诺和诺德在糖尿病和肥胖领域已经处于世界前列, 但依据路透社据报道,2024年3月,礼来的减肥药Zepbound(GLP-1, GIP双靶点)在美国的新处方中超过了Novo的Wegovy。此外,罗氏、辉瑞、勃林格殷格翰等众多公司纷纷入局使GLP靶点的竞争更加激烈。为保持肥胖领域的领先地位,诺和诺德不断壮大自己实力,期望在人工智能等新技术和全新的药物靶点上有所突破。END参考文献:1. Flagship Pioneering and Metaphore Biotechnologies Announce Research Collaboration with Novo Nordisk to Develop Next-Generation Therapeutics for Obesity Management. Retrieved May 9, 2024 from https://metaphorebio.com/news/2. 超43亿!诺和诺德出手下一代减肥疗法 动脉新医药3. 各公司官网*声明:本文仅是介绍医药疾病领域研究进展或简述研究概况或分享医药相关讯息,并非也不会进行治疗或诊断方案推荐,也不对相关投资构成任何建议。内容如有疏漏,欢迎沟通指出!点击下方“药渡“,关注更多精彩内容中国CGT领域最强城市排名,谁位居TOP1?PROTAC设计中Linker特性的探索与创新减肥神药司美格鲁肽(Ozempic)被爆生产成本低于5美元/月?点击蓝字 关注我们
信使RNA并购
2024-02-17
作者|YY 作为当今最炙手可热的药物,诺和诺德的Wegovy(司美格鲁肽)和礼来的Zepbound(替尔泊肽)之间的直接较量代表着这个领域最高水平的抗衡。这两款GLP-1受体激动剂之间的华山论剑被视为肥胖症领域内最高的竞争级别。减肥药在2030年前达到1000亿美元已经被很多华尔街分析师视作必然。高盛预计2030年美国将至少有1500万肥胖症成年患者使用减肥药物。从图1给出的Wegovy/Ozempic和Mounjaro(Zepbound用于糖尿病的另称)与其它超级重磅炸弹药物(Liptor, Humira, Viagra)的市场占有增长趋势对比来看,就不难发现GLP-1药物自从上市以来就迅速攫取了大量的销售额。 图1. Ozempic/Wegovy,Moujaro与其它超级重磅炸弹销售额增长趋势对比。(图片来源:Bloomberg)Morgan Stanley分析师预计2024年Zepbound将实现22亿美元的销售额,而美国银行更加乐观,他们给出的今年Zepbound年销售额预计达到27亿美元的水准,也有分析师给出了37.9亿美元的预测。反观诺和诺德的GLP-1资产,如果将semaglutide为活性物质的药物Ozempic, Wegovy和Rybelsus“合并同类项”,semaglutide在2024年的销售总额估计能够超过280亿美元,从而超越Keytruda成为2024年全球药王(图2)。分析师预测,2024 年诺和诺德和礼来的销售收入将分别增长至少 15%。Ozempic/Wegovy 和Mounjaro/ Zepbound 的总销售额预计将从2023的220亿美元增加到2028年的570亿美元。 图2. 预计2024年全球销售额前十药物。(图片来源:Evaluate)无论Wegovy(司美格鲁肽)和Zepbound(替尔泊肽)在2024年将交出怎样的业绩,从目前情况来看礼来和诺和诺德在未来相当长的一段时间内称霸减肥药市场将没有悬念。礼来的Zepbound将逐渐增加市场占有率,在2029年前后甚至有望领先诺和诺德一个身位(图3)。这两家减肥药巨头之间的较量将是减肥药领域内长期的主旋律。 图3. Bloomberg预计2030年减肥药市场规模(按公司以及减肥药)。(数据及图片来源:Bloomberg) 01 诺和诺德:“受体差异化”赌明天诺和诺德显然并不满足于现有的支柱资产Wegovy。尽管它目前是减肥药领域无可争议的王者,礼来的Zepbound还需要3-4年才能实现与Wegovy的平起平坐,但诺和诺德最近一系列的行为显示出了它们在减肥药市场占有策略上未雨绸缪的态度。2024年1月传出诺和诺德将花费2.56亿美元收购一项机制尚未经过验证的临床前项目。这种豪掷千金的做法在当今明显收紧的医药并购市场上显得特立独行。在并购交易陷入低潮的情况下,大部分收购方都采取了持币观望并且重点收购临床数据优异的公司或者资产。但诺和诺德这笔2.56亿美元交易的对象却是一家成立于2018年的瑞士初创公司EraCal Therapeutics的资产Era-379。根据报道,Era-379是一款口服小分子GLP-1受体激动剂候选药。虽然诺和诺德CEO Lars Fruergaard Jørgensen在不久前结束的摩根大通医疗保健年会上表示,患者对于皮下注射的GLP-1减肥药依从性很高,但很明显,他们意识到开发小分子减肥药的重要性。这笔交易正是他们战略意图的体现,毕竟直接对手礼来的管线中存在一款众望所归的小分子口服减肥药资产orforglipron,诺和诺德必须选择跟进。Era-379是一款目前还很神秘的候选药,若不是诺和诺德的收购,恐怕不会有太多人留意到它。Era-379的作用机制尚未公开,结构也没有透露,但 EraCal 认为他们的资产是“与众不同”的,并且目标是实现减重的新机制。Era-379 的靶标也处于保密状态,看上去没有走传统的GLP-1受体激动剂的道路,可能也不是常见的GIP或者Glucagon受体激动剂。EraCal透露称,Era-379靶向的是一种参与外周肝脑信号传导的蛋白质,并且它与GLP-1药物可以产生协同作用。在临床前实验中,每日一次口服 Era-379的单一疗法在两周内使肥胖小鼠的体重减轻了 20% 以上。由于Era-379 不结合已知的肥胖症药物靶点,如血清素 5HT2C 或 GLP-1 受体,也不结合经典的神经递质靶点,如多巴胺或大麻素系统,这可能意味着这款小分子药物在目前GLP-1药物副作用方面有望得到突破。在收购Era-379之前,诺和诺德收购了 Embark Biotech 和 Inversago Pharma,与 Omega Therapeutics 建立了合作,并为在竞争日益激烈的领域巩固其领先地位。值得注意的是,诺和诺德的收购对象在开发减肥药物时针对了不同的靶标。Embark的主要减肥资产时EMB1 激动剂。EMB1 是一种名不见经传的脂肪细胞 G 蛋白偶联受体,EMB1激动剂可以通过增加葡萄糖摄取和能量消耗来减轻体重。Embark在研的受体还包括GPR3,这是一种活性 G 蛋白偶联受体,被称为“生热脂肪活性的重要调节剂”。而被诺和诺德斥资10.8亿美元收购的Inversago Pharma,其研究靶标为1 型大麻素受体(cannabinoid receptor type 1), 1 型大麻素受体在新陈代谢和调节人的食欲方面发挥着作用。再加上此次对Era-379的收购,诺和诺德开发减肥新机制,实现更高层次的减肥目标的战略动机已经显露无遗。 02 礼来:一把好牌还要摸从减重数据角度来看,礼来的Zepbound似乎已经领先Wegovy半个身位,尽管市场占有率上赶超对手尚需时日。除了等待Zepbound反超Wegovy之外,礼来的管线中还有一干喷薄欲出的减肥资产,其中最值得关注的是新一代减肥多肽药物retatrutide(图4)和orfoglipron(图5)的III期结果。前者是号称开创减肥药3G(GLP-1/GIP/Glucagon三重受体共激动剂)时代的首创新药,后者是有望最先登场的小分子GLP-1口服减肥药先驱。礼来的研究实验室总裁 Dan Skovronsky在不久前结束的摩根大通医疗保健年会上坦诚,想要在减重数据上超越tirzepatide将是一件非常具有挑战性的目标。然而retatrutide已经给出的2期研究数据,48周平均减重24.2%的表现仍然给人们足够的遐想空间。图4. Retatrutide化学结构。图5. Orforglipron化学结构。Orforglipron 和retatrutide的 III 期肥胖项目正在进行中,预计2025年将获得数据,但礼来将在 2024 年报告 Zepbound 在治疗由肥胖引起的合并症方面的 II 期和 III 期数据。针对心力衰竭和阻塞性睡眠呼吸暂停患者的 III 期临床试验以及针对非酒精性脂肪性肝炎 (NASH,现在被称作MASH) 的 II 期试验将于今年公布。这些数据非常重要,可以帮助人们更好地了解减肥带来的医疗益处的范围,关键是增加付款人报销费用的可能性,这有可能对减肥药的命运产生决定性的影响。除了手中的一副好牌之外,礼来也选择了同诺和相似的外部挖潜的策略。他们去年斥资19.25 亿美元收购了 Versanis Bio,并引入了单克隆抗体 bimagrumab。该抗体针对 II 型激活素 A 和 B 受体,已被证明可以减少体脂量,同时增加瘦体重。礼来计划于 2024 年测试Zepbound与 bimagrumab联合疗法在减肥方面的表现。在减重药领域,诺和诺德和礼来谁能号令天下?从已有数据和商业化布局来看,未来可能各分半壁江山。参考资料:[1] Constantino, A. K. The weight loss drug boom isn’t over yet — here’s what to expect in the year ahead. CNBC. 17. 12. 2023.[2] Tartar, A. et al. New Weight-Loss Drugs Like Wegovy Will Supercharge Pharma Revenue. Bloomberg. 11. 01. 2024.[3] Wienberg, C. Novo Outshined by Smaller Obesity Rival on Danish Stock Market. Bloomberg. 13. 12. 2023.[4] Constantino, A. K. Novo Nordisk to acquire obesity drug maker Inversago Pharma for up to $1 billion. CNBC. 10. 08. 2023.[5] Lilly's phase 2 retatrutide results published in The New England Journal of Medicine show the investigational molecule achieved up to 17.5% mean weight reduction at 24 weeks in adults with obesity and overweight. Eli Lilly Press Release. 26. 06. 2023.[6] Wainer, D. A Tale of Two Pharmas: Can Obesity Firms Continue Their Outperformance in 2024? The Wall Street Journal. 27. 12. 2023.[7] Jackson, M. Lilly To Deliver More Proof Points In Obesity, Keep Building Pipeline In 2024. 23. 01. 2024. 2024活动预告 3月8-9日,XDC唯新不破!2024 BiG ADC专题研讨会 关键词: 临床适应症拓展;靶点&立项;双抗ADC;联用策略;下一代linker-payload;核药▼▌更多分享嘉宾即将揭晓参会注册▼会议门票:审核制(免费);含1场主论坛+4场分论坛,不含餐晚宴门票:费用:2800元/人;含1场主论坛+4场分论坛,3月8日晚宴、3月9日午餐会员/特邀:审核制(免费,仅限BiG会员/特邀嘉宾);权益同晚宴门票共建Biomedical创新生态圈!如何加入BiG会员?
并购
100 项与 Era-379 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 肥胖 | 临床前 | 瑞士 | 2024-01-26 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
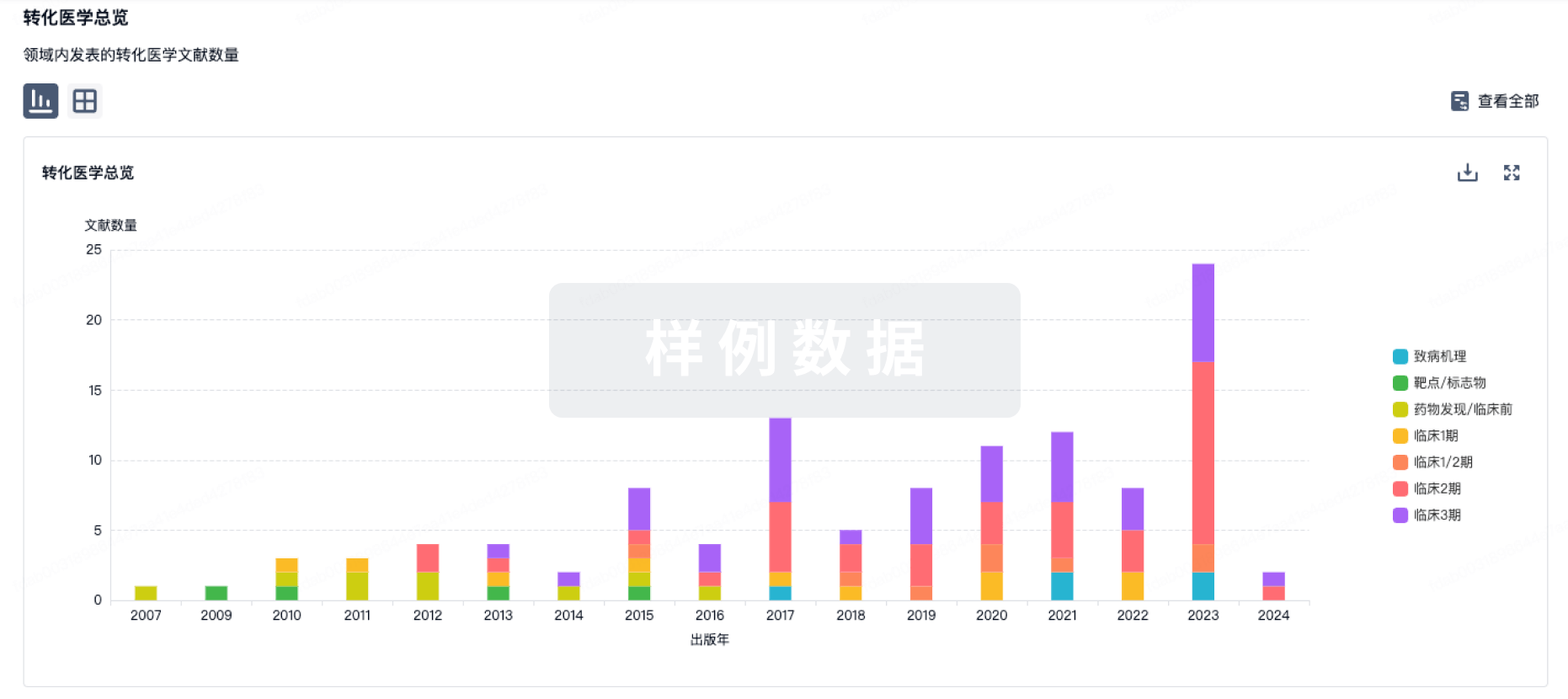
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
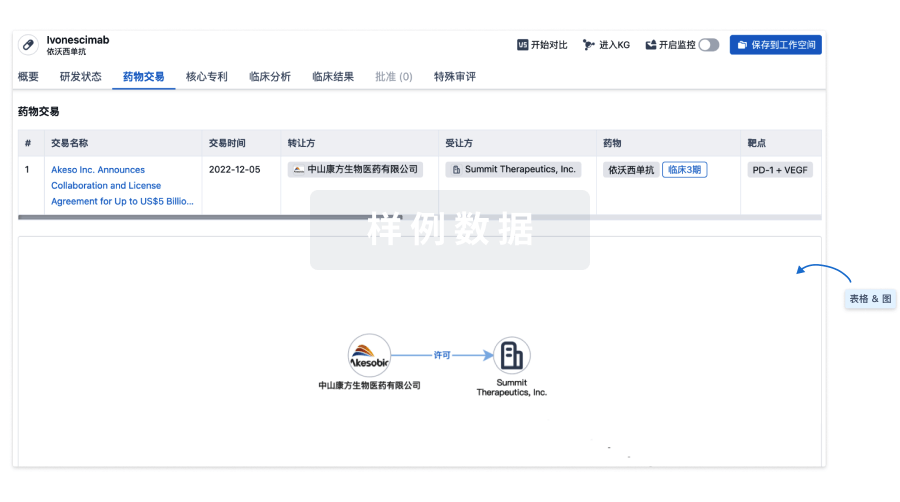
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
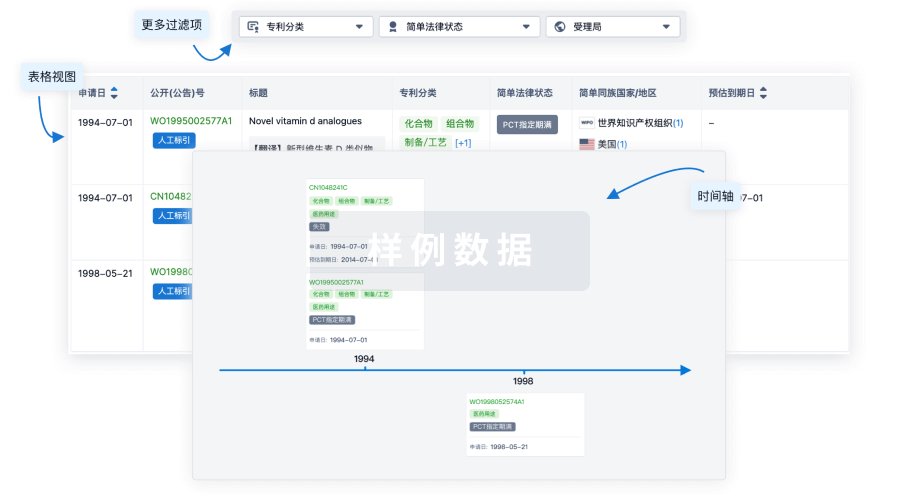
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
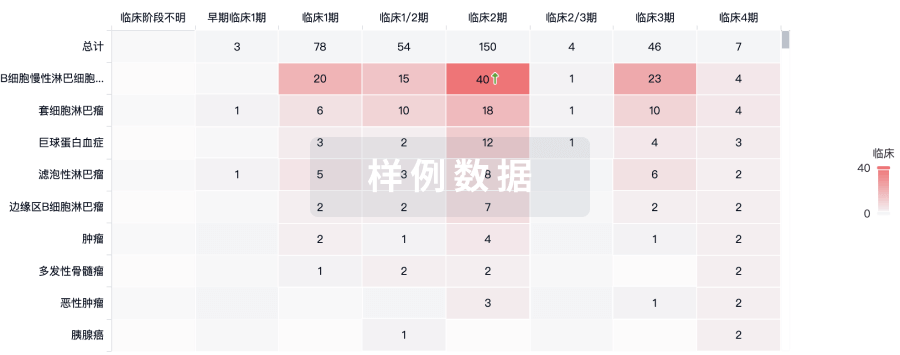
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
批准
利用最新的监管批准信息加速您的研究。
登录
或
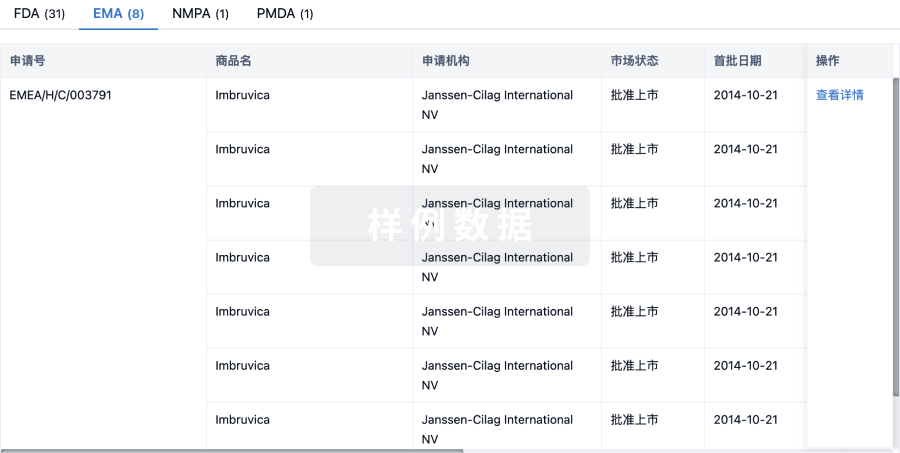
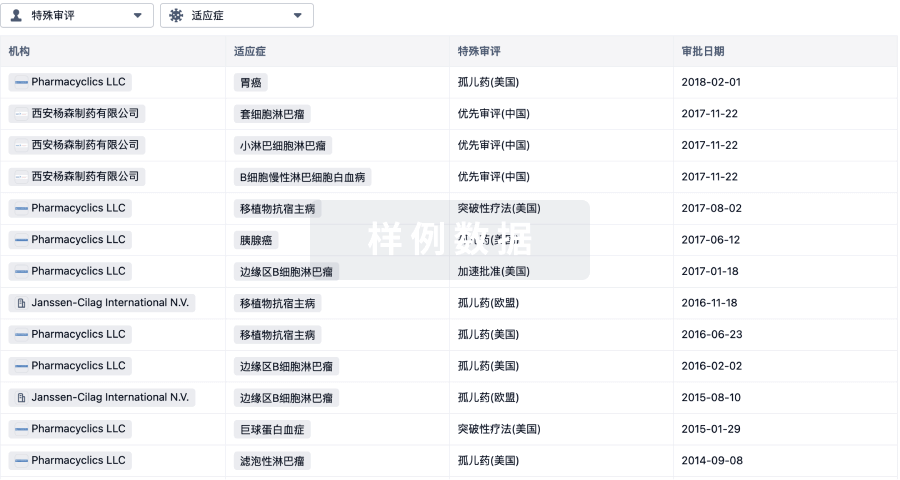
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用
