更新于:2024-09-27
Anti-CLL1 THIOMAB-PBD conjugate(Genentech)
更新于:2024-09-27
概要
基本信息
原研机构 |
在研机构 |
非在研机构- |
最高研发阶段药物发现 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
结构
使用我们的XDC技术数据为新药研发加速。
登录
或

关联
100 项与 Anti-CLL1 THIOMAB-PBD conjugate(Genentech) 相关的临床结果
登录后查看更多信息
100 项与 Anti-CLL1 THIOMAB-PBD conjugate(Genentech) 相关的转化医学
登录后查看更多信息
100 项与 Anti-CLL1 THIOMAB-PBD conjugate(Genentech) 相关的专利(医药)
登录后查看更多信息
4
项与 Anti-CLL1 THIOMAB-PBD conjugate(Genentech) 相关的新闻(医药)2023-08-31
近日,一家2021年成立的生物制药初创公司Aarvik Therapeutics的团队在mAbs期刊上投稿了一篇题为Exploration of the antibody-drug conjugate clinical landscape的文章,详细阐述了ADC药物的前景和未来发展,并对现阶段ADC的现状提出了总结。改文章指出迄今为止,共有超过260种ADC进行了临床试验,其中11款ADC药物成功获得FDA批准,约有164款正在临床试验中但尚未批准,还有92个经过临床试验后停止开发的ADC药物。而对于那些半途而废的ADC们,尽管它们历经失败,从其临床停止的原因而引以为鉴,可能对于ADC赛道具有更深刻的意义,能够为ADC的发展排除错误选项,本文将详细阐述这些ADC的特征。中止ADC的特征总体而言,所有中止的ADC可归因于以下三个原因中的一个或多个:①由于不可耐受的毒性而导致的治疗益处不足。②由于功效不足而导致的治疗益处不优于当前的治疗标准。③商务/商业考虑。不可耐受毒性的原因其中,大约29%的经临床测试的ADC将不可耐受的毒性列为项目终止的原因。这些不可耐受的毒性的原因可能有:①靶向非肿瘤细胞的毒性问题;②外源性抗原表达太高,使得生物暴露度高,没有足够的抗体结合,因此必须使用非常高效力的有效载荷而导致的毒性;③导致有效载荷在非肿瘤区域释放的不稳定Linker;④可能是由于ADC胞饮作用而导致的非靶向毒性;⑤有效载荷代谢转化为毒性更大的代谢物。不可耐受事件的案例从实际上发生的案例来看,例如:1、靶向CD44v6的ADC药物Bivatuzumab mertansine,这款药物由靶向CD44抗人CD44v6抗体与DM1 Payload组成,停止临床的原因在于CD44v6表达于人体皮肤表面角质层,靶向非肿瘤细胞的脱靶毒性导致患者出现了严重至危及生命的皮肤脱落副作用。2、靶向CD138的ADC Indatuximab ravtansine,CD138在上皮细胞中表达,而皮肤和胃肠道的上皮细胞被靶向后,可以作为可溶性成分流入血浆,产生了强烈毒性。3、靶向EphA2的ADC MEDI-547则可能因为EphA2是一种血管生成相关的受体,而这种受体被靶向后,不仅仅出现了出血和凝血的副作用,还有皮肤、神经等方面的严重副作用。4、辉瑞靶向TROP2的ADC PF-06664178(RN927C),与吉利德已上市的TROP2 ADC Trodelvy不同的是,PF-06664178采用的是auristatin衍生物作为Payload,与吉利德选择的较低效力的拓扑异构酶I抑制剂相比毒性更强,在剂量爬坡过程中,低剂量组(每3周4.8 mg/kg剂量)治疗的患者中就出现了皮疹,粘膜炎和中性粒细胞减少症等不良事件,而在这一低剂量对患者几乎没有疗效,使得临床治疗窗口较小,因此而暂停临床。值得一提的是,另外一种同样采用auristatin衍生物的Nectin-4 ADC Padcev虽然成功上市,但也存在皮肤毒性,因此被FDA黑框警告了。5、罗氏/基因泰克开发过一款FcRH5-ADC药物DFRF4539A,然而,经过临床研究表明,尽管在患者中实现了目标药物暴露,但该患者群体的缓解率普遍较低,DFRF4539A展现出低活性。关于FcRH5-ADC的开发随即被停止。其失败原因后续分析认为有三点:其一,患者群体中ADC所需的阈值是未知的。这使得DFRF4539A可能无法杀伤表达内源性水平FcRH5的多发性骨髓瘤细胞。其二,由于多发性骨髓瘤患者血液中可溶性FcRH5水平升高。FcRH5的这种脱落形式可能导致DFRF4539A与MM细胞膜结合FcRH5的结合减少。其三,研究中没有直接评估多发性骨髓瘤细胞对DFRF4539A的内化程度。因此,即使做到了将足够的MMAE递送到多发性骨髓瘤细胞的细胞表面,但细胞内MMAE浓度不足以杀死这些细胞。6、与罗氏已上市的CD79b ADC Polatuzumab Vedotin相比,它的“兄弟”管线iladatuzumab vedotin显然没有Polatuzumab Vedotin的好运。虽然Payload和Linker全一样,采用了半胱氨酸工程抗体的iladatuzumab vedotin反而终止了临床。原因主要是眼部毒性问题,而疗效相比自己的“兄弟”Polatuzumab Vedotin也没有改善。7、作为选择了首款上市的ADC同靶点(CD33)的几位竞争管线,AVE9633,IMGN779,SGN-CD33A等都因为各种原因招致失败,AVE9633在低于毒性剂量没有临床活性,SGN-CD33A与甲基化药物联用后出现了致命的感染,IMGN779虽说似乎没有披露原因,也可能是IMGN这家公司本身为了推动FRα ADC上市的商业考虑而将其“断臂”,但其在剂量方案提升后就戛然而止,也可能和低于毒性剂量没有临床疗效相关。8、放在近期,Mersana Therapeutics的NaPi2b ADC Upifitamab rilsodotin的5人死亡的案例虽然具体原因不明,可能和Payload过大有关, Upifitamab rilsodotin的DAR值(抗体药物偶联比值)有10。从Payload看出的现象从Payload的角度来看,在所有的这些被停止的临床管线中,微管抑制剂(如auristatin衍生物)占据总数的63%(58项),其次是用于DNA合成抑制剂的Payload。拓扑异构酶I抑制剂、靶向小分子和未披露的有效载荷加起来占10%。左图为中止ADC的Payload 右图为ADC总Payload如果以失败率来看,临床最多的微管抑制剂和其次的DNA合成抑制剂临床暂停也最多似乎不足为奇,不过DNA合成抑制剂的失败率似乎有点高。与之形成对比的则是拓扑异构酶I抑制剂的失败率似乎很低,而且著名的HER2-ADC DS-8201(Enhertu)和吉利德的TROP2 ADC Trodelvy都选择了拓扑异构酶I抑制剂,而这两款药物都是或即将成为重磅炸弹。疗效不足的ADC们除了不可耐受的毒性,功效不足也是ADC停用的一个原因。导致疗效不足的因素包括:①低肿瘤靶抗原密度和/或被停用ADC的内化特性差。②有效载荷效能不足。③异源DAR ADC产品导致有效载荷剂量达不到最佳剂量。④肿瘤外有效载荷释放和/或肿瘤内药物释放不完全。⑤由于PK特性差,ADC清除迅速。⑥未能证明疗效优于标准治疗。⑦肿瘤内药物外排转运蛋白升高介导的多药耐药性。疗效不足ADC的典型案例在有数据可查的停用ADC候选药物中,功效不足可能是约47%病例的促成因素。这些被证明疗效不足以保证进一步临床试验的候选药物包括但不限于DPEP3-ADC(Tamrintamab pamozirine(SC-003)患者应答率仅有4%),之前提过的辉瑞PF-06664178,诺华靶向CDH3的ADC PCA-062(47例患者只有一例部分缓解)这些药物失败的原因主要还是异源肿瘤表达和/或肿瘤抗原密度不足以诱导有效的ADC内化。另外Payload的效力不足也可能是疗效不足的原因。靶向HER2的ADC NJH395和SBT6050临床终止似乎是因为都选择了TLR7和TLR8激动剂这俩TLR激动剂,而导致Payload低效。百奥泰的BAT8001,BAT8003似乎都是因为美登素药物衍生物(微管抑制剂)Payload的效力不足而接连放弃,百奥泰随即去开发了采用Payload是拓扑异构酶I抑制剂的BAT8010。Linker不良也可能是效力不足的原因之一:罗氏的MUC16 ADC sofituzumab vedotin(DMUC5754A)在复发性卵巢癌患者中进行了临床,然而其患者ORR只有17%(一例完全缓解,四例部分缓解),采用的Linker是非特异性半胱氨酸,与其相比,同样是罗氏的同一靶点管线DMUC4064A在采用了Thiomab定点偶联(特异性半胱氨酸)ORR率则达到了45%。因此sofituzumab vedotin遭到了淘汰。CMB-401 (MUC1)是ADC因疗效不足而中止的另一个例子,其部分原因可能是不良的接头选择导致肿瘤外有效载荷释放。有人认为,这种刺孢霉素ADC未能引起单次部分缓解是由于使用了不稳定的酰胺接头。而MEDI4267则是因为药代动力学差,同比于罗氏已上市的首款HER2 ADC TDM-1,这种靶向HER2的tubulysin Payload ADC在最大耐受剂量下的半衰期很短,清除率很高,这使得其毒性不可耐受。而除此之外,还有七款ADC的临床被证明是不如标准治疗组,七款分别为:rovalpituzumab tesirine (DLL3-ADC),depatuxizumab mafodotin(EGFR VIII-ADC)、AMG 595 (EGFRvIII-ADC),AGS16F (ENPP3),glembatumumab vedotin (gpNMB-ADC),ifastuzumab vedotin (NaPi-2b ADC)。小编总结这些ADC的临床中止就像很多发表的各学科的阴性论文那样,虽然几乎90%是阴性结果,但仍然具有一定意义,应当鼓励阴性结果的发布,可以为研究排除一定的错误选项,将治疗导向正轨,以此惠及更多的患者。而从细节来看,标靶以及抗体,Linker,Payload的选择,有效载荷共轭的改进都是ADC发展的必不可缺的因素,而一步步更新迭代,相信能够获得更能够造福患者群体的ADC。参考来源:doi.org/10.1080/19420862.2023.2229101
抗体药物偶联物
2023-05-19
1 倍癌霉素-PBD异二聚体介绍倍癌霉素-PBD异二聚体是由倍癌霉素和吡咯并苯二氮䓬(PBD)两种DNA烷化剂构成的化合物(图1.1)。倍癌霉素和PBD分别会与腺嘌呤(A)和鸟嘌呤(G)发生交联。早在2000年代初,已有报告描述该异二聚体的交联能力和序列选择性,并提出其可以作为潜在的小分子抗癌药。由于对称的PBD二聚体作为有效载荷的ADC具有很好的药效,人们考虑到该类异二聚体有和PBD二聚体类似的强细胞毒性,开始思考倍癌霉素-PBD异二聚体是否也能成为ADC的有效载荷?图1.1几类倍癌霉素-PBD异二聚体的结构示意图2 倍癌霉素-PBD异二聚体的结构多样性和合成路线14种已知的倍癌霉素-PBD异二聚体都有同样的PBD(天然产物DC-81的衍生物)母核,其不同的地方在于侧链为不同的倍癌霉素类似物和连接子。异二聚体1(图1.1)的组成部分之CPI烷化剂是从天然产物CC-1065中发现,其他异二聚体的倍癌霉素结构都是该烷化剂的变异体。其中研究最为广泛的是CBI单元,包括异二聚体2–11。同时,还有含seco-CBI氨基衍生物的倍癌霉素-PBD(12),以及两个非手性烷化剂衍生物,seco-氨基CBI衍生物(13)和更简单的CI烷化剂(14)。二聚体中连接两个烷化剂的是聚亚甲基链(2–12),或者由聚亚甲基链加上吲哚(1)或苯并呋喃(13,14)直接或通过酰胺连接到倍癌霉素的末端。通过酰胺键连接到倍癌霉素的末端的方式模拟了所有倍癌霉素天然产物中的结构序列。这样,至少在单烷基化剂的情况下可以增加细胞毒性。倍癌霉素-PBD的合成路线基于两种单体和对称二聚体合成。代表性合成路线如图1.2所示,末端具有羧酸的聚亚甲基链连接到PBD单体的C8位置。由香草醛酸15或香草醛19分别经过8或9步可以得到中间产物16或20。通常化合物17或化合物21盐酸脱Boc保护基后,由1-乙基-3-(3-二甲基-乙基氨基丙基)碳二亚胺(EDCI)催化与化合物16或化合物20缩合生成通过酰胺键连接的二聚体(如18和22的合成)。需要注意当保护基团是芴甲氧羰基(Fmoc)(如化合物18),使用四丁基氟化铵(TBAF)脱保护也会导致seco-CPI烷化亚基的螺环化生成化合物1,而添加烯丙氧羰基(Alloc)可以在保持CBI为seco形式的条件下脱Fmoc保护(如3-5)。另外为了合成化合物11,需要在脱Alloc保护基之前,将化合物22(n=5)的seco-CBI环化。图1.2中用作起始材料的倍癌霉素都是来源于细胞毒性更强的“天然产物”对映体。化合物21通过手性高效液相色谱(HPLC)纯化获得。容易获得的化合物21,使合成S-seco-amino CBI类似物12.3变得更容易。化合物21的三氟甲磺酸酯衍生物与二苯甲酮亚胺发生Pd催化的胺化反应,然后亚胺作为正交保护基团,在倒数第二步的酸性条件下裂解为12。非手性和苯环、萘环结构使得13和14更易合成但是,由于化合物13的合成得率太低(<1%)和14较弱的细胞毒性,使得两个产物不适合应用在ADC上。图1.2 代表性倍癌霉素-PBD异二聚体1和3-5的合成路线3 倍癌霉素-PBD二聚体的活性3.1 DNA烷基化-序列选择性和交联效率二聚体1被设计为在相反的DNA链上腺嘌呤N3和鸟嘌呤的C2-NH2之间交联。数据表明,1与长度为20bp含有两个5′-CAAT-TA*-3′基序的寡核苷酸片段交联。在该序列中,星号标记为可被CPI烷基化的作用位点之腺嘌呤,下划线C对应于PBD的作用位点之鸟嘌呤。CPI及其S-对映体侧链从烷基化腺嘌呤向5′-方向延伸,同时,被干预的AT碱基对产生更窄和更深的小凹槽,是倍癌霉素类似物的作用位点。实验数据表明,1相应的DNA烷基化的靶序列为20 bp。这是由于烷基化寡核苷酸的热裂解,其选择性发生在DNA正链的两个腺嘌呤中,与腺嘌呤N3烷基化后的易脱环和链裂解一致。此外,当DNA反向链中的作用位点鸟嘌呤被肌苷(缺少C2-NH2基团)取代时,1与DNA不会发生交联。最近的分子动力学模拟显示该序列可成为交联的兼容位点,这表明异二聚体1可以忽略DNA结构畸变,与DNA发生交联(图1.3)。但是含有插入不同数量AT碱基对的替代序列与1的交联程度变差。对于二聚体2-12的结合序列特征研究较少,然而,对2、5、7和10与有240对碱基对的DNA序列的腺嘌呤烷基化位点的检测表明,所有化合物都具有相似的热裂解位点,并且这些位点与CBI烷基化的位点相匹配。这表明CBI结构决定二聚体的总体序列选择性,并且与其连接的PBD结构既不限制被烷基化的位点,也不改变CBI的识别序列。然而,基于对热裂解所需的相对浓度的观察,PBD使CBI烷基化效率更高。使用线性化质粒研究了2-10对有5400对碱基对的裸DNA的交联能力,发现能使50% 的DNA发生交联反应所需的二聚体浓度(C50)差异较大,该浓度与CBI对映体形式、连接子链的长度(n=3,5更佳)有相关性。与对称的CPI和PBD二聚体相类似,异二聚体连接子链长度、与碱基数量的匹配会影响交联强度。对于3、5和8,在低至1 nM的浓度下即可检测到交联,即一个线性DNA片段至少对应于一个二聚体分子。对称的PBD二聚体DSB-120也观察到类似的高效交联,但当头对头试验中比较DSB-120和5在整体细胞中交联能力时,5的活性至少比DSB-100的活性高1000倍。细胞中CBI–PBD二聚体的极强的交联能力可能与倍癌霉素的反应特性有关,其中倍癌霉素比其他生物亲核试剂对DNA的选择特异性高使倍癌霉素-PBD异二聚体在细胞中具有更强的DNA交联能力。利用线性化质粒DNA研究13的交联能力,发现13的交联效率比对称的PBD二聚体SJG-136低至少100倍。其中一个可能是因为异二聚体的长度和交联位点没有很好地匹配(13和1的接头分别含有2和3个亚甲基,而2和3的单个亚甲基的差异,使其交联C50相差300倍)。对13的4个潜在交联位点的分子动力学模拟表明,虽不是很理想,但最适合的是5′-A*TTTC3′这5个碱基序列。图1.3 有效载荷1(深蓝色)的分子动力学模拟示意图。有效载荷1的CPI和PBD单位分别与序列5‘-GCCAATTA*GC-3’的A8(黄色)和G18(紫色)共轭结合。分子模拟显示异二聚体与DNA小凹槽很好的结合并且对中心的AT碱基影响较少。3.2 体外细胞毒性倍癌霉素-PBD异二聚体的细胞毒性较强,化合物1对细胞增殖的半抑制浓度从47 pM (SW480)到5.1 nM(A549)。CBI-PBD二聚体2-10在人源和鼠源肿瘤细胞系的细胞毒性数据发现,IC50的范围差异有35000倍,其中,连接子链长度为3或5,并且含S-CBI对映异构体的二聚体对细胞的杀伤能力更强。在SKOV 3(人卵巢癌细胞)中,二聚体与DNA的交联作用与细胞毒作用呈正相关(图1.4)。其中,DSB-120是个例外,其交联能力强但是细胞毒性较弱。值得注意的是,这可能与DSB-120细胞毒性较弱有关,与细胞毒性最强的5相比,DSB-120的细胞毒性弱1000倍,该特点与两种二聚体在SKOVk3细胞中交联能力相差1000倍相对应。曾有报道,5的微小结构变化使异二聚体的任何一端都不能烷基化DNA。PBD端失活导致细胞毒性减弱约400倍,CBI端失活使细胞毒性减弱约十万倍,这导致二聚体的细胞毒性弱于PBD单体DC-81。因此,在CBI–PBD二聚体中,CBI决定了序列选择性和细胞毒性效力。图1.4 CBI-PBD异二聚体2-10(圆圈)和PBD二聚体DSB-120(方形)的DNA交联强度(C50使用线性质粒DNA测量)和对SKOV3细胞毒性(药物处理4小时后测量的IC50)的关系。CBI-PBD异二聚体交联强度与细胞杀伤相关性R2=0.89。实验数据显示,使用5处理细胞5天,细胞杀伤作用进一步增强,在5个肿瘤细胞系中,IC50值在3–4 pM范围内。其他9个肿瘤细胞系呈现5敏感性差异,细胞杀伤作用范围更大(非小细胞肺癌细胞系NCI-H1781的IC50为9.8 pM,乳腺癌细胞系HCC1569 X2的IC50为130 pM)。这些数据表明,5对P-糖蛋白的表达水平不敏感,无论二聚体的CBI末端是seco(5)还是spircyclic(11)形式,都观察到类似的细胞毒性水平。对氨基CBI–PBD二聚体12观察发现,当加入单烷基化剂时,seco-CBI和seco-氨基CBI生成相同毒性化合物(处理细胞4小时)。事实上,氨基CBI与其苯酚类似物具有许多类似的性质,如都具有相同的对映体依赖的序列选择性。然而,氨基-CBI–PBD 12的细胞毒性显著低于与其相类似的苯酚异二聚体5,二聚体处理细胞4天后发现IC50值的范围从0.5-20 nM。这可能是因为,CBI是非常稳定的,从seco-氨基CBI衍生的螺环丙基中间体的活性高,在生理条件下进行发生分解,半衰期约为一小时。该特性使氨基CBI作为ADC的有效载荷,氨基必须被掩蔽直到从ADC释放,且标准IC50测定可能不会准确地反映此类有效载荷的细胞毒性潜力。这表明该类化合物分解的不稳定性在限制系统性释放有效载荷毒性方面可能是一个潜在的优势。倍癌霉素烷基结构的非手性异构体也被提出可通过螺环中间体与DNA反应,尽管这尚未被证实。然而,非手性seco-氨基CBI和seco-CI 的单体对腺嘌呤的烷基化显示出与包含完整吲哚环的相应化合物相似的序列选择性,并且对于非手性seco氨基CBI,IC50值在亚微摩尔范围内。然而,添加PBD产生的异二聚体13和14仅略微增强细胞毒性(例如,使用二聚体处理P815小鼠肥大细胞瘤细胞3天后,IC50值分别为26 nM和0.56µM)。这两种异二聚体比seco-CBI的单烷基化剂的细胞毒性更小,这可能是因为其相对较弱的DNA交联能力。3.3 体内抗肿瘤活性目前有针对倍癌霉素-PBDs二聚体3、5和8的体内抗肿瘤活性研究,均以其各自的最大耐受剂量单次静脉注射(i.v.)给药至皮下WiDr人结肠癌异种移植瘤小鼠模型。尽管3,8和PBD二聚体DSB-120没有抗肿瘤作用,但5延迟肿瘤生长,平均肿瘤直径从8增加到17 mM的生长时间为41天,而对照组是20天。4 基于倍癌霉素-PBD二聚体的ADC关于倍癌霉素-PBD二聚体有效载荷,有效载荷-连接子合成以及ADC制备和活性的所有报告都在专利中。目前,所有的实例都基于异二聚体5,因为其具有最强的细胞毒性和相对简单的结构。4.1 通过Seco-CBI苯酚连接的ADC倍癌霉素-PBD二聚体有两个位置可与连接子连接。倍癌霉素苯酚可以通过氨基苄基(PABE)自降解间隔子连接到二肽蛋白酶可裂解接头上。该方法已经成功将5和马来酰亚胺-Val–Cit二肽连接形成有效载荷-连接子23(图1.5)。该有效载荷-连接子包含马来酰亚胺,该部分可以与THIOMAB反应™ 抗体(抗HER2-4D5-HC-A118C)形成药物抗体比(DAR)为1.6的ADC 23a。然而,可能由于有效载荷-连接子的疏水性,ADC出现聚集。此外,ADC仅对高表达人表皮生长因子受体2(HER2)的SK-BR-3细胞系造成50%的生长抑制。推测其不能完全抑制细胞生长可能是ADC聚集的结果。另一种可能是,当释放的物质是CBI苯酚时,PABE间隔子的自裂解较慢。图1.5 倍癌霉素-PBD 异二聚体-连接子和ADC在专利中的结构示意图4.2 通过蛋白酶可裂解连接子连接到PBD胺的ADC将倍癌霉素-PBD二聚体连接到连接子的另一个位置是PBD的N10位置。这种有效载荷-连接子的例子如24所示(图1.5),其中瓜氨酸在连接子中被赖氨酸取代。图1.6展示了24的合成步骤,其合成策略是在PBD二氮䓬环形成之前引入连接子的Lys–PABC(对氨基苄基氨基甲酸酯)部分。起始材料27可用作有效载荷2–10合成的中间体。将其转化为28,然后与N-甲基哌嗪氨基甲酸酯保护型seco-CBI苯酚偶联。脱去产物30的叔丁氧基羰基(Boc)保护基,将胺转化为相应的异氰酸酯。然后脱去32的乙酸保护基,醇氧化为相应的醛,导致二氮䓬环的自发形成。从33开始,后续的五个步骤(依次进行脱保护和偶联反应以引入缬氨酸和马来酰亚胺结构,最终去除赖氨酸Boc保护基)产生了所需的有效载荷-接头24。尽管该路线具有多步骤性质,但优化后的合成方法可进行放大,最终能够获得>100mg的高纯度产品。加入氨基甲酸酯将seco-CBI苯酚制成前药对于增加有效载荷-连接子的溶解性以及减少最终偶联物的聚集有重要作用。有效载荷-连接子与抗HER2和抗CD22的 THIOMAB ™ 抗体偶联形成ADC24a和24b(图1.5),其药物抗体比分别为1.9和1.7。将连接子连接到PBD的N10氨基使亲水前药(如N-甲基哌嗪氨基甲酸酯)在有效载荷-连接子24中的CBI酚上结合,形成聚集水平较低的ADC(例如24a和24b)。在MMTV-HER2 Fo5乳腺转基因肿瘤模型中,抗HER2 ADC(24a)单次静脉注射剂量为3或10 mg/kg后,26天内肿瘤停滞或消退(图1.7)。对照ADC(24b)在10mg/kg也具有肿瘤杀伤活性,在较低剂量时才可能会与抗HER2 ADC(24a)有所区分。这种脱靶毒性通常在具有较强毒性有效载荷的ADC的高剂量组中可见,因为ADC在血液循环中是稳定的,这种脱靶毒性可能是非特异胞饮作用的结果。图1.6 有效载荷-连接子24的合成路线4.3 通过二硫化物连接子连接到PBD胺的ADC除了蛋白酶可裂解的二肽和模拟肽的连接子外,倍癌霉素–PBD二聚体也能与二硫化物连接子连接。一种新的自降解的二硫化物连接子通过PBD的N10氨基连接到5上,形成有效载荷-连接子25。除了含有氨基甲酸酯CBI前药的25,还有类似的包含磷酸盐前药的26。有效载荷-连接子25和26中活性3-硝基吡啶二硫键与THIOMAB™ 抗体硫醇发生取代发应,分别产生二硫化物ADC 25a和26a(抗HER2-7C2-LC-K149C),以及25b和26b(抗CD22-LC-K149C)。THIOMAB™ 抗体的突变位点为LC-K149C,是因为其体内稳定性优于HC-118C。在MMTV-HER2 Fo5乳腺转基因肿瘤模型中,单次静脉注射的抗HER2 ADC(25a和26a)具有剂量依赖性活性,剂量为5mg/kg时,肿瘤在43天内完全消退(图1.8a)。这种杀伤活性具有特异性的,因为抗CD22 ADC(25b,26b)在相同剂量下仅产生微弱的抑制作用。鉴于倍癌霉素–PBD二聚体的作用机制(DNA交联)与获批的抗HER2 ADC曲妥珠单抗–DM1(微管蛋白结合)的不同,两种ADC有用作联合治疗的可能。重要的是,T-DM1与26a的抗体识别不同的表位(T-DM1表位为4D5,26a表位为7C2),两种ADC不会发生冲突。当seco CBI–PBD ADC 26a与T–DM1在HCC1569x2异种移植瘤模型中组合给药时,组合在相同剂量下的疗效优于单独的ADC(图1.8b)。图1.7抗HER2蛋白酶裂解seco-CBI-PBD ADC 24a 在Fo5 转基因乳腺癌模型中单次静脉注射给药的体内药效。图1.8 抗HER2二硫键连接的seco-CBI-PBD ADC 25a和26a在Fo5 转基因乳腺癌模型中单次静脉注射给药(a)和 ADC 26a 在 HCC1569x2 移植瘤模型中单次静脉注射或联合T-DM1(b)的体内药效。5 倍癌霉素–PiBD二聚体PBD单体的吡咯环可以被哌啶环取代,且对DNA的良好结合力不变,哌啶并苯二氮䓬(PiBD,又称PDD)和其苯并类似物,如异喹啉啶基苯二氮䓬)已被报道用于ADC有效载荷的对称二聚体。最近的2篇专利也描述了它们与倍癌霉素形成的异二聚体中可作为ADC有效载荷(图1.9)。34–37的合成遵循图1.2中的类似方法,用对映哌啶衍生物代替吡咯烷衍生物,在C12a形成所需的立体化学结构,与试剂反应在C9引入所需的连接子。异二聚体36的细胞毒性最强,有效载荷连续作用三天,头颈癌细胞FaDu的IC50为10pM,前列腺癌细胞PC3的IC50为30pM。图1.9 代表性倍癌霉素-PiBD异二聚体结构式和倍癌霉素-IQB有效载荷-连接子42,43 的合成路线示意图。化合物37是含苯酚和氨基CBI的CBI–IQB二聚体系列中细胞毒性最强的分子,聚亚甲基连接子的亚甲基的长度为1-5。二聚体37对白血病细胞系具有特别的细胞毒性(AML2和HL60中的IC50分别为0.07和0.12 pg/ml),并被纳入有效载荷-连接子的例子中。这些效载荷-连接子含一个马来酰亚胺,一个八甘醇间隔子,一个Val-Ala蛋白酶裂解二肽连接子。Val-Ala二肽通过PAB单元与CBI苯酚或二氮杂氮连接。图1.9描述了两个含PABC二氮䓬连接子合成的例子。由香草醛分八步形成苯胺38,38与五氟碳酸苯酯39反应直接引入二肽PABC部分。叔丁基二甲基甲硅烷基(TBS)保护基的脱除和氧化导致IQB环系统的形成。酯水解后,使用HATU作为偶联剂,使酸40与CBI碳酸酯41反应。随后,在裂解或保留CBI碳酸盐的条件下进行Alloc脱保护,从而在与马来酰亚胺–8单元聚乙二醇(PEG8)–N-羟基-琥珀酰亚胺(NHS)反应后,形成有效载荷-连接子42和43。这些有效载荷-连接子与抗白细胞介素-1受体辅助蛋白抗体偶联,该抗体含有S156C半胱氨酸替代物,最后产生药物抗体比为1.7–2.0且聚集水平低的ADC。该ADC显示出对抗原依赖的细胞毒性,且IC50在较低的ng/mL范围。然而,目前还没有含倍癌霉素-PiBD二聚体的ADC的体内抗肿瘤活性报告。6 结论对倍癌霉素-PBD和倍癌霉素-PiBD二聚体用作ADC有效载荷的研究较少。部分原因可能是,与单烷基化剂或对称二聚体相比,异二聚体的合成难度更大。然而,特定结构的倍癌霉素-PBD是已知的最有效的DNA交联剂和细胞毒性小分子,并且有足够的临床前证据表明,异二聚体作为有效载荷可以产生具有显著抗肿瘤活性的ADC。目前尚不清楚的是,这些异二聚体及其DNA加合物是否比其相关的对称二聚体更具有优势。这个问题取决于倍癌霉素-PBD的ADC的安全性,而这一点尚未有报道。
抗体药物偶联物申请上市
2023-03-12
点击上方的 行舟Drug ▲ 添加关注导读抗体偶联药物( Antibody - Drug Conjugate,ADC)由抗体、连接子和小分子毒素组成,在兼具高度靶向性和高细胞毒性优势的同时,由于其结构的多样性和复杂性,以及循环系统中释放的小分子毒素含量较低等特殊性,给其药代动力学研究带来了诸多挑战......1、ADC分子设计在ADC 分子中: ①靶点和抗体的选择是ADC 药物设计的起点,是药物适应症的决定性因素,选择的靶抗原通常应在肿瘤或疾病相关且高水平表达; ②连接子在ADC 的体内循环过程中应足够稳定,ADC 药物进入靶细胞后应能将小分子毒素以高效活性的形式快速释放; ③小分子毒素应对于肿瘤细胞具有高效的杀伤作用。靶点、抗体、连接子等因素均可对ADC药物的有效安全性造成影响,以下将对逐一进行讨论。1. 1 靶抗原和抗体在确定了目标适应症后,首先需考虑的是哪些抗原在该类肿瘤细胞表面具有特异性且高水平的表达。理想情况下,选择的抗原应高度均匀地表达在靶细胞表面,且在正常组织或细胞表面不表达或少表达; 抗原应是不分泌型的,分泌型抗原可与体内循环系统中的ADC 药物或裸抗结合,从而导致与肿瘤细胞结合的ADC 药物减少,影响药物的疗效和安全性; ADC 药物与抗原结合以后,需要具有合适的内吞途径并具有一定的内吞速率,在细胞内通过酶降解释放小分子毒素。当前,缺乏疗效和脱靶毒性是ADC 药物面临的主要挑战,其中一个重要原因便是靶抗原的低水平表达和内化速率有限。目前研究人员正在开发解决抗原低表达和内化速度低的方法,如采用抗肿瘤血管生成抗体或双特异性抗体设计非内化型的ADC 药物:①采用抗血管生成抗体避免内化过程,但可能会出现脱靶效应而影响正常血管的生成,需要谨慎选择靶抗原和相应抗体;②使用双特异性抗体靶向一种抗原的两个非重叠表位,以增强抗体与抗原之间的亲和力。在ROSSIN等设计的ADC 药物中,采用缺失Fc 区的双抗体靶向抗原,利用额外的化学激活剂在肿瘤细胞外切割连接子,从而释放出游离小分子药物并渗透到肿瘤细胞中,通过这种方式避免因肿瘤细胞的间质压和上皮屏障等造成的内化不足,从而提高抗肿瘤活性。双特异性抗体也可选择性结合肿瘤细胞上的两个不同抗原,从而降低脱靶毒性。研究显示,一些ADC 药物可利用连接子的物理和化学特性以及肿瘤微环境释放游离的小分子毒素,从而杀伤相邻的抗原表达阴性的肿瘤细胞,这个过程即为旁观者杀伤效应。一些ADC 药物内化后可被代谢释放出不带电荷、可穿透细胞膜的细胞毒性代谢物,并杀伤临近的抗原表达阴性的癌细胞。旁观者杀伤效应对于抗原表达不均一的肿瘤细胞具有重要意义。需要注意的是,即使是相同靶点,肿瘤类型不同也会影响ADC 的治疗效果,即,同一ADC 药物在不同适应症患者中可能会呈现出不同PK 特征和有效安全性。如,Besponsa是靶向CD22 的Inotuzumab 与烯二炔毒素Ozogamicin 的抗体偶联药物,2017 年被FDA批准用于成人复发难治B 细胞急性淋巴细胞白血病,但Besponsa在复发难治的非霍奇金淋巴瘤的Ⅲ期临床试验却因疗效不佳终止。在免疫球蛋白G( IgG) 类抗体中,通常会使用IgG1、IgG2 和IgG4 开发治疗用生物制品( 半衰期约18 ~ 21 d) ,IgG3 由于与FcRn 的受体结合率较低,导致其清除速度较快( 半衰期约为7 d) 因而较少被应用。目前很多ADC 药物使用的是IgG1 亚型,IgG1 亚型可以发挥抗体依赖的细胞介导的细胞毒性作用( Antibody Dependent Cellular Cytotoxicity,ADCC) 和补体依赖的细胞毒性作用( Complement Dependent Cytotoxicity,CDC) 进一步提高ADC 活性。同时,还需要考虑选择的抗体分子量大小,当抗体分子量太大时,难以透过毛细管内皮层和细胞外间隙,抗体的分子量太小可能会影响其在体内的半衰期。总体而言,理想的抗体应具有良好的靶向功能,有效地将小分子药物递送到靶细胞中,同时具有较低的免疫原性,且抗体上需具有合适的连接位点与连接子偶联,抗体与抗原结合后可具有一定的内吞速度和有合适的内吞途径,所选择的抗体可保持裸抗的全部或部分功能。如,首个获批的单药治疗实体瘤的ADC 药物恩美曲妥珠单抗( Kadcyla,T - DM1) ,是由曲妥珠单抗和小分子微管抑制剂DM1( 美登素衍生物) 偶联而成,其中抗体部分为曲妥珠单抗,保持了其裸抗的ADCC 活性。1. 2 小分子药物抗体的肿瘤穿透能力限制、抗原表达量低和内吞效率的限制等因素均可造成细胞内的小分子毒素药物浓度较低,因此小分子毒素需具有较高的细胞毒性。通常情况下,ADC 药物的小分子毒素的靶点位于细胞内,若ADC 药物无法转运至细胞内将会影响药物的有效性和安全性,且在细胞外或解离后可能会对旁边的正常细胞产生毒性。另外,需要考虑小分子对ADC 药物整体性质的影响,如可能会影响ADC 药物的内吞效率、ADC 药物的极性以及免疫原性。同时,小分子毒素在水性缓冲溶液中通常需具有适当的溶解度,以便于与抗体偶联,偶联后的小分子毒素应具有一定的稳定性。目前采用的小分子毒素主要有美登素、奥利斯他汀、蒽环类药物和喜树碱类似物等。1. 3 连接子所选择的连接子在血浆中需能稳定存在,以避免小分子毒素提前释放损伤正常的组织或细胞。当ADC 药物被内吞到靶细胞后,选择的连接子需能够快速释放有效的活性成分。另外,也应该考虑到选择的连接子的分子量和极性对ADC 药物整体性质的影响。连接子可分为裂解型和非裂解型,裂解型的连接子可利用肿瘤微环境和正常生理环境的差异来释放可能透膜并产生旁观者效应的小分子毒素。非裂解型的连接子通常在抗原- 抗体复合物进入胞内的溶酶体后,断开抗体和连接子的连接。两种类型的连接子分别具有其优缺点,非裂解型的连接子比可裂解的连接子更稳定,可减少脱靶毒性,改善多重耐药性( multi - drug resistance,MDR) 现象; 裂解型的连接子产生的代谢产物被动扩散更易进入胞内产生旁观者杀伤效应,对于靶抗原表达异质性的肿瘤有重要意义,但比非裂解型更易出现脱靶。与裂解型的连接子相比,采用非可裂解型的连接子在抗原选择上更为严格。恩美曲妥珠单抗( Kadcyla) 采用非裂解型的硫醚连接子与美登素衍生物连接,由于ADC 在细胞内代谢产生了离子化的代谢产物、渗透性较差,对周围正常细胞的影响较小,Kadcyla表现出了可接受的安全性。连接子的性质会对药物在体内的代谢途径产生较大的影响,对ADC 药物的设计有重要的影响。1. 4 连接位点和药物-抗体比ADC 药物的药效主要取决于肿瘤细胞中小分子毒素浓度,因此药物抗体偶联比( Drug Antibody Ratio,DAR) 是ADC 药物药效的重要影响因素。目前多个研究致力于改善ADC 药物的DAR,以期增加药物在肿瘤细胞中的浓度。但研究发现,并非DAR 越高药效越好,这可能与小分子毒素的极性等因素相关,从安全性角度讲DAR 越高对正常组织的毒性也可能随之增加。在ZHANG 等的研究中,当DAR 提高到一定程度后ADC 药物的活性并未进一步增加。选择适宜的DAR 对于肿瘤细胞中有效浓度具有重要意义。连接位点与ADC 药物的均一性相关,也是DAR分子设计的重要考量因素之一。抗体上的半胱氨酸( 8 个) 和赖氨酸残基( 80 个) 较易发生化学反应而被修饰,因此常作为与效应分子结合的位点。在早期ADC 的开发研究中,通常选择抗体上的赖氨酸作为结合位点,因每个抗体上的赖氨酸残基可达80 个,导致了很大的异质性。而每个抗体上只有8 个游离的半胱氨酸可通过二硫键与连接子连接,用半胱氨酸作为连接位点有助于降低ADC 的异质性。JUNUTULA等报道了一类新型的THIOMAB - 药物偶联物( TDC) ,用工程化的位点特异性半胱氨酸,具有更明确的DAR,异质性更小。中国食品药品检定研究院2018- 07 - 20 发布的《抗体偶联药物质量控制和临床前评价专家共识》中,药物主要偶联位点、DAR 和药物载药量分布是ADC药物质量控制的重要组成部分。2、ADC 药物的PK 特征ADC 药物的吸收、分布、代谢和消除对其PK 和PK / PD 关系的理解至关重要,在药物研发过程中会影响候选分子的选择。由于ADC 药物的结构组成中同时包括大分子抗体和小分子毒素,其ADME 特性表征时可能需要混合的方法。因ADC 药物在临床上多通过静脉给药,在此不讨论其吸收特性。从分子量大小和空间体积方面讲,ADC 药物结构中的主体主要是抗体,因此表现出诸多与裸抗类似的药代动力学特征,具有抗体药物的主要药代动力学特征及作用机制,如靶点介导的药物清除、FcRn 受体循环及非特异性蛋白酶降解等。ADC 药物与小分子药物和抗体药物的主要PK 特征比较,见表1。总体而言,ADC 药物通常经过静脉给药,分布与抗体药物类似,同时具有抗体和小分子的代谢和清除途径,在低剂量下呈非线性、高剂量下表现出线性特征。ADC 药物最重要的特征之一是其多样性。因抗体上所偶联的小分子毒素数量和/或结合位点的不同,导致ADC 是由多种不同分子组成的混合物,而当ADC 进入体内后,小分子毒素通过酶解或化学反应从ADC 药物上逐渐解离下来,进一步增加了ADC 药物在体内的多样性。这种不断变化的多样性是ADC 药物的PK 研究的重要挑战之一。2. 1 分布ADC 药物的空间结构主要由抗体构成,因此体内分布通常与未结合的抗体相似。ADC 药物给药后初期的分布主要局限在血管内,中央室的分布容积与血浆容积相似( ~ 50 mL·kg - 1 ) ,之后扩展到组织间隙中,稳态分布体积约为150 ~ 200 mL·kg - 1。与裸抗相似,ADC 药物难以穿过血管上皮细胞,组织分布程度较低,扩散缓慢,在血流量大的组织,如肝、肾、肺、脾和心脏中的分布程度更高。与裸抗相似,ADC药物的分布也同样会受到靶抗原表达和内化速率的影响。药物通过抗原的非特异性或特异性结合将裸抗分布到非靶标组织上通常不具有药理作用,但在ADC 药物中,由于后续会释放小分子毒素或其类似物,因此在相同组织中的分布和积累可能会产生具有临床意义的药理/毒性作用。了解ADC 药物的分布对于理解药理/毒性作用具有重要意义。肿瘤细胞或正常组织可能会释放抗原进入循环系统中,与ADC 药物结合清除ADC 药物并影响其分布。ADC 药物与可溶性抗原结合后形成的复合物可被肝摄取并清除,并在此过程中在肝释放出大量的小分子毒素造成潜在的肝毒性。在啮齿类动物研究结果显示,抗体与单甲基金刚烷胺E( MMAE) 结合会影响其组织分布,与未结合的抗体相比,会增加肝的摄取; 其他研究中也看到了类似的现象,小分子毒素的结合对ADC 药物CMD - 193 在人体正常组织和肿瘤中的分布产生了显著影响: 肿瘤的摄取降低,更多地分布在肝中。在上述案例中,ADC 药物的抗体分布研究采用的是标记抗体的方法。但同时,了解游离和结合的小分子毒素的组织分布也很重要,有研究者开展了在抗体和小分子毒素上进行双重放射性同位素标记研究,结果显示,小分子毒素MMAE 与抗体在多数组织中分布相似,但在肝中小分子毒素的浓度高于抗体。2. 2 代谢和排泄抗体主要通过靶点介导和非特异性摄取进入细胞,并通过蛋白水解从体内清除。与裸抗不同,ADC的代谢存在其独有的特点,可通过两种不同的途径( 解偶联和分解代谢) 释放细胞毒性代谢产物。①解偶联: 连接子裂解,释放出游离的小分子毒素,并保留抗体骨架; ②分解代谢: ADC 药物中的抗体部分蛋白水解为多肽/氨基酸,同时产生游离小分子毒素,或带有连接子的小分子毒素,或带有氨基酸-连接子的小分子毒素类似物,这些代谢产物仍可具有较高的细胞毒性。通常两种代谢途径在体内同时发生,以哪种途径为主取决于连接子稳定性、结合位点和总载药量等因素。对于具有易被酶或化学裂解连接的连接子( 如二硫键) 的ADC 药物,通过解偶联过程释放细胞毒性药物可能是主要的途径。若为非裂解型连接子,体内代谢途径可能以分解代谢释放游离小分子及其结构类似物为主。例如,采用非裂解型偶联子的恩美曲妥珠单抗( Kadcyla) ,体内代谢会形成带有氨基酸残基和/或链接子的效应分子,其中,血浆中MCC - DM1的浓度Cmax值远高于游离的DM1。由ADC 药物代谢产生的游离小分子毒素及其结构类似物在体内会继续进行代谢和生物转化( 如通过细胞色素P450 酶代谢) ,理论上也存在与其他小分子治疗药物发生药物相互作用( Drug - Drug Interaction,DDI) 的可能,进而影响ADC 药物分解代谢物或其他合并用药的血药浓度。但鉴于ADC 药物在体内循环系统中释放出的小分子毒素浓度较低,通常产生DDI的风险较低。3、ADC 药物的PK 研究考虑3. 1 目标分析物ADC 药物的PK 研究主要内容包括ADC 药物的稳定性、血药浓度-时间曲线、分布、代谢及排泄过程等; 若小分子药物是新化合物,建议综合应用体内外研究方法,定性和/或定量检测手段,对小分子药物的系统暴露量、血浆蛋白结合及排泄特征、肿瘤和正常组织的摄取/分布特征等进行详细研究,必要时,应对小分子药物代谢产物进行系统暴露量、代谢产物谱、分布、脱落方式、断裂点等研究。常用于表征ADC 药物PK 特征的分析物包括结合型抗体( 至少偶联一个小分子毒素的抗体) 、总抗体( 偶联和未偶联小分子毒素的抗体) 、结合型效应分子、游离小分子毒素及其类似物。不同分析物的PK所反映的内容和意义不同,整体上构成ADC 药物在体内代谢的全貌。体内ADC 药物浓度的降低存在两种清除途径:①抗体部分通过酶降解等方式解体; ②小分子毒素从抗体上完全解离( 即DAR 变为0) 。而影响总抗体的浓度的途径仅有途径①。所以通常会观察到ADC 药物具有更快的清除率,与总抗体浓度清除速度的差异即为效应分子从ADC 药物上完全解离的速度,侧面反映ADC 药物在血液中稳定性,即对比ADC 给药后总抗体与结合型抗体的清除速度,观察到的差异反映的是效应分子从ADC 药物上完全解离的速度。偶联药物对抗体代谢的影响可以通过给予裸抗体和ADC 药物测得的总抗体PK 进行比较,从而评价小分子药物连接到抗体后对抗体清除速率的影响。在一些ADC 药物的研究中发现,与小分子毒素结合后,可能会加快抗体的清除速度,DAR 高的ADC 药物清除更快。3. 2 免疫原性与其他大分子生物疗法类似,ADC 药物在人体内也可诱导免疫反应产生抗药抗体( Anti - therapeutic Antibody,ATA) 。内在因素( 产品相关的) 和外在因素( 患者相关的) 均可能会影响ATA 的发生率,如,ADC药物的相关变体( 如三级结构变形) 可能会增加免疫原性的风险。体内产生的ATA 会中和ADC 药物,是ADC 药物的一种清除途径,增大了ADC 药物本身和裸抗体的清除率。与单抗一样,在临床试验过程中也需要严格监控和评估ADC 药物的免疫原性。3. 3 PK/PD 分析PK/PD 建模可定量反映药物剂量和药理作用( 响应) 之间的联系,是新药研发中的重要组成部分。全面评估暴露- 反应( Exposure - Response,ER) 关系可为患者的给药剂量、用药频率和剂量调整等提供建议。对于未结合的裸抗,ADC 药物通常具有较窄的治疗指数,因此更加需要完善ER 分析用于指导临床研究和实际用药。ADC 药物研发中的PK/PD 分析有其自身的特点和挑战,如,ADC 药物可能会同时存在多种药理作用机制( 例如靶点特异性毒性和非特异性毒性) ,体内代谢会产生多种活性分析物( 例如ADC、总抗体、游离小分子及其结构类似物) ,不同分析物具有不同的药理/毒性作用,在进行PK/PD 研究时应对分析物进行充分考察。体内多种活性物质的存在使ER 关系的建立更加复杂。所选择的驱动药物作用的关键分析物不同,得到的ER 关系建模的结果也可能会存在差异。如,在T - DM1 的研发和申报中,申请人所建立的ER PK/PD 模型中,采用的驱动分析物为NCA 预测的T -DM1 的AUC 和Cmax、总抗体的AUC 以及DM1 的Cmax,建立的ER 模型显示暴露量与药物疗效无明显的相关性。FDA 在审评过程中建立的ER 模型采用的驱动分析物为模型预测的T - DM1 的AUC 和Cmin,模型结果显示对于低暴露量的受试者可考虑增加用药剂量以提高疗效。3. 4 多种研究相结合ADC 药物代谢机制和代谢产物研究需要体外研究和体内研究、动物研究和人体研究相结合,共同协作、多管齐下。合理的体外研究和动物研究( 包括在表达目标的细胞系中进行的分解代谢研究以及跨物种的血浆稳定性研究) 有助于阐明ADC 的代谢机制和途径,可用以鉴定ADC 分解代谢产物并建立临床前物种的相关性等,为人体内的临床试验提供参考。例如,在T-DM1 的研发过程中,在大鼠中进行了两项物质平衡研究,分别探索了大鼠体内ADC 和DM1的代谢途径和回收率,为T-DM1 在人体内的临床研究奠定了基础,同时,研究发现DM1 主要通过CYP3A4 /5 代谢,因此在T-DM1 的说明书中建议不与强CYP3A4 抑制剂合并用药,并在上市后继续完成肝损伤患者中T-DM1 的PK 研究。参考:中国临床药理学杂志文章信息源于公众号小白学药,登载该文章目的为更广泛的传递行业信息,不代表赞同其观点或对其真实性负责。文章版权归原作者及原出处所有,文章内容仅供参考。本网拥有对此声明的最终解释权,若无意侵犯版权,请联系小编删除。学如逆水行舟,不进则退;心似平原走马,易放难收。行舟Drug每日更新 欢迎订阅+医药大数据|行业动态|政策解读
抗体药物偶联物
100 项与 Anti-CLL1 THIOMAB-PBD conjugate(Genentech) 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 急性髓性白血病 | 药物发现 | 美国 | - |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
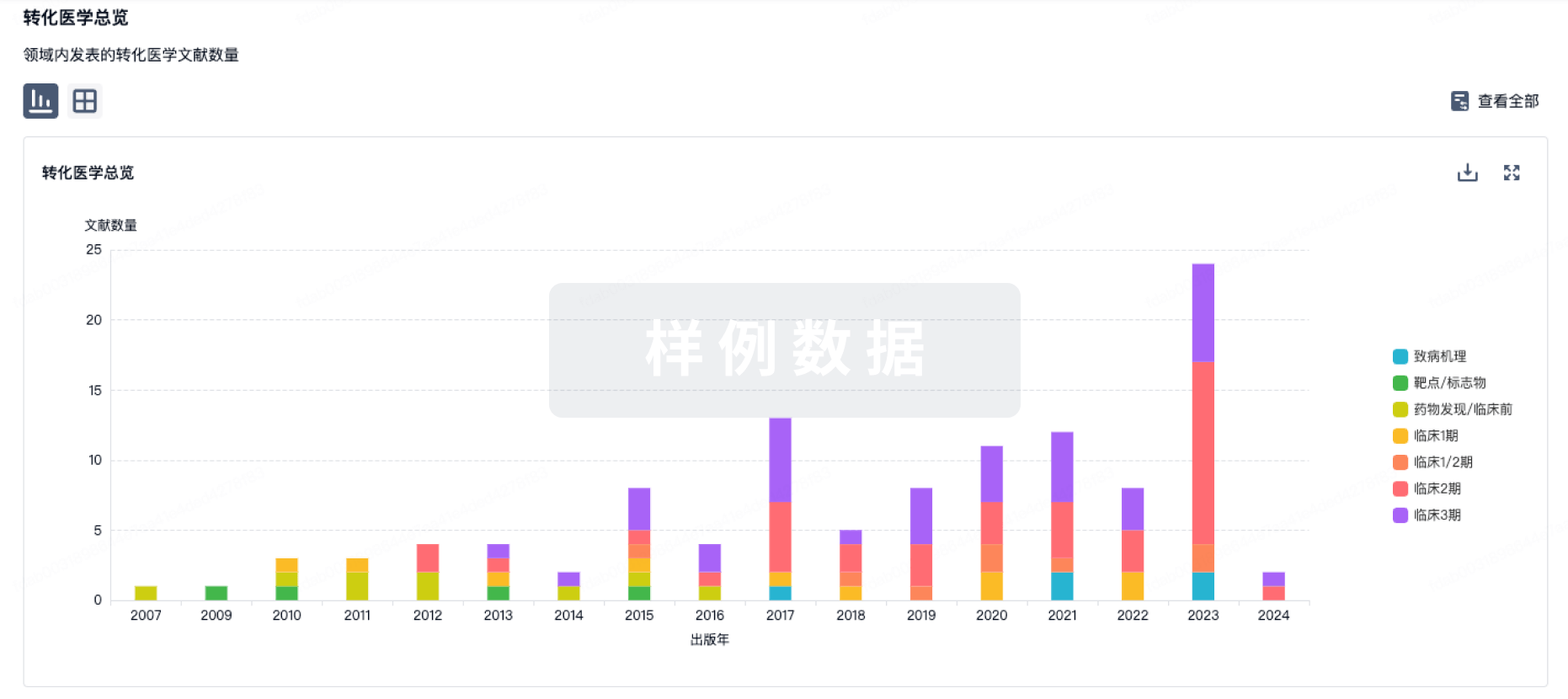
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
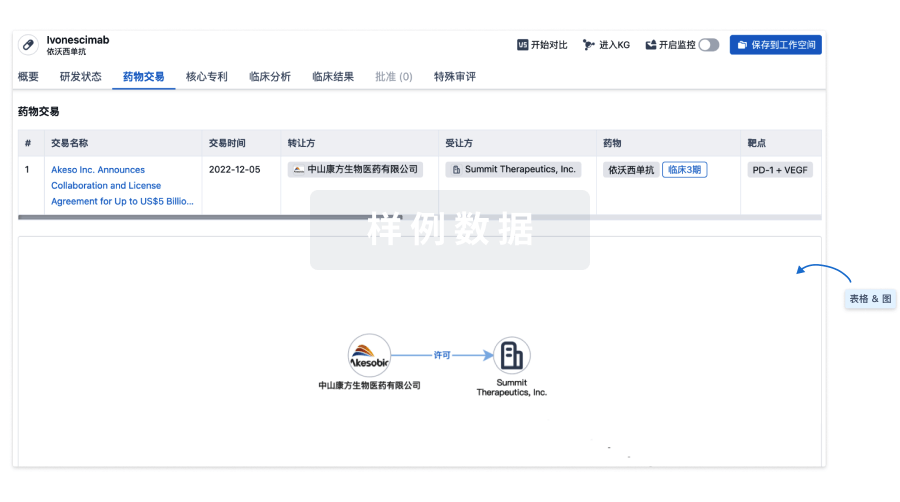
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
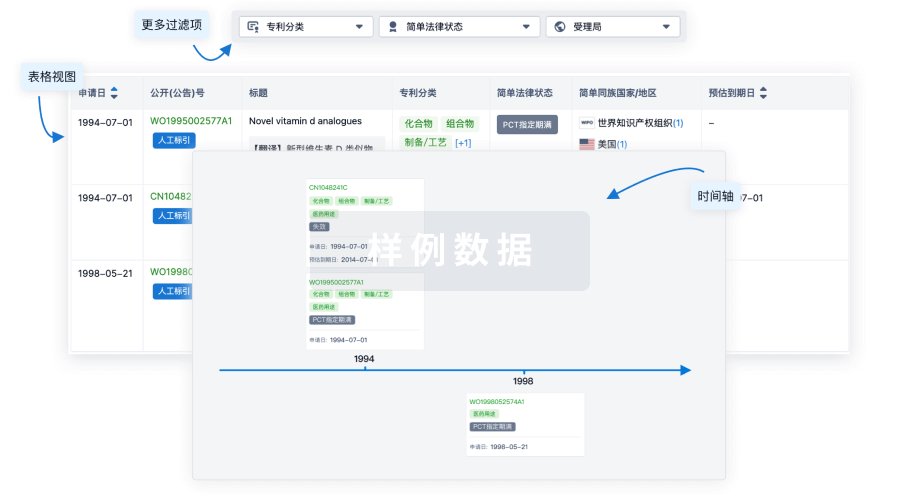
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
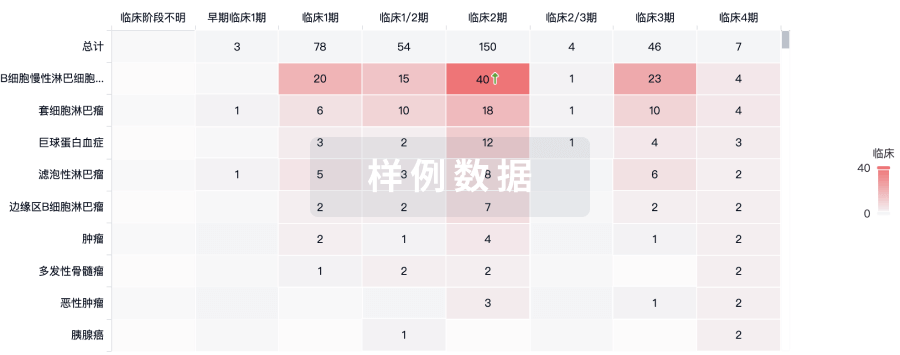
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
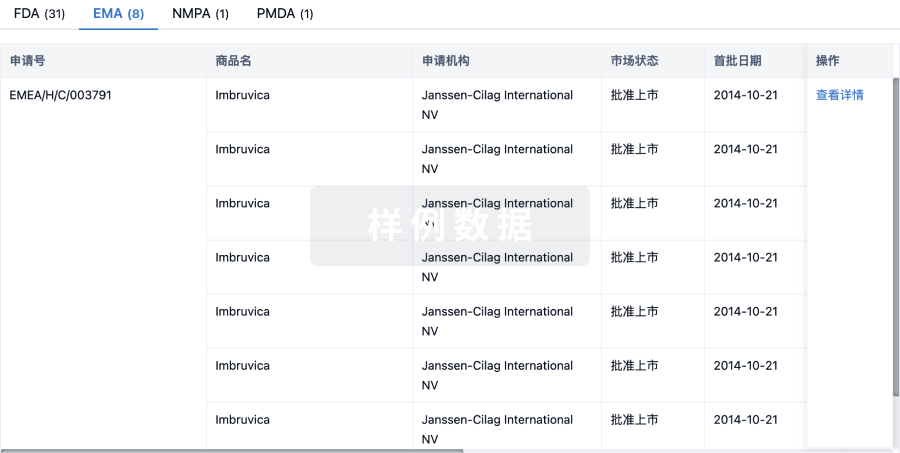
批准
利用最新的监管批准信息加速您的研究。
登录
或
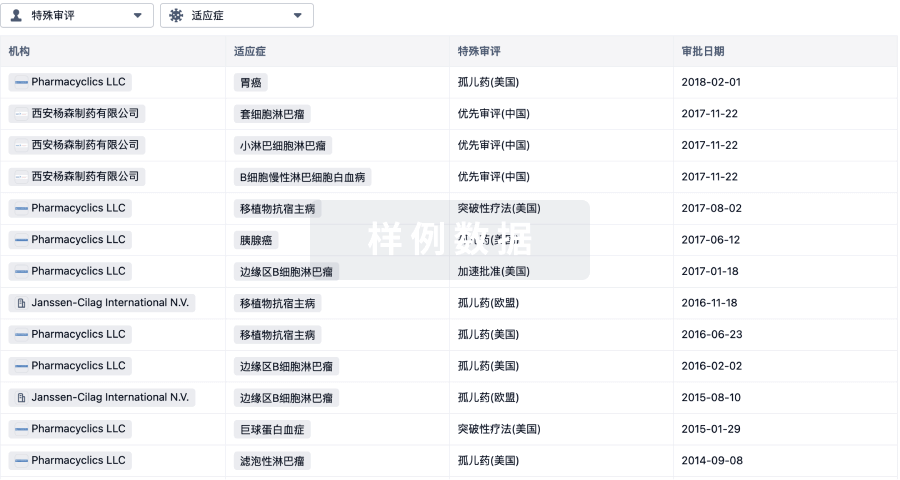
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用

