更新于:2024-09-28
Semaglutide biosimilar (G2GBIO)
司美格鲁肽生物类似药 (G2GBIO)
更新于:2024-09-28
概要
基本信息
原研机构 |
在研机构 |
非在研机构- |
最高研发阶段临床前 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
序列信息
Sequence Code 66716

关联
100 项与 司美格鲁肽生物类似药 (G2GBIO) 相关的临床结果
登录后查看更多信息
100 项与 司美格鲁肽生物类似药 (G2GBIO) 相关的转化医学
登录后查看更多信息
100 项与 司美格鲁肽生物类似药 (G2GBIO) 相关的专利(医药)
登录后查看更多信息
4
项与 司美格鲁肽生物类似药 (G2GBIO) 相关的新闻(医药)2024-08-02
·赛柏蓝
作者 | 陈芋
来源 | 赛柏蓝
01
22万例患者数据对比
“减肥神药”能“戒烟”?
去年6月,《柳叶刀》子刊eBioMedicine 上发表的一项研究表明,司美格鲁肽在减少大鼠酒精摄入和预防复发方面具有潜力。 时隔一年,司美格鲁肽再次在干预烟草成瘾方面释放出积极信号。
近日,发表于《内科学年鉴》(Annals of Internal Mediciane)的一项研究结果显示,相比使用其它降糖药物的患者,接受司美格鲁肽治疗的糖尿病合并TUD(即烟草使用障碍,指对烟草出现耐受现象并已成瘾)的患者,需要戒烟治疗的可能性降低32%。
该研究分析了22万多例诊断为2型糖尿病合并TUD患者的电子健康记录数据。这些患者在2017年12月-2023年3月期间有就诊记录,且过去一年内未使用任何降糖药物,同时至少符合司美格鲁肽的一种适应症。
研究团队比较了司美格鲁肽(5967例患者)与其它7种降糖药物(胰岛素、二甲双胍、二肽基肽酶-4抑制剂、钠‑葡萄糖共转运蛋白2抑制剂、磺脲类、噻唑烷二酮类和其它GLP-1RA类药物,共216975例患者)对12个月随访期间戒烟效果的影响,戒烟效果通过发生的TUD相关医疗服务(TUD诊断就医、戒烟药物处方和戒烟咨询)来衡量。
结果显示,与使用其他降糖药物相比,接受司美格鲁肽治疗的患者与TUD诊断就医几率显著降低相关。
其中,司美格鲁肽与使用胰岛素的效果差距更明显,司美格鲁肽可使TUD诊断就医几率降低32%,使需要戒烟药物处方的几率降低68%。
与其它GLP-1RA类药物相比,使用司美格鲁肽的患者TUD诊断就医几率降低幅度约12%,需要戒烟药物处方的几率降低38%。
不过,研究人员也指出,尽管该研究结果与司美格鲁肽对戒烟具有潜在益处的假设一致,但仍需要在未来的临床研究中进一步验证,目前尚不建议将司美格鲁肽常规用于戒烟。
02
获批用于预防中风、心脏病
司美格鲁肽适应症持续扩展中
在司美格鲁肽的基础治疗领域——糖尿病、肥胖,许多患者都存在并发症。
据世界卫生组织统计,糖尿病并发症高达100多种,是已知并发症最多的一种疾病。
去年8月发表于《糖尿病肥胖与代谢》(Diabetes,Obesity and Metabolism)的一项研究报告显示,在中国,近九成肥胖患者存在并发症,其中25.8%的肥胖患者有一种并发症,30.6%有两种并发症,22.8%有三种并发症,其余有四到八种并发症。
与二甲双胍不会只用于糖尿病治疗一样,司美格鲁肽的适应症也不会止步于糖尿病和肥胖。
7月25日,诺和诺德宣布欧洲药品管理局批准其司美格鲁肽(Wegovy)用于预防中风和心脏病。
该决定主要基于一项长达5年的SELECT临床试验,试验对17600人的用药情况进行了追踪,发现与安慰剂相比,司美格鲁肽能够将心血管事件(如心血管死亡、非致死性卒中和非致死性心肌梗死等)风险显著降低20%,且结果不受年龄、性别、种族、民族、体重指数 (BMI) 和肾功能受损程度的影响。
在欧盟批准的几天前,英国也批准了司美格鲁肽用于预防心脏病和中风,适应人群为BMI≥27 且已经被诊断患有心血管疾病的患者。
此外,司美格鲁肽还有慢性肾病、射血分数保留心衰、非酒精性脂肪性肝炎、阿尔兹海默症等更多领域的适应症探索“在路上”。这也刺激了更多药企布局。
今年4月,杭州九源基因递交的司美格鲁肽注射液“吉优泰”上市申请获受理,这是中国首款申报上市的司美格鲁肽生物类似药;6月,丽珠集团新北江制药的司美格鲁肽注射液上市申请也获受理。
除了上述两家已进入申请上市阶段的药企,还有更多企业处在临床阶段,包括翰宇药业、华润双鹤、正大天晴、特瑞药业、成都倍特等。
作为最受关注的GLP-1受体激动剂类药物,待司美格鲁肽专利到期后,其在国内市场的竞争也将更加激烈。
END
内容沟通:郑瑶(13810174402)
医药代理商产品交流群
扫描下方二维码加入
银发经济市场机遇表交流群
扫描下方二维码加入
左下角「关注账号」,右下角「在看」,防止失联
临床研究
2024-07-25
·药研网
手握潜在的国内首款司美格鲁肽生物类似药,杭州九源基因再启港股IPO。
据港交所7月24日披露,杭州九源基因工程股份有限公司向港交所主板提交上市申请。华泰国际、中信证券为联席保荐人。该公司曾于1月22日向港交所递交过上市申请。一国产GLP-1药企递交IPO招股书,估值约8.3亿元人民币
来源:港交所
九源基因已于今年6月份获得证监会的备案通知书,这意味该公司已获得进入聆讯阶段的前置条件。
据招股书透露,九源基因于1993年创立,是国内将基因工程应用于医药行业的先行者,拥有逾30年生物药品及医疗器械研发、生产及商业化经验。公司专注于四大快速增长中的治疗领域:骨科、代谢疾病、肿瘤及血液。据CIC称,这四大领域占 2023 年中国药品销售总额的 51.5%。
值得一提的是,九源基因瞄准了大火的GLP-1类药物赛道进行研发投入,且已成为临床试验进度较快的国产GLP-1。此次IPO九源基因计划通过商业化其司美格鲁肽生物类似药JY29-2(吉优泰)创造新的增长动力。
九源基因表示,为最大限度地发挥JY29-2的商业潜力,减轻价格限制对公司财务业绩的负面影响,其已采取措施,包括为即将实现商业化的JY29-2扩大销售及市场团队;及为即将推出的JY29-2升级及扩大生产能力。
图源:招股书
九源基因已围绕其“四大治疗领域”—骨科、代谢疾病、肿瘤及血液建立多元化的产品组合,当中包括8款已上市产品,以及超过10款在研产品(包括中国首款获得IND批准并递交NDA申请的司美格鲁肽生物类似药JY29-2)。
下表:九源基因上市产品
九源基因已上市产品:
骨优导:中国首款重组人骨形态发生蛋白-2(rhBMP-2)骨修复材料,于2022年按销售收入计,在中国骨修复材料市场中排名第二,市场份额17.2%;
吉粒芬:首款国产并获准于中国销售的人粒细胞刺激因子(hG-CSF),按销售收入计,在所有G-CSF药物中,吉粒芬于2022 年在中国排名第八,市场份额1.8%;
吉派林:中国首款商业化的国产仿制低分子量肝素钠产品,按销售收入计,吉派林于2022年在中国低分子量肝素钠市场达0.5%;
亿喏佳:依诺肝素钠仿制产品,于2022年在中国所有依诺肝素钠中排名第四,市场份额达8.1%;
吉巨芬:注射用人白介素-11(hIL-11),于2022年在中国所有白介素-11中排名第四,市场份额达8.2%。
其他还包括肿瘤治疗领域的化学仿制药吉欧停(盐酸帕洛诺司琼注射液)、吉芙惟(氟维司群注射液)、吉坦苏(注射用福沙匹坦双葡甲胺)。
下表:九源基因主要在研产品
JY29-2(吉优泰®):中国首款取得IND批准并完成III期临床试验的司美格鲁肽生物类似药,今年4月,该药物用于成人2型糖尿病患者的血糖控制的NDA已获获受理。这也是中国第一家申报上市的司美格鲁肽生物类似药。
JY29-2(吉可亲®):针对肥胖症及超重的适应症也于2024年1月取得临床试验申请批准,正在筹备Ⅲ期试验,预计于2024年开始该试验的患者入组。此外,九源基因还在开发口服司美格鲁肽生物类似药用于治疗肥胖症及超重,目前正处于临床前研究阶段。
JY23:一款将rhBMP-2与多款不同骨传导生物材料结合而成的下一世代骨修复材料,与骨优导相比,JY23在临床前研究中展现出更可控的释放能力及更好的骨传导性能。
JY06(吉新芬®):是一款用于治疗肿瘤化疗后中性粒细胞减少症的长效G-CSF产品,并为一款3类生物制品,已于2023年5月向国家药监局递交NDA。
九源基因在GLP-1受体激动剂类药物的研发上拥有近20年的经验,并通过与中美华东合作开发出中国首款获得IDN批准的利拉鲁肽在研生物类似药。受惠于所积累的研发经验,公司后面进一步开发出另一款GLP-1受体激动剂JY29-2。
司美格鲁肽生物类似药JY29-2被认为是九源基因的下一个重磅产品。司美格鲁肽是目前最畅销的GLP-1类药物,其化合物专利预计将于2026年到期。诺和诺德2023年大卖212亿美元,司美格鲁肽注射版降糖药Ozempic销售额138.89亿美元,同比增长60%;口服降糖Rybelsus销售额27.20亿美元,同比增长66%,该产品前不久在国内也获批上市。
回到业绩层面来看,多款产品组合为九源基因带来了连续三年营收逾10亿元的年收入。2021年至2024年截至4月30日止四个月,九源基因的收益分别约为13.07亿元、11.25亿元、12.87亿元、4.73亿元。其中,已上市产品收益占总收益比例较高,分别为87.6%、93.8%、91.5%及85.7%。
九源基因主要收入来源:骨优导
九源基因的大部分上市产品及在研产品均为生物类似药或小分子仿制药。2021年至2024年截至4月30日止四个月,其毛利率分别达到72.7%、75.9%、77.0%及74.9%,纯利率分别为9.1%、5.3%、9.3%及14.9%。
在营运资本方面,九源基因的现金储备较低,截至2024年5月31日,现金及其等价物仅为7704万元。不过其负债水平较低,流动负债总额为3.6亿元,流动资产净值为5.7亿元。
值得注意的是,九源基因曾获得华东医药、浙大网新(600797)、杭州金投的投资。股权架构方面,华东医药通过其全资子公司中美华东持有九源基因发行股本总额的约21.06%,为单一最大股东。
End
声明:本公众号所有发文章(包括原创及转载文章)系出于传递更多信息之目的,且注明来源和作者。本公众号欢迎分享朋友圈或大群,谢绝媒体或机构未经授权以任何形式转载至其他平台。
转载/商务/投稿 | 联系微信 wfj_GM
商务合作
稿件征集
点击了解详情
往期回顾
1
5月| 20家药企裁员(附名单)
2
18亿美元,ADC又出海! 宜联生物宣布新授权
3
2024 ASCO| 默沙东/科伦TROP2 ADC、信达、礼新CLDN18.2 ADC数据公布
生物类似药IPO上市批准
2024-07-24
GLP-1减肥药物,已经带不动上市公司的股价了。
7月9日,博瑞医药减重药物BGM0504公布了二期肥胖/超重临床研究盲态下初步优良结果,不仅股价未能刺激上涨,反而次日大跌。
7月19日,礼来的替尔泊肽减重适应症正式获得NMPA的批准,围绕其制造多肽产业链CXO也并未出现明显的异动,消息与股价似乎已经脱敏。
如果说脱敏是因为博瑞医药的初步数据不够完整,以及替尔泊肽减重适应症的获批早有预期,但甘李药业最新公布的更重磅临床数据也未能刺激市场。
7月22日,甘李药业发布GLP-1受体激动剂GZR18注射液在IIb期单双周给药临床数据:每两周一次12mg、18mg、24mg、48mg以及每周一次24mgGZR18注射液治疗30周后,平均体重较基线变化百分比分别为-11.15%、-13.22%、-14.25%、-17.29%和-17.78%,每两周一次48mg与每周一次24mgGZR18注射液的临床疗效和安全性相当。
甘李药业的GZR18作为GLP-1单靶点药物,通过差异化设计在患者耐受情况下提升给药剂量(替尔泊肽最高剂量为一周15mg),达到了媲美双靶点激动剂的减重效果(替尔泊肽72周减重20.1%),实属可贵。
即便如此,数据公布后依旧未能刺激公司股价,7月23日甘李药业股价收报43.14元,下跌4.58%。
是什么,导致了药企股价与GLP-1药物的关键临床数据脱敏?
01
江山代有才人出
GLP-1领域竞争内卷,新药物迭代速度飞快,前脚某药物数据出炉看起来是“同类最佳”,没过多久可能又被新的管线超越。
半年以前,我们对于潜在减重效果最强管线的认知还是在于礼来的GCGR/GIPR/GLP-1R三重激动剂Retatrutide,每周注射一次12mg的Retatrutide,48周治疗时间可助肥胖者体重减轻24.2%。
礼来GLP-1三靶点激动剂看似无懈可击,但架不住其他MNC通过不同方向对其进行“弱点攻击”,分别是依从性(长效、摄入方式)、减重速度等角度。
从更长注射周期的角度,安进的AMG-133完成了对现有GLP-1药物的超越,AMG-133的一期临床试验结果显示,肥胖患者只需每月注射一次AMG-133,治疗85天后体重可降低14.5%;同时,接受高剂量AMG-133治疗的患者,在停药150天后仍然维持体重减轻超过10%。
在减重速度方面,市场也有潜在新宠。罗氏在在今年5月公布了GLP-1/GIP双重受体激动剂CT-388的1b期临床数据:肥胖患者接受每周一次皮下注射CT-388,24周后患者平均体重减轻18.8%。这一减重疗效数据也超越了礼来的Retatrutide,其披露的临床试验数据显示,24周治疗的最高剂量组12mg患者减重幅度为17.5%。
反观国内,虽然远没有升级到迭代三靶点注射药物的先进性,但内卷的激烈程度并不亚于海外,这相信是甘李药业GZR18未能带动公司市值的重要原因之一。
GZR18可谓是前有猛虎后有追兵,尽管做出了优异甚至“同类最佳”潜力的临床数据,但目前处于2b期临床不占据进度优势。目前,礼来的Retatrutide已经在国内开启了多项三期临床,对现有在研早期GLP-1管线形成了碾压之势;同时信达生物的玛度仕肽虽然非头对头比较数据不及GZR18,但已递交上市申请。
国内后发的部分GLP-1双靶点分子,也不乏有“同类最佳”的潜力苗子,如众生药业GLP-1/GIP双重激动剂RAY1225一期临床数据显示:肥胖受试者接受两周一次滴定给药(总治疗剂量9mg和12mg),6周后患者平均降幅分别为5.33%和7.9%。
甘李药业的GZR18,或许需要一个BD或者加快临床推进速度了。
02
减肥药国内商业化顺序
最终,新药管线的潜力还是要落地到商业化的层面。
全球GLP-1市场固然广阔,2022年相关药物销售额高达222.27亿美元。若仅计算肥胖和糖尿病2大适应症,机构预计2030年美国GLP-1市场规模将达到900亿美元。据华鑫医药统计,2030年预计2500-8700万糖尿病及肥胖患者使用GLP-1药物,中性评估约有461亿元市场潜力。
值得注意的是,全球临床在研GLP-1药物超过100款,其中接近50%的分子来自国内药企。那么这意味着,国内的市场不到美国的1/10,但却有近50款药物争夺这部分市场。
参考过去PD-1的情况,先发的药物能够占据较大的优势,同时可能只有极少数的后发者能够像PD-1中的斯鲁利单抗一样通过差异化适应症、疗效及商业化能力多层面加持突围而出。
目前,已经获得减重适应症批文并商业化的GLP-1药物主要有4款,分别是华东医药的利拉鲁肽、仁会生物的贝那鲁肽、诺和诺德的司美格鲁肽和礼来的替尔泊肽,这是属于先发的“第一梯队”。
其次第二梯队处于NDA阶段的有两款药物,分别是信达生物的玛度仕肽(2024年2月)和华东医药的司美格鲁肽生物类似药(2024年4月),只不过由于司美格鲁肽专利未到期,前者面市将会更快。
第三梯队更为拥挤,全部都是处于临床三期阶段的分子。其中,礼来独占三个席位,分别是三靶点激动剂Retatrutide、复方减肥注射药CagriSem和口服片剂Orforglipron,而诺和诺德则是有一款司美格鲁肽片剂处于临床三期。
国产选手层面,进入临床三期的选手更多,包括先为达的Ecnoglutide、鸿运华宁的GMA105、恒瑞医药的诺利糖肽和HRS-7535、石药集团的TJ103和TG103等。不过,这大多数都是GLP-1单靶点注射药物,以Fast follow策略产物为主,恒瑞医药HRS-7535在其中的剂型较为独特,是口服片剂,进度可算国内前三。
后发的GLP-1药物研发厂商需要思量,在面对如此多的先发对手的背景下,未来要通过何种差异化来实现突围?
03
海外能够获得融资的减肥药新星
BMO Capital Markets的董事总经理Evan Seigerman表示,规模较小的代谢Biotech们在减重药物的研究进度上远远落后于礼来和诺和诺德,如果现在不处于第二阶段,那么到2028年或2029年将很难获得批准。
GlobalData的制药分析师Costanza Alciati则表示,尽管GLP-1主导市场是确定性趋势,但新进入者已经在寻找下一个可能彻底改变该领域的药物类型。
不妨放眼海外,过去几年进入减肥药领域并获得大额融资和BD合作的Biotech,正在做什么方向?
1)口服+多靶点激动剂:Metsera公司(融资3.5亿美元)通过对外BD引进构建了丰富的减重产品管线组合,包括初入临床阶段的DD02S,以及临床前阶段的DD03、DD07、DD14、DD15。从管线特征来看,DD02S是一款口服的GLP-1激动剂,而临床前阶段的分子大部分为多靶点的口服激动剂,旨在解决注射方式的局限性且提升口服药物减重疗效,如DD03是GLP-1/GCG/GIP三重激动剂,DD15则是GLP-1R/GIPR/GCGR三重激动剂。
2)新靶点新机制/GLP-1伴侣:全新的减重靶点无疑具备很强的吸引力,如35Pharma正研发TGF-β超家族靶点对代谢领域如减重适应症的影响,目标靶点包括其中的激活素Activins、TGF-βs等;
与诺和诺德达成合作的EraCal Therapeutics也是一个开发新靶点的典型Biotech代表,其开发了一种口服小分子资产,利用新的作用机制来调节食欲和体重,靶向一种控制外周肝脑信号传导的未公开蛋白质。
更值得一提的是“减肥药伴侣”的开发热潮,虽然GLP-1非常能打,但随着用药人群的扩大、真实世界数据库扩充,更多的“缺点”浮现,其中备受关注的便是减肥过程中的肌肉流失。针对该副作用的开发,已经有多个Biotech获得资金支持或被并购,包括开发艾帕素的BioAge、开发ActRII受体抑制剂的Versanis(礼来收购)等。
3)铲子:在药物研发产业中,一把好用的铲子是永恒的话题,能帮助MNC在源头开发迭代分子就赢在起跑线。Flagship创立Metaphore与ProFound分别获得了诺和诺德与辉瑞的合作支持,以开发新一代的减肥药物。
Metaphore与ProFound两家公司的药物开发平台,一个是计算驱动的生物平台,另一个则拥有庞大的新型蛋白质库,均能通过不同的药物开发策略达到开发新分子的目的。
结语:之所以部分国产减肥药临床里程碑与股价脱敏,除了缺乏新的引爆点和国内格局过于内卷之外,与当下市场资金聚焦于药企创新管线转化为商业化现金流核心点有着强关联。毕竟,当一个热点过去被反复消耗炒作,情绪散去,最后那是真的要拼刺刀了。
本文转载瞪羚社 /Kris.
免责声明
本文系转载,仅做分享之用,不代表平台观点。图片、文章、字体等版权均属于原作者所有,如有侵权请告知,我们会及时处理。
------------------------------
「长按」二维码添加小达「进群」
与更多行业伙伴共探市场前沿资讯
艾美达医药咨询
艾美达(北京)医药信息咨询有限公司,成立于2014年4月,是一家专业的医药行业咨询服务提供商。公司致力于将产业政策研究与真实世界的数据挖掘深度结合,洞悉行业政策对市场的影响,通过专业的研究提供前瞻性的市场分析,为企业产品上市后的市场准入提供整体解决方案。
临床2期临床结果
100 项与 司美格鲁肽生物类似药 (G2GBIO) 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 2型糖尿病 | 临床前 | 韩国 | 2023-11-03 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
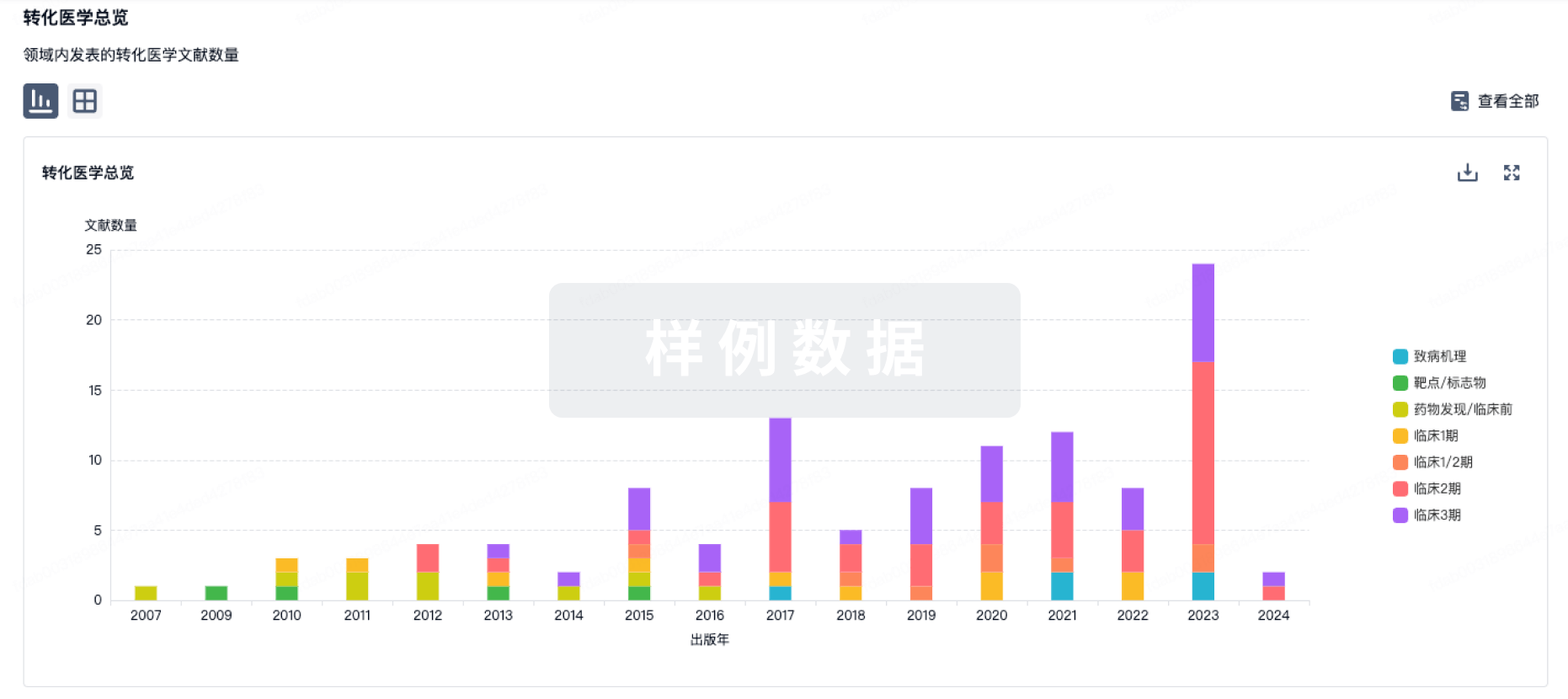
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
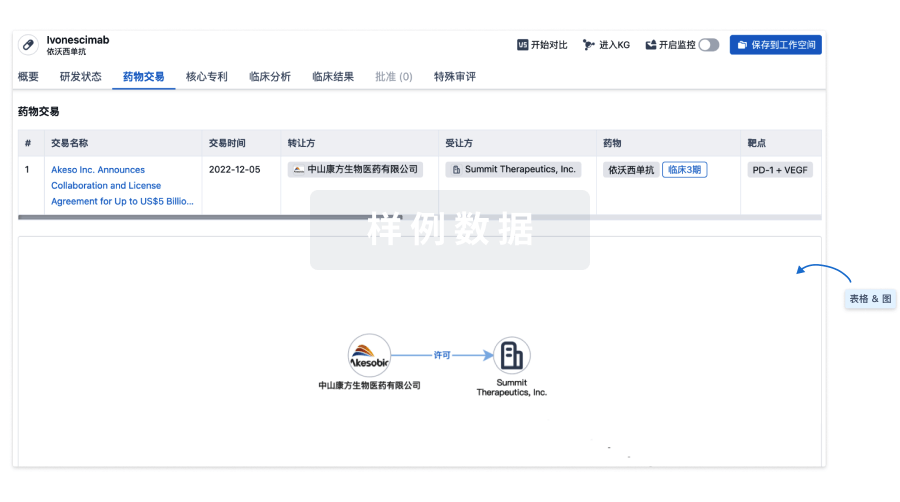
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
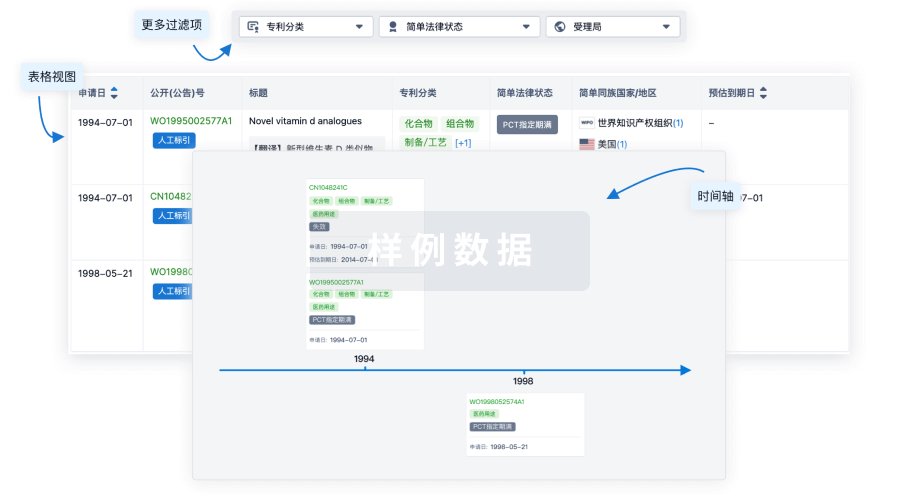
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
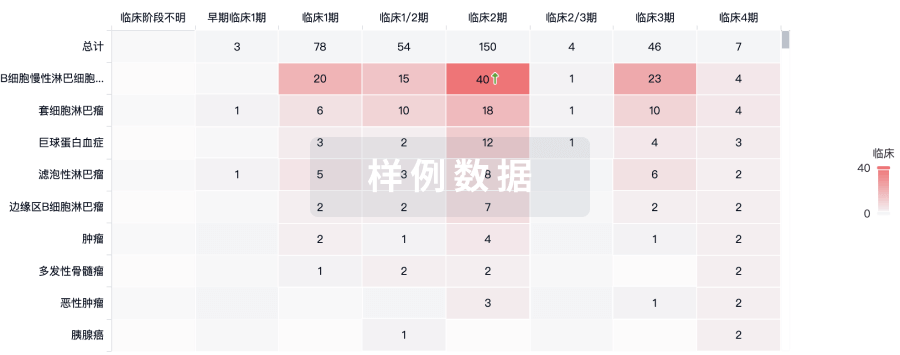
批准
利用最新的监管批准信息加速您的研究。
登录
或
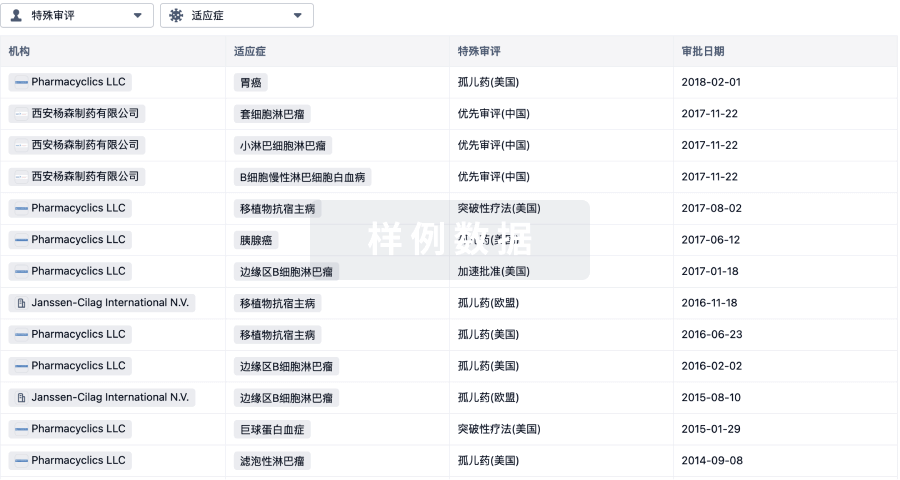
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用