更新于:2024-06-19
SBT-11-5301
更新于:2024-06-19
概要
基本信息
原研机构 |
在研机构 |
非在研机构- |
最高研发阶段临床1期 |
首次获批日期- |
最高研发阶段(中国)- |
特殊审评- |
关联
1
项与 SBT-11-5301 相关的临床试验A Randomized, Placebo-Controlled Phase 1 Study to Evaluate the Safety, Tolerability, and Pharmacokinetics of Single Ascending Doses of SBT115301 in Healthy Participants
This study will test the safety and effects of SBT115301 when given as a single dose to healthy adult volunteers. It is the first study being done in humans. Increasing dose levels will be given after the safety at lower dose levels is shown. Some participants will receive placebo, and neither the participants or the study staff will know what drug (SBT115301 or placebo) is being given.
开始日期2022-07-25 |
申办/合作机构 |
100 项与 SBT-11-5301 相关的临床结果
登录后查看更多信息
100 项与 SBT-11-5301 相关的转化医学
登录后查看更多信息
100 项与 SBT-11-5301 相关的专利(医药)
登录后查看更多信息
1
项与 SBT-11-5301 相关的新闻(医药)2023-05-09
·药明康德
▎药明康德内容团队编辑嘉宾简介:本期访谈的嘉宾Jeffrey Bluestone博士是Sonoma Biotherapeutics的首席执行官和联合创始人。该公司成立于2019年,是一家专门利用经工程化改造的调节性T细胞(Treg)开发治疗自身免疫和炎症性疾病疗法的生物技术公司。成立之初,Sonoma Bio公司便获得了4000万美元A轮融资,并在2021年完成高达2.65亿美元的B轮融资 。美国FDA于2022年批准了该公司旗下产品SBT-11-5301的1期临床试验,这是一种在研生物制品,专门用于消除高度活化的效应T细胞(Teff),这些细胞在自身免疫性和炎症性疾病中很普遍。Jeffrey Bluestone博士在免疫学领域有着深厚的研究积累,担任过多家知名学术机构的领袖。在40余年的职业生涯中,他发表了500多篇论文,他的工作为多种免疫疗法的开发提供了依据。药明康德内容团队:您好,祝贺贵公司的产品获得了IND许可!您能介绍一下您公司的新技术和治疗模式吗,以及贵公司如何利用它们来解决与细胞和基因治疗相关的难题?Jeff Bluestone博士:好的。Sonoma Bio是基于我和共同创始人在学术领域的工作,我们的研究利用了一种名为调节性T细胞的新型细胞群来探索治疗一系列疾病的可能性,如自身免疫疾病、器官移植排斥反应和其他炎症性疾病。该治疗模式实际上是基于细胞疗法,细胞疗法已经在癌症领域开辟了新的道路。我们使用一个非常不同的细胞群,这些Tregs细胞旨在关闭免疫反应或诱导一个耐受性环境,这样患者就不会继续遭受持续的自身炎症疾病的困扰。这无疑是尖端技术。到目前为止,许多细胞疗法在很大程度上局限于治疗癌症,而使用新型细胞群来治疗自身免疫性疾病的想法,已经在临床前和早期学术性临床研究中得到了测试。作为一家公司,我们认为我们的差异性与平台本身和我们所使用的细胞有关。基于数十年与这些细胞打交道的经验,我认为我们拥有一流的能力来识别、分离纯化的细胞群体,有选择地扩增它们,并赋予它们针对特定自身免疫性疾病和炎症性疾病的特异性。我们希望这将是一种一劳永逸的治疗方法,作为活体疗法的细胞将能够进入炎症部位,增殖、激活,并在很长的一段时间内治疗疾病。药明康德内容团队:您预计贵公司的方法将对哪些自身免疫性疾病产生最显著的影响,以及这将如何转化为患者的实质性获益?Jeff Bluestone博士:世界上有很多很多自身免疫性疾病,已经有超过80种疾病被报道。我们有目的性地选择了其中几种,以便将我们的首批疗法应用于这些疾病领域。首先是我们的产品SBT-77-7101,它是一种CAR-Treg。CARs是嵌合抗原受体,已被用于癌症治疗,它结合了一种能识别组织上某个靶点的抗体,并与激活Tregs的信号传导结构域构成融合蛋白。这种疗法针对的是类风湿性关节炎患者关节中存在的一种蛋白质,即所谓的瓜氨酸化蛋白,这是这种疾病患者中典型的生物标志物,因为瓜氨酸化蛋白是一种在自身免疫组织和炎症组织中积累的新抗原,实际上会诱发这些患者产生自身抗体。该产品目前正准备进入临床,它将被用于治疗那些经其他药物治疗后失败并且疾病仍处于活动状态的类风湿性关节炎患者。我们对其他适应症也非常感兴趣,其中最突出的是炎症性肠病,包括克罗恩病和溃疡性结肠炎,我们计划尝试开发独特的CARs和TCRs,并将其设计进我们的Tregs中,使这些细胞能够识别存在于那些炎症组织中的蛋白质,以此实现免疫调节和免疫耐受。我们希望通过这些疗法能够针对性地治疗那些表达特定抗原的疾病患者,从而实现高度特异性和选择性的免疫抑制。最后,免疫系统是一个高度平衡的系统,一些挑战不仅与Tregs的缺失或丧失有关,而且还与难以控制的效应细胞扩增有关。因此,我们也在开发一种名为SBT-11-5301的药物,旨在消除这些过度激活的效应细胞,从而使免疫系统重新达到平衡。我们设想了一种连续的组合疗法,在这种疗法组合中,SBT-11-5301被用于患者的预治疗(pre-condition),随后再采用Treg进行治疗。药明康德内容团队:在您看来,在充分发挥贵公司新技术的潜力方面还有哪些主要挑战,您认为潜在的解决方案又有哪些?此外,在此过程中,您预计会有什么重大里程碑吗?Jeff Bluestone博士:我认为在我们的领域,现在的关键挑战是机制验证。证明这些细胞能够被开发为产生持久缓解的疗法,成为了我们的最高目标。其中最重要的挑战是挑选合适的疾病和患者群体,以便我们能观察到临床效果。正如我所说,这些细胞是数量较少且独特的细胞群,需要一些高度有效的纯化策略。如何分离这些高纯度的细胞并将其制造到具有治疗能力的水平,同时确保它们的稳定性——不会转化为效应细胞,使得它们能够行使Tregs所表达的多种功能——包括免疫抑制活性和组织修复活性等,在这些方面仍然存在着挑战。最后,执行冷冻保存方案,使我们能够以一种可运输到世界各地去救治患者的方式来冻存这些细胞。我相信我们已经在这些挑战中取得了进展,这非常关键。对我们来说,关键的里程碑是让这些细胞进入病患体内,并证明这种疗法能够缓解疾病进展,而且能以安全和持久的方式做到这一点。到目前为止,我们确实取得了重要进展。我们的效应T细胞调节生物制品SBT-11-5301已经进入临床阶段,我们最新的研发和制造中心已经破土动工,这都是公司的重要里程碑。我们还提交了早期数据,凸显了我们的Treg疗法在类风湿性关节炎中的潜力,并期望这一主导项目将在今年进入临床阶段。▲Sonoma Biotherapeutics的产品管线(图片来源:Sonoma Bio公司官网)药明康德内容团队:除了技术进步之外,您认为阻碍细胞和基因治疗领域取得进展的最主要障碍是什么?Jeff Bluestone博士:这是一种新的治疗模式。因此,我们高度专注于进入临床阶段并证明其有效性。我们所面临的障碍是该领域每个人都面临的障碍——如何制造出一种强大的、持久的、具备功能性的活体疗法。我们使用的是自体细胞,这意味着细胞来自接受治疗的患者本身,因此,需要了解在构建这种新疗法时将面临哪些监管方面的挑战。此外,确保如果我们在治疗像类风湿性关节炎患者这样的慢性病患者时,疗效确实能够持久维持下去。我们也像细胞和基因治疗领域的其他公司一样,非常专注于早期的发现工作和更多的基础科学工作,以确保我们不仅能够开发出一种功能性的疗法,而且能够让全世界的人都能获得这种疗法,以此在治疗中实现平等。我们的首批适应症之一很可能是针对那些因为难以获得药物而受到忽视的少数群体的疾病,所以我们对未来的发展方向感到兴奋,我们知道障碍是存在的,但我们有信心,我们将能够实现这些细胞的治疗应用。药明康德内容团队:您对未来五年细胞和基因治疗领域的发展有什么期望?Jeff Bluestone博士:我真的相信,我们正处于一种新疗法诞生的前夕,这是一种平台式的疗法,将改变我们对于治疗这些慢性疾病患者的思考方式。这让我想起了20世纪末的工业革命,在那次工业革命中,我们处理事物的方式发生了根本性的变化。我认为过去几十年间的生物革命将使21世纪医学的发展方式类似于我们在上个世纪改变工业流程的方式。正因为如此,我认为细胞和基因治疗是将要引领潮流的领域。我相信,如果成功的话,我们将开发出让那些病情最重的患者一次治疗,终身获益的治疗方法,这些治疗方法将具有持久性并且能够实现治愈。药明康德内容团队:在您看来,关于生物技术和医药行业的研发效率和生产力等方面,目前的状况如何,您认为是否有提升的空间?如果有,可以采取什么措施来实现提升?Jeff Bluestone博士:我认为研发效率和行业生产力在总体上取决于两个方面——在研的治疗模式是什么、以及它是如何被测试的。我认为,对我们来说,让我们的研究人员、早期发现科学家、以及制造团队之间进行密切合作,将是我们建立团队的关键。因为研发效率实际上是研究和开发之间的联系。事实上,我们越是能够密切合作,我们就越能开发出有效和可靠的治疗方法。显然,疫情对合作产生了很大影响,我认为随着我们走出疫情,我们将有希望不仅在我们公司内部建立合作关系,还要提高研发效率,在提供互补技术和洞见的公司之间建立更强大的关系,这将使我们真正以更积极的方式推动这些疗法的发展。图片来源:123RF药明康德内容团队:您认为在哪些方面有降低成本的机会,为患者提供更大的益处?Jeff Bluestone博士:我认为有很多方法可以降低成本。首先,最重要的是了解我们在这里谈论的疗法,即细胞和基因疗法,它们有可能成为一劳永逸的疗法。我认为我们还可以考虑在确诊前更早地介入这些疾病,例如,当有证据表明存在自身免疫性疾病迹象,但还没有发生完全的组织破坏时,在这种情况下,如果我们能够在疾病早期就有效地使用这些疗法,就可以避免慢性疾病的长期成本,如关节置换、移植或组织重建。这意味着真正了解如何确诊这些疾病并识别那些面临患病风险的人,因为这些人群才是你想要尽早介入治疗的人。最近,我参与了一种刚刚被批准用于治疗1型糖尿病的药物teplizumab的开发。这种药物实际上是在患者真正在临床上被确诊之前就对他们进行治疗,尽管他们已经患有自身免疫性1型糖尿病。因此,这类机会将改变成本结构,因为它将避免这些破坏性疾病所带来的一些最昂贵的下游后果。药明康德内容团队:您预计2023年及以后,会有哪些对患者的生活产生重大影响的激动人心的进展?Jeff Bluestone博士:我想我们都意识到,细胞疗法的进展可能首先出现在癌症领域,当我们开始了解如何通过这些细胞直接针对不同的癌症,包括实体瘤和其他液体肿瘤,我认为这将改变我们对这种新疗法的思考方式。此外,胚胎和成人干细胞、用于治疗的T细胞等方面也可能会取得进展,其他的细胞类型如自然杀伤(NK)细胞也可能参与其中。在操纵基因组的新方法方面也可能取得进展,使这些细胞具有更强大的功能、稳定性和有效性。我认为这些都将在2023年发生,我们将看到这些进展对人们的生活产生影响。在调节性T细胞方面,关于我们的专业领域和我们的产品,我认为我们将再次能够利用细胞的多功能组织修复治疗特性,我想,在2023年你将看到一些公司(包括我们自己),真正展示这些细胞的力量,作为新一代的细胞疗法来治疗癌症以外的疾病。我真的很高兴看到在这个领域的所有人都在努力开发这些新治疗方法。我认为在非癌症领域的细胞治疗正处于一个非常激动人心的时刻。药明康德内容团队:鉴于新治疗模式的出现,您预计FDA审批程序在未来十年会有什么变化?Jeff Bluestone博士:我认为美国FDA已经在前瞻性地思考如何将细胞和基因疗法作为药物来考虑,以及如何考虑批准问题。他们已经组织了一个名为OTAT的新小组,该小组雇用了很多人员来审查这些方案或思考如何制定IND(用于获得批准进行人体试验的申请文件),其方式是灵活的,可以随着时间的推移进行调整。理解细胞治疗领域,它作为一种药物意味着什么?拥有一种可以进行化学分析并确保每次生产都相同的小分子药物是另一回事。细胞来自不同的人,当它来自不同的人时,它们不会完全一样。我看到美国FDA正在开发各种方法来了解这些细胞的关键属性,以便每次都能可靠地进行化验或分析,并让患者相信他们获得的细胞将发挥作用。这对监管机构和我们这些试图开发这类疗法的人来说,都将是一个挑战,要确保批准的范围足够广泛,既能够应对该领域的创新,同时还能保持疗法的安全性和有效性。药明康德内容团队:感谢您的精辟见解!作为药明康德旗下专注于细胞和基因疗法的CTDMO,药明生基致力于加速和变革基因和细胞治疗及其他高端治疗的开发、测试、生产和商业化。药明生基能够助力全球客户将更多创新疗法早日推向市场,造福病患。如您有相关业务需求,欢迎点击下方图片填写具体信息。▲如您有任何业务需求,请长按扫描上方二维码,或点击文末“阅读原文/Read more”,即可访问业务对接平台,填写业务需求信息▲欲了解更多前沿技术在生物医药产业中的应用,请长按扫描上方二维码,即可访问“药明直播间”,观看相关话题的直播讨论与精彩回放免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。版权说明:本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「药明康德」微信公众号回复“转载”,获取转载须知。分享,点赞,在看,聚焦全球生物医药健康创新
细胞疗法免疫疗法临床1期基因疗法临床申请
100 项与 SBT-11-5301 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 自身免疫性疾病 | 临床1期 | 美国 | - | |
| 炎症 | 临床1期 | 美国 | - | |
| 1型糖尿病 | 临床前 | 美国 | - |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
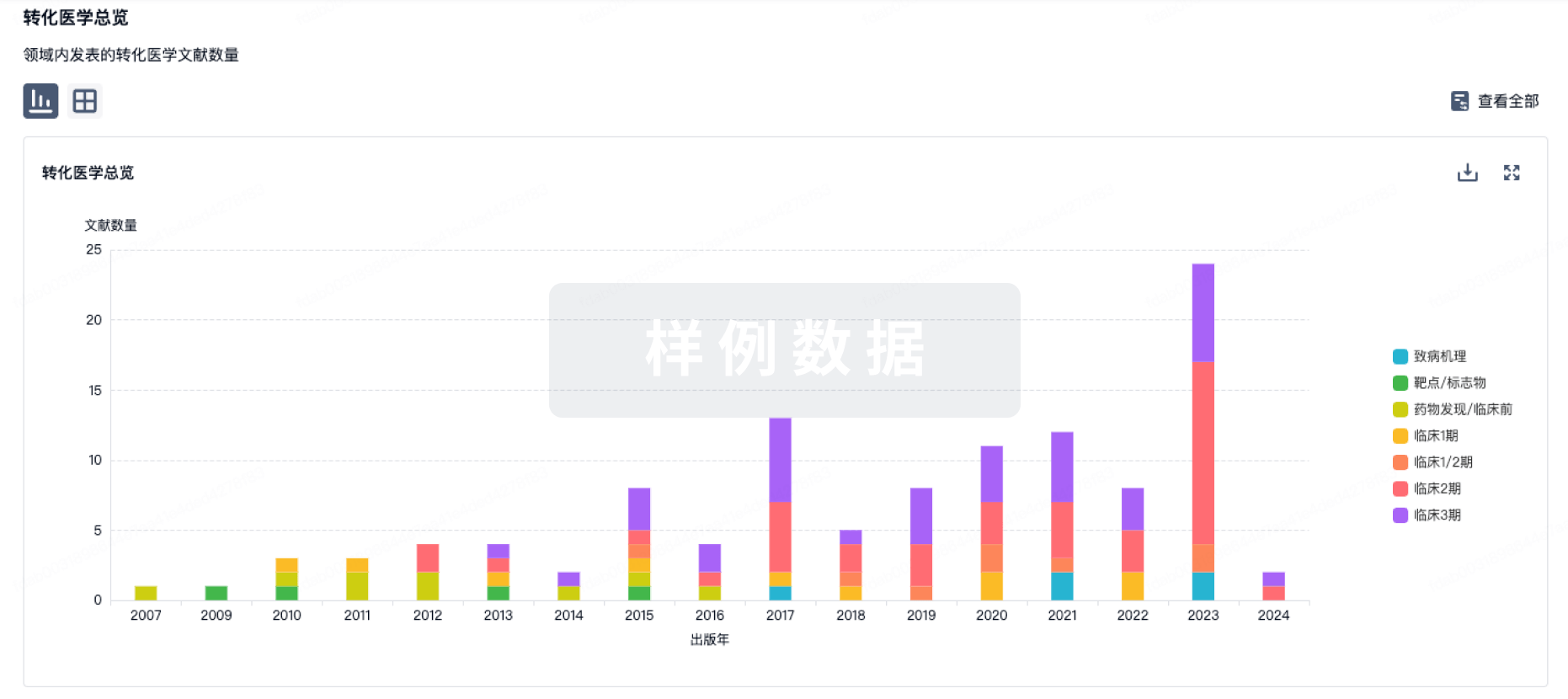
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
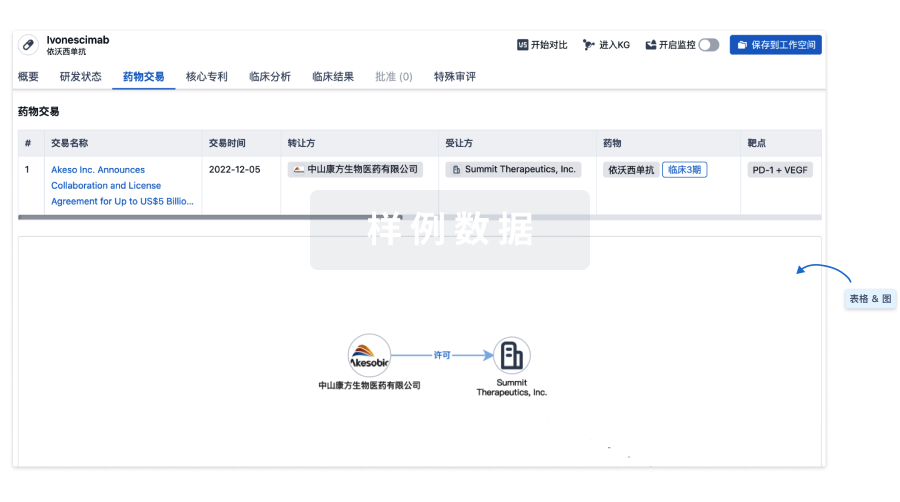
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
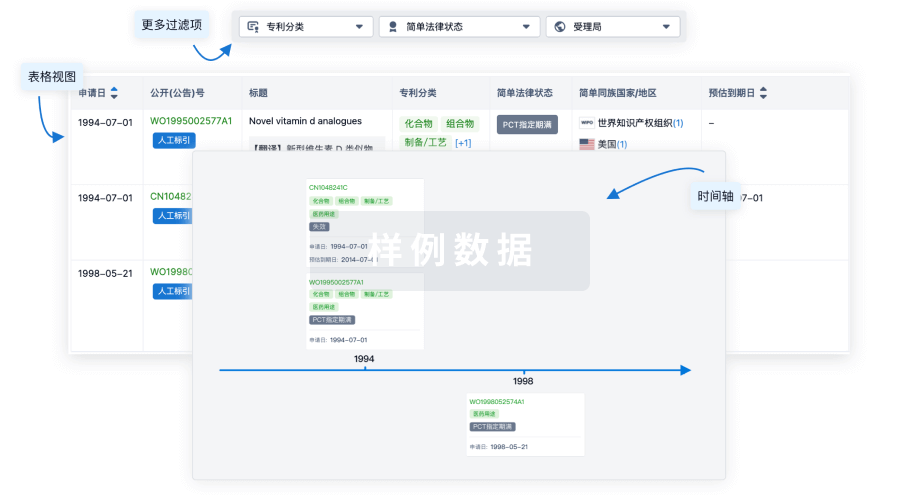
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
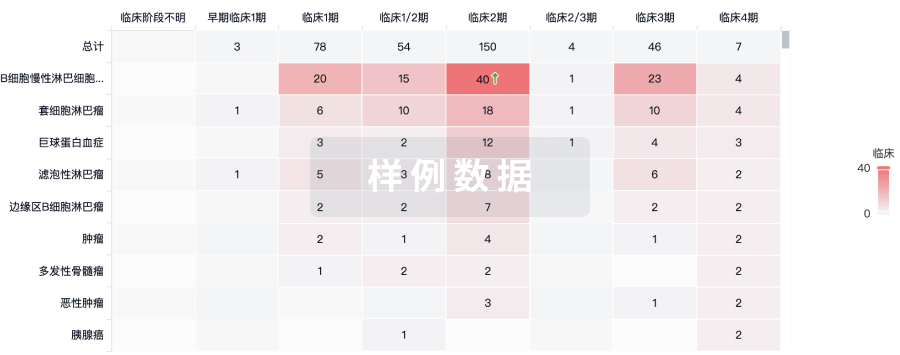
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
批准
利用最新的监管批准信息加速您的研究。
登录
或
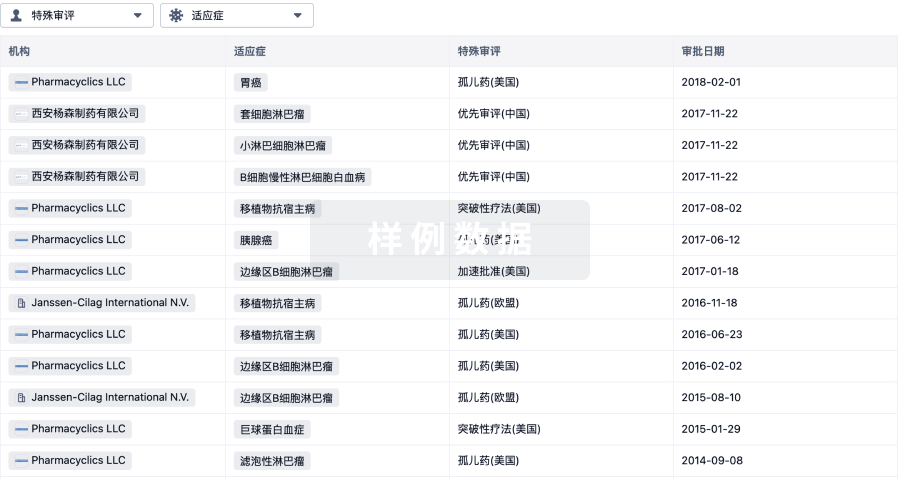
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用

