更新于:2024-12-21
TQA-3038
更新于:2024-12-21
概要
基本信息
原研机构 |
在研机构 |
非在研机构- |
最高研发阶段临床1/2期 |
首次获批日期- |
最高研发阶段(中国)临床1/2期 |
特殊审评- |
登录后查看时间轴
关联
4
项与 TQA-3038 相关的临床试验评价 TQA3038 注射液在慢性乙型肝炎患者中安全性、耐受性、药代动力学特征和抗病毒疗效的 Ib/IIa 期临床试验
Ib期临床试验:
主要目的:
评价TQA3038注射液联合/不联合核苷酸类药物在初治/经治慢乙肝患者中的安全性和耐受性
次要目的:
评价TQA3038注射液联合/不联合核苷酸类药物在初治/经治慢乙肝患者中的抗病毒疗效
评价TQA3038注射液在初治/经治慢乙肝患者中的药代动力学(PK)特征
评价TQA3038注射液的免疫原性 IIa期临床试验:
主要目的:
评价TQA3038注射液联合核苷酸类药物在经治慢乙肝患者中的抗病毒疗效
次要目的:
评价TQA3038注射液联合核苷酸类药物在经治慢乙肝患者中的安全性和耐受性
开始日期2024-07-19 |
申办/合作机构 |
A Phase Ib/IIa Clinical Trial to Evaluate the Safety, Tolerability, Pharmacokinetic, and Antiviral Efficacy of TQA3038 Injection in Patients With Chronic Hepatitis B
This study is divided into two parts. Phase Ib is a randomized, double-blind, placebo-controlled trial, designed to evaluate the safety, tolerability, pharmacokinetic characteristics, preliminary efficacy, and immunogenicity of TQA3038 injection in patients with chronic hepatitis B. It is expected to include 72 subjects. Phase IIa adopted an open-label, randomized, parallel-controlled design, with a total of 90 subjects included, mainly evaluating the changes in serum HBsAg compared to baseline at the end of the 48th week.
开始日期2024-06-01 |
申办/合作机构 |
A Phase 1, Randomized, Double-Blinded, Placebo-Controlled Study to Evaluate the Safety, Tolerability, Pharmacokinetics of TQA3038 Injection in Healthy Adult Subjects.
This is a phase 1 study in which healthy adult subjects will receive TQA3038 or placebo and will be assessed for safety, tolerability, pharmacokinetics.
In the single ascending dose (SAD) part, healthy adult subjects will receive one dose of TQA3038 or placebo, administered subcutaneously (SC).
In the single ascending dose (SAD) part, healthy adult subjects will receive one dose of TQA3038 or placebo, administered subcutaneously (SC).
开始日期2023-11-30 |
申办/合作机构 |
100 项与 TQA-3038 相关的临床结果
登录后查看更多信息
100 项与 TQA-3038 相关的转化医学
登录后查看更多信息
100 项与 TQA-3038 相关的专利(医药)
登录后查看更多信息
22
项与 TQA-3038 相关的新闻(医药)2024-09-18
·药智网
一个新药IP能否成功,其最关键的因素无外乎两点,商业化与成药性。
以ADC为例,一方面截至目前全球(中美欧日)已有17款新药获批上市,另一方面Enhertu年销售额突破20亿美元,无论是成药性还是商业化均满足了相关条件,是新药领域成功的显著代表。
但同时,近年来迅速发展的“小核酸”领域,其IP成功的前提条件也已完备。
一方面,小核酸三巨头(ionis、alnylam与sarepta)负责解决小核酸成药性问题,利用偶联物、脂质纳米颗粒和生物材料解决了双链siRNA分子大,带电荷高,易生物降解等一个又一个局限性;
另一方面,诺华则率领MNC验证小核酸药物的商业化逻辑,上市产品销量与日俱增,2024年上半年业绩中,siRNA长效降脂针Leqvio的销量同比增速达137%,是在售药品中的增长之最。
很明显,小核酸领域已初具当初ADC爆发前的底层逻辑,有望成为继ADC之后的又一高景气前沿领域。
优势明显
资本推动国内小核酸领域爆发
所谓小核酸疗法,是基于中心法则,在基因转录后、蛋白质翻译前阶段进行调控的创新疗法,目前较为成熟的技术主要有ASO、RNAi两类。目前在遗传疾病、肿瘤、病毒感染等疾病的治疗上应用广泛,有望成为继小分子药物和抗体药物后的第三大类药物。
图注:核酸药物分类,图片来源:中信证券
现阶段,小核酸药物已在临床中初步展现出治愈疾病、替代现有疗法和填补空白适应症的能力,相继出现Leqvio 和Spinraza 等重磅品种。与现有疗法相比,小核酸疗法的优势主要体现在以下几点:
研发周期短:由于作用目标绕开了蛋白质翻译环节,原则上无需考虑蛋白质的复杂机构,只需要针对致病基因序列或者关键转录环节进行RNA片段设计,靶点筛选迅速,研发速度快。
治疗范围大:虽说小核酸药物的适应症大多集中在DMD等基因层面罕见病上,但理论上由于小核酸的成药性不受限于蛋白质,理论上可以适用于任何拥有mRNA的序列信息的遗传疾病和其他难治疾病。
效果持久:由于小核酸药物可以在体内被循环多次使用,因此药物的使用频率大幅下降,部分新药甚至能做到半年一次,这对于多数慢性病而言,无疑是提供了巨大的临床价值。
安全性高:小核酸药物给药剂量小、频率低,是天然存在的生物过程,可被生物降解,细胞毒性和免疫原性低,在mRNA层面进行干预,对基因组无影响。
耐药抗性高:由于抗体和小分子主要通过调节细胞信号通路和代谢等方式发挥治疗作用,因此可能会由于补偿通路上调或抗原表达下降等因素产生耐药性,而小核酸药物直接调节上游基因表达,因此相对不易产生耐药性。
而也正是因为上述核心优势,小核酸领域理想中能给医药领域带来的意义也越来越被重视,整体情况与早几年的抗体药物非常类似,就现阶段而言,国内小核酸领域无论是BD交易,还是融资领域的表现均极为亮眼。
就BD交易领域而言,仅2024年初,国内就有瑞博生物与舶望制药分别于德国勃林格殷格翰与诺华达成合作协议,目标直指小核酸创新疗法,交易金额达数十亿美元。
2024年小核酸领域融资详情(截止9月13日,点击查看大图)
数据来源:公开数据整理、药智数据
而在国内融资领域,截止目前,小核酸领域已出现了23起融资事件,融资金额总额近30亿元。其中,促成融资的主要因素除各biotech企业的创新技术平台外,上下游的原料药、CDMO、AI企业也在积极入局。
技术助力
国内企业跳跃式布局
回想当初Alnylam创立的那个年代,有魄力创立一家RNAi企业无外乎在70年代末或80年代初创办一家单克隆抗体治疗公司,是充满冒险的举动。
但如今,经过小核酸三剑客对路径的充分探索之后,领域内血液稳定性不佳、主动靶向性差、细胞内吞能力差等局限性,通过修饰与递送方面的技术革新已得到较好地解决,相关药物开发成功率骤升,截止目前已有多款新药上市,且收入稳步上升。
类型
药品名称
公司
2023年销售额(美元)
增速
ASO
Spinraza
lonis &Biogen
17.41
-3%
Eteplirsen
Sarepta
5.41
6%
Golodirsen
Sarepta
1.3
11%
Viltepso
Nippon Shinyalku
1.3
/
Tegsedi
lonis
0.3
16%
Waylivra
Qalsody
lonis &Biogen
0.1
/
Nedosiran
诺和诺德
/
/
eplontersen
阿斯利康&lonis
/
/
siRNA
Amvuttra
Alnylam
5.6
494%
Leqvio
Alnylam &诺华
3.55
217%
Onpattro
Alnylam
3.55
-36%
Casimersen
Sarepta
2.7
28%
Givlaari
Alnylam
2.2
27%
Oxlumo
Alnylam
1.1
57%
核酸适配体
lzervay
安斯泰来
0.78
-3%
数据来源:公开数据整理
小核酸产业发展至今,其整体构成已初步完备,成员主要可以分为三种不同类型,其一是作为领域中流砥柱的头部biotech企业,其二是作为市场化主要推动力的MNC企业,其三则是进度追赶迅速的biotech后继者。
而对于国内小核酸产业而言,现阶段绝大多数biotech企业尚只是扮演“追赶者”角色,在源头技术创新领域与海外头部Biotech企业仍有较大差距。不过,在新药适应症布局上,国内企业却在开拓者的研究基础上,前瞻性地跳过了罕见病研发阶段,转而考虑病患基础更大、受众群体更广泛、临床需求更明确、未来趋势更明显的慢病领域发展。
对比海内外小核酸的适应症布局,除两者均作为重点发展的肿瘤领域外,国内对遗传性罕见病的布局不同于海外,进入临床阶段的管线占比仅7.8%,眼科等感觉器官的占比也比较类似,总体上,国内小核酸领域在代谢、感染与心血管等慢病领域的适应症研究比例则远高于海外。
企业
代表管线
专注领域
靶点
适应症
临床阶段
圣诺生物
STP-702
siRNA
PA protein;M1 protein
流感病毒感染
注册申请
STP-122G
siRNA
Factor XI
血栓
临床I期
STP707
siRNA
PTGS2;TGFB1
实体瘤
临床I期
科特拉尼
siRNA
PTGS2;TGFB1
皮肤鳞状细胞癌;肝细胞癌
临床II期
舶望制药
BW-01
siRNA
PA protein;M1 protein
心血管疾病;重度高甘油三酯血症
临床Ⅱ期
BW-03
siRNA
PA protein;M1 protein
慢性乙肝
临床Ⅰ期
瑞博生物
考多西兰 cosdosiran
siRNA
CASP2
视神经病变;闭角型青光眼
临床Ⅲ期
RBD-4059
siRNA
Factor XI
冠状动脉疾病;血栓栓塞;栓塞和血栓形成
临床Ⅱ期
RBD5044
siRNA
ApoC-III
高脂血症
临床Ⅰ期
IONIS-GCGRRx
ASO
GCGR
2型糖尿病
临床Ⅱ期
天龙药业
YKYY-015
核酸偶联药物;siRNA
PCSK9;ASGPR
原发性高胆固醇血症;混合型高脂血症
临床申请
CT102
ASO
IGF1R
肝细胞癌;肝癌
临床Ⅱ期
君实生物+润佳医药
RP-910
siRNA
PCSK9
心血管疾病;血脂异常
临床Ⅰ期
JS401
siRNA
ANGPTL3
高脂血症
临床Ⅰ期
维亚臻生物
VSA-001
siRNA
ApoC-III
脂蛋白脂肪酶缺乏症;重度高甘油三酯血症
临床Ⅲ期
VSA-003
siRNA
ANGPTL3
原发性高胆固醇血症;混合型血脂异常;纯合子型家族性高胆固醇血症
临床Ⅰ期
VSA-006
siRNA
HSD17B13
非酒精性脂肪性肝炎
临床Ⅱ期
海昶生物
HC-0201
ASO
AKT1
肾细胞癌;胰腺癌;原发性肾细胞癌
临床Ⅱ期
HC-0301
ASO
AKT1
肝癌;原发性肝癌
临床Ⅱ期
腾盛博药
VIR-2218
核酸偶联药物;siRNA
ASGPR
丁型肝炎病毒感染;肝炎;慢性乙肝;乙型肝炎病毒感染
临床Ⅱ期
恒瑞医药
hrs-5635
siRNA
-
乙肝
临床Ⅱ期
信达生物
SGB-3908
siRNA
AGT
原发性高血压;高血压
临床Ⅰ期
舶临医药
BW-00112
siRNA
-
混合型血脂异常;血脂异常;重度高甘油三酯血症
临床Ⅱ期
正大天晴
TQA-3038
核酸偶联药物;siRNA
ASGPR
慢性乙肝;乙型肝炎
临床Ⅱ期
中天生物+合一生技
SNS812
siRNA
SARS-CoV-2
SARS-CoV-2感染;2019冠状病毒病
临床Ⅱ期
圣因生物
SGB-3403
siRNA
PCSK9
杂合子型家族性高胆固醇血症;高脂血症;低密度脂蛋白胆固醇;高胆固醇血症;动脉粥样硬化性心血管疾病
临床Ⅰ期
星曜坤泽生物
HT-101
核酸偶联药物;siRNA
HBsAg
慢性乙肝
临床Ⅰ期
中美瑞康
RAG-17
核酸偶联药物;siRNA
SOD1
SOD1基因突变肌萎缩侧索硬化症;肌萎缩侧索硬化
临床Ⅰ期
艾码生物
ER-2001
siRNA
HTT
亨廷顿舞蹈症
临床Ⅰ期
靖因药业
SRSD-101
siRNA
PCSK9
原发性高胆固醇血症;高低密度脂蛋白胆固醇血症
临床Ⅰ期
炫景瑞医药+炫景生物
RG002C0106
核酸偶联药物;siRNA
ASGPR
补体介导的原发性肾小球疾病;补体介导的继发性肾小球疾病
临床Ⅰ期
必贝特医药
BEBT-507
siRNA
-
铁代谢紊乱
临床申请
浩博医药
AHB-137
ASO
HBV
慢性乙肝
临床Ⅱ期
视航生物
SHJ-002
ASO
miR-328
干眼症;角膜糜烂;近视
临床Ⅱ期
数据来源:药智数据
其中,或许主要是考虑到小核酸疗法的长效性特点对于慢病患者的致命吸引力,从进入临床阶段的具体管线中来看,高血脂高血压、乙肝、MASH等热门慢性疾病则是国内企业的一致突破点。
就高血脂领域而言,由于越来越多长效降脂靶点的发现,以及Leqvio在降血脂方面取得的商业化成功,让越来越多人看到了小核酸药物在高血脂适应症方面的巨大潜力,近年来全球针对高血脂的小核酸新药越来越多,在国内领域血脂代谢领域的布局管线也是最多的,主要玩家包括瑞博生物的RBD5044、维亚臻生物的VSA-001、天龙药业的YKYY-015、舶临医药的BW-00112、圣因生物的SGB-3403、靖因药业的SRSD-101等;
就高血压而言, 虽然目前治疗方案已经相当成熟,但受限于患者服药依从性差等问题,导致绝大部分的高血压患者的血压控制并不达标,而siRNA药物可直接作用于降低血管紧张素原(AGT)的表达,不仅安全性、有效性俱佳,更关键的是效果持久(一针管半年),国内重点管线有信达生物的SGB-3908、瑞博生物的RBD-9079、圣诺医药STP-136G等;
就乙肝而言,常规核苷类药物只能抑制乙肝病毒的复制从而缓解炎症,无法治愈乙肝,而且需要终身服药。而小核酸疗法理论上可以达到清除HBsAg达到乙肝的功能性治愈,因此小核酸用于乙肝治疗的研究成为目前该领域最前景的治疗方式,目前除海外AHB-137、bepirovirsen研究较靠前外,国内领域的布局企业还有恒瑞、舒泰神、腾盛博药、齐鲁、舶望、正大天晴、星曜坤泽等相关产品。
就MASH而言,由于MASH发病机制未明,全球药企从各种可能成药的方向进行探索,而以礼来、勃林格殷格翰为代表的MNC们正在试图以小核酸来入局,MNC们在MASH赛道布局小核酸技术的热情不断升温,但其实MASH小核酸疗法的最大竞争对手并非自身,而在于近年来异军突起的GLP-1药物,国内相关布局企业尚不多,维亚臻生物VSA-006算是比较具有代表性的产品。
很明显,小核酸疗法之所以在慢病领域爆发如此大的能量,从作用机理上强调“从源头解决慢性病”,而从市场层面则主要是解决了慢病药物依从性的问题。
尽管现阶段来看,小核酸药物在全球领域的适应症仍以罕见病、遗传病为主,但国内小核酸领域已经将目光看向了更远的慢病市场,这无疑是更具前瞻性的市场判断,而这种跳跃式的产业布局也或许能让中国企业在小核酸领域实现弯道超车也说不定。
各司其职
环节发力是产业链的未来趋势
当然,上述所讲的内容大多集中在技术端,但新药绝不仅仅只有技术,产业端的问题对于企业而言同样重要。
虽然小核酸药物在理论上可靶向传统药物分子无法成药的靶点,理论上具有研发周期短、治疗范围大等多种优势,但其实,目前国内小核酸企业总体仍表现为研发风险高、研发进度慢的整体局面,这主要是由于人才与资金所致。
当然,这样的情况并非小核酸领域独有,而是广泛存在于绝大多数创新疗法领域,但至少未来很长时间内,小核酸biotech企业在没有大额BD交易的情况下,仅依靠融资来推动研发、推动商业化,理论上不太可能。所以,在小核酸领域的项目交易注定更加频繁与活跃,如以达成外部合作的形式与齐鲁制药、信达生物、君实生物、华东医药绑定,或许也是一个不错的选择。
另外,由于小核酸产业作为复杂且精细的创新领域,从上游核酸单体和试剂生产到下游的产品商业化环节,对于绝大多数企业而言,都很难独立完成,寻求多方势力的合作,才是现阶段的主流。比如中游环节利用CRO企业高度的技术创新和精细的工艺控制,以确保药物的有效性和安全性,下游环节,利用CDMO的研发、生产外包实现成本的降低,加速药物研发进程。
而博腾股份小核酸技术平台,可提供多种小核苷酸及其衍生物CDMO服务,并进行一站式开发和生产,旨在解决其CMC研发存在亟须解决的诸多难点与痛点。
未来展望
小核酸药物的未来发展,在经历成药性与商业化的双重验证之后,其增长趋势几乎已可以肯定。并且这个势头还会随着未来资源的逐渐倾斜,而越发明显。
对于国内现阶段的小核酸市场,一方面在资本市场的推动之下,越来越多技术性公司正在加速入局,导致整个小核酸疗法的市场盘越来越大,也越来越受关注,这对于整个产业链都是好事。
而另一方面,更难能可贵的是,国内头部小核酸企业未像早些年一般对海外创新技术进行跟随式布局,反而有意避开了竞争力与市场空间不大的罕见病、遗传病领域,转而下注各种“慢病”,这样前瞻性的行为既保证了国内企业在海外市场的差异化,也强调了中国新药研究思想的根本转变。
未来,资本、创新biotech、大型药企与CXO企业的行业组合,在强调“各司其职”的核心理念下,也必将能更快速、更高效、更性价比地推动整个小核酸产业进步,最终反哺相关企业业务迅速增长。
综合来看,小核酸药物极有望成为继小分子药物和抗体药物之后的第三代颠覆性新疗法,我们拭目以待。
来源 | 博药(药智网获取授权转载)
撰稿 | 头孢
责任编辑 | 八角
声明:本文系药智网转载内容,图片、文字版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请在本平台留言,我们将在第一时间删除。
商务合作 | 王存星 19922864877(同微信)
阅读原文,是受欢迎的文章哦
上市批准抗体药物偶联物核酸药物siRNA信使RNA
2024-08-06
招募受试者
正大天晴药业集团股份有限公司正在全国开展一项“评价TQA3038注射液在慢性乙型肝炎患者中安全性、耐受性、药代动力学特征和抗病毒疗效的Ib/IIa期临床试验”。这项研究已得到国家药品监督管理总局的批准(批件号:2023LP02075)并通过中心伦理,现在全国招募受试者。
试验药物简介
TQA3038注射液是正大天晴自主研发的一种靶向乙型肝炎病毒(HBV)的小干扰RNA(siRNA)药物,注册分类为化药1类。
TQA3038作为GalNAc缀合的siRNA药物,可富集于肝脏,有效地降解靶向的RNA,抑制相关蛋白的翻译,从而阻断乙肝病毒的复制,有望在临床上显著提高患者的功能性治愈率。TQA3038采用具有自主知识产权的核酸序列,与目前临床进展最快的siRNA相比,具有更强的体外及体内抗病毒活性。
主要入选标准
(1)书面文件证明诊断为慢性乙型肝炎:血清HBsAg阳性且持续6个月以上;
(2)经治的慢乙肝:受试者必须在筛选前已接受口服核苷(酸)类药物治疗≥6个月且在筛选期前稳定治疗方案≥3个月;
(3)初治的慢乙肝:筛选时受试者从未接受过慢乙肝抗病毒治疗(口服核苷(酸)类药物及干扰素),或既往曾不规律抗病毒治疗,但入组前3个月未接受任何慢乙肝抗病毒治疗。
主要排除标准
(1)活动性病理性出血史者,或有出血倾向者;
(2)有过量饮酒史的受试者:过量饮酒史定义为:过去12个月每周饮用乙醇(酒精)男性>210g,女性>140g。乙醇摄入量(g) = 饮酒量( ml) × 酒精度数% × 0.8。或试验期间不能禁酒者;
(3)合并其它病毒如 HAV(由抗HAV-IgM证实)、HCV(由抗-HCV抗体证实,必要时加查 HCV-RNA)、HDV(由抗-HDV IgM证实)、HEV(由抗-HEV IgM证实)、HIV(由Anti-HIV证实)、梅毒(梅毒抗体阳性者,经研究者判断需治疗者)等感染;
(4)筛选前1年内有肝组织病理结果提示Metavir F3 或F4;腹部超声检查提示存在肝硬化;既往曾有肝功能失代偿期病史或筛选期有肝功能失代偿者,如腹水、肝性脑病、食管胃底静脉曲张出血等;
(5)除慢性HBV感染以外的其他慢性肝病史;
(6)筛选前或筛选时患者有肝细胞癌(HCC)的病史,或者可能有患肝细胞癌的风险;
(7)筛选前5年内有恶性肿瘤病史,除外特定经手术切除可完全治愈的肿瘤(如皮肤基底细胞癌等)。
研究中心信息
如果您符合以上条件或有意向参加该项研究,请扫描下方二维码报名。
正大天晴药业集团是集药品的科研、生产和销售为一体的创新型医药集团企业,员工14000多人,是国内抗肿瘤、肝病、呼吸领域的知名企业,位列中国医药工业百强榜第13位,为中国医药研发产品线最佳工业企业。
正大天晴始终将科技创新作为企业可持续发展的重要战略,为积极研制创新和高品质药品不懈努力,重点打造肿瘤、肝病、呼吸等产品集群。公司年研发投入占销售收入的17%,在研项目148个,其中创新药80个,先后承担国家重大专项课题33项,累计有效申请及专利3080项,拥有有效授权专利1137项,形成了“上市一代、储备一代、研发一代”的良性格局。
健康科技,温暖更多生命。为社会提供优质产品是我们不变的初心,正大天晴希望为患者提供更佳的健康解决方案,为提高公众健康水平与药品可及性不懈努力。
注:以上数据来自正大天晴内部报表,统计时间截至2023年底
siRNA临床结果临床申请
2024-07-05
·药时代
编者按:近几月Hepatitis B Foundation网站乙肝新药表单更新迟滞,为帮助大家更准确及时地获取全球乙肝新药最前沿信息,肝霖君查询各大药企官网更新的产品管线信息和相关网络资料中的乙肝新药报道做了系统整理,并汇总了慢乙肝新药与新药联合、新药与现有药物联合治疗的临床研究进展。
本期表单更新有:siRNA药物HRS-5635进入临床II期、TQA3038进入临床Ib/IIa期;停止FXR激动剂EYP001在慢乙肝领域的进一步开发。
新药联合治疗的探索明显加速,包括新药与新药联合、新药与现有药物的联合。许多新药单药在I期或II期研究中未达到主要疗效目标,企业便积极开始了不同联合治疗方案的探索。这也将是未来乙肝全面临床治愈的必要策略。
新药相关联合用药临床研究汇总
部分新药进展
HRS-5635
恒瑞医药的siRNA药物HRS-5635进入临床II期(CTR20241805),这是一项多中心、随机开放、平行设计研究,旨在评估不同剂量、给药间隔和疗程的HRS-5635注射液治疗NA经治获病毒学抑制慢乙肝患者的有效性和安全性。
TQA3038
正大天晴的siRNA药物TQA3038进入临床Ib/IIa期(CTR20241960),该随机双盲、平行分组研究旨在评价TQA3038注射液±NAs在初治/NA经治慢乙肝患者中的安全性、PK和抗病毒疗效,目前尚未招募。
EYP001
EYP001是Enyo Pharma开发的一款FXR激动剂,公司官网最新产品线布局已无该产品治疗慢乙肝的介绍,EYP001用于Alport综合征和NASH患者慢性肾病处于临床II期;根据ClinicalTrials.gov信息,在慢乙肝治疗领域除了已经完成的研究外,EYP001+NA治疗慢乙肝的IIa期研究终止,EYP001在慢乙肝领域的开发终止。
AB-729+NA+durvalumab
AB-729是Arbutus Biopharma和齐鲁制药共同开发的一款siRNA药物,目前处于临床II期阶段。2024年1月,Arbutus Biopharma在ClinicalTrials.gov新登记了一项开放标签、多中心IIa期研究(NCT06245291,AB-729-203),旨在评估病毒学抑制的慢乙肝患者接受AB-729+NA+durvalumab治疗48周的安全性、耐受性和药效学,其中PD-L1抑制剂durvalumab采用间歇性给药,目前该研究正在招募中。
Bepirovirsen+ETV±VE03702
Bepirovirsen是GSK和Ionis Pharma共同开发的反义RNA,目前处于临床III期阶段;VE03702是维申医药开发的一款TLR7和TLR8双激动剂,目前处于临床前阶段。Bepirovirsen+ETV±VE03702的联合治疗策略正处于临床前探索阶段。
封面图来源:pixabay
版权声明/免责声明
本文为授权转载文章。
本文仅作信息交流之目的,不提供任何商用、医用、投资用建议。
文中图片、视频、字体、音乐等素材或为药时代购买的授权正版作品,或来自微信公共图片库,或取自公司官网/网络,部分素材根据CC0协议使用,版权归拥有者,药时代尽力注明来源。
如有任何问题,请与我们联系。
衷心感谢!
药时代官方网站:www.drugtimes.cn
联系方式:
电话:13651980212
微信:27674131
邮箱:contact@drugtimes.cn
mRNA CAR-T二期临床试验成功,公司股价却暴跌35%!
吉利德:Trodelvy的一线生机
诺华浙江海盐生产基地启建!扩增放射配体疗法产能
点击这里,发现价值信息!
siRNA临床2期临床1期
100 项与 TQA-3038 相关的药物交易
登录后查看更多信息
研发状态
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 慢性乙型肝炎 | 临床2期 | 中国 | 2024-06-01 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
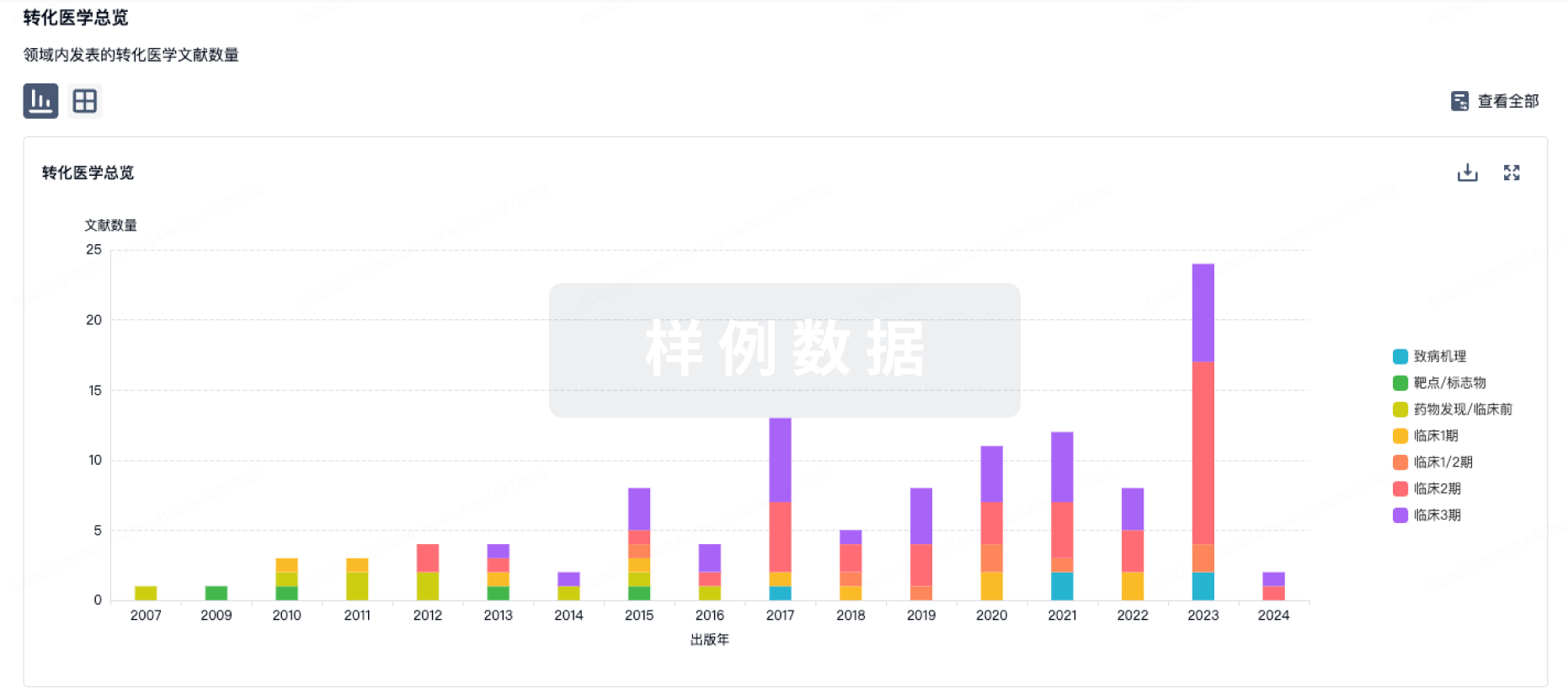
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
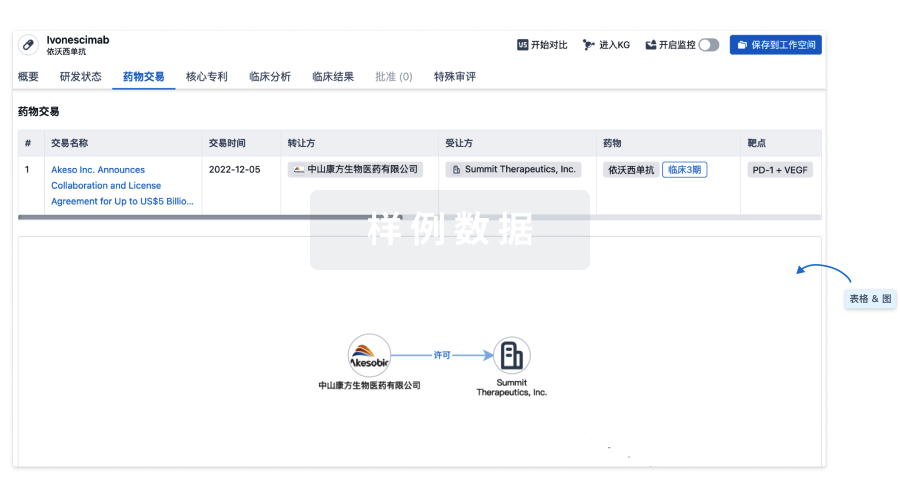
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
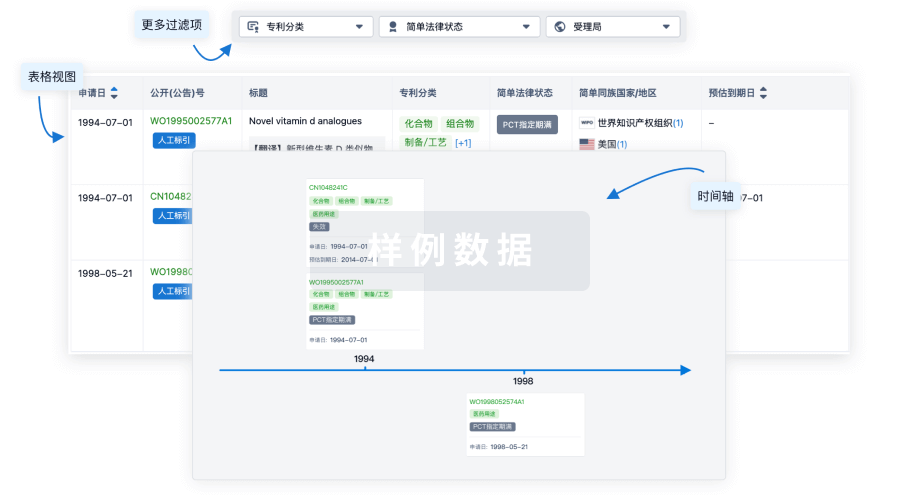
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
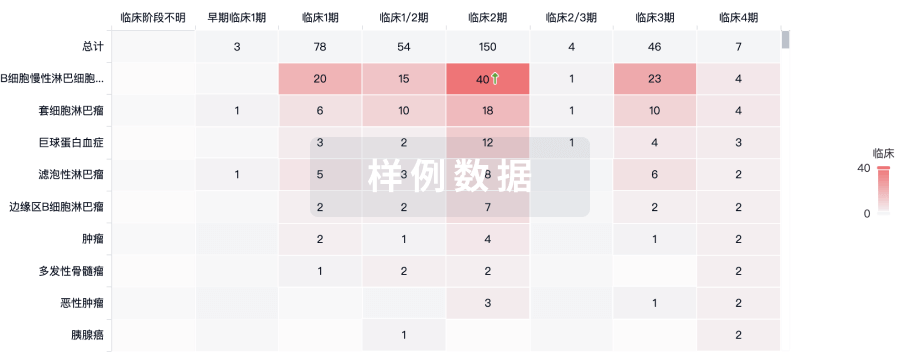
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
批准
利用最新的监管批准信息加速您的研究。
登录
或
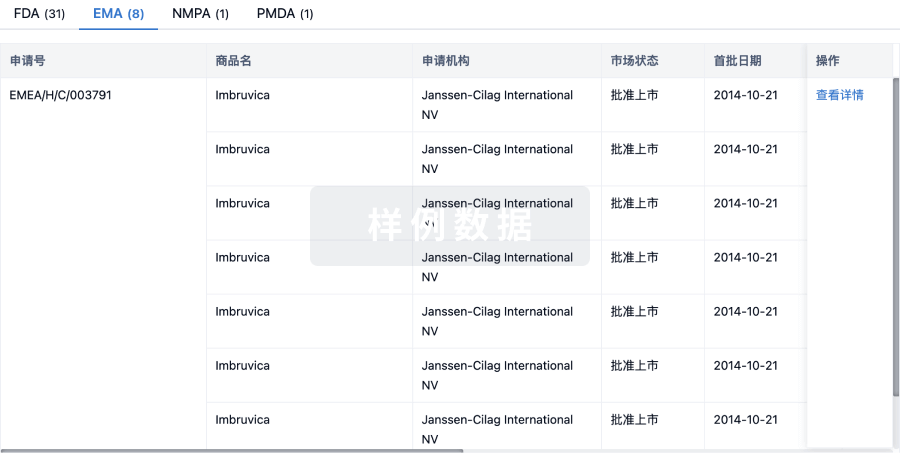
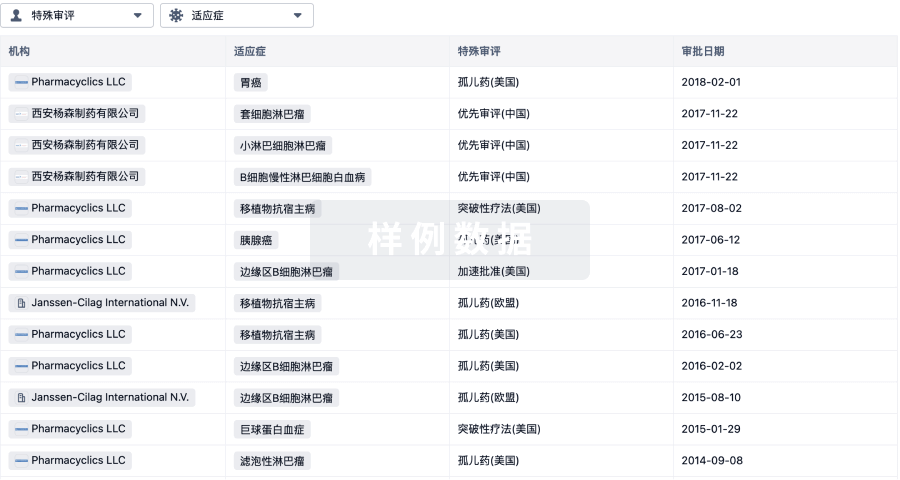
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用


