更新于:2024-09-19
Recombinant human growth hormone(BioGeneric Pharma SAE)
重组人生长激素(BioGeneric Pharma SAE)
更新于:2024-09-19
概要
基本信息
非在研机构- |
最高研发阶段批准上市 |
首次获批日期 (2013-01-01), |
最高研发阶段(中国)- |
特殊审评- |
登录后查看首次获批时间轴
序列信息
Sequence Code 26401985

当前序列信息引自: *****
关联
100 项与 重组人生长激素(BioGeneric Pharma SAE) 相关的临床结果
登录后查看更多信息
100 项与 重组人生长激素(BioGeneric Pharma SAE) 相关的转化医学
登录后查看更多信息
100 项与 重组人生长激素(BioGeneric Pharma SAE) 相关的专利(医药)
登录后查看更多信息
9
项与 重组人生长激素(BioGeneric Pharma SAE) 相关的新闻(医药)2024-07-15
·动脉网
生物制造被认为具有引领“第四次工业革命”的潜力。
目前,合成生物学已应用于医疗健康、食品消费、美妆护肤、化工、能源、材料、农业等众多细分领域,正在为市场带来不可估量的想象力。据经济合作组织预测,到2030年相关产业规模将达到全球工业生产总值的35%。
据动脉橙数据库不完全统计,2024年以来全球范围内合成生物学领域已完成24起投资,其中多起投资超过亿元。在今年上半年宣布完成融资的合成生物学企业中,动脉网注意到一家背靠传统药企、未有产品上市却接连斩获多轮亿元融资的君合盟生物制药(杭州)有限公司(以下简称:君合盟)。
君合盟成立于合成生物学还未成为热门赛道的2020年,基于创始核心团队平均20年的研发和大规模产业化经验搭建的重组蛋白药物开发平台,已成功布局聚焦医美与消费医疗并向严肃医疗拓展的5条核心管线,其中进展最快的重组人生长激素注射液已完成III期临床入组,在6月底君合盟举办的首次技术开放日,围绕技术难点、管线布局、产业化动向等问题,动脉网与君合盟董事长徐葵、CMC研发总监沈玉保博士、临床医学总监林丹花及特邀顾问、高级工程师顾其胜教授进行了对话。
君合盟杭州总部
20年产品开发和大规模产业化经验,君合盟打造全长氨基酸序列与三螺旋结构的重组I/III型人胶原蛋白
研发日当天,君合盟宣布已成功突破重组人胶原蛋白的规模化发酵与纯化技术,实现二十吨发酵体系下的稳定表达,并顺利完成相关产品的工业化生产工艺的开发。新闻稿显示,这标志着行业由动物源胶原向重组人胶原替代转型的过程中迈出了重要一步,更预示着产业正加速迈入使用重组人胶原蛋白材料的新时代。
从胶原蛋白的研发历程来看,胶原蛋白已经历过以动物源胶原蛋白提取产品为主的早期应用阶段,正在实现从基于结构生物学、基因工程学和蛋白质工程学开发重组胶原蛋白技术的快速发展阶段向开发重组胶原蛋白更多应用场景的商业化探索阶段的跨越。
君合盟董事长徐葵
对于君合盟而言,这种跨越也体现在产品的布局上。“秉持着‘让患者受益’的研发思路,君合盟没有仅局限在消费医疗领域,而是同时兼顾严肃医疗布局。”君合盟董事长徐葵说。以君合盟在胶原蛋白产品的布局为例,目前君合盟在研两种类型的胶原蛋白,分别为重组I型人胶原蛋白及重组III型人胶原蛋白。“这两种类型的胶原蛋白不仅能够满足皮肤填充、祛皱护肤等消费医疗领域的需求,还能够在严肃医疗领域,如再生医学的人工血管、支架材料等方面,发挥重要作用。”君合盟特邀顾问、高级工程师顾其胜教授指出。
君合盟特邀顾问、高级工程师顾其胜教授
据介绍,君合盟重组I型人胶原蛋白及重组Ⅲ型人胶原蛋白与天然I/Ⅲ型人胶原蛋白结构高度一致,同时实现了全长氨基酸序列与三螺旋结构,生物学活性完整,稳定性强。目前,其重组Ⅲ型人胶原蛋白已申报II类医疗器械,Ⅲ类医疗器械的临床前研究正在进行中。
核心团队平均20多年的研发和大规模产业化经验是产品开发的基础。君合盟CMC研发总监沈玉保博士曾担任国家一类创新药“重组VLP蛋白质疫苗”的研发总负责人,主持并实施多个基因工程药物、生化药物、长效表达与制备平台的构建,同时主持PEG化长效蛋白质药物的研究与开发;临床医学总监林丹花则主导完成过超10款创新药全生命周期的临床开发,覆盖内分泌CNS、心血管、肿瘤等多个疾病领域、具有近20年生物医药行业临床、项目管理和监管政策研究的经验。
而君合盟的董事长徐葵曾领导建设过亚太地区共享服务中心及跨境业务、累计实现营业收入超百亿元人民币,拥有十余年的跨国企业管理经验。这成为君合盟产品最终走通商业化的有力支撑之一。
突破制备瓶颈,四大技术平台兼顾创新性+成药性
目前,市场上主流的胶原蛋白制备方法主要有动物源提取和基因工程法两种。动物源提取产品尽管能够保持完整的三螺旋结构和生物学特性,但其疾病感染风险、免疫排异风险、产能限制及纯度控制的难题,制约着更广泛的应用;基因工程法虽然能够规避部分难题,但技术成熟度、生物活性问题及成本仍需要一定时间来攻克。
提取和纯化是胶原蛋白产品开发的核心,如何在不损害胶原蛋白原有性质的前提下,高效去除杂质、提升纯度,成为每一个产业化团队必须考虑的问题。“在胶原蛋白产品的开发中,我们模拟天然胶原蛋白人体内的产生过程,设计技术路线,制备在序列长度、组成、高级结构等方面与天然人胶原蛋白相一致的重组人胶原蛋白。”沈玉保博士说。
君合盟CMC研发总监沈玉保博士
基于此,君合盟打造了兼具创新性和成药性的重组蛋白药物核心技术及产品开发平台,包括四个部分:原核Fc融合蛋白缓释平台、蛋白质高效表达平台、蛋白质分离纯化平台和蛋白质体外复制&自组装平台。应用平台技术,君合盟成功解决了动物源胶原蛋白的免疫原性,及重组人源化胶原蛋白功能性片段不能行使三螺旋的全部生物学功能问题,并成功突破制备技术及规模的产业化难题。
同时,借助平台技术,在确保提取效率和纯度的同时,君合盟还大幅降低了生产成本并突破了非天然Fc融合蛋白体外折叠的限制,是目前在研较少与天然人胶原蛋白结构组成、序列长度及生物学功能相一致的重组人胶原蛋白产品。
围绕目前开发的重组人胶原蛋白产品,君合盟也正在探索新的适应症范围。“这种探索主要分为两个方面,一是新型功能材料,包括人工皮肤、人工血管和人工角膜等;二是新型仿生材料,依靠材料本身的天然特性,结合人体细胞或组织的自然构成制备新型环境友好材料。也就是说,我们希望在胶原蛋白原料开发的基础上,实现更仿生、更智能、更友好的终端产品开发,实现技术创新、材料创新、产品创新和应用领域的拓展。”沈玉保博士说。
“另一个方面来说,医美领域新型复合材料的不断出现和应用,去满足日益增长的临床需求已经成为了医美市场的一种趋势。”顾其胜教授说。
从这个角度而言,君合盟更具有其独特的优势。目前君合盟产品的布局,除胶原蛋白之外,还有重组A型肉毒毒素和重组人生长激素。
重组A型肉毒毒素已达商业化规模,重组人生长激素已进入临床Ⅲ期
君合盟生产车间
据介绍,目前,君合盟在通化与杭州两地均布局生产车间。其中,位于通化的重组A型肉毒毒素生产线于2023年7月开始生产,最大年产量可达400万支。
君合盟的JHM03重组A型肉毒毒素采用基因工程大肠杆菌发酵,利用合成生物学和重组蛋白高表达技术,打造出由150 kDa单一分子构成的重组A型肉毒毒素,有效解决了传统肉毒毒素生产菌株肉毒杆菌的生物安全问题,同时生产工艺步骤大幅缩减,流程时间大幅缩短,具备纯度高、免疫风险低、安全性好、生产成本低、批次间一致性稳定等多重优势。目前,采用5L的发酵罐生产,已可以充分满足商业化规模的需求。
君合盟临床医学总监林丹花
据临床医学总监林丹花介绍,目前重组A型肉毒毒素已于四月底完成以成人中重度眉间纹为适应症的I期临床试验,正在进行Ⅱ期临床试验随访,是全球第二家进入临床阶段的重组A型肉毒毒素。而在适应症方面,除了眉间纹之外,君合盟已申请成人脑卒中后的上肢痉挛适应症,进一步扩展重组A型肉毒毒素在严肃医疗领域的应用,预计今年9月份获得临床试验许可,随后进入临床试验。
生长激素是君合盟目前进展最快的管线。在这方面,君合盟共打造了两款产品——JHM01重组人生长激素注射液与JHM02重组长效生长激素,均由位于杭州的生长激素生产线生产。
JHM01适应症为儿童生成激素分泌不足所致的生长障碍,目前已进入Ⅲ期临床试验。Ⅰ期临床试验结果显示,JHM01 PK、PD特性与诺泽®生物等效。在Ⅲ期临床试验中,君合盟共招募180例患者,通过每日一次给药进行随机开放阳性药对照试验,目前已经完成患者入组。利用君合盟特有的技术路线进行生产,有望解决现有产品患者费用负担重、渗透率和治疗率低的困境,并实现国产替代。
JHM02采用大肠杆菌来表达Fc融合蛋白,具有相对CHO细胞表达显著降低的制备成本。在分子设计方面,君合盟通过对人体内GH-GHR作用机制的充分研究,自主开发了具有完全自主知识产权的分子结构。临床前动物试验结果显示,JHM02有望实现双周给药,相较现在已上市长效生长激素每周给药一次,可以更好改善患者的依从性。
访谈的最后,君合盟董事长徐葵透露,在生物医药行业的出海趋势下,目前君合盟在研管线均有国际化计划,正在进行技术交流和BD商业化合作的洽谈。“在管线布局和推动中,我们始终坚持患者需求导向、市场驱动研发的思路,并保持开放、积极的态度不断‘向前一步’。”
不久前,君合盟完成了由通化东宝投资的1亿元的B1轮融资,新闻稿显示,未来将借助通化东宝在临床、商业化方面的优势和资源,积极推进公司核心管线的研发进程,结合市场需求不断丰富、迭代创新重组蛋白产品管线,早日造福广大患者与用户。
在生物制造的政策东风下,我们期待君合盟生物迈向新高度。
近
期
推
荐
声明:动脉网所刊载内容之知识产权为动脉网及相关权利人专属所有或持有。未经许可,禁止进行转载、摘编、复制及建立镜像等任何使用。
动脉网,未来医疗服务平台
生物类似药临床3期
2024-03-29
选对技术,需要战略性眼光;斩难关,需要屡败屡战的坚韧;让价值无可替代,需要扎实的积累。什么样的企业能在艰难期打造有临床价值的创新产品?首支PEG长效生长激素的故事,就是一种答案。20年前,当看到公司用自己差不多一年半的工资,从国外堪堪买回5g的聚乙二醇(PEG),以作为研发长效生长激素的原材料时,金赛药业原核工艺部负责人王俊才不免感叹:太金贵了!但没办法,当时国内没有一家公司有能力生产PEG,唯一的途径是从国外极少的生产商处购买。王俊才至今也忘不了:“1gPEG的价格约为3200元,我那时1个月工资才1000多块钱。每次做实验,都十分谨慎,称量都是毫克计。”拿着这昂贵又稀缺的原材料,金赛要做鲜少企业愿意做、能做成的事——自研出全球第一支PEG化长效重组人生长激素。这注定是条艰险、孤独的道路。2002年专利阻击战,2004年临床I期,2006年陆续进入临床II、III期,2009年起长达4、5年艰难的审评及GMP核查过程……12年曲折岁月,嵌进整个研发团队一生。终在2014年,金赛上市了全球首创长效生长激素产品金赛增,用于内源性生长激素缺乏所引起的儿童生长缓慢(GHD),结束了60年来生长激素需每天注射一次的历史,开启了生长激素周治疗时代。“12年磨一剑”,这是最好的注解。近10年,纵使有不少药企纷纷参与到研发中来,金赛增所在的市场仍无任何竞品上市。2024年,国产长效生长激素研发竞争态势变得相当激烈,但仍唯独金赛增,具备长时间的安全性临床研究,拥有10年注册临床、10年真实世界数据以及超10万例中国患儿临床应用的独家优势。作为生长激素的赛道引领者,金赛接下来要做的,仍如20年前一样:创造趋势。基于未被满足的临床需求,不断拓宽产品应用的边界,这也确保了金赛增的价值不可替代、可长期持续。01选择PEG技术后的12年从2002年递交PEG化学修饰技术的专利申请,到2014年金赛增上市,共12年。金赛能跑赢全球大药企,造出全球首创长效生长激素产品,离不开这曲折的12年,更离不开PEG这一技术底层逻辑。金赛药业成立之初的金磊金赛创始人金磊,20年前决定战略性研发长效生长激素时,具备了两大前提优势。一是,长效生长激素已在国际上有了理论基础,而金磊用数年时间“吃透”了生长激素研究,其扎实的基本功基础和经验助其成为了开拓者;二是千禧年后PEG开始逐渐成为蛋白质长效化主流技术,FDA已验证其技术可行性。但在当时的国内,选择PEG来研发长效生长激素,仍是一场巨大的冒险。全球上市的PEG修饰药物当时能用一只手数过来,且基本都是在2010年后才陆续上市,在此之前算是空白。“当时,国内还没有人进行PEG化药物修饰技术研究,我们是第一家。同时我们还是国际上第一家试做生物大分子长效制剂的企业。”王俊才回忆道。这意味着,PEG这一原材料是稀缺的,只能依赖进口,价格高昂,且对PEG标准要求很高,必须保证其均匀性和纯度。尽管起初金赛一次性通过了技术审评,顺利进入到临床试验研究阶段,但这条路还没有成功的应用先例。能否保持较长的浓度,保留生物学活性,以及确保长期使用的安全性,是待解决的研发难点。可以说,这条路走对了是殿堂,走错了,便是深渊。但金磊及研发团队仍坚定选择了这一路径,原因不止是掌握的技术优势,更是需求使然。短效产品的局限性就摆在那里:儿童需每日注射,但频繁注射会造成心理压力,漏针现象严重,依从性欠佳,治疗效果有的大打折扣。而如果“从众”选择缓释微球作为主流的长效技术,由于技术限制,注射的针头很粗,易让患者非常疼痛,有效性和安全性也都缺乏。曾有海外明星公司沿该技术推出了长效生长激素,但上市没几年便退出市场,且其工艺极其复杂。而PEG长效生长激素的核心原理是什么?简单来说,通过天然肽键键合方式,将天然结构的生长激素和惰性PEG相连,如同为生长激素加了一层“金钟罩”,大大降低了被肾脏过滤的速度,同时减少蛋白酶降解作用,可更长时间发挥药效。每周注射一次,能达到每天注射治疗的效果。2004年开始,金赛陆续启动了I到III期的临床试验。在此之前,金赛遇到了首个棘手的问题——专利。与知名MNC间关于PEG化生长激素的专利抗衡,倏然而至。要想“以小胜大”,必须抢占时间,非常懂行,兼具勇气。仔细研究专利法后,金赛最终提供了确切的原始研发资料,证实了在该领域研发时间最早、技术更领先、更具有开创性,打赢了专利战。但几年后,自2009年迎来首次专家上会会审起,真正漫长而艰难的质控及审评一关,又悄然开始。“药监局出台了新的政策,增加新药上会评审和生产现场核查。药审中心组织了药学、非临床研究、临床及统计学的专家,对药品的安全性,有效性和质量可控性进行再评价。”王俊才向E药经理人分享道。面对这款全球首创产品,审评又格外严格谨慎。金赛按要求数次提交了补充材料,期间,“我们完善了质量可控性和产品一致性,以及完善了相关蛋白的分析方法、PEG残留质控方法、PEG修饰度检测方法……很多方法都得突破常规思维,带有很大的挑战性。”王俊才感慨道。让他印象最深的时间段,是在最后一次补充资料研究期间。那时正值春节,金磊带着整个项目组不舍昼夜地做实验、整理材料,最终终于通过了技术审评和生产现场核查,完成了国内首个PEG修饰药物的分析方法和标准建立。金赛药业“重组人生长激素系列产品研制与产业化”项目获得国家科技进步二等奖10年的“煎熬”及屡败屡战,王俊才记忆犹新,每一位研发技术人员也都毕生难忘。60年来,全球生长激素产品需每天注射一次,这对于儿童及背后家庭来说都是种痛苦。而PEG无毒,具有良好的水溶性,可增大生长激素分子量的作用,使肾脏代谢速度变慢,更长时间发挥药效。难得的技术突破,为金赛增提供了莫大的科学及社会价值。02用真实世界数据说话克服了专利、研发及审评难题后,首款长效生长激素还要面临从零开始打开市场的问题。当时,在医生和患者的认知里,有关长效生长激素的知识几乎是一片空白。上市初期,对于此类一周注射一次的产品,不少医生对此抱有怀疑,甚至不认为中国具备推出全球“首个且唯一一个”创新产品的能力,患者及家庭了解的匮乏更不必多说。而让市场了解、熟悉和信任的最好方式,是用充分、扎实的临床数据证明长期应用的疗效与安全性。一款药品必须经过至少5年上市后临床验证,才能充分证明安全性,很多药品虽获批上市,但在真实世界应用中因出现严重不良反应而退市。此外,对在中国首次申请上市的药品医疗器械,注册申请人应提供是否存在人种差异的临床试验数据。所以自2014年产品上市起,金赛没有急着去追求商业化成绩,而以大的研发投入和精力放在了IV期真实世界临床及其他适应证的拓展上。经过10年的积累,至今,金赛增是国内唯一拥有长达3年及以上安全性临床研究的长效生长激素,也是全球唯一在真实世界中超过10万例临床应用的长效生长激素。试验样本量最为庞大,在全国多地80余家医院展开。且研究人种是中国患儿,唯一具备中国人群长时间的用药经验,另在不良反应和抗体两大指标表现上,也可谓同行最优。长时间的临床也有力证明了,一方面,PEG技术的确能规避其他主流长效制剂技术一定的缺陷。以蛋白质融合技术为例,多项试验发现,这项技术存在免疫原性、纯化困难等诸多安全隐患,需长期监测尚未发现的细胞毒性等副作用。另一方面,金赛增的分子量和PEG结构(40 kda ,U型)相较于同类型产品表现更好,且是迄今唯一经长时间临床验证具有良好安全性的经典PEG化技术应用,既可保证生长激素的稳定性和安全性,也可保证制备过程中产物的高度均一性。据悉,金赛增的半衰期长达32小时,U形PEG形成的空间位阻又可以使药物免疫原性变得极低。一项关键III期临床数据显示,金赛增的年化生长速率可达13.41cm/y,较短效明显改善,也优于已公布的其他长效生长激素研究结果。2023年,国际著名期刊Journal of Clinical Endocrinology& Metabolism发表了金赛增治疗生长激素缺乏症儿童最大样本量、多中心、前瞻性、长达3年随访的真实世界研究数据,研究旨在评估在真实世界中使用该产品的长期有效性、安全性以及剂量对患者结局的影响。结果显示,身高标准差、年生长速率、安全性等关键指标表现均为积极,0.2mg/kg/w组获益尤其突出。10年注册临床和10年真实世界数据积打下的“基本盘”,让金赛增获得了业内的权威认可,为其打造了差异化的长期竞争优势,其临床突破也可谓是全球重组生长激素研发领域的重大进步。03未来如何赢?知来路,明未来。金赛药业的成立与成长,始终伴随着创始人及研发团队对初心的坚守。很多年前,金磊回国探亲时,他在教育部组织的社会实践考察中走访了一些贫困地区,看到许多十几岁的儿童身高还不足1米,其上学、就业、心理状态被严重影响。然而,很多人从未听过生长激素,即使知道有矮小治疗产品,由于被进口垄断,也无力承担高昂的治疗费用。医生端也是极其匮乏,在那个年代国内有能力治疗矮小疾病的医生,还不到20个人。强大的需求,让金磊毅然回国创立了金赛药业,先让国人有了自己的生长激素,再是推动了生长激素从短效粉针、水针再到长效水针的迭代升级。首款国产生长激素(赛增)问世截至目前,我国现存4-15 岁需治疗的矮小症人口仍超700万,但接受规范生长激素治疗的人群比例低于5%,渗透率仍处于较低水平,具有更高依从性的长效水针,依然具备很大的拓展空间。临床需求是一家低调做研发、求突破的药企最大的动力,几年前开始,金赛药业关于超长效水针生长激素的研发工作便已如火如荼地进行。另在几大极具市场规模的重磅适应证拓展上,金赛增已先于全球同类型产品取得了领先的研发成果。生长激素主要适应证有生长激素缺乏症(GHD),特发性矮身材(ISS),先天性卵巢发育不全综合征(Turner综合征),小于胎龄儿(SGA),以及PraderWilli综合征。截至目前,金赛增治疗ISS、Turner综合征所致儿童生长障碍等适应证已进入上市评审阶段,2024年有望获批上市,另外小于胎龄儿适应证也已完成II期临床。可以看到,未来覆盖更多重磅适应证的金赛增,其市场渗透率将进一步提高,继续占领强大的市场份额。其中,ISS尤其有望带来可观的市场空间。ISS是由多种尚无可认知病因引起,约占所有身材矮小儿童的60%-80%。临床研究表明,经过52周的治疗,ISS患者对金赛增的治疗耐受性良好,糖脂代谢指标均正常,且保持稳定。其中0.2 mg/kg/w的高剂量组金赛增治疗后HV(生长速率)增长5.88cm/y,达到10.04cm/y,充分地验证了产品的安全性与疗效。另值得注意的是,金赛增,以及金赛研发的所有生长激素产品,在出海国际化上蕴含了很大的市场机遇。国内的生长激素产品有较强的海外价格竞争力和毛利率表现,其中,金赛药业很早布局海外市场,金赛增有望直接进入美国III期临床,并有望在几年内上市,这将成为其新的重磅增长空间,持续扩充想象边界。且正如金磊所盼,通过在生长激素领域的迭代升级,横向扩展和纵深,以及在生产工艺上的不断优化,一切都会有效带领行业站在新的起点,迈入新的发展阶段,于整个行业的进步来说意义非凡。2024年,中国医药创新也迎来了一个里程碑式的转折和开端。复盘金赛增20年的成长历程,同样有利于在这一关键时间节点,回答“什么样的企业能做出有价值的创新产品”这一问题。精彩推荐CM10 | 集采 | 国谈 | 医保动态 | 药审 | 人才 | 薪资 | 榜单 | CAR-T | PD-1 | mRNA | 单抗 | 商业化 | 国际化 | 猎药人系列专题 | 出海启思会 | 声音·责任 | 创百汇 | E药经理人理事会 | 微解药直播 | 大国新药 | 营销硬观点 | 投资人去哪儿 | 分析师看赛道 | 药事每周谈 | 医药界·E药经理人 | 中国医药手册创新100强榜单 | 恒瑞 | 中国生物制药 | 百济 | 石药 | 信达 | 君实 | 复宏汉霖 |翰森 | 康方生物 | 上海医药 | 和黄医药 | 东阳光药 | 荣昌 | 亚盛医药 | 齐鲁制药 | 康宁杰瑞 | 贝达药业 | 微芯生物 | 复星医药 |再鼎医药|亚虹医药跨国药企50强榜单 | 辉瑞 | 艾伯维 | 诺华 | 强生 | 罗氏 | BMS | 默克 | 赛诺菲 | AZ | GSK | 武田 | 吉利德科学 | 礼来 | 安进 | 诺和诺德 | 拜耳 | 莫德纳 | BI | 晖致 | 再生元
2024-01-30
Part 1全球药物批准/研发动态01全球新药批准情况本周全球(不含中国)新药批准共计2个,其中:NDA批准1个,新适应症批准1个。02全球新药申报进展本周全球(不含中国)新药申报共计4个,其中:NDA申报进展1个,BLA申报进展2个。本周全球(不含中国)新药申报进展中,监管机构特殊资格认定药物共计9个,其中:化学药2个,生物药6个,细胞疗法1个。03全球新药研发进展本周全球(不含中国)新药临床研发状态更新共计25条,涉及肿瘤,血液和淋巴系统疾病,病理状态、体征和症状,遗传和代谢病,呼吸系统疾病,皮肤病,消化系统疾病以及泌尿和生殖系统疾病共计8个领域。全球新药研发进展详情(部分)04全球医药交易事件本周全球(含中国)医药交易时间共计25起,涉及药物权益转让、公司并购等多起交易事件。全球医药交易时间汇总表(部分)Part 2国内药物批准/研发动态01国内新药批准情况本周国内新药批准共计2个,其中:NDA批准1个,新剂型批准1个。02国内新药临床默示许可进展本周获CDE临床默示许可的国内新药共计45个,涉及74个受理号。其中化学药22个,治疗用生物制品23个。本周国内新药临床默示许可进展(部分)03国内新药申报进展本周共有8个新药向CDE提交上市申请,其中化学药4个,治疗用生物制品3个,预防用生物制品1个。本周共有45个新药向CDE提交临床申请,涉及65个受理号。其中化学药19个,治疗用生物制品23个,预防用生物制品3个。国内新药临床申报情况(部分)本周国内新药申报进展中,NMPA特殊资格认定药物共计1个,为生物药。04国内新药研发进展本周国内新药临床研发状态更新共计6条,涉及肿瘤,皮肤病,血液和淋巴系统疾病以及感染共计4个领域。其中化学药1个,生物药4个,疫苗1个。05国内新药研发领域政策法规动态国家药监局药审中心关于发布《放射性治疗药物非临床研究技术指导原则》的通告(2024年第9号)为规范和指导放射性治疗药物的非临床研究与评价,在国家药品监督管理局的部署下,药审中心组织制定了《放射性治疗药物非临床研究技术指导原则》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管〔2020〕9号)要求,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。06国内新药研发领域热点新闻长效生长激素迎来新入局者,百亿市场格局生变近日,特宝生物的长效人生长激素——怡培生长激素(商品名:益佩生),上市申请获受理,用于治疗内源性生长激素分泌不足所致的儿童生长障碍。受此消息影响,特宝生物股价大涨。此次怡培生长激素的获批,意味着在长效生长激素领域迎来了新的搅局者。目前该领域格局如何?未来将如何演变?长效生长激素市场,国内金赛药业一家独大生长激素缺乏症(GHD)是一种严重的罕见病,以身材矮小和代谢并发症为特征。在GHD患者中,由于垂体不能产生足够的生长激素,不仅影响到儿童身高,而且对儿童的整体内分泌健康和发育也至关重要。目前补充生长激素是公认的对儿童GHD最有效的治疗方式之一。生长激素(Human Growth
Hormone)即由人体脑垂体前叶分泌的一种肽类激素,它由191个氨基酸组成,能促进骨骼、内脏和全身生长,并促进蛋白质合成,影响脂肪和矿物质代谢,在人体生长发育中起着关键性作用。一般情况下,生长激素是通过基因重组大肠杆菌分泌型表达技术生产的,在氨基酸含量、序列和蛋白质结构上与人生长激素完全一致。目前已上市的生长激素主要有三大类别,分别是:每天注射一次的重组人生长激素注射用冻干粉针剂(即短效粉针)和重组人生长激素注射液(短效水针),以及每周注射一次的聚乙二醇重组人生长激素注射液(长效水针)。最早上市的短效粉针,由于冻干可影响肽链的空间结构,且需要患者自行溶解,易污染、操作复杂等,已逐渐被短效水针取代。随着技术迭代,长效剂型横空出世。该剂型注射频率为一周一次,与短效剂型每天注射一次相比,大大提高了患者对生长激素疗法的接受度、耐受性等。因此,生长激素市场的竞争,已聚焦在长效剂型。目前长效生长激素领域,国内只有长春高新子公司金赛药业的聚乙二醇(PEG)重组人生长激素注射液(商品名:金赛增)获批上市。金赛增是全球第一支PEG化长效生长激素制剂,于2014年在国内获批上市,适应症为内源性生长激素缺乏所引起的儿童生长缓慢,以及特发性身材矮小、先天性卵巢发育不全综合征(Turner综合征)所致的儿童生长障碍。金赛增的上市,标志着国内生长激素周治疗时代正式开启。同时也让金赛药业成为了国内唯一拥有完整的粉针剂、水针剂、长效水针剂全产品线的生长激素厂商。十年来,金赛药业在国内长效生长激素领域一直一家独大,2022年,金赛增公立医疗机构销售额约为4.89亿元,同比增长33.71%。特宝生物入局,百亿生长激素市场格局生变据Frost &
Sullivan数据显示,2018-2030年,全球儿童生长激素缺乏症的治疗市场规模按照年复合增长率6.4%递增,预计到2030年,这一市场规模将达到60亿美元。在国内,根据中华医学会的数据,因生长激素缺乏症而真正接受治疗的患儿不足3万名,药物治疗渗透率不到1%。相比于欧美发达国家10%以上的渗透率,国内生长激素市场存在巨大的提高空间。据Frost &
Sullivan数据显示,到2030年国内相关市场规模将增长至48亿美元。此次特宝生物的怡培生长激素上市申请获受理,将结束金赛药业在国内长效生长激素领域一家独大的局面。据悉,怡培生长激素采用40kD Y型分支聚乙二醇(YPEG)分子对人生长激素(rhGH)进行单分子修饰,优选高生物学活性、非N-末端位点为主的修饰组分,在保证疗效的同时,旨在降低给药剂量,获得更佳的长期药物安全性。II/III期研究(n=43)结果显示,GHD患者接受12周的治疗后,怡培生长激素100、120、140μg/kg/周组和重组人生长激素35μg/kg/天组(对照组)的身高增长速度分别为7.07、10.39、12.27和11.58厘米/年。可见在独占市场十年后,金赛增将直面一个强力的竞争对手,国内超百亿生长激素市场格局将发生变化。分食长效生长激素市场,国内药企蓄势待发当前全球共有4款长效生长激素获批上市。除了金赛药业的金赛增外,其余均为海外药企产品,分别是诺和诺德的Sogroya、Ascendis的Skytrofa和辉瑞的Ngenla。诺和诺德的Sogroya于2020年9月获FDA批准上市,用于治疗成人生长激素缺乏症(AGHD),是FDA批准的首款成人长效人生长激素,其通过将天然的人生长激素经过修饰与血浆蛋白白蛋白结合延长半衰期,达到每周注射1次的频率。2023年4月,Sogroya获FDA批准扩大适应症,用于治疗2.5岁及以上儿童的生长激素缺乏症。丹麦药企Ascendis的Skytrofa于2021年8月获FDA批准,用于治疗1岁及以上儿童的生长激素缺乏症。辉瑞的Ngenla于2023年6月获FDA批准,用于治疗3岁以上内源性生长激素分泌不足导致生长缓慢的儿童患者。目前,诺和诺德的Sogroya和Ascendis的Skytrofa已在国内进入III期临床试验阶段。本土一众药企也在试图抢食长效生长激素这块大蛋糕,不过由于长效化技术存在一定壁垒,国内竞争者较为有限,进入III期临床及以上阶段的有安科生物和天境生物等。安科生物的PEG化重组人生长激素注射液于2019年就已完成临床试验,不过一直处于报产前准备阶段。天境生物/济川药业的伊坦长效生长激素(TJ101)则通过Fc片段融合蛋白的方式,延长了半衰期,具有半个月注射1次的可能;同时,其分子改造没有引入外源物质,最大程度上避免了肾毒性等问题。目前,TJ101
III期临床已经成功,潜在价值释放在即。在商业化方面,TJ101由儿科领域拥有显著渠道优势的济川药业负责。Ascendis的Skytrofa(隆培促生长素)的大中华区权益由国内维昇药业获得,隆培促生长素是一种新型的未经修饰的长效生长激素剂型,其制备过程为将生长激素暂时连接到长效载体形成前药,在一定时间内在体内释放。维昇药业曾宣布该产品在中国的III期临床试验达到了主要终点——治疗52周后,患者的年化生长速率为10.66厘米/年,与每天注射的短效生长激素相比达成非劣效性。维昇药业计划在完成所有准备工作后,向中国药监局递交上市许可申请。由上可以看出,目前市场上主流的长效生长激素产品主要使用PEG或是蛋白作为缓释载体。未来长效剂型的上市进度,是各相关企业在生长激素领域抢跑的关键。此外在患者的依从性上虽然长效生长激素相比水针和粉针有明显优势,但是长效剂型价格相对较高,患者年用药金额高达15万元左右,水针价格仅是其三分之一左右,较高的价格为长效剂型的推广带来一定难度。从制剂的注射频率来看依旧是周制剂,尚无月制剂、两周制剂的突破。因此,未来如何降低成本、延长注射间隔时间,成为后来者突围的方向。咨询、合作请联系作者小D有话说为方便读者阅读及保存,我们将周报原文整理成了PDF版本,如需获取全文,可点击最上方蓝字,在药渡Daily公众号后台回复“0130周报”,即可下载。
放射疗法疫苗并购临床申请细胞疗法
100 项与 重组人生长激素(BioGeneric Pharma SAE) 相关的药物交易
登录后查看更多信息
外链
| KEGG | Wiki | ATC | Drug Bank |
|---|---|---|---|
| - | - | - |
研发状态
10 条最早获批的记录, 后查看更多信息
登录
| 适应症 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|
| 生长激素缺乏症 | - | 2013-01-01 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
No Data | |||||||
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
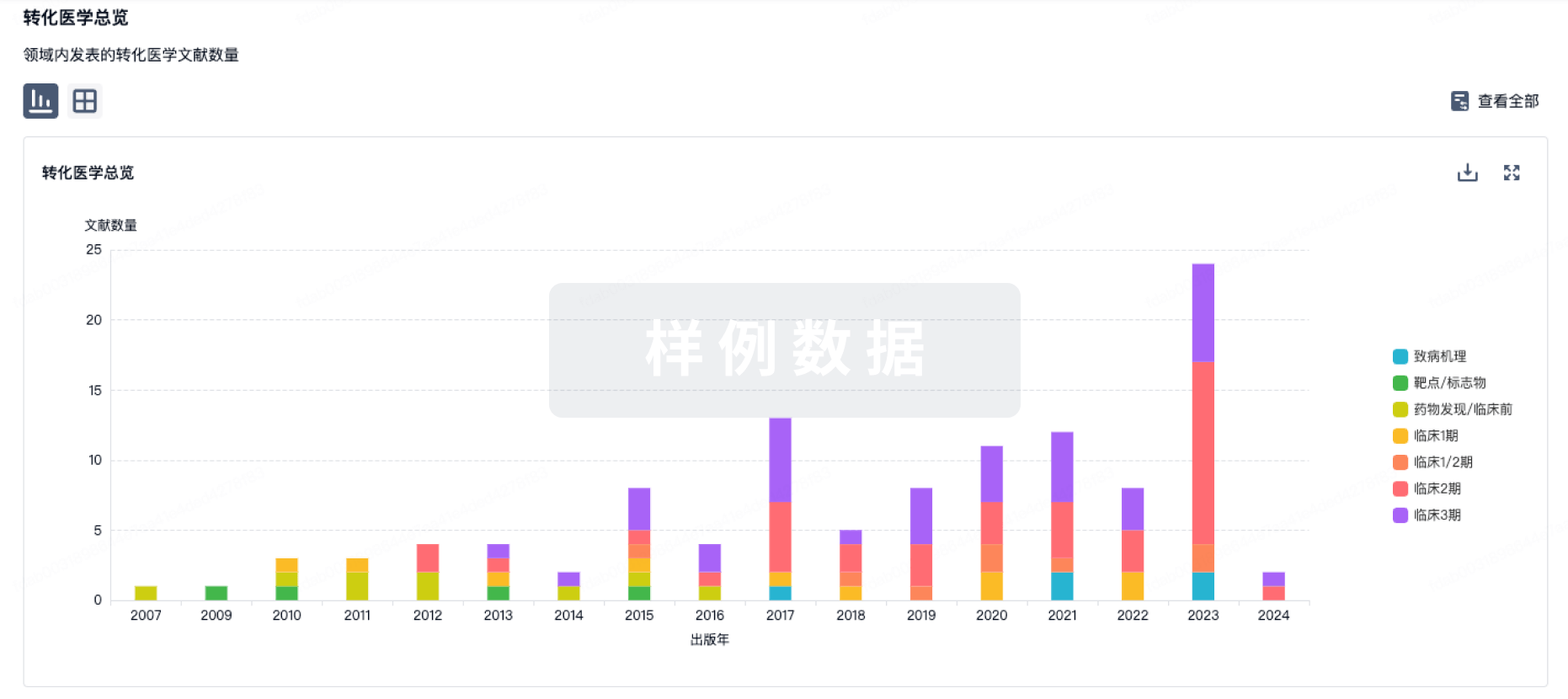
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
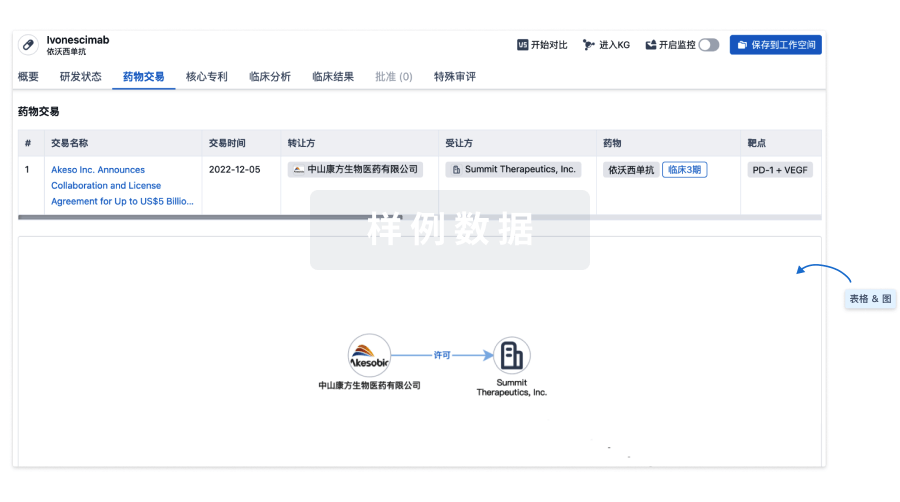
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
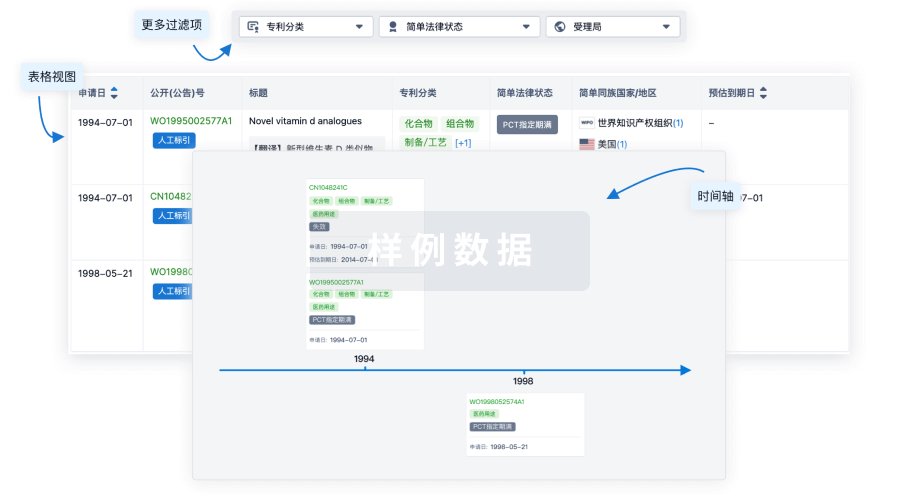
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
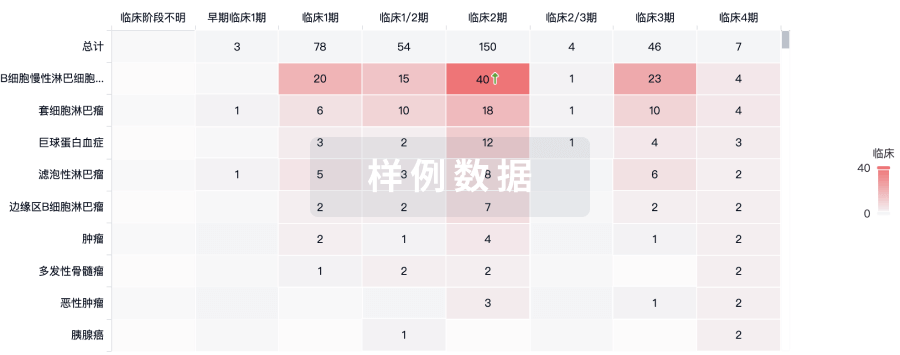
批准
利用最新的监管批准信息加速您的研究。
登录
或
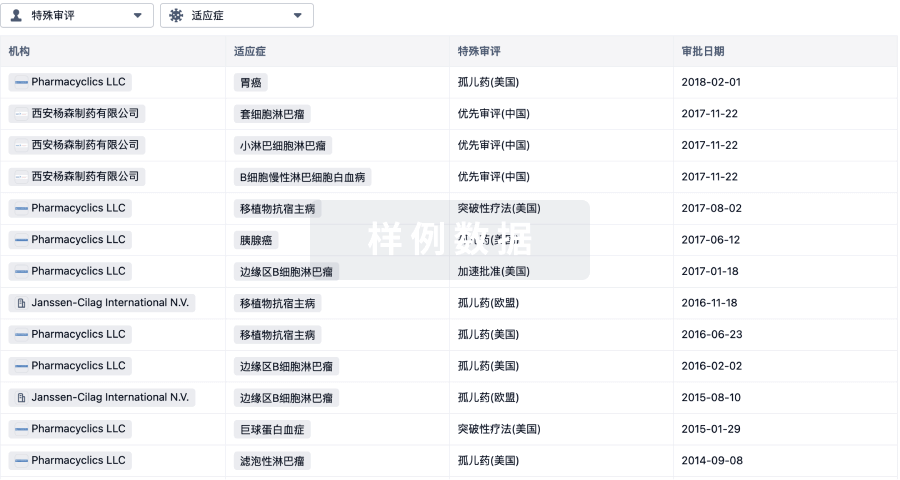
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
标准版
¥16800
元/账号/年
新药情报库 | 省钱又好用!
立即使用
来和芽仔聊天吧
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用